TPM 02
Sintesis Kitosan Dari Cangkang Udang
Ahmad Fadli1, Ervina1, Drastinawati1 dan Feblil Huda2
1Jurusan Teknik Kimia, Fakultas Teknik, Universitas Riau
2Jurusan Teknik Mesin, Fakultas Teknik, Universitas Riau
Kampus Binawidya Km 12,5 Pekanbaru 28293 [email protected]
Abstrak
Kitosan merupakan polimer rantai panjang yang disusun oleh monomer-monomer glukosamin (2-amino-2-deoksi-D-glukosa). Biopolimer ini disusun oleh dua jenis amino yaitu glukosamin (2-amino-2-deoksi-D-glukosa, 70-80%) dan N-asetil glukosamin (2-asetamino-2- deoksi-D-glukosa, 20-30%). Tujuan penelitian ini adalah mempelajari pengaruh waktu reaksi pada proses deasetilasi terhadap karakteristik kitosan. Cangkang udang yang telah
dibersihkan kemudian dikeringkan di dalam oven dengan suhu 105oC untuk menghilangkan
kadar airnya. Penghilangan protein dilakukan dengan mereaksikan serbuk cangkang dengan NaOH pada rasio berat cangkang udang dengan volume larutan NaOH 1:20. Kemudian disaring dengan kertas saring untuk diambil residunya dan dicuci menggunakan akuades sampai pH netral. Proses demineralisasi dilakukan dengan mereaksikan serbuk cangkang udang hasil proses deproteinasi dengan HCl 1 N dengan rasio berat kulit udang dengan volume larutan NaOH 1:15. Endapan hasil penyaringan dikeringkan dalam oven pada suhu
100 0C selama 4 jam. Karakteristik kitosan yang diperoleh dari pengaruh rasio massa kitin
dengan volume larutan NaOH 1:20 pada proses deasetilasi menghasilkan kitosan dengan konsentrasi 86,02%. Waktu reaksi menjadi faktor yang berpengaruh dalam menghasilkan kitosan dengan konsentrasi tinggi. Diperoleh waktu reaksi optimum yang akan menghasilkan kitosan berkonsentrasi tinggi adalah 3 jam.
Kata kunci: Deasetilasi, Demineralisasi, Deproteinasi, Kitin, Kitosan. 1.0 PENDAHULUAN
Biomaterial diartikan sebagai suatu material baik, bersifat alami maupun buatan (sintetis) yang digunakan dalam sistem biologi dengan tujuan untuk memperbaiki (repair), memulihkan (restore) atau mengganti (replace) jaringan yang rusak atau sebagai interface dengan lingkungan fisiologis (Darwin, 2008). Pemilihan biomaterial yang tepat sangat diperlukan dalam proses implantasi. Tentunya biomaterial yang dipilih adalah yang mudah diperoleh, biokompatibel atau sesuai dengan jaringan keras dalam komposisi dan morfologi, bioaktif dan tidak toksik (Riyani, 2005).
Kitosan telah digunakan secara luas dalam bidang medis terutama sebagai biopolimer yang biasanya digabungkan dengan material pengganti tulang dan gigi karena bersifat biocompatible, biodegradable, bioresorbabledan non-toksik (Nather dkk, 2005). Kitosan biasanya digabungkan dengan senyawa kalsium fosfat seperti HAp untuk dibentuk menjadi pelet berpori yang menyediakan jaringan untuk migrasi sel sehingga memungkinkan
Gambar 1. (A) Ebi dan B) Limbah Cangkang Hasil Industri Ebi
hasil deasetilasi kitin yang dapat diperoleh dari cangkang hewan laut seperti udang dan kepiting.
Limbah cangkang udang dapat diperoleh dari industri pengolahan udang ebi yang ada di Kabupaten Indragiri Hilir dengan jumlah limbah sekitar 1-3 ton/bulan.Limbah cangkang yang dihasilkan dari proses pengolahan udang tersebut berkisar antara 30-75% dari berat total udang (Darmawan dkk, 2007). Cangkang udang diketahui mengandung kitin sebesar 18,7% (Mawarda dkk, 2011).
Tujuan penelitian ini adalah mempelajari pengaruh waktu reaksi pada proses deasetilasi terhadap karakteristik kitosan. Sintesa kitosan telah dilakukan oleh beberapa peneliti diantaranya yaitu Ramadhan dkk (2010), melakukan penelitian dengan menggunakan sampel yang berbeda yaitu kulit udang putih (Litopenaeus vennamel). Proses deasetilasi kitin menjadi kitosan dilakukan dengan pengerjaan secara bertahap dalam
larutan NaOH 50% dengan rasio massa kitin dengan larutan 1:20 (b/v) pada suhu 120oC
dengan kecepatan pengadukan 50 rpm. Hasil penelitian yang diperoleh memperlihatkan waktu deasetilasi kitin selama 3 x 3 jam dengan penghilangan warna menggunakan natrium hipoklorat menghasilkan kitosan dengan derajat deasetilaasi 100%. Bentuk cangkang udang di tampilkan pada Gambar 1.
2.0 METODOLOGI 2.1 Bahan dan Alat
Bahan baku penelitian ini adalah limbah ebi diperoleh dari hasil pengolahan industri udang ebi yang berasal dari desa Kuala Enok Kecamatan Indaragiri Hilir-Riau, NaOH (Merck, Jerman), HCl (Merck, Jerman), dan aquadest (Brataco Chemikal, Indonesia).
Alat-alat yang digunakan adalah timbangan analitik, ayakan (50mesh), magnetic stirrer (Dragon lab, China), penangas air, beaker glass, gelas ukur 100 ml, labu ukur 100 mL, pH meter (Hanna Instrument, Romania), kertas indikator pH, termometer raksa, oven, furnace, cawan porselin, statif & klem, batang pengaduk, corong, kertas saring whatman 42,
2.2 Prosedur Penelitian
Proses sintesis kitosan secara kimiawi. Purwantiningsih (1992) telah mengekstraksi kitin melalui tahap deproteinasi dan tahap demineralisasi. Setiap proses diikuti dengan tahap pencucian, pembilasan, penetralan pH, dan pengeringan.
Tahap deproteinasi dapat dilakukan dengan menggunakan larutan NaOH 3,5%
(Rasio 1:10 (b/v)) selama 2 jam pada suhu 65○C dan tahap demineralisasi dapat dilakukan
dengan menggunakan larutan HCl 1N (Rasio 1:10 (b/v)) selama 1 jam pada suhu 30○C,
sedangkan pada tahap deasetilasi dapat dilakukan dengan menggunakan NaOH 50% (Rasio
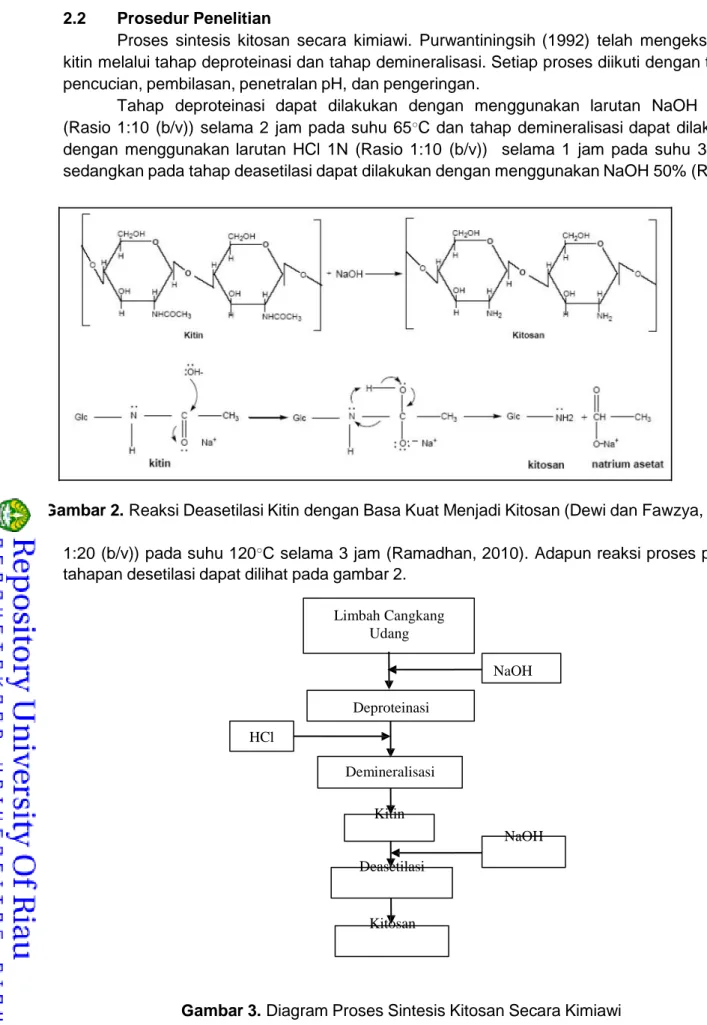
Gambar 2. Reaksi Deasetilasi Kitin dengan Basa Kuat Menjadi Kitosan (Dewi dan Fawzya, 2006)
1:20 (b/v)) pada suhu 120○C selama 3 jam (Ramadhan, 2010). Adapun reaksi proses pada
tahapan desetilasi dapat dilihat pada gambar 2.
Limbah Cangkang Udang NaOH Deproteinasi HCl Demineralisasi Kitin NaOH Deasetilasi Kitosan
Persiapan bahan baku diawali dengan membersihkan kulit udang dengan cara dicuci berkali-kali dengan akuades hingga kotorannya hilang. setelah itu dioven untuk
menghilangkan kadar airnya dengan suhu 105 oC hingga nilainya konstan. Cangkang udang
yang sudah kering diblender hingga halus kemudian diayak dengan ukuran partikel 50 mesh. mengencerkan larutan HCl 36% menjadi 1 N menggunakan aquadest.
Prosedur sintesis kitin dan kitosan yang dilakukan menggunakan metode kimiawi merujuk pada Drastinawati (2002) dengan modifikasi terhadap bahan baku. Pada penelitian Drastinawati menggunakan bahan baku berupa limbah cangkang udang basah sedangkan pada penelitian ini menggunakan limbah cangkang pengolahan ebi. Adapun tahapannya meliputi Isolasi kitin dan tarnsfomasi kitin. Kitin yang diperoleh diidentifikasi dengan menggunakan spektroskopi infra merah atau lebih dikenal dengan Fourier Transform Infra Red (FTIR).
Larutan NaOH 3,5% dibuat dengan cara melarutkan 105,35 gram NaOH dilarutkan kedalam 3010 ml aquadest dan larutan NaOH 50% dibuat dengan cara melarutkan 400 gram NaOH dilarutkan ke dalam 800 ml aquadest. Untuk larutan HCl 1 N dibuat dengan cara mengencerkan larutan HCl 36% menjadi 1 N menggunakan aquadest. Pada rasio 1:20 dilakukan variasi waktu reaksi 0,5 jam dan 3 jam. Proses deasetilasi kitin menjadi kitosan dilakukan dengan pengerjaan secara bertahap dalam larutan NaOH 50% dengan rasio
massa kitin dengan larutan 1:20 (b/v) pada suhu 120oC dengan kecepatan pengadukan 50
rpm.
3.0 HASIL DAN PEMBAHASAN
3.1 Analisa Kitosan menggunakan FTIR
Analisa terhadap Spektra IR menyajikan informasi tentang gugus fungsional dari produk yang dianalisis sehingga dapat disimpulkan bahwa senyawa yang dimaksud mempunyai gugus fungsional yang sama dengan senyawa yang diharapkan. Kitin yang diperoleh diidentifikasi dengan menggunakan spektroskopi inframerah. Identifikasi ini dilakukan untuk mengetahui gugus fungsi kitin yang diperoleh dapat dilihat pada Gambar 4 dan Gambar 5.
Dari hasil analisa FTIR kitin diperoleh derajat deasetilasi kitin yaitu 60,01%. Nilai
kadar ini sudah memenuhi standar mutu kitin yaitu ≥ 15%. Tingginya perolehan derajat
deasetilasi ini menunjukkan bahwa sebagian besar kitin sudah berubah menjadi kitosan. Hal ini menunjukkan bahwa kenaikan waktu reaksi mempengaruhi banyaknya presentae molekul NaOH yang teradisi kitin sehingga penyebabkan gugus asetil yang terlepas pun semakin banyak (Rokhati, 2006). Faktor pendorong terjadinya peningkatan derajatdeasetilasi kitosan adalah faktor morfologi rantai kitin yang gugus asetamidanya semakin berkurang pada saat waktu deasetilasi meningkat, kitin dengan gugus asetamida yang berkurang mengalami perubahan morfologi, sehingga memungkinkan proses hidrolisis
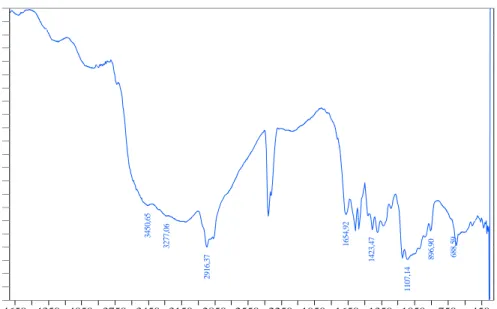
3450 ,6 5 3277 ,0 6 2916 ,3 7 1654 ,9 2 1423 ,4 7 1107 ,1 4 896 ,9 0 688 ,5 9 3446 ,7 9 3277 ,0 6 2879 ,7 2 1654 ,9 2 1423 ,4 7 1091 ,7 1 856 ,3 9 686 ,6 6 110 %T 107,5 105 102,5 100 97,5 95 92,5 90 87,5 85 82,5 80 77,5 75 72,5 70 67,5 65 62,5 60 57,5 55 4650 4350 4050 3750 3450 3150 2850 2550 2250 1950 1650 1350 1050 750 450 Sampel 1banding 20 (6) 1/cm
Gambar 4. Analisa Gugus Fungsi Kitosan Rasio 1:20 dengan FTIR dengan Waktu Reaksi
0,5 Jam 110 %T 107,5 105 102,5 100 97,5 95 92,5 90 87,5 85 82,5 80 77,5 75 72,5 70 67,5 65 62,5 60 57,5 55 52,5 50 4400 4000 3600 3200 2800 2400 2000 1800 1600 1400 1200 1000 800 600 400
Sampel 1banding 20 (1) Smooth 1/cm
Gambar 5. Analisa Gugus Fungsi Kitosan Rasio 1:20 dengan FTIR dengan Waktu Reaksi 3
Jam
Gambar 4 menunjukkan bahwa pada spektra kitosan waktu reaksi 0,5 jam menunjukkan serapan vibrasi OH yaitu pada 3454,51, kemudian vibrasi ulur N-H pada
3284,77. Serapan lainnya adalah pada 2879,72 cm-1 merupakan vibrasi ulur dari gugus C-H
metilen. Vibrasi guntingan NH2 dan N-H bengkokan muncul pada bilangan gelombang
1656,85 cm-1. Kemudian adanya serapan CH3 pada 1425,50 cm-1. Adanya serapan pada
1064,71 cm-1 pada kitosan cangkang udang menunjukkan vibrasi C-O-C. Vibrasi kibasan N-
H muncul pada 896,90 cm-1. Perbedaan yang terjadi setelah tahap deasetilasi adalah tidak
munculnya vibrasi gugus C=O ulur dari gugus amida (-NHCO) pada 1680 cm-1 yang
menandakan hilang atau telah berkurangknya gugus C=O pada kitosan, serta munculnya -1
%
D
er
a
ja
t
D
eas
et
il
a
si
Gambar 5 menunjukkan bahwa pada spektra kitosan waktu reaksi 0,5 jam
menunjukkan serapan vibrasi OH yaitu pada 3448,72 cm-1, kemudian vibrasi ulur N-H pada
3292,49 cm-1. Serapan lainnya adalah pada 2879,72 cm-1 merupakan vibrasi ulur dari gugus
C-H metilen. Vibrasi guntingan NH2 dan N-H bengkokan muncul pada bilangan gelombang
1660,71 cm-1. Kemudian adanya serapan CH3 pada 1423,47 cm-1. Adanya serapan pada
1107,14 cm-1 pada kitosan cangkang udang menunjukkan vibrasi C-O-C. Vibrasi kibasan N-
H muncul pada 896,90 cm-1. Perbedaan yang terjadi setelah tahap deasetilasi adalah tidak
munculnya vibrasi gugus C=O ulur dari gugus amida (-NHCO) pada 1680 cm-1 yang
menandakan hilang atau telah berkurangknya gugus C=O pada kitosan, serta munculnya
serapan pada 665,44 cm-1 yang merupakan vibrasi dari gugus kibasan dan pelintiran NH2.
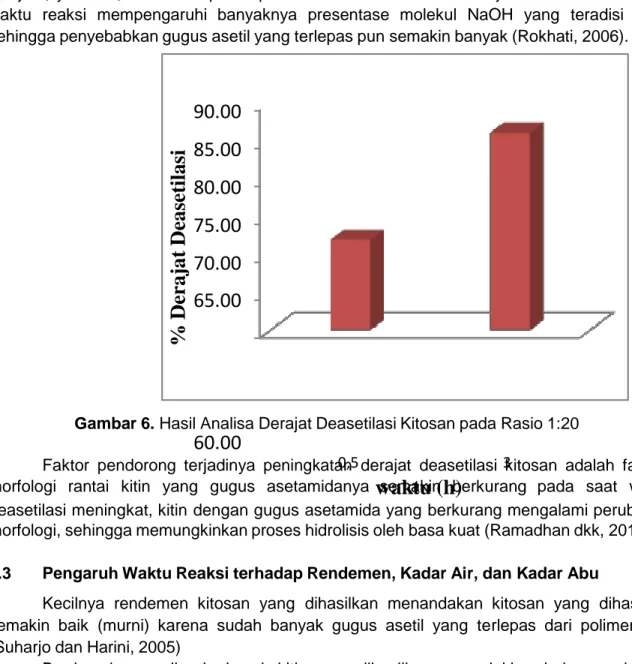
3.2 Pengaruh Waktu Reaksi Terhadap Derajat Deasetilasi Kitosan
Hasil derajat deasetilasi kitosan tertinggi 86,02% pada rasio 1:20 dengan waktu reaksi 3 jam. Sedangkan derajat deasetilasi terendah terdapat pada perlakuan waktu reaksi 0,5 jam, yaitu 71,92 % ditampilkan pada Gambar 6. Hal ini menunjukkan bahwa kenaikan waktu reaksi mempengaruhi banyaknya presentase molekul NaOH yang teradisi kitin sehingga penyebabkan gugus asetil yang terlepas pun semakin banyak (Rokhati, 2006).
90.00
85.00
80.00
75.00
70.00
65.00
Gambar 6. Hasil Analisa Derajat Deasetilasi Kitosan pada Rasio 1:20
60.00
Faktor pendorong terjadinya peningkata0n,5 derajat deasetilasi 3kitosan adalah faktor
morfologi rantai kitin yang gugus asetamidanya
w
sea
mk
atu
kin(h
b)
erkurang pada saat waktudeasetilasi meningkat, kitin dengan gugus asetamida yang berkurang mengalami perubahan morfologi, sehingga memungkinkan proses hidrolisis oleh basa kuat (Ramadhan dkk, 2010).
3.3 Pengaruh Waktu Reaksi terhadap Rendemen, Kadar Air, dan Kadar Abu
Kecilnya rendemen kitosan yang dihasilkan menandakan kitosan yang dihasilkan semakin baik (murni) karena sudah banyak gugus asetil yang terlepas dari polimer kitin (Suharjo dan Harini, 2005)
Berdasarkan analisa kadar air kitin yang dihasilkan menunjukkan bahwa perlakuan variasi waktureaksi terhadap rasio massa kitin dan larutan pada proses deasetilasi tidak
memiliki pengaruh yang signifikan. Dalam pembuatan kitosan kadar air banyak dipengaruhi oleh proses pengeringan serta kitosan itu sendiri dalam menyerap uap air dari lingkungannya. Kadar air kitosan tidak dipengaruhi oleh jumlah bahan, nisbah dan waktu prosesnya, tetapi oleh waktu pengeringan terhadap kitosan yang dihasilkan (Wardhani, 2007).
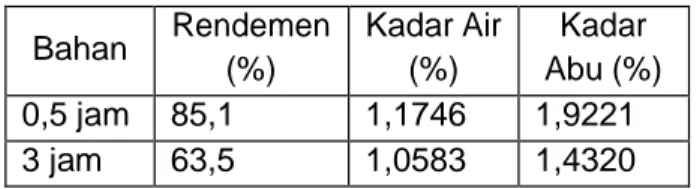
Tabel 1. Hasil Analisa Rendemen, Kadar Air, Dan Kadar Abu Pada Rasio 1:20
Bahan Rendemen (%) Kadar Air (%) Kadar Abu (%) 0,5 jam 85,1 1,1746 1,9221 3 jam 63,5 1,0583 1,4320
Setelah mengalami proses demineraisasi, kandungan mineral berkurang sehingga diperoleh kitin dengan kadar abu yang lebih sedikit 1,4320%. Menurut Bastman (1989), kitosan mengandung gugus hidroksil yang bertindak sebagai donor elektron dan dapat berperan sebagai amino pengganti (amino exchanger). Disamping itu kitosan dapat berinteraksi dengan zat-zat organik lainnya termasuk dengan sisa-sisa mineral yang terkandung pada bahan.
4.0 KESIMPULAN
Kitosan dapat di konversi dari kitin yang terdapat pada cangkang udang hasil limbah industri ebi. Analisa gugus fungsi kitosan rasio 1:20 menunjukkan serapan vibrasi yang memiliki nilai data serapan yang memiliki perbedaan kecil antara waktu reaksi 0,5 jam dengan 3 jam. Kitosan dengan rasio 1:20 waktu reaksi 0,5 jam memiliki derajat deasetilasi 71,92%, sedangkan hasil analisa derajat deasetilasi menunjukkan bahwa pada waktu reaksi 3 jam diperoleh derajat deasetilasi kitosan 86,02%. Pengaruh waktu reaksi terhadap hasil analisa rendemen, kadar air, dan kadar abu menunjukkan pengurangan yang signifikan.
Ucapan Terima Kasih
Penulis mengucapkan terima kasih kepada kemenristek dikti yang membiayai penelitian ini melalui Skim Penelitian Strategis Nasional 2016.
Daftar Pustaka
Bastman, S. 1989. Studies on Degradetion and Extraction of Chitin and Chitosan from Prawn Shells. Thesis. The departement of Mechanical Manufacturing. Aeonautical and Chemical Engineering. The Queen’s University.
Darmawan, E., Mulyaningsih, S., Firdaus, F. 2007. Karakteristik Khitosan yang Dihasilkan dari Limbah Kulit Udang dan Daya Hambatnya terhadap Pertumbuhan Candida albicans. LOGIKA. Yogyakarta: Bidang Farmakologi dan Bioteknologi, Farmasi FMIPA UII Yogyakarta, Bidang Material dan Komposit, DPPM UII Yogyakarta, Universitas Islam Indonesia Yogyakarta. Vol.4: 207-213.
Darwin, D. 2008. Aplikasi Teknik Isotop dan Radiasi pada Pembuatan Biomaterial untuk Keperluan Klinis.http://nhc.batan.go.id [3 April 2015: 09:20]
Dewi, A. S. & Fawzya, Y, N. 2006, Pendahuluan: Penggunaan berulang larutan Natrium Hidroksida dalam Pembuatan kitosan, Prosiding Seminar Nasional Himpunan Kimia
Drastinawati. 2002. Pemanfaatan Khitin dan Khitosan dari Kulit Udang Sebagai Material Penyerap Ion Kadmium, Tembaga dan Timbal. Tesis. Universitas Andalas Padang. Mawarda, P.C., Triana, R., dan Nasrudin . 2011. Fungsionalisasi Limbah Cangkang Udang
Untuk Meningkatkan Kandungan Kalsium Susu Kedelai Sebagai Penambah Gizi Masyarakat. Skripsi. Bogor: Institut Pertanian Bogor
Nather, A., Zameer, A., 2005. Bone Grafts And Bone Substitutes - Basic Science and Clinical Applications. World Scientific Publishing Co. Pte. Ltd.
Purwantiningsih. 1992. Isolasi Kitin dan komposisi Senyawa Kimia Limbah Udang Windu (Panaeus monodon). Tesis. Bandung: Institut Teknologi Banding (ITB).
Ramadhan, L, O, A, N.,Radiman, C, L., Wahyuningrum, D. 2010. Deasetilasi Kitin Secara Bertahap Dan Pengaruhnya Terhadap Derajat Deasetilasi Serta Massa Molekul Kitosan. Jurnal kima indonesia. Vol 5(1): 17-21.
Riyani, E. 2005. Karakterisasi Senyawa Kalsium fosfat Karbonat HAsil Presipitasi Menggunakan XRD,SEM,dan EDXA Pengaruh Perubahan Ion F- dan Mg+. Skripsi. Departemen Fisika.Fakultas Matematika dan IPA. Bogor: Institut Pertanian Bogor. Rokhati, N. 2006. Pengaruh Derajat Deasetilasi Khitosan Dari Kulit Udang Terhadap
Aplikasinya Sebagai Pengawet Makanan. Skripsi. Semaran: Universitas Diponegoro. 10(2): 54-58.
Suharjo dan Harini, N. 2005. Ektraksi Chitosan dari Cangkang Udang Windu (Penaeus Monodon SP) secara Fisika-Kimia (Kajian Berdasarkan Ukuran Pertikel Tepung Chitin dan Konsetrasi NaOH). Skripsi. Malang: Universitas Muhammadiyah. 1(1): 7- 15.
Wardhani, I. K. 2007. Mempelajari Mutu Silase dan Kitosan dari Ampas Silase Limbah Udang. Skripsi. Bogor: Institut Pertanian Bogor.
Zhao F, Yin Y, Lu W, Leong J, Zhang W, Zhang J, Zhang M, Kangde K. 2002. Preparation and histological evaluation of biomimetic three-dimensional hydroxyapatite / chitosan- gelation network composite scaffolds. Biomaterials 23 : 3227-3234.