STUDI KELARUTAN KITOSAN DALAM
LARUTAN ASAM ASKORBAT
SKRIPSI
MILA AMELIA
080822016
PROGRAM STUDI SARJANA KIMIA
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
STUDI KELARUTAN KITOSAN DALAM LARUTAN ASAM ASKORBAT
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
MILA AMELIA 080822016
PROGRAM STUDI SARJANA KIMIA DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : STUDI KELARUTAN KITOSAN DALAM LARUTAN ASAM ASKORBAT
Kategori : SKRIPSI
Nama : MILA AMELIA
Nomor Induk Mahasiswa : 080822016
Program Studi : SARJANA (S-1) KIMIA EKSTENSI
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, September 2010
Komisi Pembimbing :
Pembimbing II Pembimbing I
Prof. Dr. Zul Alfian, M.Sc. Prof. Dr. Harry Agusnar, M.Sc, M.Phil. NIP.195504051983031002 NIP. 195308171983031002
Diketahui/Disetujui oleh
Departemen Kimia FMIPA USU Ketua,
PERNYATAAN
STUDI KELARUTAN KITOSAN DALAM LARUTAN ASAM ASKORBAT
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan, September 2010
PENGHARGAAN
Bismillahirrahmaanirrahim, segala puji dan syukur penulis persembahkan atas
kehadirat ALLAH SWT, berkat petunjuk dan ridho-Nya, penulis dapat menyelesaikan
skripsi untuk memenuhi persyaratan dalam memperoleh gelar Sarjana Sains bidang
Kimia pada Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera
Utara dengan judul “Studi Kelarutan Kitosan Dalam Larutan Asam Askorbat”.
Shalawat dan salam kepada Rasulullah Muhammad SAW, semoga kesabaran beliau
dapat menjadi contoh teladan dalam perjalanan skripsi dan kerja-kerja selanjutnya.
Penulis mengucapkan terima kasih dan penghargaan khusus kepada kedua
orang tua tercinta, Ayahanda Suherman dan Ibunda Aswita dan nenek penulis Animar
yang telah memberikan motivasi baik moral, materil dan perhatian yang tulus kepada
penulis sepanjang perkuliahan sampai selesai skripsi ini. Penulis mengucapkan terima
kasih juga kepada kakak dan adik-adik penulis: Renny Tania, S.Psi; Winda Pratiwi,
A.Md serta Mhd. Fauzi yang selalu memberi semangat dan dukungan yang berarti
pada penulis.
Dalam penyusunan skripsi ini penulis banyak memperoleh bantuan dan
bimbingan dari berbagai pihak. Untuk itu pada kesempatan ini penulis menyampaikan
terima kasih yang sebesar-besarnya kepada :
1. Bapak Prof. Dr. Harry Agusnar, M.Sc., M.Phil selaku dosen pembimbing 1
yang telah memberikan judul skripsi dan waktunya untuk membimbing serta
mengarahkan penulis sehingga selesai penulisan skripsi ini.
2. Bapak Prof. Dr.Zul Alfian, M.Sc selaku dosen pembimbing 2 yang telah
mengarahkan penulis sehingga selesai penulisan skripsi ini.
3. Ibu DR. Rumondang Bulan Nst, MS, dan Bapak Drs Firman Sebayang, MS,
5. Sahabat-sahabat penulis senasib dan seperjuangan Yeni Mardhia, S.Si; Fitria
Permatasari Situmorang, S.Si; Anggia murni, Nora Anggreini yang selalu
memberi dorongan dan semangat dalam suka dan duka demi penyelesaian
skripsi ini sehingga skripsi ini dapat terselesaikan dengan baik dan semoga
akan tetap menjadi sahabatku yang terbaik.
6. Terima kasih juga penulis ucapkan pada Alfieni Putri, Riri Mardawati, Nur
Indah Ritonga dan Kak Nathalin yang telah memberikan semangat dan
saran-sarannya..
7. Semua pihak yang telah berperan serta baik langsung ataupun tidak langsung
sehingga skripsi ini dapat terselesaikan. Kiranya hanya Allah SWT yang
akan membalas semua kebaikan yang telah diberikan secara tulus kepada
penulis.
Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan, oleh
karena itu penulis mengharapkan saran yang bersifat membangun demi kesempurnaan
skripsi ini.
Akhir kata saya berharap semoga Skripsi ini dapat bermanfaat bagi kita semua.
Medan, September 2010
ABSTRAK
STUDY OF SOLUBILITY OF CHITOSAN IN A SOLUTION OF ASCORBIC ACID
ABSTRACT
DAFTAR ISI
Halaman
Persetujuan ii
Pernyataan iii
Penghargaan iv
Abstrak vi
Abstract vii
Daftar Isi viii
Daftar Tabel x
Daftar Lampiran xi
BAB 1 PENDAHULUAN 1
1.6 Metodologi Penelitian 2
1.7 Lokasi Penelitian 2
BAB 2 TINJAUAN PUSTAKA 3
2.1 Kitosan 3
2.1.1 Sumber Kitosan 4
2.1.2 Sifat-sifat Kitosan 4
2.2 Kegunaan Kitosan 7
2.2.1 Industri Tekstil 7
2.2.2 Bidang Fotografi 8
2.2.3 Bidang Kedokteran/Kesehatan 8 2.2.4. Industri Fungisida 8 2.2.5 Industri Kosmetika 9 2.2.6 Industri Pengolahan Pangan 9
2.2.7 Penanganan Limbah 9
BAB 3 METODE PENELITIAN 16
3.1 Bahan-bahan 16
3.2 Alat-alat 16
3.3 Prosedur Penelitian 17
3.3.1 Pembuatan Larutan Asam Askorbat 0,25% 17 3.3.2 Pembuatan Larutan Asam Askorbat 0,50% 17 3.3.3 Pembuatan Larutan Asam Askorbat 0,75% 17 3.3.4 Pembuatan Larutan Asam Askorbat 1,00% 17 3.3.5 Pembuatan Larutan Asam Askorbat 1,25% 17 3.3.6 Penentuan Kelarutan Kitosan dalam Larutan Asam Askorbat 18 3.4 Bagan Penelitian 19 3.4.1 Pembuatan Larutan Asam Akorbat 0,25% 19 3.4.2 Penentuan Kelarutan Kitosan dalam Larutan Asam Askorbat
0,25% 20
BAB 4 DATA DAN HASIL PEMBAHASAN 21
4.1 Hasil Penelitian 21
4.2 Pembahasan 24
4.2.1 Penentuan Derajat Deasetilasi 24 4.2.2 Kelarutan Kitosan dalam Larutan Asam askorbat 25 4.2.3 Analisis Spektrum FT-IR Serbuk Kitosan 26 4.2.4 Analisis Spektrum FT-IR Kitosan dalam Larutan
Asam Askorbat 1,00% 27
4.2.5 Analisis Spektrum FT-IR Serbuk Asam Askorbat 28
BAB 5 KESIMPULAN DAN SARAN 29
5.1 Kesimpulan 29
5.2 Saran 29
DAFTAR TABEL
Halaman
Tabel 2.1 Sumber-sumber Kitin dan Kitosan 4 Tabel 2.2 Kelarutan Kitosan pada Berbagai Pelarut Asam Organik 6 Tabel 4.1 Data hasil Pengukuran kelarutan Kitosan dalam Larutan Asam Askorbat
0,25% 20
Tabel 4.2 Data hasil Pengukuran kelarutan Kitosan dalam Larutan Asam Askorbat
0,50% 22
Tabel 4.3 Data hasil Pengukuran kelarutan Kitosan dalam Larutan Asam Askorbat
0,75% 22
Tabel 4.4 Data hasil Pengukuran kelarutan Kitosan dalam Larutan Asam Askorbat
1,00% 23
Tabel 4.5 Data hasil Pengukuran kelarutan Kitosan dalam Larutan Asam Askorbat
DAFTAR LAMPIRAN
Halaman
ABSTRAK
STUDY OF SOLUBILITY OF CHITOSAN IN A SOLUTION OF ASCORBIC ACID
ABSTRACT
BAB 1
PENDAHULUAN
1.1.Latar Belakang
Kitosan adalah turunan utama dari kitin, dan pertama sekali ditemukan oleh Hoppe
Seylor pada tahun 1894 (Muzzarelli, 1978). Kitosan mempunyai sifat dan karakteristik
yang berbeda, ini tergantung sumber kitosan yang diperoleh. Kitosan larut pada
beberapa larutan asam organik didapati pada pH 4 tetapi tidak larut pada pH lebih
besar dari 6,5. Selama ini melarutkan kitosan hanya menggunakan larutan asam asetat
1%, begitu juga dengan penggunaan asam formiat 10% didapati kitosan larut (Robert,
1992). Penggunaan asam sitrat dan asam maleat 10% didapati juga kitosan larut. Jika
konsentrasi larutan dinaikkan, kitosan tidak akan mengalami hidrolisis karena menurut
Muzzarelli (1977), kenaikkan konsentrasi larutan tidak dapat mengubah bentuk.
Kitosan dipengaruhi beberapa faktor seperti berat molekul dan derajat deasetilasi.
Menurut Tokura (1982), kelarutan kitosan dilihat dari sumber kitin yang
diperoleh dan konsentrasi larutan yang digunakan. Agusnar (2006), melaporkan
bahwa campuran larutan asam asetat dan glycerin dengan nisbah 1:1 didapati
menghasilkan larutan gel yang jernih.
Berdasarkan uraian diatas, peneliti ingin menggunakan larutan asam askorbat
untuk melarutkan kitosan yang diperoleh dari kulit udang.
1.2.Permasalahan
1.3. Pembatasan Masalah
Penelitian ini dibatasi pada, karakteristik kitosan dengan variasi berat 0,5g; 1,0g; 1,5g;
2,0g; 2,5g, 3,0g kitosan dengan konsentrasi larutan asam askorbat 0,25%; 0,50%;
0,75%; 1,00% dan 1,25%.
1.4. Tujuan Penelitian
Tujuan penelitian ini untuk mengetahui kelarutan kitosan dalam larutan asam
askorbat.
1.5. Manfaat Penelitian
Diharapkan hasil yang diperoleh dari penelitian ini memberikan suatu informasi
untuk mengetahui seberapa besar kelarutan kitosan dalam larutan asam askorbat untuk
mengikat asam lemak bebas.
1.6. Metodologi Penelitian
Penelitian ini dilakukan secara eksperimental laboratorium yaitu untuk mengetahui
sejauh mana kelarutan kitosan dalam larutan asam askorbat dengan variasi berat
kitosan dengan konsentrasi larutan asam askorbat yang berbeda-beda. Kemudian
dikarakterisasi dengan spektroskopi FT-IR.
1.7. Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Penelitian Fakultas Matematika dan Ilmu
Pengetahuan Alam (FMIPA) Universitas Sumatera Utara. Karakterisasi analisis
BAB 2
TINJAUAN PUSTAKA
2.1. Kitosan
Kitosan dengan rumus molekul (C6H11NO4)n yang dapat diperoleh dari deasetilasi
kitin. Kitosan juga dijumpai secara alamiah di beberapa organisme. Adapun struktur
kitosan:
Gambar 2.1 Struktur Kitosan
Proses deasetilasi kitin dapat dilakukan dengan cara kimiawi atau enzimatik.
Ternyata penghilangan gugus asetil kitin meningkatkan kelarutannya, sehingga
kitosan lebih banyak digunakan daripada kitin, antara lain di industri kertas, pangan,
farmasi, fotografi, kosmetika. Selain itu kitosan juga bersifat nontoksik,
biokompatibel, dan biodegradabel sehingga aman digunakan.
Perkembangan penggunaan kitosan meningkat pada tahun 1940-an terlebih
dengan makin diperlukannya bahan alami oleh berbagai industri sekitar tahun
1970-an. Penggunaan kitosan untuk aplikasi khusus seperti farmasi, kesehatan, bidang
2.1.1. Sumber Kitosan
Kitosan merupakan senyawa kimia yang berasal dari bahan hayati kitin, suatu
senyawa organik yang melimpah di alam ini setelah selulosa. Kitin ini umumnya
diperoleh dari kerangka hewan invertebrata dari kelompok Arthopoda sp, Molusca sp,
Coelenterata sp, Annelida sp, Nematoda sp, dan beberapa dari kelompok jamur. Selain
dari kerangka hewan invertebrate, juga banyak ditemukan pada bagian insang ikan,
trachea, dinding usus dan pada kulit cumi-cumi. Sebagai sumber utamanya ialah
cangkang Crustaceae sp, yaitu udang, lobster, kepiting, dan hewan yang bercangkang
lainnya, terutama asal l
memberdayakan limbah udan
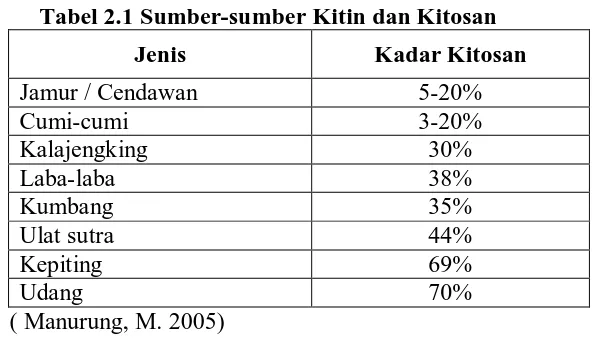
Dari tabel 2.1 dibawah ini bahwa sumber kitin dan kitosan yang banyak adalah
terdapat pada udang-udangan (70%).
Tabel 2.1 Sumber-sumber Kitin dan Kitosan
Jenis Kadar Kitosan
Jamur / Cendawan 5-20%
Cumi-cumi 3-20%
Kalajengking 30%
Laba-laba 38%
2.1.2. Sifat-sifat Kitosan
Kitosan merupakan padatan amorf yang berwarna putih kekuningan. Kelarutan
kitosan yang paling baik ialah dalam larutan asam asetat 2%. (Sugita, P. 2009).
Kitosan mudah mengalami degradasi secara biologis dan tidak beracun, kationik kuat,
flokulan dan koagulan yang baik, mudah membentuk membran atau film serta
membentuk gel dengan anion bervalensi ganda. Kitosan tidak larut dalam air,
dengan cepat dalam asam organik seperti asam formiat, asam sitrat dan asam asetat
(Mat,B.Zakaria. 1995).
Kitosan juga sedikit larut dalam HCl dan HNO3 0,5%, H3PO4. Sedangkan
dalam H2SO4 tidak larut. Kitosan juga tidak larut dalam beberapa pelarut organik
seperti alkohol, aseton, dimetil formida dan dimetil sulfoksida tetapi kitosan larut
dengan baik dengan asam formiat berkonsentrasi (0,2-100)% dalam air
(Knorr,D.1987). Sifat-sifat kitosan dihubungkan dengan adanya gugus amino dan
hidoksil yang terikat. Adanya reaktifitas kimia yang tinggi dan menyumbangkan sifat
sifat polielektrolit kation, sehingga dapat berperan sebagai amino pengganti.
Perbedaan kandungan amida adalah sebagai patokan untuk menentukan apakah
polimer ini dalam bentuk kitin atau kitosan. Kitosan mengandung gugus amida 60%
sebaiknya lebih kecil dari 60% adalah kitin (Harahap,V.U. 1995).
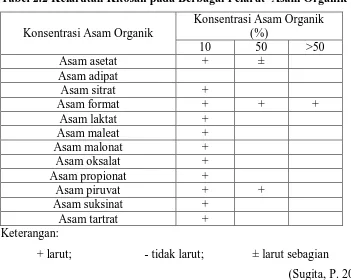
Kitosan larut pada kebanyakan larutan asam organik (Tabel 2.2) pada pH
sekitar 4,0, tetapi tidak larut pada pH lebih besar dari 6,5, juga tidak larut dalam
pelarut air, alkohol, dan aseton. Dalam asam mineral pekat seperti HCl dan HNO3,
kitosan larut pada konsentrasi 0,15-1,1%, tetapi tidak larut pada konsentrasi 10%.
Kitosan tidak larut dalam H2SO4 pada berbagai konsentrasi, sedangkan di dalam
H3PO4 tidak larut pada konsentrasi 1% sementara pada konsentrasi 0,1% sedikit larut.
Perlu untuk kita ketahui, bahwa kelarutan kitosan dipengaruhi oleh bobot molekul,
derajat deasetilasi dan rotasi spesifiknya yang beragam bergantung pada sumber dan
Tabel 2.2 Kelarutan Kitosan pada Berbagai Pelarut Asam Organik
Konsentrasi Asam Organik
Konsentrasi Asam Organik (%)
Kitosan memiliki sifat unik yang dapat digunakan dalam berbagai cara serta
memiliki kegunaan yang beragam, antara lain sebagai bahan perekat, aditif untuk
kertas dan tekstil, penjernih air minum, serta untuk mempercepat penyembuhan luka,
dan memperbaiki sifat pengikatan warna. Kitosan merupakan pengkelat yang kuat
untuk ion logam transisi.
Menurut Robert, G. A. F. (1992), kitosan merupakan suatu biopolimer alam
yang reaktif yang dapat melakukan perubahan-perubahan kimia. Karena ini banyak
turunan kitosan dapat dibuat dengan mudah. Beberapa turunan kitosan yag telah
dihasilkan dan juga telah diketahui kegunaannya antara lain:
a. N-karboksialkil kitosan, digunakan sebagai penggumpal ion logam
b. Asetil kitosan, digunakan dalam industri tekstil dan membran
c. Kitosan glukan, digunakan sebagai pengkelat ion logam dan agen penggumpal
misalnya:
1. Untuk industri kertas, kaca, kain, dan pewarna
2. Dalam industri kosmetik
3. Dalam bidang pertanian dan makanan
4. Dalam industri semen
5. Dalam bidang kesehatan
6. Untuk penyerapan ion logam
2.2. Kegunaan Kitosan
Dewasa ini aplikasi kitin dan kitosan sangat banyak dan meluas. Dibidang industri,
kitin dan kitosan berperan antara lain sebagai kogulan polielektrolit pengolahan
limbah cair, pengikat dan penyerap ion logam, mikroorganisme, pewarna, residu
peptisida, lemak, mineral dan asam organik, gel dan pertukaran ion, pembentuk film
dan membran mudah terurai, meningkatkan kualitas kertas, pulp, dan produk tekstil.
(Sugita, P. 2009).
Kitin dan kitosan dapat diterapkan di bidang industri maupun bidang
kesehatan, diantaranya : Industri tekstil, bidang fotografi, bidang
kedokteran/kesehatan, industri fungisida, industri kosmetika, industri pengolahan
pangan, serta penangan limbah.
2.2.1. Industri Tekstil
Serat tenun dapat dibuat dari kitin dengan cara membuat suspensi kitin dalam asam
maka akan terbentuk serat tenun yang potensial untuk industri tekstil. Pada kerajinan
batik, pasta kitosan dapat menggantikan ''malam'' (wax) sebagai media pembatikan.
2.2.2. Bidang Fotografi
Jika kitin dilarutkan dalam larutan dimetilasetamida LICI, maka dari larutan ini dapat
dibuat film untuk berbagai kegunaan. Pada industri film untuk fotografi, penambahan
tembaga kitosan dapat memperbaiki mutu film yaitu untuk meningkatkan
fotosensitivitasnya.
2.2.3. Bidang Kedokteran/Kesehatan
Kitin dan turunannya (karboksimetil kitin, hidroksietil kitin dan etil kitin) dapat
digunakan sebagai bahan dasar pembuatan benang operasi. Benang operasi ini
mempunyai keunggulan dapat diurai dan diserap dalam jaringan tubuh, tidak toksik,
dapat disterilisasi dan dapat disimpan lama.
Kitin dan kitosan dapat digunakan sebagai bahan pemercepat penyembuhan
luka bakar, lebih baik dari yang terbuat dari tulang rawan. Selain itu juga sebagai
bahan pembuatan garam-garam glukosamin yang mempunyai banyak manfaat di
bidang kedokteran. Misalnya untuk menyembuhkan influenza, radang usus dan sakit
tulang.
Glukosamin terasetilasi merupakan bahan antitumor, sedangkan glukosamin
sendiri bersifat toksik terhadap sel-sel tumor sehingga dapat menurunkan kadar
kolesterol darah dan kolesterol liver. Karena kitin tidak dapat dicerna dalam
pencernaan, maka ia berfungsi sebagai dietary fiber yang berguna melancarkan
2.2.4. Industri Fungisida
Kitosan mempunyai sifat antimikrobia melawan jamur lebih kuat dari Kitin. Jika
Kitosan ditambahkan pada tanah, maka akan menstimulir pertumbuhan mikrobia
mikrobia yang dapat mengurai jamur. Selain itu Kitosan juga dapat disemprotkan
langsung pada tanaman. Misalnya larutan 0,4% kitosan jika disemprotkan pada
tanaman tomat dapat menghilangkan virus tobacco mozaik.
2.2.5. Industri Kosmetika
Kini telah dikembangkan produk baru shampoo kering mengandung kitin yang
disuspensi dalam alkohol. Termasuk pembuatan lotion dan shampoo cair yang
mengandung 0,5 - 6,0 % garam kitosan. Shampoo ini mempunyai kelebihan dapat
meningkatkan kekuatan dan berkilaunya rambut, karena adanya interaksi antara
polimer tersebut dengan protein rambut.
2.2.6. Industri Pengolahan Pangan
Karena sifat kitin dan kitosan yang dapat mengikat air dan lemak, maka keduanya
dapat digunakan sebagai media pewarnaan makanan. Mikrokristalin kitin jika
ditambahkan pada adonan akan dapat meningkatkan pengembangan volume roti tawar
yang dihasilkan. Selain itu juga sebagai pengental dan pembentuk emulsi lebih baik
dari pada mikrokristalin sellulosa. Pada pemanasan tinggi kitin akan menghasilkan
pyrazine yang potensial sebagai zat penambah cita rasa.
Karena sifatnya yang dapat bereaksi dengan asam-asam seperti polifenol,
maka kitosan sangat cocok untuk menurunkan kadar asam pada buah-buahan, sayuran
dan ekstrak kopi. Bahkan terakhir diketahui dapat sebagai penjernih jus apel lebih
2.2.7. Penanganan Limbah
Karena sifat polikationiknya, kitosan dapat dimanfaatkan sebagai agensia penggumpal
dalam penanganan limbah terutama limbah berprotein yang kemudian dapat
dimanfaatkan sebagai pakan ternak. Pada penanganan limbah cair, kitosan sebagai
chelating agent yang dapat menyerap logam beracun seperti mercuri, timah, tembaga,
pluranium dan uranium dalam perairan dan untuk mengikat zat warna tekstil dalam air
limbah (Krissetiana, H. 2004).
2.3. Karakteristik Kitosan
Karakteristik kitosan yang paling sering dianalisa adalah viskositas, derajat
deasetilasi, berat molekul, pH, residu protein, kadar air, kadar abu, kandungan lemak.
Kadar logam berat, warna dan lain-lain yang bersangkutan dengan tujuan penggunaan.
Menurut Roberts (1992), standar mutu kitosan maupun polimernya belum ada,
sehingga analisa kitosan ditujukan untuk menentukan karakterisasi yang berhubungan
dengan sumber bahan kitosan dan tujuan penggunaannya.
Berat molekul merupakan salah satu parameter yang dapat membedakan kitin
dan kitosan dengan adanya pengurangan berat molekul pada kitosan akibat proses
deasetilasi yang menghilangkan gugus asetil pada kitin.
Metode yang paling sederhana untuk menentukan berat molekul dari kitin dan
kitosan yaitu dengan viskometri (Kumar, 2000). Pada metoda ini berat molekul
polimer ditentukan dengan persamaan Mark-Houwink, yaitu:
Dimana K dan α merupakan tetapan yang khas untuk sistem polimer-pelarut
tertentu (Sopyan, 2001). Harga viskositas intrinsik atau [η] diperoleh dari nilai
viskositas spesifik (ηsp) pada konsentrasi mendekati nol. Viskositas spesifik (ηsp) dapat
ditentukan dengan mengetahui waktu alir larutan dan pelarut pada alat viskometer.
[η] = K.Mα
Dimana t2 adalah waktu alir larutan dan t1 adalah waktu alir pelarut ( Firman, 1991).
2.4. Asam Askorbat (Vitamin C)
2.4.1. Struktur Asam Askorbat
Asam askorbat merupakan senyawa yang mudah larut dalam air, mempunyai sifat
asam dan sifat pereduksi yang kuat. Sifat-sifat tersebut terutama disebabkan adanya
struktur enediol yang berkonjugasi dengan gugus karbonil dalam cincin lakton.
Bentuk asam askorbat yang ada di alam terutama adalah L-asam askorbat. D-asam
askorbat jarang terdapat di alam dan hanya memiliki 10 persen aktivitas asam
askorbat. Biasanya D-asam askorbat ditambah ke dalam bahan pangan sebagai
antioksidan, bukan sebagai sumber asam askorbat (Andarwulan, N. 1992).
Gambar 2.2 Struktur Kimia dari Asam Askorbat
(Poedjiadi, A. 2006)
ηsp = ………(2)
t2 – t1
t1
O
C
C
C
HC
HOCH
CH2OH O HO
2.4.2. Sifat-sifat Asam Askorbat
Asam askorbat dalam bentuk murni merupakan kristal putih tidak berwarna, tidak
berbau, dan mencair pada suhu 190-1920C. Senyawa ini bersifat reduktor kuat dan
mempunyai rasa asam. Asam askorbat sangat mudah larut dalam air ( 1 gram dapat
larut sempurna dalam 3 ml air), sedikit larut dalam alkohol (1 gram dalam 50 gram
alkohol absolute atau 100 ml gliserin) dan tidak larut dalam benzene, eter, kloroform,
minyak dan sejenisnya. Walaupun asam askorbat stabil dalam bentuk kristal tetapi
mudah rusak atau terdegradasi jika berada dalam bentuk larutan, terutama jika
terdapat udara, logam-logam sepeti Cu dan Fe. Sifat yang paling utama dari asam
askorbat adalah kemampuan mereduksi logam, terutama Cu dan Ag (Andarwulan, N.
1992).
2.4.3. Sumber Asam Askorbat
Asam askorbat pada umumnya hanya terdapat di dalam pangan nabati, yaitu sayur dan
buah terutama yang asam, seperti jeruk, nenas, rambutan, pepaya, gandaria, dan tomat.
Asam askorbat juga banyak terdapat di dalam sayuran daun-daunan dan jenis kol.
(Almatsier, S. 1998)
2.4.4. Manfaat Asam Askorbat
Beberapa manfaat dari asam askorbat, yaitu:
1. Asam askorbat dapat memperkuat otot jantung
2. Asam askorbat berperan penting melelui proses metabolisme kolesterol,
karena dalam proses metabolisme kolesterol
3. Asam askorbat dapat meningkatkan laju kolesterol yang dibuang dalam bentuk
asam empedu dan mengatur metabolisme kolesterol
4. Asam askorbat dapat meningkatkan kadar HDL dan berfungsi sebagi pencahar
6. Asam askorbat sangat berperan dalam sintesis kolagen sehingga dapat
mencegah terserang penyakit jantung koroner
7. Sebagai penambah sistem kekebalan tubuh
8. Memperbaiki sel-sel yang rusak akibat radikal bebas
9. Menghambat penuaan dini
10.Berperan dalam pembentukan kolagen yang sangat bermanfaat untuk
penyembuhan luka
11. Menghambat sel kanker, terutama kanker paru-paru, prostate, payudara, usus
besar, empedu dan otak
(http:www.sobatsehat.com/2010/03/21/sejuta-manfaat-vitamin-c-yang-wajib-anda-ketahui/)
2.5. Spektroskopi Infra Merah dan FTIR
Spektroskopi adalah ilmu yang mempelajari segala sesuatu tentang interaksi antara
materi dengan radiasi elektromagnetik (REM). Interaksi yang terjadi dalam
spektroskopi inframerah ini merupakan interaksi dengan REM melalui absorbansi
radiasi. Pancaran inframerah pada umumnya mengacu pada bagian spektrum
elektromagnetik yang terletak diantara daerah tampak dan gelombang mikro. Molekul
menyerap radiasi elektromagnetik dengan panjang gelombang yang khusus.
Absorbansi cahaya ultraviolet mengakibatkan pindahnya sebuah elektron ke orbital
dengan energi yang lebih tinggi. Radiasi inframerah tidak cukup mengandung energi
untuk melakukan eksitasi tersebut, absorbsinya hanya mengakibatkan membesarnya
amflitudo getaran atom-atom yang terikat satu sama lain (Sudarmadji, 1989).
Energi dari kebanyakan vibrasi molekul berhubungan dengan daerah vibrasi
molekul yang dideteksi dan dapat diukur pada spektrofotometer infra merah. Spektra
didaerah infra merah dapat digunakan untuk mempelajari sifat-sifat bahan, perubahan
struktur yang sedikit saja dapat memberikan perubahan yang dapat diamati pada
Menurut Sastrohamidjojo (1992), panjang gelombang yang diserap oleh
berbagai tipe ikatan tergantung pada jenis vibrasi ikatan tersebut. Oleh karena itu
berbagai jenis ikatan mengabsorbsi radiasi inframerah pada panjang gelombang yang
berbeda.
Perubahan ini sangat spesifik dan merupakan sidik jari suatu molekul dengan
membandingkan spektogram yang dihasilkan oleh bahan yang diuji terhadap bahan
yang sudah diketahui secara kualitatif. Penerapan secara kualitatif dapat dilakukan
dengan membandingkan fungsi puncak pada panjang gelombang terkait yang
dihasilkan ole zat-zat yang diujikan dan zat standart. Spectra infra merah ditujukan
terutama untuk senyawa organik yaitu analisis gugus fungsi yang dimiliki oleh
senyawa tersebut (Mulja, M. 1995).
Jumlah energi yang diserap juga bervariasi untuk setiap ikatan. Hal ini
disebabkan karena terjadinya perubahan momen ikatan sewaktu absorbsi. Ikatan
nonpolar (C-H atau C-C) pada umumnya memberikan absorbsi lemah, sedangkan
ikatan polar (C-O) akan terlihat sebagai absorbsi yang kuat.
Spektroskopi FTIR dapat digunakan untuk menganalisa kualitatif maupun
kuantitatif. Analisa kualitatif spektroskopi FTIR secara umum dipergunakan untuk
identifikasi gugus-gugus fungsional yang terdapat dalam suatu senyawa yang
dianalisa (Silverstein, 1986). Dua variasi instrumental dari spektroskopi infra merah
yaitu metode dispersif yang lebih tua, dimana prisma atau kisi dipakai untuk
mendispersikan radiasi infra merah, dan metode Frourier Transform (FT) yang lebih
akhir, yang menggunakan prinsip interferometri.
Kelebihan-kelebihan dari FT-IR mencakup persyaratan ukuran sampel yang
kecil, perkembanagan spektrum yang cepat, dan karena instrumen ini memiliki
komputer yang terdedikasi, kemampuan untuk menyimpan dan memanipulasi
spektrum (Stevens, 2001). Spektroskopi FTIR (fourier transform infrared) pada
prinsipnya sama dengan spektroskopi inframerah, hanya saja spektroskopi FTIR
ditambahkan alat optik (fourier transform) untuk menghasilkan spektra yang lebih
Analisa kuantitatif dari spektroskopi FTIR dapat dilakukan berdasarkan
spektra inframerah yang dihasilkan, salah satu contohnya adalah penentuan derajat
deasetilasi dari kitin dan kitosan menggunakan persamaan Domszy dan Robers (Khan,
2002).
%DD = 1 – [(A1655/ A3450) x 1/1,33] x 100%
Dimana:
A1655 = absorbansi pada bilangan gelombang 1655 cm-1
A3450 = absorbansi pada bilangan gelombang 3450 cm-1
1,33 = tetapan yang diperoleh dari perbandingan A1655/A3450 untuk kitosan dengan
asetilasi penuh
Metode yang digunakan untuk menentukan absorbsi pada spektra inframerah
adalah metode garis dasar (base line). Dengan metode ini , transmitan pada bilangan
gelombang yang diinginkan ditentukan dengan memperbandingkan jarak antara dasar
pita dan puncak pita pada bilangan gelombang yang diinginkan tersebut, yang secara
matematis diberikan melalui persamaan berikut ini:
Karena absorbansi merupakan logaritma negatif dari transmitan, maka absorbansi
dapat dinyatakan sebagai berikut:
Dengan I dan Io merupakan intensitas sisa dan intensitas awal.
I
Transmintan (T) = ……….. (1)
Io
I Io
gelombang tertentu direkam sebagai 100%T (dalam keadaan ideal). Bila suatu
senyawa menyerap radiasi pada suatu panjang gelombang tertentu, intensitas radiasi
yang diteruskan oleh contoh akan berkurang. Ini menyebabkan suatu penurunan %T
dan terlihat didalam spektrum sebagai suatu sumur, yang disebut sebagai puncak
absorpsi atau pita absorpsi. Bagian spektrum dimana %T menunjukkan angka 100
(atau hampir 100) disebut garis dasar (baase line), yang didalam spektrum inframerah
BAB 3
METODE PENELITIAN
3.1. Bahan-bahan
– Kitosan
– Asam askorbat
– Akuadest
3.2. Alat-alat
– Timbangan Elektrik Chyo Electronic Balance
– Pengaduk mekanik Jar Test
– Gelas beaker Pyrex
– Gelas ukur Pyrex
– Labu takar Pyrex
– Plat kaca
– Botol akuadest
– Pipet tetes
3.3. Prosedur Penelitian
3.3.1. Pembuatan Larutan Asam Askorbat 0,25%
Sebanyak 2,5 gram asam askorbat dimasukkan dalam labu takar 1000 mL dan
diencerkan dengan akuadest sampai garis tanda, kemudian dihomogenkan sehingga
diperoleh larutan asam askorbat 0,25%.
3.3.2. Pembuatan Larutan Asam Askorbat 0,50%
Sebanyak 5,0 gram asam askorbat dimasukkan dalam labu takar 1000 mL dan
diencerkan dengan akuadest sampai garis tanda, kemudian dihomogenkan sehingga
diperoleh larutan asam askorbat 0,50%.
3.3.3. Pembuatan Larutan Asam Askorbat 0,75%
Sebanyak 7,5 gram asam askorbat dimasukkan dalam labu takar 1000 mL dan
diencerkan dengan akuadest sampai garis tanda, kemudian dihomogenkan sehingga
diperoleh larutan asam askorbat 0,75%.
3.3.4. Pembuatan Larutan Asam Askorbat 1,00%
Sebanyak 10 gram asam askorbat dimasukkan dalam labu takar 1000 mL dan
diencerkan dengan akuadest sampai garis tanda, kemudian dihomogenkan sehingga
diperoleh larutan asam askorbat 1,00%.
3.3.5. Pembuatan Larutan Asam Askorbat 1,25%
Sebanyak 12,5 gram asam askorbat dimasukkan dalam labu takar 1000 mL dan
diencerkan dengan akuadest sampai garis tanda, kemudian dihomogenkan sehingga
3.3.6. Penentuan Kelarutan Kitosan dalam Larutan Asam Askorbat
Sebanyak 0,5g; 1,0g; 1,5g; 2,0g; 2,5g; 3,0 g kitosan di timbang dan dimasukkan ke
dalam gelas beaker lalu dilarutkan dengan 100mL larutan asam askorbat 0,25%
hingga larutan homogen. Larutan gel kitosan yang terbentuk dituang dalam plat kaca
kemudian dikeringkan pada suhu kamar hingga terbentuk film. Film yang terbentuk
BAB 4
DATA DAN HASIL PEMBAHASAN
4.1. Hasil Penelitian
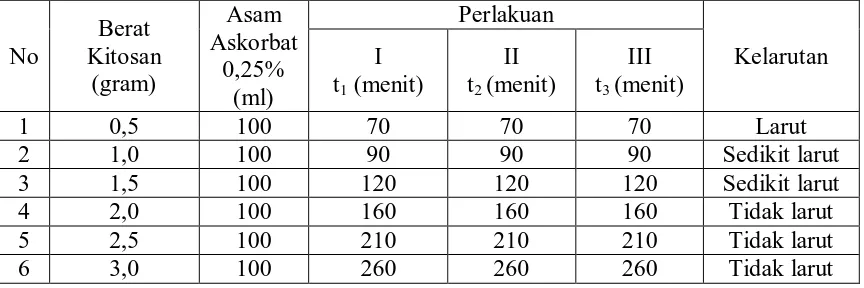
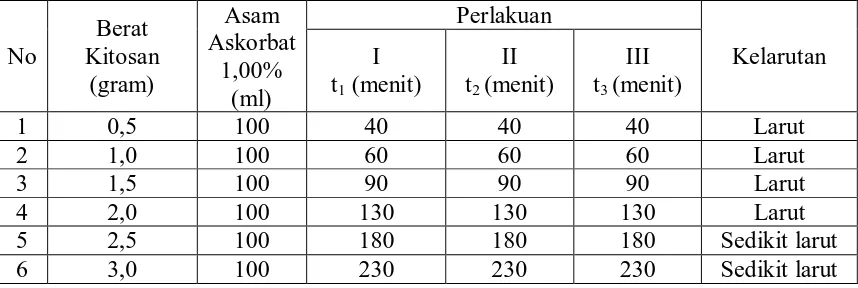
Data hasil pengukuran kelarutan kitosan dalam larutan asam askorbat 0,25%; larutan
asam askorbat 0,50%; larutan asam askorbat 0,75%; larutan asam askorbat 1,00%;
larutan asam askorbat 1,25% dapat dilihat pada tabel sebagai berikut :
Tabel 4.1 Data Hasil Pengukuran Kelarutan Kitosan dalam Larutan Asam
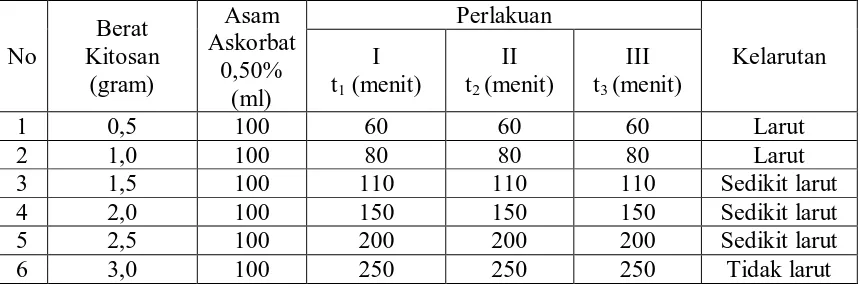
Tabel 4.2 Data Hasil Pengukuran Kelarutan Kitosan dalam Larutan Asam
Tabel 4.3 Data Hasil Pengukuran Kelarutan Kitosan dalam Larutan Asam
Tabel 4.4 Data Hasil Pengukuran Kelarutan Kitosan dalam Larutan Asam
Tabel 4.5 Data Hasil Pengukuran Kelarutan Kitosan dalam Larutan Asam
Askorbat 1,25%
Larut : Campuran homogen antara kitosan dan larutan asam askorbat yang saling melarutkan dan masing-masing zat penyusunnya tidak dapat dibedakan lagi secara fisik.
Sedikit larut : Campuran antara kitosan dengan larutan asam askorbat, dimana campuran tersebut membentuk koloid dalam larutan.
4.2. Pembahasan
4.2.1. Penentuan Derajat Deasetilasi
Analisis kuantitatif dari spektroskopi FT-IR dapat dilakukan berdasarkan
spektrum Infra merah yang dihasilkan, dimana penentuan derajat deasetilasi dari
kitosan menggunakan persamaan Domszy dan Robers (Khan, 2002).
%
A1655 = absorbansi pada bilangan gelombang 1655 cm-1
A3450 = absorbansi pada bilangan gelombang 3450 cm-1
1,33 = tetapan yang diperoleh dari perbandingan A1655/A3450 untuk kitosan dengan
asetilasi penuh
Sebagai contoh perhitungan serbuk kitosan :
Jadi, derajat deasetilasi serbuk kitosan adalah 82,87%.
Sebagai contoh perhitungan kitosan dalam larutan asam askorbat :
Jadi, derajat deasetilasi kitosan dalam larutan asam askorbat adalah 82,82%
4.2.2. Kelarutan Kitosan dalam Larutan Asam Askorbat
Dari tabel 4.1; 4.2; 4.3; 4.4; dan 4.5 dapat dilihat bahwa kelarutan kitosan dengan
variasi berat 0,5g; 1,0g; 1,5g; 2,0g; 2,5g dan 3,0g dalam larutan asam askorbat dengan
variasi konsentrasi 0,25%; 0,50%; 0,75%; 1,00% dan 1,25% memiliki hasil kelarutan
yang berbeda. Dimana dari kelima konsentrasi larutan asam askorbat tersebut yang
memiliki kelarutan kitosan yang baik yaitu pada konsentrasi larutan asam askorbat
1,00% karena konsentrasi tersebut merupakan konsentrasi yang normal untuk
pengukuran kelarutan kitosan dan untuk mengukur berat molekul kitosan.
4.2.3. Analisis Spektrum FT-IR Serbuk Kitosan
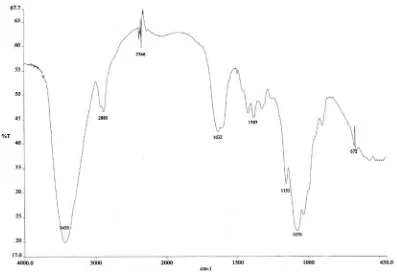
Hasil analisis spektroskopi FT-IR serbuk kitosan dapat dilihat pada gambar 4.1
dibawah ini.
Gambar 4.1 Spektrum FT-IR Serbuk Kitosan
Dari gambar 4.1 diatas diperoleh puncak sebagai berikut : Pita serapan pada bilangan
gelombang 3435 cm-1 menunjukkan adanya gugus hidroksil (-OH). Adanya puncak di
daerah 2880 cm-1 menunjukkan adanya ikatan –CH alifatis. Pita serapan pada bilangan
gelombang 1632 cm-1 menunjukkan adanya gugus C=O, sedangkan pada bilangan
4.2.4. Analisis Spektrum FT-IR Kitosan dalam Larutan Asam Askorbat 1,00%
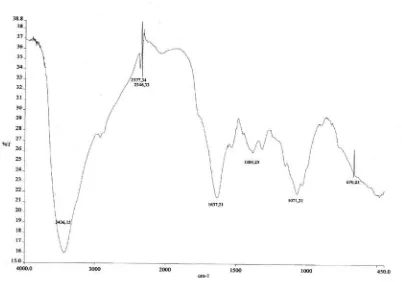
Hasil analisis spektroskopi FT-IR kitosan dalam larutan asam askorbat 1,00% dapat
dilihat pada gambar 4.2 di bawah ini.
Gambar 4.2 Spektrum FT-IR Kitosan dalam Larutan Asam Askorbat 1,00%
Dari gambar 4.2 diatas diperoleh puncak sebagai berikut: Pita serapan pada bilangan
gelombang 3436,15 cm-1 menunjukkan adanya gugus hidroksil (-OH). Adanya puncak
di daerah 2880 cm-1 menunjukkan adanya ikatan –CH alifatis. Pita serapan pada
bilangan gelombang 1637 cm-1 menunjukkan adanya gugus C=O, sedangkan pada
4.2.5. Analisis Spektrum FT-IR Serbuk Asam Askorbat
Hasil analisis spektroskopi FT-IR serbuk asam askorbat dapat dilihat pada gambar 4.3
dibawah ini.
Gambar 4.3 Spektrum FT-IR Serbuk Asam Askorbat
Dari gambar 4.3 diatas diperoleh puncak sebagai berikut: Pita serapan pada bilangan
gelombang 3033 cm-1 menunjukkan adanya gugus hidroksil (-OH). Adanya puncak di
daerah 1754 cm-1 menunjukkan adanya ikatan C=O. Pita serapan pada daerah 1679
cm-1 menunjukkan adanya ikatan C=C, sedangkan pada bilangan gelombang
1497-1458 cm-1 menunjukkan adanya ikatan –CH2, selanjutnya pita serapan pada bilangan
BAB 5
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Dari hasil penelitian yang dilakukan dapat diperoleh kesimpulan bahwa kitosan 1,0
gram larut dalam larutan asam askorbat 1,00%. Hasil uji karakterisasi didapati derajat
deasetilasi kitosan 82,87% dan derajat deasetilasi kitosan dalam larutan asam askorbat
adalah 82,82%. Ini menunjukkan asam askorbat sangat sesuai untuk kelarutan kitosan.
5.2. Saran
Disarankan bagi peneliti selanjutnya agar dapat meneliti kelarutan kitosan dengan
DAFTAR PUSTAKA
Agusnar, H. 2006. Penggunaan Glutaraldehid Kitosan Untuk Menurunkan
Konsentrasi Ion Logam Cr3+ Menggunakan Ekstraksi Fasa Padat Dalam Sistem Aquatik. Disertasi Universitas Sumatera Utara.
Almatsier, S. 1998. Prinsip Dasar Ilmu Gizi. Jakarta: PT. Gramedia Pustaka Utama.
Andarwulan, N. 1992. Kimia Vitamin. Jakarta: C.V. Rajawali.
Fessenden & Fessenden. 1992. Kimia Organik. Jilid I. Jakarta: Erlangga.
Firman. 1999. Kimia Polimer. Bandung: ITB.
Harahap, V.U. 1995. Optimasi Proses Pembuatan Kitosan dari Limbah Udang. Fakultas Teknologi Pertanian IPB. Bogor.
sehat.com/2010/03/21/sejuta-manfaat-vitamin-c-yang-wajib-anda-ketahui Diakses tanggal 21 Maret, 2010.
Khan, A. Peh, K. & Ching, S. 2002. Reporting degree of deaacytelation values of
chitosan : the influence of analytical methods. J. Pawn Pharmaceut Sci 5 (3).
Knoor, D. 1987. Use of Chotonous Polimer in Food, Food Technology, (I), p.85.
Kumar,M.N.V.R. 2000. A Review of Chitin and Chitosan Applications. India: Department of Chemistry, University of Roorkee.
Krissetiana, H. 2004. Kitin dan Kitosan dari Limbah Udang. Suara Merdeka.
Diakses tanggal 17 Mei, 2010.
Manurung, M. 2005. Pembuatan dan Penggunaan Kitosan Manik Sebagai Adsorben
Untuk Menurunkan Kadar Limbah Cair Industri. Skripsi Jurusan Kimia
FMIPA USU.
Mat,B. Zakaria. 1995.Chitin and Chitosan. University Kebangsaan Malaysia.
Mulja, M. 1995. Analisis Instrumental. Surabaya: Airlangga Press.
Sugita, P. 2009. Kitosan: Sumber Biomaterial Masa Depan. Bogor: IPB Press.
Sastrohamidjojo, & Hardjono. 1992. Spektroskopi Inframerah. Yogyakarta: Liberty.
Siverstein, M., Robert, Bassler, Clayton, G., Morril, C., & Trence. 1986. Penyidikan
Spektrometik Senyawa Organik. Jakarta: Erlangga.
Sopyan, I., 2001. Kimia Polimer. Jakarta: Pradnya Paramita.
Stevent, M.P. 2001. Kimia Polimer, Cetakan I, Jakarta: Pradya Paramitha.
Sudarmadji, Slamet, Haryono, Bambang, dan Suhardi. 1989. Analisa Bahan Makanan
dan Pertanian. Yogyakarta: Liberty.