BAB II
TINJAUAN PUSTAKA
2.1. Karakter Fisiologi Kareta. Pembentukan Karet
Biosintesis lateks berlangsung pada sel-sel pembuluh lateks, di dalam jaringan pembuluh lateks pada kulit batang tanaman karet. Metabolisme pembentukan partikel karet (poliisoprena) melalui siklus asam mevalonat yang sangat rumit. Partikel karet itu sendiri terdiri dari 90% berat kering lateks atau 35 - 50% dari berat segar (Jacob et al., 1997).
Tahapan pembentukan glukosa dapat dibedakan atas 4 tahap yakni:
1. Dimulai dari sebuah molekul CO2 dikonversi dari bentuk inorganiknya menjadi molekul
organik melalui pengikatan gula 5C (ribulose bisphosphate atau RuBP). Dikatalisasi oleh enzim RuBP carboxilase (Rubisco) sehingga terbentuk gula 6C, senyawa ini pecah menjadi 3-phosphoglicerate.
2. Tiap molekul 3-phosphoglicerate menerima tambahan grup fosfat sehingga terbentuk 1,3-Bisphosphoglicerate (fosforilasi ATP).
3. Kemudian NADPH dioksidasi dan elektron yang ditransfer ke 1,3-Bisphosphoglicerate memecah molekul dengan tereduksi menjadi gliceraldehide 3-phosphate menjadi bahan untuk pembentukan glukosa.
4. Tahap terakhir dari siklus ini adalah regenerasi RuBP. gliceraldehide 3-phosphate dikonversi menjadi RuBP melalui sebuah seri reaksi yang melibatkan fosforilasi molekul oleh ATP.
Pada proses pembentukan karet, terdapat 2 tahap utama yaitu :
a. Glikolosis
1.
Glikolisis adalah proses pembentukan glukosa
menjadi glukosa - 6 –fosfat.
2.
Selanjutnya glukosa - 6 –fosfat
dipecah
menjadi
Fruktosa 1,6 difosfat.
3.
Lalu
membentuk
3 fosfogliseraldehid (PGAL).
4.
Pada akhir proses glikolisis diperoleh 3 molekul glukosa yaitu 2 molekul asam
piruvat dan 2 molekul NADH, lalu molekul ini merupakan prekusor utama dari
cis-poliisoprena dengan pembentukan energi biokimia berupa ATP serta akumulasi
senyawa pereduksi NAD(P)H. yang berfungsi sebagai sumber elektron berenergi
tinggi dan 2 molekul ATP.
5.
Dan selanjutnya menjadi molekul asetat atau asetil-coA dan membentuk energi (ATP
& NAD(P)H.
b. Anabolisme poliisoprena
1. Asetil-CoA yang dihasilkan dari glikolisis selanjutnya akan menghasilkan isopentenil pirofosfat (IPP) dengang energi ATP & NADPH.
2. 2 Selanjutnya Isopentenil pirofosfat dikatalis oleh enzim isopentenil-difosfat isomerase membentuk dimetilalil pirofosfat (DMAPP).
3. Dan enzim preniltransferase membentuk dimetilalil pirofosfat (DMAPP) dan IPP membentuk partikel karet. (Taiz & Zeiger 1998).
b. Pengaliran Lateks
Tekanan turgor merupakan tekanan isi sel dengan dinding sel. Jumlah isi sel berpengaruh pada besar kecilnya tekanan pada dinding sel. Tekanan turgor akan meningkat seiring dengan meningkatnya kadar air. Tekanan turgor yang besar akan meningkatkan aliran lateks yang keluar dari pembuluh lateks (Gomez, 1983).
Lateks berada dalam pembuluhnya pada tekanan turgor 10 – 14 atm. Pada waktu
penyadapannya, lateks mengalir karena tekanan turgor di dalam sel lebih besar dari pada
tekanan di luar sel. Segera setelah pohon disadap, tekanan turgor menurun dan air dari sel
- sel tetangga menembus dinding pembuluh lateks sehingga lateks mengalir pada irisan
sadap. Lateks mengalir karena tekanan turgor di dalam sel lebih besar dari pada tekanan
di luar sel. Setelah lateks mengalir, tekanan turgor dalam pembuluh akan menurun,
kemudian dinding sel mengkerut dan sebagian pecah.
Pada waktu yang bersamaan air dari dinding sel keluar dan untuk menjaga keseimbangan
air tanaman, dengan cara air masuk ke dalam pembuluh lateks untuk pemulihan
keseimbangan tekanan yang terganggu akibat penyadapan (Lacrotte, 1989).
Atas dasar temuan fisika dan kimia itu penyadapan sebaiknya dilakukan saat
tekanan turgor masih tinggi, yaitu belum terjadi pengurangan isi sel melalui transpirasi.
Peningkatan intensitas sinar matahari, akan menyebabkan membukanya stomata yang
akan mempercepat transpirasi.
Lamanya aliran lateks ditentukan oleh besarnya tekanan turgor dalam pembuluh
lateks dan koagulasi pada alur sadap. Pada saat tanaman karet disadap
tekanan turgor
tetap dipertahankan meskipun kandungan air di jaringan menurun. Hal ini terjadi melalui
penurunan potensial osmotik daun yang disebut penyesuaian osmotik. Penyesuaian
osmotik dapat dilakukan melalui akumulasi atau sintesis zat terlarut yang menurunkan
potensial solut dan mempertahankan turgor sel (Milford,1969). Kandungan osmotikum
yang tinggi dalam lateks seperti sukrosa, kuebrakitol, ion mineral, serta tersedianya air
yang cukup merupakan kondisi ideal agar tekanan turgor mencapai maksimum. Kondisi
tersebut memungkinkan berlangsungnya aliran lateks yang cukup lama serta indeks
penyumbatan (plugging index) rendah sehingga produksi meningkat (Sumarmadji dan
Atminingsih, 2013).
Floem pada kulit karet tidak hanya berfungsi sebagai tempat sintesis lateks,
tetapi juga sebagai saluran untuk transpor asimilat dari daun ke seluruh tanaman
.
Tinggi
rendahnya aliran lateks bergantung pada jenis klon, panjang irisan sadap, interval
penyadapan dan pemberian stimulan. Semakin pendek irisan, tekanan aliran lateks makin
tinggi karena semakin pendek irisan gangguan terhadap angkutan asimilat semakin kecil
(Suhermanto dan Sumarmadji, 2005). Hal sama juga dinyatakan Sumarmadji (2005)
bahwa panjang irisan S/3U d2.ET.2.5% lebih baik dari kontrol S/2 d2 tanpa stimulan.
Pada bagian lain, Sumarmadji
et al.,(2009) menyatakan tidak didapati perbedaan yang
nyata antara irisan Sc20U d3 ET2.5%.Pa0.5.18/y (2w) dan S/4U d3 ET2.5%Pa0.5.18/y
(2w) dengan sistem S/2 d3.ET2.5%.Ga1.0 9/y (m). Hal ini sejalan dengan hasil penelitian
Woelan et al., (2012) pada klon IRR 202, 208, 210 dan 220 yang tergolong sebagai klon
QS
respons terhadap interval penyadapan rendah, sedangkan klon IRR 213 dan 214
sebagai klon SS respon terhadap interval penyadapan tinggi.
2.2. Histologis Kulit Tanaman Karet
Lateks didapati pada hampir di semua bagian organ tanaman karet seperti batang, daun, bunga, buah, dan akar, tetapi paling banyak didapati pada pembuluh lateks berada di jaringan kayu pada bagian kulit batang (Siregar, 1995). Lateks diperoleh dengan cara disadap atau melukai kulit batang tanaman karet hingga pembuluh latisifer terbuka
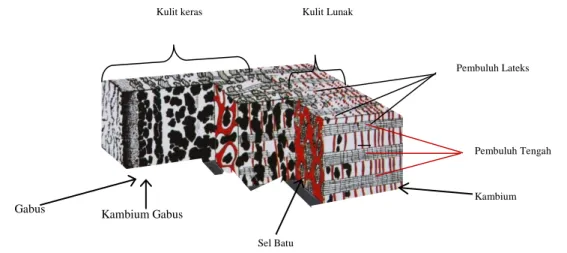
Pada penampang melintang kulit karet, dibagian tengah terdapat jaringan kayu (xylem) yang dilapisi oleh kambium, sedangkan bagian luar dijumpai kulit lunak, menyusul kulit keras. Pada bagian luar dari penampang melintang tersebut terdapat sel gabus, yang dapat dibedakan dari
lapisan lainnya. Pada bagian dalam kulit lunak tersebut terdapat sederetan pembuluh tapis atau floem (Gambar 2.1).
Pembuluh lateks merupakan suatu sistem pembuluh berupa pipa saluran di dalam jaringan floem yang halus dan berada dekat dengan kambium. Secara anatomi, proses awal terbentuknya pembuluh lateks melalui pembentukan sel tunggal, kemudian diikuti dengan pembentukan jaringan pembuluh ( Jacob et al.,1989)
Ketebalan kulit karet dan jumlah baris pembuluh lateks semakin meningkat dengan bertambahnya umur tanaman, walaupun terdapat perbedaan penyebaran pembuluh lateks setiap jenis klon.
Pada umumnya sekitar 30 - 40% pembuluh lateksterletak pada jarak 1 mm dari kambium. Jumlah pembuluh lateks akan menurun dengan semakin jauh dari kambium (Jacob et al., 1989). D’Auzac dan Jacob (1989) juga menemukan hal yang sama, yakni semakin dekat dengan kambium maka pembuluh lateks akan lebih kecil, dengan ukuran 30 µm. Penelitian Santoso (1994) pada 11 jenis klon menyimpulkan bahwa PB 28/59 memiliki jumlah pembuluh lateks lebih tinggi dibandingkan dengan RRIM 600, PR 107, AVROS 2037, GT1 dan RRIM 623.
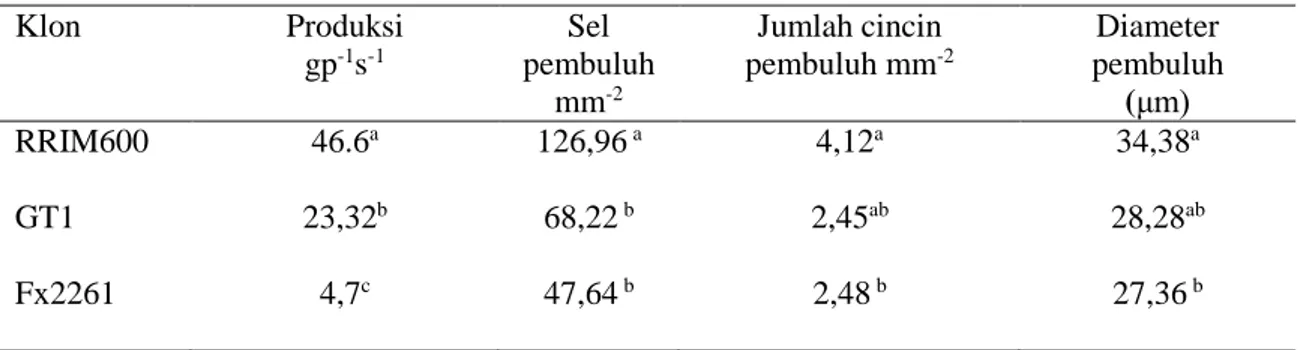
Hasil pengamatan Mesquita et al., (2006) menyatakan bahwa pembuluh lateks dari
beberapa klon karet menunjukkan bahwa pada klon RRIM memiliki produksi, panjang sel
Gambar 2.1. Penampang Kulit Karet Sumber : Jacob et al., 1989
Kambium Sel Batu Kulit keras Kulit keras Kulit Lunak Kulit Lunak Kambium Gabus Gabus Pembuluh Lateks Pembuluh Tengah 14
pembuluh, jumlah cincin dan diameter pembuluh lebih tinggi dibanding klon GT1 dan
Fx2261, semakin besar diameter pembuluh lateks, semakin banyak sel pembuluh dan
jumlah cincin sehingga menyebabkan semakin tingginya produksi (Tabel 2.1).
Tabel 2.1. Pengamatan Histologi Pembuluh Lateks beberapa Klon Karet
Klon Produksi gp-1s-1 Sel pembuluh mm-2 Jumlah cincin pembuluh mm-2 Diameter pembuluh (μm) RRIM600 46.6a 126,96 a 4,12a 34,38a GT1 23,32b 68,22 b 2,45ab 28,28ab Fx2261 4,7c 47,64 b 2,48 b 27,36 b Sumber : Mesquita et al. 2006
Hal ini sejalan dengan pernyataan de Fay dan Jacob, (1989) yangmenyatakan bahwa jumlah baris pembuluh lateks pada prinsipnya merupakan ciri khas suatu klon dan setiap klon karet bervariasi dalam jumlah dan susunan pembuluh lateks. Siregar (1995) menambahkan, bahwa pembuluh lateks berbentuk silindris dengan ukuran dan jumlah yang bervariasi tergantung pada klonnya. Hal ini yang menyebabkan perbedaan potensi produksi antar klon karet. Perkembangan pembuluh lateks tergantung pada tingkat pertumbuhan tanaman, dan faktor lain seperti kepadatan tanaman dan status hara.
Pada tanaman karet umur kurang dari 5 tahun (0-5) pembuluh lateks jaraknya 4-5
mm dari kambium, sedangkan umur 5 tahun (5-10), jarak pembuluh lateks masih dekat
dengan kambium, tetapi belum melebar sampai kambium. Pada karet umur 25 tahun
sudah 75% pembuluh lateks tersebar merata hingga sangat dekat dengan kambium.
Santoso (1994), melaporkan bahwa lateks yang keluar dari karet muda lebih sedikit
mengandung kadar karet kering dibandingkan dengan lateks yang keluar tanaman
berumur 5-10 tahun. Hal ini disebabkan lateks yang berasal dari karet muda lebih banyak
mengandung air, sehingga proses penggumpalan lateks menjadi lebih lama dan viskositas
lateksnya rendah.
Pada tanaman semaian (seedling), semakin keatas batang karet berbentuk
conis.
Semakin tinggi pohon semakin tipis kulitnya. Pembuluh lateks yang dimiliki juga
semakin sedikit. Berbeda halnya jika diamati dari atas ke bawah. Bagian bawah kulit
batang karet lebih tebal dibandingkan dengan bagian atasnya, sehingga jumlah pembuluh
lateks lebih banyak daripada bagian atas.
Pada umumnya tanaman yang berasal dari okulasi (klon), batangnya berbentuk
silindris, sehingga ketebalan kulit di atas pertautan okulasi tidak memiliki perbedaan
jumlah pembuluh lateks pada bagian atas dan bawah (Santoso 1994 ).
2.3. Stimulan Cair dan Gas
Dalam upaya meningkatkan produktivitas tanaman karet, penelitian sistem eksploitasi terus dilakukan untuk mencari metode yang paling tepat untuk menghasilkan produksi yang tinggi dengan terhindar dari stres. Salah satu upaya yang sering dilakukan untuk meningkatkan produksi tersebut adalah dengan menggunakan stimulan (Sumarmadji, 2009). Hal ini juga dijelaskan oleh Junaidi dan Karyudi (2010) bahwa pemakaian stimulan pada pohon karet dewasa, sudah merupakan bagian integral dari sistem sadap terutama pada perkebunan besar.
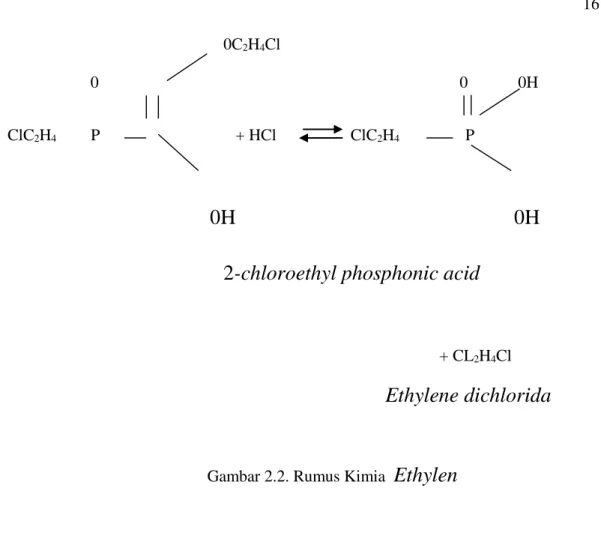
Stimulan merupakan formula yang dibuat dengan berbagai vitamin dan zat pengatur tumbuh yang akan mempengaruhi laju aliran lateks. Bahan aktif untuk stimulan cair yang umum digunakan adalah etefon (2-chloroethyl phosponic acid (Gambar 2.2).
0C2H4Cl
0 0 0H
ClC2H4 P + HCl ClC2H4 P
0H
0H
2
-chloroethyl phosphonic acid
+ CL2H4Cl
Ethylene dichlorida
Gambar 2.2. Rumus Kimia
Ethylen
Mekanisme kerja stimulan cair diawali dengan terhidrolisisnya etepon menghasilkan gas etilen, yang kemudian diserap oleh pembuluh lateks. Gas etilen tersebut akan mendorong stabilitas lateks untuk mengalir lebih lama (misalnya dari 3 - 4 jam menjadi 9 -10 jam), sehingga produksi lateks harian dapat meningkat khususnya pada klon yang responsif.
Pemberian stimulan berpengaruh terhadap fisiologis tanaman karet antara lain: 1). membuat dinding sel elastis, 2). mempercepat dan meningkatkan aktivitas enzim dalam biosintetis lateks, dan 3). membuat daerah aliran lateks menjadi semakin cepat. Ketiga peran stimulan tersebut berpengaruh terhadap peningkatan kecepatan aliran lateks sehingga lateks yang dihasilkan lebih banyak (Eschbach dan Lacrotte, 1989). Penggunaan stimulan sangat penting untuk memperpanjang lama aliran lateks pada tanaman karet. Stimulan dapat meningkatkan produksi lateks dengan cara memperlama aliran lateks, karena penyumbatan pembuluh lateks dapat ditekan (Jacob et al.,1989).
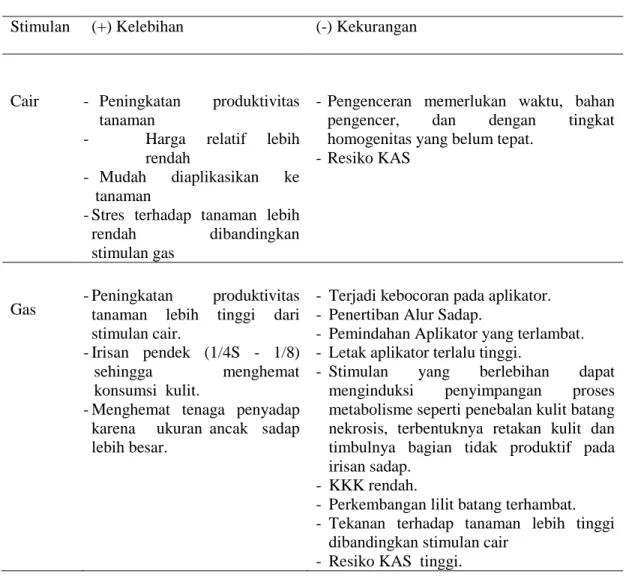
Tabel 2.2. Karakteristik Stimulan Cair dan Gas
Hal ini sejalan hasil penelitian (Yew, 1989), pemberian stimulan dapat meningkatkan produksi mencapai 50%, dibandingkan tanpa penggunaannya.
Rajagopal et al., (2004) menambahkan penggunaan stimulan dapat meningkatkan produksi lateks sekitar 18 -29%. Jetro dan Simon (2007) menambahkan pemberian stimulan etefon 5% akan meningkatkan sukrosa dan tidak menimbulkan KAS.
Selain stimulan cair, sistem sadap pada tanaman karet dapat juga menggunakan stimulan gas. Penggunaan stimulan gas telah sejak lama diperkenalkan, akan tetapi penggunaanya di kalangan pekebun karet tidak sebanyak stimulan cair karena harganya relatif lebih mahal.
Stimulan (+) Kelebihan (-) Kekurangan
Cair - Peningkatan produktivitas tanaman
- Harga relatif lebih rendah
- Mudah diaplikasikan ke tanaman
-Stres terhadap tanaman lebih rendah dibandingkan stimulan gas
-Pengenceran memerlukan waktu, bahan pengencer, dan dengan tingkat homogenitas yang belum tepat.
-Resiko KAS
Gas -Peningkatan tanaman lebih tinggi dari produktivitas stimulan cair.
-Irisan pendek (1/4S - 1/8) sehingga menghemat konsumsi kulit.
-Menghemat tenaga penyadap karena ukuran ancak sadap lebih besar.
- Terjadi kebocoran pada aplikator. - Penertiban Alur Sadap.
- Pemindahan Aplikator yang terlambat. - Letak aplikator terlalu tinggi.
- Stimulan yang berlebihan dapat menginduksi penyimpangan proses metabolisme seperti penebalan kulit batang nekrosis, terbentuknya retakan kulit dan timbulnya bagian tidak produktif pada irisan sadap.
- KKK rendah.
- Perkembangan lilit batang terhambat. - Tekanan terhadap tanaman lebih tinggi
dibandingkan stimulan cair - Resiko KAS tinggi.
Stimulan gas memberikan stres yang lebih besar dibandingkan dengan penggunaan stimulan konvensional. Beberapa kasus dijumpai di tingkat pengguna ketika pemakaian stimulan gas yang tidak terkendali dan tidak sesuai prosedur menyebabkan peningkatan kering alur sadap (KAS). Karakteristik dari stimulan cair dan gas tertera pada Tabel 2.2. (Junaidi et al., 2010).
Pada stimulan cair, aplikasi sesuai perlakuan masih perlu dilakukan pengenceran, karena kosentrasi yang diperdagangkan hanya 10%.
Pengenceran menjadi 2,5% dan 5% memerlukan waktu, bahan pengencer dan tingkat homogenitas yang belum tepat. Pada sisi lain, stimulan cair ini memiliki harga yang relatif lebih murah sehingga mudah diperoleh.
Stimulan gas merupakan senyawa etilen tidak harus melalui proses hidrolisis terlebih dahulu sebelum digunakan, sehingga dapat langsung diaplikasikan ke jaringan tanaman. Karyudi et al., (2006) menyatakan penggunaan gas etilen dapat meningkatkan produktivitas rata – rata 75-100%, karena stimulan dengan bahan aktif gas etilen diserap langsung oleh tanaman karet dengan jumlah yang lebih banyak. Hasil penelitian Sainoi dan Sdoodee (2011) pada berbagai sistem eksploitasi ditemukan hubungan perlakuan S/6 d3 6d/7 ETG 99% 36/y (9d) diperoleh hasil tertinggi.
Pemakaian stimulan gas akan meningkatkan produksi, menghemat konsumsi kulit
dan menurunkan biaya tenaga kerja sehingga keuntungannya maksimum. Semakin
pendek irisan sadap yang dikombinasikan dengan stimulant, maka semakin tinggi
produksi, bila dibandingkan dengan irisan panjang tanpa stimulan. Hal ini sejalan
dengan penelitian Karyudi
et al.,
(2006), Rodrigo
et al., (2006) dan Obouyeba
et al.,
(2009) penggunaan stimulan yang dikombinasikan dengan irisan sadap pendek yaitu
sekitar (S/4 - S/8), meningkatkan produktivitas tanaman dan diharapkan dapat
menghemat pemakaian kulit. Hasil penelitian Junaidi (2013) penggunaan stimulan gas
(S/2Ud3 + stimulan gas) dapat meningkatkan produktivitas tanaman mencapai
200.61% dibandingkan dengan stimulan cair.
Kesalahan aplikasi stimulan dan sistem sadap karet, akan menimbulkan dampak terhadap produksi yang semakin menurun dan singkatnya umur ekonomi tanaman. Sumarmadji dan Atmaningsih, (2013) menyatakan kesalahan dalam sistem eksploitasi seperti panjang irisan dan frekuensi sadap, serta aplikasi stimulant dalam jangka panjang akan menurun produktivitas, sekaligus mempersingkat umur ekonomis. Penggunaan stimulan yang berlebihan dapat menginduksi penyimpangan proses metabolisme, seperti penebalan kulit batang, nekrosis, terbentuknya retakan pada kulit, dan timbulnya bagian tidak produktif pada irisan eksploitasi (Paranjothy et al.,1979). Pemakaian etepon yang melampaui kebutuhan juga mengakibatkan berhentinya aliran lateks yang disebabkan oleh koagulasi partikel karet yang dikenal dengan istilah KAS (Tistama 2009).
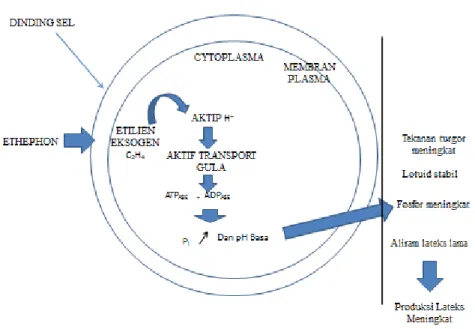
Gambar 2.3. Fisiologi etilen terhadap penundaan penggumpalan pada pembuluh lateks dan masa aliran lateks. Dimodifikasi dari Escbach dan Lacrotte, (1989).
Keutamaan dari etefon adalah potensi kemampuannya melepas etilen kejaringan floem melalui proses hidrolisis (Gambar 2.3). Etilen cenderung menstimulasi pompa proton H+/sukrosa yang
mengaktifkan transport gula ke dalam sel - sel pembuluh lateks. Etilen mengaktifkan pompa - pompa proton ATPase dan Pase maka pH disekitar serum lutoid asam (asidifikasi) dan pH disekitar
sitosol basa (basifikasi), sehingga lutoid stabil.
Peran stabilisasi lutoid sangat penting karena jika lotuid pecah, maka kation - kation akan bereaksi dengan partikel karet yang bermuatan negatif sehingga terjadi koagulasi.Proses koagulasi menyebabkan lateks berhenti menetes (Jacob et al., 1992).
2.3. Hipotesis penelitian
1. Terdapat perbedaan karakter anatomi, morfo- fisiologi lateks dan hasil pada klon PB 260 dan BPM 1 umur 15 tahun.
2. Terdapat pengaruh sistem sadap, aplikasi stimulan terhadap fisiologi lateks klon BPM 1 dan PB 260.