METODE PENELITIAN
Waktu dan Tempat
Penelitian ini dilaksanakan pada bulan September 2016 - Maret 2017 di
Laboratorium Budidaya Hutan Progam Studi Kehutanan, Fakultas Kehutanan dan
Rumah Kaca Fakultas Pertanian, Universitas Sumatera Utara.
Alat dan Bahan
Alat yang digunakan dalam penelitian adalah refraktometer (S/Mill-E salinitas), timbangan (Camry; Model: EK3820), kamera digital, ember, cutter,
gunting, jangka sorong, penggaris, seng, cangkul, micro pipette, pipette tips, botol
kocok, botol ekstrak, kertas saring, corong, oven, RP-18, silika gel TLC/ 2D, hair
drayer, chamber, scanner Canon PIXMA E400, dan alat tulis.
Bahan yang digunakan dalam penelitian adalah propagulR.apiculata yang
sehat dan matang, label nama, pasir sungai (tidak memiliki salinitas), bubuk
garam komersial, botol plastik 1.5 liter, tap water, standar dolichol dan
polyprenol, n-heksan, etanol, KOH, aquades, toluen, etil asetat, aseton, silika gel
60-TLC, dan iodin.
Prosedur Penelitian
Propagul R.apiculata yang matang dan sehat dikumpulkan dari Pangkalan
Susu, Sumatera Utara yang kemudian ditanam dalam pot botol dengan pasir di bawah variasi salinitas selama 3 bulan di Rumah Kaca Fakultas Pertanian, Universitas Sumatera Utara. Propagul dewasa R. apiculata berwarna hijau
protokol pabrik. Setiap pot diisi dengan 1.000 mℓ solusi air laut buatan. Salinitas
dalam penelitian ini didefinisikan sebagai massa bubuk garam / massa larutan (Basyuni et al., 2009). Dalam setiap pot, perlakuan variasi salinitas diperiksa
setiap minggu selama percobaan menggunakan refraktometer dan diganti dengan solusi air laut yang baru untuk mempertahankan variasi salinitas yang konstan selama penelitian.
Setelah 3 bulan budidaya di bawah variasi salinitas, semai R. apiculata
kemudian dibagi menjadi dua kelompok perlakuan yang kemudian ditumbuhkan
selama 3 bulan. Kelompok pertama terus menerus dalam variasi salinitas dan kelompok kedua dalam adaptasi air tawar. Pada masa adaptasi air tawar, air tawar diaplikasikan beberapa kali untuk membersihkan solusi salinitas dari sistem akar
sebelum masa adaptasi air tawar dimulai. Setelah 6 bulan pertumbuhan semai
R. apiculata dipanen dan dicuci daun, batang, dan akar yang kemudian disimpan
pada suhu -4ºC untuk analisis lebih lanjut.
Pengukuran pertumbuhan
Pertumbuhan semai R. apiculata dibawah salinitas dan adaptasi air tawar
ditentukan oleh tinggi dan diameter semai R.apiculata . Dengan demikian, tinggi dan diameter semai R. apiculata setelah 6 bulan merupakan parameter pertumbuhan dalam penelitian ini.
Pengukuran jumlah dan luas daun
Perhitungan jumlah daun semai R. apiculata dilakukan pada usia 6 bulan
R. apiculata kemudian dihitung luas daun menggunakan software ImageJ
(Scheneider et al., 2012).
Pengukuran biomassa
Pengukuran biomassa semai R. apiculata dilakukan dengan menggunakan teknik sampling destruktif. Semai R. apiculata dipisahkan menjadi komponen daun, batang, dan akar untuk ditimbang sebelum pengeringan. Pengukuran
biomassa semai R. apiculata dilakukan dengan mengukur berat kering daun, batang, dan akar dengan menggunakan neraca analitik setelah dilakukan
pengeringan dengan oven pada suhu 75ºC selama 48 jam.
Analisis statistik
Pengukuran pertumbuhan dan biomassa semai R. apiculata menggunakan
analisis statistik Rancangan Acak Lengkap (RAL) dengan 5 taraf perbandingan
variasi salinitas 0.0%, 0.5%, 1.5%, 2.0%, dan 3.0%.
Model linear RAL:
Yij = μ + τi + εij Keterangan :
Yij = hasil pengamatan pada perlakuan ke-i dan ulangan ke-j
μ = nilai rataan umum (mean)
τi = pengaruh faktor perlakuan ke-i
εij = pengaruh galat perlakuan ke-i ulangan ke-j
i = 1, 2, 3, 4, 5
j = 1, 2, 3, 4, 5, 6, 7, 8, 9, 10
Data pengukuran pertumbuhan dan biomassa semai R. apiculata dianalisis
membandingkan perlakuan variasi salinitas terhadap kontrol. Nilai P<0.05
dipakai sebagai batas untuk menunjukkan pengaruh perlakuan.
Bahan tanaman
Daun dan akar semai R. apiculata yang telah dipanen dari Rumah Kaca Fakultas Pertanian, Universitas Sumatera Utara dikumpulkan. Semua sampel
segar disimpan di lemari es sampai bahan tanaman digunakan untuk dianalisis.
Isolasi polyisoprenoid alkohol
Daun dan akar semai R. apiculata dikeringkan pada suhu 60°C-75°C
selama 1-2 hari. Daun dan akar semai R.apiculata yang sudah kering dihancurkan
menjadi bubuk halus kemudian direndam dalam pelarut kloroform / metanol (2:1,
vol/vol) selama 48 jam. Ekstrak lipid dari daun dan akar semai R. apiculata
disaponifikasi pada suhu 65°C selama 24 jam dalam kosentrasi 0.45 g KOH, 2 ml
etanol, dan 2 ml aquades. NSL (non saponifiable lipid) jaringan daun dan akar
semai R. apiculata kemudian dilarutkan dengan n-heksan dan siap untuk
dianalisis (Kurisaki et al., 1997; Sagami et al., 1992).
Analisis dengan dua dimensi kromatografi
Dimensi pertama TLC dilakukan selama 60 menit diatas silika-gel
(20 x 3 cm) dengan sistem pelarut toluene-etil asetat (9:1) (Sagami et al., 1992).
Tepi longitudinal dari dimensi pertama TLC dengan lebar 1 cm dan zona
konsentrasi dari fase reverse C-18 TLC yang dijepit dengan cara menggunakan
dua magnet batangan (4.0 x 1.1 x 0.8 cm) dengan menghadap setiap fase gel. Plat
TLC yang terikat kemudian dikembangkan tegak lurus ke dimensi pertama untuk
Dimensi kedua fase reverse RP-18 silika-gel TLC dilakukan dengan
pelarut aseton selama 30 menit. Posisi polyisoprenoid alkohol dipisahkan dan
dikembangkan oleh silika-gel dua dimensi TLC, kemudian diidentifikasi dan
divisualisasikan dengan uap yodium (iodine vapor). Gambar kromatografi yang
diperoleh kemudian discan. Konsentrasi polyprenol dan dolichol yang terdeteksi
pada HPTLC RP-18 diukur dengan menggunakan ImageJ dengan standar dolichol
HASIL DAN PEMBAHASAN
Efek salinitas dan adaptasi air tawarpada pertumbuhan semai R. apiculata
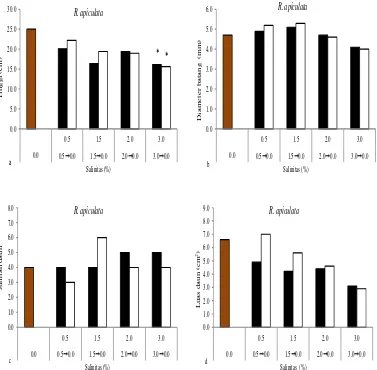
Parameter pertumbuhan diukur berdasarkan tinggi dan diameter semai
R. apiculata. Tinggi semai R. apiculata secara signifikan tumbuh pada konsentrasi
3.0% dan 3.0% → 0.0% (Gambar 1a). Semai tertinggi R. apiculata sebesar 24.9 cm pada salinitas 0.0 % dan terendah sebesar 15.6 cm pada salinitas
3.0% → 0.0% serta diameter tertinggi R. apiculata sebesar 5.3 mm pada salinitas 1.5% → 0.0% dan terendah sebesar 4.0 mm pada salinitas 3.0% → 0.0%. Dari
data diatas dapat disarankan bahwa semai R. apiculata mengalami penurunan
pertumbuhan seiring dengan tingginya salinitas. Pada umumnya mangrove toleran
terhadap salinitas tinggi tetapi toleransi terhadap salinitas antar jenis mangrove
bervariasi. Sebagai contoh jenis R. apiculata tumbuh baik pada salinitas 1.5%
(Kathiresan dan Thangam, 1990; Kathiresan et al., 1996).
Penelitian Basyuni et al., (2014)melaporkan bahwa R. stylosa mengalami
penurunan pertumbuhan pada salinitas lebih dari 0.5% tetapi A. marina tumbuh
baik pada salinitas 2.0% dan akan menurun pertumbuhannya jika salinitas lebih
dari 2.0%. Fakta eksperimental ini mengindikasikan bahwa pada salinitas tinggi,
mangrove menghabiskan energi lebih untuk memelihara keseimbangan air dan
konsentrasi ion dibandingkan untuk produksi primer dan pertumbuhan
(Chlough, 1984).
Pada mangrove, pengeluaran Na+ dari xilem dilakukan melalui adaptasi
anatomi yang mereduksi atau mencegah pergerakan apoplastik larutan dari luar
akar ke xilem untuk memastikan bahwa membran seluler dan transporter dapat
Kemampuan metabolisme tanaman akan terganggu jika konsentrasi garam tinggi.
Garam akan terkonsentrasi di vakuola dan solusi organik yang sesuai untuk
tanaman akan terakumulasi di sitoplasma (Flowers et al., 2015). Peningkatan
salinitas akan menghambat pertumbuhan semai mangrove. Basyuni et al., (2009)
menguji penambahan terpenoid mRNA sintesis untuk melihat pengaruhnya
terhadap salinitas pada K. candel dan B. gymnorrhiza dengan hasil terpenoid dapat
mengatasi cekaman salinitas.
0.0
Efek salinitas dan adaptasi air tawarpada jumlah daun dan luas daun semai R. apiculata
Salinitas dan adaptasi air tawar tidak memiliki efek yang tetap pada jumlah
daun dan luas daun semai R. apiculata (Gambar 1 c-d). Perbedaan jumlah daun
dan luas daun semai R. apiculata secara statistik tidak ditemukan. Jumlah daun
semai R. apiculata tertinggi sebanyak 6 helai daun pada salinitas 1.5% → 0.0 %
dan terendah sebanyak 3 helai daun pada salinitas 0.5% → 0.0% ser ta luas daun tertinggi R. apiculata sebesar 6.8 cm2 pada salinitas 0.5% → 0.0% dan terendah
sebesar 3.1 cm2 pada salinitas 3.0%. Hasil ini sesuai dengan penelitian
Kathiresan dan Rajendran (2002) yang menyatakan bahwa salinitas tidak memiliki
efek pada jumlah dan dan luas daun pada semai R. mucronata di India.
Efek salinitas dan adaptasi air tawar pada biomassa semai R. apiculata
Biomassa semai R. apiculata dengan variasi salinitas dan adaptasi air
tawar dapat dilihat pada Gambar 2. Perbedaan berat basah dan berat kering daun
dan akar semai R. apiculata dibawah pengaruh salinitas dan adaptasi air tawar
secara statistik tidak ditemukan (Gambar 2 a-b e-f).
Perbedaan secara statistik juga tidak ditemukan pada berat basah dan berat
kering batang semai R. apiculata kecuali pada salinitas 3.0% dan 3.0% → 0.0% untuk berat basah batang serta salinitas 3.0% → 0.0% untuk berat kering batang
semai R. apiculata terdapat perbedaan yang signifikan (Gambar 2 c-d). Berat
basah daun semai R. apiculata tertinggi sebesar 7.4 g pada salinitas 1.5% → 0.0%
R. apiculata tertinggi sebesar 2.2 g pada salinitas 0.0 % dan sebesar 0.9 g pada
salinitas 3.0% → 0.0% sedangkan berat kering batang semai R. apiculata
tertinggi sebesar 1.5 g pada salinitas 0.0 % dan terendah sebesar 0.4 g pada
salinitas 3.0% → 0.0%. Berat basah akar semai R. apiculata sebesar 5.3 g pada salinitas 1.5% → 0.0 % dan terendah sebesar 1.1 g pada salinitas 3.0% → 0.0% sedangkan berat kering akar semai R. apiculata tertinggi sebesar 2.5 g pada
salinitas 0.5% → 0.0% dan terendah 0.4 g pada salinitas 3.0% → 0.0%. Hal ini sesuai dengan studi Lin dan Sternbberg (1993) yang melaporkan bahwa fluktuasi
salinitas memiliki dampak negatif yang signifikan pada fotosintesis dan
pertumbuhan.
Analisis polyisoprenoid pada jaringan daun dan akar semai R. apiculata
Analisis polyisoprenoid semai pada jaringan daun dan akar semai
R. apiculata dilakukan dengan dua dimensi TLC (Sagami et al., 1992) untuk
memisahkan polyisoprenoid ke dalam keluarga polyprenol dan dolichol. Tabel 1
dan 2 meringkaskan hasil penelitian secara analitikal distribusi polyprenol dan
atau dolichol dan panjang rantai karbon setiap keluarga polyprenol dan dolichol.
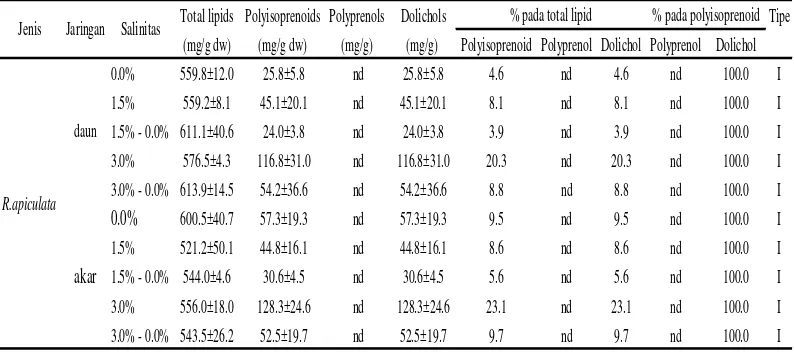
Tabel 1. Nilai total lipid dan distribusi polyprenol dan dolichol pada jaringan akar dan daun semai R.apiculata
Total lipids Polyisoprenoids Polyprenols Dolichols Tipe (mg/g dw) (mg/g dw) (mg/g) (mg/g) Polyisoprenoid Polyprenol Dolichol Polyprenol Dolichol 0.0% 559.8±12.0 25.8±5.8 nd 25.8±5.8 4.6 nd 4.6 nd 100.0 I 1.5% 559.2±8.1 45.1±20.1 nd 45.1±20.1 8.1 nd 8.1 nd 100.0 I 1.5% - 0.0% 611.1±40.6 24.0±3.8 nd 24.0±3.8 3.9 nd 3.9 nd 100.0 I 3.0% 576.5±4.3 116.8±31.0 nd 116.8±31.0 20.3 nd 20.3 nd 100.0 I 3.0% - 0.0% 613.9±14.5 54.2±36.6 nd 54.2±36.6 8.8 nd 8.8 nd 100.0 I
0.0% 600.5±40.7 57.3±19.3 nd 57.3±19.3 9.5 nd 9.5 nd 100.0 I 1.5% 521.2±50.1 44.8±16.1 nd 44.8±16.1 8.6 nd 8.6 nd 100.0 I 1.5% - 0.0% 544.0±4.6 30.6±4.5 nd 30.6±4.5 5.6 nd 5.6 nd 100.0 I 3.0% 556.0±18.0 128.3±24.6 nd 128.3±24.6 23.1 nd 23.1 nd 100.0 I 3.0% - 0.0% 543.5±26.2 52.5±19.7 nd 52.5±19.7 9.7 nd 9.7 nd 100.0 I
R.apiculata
daun
Jenis Jaringan Salinitas % pada total lipid % pada polyisoprenoid
akar
Nilai total lipid pada jaringan daun semai R. apiculata (Tabel 1) berkisar
dari 559.2 - 613.9 mg g-1 berat kering dengan nilai rata-rata 584.1 mg g-1 berat
kering dengan yang terendah serta tertinggi terdapat pada salinitas 1.5% dan
salinitas 3.0% → 0.0%. Perbanding nilai total lipid pada jaringan akar semai
R. apiculata berkisar dari 521.2 – 600.5 mg g-1 berat kering dengan nilai rata-rata
553.0 mg g-1 berat kering dengan yang terendah serta tertinggi terdapat pada
salinitas 1.5% dan salinitas 0.0%. Secara kuantitatif, polyisoprenoid tertinggi
terdapat pada jaringan akar semai R. apiculata (128.3 mg g-1 berat kering pada
salinitas 3.0%). Nilai polyisoprenoid terendah terdapat pada jaringan daun semai
R. apiculata (24.0 mg g-1 berat kering pada salinitas 1.5% → 0.0%). Cekaman salinitas mempengaruhi semua proses utama seperti pertumbuhan, fotosintesis,
sintesis protein, dan energi serta metabolisme lipid (Parida dan Das, 2005).
Distribusi metabolit sekunder di tanaman jauh lebih terbatas daripada
metabolit primer. Produksi senyawa metabolit sekunder terkadang rendah (< 1%
berat kering) dan tergantung dari jenis, fisiologi, serta perkembangan tanaman
(Zhong, 2011). Distribusi polyprenol dan dolichol di daun dapat diklasifikasikan
kedalam tiga tipe (I, II, III) (Basyuni et al., 2016). Tipe I, dolichol mendominasi
polyprenol (lebih dari 90.0%). Pada penelitian ini dolichol ditemukan pada semua
jaringan daun dan akar R. apiculata (Tabel 1). Hal ini sesuai dengan studi
Skorupinska et al., (2003) yang menyatakan bahwa pemisahan keluarga
polyisoprenoid alkohol dengan kromatografi menunjukkan bahwa akar C. geoides
terakumulasi campuran alkohol jenuh dan tak jenuh, dengan dolichol (α-jenuh)
sebagai senyawa dominan utama (Dol-16 sebagai bentuk dominasi). Sedangkan
geoides. Dominasi utama polyisoprenoid di akar A. marina, B. gymnorrhiza, E.
agallocha, H. littoralis, dan S. alba ditemukan dolichol lebih dominan daripada
polyprenol, sama seperti yang ditemukan pada tipe-I di daun. Pada A. marina,
E. agallocha, H. littoralis, dan S. alba ditemukan dolichol tanpa polyprenol.
Analisis polyisoprenoid di daun mangrove, polyisoprenoid alkohol utama bukan
polyprenol melainkan dolichol yang terdeteksi di daun A. marina dan
B. gymnorrhiza, dan daun tua B. gymnorrhiza. Pada daun B. gymnorrhiza
senyawa polyprenol tidak terdeteksi (Basyuni et al., 2016). Tipe II, polyprenol
dan dolichol sama hadir. Pada penelitian ini polyprenol dan dolichol
sama-sama yang hadir tidak ditemukan pada jaringan akar dan daun semai R. apiculata.
Tipe III, polyprenol mendominasi dolichol tidak ditemukan. Pada penelitian ini
polyprenol yang mendominasi dolichol pada jaringan akar dan daun semai
R. apiculata tidak ditemui.
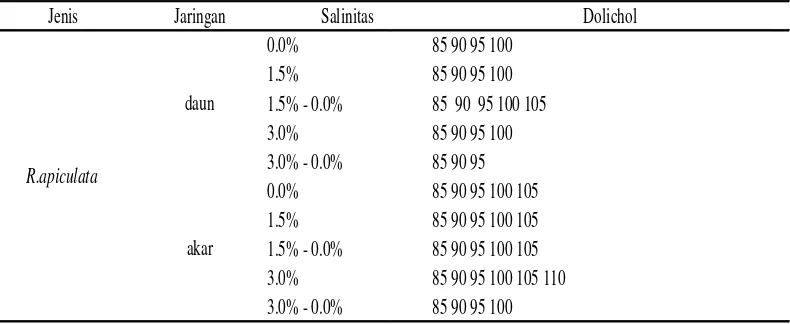
Tabel 2. Panjang rantai karbon dolichol pada jaringan akar dan daun semai R.apiculata*
Jenis Jaringan Salinitas Dolichol
*Angka mengacu pada panjang rantai karbon polyisoprenoid alkohol
Tabel 2 dan Gambar 3 menggambarkan distribusi senyawa dolichol pada
jaringan daun semai R. apiculata dengan panjang rantai karbon C85-C100, C85-C100,
C85-C105, C85-C100, C85-C95 ditemukan salinitas 0.0%, 1.5% , 1.5% → 0.0%, 3.0%,
semai R. apiculata dapat dilihat pada Tabel 2 dan Gambar 4 dengan panjang
rantai karbon C85-C105, C85-C105, C85-C105, C85-C110, C85-C100 ditemukan salinitas
0.0%, 1.5% , 1.5% → 0.0%, 3.0%, dan 3.0% → 0.0%. Dari tabel 2 juga
menunjukkan bahwa dolichol mendominasi di jaringan akar semai R. apiculata
dengan panjang rantai karbon C85-C110 (salinitas 3.0%). Sedangkan senyawa
polyprenol tidak ditemukan baik pada jaringan daun maupun akar semai
R. apiculata.
Gambar 4. Kromatografi lapis tipis dua dimensi (2D-TLC) polyisoprenoid alkohol dari jaringan akar semai R. apiculata salinitas 0.0% (A), 1.5% (B), 1.5% → 0.0% (C), 3.0% (D), 3.0% → 0.0% (E). Angka karbon mengacu pada panjang rantai karbon polyisoprenoid alkohol.
Perbedaan panjang rantai polyisoprenoid yang terdapat pada daun dan akar
semai R. apiculata dapat diakibatkan oleh beberapa faktor antara lain peningkatan
umur (penuaan jaringan) (Swierzewski dan Danikiewicz, 2005), cekaman salinitas
(Oku et al., 2003), perbedaan jaringan (Tateyama et al., 1999;
Sumacz dan Swiezewska, 2011), dan cahaya (Swierzewski dan Danikiewicz,
2005); Basyuni et al., 2012). Panjang rantai dolichol bervariasi dari setiap
jaringan pada jenis tanaman yang sama dan muncul dari keluarga yang berbeda
(Tateyama et al., 1999). Di akar, dominasi utama dolichol melebihi polyprenol
ditemui di Ae. corniculatum, Av. alba, Av. lanata, Av. officinalis, B. parviflora,
C. tagal, N. fruticans, R.apiculata, R. mucronata, S. caseolaris, dan X.granatum
sama dengan ditemukan di daun dengan tipe-I. Kehadiran dolichol di semua
jaringan tanaman (jaringan daun, akar, dan bunga) menyatakan secara tidak
langsung bahwa polyprenol mungkin tidak berperan penting dalam mangrove,
meskipun fungsi dari polyprenol di dalam dunia tumbuhan belum jelas
(Basyuni et al., 2017).
Distribusi dolichol ditemukan di semua jaringan tumbuhan, yang
mengindikasikan bahwa dolichol digunakan sebagai gula-pembawa lipid didalam
biosintesis N-glikoprotein (Kurisaki et al., 1997; Pattison dan Amtmann, 2009).
Dolichol banyak terlibat di dalam proses selular. Peran dolichol di dalam
glikosilasi protein dan modifikasi lainnya, dolichol bebas juga memiliki fungsi
biologis penting sebagai lipid (Chojnacki dan Dallner, 1988; Bizzarri et al., 2003).
Polyprenol reduktase mungkin aktif di daun mangrove untuk mengkatalis reduksi
polyprenol ke dolichol. Kehadiran dominasi dolichol mungkin merupakan hasil
dari kondisi iklim tropika atau sub tropika (Basyuni et al., 2012; 2016). Mutasi
yag terjadi pada STT3a pada Arabidopsis, sebuah sub unit dari
oligosaccharyltransferase yang rumit bertanggung jawab untuk protein
N-glikosilasi yang juga berdampak pada dinding sel, terutama dibawah tekanan
KESIMPULAN DAN SARAN
Pertumbuhan terbaik semai R. apiculata terdapat pada salinitas 1.5 %.
Distribusi polyprenol dan dolichol pada jaringan akar dan daun R. apiculata
termasuk tipe I dengan panjang rantai karbon C85-C100, C85-C100, C85-C105,
C85-C100, C85-C95 pada jaringan daun serta panjang rantai karbon C85-C105,
C85-C105, C85-C105, C85-C110, C85-C100 pada jaringan akar pada salinitas 0.0%,
1.5%, 1.5% → 0.0%, 3.0%, dan 3.0% → 0.0%.
Saran
Perlunya dilakukan studi lanjut terhadap pertumbuhan dan senyawa