BAB II
TINJAUAN PUSTAKA 2.1 Uraian Sotong
Sotong merupakan moluska yang termasuk kelas cephalopoda (kaki hewan terletak di kepala) yang terdiri dari cangkang internal yang terletak didalam mantel, berwarna putih, berbentuk oval dan tebal, serta terbuat dari kapur. Tubuh relatif pendek menyerupai kantung. Mantelnya berwarna merah jambu kehitaman dan di selubungi selaput tipis dan pada kedua sisinya terdapat sirip lateral yang memanjang dari ujung dorsal sampai ventral. (Oemarjati, 1990).
Sotong hidup didasar laut, yang memakan hewan Avertebrata yang berada diatas permukaan dasar laut, seperti ikan-ikan kecil, krustacea, udang dan kepiting. Sotong banyak mengandung jenis asam amino esensial yang penting bagi manusia serta mengandung asam lemak tidak jenuh.
Adapun taksonomi dari sotong adalah sebagai berikut: Kingdom : Animalia
Filum : Moluska Kelas : Cephalopoda Sub kelas : Coleoidea. Ordo : Sepioidea Genus : Sepia
2.2 Pencemaran Air Dan Lingkungan
Kegiatan industri dan teknologi dapat memberikan dampak langsung, disamping juga memberikan dampak tak langsung. Dikatakan dampak langsung apabila akibat kegiatan industru dan teknologi tersebut dapat langsung dirasakan oleh manusia. Dampak langsung yang bersifat positif memang diharapkan. Akan tetapi dampak langsung yang bersifat negatif, yang mengurangi kualitas hidup manusia, harus dihindari atau dikurangi (Wardhana, 2001).
Air merupakan zat yang penting dalam kehidupan makhluk hidup. Apabila air sudah tercemar logam-logam yang berbahaya akan mengakibatkan hal-hal yang buruk bagi kehidupan (Darmono, 1995).
Berbagai macam kegiatan industri dan tekhnologi yang ada saat ini apabila tidak disertai dengan program pengelolaan limbah yang baik akan memungkinkan terjadinya pencemaran air, baik secara langsung maupun secara tidak langsung. Bahan buangan dan air limbah yang berasal dari kegiatan industri adalah penyebab utama terjadinya pencemaran air.
Komponen pencemar air tersebut terdiri dari bahan buangan padat, bahan buangan organic, bahan buangan anorganik, bahan buangan olahan bahan makanan, bahan buangan cairan berminyak, bahan buangan zat kimia.
Umumnya limbah B3 adalah senyawa organik. Namun, ada juga yang berbentuk bahan anorganik. Limbah dalam bentuk anorganik dapat menimbulkan bahaya karena sifatnya yang reaktif, beracun atau mengandung elemen-elemen yang dipandang beracun, misalnya logam berat (Supardi,1985). Bahan buangan anorganik pada umumnya berupa limbah yang tidak dapat membusuk dan sulit didegradasi oleh mikroorganisme. Apabila bahan buangan anorganik ini masuk ke
air lingkungan maka akan terjadi peningkatan jumlah ion logam didalam air. Bahan buangan organik biasanya berasal dari industri yang melibatkan penggunaan unsur-unsur logam seperti timbal (Pb), Arsen (As), Kadmium (Cd), Air raksa (Hg), Krom (Cr) dan lain-lain (Wardhana, 2001).
Air sering tercemar oleh berbagai komponen anorganik, diantaranya berbagai jenis logam berat yang berbahaya, yang beberapa diantaranya banyak digunakan dalam berbagai keperluan sehingga diproduksi secara kontiniu dalam skala industri. Industri-industri logam berat tersebut harus mendapatkan pengawasan yang ketat sehingga tidak membahayakan bagi para pekerja maupun lingkungan sekitarnya.
Pencemaran logam berat terhadap alam lingkungan merupakan suatau proses yang erat hubungannya dengan penggunaan logam tersebut oleh manusia. Pada awalnya penggunaan logam sebagai alat, belum di ketahui pengaruh pencemaran terhadap lingkungan. Proses oksidasi dari logam yang menyebabkan perkaratan sebetulnya merupakan tanda-tanda adanya hal tersebut diatas. Tahun demi tahun ilmu kimia berkembang dengan cepat dan dengan mulai ditemukannya garam logam (HgNO3, HgCl, CdCl, dan lain-lain). (Darmono, 1995)
Pada laut lepas, kontaminasi logam biasanya terjadi secara langsung dari atmosfer atau karena tumpahan minyak dari kapal tanker yang melewatinya, sedangkan di daerah sekitar pantai kontaminasi logam kebanyakkan berasal dari muara sungai yang kontaminasi logam kebanyakan berasal dari muara sungai yang terkontaminasi oleh limbah buangan industri atau pertambangan. Jenis air mempengaruhi kandungan logam di dalamnya (air tawar, air payau dan air laut). Air sungai di daerah hulu mungkin kandungan logamnya akan berbeda dengan air
sungai dekat muara. Hal ini disebabkan dalam perjalanan air tersebut mengalami beberapa kontaminasi baik karena erosi maupun pencemaran dari sepanjang tepi sungai. (Darmono, 1995).
2.3. Toksisitas Logam Pada Jenis Krustasea
Dalam rangka analisis keadaan lingkungan, masalah indicator biologis perlu diketahui dan ditentukan. Indikator biologis dalam hal ini merupakan petunjuk ada tidaknya kenaikan keadaan lingkungan dari keadaan garis dasar, melalui analisa kandungan logam atau kandungan senyawa kimia tertentu yang terdapat di dalam hewan maupun tanaman. Indikator biologis dapat ditentukan dari hewan atau tanaman yang terletak pada daur pencemaran lingkungan sebelum sampai kepada manusia. Apabila pencemaran lingkungan diperkirakan melalui jalur air maka indicator biologisnya dapat ditentukan melalui hewan tanaman yang hidup atau tumbuh di air, baik air sungai, air danau maupun air laut. Indikator biologis yang ada pada jalur air dan mungkin akan sampai kepada manusia adalah :
1. Phytoplankton 2. Zooplankton 3. Mollusca 4. Krustacea
5. Ikan dan sejenisnya (Wardhana, 2001)
Jenis krustasea yang hidup di dalam air terdiri dari atas banyak spesies, seperti udang, kepiting dan lobster yang biasanya hidup didasar air. Jenis organisme ini pergerakannya relatif tidak secepat jenis ikan untuk dapat menghindari pengaruh polusi logam dalam air. Karena bergerak dan mencari
makan di dasar air, sedangkan lokasi tersebut merupakan tempat endapan dari berbagai jenis limbah, maka jenis krustasea ini merupakan indikator yang baik untuk mengetahui terjadinya polusi lingkungan (Darmono, 1995)
Daya toksisitas suatu logam berat juga sangat bergantung pada kualitas lingkungan tempat hewan krustasea air ini hidup. Hal tersebut terjadi terutama pada kadar logam yang tidak terlalu tinggi di dalam air, yaitu dosis subletal atau subtoksik. Pengaruh lingkungan itu sendiri terdiri dari lingkungan fisik seperti suhu air atau lingkungan kimiawi, seperti kadar garam dan oksigen terlarut (Darmono, 2001).
2.4 Logam Berat
Disebut logam berat berbahaya karena memiliki rapat massa tinggi dan sejumlah konsentrasi kecil dapat bersifat racun dan berbahaya. Logam berat merupakan komponen alami tanah. Elemen ini tidak dapat didegradasi maupun dihancurkan. Logam berat dapat masuk ke dalam tubuh manusia lewat makanan, air minum, atau melalui udara (Martaningtyas, 2005).
Arsen (AS), merkuri (Hg), kadmium (Cd), timbal (Pb), adalah jenis logam yang termasuk kelompok logam yang beracun dan berbahaya bagi kehidupan makhluk hidup. Beberapa logam lain yang juga cukup berbahaya aluminium (Al), kromium (Cr).
Logam berat menjadi berbahaya disebabkan sistem bioakumulasi. Bioakumulasi berarti peningkatan konsentrasi unsur kimia tersebut dalam tubuh makhluk hidup sesuai piramida makanan. Akumulasi atau peningkatan konsentrasi logam berat di alam mengakibatkan konsentrasi logam berat di tubuh manusia adalah tertinggi. Jumlah yang terakumulasi setara dengan jumlah logam
berat yang tersimpan dalam tubuh ditambah jumlah yang diambil dari makanan, minuman, atau udara yang terhirup. Jumlah logam berat yang terakumulasi lebih cepat dibandingkan dengan jumlah yang terekskresi dan terdegradasi (Martaningtyas, 2005).
2.4.1 Timbal (Pb)
Timbal adalah sejenis logam abu-abu kebiruan, mempunyai kerapatan yang tinggi, sangat lembut dan mudah meleleh. Larut dalam HNO3 pekat, sedikit
larut dalam HCl dan H2SO4 encer ( Vogel, 1979).
Logam ini penting dalam industri modern yang digunakan untuk pembuatan pipa air karena sifat ketahanannya terhadap korosi dalam segala kondisi dan rentang waktu lama. Pigmen Pb juga digunakan untuk pembuatan cat, baterai, dan campuran bahan bakar bensin tetraetil.
Pb dalam batuan berada pada struktur silikat yang menggantikan unsur kalsium/Ca, dan baru dapat diserap oleh tumbuhan ketika Pb dalam mineral utama terpisah oleh proses pelapukan. Pb di dalam tanah mempunyai kecenderungan terikat oleh bahan organik dan sering terkonsentrasi pada bagian atas tanah karena menyatu dengan tumbuhan, dan kemudian terakumulasi sebagai hasil pelapukan di dalam lapisan humus. Bijih logam timbal (Pb) yang terbentuk dalam cebakan-cebakan dan sedimen terikat dengan mineral-mineral utama seperti: PbS, PbCO3,
PbSO4 dan PbMnO4.
Dampak dari keracunan Pb adalah dapat menyebabkan hipertensi dan salah satu faktor penyebab penyakit hati. Keracunan Pb dapat juga mengakibatkan gangguan sintesis darah, hipertensi, hiperaktivitas, dan kerusakan otak
2.3.2. Kadmium (Cd)
Kadmium adalah logam yang berwarna putih keperakan, lunak dan tahan korosi. Kadmium didapat pula pada limbah berbagai jenis pertambangan logam yang tercampur kadmium seperti timah hitam dan seng. Dengan demikian, kadmium dapat ditemukan di dalam perairan, baik di dalam sedimen maupun di dalam penyediaan air minum (Slamet, 1994).
Logam kadmium sangat banyak digunakan dalam kehidupan sehari-hari manusia. Antara lain sebagai bahan stabilisasi, bahan pewarna dalam industri plastik dan pada elekrtoplating dan juga digunakan untuk solder dan baterai (Palar. 1994).
Senyawa kadmium juga digunakan sebagai bahan fotografi, pembuatan tabung TV, cat, karet, kembang api, percetakan tekstil dan pigmen untuk gelas dan email gigi ( Herman, 2006).
Kadmium dalam tubuh terakumulasi dalam hati dan terutama terikat sebagai metalotionein mengandung unsur sistein, dimana Cd terikat dalam gugus sufhidril (-SH) dalam enzim seperti karboksil sisteinil, histidil, hidroksil, dan fosfatil dari protein purin. Kemungkinan besar pengaruh toksisitas Cd disebabkan oleh interaksi antara Cd dan protein tersebut, sehingga menimbulkan hambatan terhadap aktivitas kerja enzim dalam tubuh. ( Darmono, 2001).
2.5. Dekstruksi Logam 2.5.1. Dekstruksi Basah
Tekhnik dekstruksi basah adalah dengan memanaskan sampel organik dengan penambahan asam mineral pengoksidasi atau campuran asam-asam mineral tersebut. Penambahan asam mineral pengoksidasi dan pemanasan yang
cukup dalam beberapa menit dapat mengoksidasi sampel secara sempurna, sehingga menghasilkan ion logam dalam larutan asam sebagai sampel anorganik untuk dianalisis selanjutnya. Dekstruksi basah biasanya menggunakan H2SO4,
HNO3 dan HClO4 atau campuran dari ketiga asam mineral tersebut (Andeson,
1987).
2.5.2. Dekstruksi Kering
Dekstruksi kering merupakan tekhnik yang umum digunakan untuk mendekomposisi bahan organik. Sampel diletakkan di dalam krusibel dan dipanaskan sampai semua materi organik terurai dan meninggalakan residu anorganik yang tidak menguap dalam logam oksida. Temperatur yang paling umum digunakan adalah 500-550oC. Selain unsur C, H dan N, beberapa laogam
akan hilang dengan dekstruksi kering ini, diantaranya halogen, S, Se, P, As, Sb, Ge, Ti, Hg (Anderson, 1987).
2.6 Spektrofotometri Serapan Atom
Metode SSA berprinsip pada absorpsi cahaya oleh atom. Atom-atom menyerap cahaya tersebut pada panjang gelombang tertentu, tergantung pada unsurnya. Cahaya pada panjang gelombang tertentu mempunyai cukup energi untuk mengubah tingkat elektron suatu atom. Transisi elektron suatu unsur bersifat spesifik. Dengan absorpsi energi, berarti memperoleh lebih banyak energi, suatu atom pada keadaan dasar akan tereksitasi ke tingkat energi yang lebih tinggi ( Khopkar, 2003).
Pembentukan atom-atom logam gas dalam nyala dapat terjadi bila suatu larutan sampel yang mengandung logam dimasukkan ke dalam nyala. Peristiwa yang terjadi secara singkat setelah sampel dimasukkan ke dalam nyala adalah:
1. Penguapan pelarut yang meninggalkan residu padat
2. Perubahan zat padat dengan disosiasi menjadi atom-atom penyusunnya, yang mula-mula akan berada dalam keadaan dasar
3. Beberapa atom dapat tereksitasi oleh energi termal nyala ke tingkatan-tingkatan energi yang lebih tinggi, dan mencapai kondisi dalam mana atom akan memancarkan energi ( Vogel, 1989 ).
Metode spektrofotometri Serapan Atom mempunyai beberapa kelebihan dibandingkan metode spektrofotmetri nyala. Pada metoda spektrofotometri nyala, emisi tergantung pada sumber eksitasi. Bila eksitasi dilakukan secara termal maka ia bergantung pada temperatur sumber. Selain itu eksitasi termal tidak selalu spesifik, dan eksitasi secara secara serentak pada berbagai jenis logam dalam suatu sampel dapat saja terjadi. Pada metode Spektrofotometri Serapan Atom, perbandingan banyaknya atom yang tereksitasi terhadap atom yang berada pada tingkat dasar harus cukup besar, karena metode serapan atom hanya tergantung pada perbandingan ini dan tidak bergantung pada nyala. Metode serapan sangatlah spesifik. Logam–logam yang menbentuk campuran kompleks dapat dianalisis dan selain itu tidak selalu diperlukan sumber energi yang besar. Ini tidak berarti bahwa faktor suhu pada Spektrofotometri Serapan Atom tidak diperlukan pengontrolan, karena walaupun pengukuran absorban atom-atom di dalam nyala tidak dipengaruhi oleh suhu nyala secara langsung, tetapi secara tidak langsung suhu nyala tersebut berpengaruh juga terhadap absorban ( Khopkar, 2002 ).
2.6.1. Instrumentasi
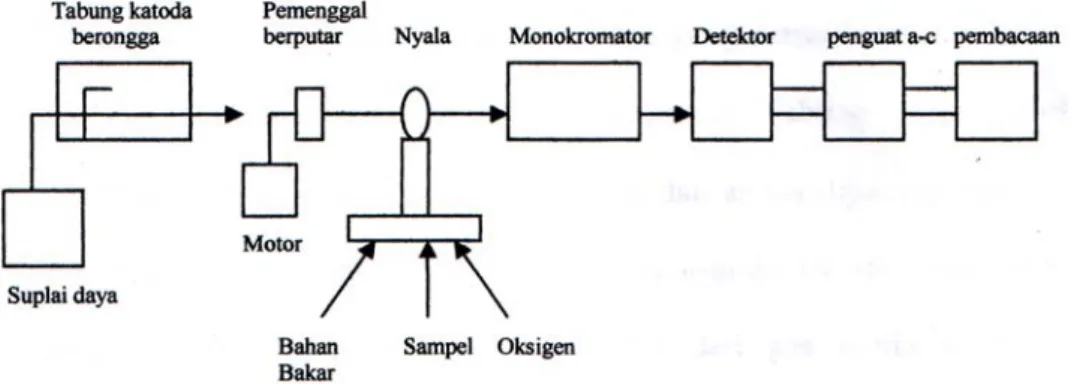
Gambar dibawah ini menunjukkan bentuk bagan komponen penting dari spekrtofotometer serapan atom (Day and Underwood, 1989).
Gambar 1. Komponen Spektrofotometri Serapan Atom Komponen penting dari spektrofotometri serapan atom adalah a. Sumber Sinar
Sumber sinar yang lazim dipakai adalah lampu katoda berongga (hollow
cathoda lamp). Lampu ini terdiri atas tabung kaca tertutup yang mengandung
suatu katoda dan anoda. Katoda sendiri berbentuk silinder berongga yang terbuat dari logam atau dilapisi dengan logam tertentu. Tabung logam ini diisi dengan gas mulia (neon atau argon). Bila antara anoda dan katoda diberi selisih tegangan yang tinggi (600 volt), maka katoda akan memancarkan berkas-berkas elektron yang bergerak menuju anoda yang mana kecepatan dan energinya sangat tinggi. Elektron-elektron dengan energi ini dalam perjalanannya menuju anoda akan bertabrakan dengan gas-gas mulia yang diisikan tadi. Akibat dari tabrakan-tabrakan ini membuat unsur-unsur gas mulia akan kehilangan elektron dan menjadi ion bermuatan positif ini selanjutnya akan bergerak ke katoda dengan kecepatan dan energi yang tinggi pula. Sebagaimana disebutkan diatas, pada katoda terdapat unsur-unsur ini akan ditabrak oleh ion-ion positif gas mulia. Akibat tabrakan ini, unsur-unsur akan terlempar keluar dari permukaan katoda. Atom-atom unsur dari katoda ini mungkin akan mengalami eksitasi ke tingkat energi-energi elektron yang lebih tinggi dan akan memancarkan spektrum
pancaran dari unsur yang sama dengan unsur yang akan dianalisis (Rohman, 2007).
b. Bahan Bakar dan Bahan Pengoksidasi
Untuk mengubah unsur metalik menjadi uap atau hasil disosiasi diperlukan energi panas. Temperatur harus benar-benar terkendali dengan sangat hati-hati agar proses atomisasinya sempurna. Ionisasi harus dihindarkan dan ini dapat terjadi bila temperatur terlalu tinggi. Gambar dibawah ini menunjukkan suatu tipe atomiser nyala (Khopkar, 2002).
Umumnya bahan bakar yang digunakan adalah hidrogen, asetilen dan propana, sedangkan oksidatornya adalah udara, oksigen dan NO2. Temperatur dari
berbagai nyala dapat dilihat pada tabel dibawah ini:
Tabel 1. Temperatur nyala dengan berbagai kombinasi bahan bakar dan bahan pengoksidasi (Harris, 1982)
Bahan Bakar Oksidan Temperatur Maksimum (oK) Asetilen Asetilen Asetilen Hidrogen Hidrogen Sianogen Udara Nitrogen Oksida Oksigen Udara Oksigen Oksigen 2400 – 2700 2900 – 3100 3300 – 3400 2300 – 2400 2800 – 3000 4800 c. Monokromator
Monokromator berfungsi untuk mengisolasi garis radiasi tertentu yang diinginkan dari garis-garis lain yang dipancarkan oleh lampu dalam hal ini yang sering digunakan adalah kisi difraksi karena memiliki daya pisah yang baik (Basset, J., 1994).
d. Detektor
Detektor berfungsi untuk menangkap intensitas cahaya yang tidak diserap oleh atom dalam nyala, alat yang sering digunakan adalah Photomultiplier yang mempunyai kepekaan spektral yang lebih tinggi (Basset, J., 1994).
2.7. Uji Perolehan Kembali
Uji perolehan kembali merupakan salah satu cara untuk mengetahui validitas suatu proses analisis. Didalam uji perolehan kembali, sejumlah zat murni yang diketahui jumlahnya dengan pasti ditambahkan ke dalam materi sampel yang akan dianalisis dan prosedur yang sama dilakukan seperti pada sampel. Kemudian hasil uji perolehan kembali dari sejumlah zat yang telah ditambahkan dapat dihitung. Uji perolehan kembali ini sangat penting agar evaluasi terhadap produk dapat dilakukan dengan tepat.
Kecermatan hasil analisis yang dinyatakan sebagai persen perolehan kembali (recovery) sangat tergantung pada keseluruhan tahap analisis. Oleh karena itu untuk mencapai kecermatan yang tinggi hanya dapat dilakukan dengan menggunakan peralatan yang telah dikalibrasi, menggunakan pereaksi dan pelarut yang baik, pengontrolan suhu, dan pelaksanaannya yang cermat, taat asas sesuai prosedur. Persen uji perolehan kembali dapat dihitung dengan menggunakan rumus sebagai berikut:
Uji perolehan kembali=
x100% n ditambahka yang baku Jumlah sampel dalam analit al Jumlah tot -analit al Jumlah tot (WHO, 1989)