PENCIRIAN DAN UJI
AKTIVITAS
KATALITIK
ZEOLIT ALAM
TERAKTIVASI
ABSTRAK
Cadangan zeolit alam Indonesia
cukup besar dan tersebar luas di beberapa
lokasi. Akan tetapi, zeolit alam belum
dimanfaatkan secara optimum. Zeolit
alam pada umumnya memiliki
kristalinitas yang rendah, ukuran porinya
tidak seragam, aktivitas katalitiknya
rendah, dan mengandung banyak
pengotor. Oleh karena itu perlu diaktivasi
dan dimodifikasi sebelum digunakan.
Penelitian ini bertujuan mengaktivasi
zeolit alam dengan asam dan pemanasan,
mencirikan zeolit alam yang sudah
diaktivasi, dan menguji aktivitas
katalitiknya pada reaksi interesterifikasi.
Analisis spektrum fourier transformation
infrared (FTIR) menunjukkan bahwa
struktur zeolit alam yang diaktivasi
dengan asam dan pemanasan (NZAT)
telah rusak. Sementara itu, struktur zeolit
alam yang diaktivasi dengan asam (NZA)
tidak menunjukkan perbedaan yang
signifikan terhadap zeolit alam (NZ).
Hasil analisis nisbah Si/Al pada spektrum
FTIR menunjukkan NZA memiliki
nisbah Si/Al yang lebih besar
dibandingkan nisbah Si/Al pada NZAT.
Hasil analisis dengan spekstroskopi
absorpsi atom menunjukkan kandungan
logam Na, K, Fe, dan Ca menurun. Hasil
pencirian sifat permukaan oleh Autosorb
menunjukkan NZA memiliki luas
permukaan spesifik dan volume total pori
yang lebih besar dibandingkan dengan
NZAT. Uji aktivitas katalitik NZA pada
reaksi interesterifikasi menghasilkan
produk yang menyerupai gabus berwarna
putih dengan persentase produk sebesar
35.78%.
PENDAHULUAN
Indonesia merupakan salah satu negara yang kaya akan zeolit alam, yang tersebar luas di berbagai lokasi antara lain di Bayah (Banten Selatan), Cikembar (Sukabumi), Nanggung (Tasikmalaya), Malang, Lampung, dan Sulawesi Selatan. Zeolit alam ini belum dimanfaatkan secara optimal. Upaya-upaya penelitian dan pengembangan berwawasan lingkungan terhadap sumber daya mineral tersebut perlu terus dilakukan sehingga dapat memberikan hasil yang nyata secara ekonomi (PPTM 1994).
Zeolit alam terdiri atas gugus alumina oksida dan gugus silika oksida yang masing-masing berbentuk tetrahedral dan saling dihubungkan oleh atom oksigen sedemikian rupa sehingga membentuk kerangka tiga dimensi yang disebut struktur kerangka (framework) tiga dimensi. Sifat yang dimiliki oleh zeolit dimungkinkan untuk dimodifikasi menjadi katalis, adsorben, penukar ion, maupun sebagai pengemban logam aktif (Kirk & Othmer 1995).
Zeolit alam pada umumnya memiliki kristalinitas rendah, ukuran porinya tidak seragam, aktivitas katalitiknya rendah, dan mengandung banyak pengotor. Oleh karena itu perlu diaktivasi dan dimodifikasi terlebih dahulu sebelum dapat digunakan (Handoko 2001).
Modifikasi zeolit alam dengan HCl 6 N pernah dilakukan oleh Jon H (2001). Zeolit alam setelah mendapatkan perlakuan meng-alami perubahan struktur dan komposisi. Adapun modifikasi dengan pemanasan pernah dilakukan oleh Shang CC & Lee MD (1994) pada suhu 540ºC yang ditujukan untuk membantu proses impregnasi terhadap zeolit sintetis H-ZSM5.
Penelitian ini bertujuan mengaktivasi zeolit alam dengan H2SO4, melakukan pencirian
terhadap zeolit alam yang sudah diaktivasi, dan menguji aktivitas katalitiknya pada reaksi interesterifikasi. Aktivasi dalam penelitian dilakukan dengan dua cara, yaitu perlakuan dengan asam tanpa pemanasan (nature zeolit
acid/NZA) dan perlakuan asam yang
dilanjutkan dengan pemanasan (nature zeolit
acid and termal/NZAT). Untuk melihat
proses aktivitas katalis zeolit pada penelitian ini dilakukan sintesis ester glukosa miristat yang diperoleh dari reaksi antara metil miristat dan glukosa pentaasetat dengan metode bebas pelarut yang pernah dilakukan
oleh Prihanjani (2006) dengan katalis zeolit sintetik.
Hipotesis penelitian ini adalah zeolit yang diaktivasi asam tanpa pemanasan maupun zeolit yang diaktivasi asam dengan pemanasan memiliki sifat-sifat zeolit (nisbah Si/Al, kandungan kation, dan sifat permukaan) lebih baik dibandingkan zeolit sebelum diaktivasi.
Hasil penelitian ini diharapkan dapat memberikan informasi zeolit hasil aktivasi tersebut dapat digunakan sebagai katalis dengan aktivitas katalitik yang baik.
TINJAUAN PUSTAKA
Mineral Zeolit
Mineral zeolit diperkenalkan sejak tahun 1756 oleh Cronstedt ketika menemukan stilbit yang bila dipanaskan seperti batu didih (boiling stone) karena dehidrasi molekul air yang dikandungnya. Pada tahun 1954, zeolit diklasifikasikan sebagai golongan mineral tersendiri, yang saat itu dikenal sebagai
molecular sieve materials (Gotardi & Galli
1985).
Zeolit adalah mineral yang terdiri atas kristal alumino silikat terhidrasi yang mengandung kation alkali atau alkali tanah dalam kerangka tiga dimensi. Zeolit biasanya ditulis dengan rumus kimia Mx/n [(AlO2)x
(SiO2)y. zH2O, dengan x dan y adalah
bilangan bulat, y/x sebanding atau lebih besar dari 1, n adalah valensi logam M, z adalah jumlah molekul air dalam masing-masing unit, x dan y adalah masing-masing jumlah alumina dan silika (Tang 2003). Contoh struktur 3 dimensi zeolit alam disajikan pada Gambar 1.
Gambar 1 Contoh struktur 3 dimensi zeolit alam.
Proses Pembentukkan Zeolit
Banyak penelitian yang dilakukan untuk mengetahui proses terjadinya zeolit. Salah satu asumsi awal adalah debu vulkanik yang sangat reaktif bertransformasi melalui
mekanisme peluruhan represipitasi
mem-
bentuk zeolit. Asumsi lain mengatakan bahwa zeolit alam terbentuk dari reaksi debu vulkanik yang reaktif dengan air laut yang mengandung banyak garam alkali dan alkali tanah yang berlangsung pada pH 9-10 dan suhu 300 K, tetapi proses kristalisasi memakan waktu 50.000 tahunan (Sembiring 1987).
Menurut proses pembentukkannya zeolit dapat digolongkannya menjadi dua kelompok, yaitu zeolit alam dan zeolit sintesis. Zeolit alam terbentuk karena adanya proses perubahan alam (zeolitisasi) dari batuan vulkanik tuff, sedangkan zeolit sintesis direkayasa oleh manusia secara proses kimia. Jenis zeolit sintetis disajikan pada Tabel 1 dan Tabel 2 untuk jenis mineral zeolit alam.
Tabel 1 Jenis-jenis zeolit sintetis No Nama Rumus Molekul
1 A Na12[(AlO2)12(SiO2)12].27H2O 2 X Na86 [(AlO2)86 (SiO2)106].264H2O 3 Y Na56 [(AlO2)56 (SiO2)136].250H2O 4 L K9[(AlO2)9 (SiO2)27].22H2O Sumber: Riberio (1984)
Tabel 2 Jenis mineral zeolit yang terdapat dalam batuan zeolit
Nama
Mineral Rumus Kimia Unit Sel Faujasit Na58(Al58Si134O384).18 H2O
Ferriet (Na2Mg2)(Al6Si30O72).18H2O
Hulandit Ca4(Al8Si28O72).24 H2O
Klinoptilolit (Na4K4)(Al8Si40O96).24 H2O
Mordenit Na8 (Al8Si40O96).24H2O
Natrolit Na4(Al4Si6O20).4H2O
Scolecit Ca2(Al4Si6O20).6H2O
Thomsonit (NaCa2)(Al5SI5O20).6H2O
Wairakit Ca(Al2Si4O12).2H2O
Yugawaralit Ca(Al2Si4O12).6H2O
Sumber: Clark (1979)
Sifat-Sifat Zeolit
Sifat Pertukaran Ion dari Zeolit
Kemampuan pertukaran ion zeolit merupakan salah satu parameter yang dapat digunakan dalam menentukan kualitas zeolit yang akan digunakan, biasanya dinyatakan sebagai KTK (kemampuan tukar kation). KTK adalah jumlah meq ion logam yang dapat diserap maksimum oleh 1 g zeolit
dalam kondisi kesetimbangan. Nilai KTK zeolit ini banyak tergantung pada jumlah ion Al dalam struktur zeolit.
Sifat Adsorpsi dari Zeolit
Adsorpsi adalah suatu proses penjerapan suatu zat oleh zat lainnya, yang hanya terjadi pada permukaan. Zat yang dijerap disebut fase terjerap (adsorbat) dan zat yang menjerap disebut adsorben. Adsorben pada umumnya adalah zat padat yang berrongga, contohnya adalah zeolit. Pada umumnya untuk dapat mengadsorpsi, zeolit harus didehidrasi terlebih dahulu dengan pemanasan.
Faktor-faktor yang mempengaruhi proses adsorpsi antara lain luas permukaan, ukuran partikel, dan komposisi kimia. Adapun sifat adsorbat antara lain ukuran molekul dan komposisi kimia serta konsentrasi adsorbat dalam fase cairan. Semakin kecil ukuran partikel, maka semakin besar luas permukaan padatan per satuan volume tertentu, sehingga semakin banyak zat yang diadsorpsi (Atkins 1999).
Sifat Katalis dari Zeolit
Definisi katalis yang umum diterima saat ini adalah zat yang meningkatkan laju reaksi kimia tanpa ‘dirinya sendiri’ ikut terlibat dalam reaksi secara permanen, sehingga pada akhir reaksi katalis tidak tergabung dengan senyawa produk reaksi. Adanya katalis dapat mempengaruhi faktor-faktor kinetik suatu reaksi seperti laju reaksi, energi aktivasi, sifat dasar keadaan transisi, dan lain-lain (Augustine 1996).
Berdasarkan fasenya, material katalis dapat digolongkan menjadi katalis homogen dan katalis heterogen. Katalis homogen ialah katalis yang mempunyai fase yang sama dengan fase campuran reaksinya, sedangkan katalis heterogen adalah katalis yang berbeda fase dengan campuran reaksinya.
Katalis heterogen kurang efektif dibandingkan dengan katalis homogen karena heterogenitas permukaannya. Walaupun demikian, karena mudah dipisahkan dari campuran reaksinya dan kestabilannya terhadap perlakuan panas, katalis heterogen lebih banyak digunakan dalam industri kimia.
Kemampuan zeolit untuk mengkatalisis suatu reaksi kimia terutama berhubungan dengan sifatnya sebagai padatan asam karena adanya sisi-sisi asam, baik sisi asam Bronsted maupun Lewis. Sisi asam Bronsted dapat dihasilkan dengan beberapa cara di antaranya perlakuan pemanasan terhadap bentuk
amonium zeolit untuk menghilangkan amonia sehingga diperoleh bentuk H-zeolit, perlakuan dehidrasi terhadap kation multivalen pada zeolit yang diikuti terdisosiasinya air yang terkoordinasi dalam bentuk molekul sehingga membentuk ion H+ pada permukaan zeolit, dan perlakuan asam terhadap zeolit yang stabil terhadap asam akan dapat secara langsung menukar kation dengan proton. Sisi asam Lewis dapat diperoleh dari dehidroksilasi dua gugus hidroksil yang berdekatan dengan perlakuan panas (T>750 K).
Sifat lain dari zeolit yang juga berpengaruh terhadap peranannya dalam katalisis adalah komposisi kerangka dan struktur pori zeolit, kenaikan rasio Si/Al, medan elektrostatis, kekuatan asam dari sisi Bronsted, dan perubahan struktur bangun sekunder dari zeolit.
Komposisi kerangka zeolit mengatur muatan kerangka dan mempengaruhi stabilitas pemanasan dan asam dari zeolit. Kenaikan rasio Si/Al akan berpengaruh pada stabilitas zeolit terhadap suhu tinggi dan lingkungan yang reaktif seperti naiknya keasaman. Medan elektrostatis zeolit menyebabkan interaksi adsorbsinya dengan molekul lain berubah-ubah. Kekuatan asam dari sisi asam Bronsted akan bertambah dengan naiknya rasio Si/Al dan menurunnya konsentrasi kation dalam zeolit. Sementara itu perubahan struktur unit bangun sekunder dari zeolit sangat penting dalam proses katalisis karena pori inilah yang berperan sebagai mikroreaktor dan darinya dimungkinkan untuk mendapatkan reaksi katalitik yang diinginkan menurut aturan bentuk selektivitas.
Aktivasi Zeolit
Aktivasi merupakan proses untuk menaikkan kapasitas adsorpsi sehingga diperoleh sifat yang diinginkan sesuai dengan penggunaannya. Tujuan aktivasi zeolit adalah untuk menghasilkan luas permukaan yang lebih luas melalui pembentukkan struktur berpori dan juga untuk menghilangkan senyawa-senyawa pengotor. Aktivasi zeolit dilakukan dengan pemanasan, penambahan asam, dan penambahan basa. Pada penelitian ini dilakukan aktivasi dengan penambahan asam dan pemanasan. Pada umumnya asam yang digunakan adalah asam sulfat dan asam klorida, sedangkan basa yang digunakan adalah NaOH.
Pencirian Zeolit
Analisis dengan spektrofotometer Fourier
Transformation InfraRed (FTIR)
Spektrum radiasi inframerah terletak pada kisaran bilangan gelombang 12800-10 cm-1. Berdasarkan pertimbangan instrumentasi dan aplikasi, sejauh ini yang paling banyak digunakan terbatas pada daerah 4000-760 cm-1 (daerah inframerah tengah) terutama untuk tujuan identifikasi. (Khopkar 1990).
Frekuensi dari vibrasi kerangka pada daerah inframerah tengah (400-4000 cm-1) menyediakan informasi tentang komposisi dan sifat-sifat yang berhubungan dengan interaksi tetrahedral SiO44- dan AlO45-.
Kenampakan spektrum inframerah dapat berkorelasi dengan kehadiran tipe-tipe unit struktural tertentu.
Metode Garis Dasar (Baseline)
Metode semi kuantitatif yang umumnya digunakan pada penentuan nisbah Si/Al adalah metode baseline. Sebagai ilustrasi, metode baseline disajikan dalam Gambar 2.
Suatu garis dasar (baseline) dibuat pada kedua lembah puncak lalu dihubungkan dengan menarik garis dari ujung puncak yang tegak lurus terhadap garis dasar. Selanjutnya tinggi puncak dihitung dari ujung puncak ke titik perpotongan garis dasar dengan garis yang tegak lurus terhadap garis dasar.
Gambar 2 Tinggi puncak dengan metode baseline.
Analisis Luas Permukaan Spesifik (LPS) Katalis
Luas permukaan spesifik adalah luas permukaan yang dapat menyerap gas secara merata pada satu lapisan per satuan berat. Luas permukaan menggambarkan permukaan aktif yang dapat kontak dengan reaktan sehingga berfungsi sebagai jembatan dalam proses reaksi. Semakin besar permukaan aktif dari suatu katalis diharapkan aktivitas katalis semakin baik.
Prinsip pengukuran luas permukaan spesifik adalah sejumlah serbuk zeolit (0.1-0.2 g) dialiri campuran gas nitrogen dan helium selama waktu tertentu. Selanjutnya berat campuran gas yang terserap tersebut pada permukaan zeolit disubtitusikan pada persamaan Brunaeur, Emmet, dan Teller (BET).
Menurut teori Brunaeur, Emmet, dan Teller (BET), banyaknya gas yang dapat diadsorpsi pada permukaan padatan berbanding langsung dengan luas permukaan, sehingga semakin sedikit gas nitrogen yang teradsorpsi pada permukaan, maka luas permukaan semakin kecil. Sebagai konsekuensinya jika gas nitrogen yang teradsorpsi pada permukaan padatan banyak maka luas permukaan dari padatan juga besar.
Reaksi Interesterifikasi
Sintesis gula ester asam lemak dapat dilakukan melalui dua jalur, yaitu jalur sintesis kimia dan enzimatik. Mekanisme reaksinya berlangsung dengan reaksi interesterifikasi antara gula dengan satu atau lebih trigliserida. Sintesis senyawa ester karbohidrat asam lemak biasanya berlangsung pada suhu tinggi dengan kehadiran katalis dan menggunakan pelarut toksik.
Feuge et al. (1970) melakukan reaksi esterifikasi langsung antara sukrosa dan asam lemak dengan metode bebas pelarut menggunakan katalis sabun litium, natrium, dan kalium pada suhu 170-187°C. Reaksi ini terbatas dengan adanya kecenderungan pembentukan karamelisasi sukrosa pada suhu tinggi.
Obaje (2005) telah memodifikasi metode sintesis ester gula asam lemak melalui reaksi interesterifikasi bebas pelarut pada suhu rendah (60-95°C) dengan katalis asam. Katalis yang digunakan adalah berupa asam sulfat, asam tolsilat, dan asam alkil sulfonat.
Prihanjani (2006) telah melakukan optimalisasi sintesis gula ester melalui sistem bebas pelarut dengan mereaksikan metil miristat dan glukosa pentaasetat dengan katalis zeolit sintetik pada suhu 90°C selama 6 jam. Rendemen produk yang dihasilkan adalah ± 87%. Penelitian ini dilakukan dengan metode yang sama dengan Prihanjani, akan tetapi zeolit yang digunakan adalah zeolit alam yang telah diaktivasi.
BAHAN DAN METODE
Bahan dan Alat
Bahan utama yang digunakan adalah zeolit alam ukuran 60 mesh dari Pusat Penelitian dan Pengembangan Teknologi Mineral Bandung, kertas saring, akuades, larutan, larutan H2SO4 0.2 N, larutan NH4NO3 0.1 M,
metil miristat, glukosa pentaasetat, etanol 30-40%, NaHCO3, pH universal, akuades dan
larutan akuaregia.
Alat-alat yang digunakan dalam penelitian ini adalah gelas piala (50 ml, 100 ml, dan 500 ml), labu ukur (25 ml, 50 ml, 100 ml, dan 250 ml), labu bulat, kondensor, penangas air, termometer, neraca analitik, tanur, oven pengering, kondensor, termometer, atomic
absorption spectroscopy (AAS), autosorb quantrochome 6B, spektrofotometer fourier transform infrared (FTIR) merek bruker jenis
tentor 37, dan alat-alat kaca lainnya.
Metode
Preparasi Zeolit
Contoh diambil dari Pusat Penelitian dan Pengembangan Teknologi Mineral (P3TM) Bandung. Zeolit berasal dari daerah Cikotok. Pengayakan dan penggilingan contoh zeolit dilakukan untuk memperolehpartikel-partikel yang berukuran 60 mesh karena pada ukuran ini zeolit cukup optimal dalam aktivitasnya. Diagram alir penelitian dapat dilihat pada Lampiran 1.
Penentuan Kadar Air Zeolit Alam
Cawan petri yang telah disiapkan dikeringkan dalam oven dan diketahui bobot kosongnya. Cawan petri yang berisi contoh dikeringkan dalam oven pada suhu 105ºC selanjutnya didinginkan. Setelah dingin disimpan dalam eksikator lalu ditimbang. Pengeringan dilakukan beberapa kali selama 3 jam sampai diperoleh bobot tetap.
Kadar Air = A - B x 100 % C
A = bobot contoh + cawan sebelum dikeringkan
B = bobot contoh + cawan setelah dikeringkan
C = bobot contoh
Preparasi Katalis Zeolit Alam (NZ)
Zeolit alam dari P3TM yang telah dihaluskan dengan ukuran 60 mesh direndam
dalam akuades sambil diaduk dengan pengaduk besi (sudip) selama 1 jam pada suhu kamar, kemudian disaring dan dikeringkan dalam oven pada 120°C sampai kering.
Preparasi Katalis Zeolit Alam Perlakuan Asam (Suyartono & Husaini 1991)
Contoh zeolit alam (NZ) direfluks selama 1 jam dengan larutan asam sulfat 0.2 N pada suhu 90°C sambil diaduk. Selanjutnya contoh disaring dan dicuci dengan akuades sampai pH=6. Berikutnya contoh dikeringkan dan dihaluskan sehingga diperoleh katalis zeolit alam yang diaktivasi asam (NZA).
Preparasi Katalis Zeolit Alam Perlakuan Pemanasan (Modifikasi Shang 1998)
Contoh NZA dikeringkan dalam tanur 540°C selama 12 jam, selanjutnya contoh direndam dalam larutan NH4NO3 0.1 M
selama 2 jam sebanyak tiga kali ulangan. Kemudian contoh NZA tersebut dipanaskan pada suhu 120°C selama 24 jam dan dilanjutkan dengan pemanasan pada suhu 540°C selama 4 jam sehingga diperoleh zeolit alam yang diaktivasi asam dan pemanasan (NZAT).
Pencirian Katalis
Penentuan Kandungan Kation Logam (Na, Ca, K, dan Fe)
Penentuan kandungan kation logam dalam katalis NZ, NZA, dan NZAT dilakukan dengan cara destruksi (dalam lemari asam). Hal ini dilakukan berkaitan dengan sifat kation dalam zeolit yang berperan sebagai pengontrol aktivitas katalisis. Contoh zeolit sebanyak 0.2 gram ditempatkan dalam cawan porselin ditambahkan 2 ml akuaregia (HNO3
pa:HCl pa=1:3) kemudian dipanaskan selama 30 menit. Setelah lima menit ke dalam campuran ditambahkan H2SO4 4% sebanyak
0.5 ml dan dipanaskan selama 15 menit, kemudian ditambahkan 1 ml akuaregia dan H2SO4 4% sebanyak 0.25 ml dan dibiarkan
selama 10 menit. Campuran diencerkan ke dalam labu ukur 25 ml hingga tera, sehingga diperoleh larutan contoh zeolit alam (NZ), zeolit alam yang diaktivasi asam (NZA), dan zeolit alam yang diaktivasi asam dan pemanasan (NZAT) masing-masing sebesar 0.2 g/ 25 ml atau 8000 ppm. Selanjutnya masing-masing contoh zeolit tersebut ditentukan kandungan kation logamnya (Na, Ca, K, Fe) dengan AAS.
Analisis FTIR
Contoh sebanyak 0.1 g yang telah dikeringkan pada 120oC selama 3 jam digerus dengan padatan KBr sebanyak ± 160 mg lalu ditekan pada keadaan vakum hingga diperoleh lempeng tipis yang transparan. Pengukuran dilakukan pada daerah IR tengah, yaitu pada bilangan gelombang 400-4000 cm1.
Penentuan Nisbah Si/Al dengan Metode
Baseline
Suatu garis dasar (baseline) dibuat pada kedua lembah puncak lalu dihubungkan dengan menarik garis dari ujung puncak yang tegak lurus terhadap garis dasar. Selanjutnya tinggi puncak dihitung dari ujung puncak ke titik perpotongan garis dasar dengan garis yang tegak lurus terhadap garis dasar. Selanjutnya diukur nisbah Si/Al dengan metode garis dasar pada spektrum FTIR tersebut. Pertama-tama puncak tertinggi dicatat dan diukur garis dasar yang dipilih. Kemudian besar transmitan pada bilangan gelombang 1647 cm-1 (serapan gugus Si-O) dengan transmitan pada bilangan gelombang 1045 cm-1 (serapan Al-O) maka nisbah dapat diperoleh dari hasil perbandingan tersebut.
Penentuan Luas Permukaan Spesifik, Volume Total Pori, dan Rerata Jejari Pori
Luas permukaan spesifik, volume total pori, dan rerata jejari pori didasarkan pada fenomena adsorpsi gas lapis tunggal yang berlangsung pada suhu konstan. Alat yang digunakan adalah autosorb quantrochome 6B yang berada di Departemen Teknik Gas dan Petrokimia, Fakultas Teknik, Universitas Indonesia, Depok.
Contoh zeolit ditimbang dan dimasukkan dalam wadah contoh dan dipanaskan pada suhu 200°C, selanjutnya dilakukan peng-usiran gas menggunakan gas nitrogen selama 45 menit. Kemudian contoh didinginkan dengan nitrogen cair sehingga suhu contoh mencapai 77 K. Tekanan gas nitrogen diubah sehingga jumlah gas nitrogen yang terkondensasi dapat ditentukan. Dengan diperolehnya data tersebut, maka luas permukaan spesifik, volume total pori, dan rerata jari pori dapat ditentukan.
Uji Aktivitas Katalitik Zeolit
Sintesis Ester Glukosa Miristat (Prihanjani 2006)
Sintesis ester glukosa miristat dilakukan dengan nisbah miristat dan GPA 1:1, serta zeolit sebesar 10% dari total reaktan. Sintesis
ini dimulai dengan mencampurkan metil miristat, GPA, dan zeolit yang dimasukkan ke dalam labu bulat yang dilengkapi pendingin dan pengaduk magnetik, kemudian di-panaskan pada suhu 90°C dalam penangas air mendidih selama 6 jam.
Pemisahan Ester Glukosa Miristat (Obaje 2005)
Campuran homogen yang terbentuk dari hasil sintesis ditambahkan dengan larutan etanol hangat dan dinetralkan dengan beberapa tetes larutan NaHCO3 1 M kemudian disaring
dalam kondisi hangat sampai dihasilkan endapan A dan filtrat. Filtrat yang berisi pelarut etanol diuapkan sehingga dihasilkan endapan A dan B (residu) ditambahkan heksana lalu diuapkan sampai didapatkan miristat yang tidak bereaksi. Kemudian masing-masing endapan ditambahkan etanol hangat dan didinginkan pada suhu -4°C sampai 0°C hingga terdapat endapan putih. Campuran tersebut disaring, endapan yang diperoleh adalah GPA yang tidak bereaksi dan katalis zeolit sedangkan filtratnya berisi ester glukosa asam lemak. Pelarut etanol pada filtrat dapat dihilangkan dengan cara diuapkan sampai terbentuk padatan ester glukosa miristat. Selanjutnya produk ditentukan persentase hasil.
HASIL DAN PEMBAHASAN
Aktivasi Zeolit
Kadar air zeolit alam sebelum aktivasi diukur dengan metode gravimetri, hasilnya diperoleh kadar air zeolit alam sebesar 4.01%, perhitungan dapat dilihat pada Lampiran 2. Nilai kadar air ini menunjukkan proporsi volume pori yang dihuni oleh molekul air. Semakin rendah kadar air produk zeolit semakin tinggi mutunya. Untuk nilai tersebut diusulkan tidak melebihi 5% (Goenadi 1993).
Proses aktivasi zeolit alam dilakukan dengan dua cara, yaitu perlakuan asam tanpa pemanasan dan perlakuan asam yang dilanjutkan dengan pemanasan. Pada perlakuan asam zeolit direfluks selama 1.5 jam dalam 250 ml asam sulfat 0.2 N. Aktivasi tersebut bertujuan membersihkan permukaan pori, membuang senyawa pengotor, dan mengatur kembali letak atom yang dapat dipertukarkan. Zeolit alam sebelum diaktivasi disajikan pada Gambar 2, sedangkan zeolit teraktivasi asam dapat diamati pada Gambar
3 berupa zeolit yang berwarna hijau keabu-abuan.
Gambar 3 Zeolit alam sebelum aktivasi.
Gambar 4 Zeolit alam yang diaktivasi asam.
Dari Gambar 3 dan 4 dapat diamati terjadi perubahan warna zeolit alam dari hijau menjadi hijau keabu-abuan pada zeolit yang diaktivasi asam.
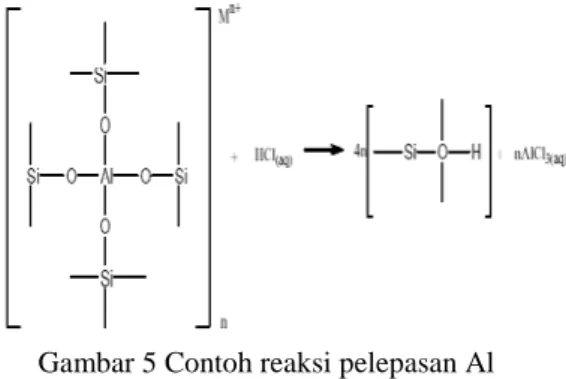
Asam sulfat dipilih sebagai perefluks karena larutan asam sulfat dapat mengekstraksi Al dalam zeolit, yaitu Al dalam kerangka zeolit menjadi Al di luar kerangka zeolit yang disebut sebagai proses dealuminasi. Berikut contoh reaksi pelepasan Al dari dalam kerangka zeolit oleh pelarut HCl pada Gambar 5.
Gambar 5 Contoh reaksi pelepasan Al dari dalam kerangka zeolit.
Cara aktivasi yang kedua adalah memberi perlakuan pemanasan pada zeolit alam yang sudah diaktivasi dengan H2SO4 pada suhu
540°C dilanjutkan dengan perendaman dalam NH4NO3 0.1 M sebanyak 3 kali ulangan.
Garam NH4NO3 adalah penukar kation..
Penambahan garam NH4NO3 bertujuan untuk
mengaktifkan zeolit secara kimia yang dilakukan sebagai penukar kation, sehingga dalam proses pertukaran ion, ion dapat disubtitusi dengan kation NH4+ yang ada pada
permukaan zeolit.
Selama pemanasan pada suhu 540oC dihasilkan zeolit yang berwarna jingga/oranye disajikan pada Gambar 6 zeolit hasil aktivasi asam dan pemanasan (NZAT). Hal ini dikarenakan zeolit mengalami perubahan struktur akibat pemanasan yang terlalu tinggi.
Gambar 6 Zeolit alam yang diaktivasi asam dan pemanasan (NZAT).
Analisis FTIR
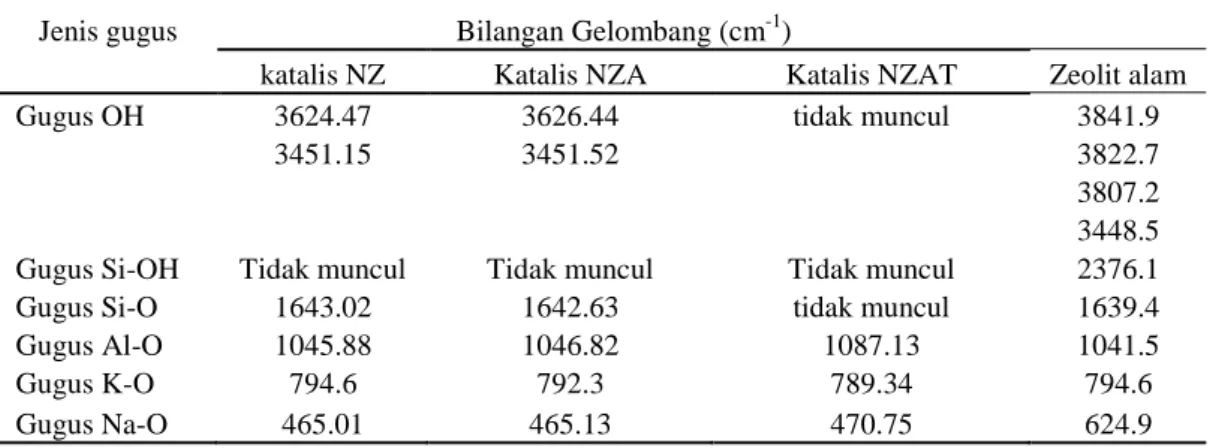
Pada Tabel 3 dapat dilihat perbandingan hasil spektrum FTIR katalis NZ, NZA, dan NZAT dengan spektrum FTIR dari zeolit alam bayah yang telah dilakukan oleh Supriatna (1995) yang menunjukkan serapan terjadi pada bilangan gelombang 3841 cm-1, 3448.5 cm-1, 3822.7 cm-1, 3807.2 cm-1 (gugus OH ulur dari air yang terjerap), 2376,1 cm-1 (gugus Si-OH), 1639.4 cm-1 (gugus Si-O), dan 1041.5 cm-1 (gugus Al-O).
Spektrum FTIR zeolit alam (NZ) dapat dilihat pada Gambar 7. Spektrum FTIR NZ menunjukkan puncak lebar pada 3624.47 cm-1 dan 3451.15 cm-1 berkaitan dengan adanya vibrasi OH ulur walau terlihat belum tajam. Pada daerah 400-1600 cm-1 terlihat bahwa puncak-puncak sudah terlihat tajam antara lain daerah serapan 1643 cm-1adanya vibrasi Si-O, dan daerah 1045 cm-1 adanya vibrasi Al-O.
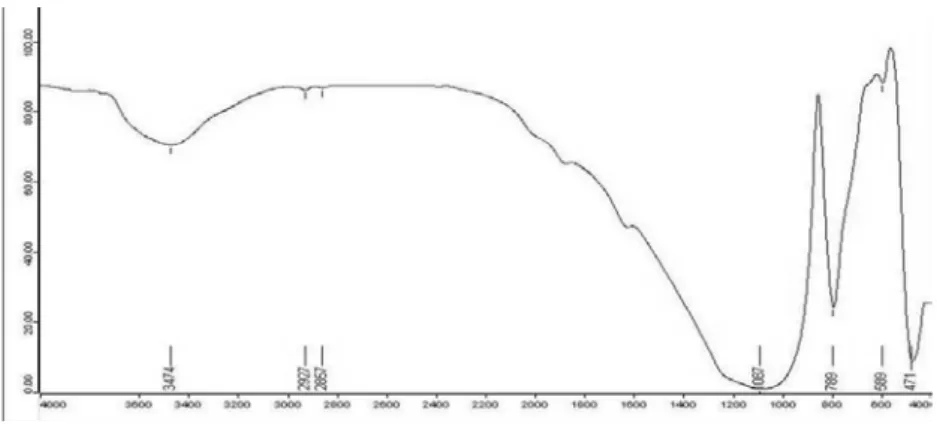
Gambar 8 menunjukkan NZA. Puncak-puncak terlihat jelas, yaitu pada 1046 cm-1 (gugus Al-O) yang lebih melebar dibandingkan NZ, bahu sekitar 1200 cm-1 (uluran asimetris), puncak 3626 cm-1 (gugus -OH) yang lebih sempit dibandingkan NZ, dan puncak pada 792 cm-1 semakin tajam dibandingkan dengan NZ.
Spektrum FTIR NZAT dapat dilihat pada Gambar 9. Adanya perubahan pada daerah vibrasi OH ulur dan Si-O ulur. Kedua puncak tidak muncul pada spektrum FTIR NZAT. Hal ini menunjukkan adanya kerusakan struktur zeolit. Kerusakan pada struktur zeolit diduga karena suhu yang digunakan pada perlakuan pemanasan terlalu tinggi. Pada contoh NZAT, spektrum FTIR juga tidak
menunjukkan adanya vibrasi OH pada daerah selebar 3500-3700 cm-1 karena tertutup oleh vibrasi -OH yang lebar.
Tabel 3 Perbandingan spektrum FTIR katalis NZ, NZA, NZAT, dengan zeolit alam bayah Supriatna (1995)
Gambar 7 Spektrum FTIR zeolit alam (NZ).
Gambar 8 Spektrum FTIR zeolit alam yang diaktivasi asam (NZA). Jenis gugus Bilangan Gelombang (cm-1)
katalis NZ Katalis NZA Katalis NZAT Zeolit alam Gugus OH 3624.47 3626.44 tidak muncul 3841.9
3451.15 3451.52 3822.7 3807.2 3448.5 Gugus Si-OH Tidak muncul Tidak muncul Tidak muncul 2376.1 Gugus Si-O 1643.02 1642.63 tidak muncul 1639.4 Gugus Al-O 1045.88 1046.82 1087.13 1041.5 Gugus K-O 794.6 792.3 789.34 794.6 Gugus Na-O 465.01 465.13 470.75 624.9
0 5 10 15 20 NZ NZA NZAT Jenis katalis K o n sen tr asi l o g am (p p m )
Logam Na Logam K Logam Ca Logam Fe
Gambar 9 Spektrum FTIR zeolit alam yang diaktivasi asam dan pemanasan (NZAT).
Analisis nisbah Si/Al
Nisbah Si/Al menunjukkan besarnya muatan negatif zeolit, semakin besar jumlah Al yang dapat menggantikan Si, maka semakin kecil nilai Si/Al dan semakin besar muatan negatif zeolit. Semakin banyak komposisi Al yang dapat dipertukarkan dalam zeolit, maka kualitas zeolit untuk pertukaran kation semakin baik. Kapasitas tukar kation zeolit tersebut semakin besar jika Si/Al kecil yang berarti muatan negatif zeolit semakin besar (Mumpton 1984). Pada umumnya semakin besar nisbah Si/Al besar dari suatu zeolit kapasitas zeolit sebagai penyerap semakin besar begitu pula dengan luas permukaan kontaknya.
Cara pengukuran nisbah Si/Al dengan metode baseline disajikan pada Lampiran 3, 4, dan 5 untuk masing-masing contoh NZ , NZA, dan NZAT. Nisbah Si/Al yang diperoleh untuk NZ dan NZA masing-masing sebesar 0.4 dan 1,untuk contoh NZAT nisbah Si/Al tidak dapat ditentukan. Hasil perhitungan nisbah ini dapat mengkelompokkan zeolit NZA ini dalam jenis zeolit kadar Si rendah (kaya Al), keadaan ini menyebabkan daya penukaran ion dari zeolit maksimum.
Aktivasi zeolit oleh asam sulfat menyebabkan terjadinya proses dealuminasi, yaitu proses keluarnya Al dari dalam kerangka zeolit menjadi Al di luar kerangka zeolit, sehingga Al dalam contoh NZA berkurang. Jumlah Al yang menurun berpengaruh terhadap nisbah Si/Al pada contoh NZA, yaitu nisbah Si/Al semakin meningkat dibandingkan dengan nisbah Si/Al pada zeolit alam murni (NZ).
Proses dealuminasi ini menurunkan kandungan Al, sehingga jumlah Al yang dapat dipertukarkan dengan kation lain semakin rendah sehingga kapasitas tukar kation zeolit tersebut semakin kecil.
Contoh zeolit yang diaktivasi asam dan pemanasan (NZAT) tidak dapat ditentukan nisbah Si/Al melalui metode baseline karena puncak Si-O tidak muncul. Hilangnya puncak Si-O diduga akibat rusaknya struktur zeolit karena pemanasan.
Analisis AAS
Penentuan kandungan kation dalam contoh katalis menggunakan alat atomic
absorption spectrophotometry (AAS). Analisis ini berkaitan dengan peranan kation sebagai pengontrol aktivitas katalitik. Rongga molekul pada zeolit dapat dimasuki kation-kation (Na, K, Ca, dan Mg) yang dapat dipertukarkan sehingga mempengaruhi muatan negatif pada kerangka. Kandungan kation-kation dalam contoh katalis dapat dilihat dalam Gambar 10.
Gambar 10 Kandungan kation dalam contoh katalis..
Gambar 10 menunjukkan kecenderungan logam kation dalam contoh katalis semakin menurun dengan adanya aktivasi zeolit yang meliputi pengasaman dan pemanasan terhadap zeolit. Akan tetapi kation logam Na
0 50 100 150 NZ NZA NZAT Jenis katalis L u as p er m u kaan sp esi fi k ( m 2/ g )
mengalami peningkatan setelah mendapatkan perlakuan. Hal ini terjadi karena pada zeolit tersebut kemungkinan masih terdapat kontaminan dan preparasi larutan yang tidak cukup baik.
Pada umumnya kation dari logam alkali seperti Na dan K dapat menyebabkan deaktivasi terhadap contoh katalis. Deaktivasi terjadi karena pori-pori yang terblokade dan sisi aktif yang tertutupi (Rodrigues et al. 2000). Adanya logam Na dalam contoh katalis akan mengurangi pembentukan kokas (coke) dan gas serta dapat bersifat racun terhadap contoh katalis.
Hasil pengamatan menunjukkan jumlah logam Na dan K sangat kecil sehingga pengaruh deaktivasi kedua logam ini sangat kecil. Kation logam K menujukkan penurunan yang signifikan pada jenis zeolit NZAT.
Pada Gambar 10 dapat diamati jumlah logam kation Ca dan Fe yang menurun secara signifikan. Adanya kation divalen dan trivalen biasanya memberikan keaktifan pada katalis zeolit. Keaktifan disebabkan kation-kation tersebut dapat mengalami hidrolisis oleh adanya uap air untuk membentuk sisi asam Bronsted.
Mn+ + H2O [MOH](n-1)+ + H+
Kation-kation dalam kerangka zeolit tersebut dapat ditukar dan disubtitusi tanpa mengubah struktur kerangka (isomorfis) yang dapat menimbulkan gradien medan elektronik dalam kanal-kanal dan ruangan zeolit.
Hasil penelitian menunjukkan kandungan logam Na, K, Fe, dan Ca pada katalis zeolit semakin menurun dengan adanya perlakuan asam dan pemanasan. Pengasaman dan pemanasan menyebabkan proses dealuminasi yang menurunkan kandungan aluminium tempat terkaitnya logam-logam penetral muatan listrik pada zeolit. Kandungan aluminium yang menurun sebanding dengan penurunan kandungan logam penetral tersebut.
Sifat Permukaan
Penentuan sifat permukaan dilakukan dengan autosorb quantachrome 6b
menggunakan gas N2. Pada penentuan sifat
permukaan tersebut, contoh padatan perlu dibebaskan dari kontaminan, misalnya air dan minyak. Proses ini dikenal dengan
degassing. Degassing dilakukan dengan
menempatkan contoh padat tersebut dalam sel gelas dan dipanaskan di bawah vakum dengan suhu konstan sebesar 200°C. Data hasil pengukuran sifat permukaan dapat dilihat pada Lampiran 6, 7, dan 8 yang ditunjukkan pada parameter multipoint BET masing-masing jenis katalis NZ, NZA, dan NZAT. Histogram luas permukaan spesifik dari beberapa katalis disajikan pada Gambar 11.
Gambar 11 Luas permukaan spesifik contoh katalis.
Luas permukaan spesifik (LPS) adalah luas permukaan tiap gram contoh katalis. Gambar 11 menunjukkan bahwa luas permukaan akan meningkat seiring dengan adanya perlakuan asam. Zeolit NZAT menunjukkan penurunan luas permukaan spesifik yang relatif besar. Peningkatan hanya terjadi pada perlakuan asam saja. Hal ini disebabkan terjadinya pembukaan pori zeolit alam yang semula tertutupi oleh pengotor melalui perlakuan dengan H2SO4.
Dengan hilangnya pengotor organik dan anorganik yang berada pada padatan katalis akan menyebabkan menurunnya volume pori. Hal ini akan mengakibatkan peningkatan luas permukaan padatan.
Perlakuan pemanasan seharusnya menyebabkan peningkatan luas permukaan spesifik karena pemanasan zeolit dapat menguapkan air yang terperangkap dalam pori-pori kristal zeolit, sehingga luas permukaan pori-pori bertambah. Akan tetapi hal ini tidak terjadi karena kemungkinan distribusi pori zeolit yang kurang merata. Hasil penelitian ini sesuai dengan yang dilaporkan Muchtar (1983), bahwa me-nurunnya luas permukaan dapat disebabkan oleh distribusi pori yang kurang merata.
Volume Total Pori dan Rerata Jejari Pori
Beberapa molekul dalam memasuki sistem mikropori zeolit akan ditahan berdasarkan kepolaran/efek interaksi lainnya dari molekul dengan zeolit. Sifat zeolit
0 0.2 0.4 0.6 0.8 1 1.2 NZA NZAT Jenis katalis V o lu m e p o ri ( c c /g ) 0 50 100 150 200 250 300 350 NZA NZAT Jenis katalis R er at a j ar i p o ri
sebagai katalis yang penting adalah mempunyai ukuran pori yang besar dan ”volume kosong tersedia” yang maksimum (Zulnely 1985).
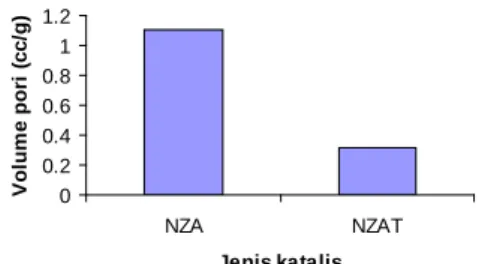
Gambar 12 memberikan informasi tentang volume total pori pada masing-masing katalis, adapun data volume pori dapat dilihat pada Lampiran 7 dan 8.
Gambar 12 Volume total pori contoh katalis
Gambar 13 Rerata jejari pori contoh katalis
Gambar 12 dan 13 menunjukkan bahwa volume total pori meningkat setelah mendapatkan perlakuan asam. Hal ini terjadi karena pori-pori zeolit menjadi lebih terbuka dengan adanya pelarutan senyawa-senyawa pengotor yang menutupi pori contoh sebelumnya. Volume pori contoh NZAT lebih sedikit setelah mendapatkan perlakuan asam dan pemanasan. Sejalan dengan hasil analisis luas permukaan spesifiknya yang mengalami penurunan juga setelah mendapatkan perlakuan, maka kecilnya volume pori diduga karena terjadi pemanasan yang terlalu tinggi.
Gambar 13 menunjukkan bahwa rerata jari pori meningkat seiring dengan perlakuan aktivasi. Contoh zeolit yang diaktivasi asam mempunyai volume pori lebih besar sehingga jari-jari pori semakin kecil karena volume pori yang besar menunjukkan jumlah pori-pori yang dimiliki cukup banyak dan volume kosong yang tersedia minimum. Sebaliknya pada contoh zeolit yang diaktivasi asam dan pemanasan, volume pori menurun menunjuk- kan jari-jari pori yang
ada besar dengan jumlah pori-pori sedikit sehingga volume kosong menjadi besar.
Reaksi Interesterifikasi
Tahap akhir dalam penelitian ini adalah uji aktivitas katalitik katalis zeolit yang telah diaktivasi pada reaksi interesterifikasi metil miristat dan glukosapentaasetat.
Berdasarkan hasil pencirian yang telah dilakukan terhadap tiga katalis zeolit, maka katalis zeolit NZA dipilih untuk diuji aktivitas katalitiknya pada reaksi interesterifikasi. Interesterifikasi dalam penelitian ini dilakukan dengan perbandingan metil miristat dan GPA 1:1, serta zeolit alam asam (NZA) sebesar 10% dari total reaktan. Kondisi reaksi yang telah dilakukan oleh Prihanjani adalah pada suhu 90°C dalam labu bulat dengan pendingin dan kondensor tegak selama 6 jam. Produk yang terbentuk dari reaksi interesterifikasi tersebut adalah ester glukosa miristat. Total presentase hasil ester glikosa miristat yang diperolehnya adalah 87.27 %.
Pada penelitian ini total ester glukosa miristat yang diperoleh adalah 35.78% atau lebih kecil dari total ester glikosa miristat Prihanjani (2006) dengan katalis zeolit sintetik. Perbedaan ini mungkin terjadi karena pemakaian jenis katalis zeolit yang berbeda, serta jumlah reaktan yang lebih kecil pada penelitian ini digunakan zeolit alam hasil aktivasi asam karena hasil pencirian menunjukkan zeolit ini lebih baik jika dilihat dari sifat permukaan, gugus yang dimiliki dan kandungan kationnya, sedangkan penelitian sebelumnya adalah zeolit sintetik. Zeolit sintetik memiliki kondisi yang lebih baik dalam mengkatalisis suatu reaksi karena struktur dan komposisi zeolit tersebut sesuai dengan kondisi yang diinginkan, misalnya dari nisbah Si/Al, luas permukaan spesifik dan volume pori. Hal ini menunjukkan sisi aktif zeolit alam asam lebih sedikit yang bereaksi dibandingkan zeolit sintetik sehingga produk yang dihasilkan lebih kecil, selain itu dapat terjadi karena penyaringan yang cepat sehingga filtrat belum terkumpul secara optimal.
Hasil spektrum FTIR ester glukosa miristat dapat dilihat pada Lampiran 10. Senyawa ester glukosa miristat dihasilkan dengan tergantinya gugus asetil (dari unit GPA) dengan gugus alifatik (dari unit metil miristat). Hal ini menunjukkan puncak khas pada bilangan gelombang 2800-3000 cm-1
dengan adanya serapan vibrasi ulur C-H pada CH3-CH2.
SIMPULAN DAN SARAN
Simpulan
Proses aktivasi berpengaruh pada sifat-sifat permukaan zeolit alam. Aktivasi dengan perlakuan asam yang dilanjutkan dengan pemanasan pada suhu 540°C menyebabkan terjadinya perubahan struktur zeolit alam. Aktivasi dengan perlakuan asam tanpa pemanasan menyebabkan meningkatnya nisbah Si/Al, luas permukaan, dan volume total pori, sedangkan rerata jari porinya menurun. Kedua proses aktivasi menyebabkan penurunan kadar sebagian besar kation yang berpengaruh terhadap aktivitas katalitik. Katalis zeolit alam yang diaktivasi dengan perlakuan asam diuji aktivitas katalitiknya pada reaksi interesterifikasi. Rendemen produk yang dihasilkan adalah 35.78%.
Saran
Pencirian zeolit alam teraktivasi disarankan tidak terbatas hanya pada FTIR, AAS, Autosorb, tetapi dapat dilakukan pencirian lebih lanjut untuk melihat bentuk kristal dengan Scanning Electron
Microscopy (SEM) dan jenis kristal dengan
X-Ray Difraction (XRD). Selanjutnya dilakukan uji katalitik pada reaksi lainnya seperti perengkahan, isomerisasi untuk menguji aktivitas katalitiknya dan selektivitas zeolit alam murni dan zeolit alam teraktivasi asam.
DAFTAR PUSTAKA
Anwar C. 1992. Sintesis katalis zeolit untuk konversi methanol-bensin. Di dalam: Prosiding Diskusi Ilmiah VII Hasil Penelitian LEMIGAS; Jakarta, 11-13 Februari 1992. Jakarta: PPPTMGB (Pusat Penelitian dan Pengembangan Teknologi Minyak dan Gas Bumi) LEMIGAS. Hlm 731-745.
[P3TM] Pusar Penelitian & Pengembangan Teknologi Mineral. 1994. Cara Uji
Pengukuran Luas Permukaan Spesifik Mineral Zeolit. Bandung: Pusat
Penelitian & Pengembangan Teknologi Mineral.
Atkins. 1999. Kimia Fisik jilid 1 Edisi ke
empat. Diterjemahkan oleh Irma I.
Kartohadiprojo. Jakarta: Erlangga. Augustine, RL. 1996. Heterogeneous
Catalysis for the Synthetic Chemistry.
New York: Marcel Dekker.
Clark. 1979. Industrial Mineral: Zeolit The
Hydrothermal Deposit. New York:
Pergamon.
Feuge RO, Zeringue Jr HJ, Weiss TJ, Brown M. 1970. Preparation of sucrose mono-laurate. Am J Oil Chem Soc 33: 424. Goenadi DH. 1993. Proposal Parameter
Standar Industri Indonesia untuk Zeolit Alam. Bogor: Pusat Penelitian Bioteknologi Perkebunan.
Goltardi G & Galli E. 1985. Natural
Zeolites. New York: Springer Verlag.
Handoko SD. 2001. Aktivitas katalitik Cr/zeolit dalam reaksi konversi katalitik fenol dan metil isobutil keton [skripsi]. Jember: Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Jember.
Handoko SD. 2001. Preparasi katalis Cr/zeolit melalui modifikasi zeolit alam. [tesis]. Jember: Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Jember.
Hisbullah. 2000. Karakteristik adsorpsi logam-logam berat menggunakan zeolit yang dimodifikasi dengan SiCl4
[skripsi]. Padang: Fakultas Teknik, Universitas Syiah Kuala.
Jon H. 2001. Pencirian zeolit alami termodifikasi asam [skripsi]. Bogor : Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Khopkar SM. 1990. Konsep Dasar Kimia
Analitik. Terjemahan A. Saptoraharjo.
Jakarta: UI Press.
Muchtar H. 1983. Penentuan pengaruh perlakuan dengan logam terhadap daya adsorpsi zeolit alam pada pemurnian wax [skripsi]. Padang: Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Andalas.
Mumpton FA. 1984. The Role of Natural
Zeolites in Agriculture and Aquaculture. Colorado: West View
Press Boulder.
Obaje OJ, penemu: URAH Resources Ltd. 25 Jan 2005. Trans-acidolysis process for the preparation of carbohydrate fatty-acid esters. US patent 6 846 916. Othmer & Kirk. 1995. Encyclopedia of
Chemical Technology. Ed ke-4. New
York: J Wiley.
Prihanjani M. 2006. Sintesis ester glukosa miristat melalui interesterifikasi antara metil miristat dan glukosa pentaasetat [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuam Alam, Institut Pertanian Bogor.
Purwaningsih H. 1998. Isomerisasi xilena dengan katalis bentonit [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Riberio RF et al. 1984. Ion Exchange
Separation With Molecular Sieves Zeolites. Boston: Martinus Nyhoff.
Rodrigues MGF, Magnoux P & Guisnet M.2000. Influence of hydrothernal treatment on acid and redox function of Ga/HZSM5 catalyst. Braz.J.Chem Eng 17: 1-6.
Rohaeni A. 2005. Penetapan kapasitas jerapan zeolit dan zeolit termodifikasi heksadesiltrimetil amoniumbromida terhadap K2Cr2O7 [skripsi]. Bogor:
Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Sembiring N. 2004. Zeolit: Mineral Masa Depan. http://www.teropong.co.id. [17 Februari 2006].
Shang CC & Lee MD 1994. Effect of hydrogen pretreatment on the acidic and catalytic properties of galium-supported H-ZSM-5 in n-hexane aromatization.
Applied Catalysis A. General 123: 7-21.
Supriatna Asep, dkk. 1996. Kinetika serapan zeolit terhadap ion sianida. Di dalam: Prosiding Seminar Nasional Kimia II. Jakarta: Fakultas Matematika dan Ilmu
Pengetahuan Alam, Universitas Islam Indonesia.
Sutarti M & Minta R. 1994. Zeolit Tinjauan
Literaturat. Jakarta: Pusat Dokumetasi
dan Informasi Ilmiah, LIPI.
Suyartono & Husaini. 1991. Tinjauan Terhadap Kegiatan Penelitian Karakteristik dan Pemanfaatan Zeolit Indonesia yang Dilakukan P3TM Periode 1980-1991. Bandung: Pusat Penelitian Pengembangan Teknologi Mineral.
Tang Y R. 2003. Adsorbent Fundamental
and Applications. Canada: J Wiley.
Zulnely. 1985. Study pendahuluan logam mangan dalam air dengan zeolit bayah [tesis]. Padang: Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Andalas.