KELAHIRAN ANAK TIKUS NORMAL DAN FERTIL HASIL
INTRACYTOPLASMIC SPERM INJECTION
SYAHRUDDIN SAID
Pusat Penelitian Bioteknologi LIPI, Jl. Raya Bogor Km. 46, Cibinong 16911
ABSTRACT
Normal Birth and Fertile of Rats through Intracytoplasmic Sperm Injection
Intarcytoplasmic sperm injection (ICSI) has progressively accepted in human infertility clinics as the method to overcome the infertility of patients with severe male factors. However, almost no information is available about fertility of offspring resulted from ICSI. The aim of this research was to test in vivo developmental rat embryos derived from ICSI and fertility of delivered offsprings was examined by randomly mated among rat-ICSI and/or non-ICSI. At 9-12 h after injection of sperm heads, 153 oocytes with two pronuclei and second polar body were transferred to 12 recipients, resulted 33 (22%) embryos were implanted and only 6 (4%) embryos developed into normal offsprings. This results was significantly lower (P<0.01) compared with transferred embryos derived from naturally mated with implantation rates 58 (92%) and offspring rates 49 (78%). When offsprings grew into adult and were randomly mated among rat-ICSI and/or non-ICSI, revealed that all of offspring derived from ICSI capable to mate and take care of pregnancy until deliver. These results demonstrated that rat embryos derived from ICSI can result in birth of live offspring, and the offspring grew into normal and fertile adult.
Key words: Offspring, normal, fertile, ICSI, rat
PENDAHULUAN
Setelah UEHARA dan YANAGIMACHI (1976, 1977) pertama kali melaporkan bahwa inti spermatozoa hamster mampu tumbuh menjadi pronuclei setelah diinjeksi kedalam sel telur hamster, intracytoplasmic sperm injection (ICSI) diaplikasikan secara luas terhadap berbagai jenis mamalia seperti pada kelinci (KEEFER, 1989), sapi (GOTO et al., 1990; GOTO, 1993), babi (IRITANI et al., 1992), manusia (PALERMO et al., 1992; BOURNE et al., 1995), mencit (AHMADI et al.,
1995; KIMURA dan YANAGIMACHI, 1995; KURETAKE et
al., 1996) dan tikus (HIRABAYASHI et al., 2002). Khususnya pada manusia, ICSI digunakan sebagai pilihan untuk mengatasi persoalan infertility pria (PALERMO et al., 1992; VAN STEIRTEGHEM et al., 1993; DEVROERY et al., 1994; NAGY et al., 1995). Akan tetapi timbul kekhawatiran akan kesuburan anak hasil ICSI. Hal ini disebabkan adanya kemungkinan kerusakan spermatozoa selama proses persiapan dan manipulasi. Begitu pula pada sel telur akan kemasukan benda asing pada saat ICSI bersama dengan spermatozoa seperti PVP (polyvinylpyrrolidone) atau runtuhan sel, dimana diketahui bahwa PVP berpengaruh jelek terhadap perkembangan sel telur (WEI dan FUKUI, 2000). Berangkat dari hal tersebut, pada penelitian ini akan mencoba menjawab kekhawatiran kemungkinan terjadinya kelainan reproduksi khususnya tingkat kesuburan anak hasil ICSI.
MATERI DAN METODE
Media
Medium dasar yang digunakan untuk manipulasi sel telur dan spermatozoa adalah modified Krebs-Ringer bicarbonate solution dengan penambahan Hepes (Hepes-mKRB). Kandungan medium ini adalah sebagai berikut; 94.6 mM NaCl, 4.78 mM KCl, 1.71 mM CaCl2, 1.19 mM KH2PO4, 1.19 mM MgSO4, 5.0 mM NaHCO3, 5.56 mM glukosa, 21.58 mM laktat, 0.5 mM Na-piruvat, 4 mg/ml BSA (A-7638; Sigma Chemical Co., St Louis, MO), 75 µg/ml K-penisilin G, 50 µg/ml streptomisin sulfat dan 20 mM Hepes (Sigma), medium ini sama dengan yang digunakan TOYODA dan CHANG (1974) untuk fertilisasi in vitro pada sel telur tikus, kecuali penurunan konsentrasi NaHCO3 dari 25.07 mM menjadi 5.0 mM dan penambahan 20 mM Hepes.
Koleksi sel telur
Tikus Wistar betina (umur 8-12 minggu) disuperovulasi dengan menyuntikkan secara intra-peritoneal 25-30 IU pregnant mare serum gonadotropin (PMSG), diikuti dengan penyuntikan 25-30 IU human
chorionic gonadotropin (hCG) 48 jam kemudian, sel
telur dikoleksi 15-16 jam setelah penyuntikan hCG. Sel kumulus dihilangkan dengan menggunakan 0,1% bovine testicular hyaluronidase (Sigma) dalam
Hepes-_____________________________________________________________________________________________ mKRB. Sel telur yang terkoleksi dicuci dan disimpan
dalam mKRB pada suhu 370C, 5% CO2 sambil menunggu persiapan mikromanipulator.
Koleksi spermatozoa dan isolasi kepala sperma
Spermatozoa dikoleksi dari cauda epididymis tikus Wistar jantan (umur 4-8 bulan) berdasarkan metode SAID et al. (1999). Pemisahan kepala spermatozoa dengan ekor dilakukan dalam media isolasi. Sonikasi dilakukan pada suhu 00C selama 10 detik dengan menggunakan Ultrasonic sonicator Model Bronson Sonifier 250 pada 30 duty cycle dan 4 out-control. Larutan spermatozoa yang telah disonikasi diencerkan dengan Hepes -mKRB dan dicuci dengan cara sentrifugasi 1,000 g selama 3 menit. Endapan spermatozoa selanjutnya dipindahkan ke kedium manipulasi spermatozoa yang mengandung 5 µg/ml
cytocalasin B.
Injeksi spermatozoa ke dalam oosit
Kepala spermatozoa dimasukkan ke dalam sitoplasma sel telur dengan menggunakan mikropipet yang dihubungkan dengan piezo -injection manipulator (PMM-150FU, Prime Tech LTD, Japan). Kepala spermatozoa dan sel telur ditempatkan bersama dalam satu drop 5 µl Hepes-mKRB mengandung 5 µg/ml cytocalasin B ditutup dengan mineral oil pada temperatur 370C. Kepala spermatozoa diaspirasi ke dalam pipet injeksi, selanjutnya ujung pipet disentuhkan ke zona pellucida sel telur dengan posisi polar body pada jam 6 atau 12. Sambil menekan, dengan sedikit elektrik piezo, zona akan terlubangi. Ujung injeksi pipet secara mekanik ditekan lebih ke dalam sel telur, dan pipet akan masuk ke dalam oolemma sel telur dengan memberikan sedikit elektrik piezo. Kepala sperma dikeluarkan dan masuk ke dalam ooplasma bersama sedikit medium manipulasi.
Embryo transfer
Resipien disiapkan dengan merangsang tikus betina dengan memasukkan batangan gelas dihubungkan dengan listrik vibrator ke dalam vagina antara pukul 19:30 dan 20:00 pada saat proestrus. Keesokan harinya antara pukul 9:00 dan 10:00 resipien dianastesi dengan menyuntikkan avertin (0.012 ml/g berat badan; Aldrich Chemical Co., Inc., Milwaukee, WI), selanjutnya ovari dan oviduct dikeluarkan melalui sedikit pembelahan pada punggung. Enam sampai sembilan embrio dimasukkan kesetiap oviduct. Setelah ditransfer vagina smear resipien diperiksa setiap hari.
Rancangan percobaan
Percobaan 1 bertujuan untuk melihat kemampuan pertumbuhan embrio hasil ICSI setelah ditransfer ke resipien. Sel telur yang berhasil diinjeksi dengan kepala spermatozoa dikultur selama 9-12 jam dengan medium mKRB dalam incubator CO2 (5% CO2 , 370C). Sel telur yang mengalami pembuahan normal (memiliki 2 pronukleus dan keluarnya polar bodi ke-2) ditransfer ke resipien. Resipien yang memperlihatkan siklus proestrus atau estrus, dimatikan kemudian diperiksa implantasi pada uterus. Resipien yang mampu memelihara kebuntingan sampai lahir, anaknya dihitung dan resipien tersebut dimatikan untuk pemeriksaan tingkat terjadinya implantasi. Percobaan 2 untuk melihat apakah anak hasil ICSI mampu tumbuh dewasa dan fertil. Anak yang diperoleh dari hasil ICSI dipelihara dengan induk titipan. Setelah berumur 21 hari anak dipelihara tersendiri sampai dewasa kelamin (berumur 2 bulan). Selanjutnya anak hasil ICSI tersebut dikawinkan baik antara sesama (jantan hasil ICSI Vs betina hasil ICSI) maupun kawin silang (jantan hasil ICSI Vs betina biasa) atau (jantan biasa vs betina hasil ICSI). Anak yang lahir dari hasil perkawinan ini dicatat.
Analisa statistik
Perbedaan tingkat implantasi dan anak yang lahir hasil ICSI dan hasil perkawinan alami dianalisa menggunakan uji X2.
HASIL
Seperti yang diperlihatkan pada Tabel 1 bahwa dari 153 embrio tahap 1 sel hasil ICSI ditransfer ke 12 ekor resipien menghasilkan 33 (22%) embrio tertanam di rahim, selanjutnya hanya 6 (4%) yang berhasil tumbuh sampai lahir dengan jenis kelamin 3 ekor jantan dan 3 ekor betina (Gb. 1). Ketika 64 embrio tahap 1 sel yang diperoleh dari hasil perkawinan alami ditransfer ke 4 ekor resipien, umumnya embrio berhasil tertanam di rahim 58 (92%) dan selanjutnya sebanyak 49 (78%) embrio berhasil lahir dengan proporsi jenis kelamin 35 ekor jantan dan 14 ekor betina. Hasil tingkat implantasi dan tingkat kelahiran anak hasil ICSI secara jelas berbeda sangat nyata (P<0,01) lebih rendah dibandingkan dengan hasil dari perkawinan alami.
Data pada Tabel 2 memperlihatkan hasil perkawinan silang baik antara sesama hasil ICSI maupun antara hasil ICSI dengan tikus hasil perkawinan alami. Dari data tersebut terlihat bahwa tikus dari hasil ICSI mampu kawin dan menghasilkan anak secara normal seperti dengan tikus hasil perkawinan alami (Gambar 2).
.
Tabel 1. Kelahiran anak tikus hasil transfer embrio tahap 1 sel hasil ICSI ke resipien
Perlakuan Jumlah resipien Jumlah embrio Jumlah implantasi Jumlah anak lahir (%) Jenis kelamin anak
ICSI 12 153 33 (222)a 6 (4)a 3 , 3
In vivo* 4 63 58 (92)b 49 (78)b 35 , 14
1
Persentasi dari jumlah embrio ditransfer.
* Embrio diperoleh dari hasil perkawinan alam.
= Jenis kelamin jantan; = Jenis kelamin betina
a,b
Berbeda di setiap kolom berbeda nyata P<0,01
Tabel 2. Hasil perkawinan silang anak hasil ICSI
Perkawinan Jumlah anak lahir Jenis kelamin Rata-rata berat lahir (gr)
ICSI ( ) Vs ICSI ( ) 16 9 , 7 6,39
ICSI ( ) Vs Biasa ( ) 12 3 , 9 6,33
ICSI ( ) Vs Biasa ( ) 18 10 , 8 4,74
Biasa ( ) Vs Biasa ( ) 17 6 , 11 6,31
= Jenis kelamin jantan; = Jenis kelamin betina
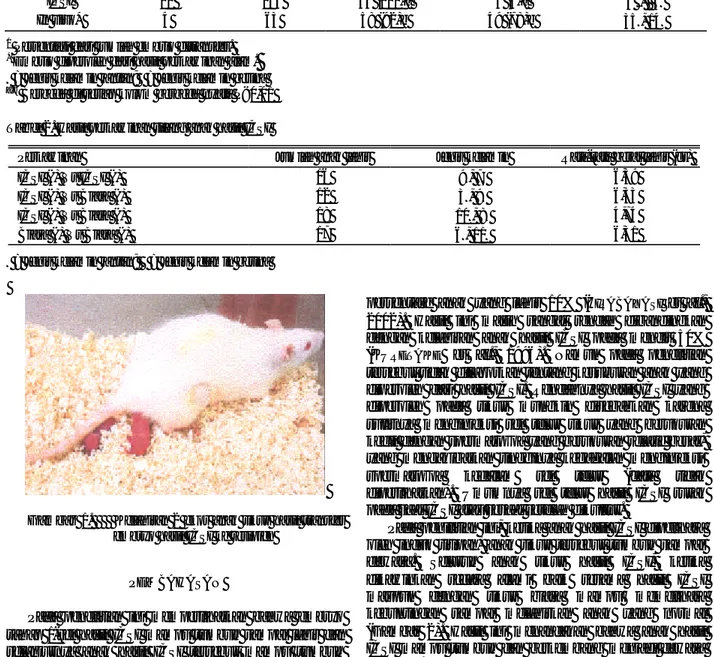
Gambar 1. Kelahiran 2 ekor anak tikus hasil transfer
embryo hasil ICSI ke resipien
PEMBAHASAN
Pada penelitian ini memperlihatkan bahwa embryo tahap 1-sel hasil ICSI mampu tumbuh sampai lahir dan selanjutnya anak hasil ICSI tersebut mampu tumbuh sampai dewasa dan melakukan perkawinan, memelihara kebuntingan sampai melahirkan anak. Hal ini menunjukkan bahwa anak yang diperoleh dari hasil ICSI mampu tumbuh sampai dewasa dan fertil. Dari 153 embrio tahap 1-sel hasil ICSI ditransfer ke 12 ekor resipien menghasilkan 33 (22%) embrio tertanam di rahim, selanjutnya hanya 6 (4%) yang berhasil tumbuh sampai lahir (Gambar 1). Hasil ini jika dibandingkan transfer embryo tahap 1-sel yang diperoleh dari hasil perkawinan alami berbeda sangat nyata (P<0,01) lebih rendah, dengan hasil implantasi 58 (92%) dan anak yang lahir sebanyak 49 (78%). Satu-satunya hasil penelitian yang melaporkan keberhasilan kelahiran anak tikus hasil ICSI dengan tingkat implantasi 19% dan
persentase anak yang lahir 10% (HIRABAYASI et al.,
2002). Hasil ini masih sangat rendah dibandingkan dengan kelahiran anak hasil ICSI pada mencit 50% (KURETAKE et al., 1996). Namun pada penelitian tersebut tidak dilaporkan tentang kesuburan anak yang diperoleh dari hasil ICSI. Rendahnya hasil ICSI yang diperoleh pada tikus mungkin disebabkan karena sulitnya menginjeksi sel telur tikus yang berukuran kecil dengan spermatozoa yang berukuran relatif besar, yang mengakibatkan tingginya kegagalan menginjeksi spermatozoa kedalam sel telur (data tidak diperlihatkan). Umumnya sel telur hasil ICSI rusak pada saat ICSI atau sesaat setelah dikultur.
Pada penilitian ini, ketika anak hasil ICSI dipelihara oleh induk titipan, anak tikus tersebut tumbuh sampai dewasa. Seluruh anak tikus hasil ICSI, ketika dikawinkan secara alami baik sesama hasil ICSI maupun dengan tikus biasa mampu memelihara kebuntingan sampai melahirkan anak yang normal (Gambar 2). Hasil ini menandakan bahwa anak hasil ICSI mampu tumbuh dan berkembang menjadi dewasa dan fertil.
Umumnya dalam pelaksanaan ICSI, medium manipulasi spermatozoa ditambahkan PVP (polyvinylpyrrolydone) untuk memudahkan kontrol spermatozoa masuk ke dalam pipet injeksi dan untuk menghindari terjadinya perlengketan spermatozoa dengan pipet injeksi. Akan tetapi PVP berefek negatif ketika PVP ikut terinjeksi bersama dengan spermatozoa ke dalam sel telur. Telah dilaporkan pada manusia bahwa PVP berefek negatif terhadap tingkat pembuahan, kualitas embryo dan tingkat pertumbuhan sampai tahap blastosis (KUCZYNSKI et al., 1996). Peningkatan terjadinya pronucleus setelah ICSI dengan
_____________________________________________________________________________________________ menurunkan konsentrasi PVP telah dilaporkan pada
sapi (WEI danFUKUI, 2000). Pada penelitian ini, tidak
Gambar 2. Anak tikus umur 1 hari hasil dari perkawinan antara tikus jantan hasil ICSI dan tikus betina biasa. Berukuran 1 cm
menggunakan PVP dalam medium manipulasi spermatozoa, selama hanya menggunakan kepala spermatozoa yang jelas diketahui tidak bergerak lagi, sangat mudah menyedotnya ke pipet injeksi. Selanjutnya selama kepala spermatozoa hanya ditempatkan pada ujung pipet injeksi, sangat mudah melepaskan kepala sperma kedalam sitoplasma sel. Dengan demikian, dengan tidak menggunakan PVP, medium yang terikut kedalam sitoplasma sel telur pada saat ICSI sangat sedikit dan kepala spermatozoa dapat bercampur langsung dengan sitoplasma sel telur. Sebaliknya ICSI dengan PVP, karena PVP menyebabkan medium menjadi kebih kental sehingga terkadang spermatozoa masih berada dalam spot PVP medium, spermatozoa tidak langsung bergabung dengan sitoplasma sel telur. Kejadian ini pada sapi mencapai 28,3% (WEI danFUKUI, 2000).
KESIMPULAN
Dari uraian di atas dapat disimpulkan bahwa ICSI pada tikus mampu melahirkan anak yang normal dan fertil. Dengan perbaikan teknik ICSI pada tikus dapat diharapkan akan mampu memberikan hasil yang lebih baik diwaktu mendatang.
DAFTAR PUSTAKA
AHMADI, A, S.C. NG, S.L. LIOW, J. ALI, A. BONGSO and S.S. RATNAM. 1995. Intracytoplasmic injection of mouse
oocytes with 5 mM Ca++ at different intervals. Hum Reprod.10, 431-435.
BOURNE, H., N. RICHING, D.Y. LIU, G.N. CLARKE, O. HARARI
and H.W.G. BAKER. 1995. Sperm preparation for intracytoplasmic injection: methods and relationship to fertilization results. Reprod Fertil Dev. 7, 177-183. DEVROERY, P., J. LIU, Z. NAGY, H. TOURNAYE, S.J. SILBER
andA.C. VAN STEIRTEGHEM. 1994. Normal fertilization of human oocytes after testicular sperm extraction and intracytoplasmic sperm injection. Fertil Steril. 62, 639-641.
GOTO, K. 1993. Bovine micro fertilization and embryo transfer. Mol Reprod Dev.;36, 288-290.
GOTO, K, A. KINOSHITA, Y. TAKUMA andK. OGAWA. 1990.
Fertilization of bovine oocytes by the injection of immobilized, killed spermatozoa Vet Rec.127, 517-520. HIRABAYASHI, M., M. KATO, T. AOTO, A. SEKIMOTO, M.
UEDA, I. MIYOSHI, N. KASAI and S. HOCHI. 2002.
Offspring derived from intracytoplasmic injection of transgenic rat sperm .Trans Res. 11, 221-228.
IRITANI, A., K. UTSUMI and Y. HOSOI. 1992. Fertilization by
assisted micromanipulation of gametes. In Embryonic Development and Manipulation in Animal Production. pp 51-57 Eds A Lawria and F Gandolfi. Portland Press, London
KEEFER, C.L. 1989. Fertilization by sperm injection in the rabbit Gam Res. 22, 59-69.
KIMURA, Y and R . YANAGIMACHI. Intracytoplasmic sperm injection in the mouse. 1995. Biol Reprod. 52, 709-720. KURETAKE, S., Y. KIMURA, K. HOSHI andR. YANAGIMACHI.
1996. Fertilization and development of mouse oocytes injected with isolated sperm heads. Biol Reprod. 55, 789-795.
KUCZYNSKI, W., J. SZAMATOWICZ, A. KRUKOWSKA, S. WOLCZYNSKI, M. SYREWICZ, and M . SZAMATOWICZ. 1996. Pronuclear formation and early embryo development after ICSI: polyvinylpyrrolidone and piezoelectric sperm immobilization effects. Hum Reprod. 11 (Abstract Bk. 1):89-90 (abstract).
NAGY, Z.P., J. LIU, H. JORIS, G. VERHEYEN, H. TOURNAYR, M. CAMUS and M.C. DERDE. 1995. The result of intracytoplasmic sperm injection is not related to any of the three basic sperm parameters. Hum Reprod. 10, 1123-1129.
PALERMO, G., H. JORIS, P. DEVROEY and A.C. VAN
STEIRTEGHEM. 1992. Pregnancies after intracytoplasmic injection of single spermatozoa into an oocyte. Lancet.
340, 17-18.
SAID, S., H. FUNAHASHI and K. NIWA. 1999. DNA stability and thiol-disulphide status of rat sperm nuclei during epididymal amturation and penetration of oocytes. Zygote, 7, 249-254.
TOYODA, Y. andM.C. CHANG. 1974. Fertilization of rat eggs in vitro by epididymal spermatozoa and the development of eggs following transfer. J. Reprod. Fertil. 36, 9-22.
UEHARA, T and R. YANAGIMACHI. 1976. Microsurgical injection of spermatozoa into hamster eggs with subsequent transformation of sperm nuclei into male pronuclei. Biol Reprod. 15, 467-470.
UEHARA, T andR. YANAGIMACHI. 1977. Behavior of nuclei of testicular, caput and cauda epididymal spermatozoa injected into hamster eggs. Biol Reprod.16, 315-321.
VAN STEIRTEGHEM, A.C., Z. NAGY, J. JORIS, J. LIU, C. STAESSEN, J. SMITZ, A. WASANTO and P . DEVROEY. 1993. High fertilization and implantation rates after intracytoplasmic sperm injection. Hum Reprod. 8, 1061-1066.
WEI, H. and Y. FUKUI. 2000. Technical improvement in intracytoplasmic sperm injection (ICSI) in cattle. J Reprod Dev. 46, 403-407.