TINJAUAN PUSTAKA
Kelapa Sawit
Kelapa sawit (Elaeis guineesis, Jacq) termasuk famili Palmae, subklas Monocotyledoneae, Klas Angiospermae, Subdivisi Tracheophyta. Nama Genus Elaeis berasal dari bahasa Yunani Elaion atau minyak, sedangkan nama guineensis berasal dari kata Guines, yaitu nama tempat dimana seseorang bernama Jacquin menemukan tanaman sawit pertama kali di pantai Guines Afrika Selatan (Hartley 1977; Ketaren 2005).
Kelapa sawit merupakan tanaman asli Afrika dan tumbuh secara alami di Afrika Selatan dan Afrika Barat. Tanaman ini dapat tumbuh baik pada daerah beriklim tropis dengan curah hujan 2000 mm/tahun dan kisaran suhu 22-32oC (Ketaren 2005). Dewasa ini tanaman kelapa sawit telah menyebar di Kongo, Indonesia, Malaysia dan Amerika Selatan. Di Indonesia sendiri, tanaman kelapa sawit pertama kali masuk pada tahun 1848 di masa pemerintahan kolonial Belanda dan ditanam pertama kali di Kebun Raya Bogor, serta mulai diusahakan dan dibudidayakan secara komersial pada tahun 1911 (Fauzi et al. 2006).
Kelapa sawit terdiri atas empat varietas, yaitu : 1) Varietas Macrocarya, tebal tempurung 5 mm, 2) Varietas Dura, tebal tempurung 3-5 mm, 3) varietas Tenera, tebal tempurung 2-3 mm, 4)Varietas Pisifera, bagian tempurung tipis (Ketaren 2005). Tenera merupakan hasil persilangan antara Dura dengan Pisifera serta ektraksi minyaknya sekitar 22-25 persen (Pahan 2006). Menurut Baryeh (2001), Tenera mempunyai yield yang paling baik yaitu 30 ton per hektar per tahun pada puncak produktivitasnya. Tenera secara luas dikembangkan karena komersial dan viabilitas pengolahan yang lebih mudah dipanen karena pohonnya relatif pendek, menghasilkan tandan buah yang baik dan kadar minyak yang lebih tinggi (Noor Azian, 1995 diacu dalam Morad et al. 2006).
Buah sawit umumnya berukuran 2-5 cm dan berat antara 3-30 gram, berwarna ungu hitam pada saat muda, kemudian menjadi berwarna kuning merah pada saat tua dan matang (Muchtadi 1992). Warna daging buah putih kuning ketika masih muda dan berwarna jingga setelah buah matang (Ketaren 2005).
Penampang melintang dan membujur buah kelapa sawit dapat dilihat pada Gambar 1. Secara anatomi, bagian-bagian buah kelapa sawit adalah:
1. Perikarp
Kelapa sawit mengandung kurang lebih 80 persen perikarp dan 20 persen buah yang dilapisi kulit yang tipis. Kelapa sawit menghasilkan 2 jenis minyak yang sifatnya sangat berbeda, yaitu minyak dari sabut (minyak sawit kasar) dan minyak dari biji (minyak inti sawit) (Somaatmadja 1981). Perikarp terdiri dari :
a. Epikarp, yaitu kulit buah yang keras dan licin
b. Mesokarp, yaitu bagian buah berserabut dan mengandung minyak dengan rendemen paling tinggi, menghasilkan minyak sawit mentah (CPO) melalui ekstraksi. Menurut Morad et al. (2006), mesokarp jumlahnya sekitar 60% dari total komposisi buah kelapa sawit dan CPO dihasilkan dari bagian ini. Mesokarp mengandung 39 persen minyak, 41 persen air dan serat 20 persen dari keseluruhan komposisi.
2. Biji, terdiri dari :
a. Endokarp (kulit biji = tempurung), berwarna hitam dan keras
b. Endosperm (kernel = daging biji) berwarna putih yang menghasilkan minyak inti sawit (PKO)
c. Lembaga/embrio
Gambar 1 Struktur buah kelapa sawit
Endosperm Mesokarpium
Epikarpium
Pengolahan Kelapa Sawit Menjadi Minyak Sawit Kasar
Pengolahan kelapa sawit untuk menghasilkan minyak sawit kasar dimulai dari penanganan bahan baku atau tandan buah segar (TBS) pada saat pemanenan hingga sampai di pabrik. Setelah tiba di pabrik, TBS selanjutnya melalui serangkaian tahapan pengolahan TBS hingga menjadi CPO melalui perebusan, perontokan (pemipilan), pelumatan (pencacahan), ekstraksi minyak, dan klarifikasi (Siregar 1999).
Perebusan
TBS yang ada di lori perebusan dimasukkan ke dalam sterilizer yang dapat ditutup dengan rapat untuk menghindari terjadinya pengeluaran steam sebagai media perebus. Proses perebusan berlangsung pada suhu 135-160oC selama 90-110 menit dengan tekanan 2.8-3.0 kg/cm2. Perebusan ini bertujuan untuk mempermudah pelepasan buah dari tandan, melunakan buah sehingga mempermudah dalam proses penghancuran, menonaktifkan enzim lipase dan oksidase yang dapat merangsang pembentukan asam lemak bebas, menurunkan kadar air di dalam jaringan buah, memudahkan pemisahan tempurung dengan inti, menguraikan pektin dan polisakarida sehingga buah menjadi lunak.
Perontokan
Perontokan bertujuan untuk memisahkan tandan dengan buah. Proses perontokan buah terjadi akibat perputaran mesin perontok. Mesin perontok buah memiliki batang-batang penghubung yang diatur dengan interval yang sama. Diameter dan panjang mesin perontok buah adalah 2.1 m dan 4 m, sementara jarak antara dua batang penghubung 40 mm.
Pelumatan (pencacahan)
Pelumatan dilakukan untuk memisahkan buah dengan biji serta untuk memudahkan proses ekstraksi minyak. Pelumatan dilakukan dengan cara pengadukan buah oleh alat yang dilengkapi lima pasang pisau berputar. Pada proses pelumatan ini perlu ditambahkan air bersuhu 90-95oC untuk
mempermudah pemisahan buah dengan biji serta untuk membuka kantong-kantong minyak sehingga mengurangi kehilangan minyak. Suhu yang rendah mengakibatkan minyak semakin kental sehingga menyulitkan ekstraksi minyak.
Ekstraksi minyak
Ekstraksi merupakan proses untuk memperoleh minyak dari buah yang telah mengalami pencacahan. Proses ekstraksi dilakukan secara mekanis untuk mengeluarkan kandungan minyak. Buah yang telah dicacah dimasukkan ke dalam mesin pengepres ulir yang terdiri atas dua ulir yang berputar berlawanan dan dilengkapi dengan saringan pengepres. Buah yang telah lumat mengeluarkan minyak melalui lubang-lubang kecil.
Selama proses ekstraksi ditambahkan air bersuhu 90-95oC sebanyak 600-800 liter/jam untuk memudahkan ekstraksi minyak. Tekanan hidrolik pada mesin pengepres berkisar antara 40-50 kg/cm2. Tekanan yang rendah menyebabkan proses ekstraksi minyak tidak maksimal.
Klarifikasi
Klarifikasi adalah proses pembersihan minyak yang bertujuan untuk mengeluarkan air dan kotoran dari minyak, memperkecil kerusakan minyak akibat oksidasi, memperkecil kehilangan minyak dan menekan biaya produksi, serta mempermudah pengolahan limbah.
Klarifikasi terdiri dari beberapa tahapan proses, yaitu pemisahan kotoran berupa serabut dan lumpur, pemisahan minyak dengan air, pengambilan minyak yang terdapat pada lumpur serta pembersihan. Pemisahan kotoran yang berupa serabut dilakukan dengan saringan getar, pemisahan kotoran yang berupa lumpur dilakukan pada decanter, pemisahan minyak dengan air terjadi pada tangki pengendapan, sedangkan pembersihan minyak dilakukan pada alat pembersih minyak (oil purifier).
Minyak hasil ekstraksi ditampung pada tangki perangkap pasir, tangki tersebut digunakan untuk memisahkan pasir dari minyak. Pemisahan pasir terjadi akibat perbedaan berat jenis antara pasir, minyak dan air dengan pemberian uap panas ke dalam tangki perangkap pasir. Minyak selanjutnya dialirkan ke dalam
saringan getar yang bertujuan untuk memisahkan benda-benda padat dalam minyak, saringan getar menggunakan kawat saringan berukuran 20 mesh.
Minyak yang telah disaring dialirkan ke dalam decanter, pada alat ini terjadi proses pemisahan kotoran berupa lumpur dengan cara sentrifugasi 6000 rpm, pada proses tersebut digunakan air panas sebagai pengencer. Lumpur yang mungkin masih terdapat pada minyak selanjutnya dipisahkan berdasarkan bobot jenis. Air yang terkandung pada minyak dihilangkan dengan alat pengering hampa agar minyak tidak mudah terhidrolisis. Minyak yang diperoleh berupa minyak sawit kasar (CPO) yang selanjutnya ditimbang dan disimpan dalam tangki penampungan. Persyaratan kualitas CPO dapat dilihat pada Tabel 1.
Lumpur yang masih mengandung minyak dari tangki pengendap dialirkan ke dalam tangki lumpur. Cairan lumpur hasil klarifikasi yang masih mengandung minyak tersebut ditampung sementara pada bak penampungan untuk di daur ulang.
Tabel 1 Persyaratan kualitas CPO*)
Karakteristik Kualitas spesial Standar kualitas I Standar kualitas II Asam lemak bebas (sebagai asam palmitat)
(% maks) 2.5 3.5 5.0
Kadar air dan kotoran (% maks) 0.25 0.25 0.25
Bilangan peroksida (meq O2/kg maks) 2.0 - -
Bilangan anisidin (maks) 4.0 - -
*) Gibon et al. (2007)
Pemurnian Minyak Sawit Kasar
Pemurnian minyak bertujuan untuk menghilangkan rasa serta bau yang tidak enak, warna yang tidak menarik serta memperpanjang masa simpan minyak sebelum dikonsumsi atau digunakan sebagai bahan baku dalam industri. Kotoran-kotoran yang ada dalam minyak dapat berupa komponen yang tidak larut dalam minyak. Komponen yang tidak larut dalam minyak adalah lendir atau getah, abu atau mineral. Komponen yang berupa suspensi koloid adalah fosfolipid, karbohidrat dan senyawa yang mengandung nitrogen, sedangkan komponen yang larut dalam minyak berupa asam lemak bebas, sterol, hidrokarbon, mono dan
digliserida serta zat warna yang terdiri dari karotenoid dan klorofil (Ketaren 2005).
Tahapan proses pemurnian minyak sawit secara kimia meliputi tiga tahap yaitu (1) degumming dan netralisasi atau deasidifikasi, (2) bleaching dan filtrasi, serta (3) deodorisasi (Basiron 2005).
Degumming
Pengolahan minyak sawit merah dari minyak sawit mentah diawali dengan degumming. Degumming diartikan sebagai suatu proses pemisahan getah atau lendir yang terdapat dalam minyak tanpa mereduksi asam lemak bebas yang ada. Getah atau lendir pada umumnya terdiri atas fosfatida, protein, dan karbohidrat. Kotoran-kotoran yang tersuspensi tersebut sukar dipisahkan bila berada dalam kondisi anhydrous, sehingga dapat diendapkan dengan cara hidrasi. Hidrasi dapat dilakukan dengan menggunakan uap, penambahan air, atau dengan penambahan larutan asam lemah (Dijkstra dan Van Opstal 1990).
Asam fosfat, cairan yang tidak berwarna dan tidak berbau. Termasuk dalam food grade dengan konsentrasi 85 persen umumnya digunakan dalam proses pemurnian minyak sawit. Asam fosfat lebih disukai penggunaannya oleh refiner minyak sawit di Malaysia karena biayanya yang lebih murah dan penanganannya lebih mudah (Morad et al. 2006). Penambahan asam fosfat sebelum netralisasi ke dalam minyak yang mengandung fosfatida yang nonhydratable umum dipraktekan untuk menjamin bahwa semua gum telah hilang selama deasidifikasi. Hidrasi dilakukan untuk membuat fosfatida menjadi tidak larut dalam minyak (Basiron 2005).
Menurut Dijkstra dan Van Opstal (1990) asam yang biasa digunakan adalah asam fosfat. Proses degumming dilakukan dengan memanaskan minyak pada suhu 70-80oC setelah ditambahkan asam fosfat (H3PO4) 0.3-0.4 persen (b/b) dengan konsentrasi 20-60 persen (b/b). Sementara menurut Akoh dan Min (2002) sebelum netralisasi minyak diberi perlakuan dengan 0.02-0.5 persen asam fosfat pada suhu 60-90oC selama 15-30 menit, membuat fosfatida yang kurang larut dalam minyak menjadi lebih mudah dihilangkan.
Menurut Basiron (2005) perlakuan pendahuluan diawali dengan degumming CPO dengan asam fosfat. Konsentrasi asam fosfat yang digunakan adalah 80-85 persen dengan jumlah 0.05 – 0.2 persen, dipanaskan sampai 90-110oC dalam waktu 15-30 menit. Tujuan penambahan asam fosfat adalah untuk mengendapkan fosfatida yang nonhydratable. Sedangkan menurut O`Brien (2004) asam yang biasanya digunakan adalah asam fosfat 85 persen, didespersikan dalam minyak pada suhu 80-100oC sebanyak 0.05-1.2 persen berat minyak.
Ooi et al. (1996) melakukan proses refining minyak sawit merah melalui 2 tahapan yaitu tahap pertama melalui proses degumming dan bleaching serta tahap kedua adalah proses deasidifikasi dan deodorisasi. Proses degumming menggunakan asam fosfat (0.5%) pada suhu 90oC selama 10 menit dilanjutkan dengan proses bleaching yang menggunakan bleaching earth (0.2%) selama 30 menit pada suhu 110oC.
Deasidifikasi
Deasidifikasi adalah proses pemisahan asam lemak bebas dalam minyak sawit kasar. Deasidifikasi dapat dilakukan dengan metode kimia, fisik, micella, biologis, reesterifikasi, ekstraksi pelarut, supercritical fluid extraction, dan teknologi membran. Deasidifikasi secara kimia dilakukan dengan cara netralisasi dengan mereaksikan asam lemak bebas dengan basa sehingga membentuk sabun (soapstock). Alkali yang biasa digunakan adalah NaOH, proses ini dikenal dengan istilah ”caustic deacidification” (Bhosle dan Subramanian 2005).
Netralisasi melalui proses kimia dengan alkali, saat ini yang paling umum digunakan adalah dengan melarutkan soda kaustik. Reaksinya adalah reaksi penyabunan yang terbentuk dari asam lemak bebas dapat dilihat pada Gambar 2. Sabun yang terbentuk dapat membantu pemisahan kotoran seperti fosfatida dan protein dengan cara membentuk emulsi. Sabun atau emulsi yang terbentuk dapat dipisahkan dari minyak dengan cara sentrifugasi (Anderson 2005).
asam lemak bebas sabun air Gambar 2 Reaksi penyabunan asam lemak bebas dengan NaOH (Bockisch 1993).
Proses deasidifikasi dilakukan dengan menggunakan larutan sodium hidroksida, dimana minyak dimasukkan ke dalam tangki kemudian dicampur dengan larutan sodium hidroksida (konsentrasinya tergantung kadar asam lemak bebas dalam minyak mentah) pada suhu 70-80oC selama 1-15 menit. Selanjutnya disentrifus untuk memisahkan sabun kemudian dicuci dengan air untuk menghilangkan sisa-sisa sabun (Ayorinde et al. 1995).
Konsentrasi larutan alkali untuk netralisasi biasa dinyatakan dengan “derajat Baume (oBe)”. Konsentrasi bahan kimia yang digunakan dalam netralisasi tergantung pada jumlah asam lemak bebas, makin besar jumlah asam lemak bebas, makin besar pula konsentrasi bahan kimia yang digunakan. Total penambahan alkali didasarkan pada jumlah alkali secara teori untuk menetralkan asam lemak bebas ditambah alkali berlebih (excess) untuk menghilangkan kotoran-kotoran lainnya. Jumlah excess alkali minimum harus digunakan sehingga penyabunan minyak netral dapat diminimalkan (Anderson 2005). Untuk minyak dengan kandungan asam lemak bebas yang rendah lebih baik dinetralkan dengan alkali encer (konsentrasi lebih kecil dari 0.15 N atau 5oBe), sedangkan asam lemak bebas dengan kadar tinggi, lebih baik dinetralkan dengan larutan alkali 10-24oBe (Basiron 2005).
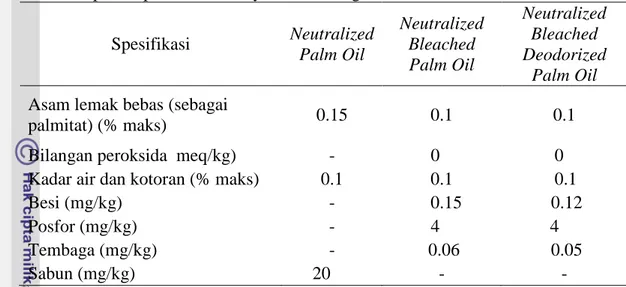
Menurut Bockisch (1993), minyak yang telah dimurnikan dengan baik memiliki kandungan asam lemak bebas sebesar 0.1 persen dan tergantung pada penggunaanya lebih lanjut. Kualitas yang diharapkan pada produk intermediet dan produk akhir proses pemurnian minyak sawit dengan alkali dapat dilihat pada Tabel 2.
Tabel 2 Kualitas yang diharapkan pada produk intermediet dan produk akhir proses pemurnian minyak sawit dengan alkali*)
Spesifikasi Neutralized Palm Oil Neutralized Bleached Palm Oil Neutralized Bleached Deodorized Palm Oil Asam lemak bebas (sebagai
palmitat) (% maks) 0.15 0.1 0.1
Bilangan peroksida meq/kg) - 0 0 Kadar air dan kotoran (% maks) 0.1 0.1 0.1
Besi (mg/kg) - 0.15 0.12 Posfor (mg/kg) - 4 4 Tembaga (mg/kg) - 0.06 0.05 Sabun (mg/kg) 20 - - *) Basiron (2005)
Menurut Akoh dan Min (2002), netralisasi harus dilakukan dengan benar atau beberapa gliserida akan tersabunkan yang mengakibatkan peningkatan refining loss. Minyak dengan bilangan asam yang rendah disebut minyak netral. Netralisasi yang baik itu bergantung pada penggunaan sejumlah natrium hidroksida yang tepat, pengadukan yang tepat, temperatur yang tepat, waktu kontak yang cukup dan pemisahan yang efisien.
Suhu dan waktu yang digunakan dalam proses netralisasi minyak harus dipertimbangkan dengan baik dan dipilih sedemikian rupa sehingga sabun yang terbentuk dalam minyak mengendap dengan kompak dan cepat. Proses pengendapan yang lambat akan memperbesar kehilangan minyak, sebab sebagian minyak akan diserap oleh sabun. Suhu proses yang tinggi serta waktu proses yang lama dapat merusak karotenoid yang merupakan pigmen alami minyak sawit (Ketaren 2005).
Pengadukan dilakukan dengan menggunakan agitator. Agitator dilengkapi dengan lengan penyapu yang masing-masing terdiri dari paddle yang berfungsi untuk mendorong cairan ke arah atas selama pengadukan. Agitator biasanya bekerja pada laju maksimum 30-35 rpm dan minimum 8-10 rpm. Pemecahan emulsi dapat terjadi pada suhu sekitar 60oC dimana sabun terpisah dari minyak jernih membentuk suatu flokulan kecil (O`Brien 2004).
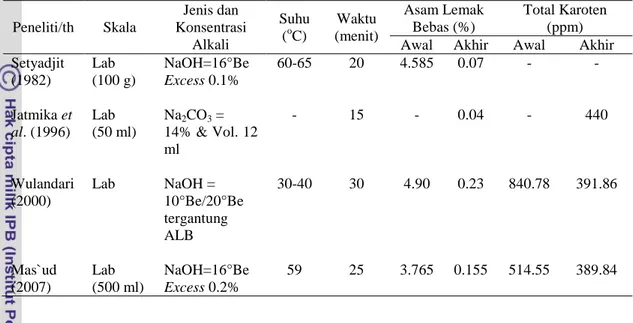
Beberapa penelitian tentang deasidifikasi minyak sawit secara kimia dapat dilihat pada Tabel 3.
Tabel 3 Hasil-hasil penelitian deasidifikasi minyak sawit
Peneliti/th Skala Jenis dan Konsentrasi Alkali Suhu (oC) Waktu (menit) Asam Lemak Bebas (%) Total Karoten (ppm)
Awal Akhir Awal Akhir
Setyadjit (1982) Jatmika et al. (1996) Wulandari (2000) Mas`ud (2007) Lab (100 g) Lab (50 ml) Lab Lab (500 ml) NaOH=16°Be Excess 0.1% Na2CO3 = 14% & Vol. 12 ml NaOH = 10°Be/20°Be tergantung ALB NaOH=16°Be Excess 0.2% 60-65 - 30-40 59 20 15 30 25 4.585 - 4.90 3.765 0.07 0.04 0.23 0.155 - - 840.78 514.55 - 440 391.86 389.84
Ooi et al. (1996) melakukan proses deasidifikasi dan deodorisasi minyak sawit merah menggunakan distilasi molukuler pada suhu antara 130oC dan 170oC serta tekanan antara 20.10-3 dan 60.10-3 mmHg. Hasil penelitian menunjukkan kondisi yang sesuai untuk refining minyak sawit merah tanpa merusak karoten adalah 150oC -170oC dan tekanan vakum 20-25.10-3 mmHg. Karoten yang dapat dipertahankan sedikitnya 80 persen dengan asam lemak bebas yang berkurang dari 2.4 persen menjadi 0.04 persen. Adapun karakteristik CPO yang digunakan dan minyak sawit merah yang dihasilkan dapat dilihat pada Tabel 4.
Tabel 4 Karakteristik CPO dan minyak sawit merah menggunakan distilasi molekuler*)
CPO Minyak sawit merah Asam lemak bebas (%)
Bilangan peroksida (meq/kg) Karoten (ppm) Vitamin E (ppm) Besi (ppm) Fosfor (ppm) 2.40 0.80 660 923 3.3 7.8 0.04 0.20 531 642 0.3 2.7 *) Ooi et al. (1996)
Unsur primer dalam lemak dan minyak kasar adalah trigliserida, tetapi lemak dan minyak kasar juga mengandung berbagai komponen minor, yang secara signifikan juga mempengaruhi sifat fisik dan kimia lemak dan minyak, khususnya adalah asam lemak bebas (O`Brien 2004).
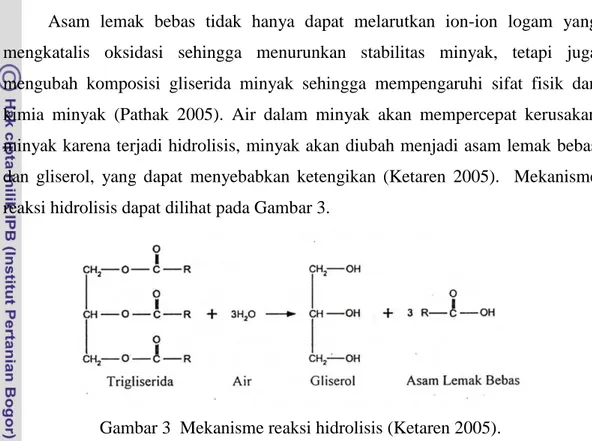
Asam lemak bebas tidak hanya dapat melarutkan ion-ion logam yang mengkatalis oksidasi sehingga menurunkan stabilitas minyak, tetapi juga mengubah komposisi gliserida minyak sehingga mempengaruhi sifat fisik dan kimia minyak (Pathak 2005). Air dalam minyak akan mempercepat kerusakan minyak karena terjadi hidrolisis, minyak akan diubah menjadi asam lemak bebas dan gliserol, yang dapat menyebabkan ketengikan (Ketaren 2005). Mekanisme reaksi hidrolisis dapat dilihat pada Gambar 3.
Gambar 3 Mekanisme reaksi hidrolisis (Ketaren 2005).
Hidrolisis terjadi pada ikatan ester dari molekul gliserida membentuk asam lemak bebas dan gliserol. Hidrolisis disebabkan oleh enzim lipolitik (lipase) yang terdapat secara alami dalam buah sawit dan oleh mikroba lipolitik. Lipase mulai aktif pada saat struktur seluler buah menjadi pecah atau rusak, utamanya selama pascapanen sawit, sedangkan hidrolisis oleh mikroba disebabkan oleh fungi yang menghasilkan enzim lipase (Ketaren 2005).
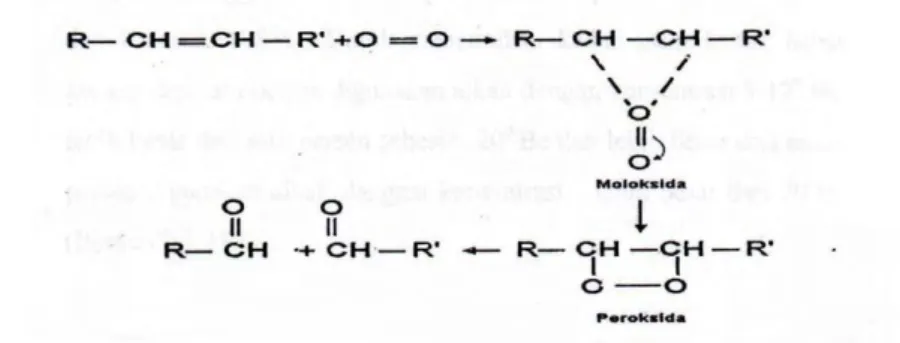
Kenaikan asam lemak bebas mempermudah proses oksidasi berantai dan pembentukan senyawa peroksida, aldehida, keton dan polimer. Oksidasi berantai menyebabkan penguraian konstituen aroma, flavor dan vitamin. Pembentukan senyawa seperti peroksida, aldehida, dan keton menyebabkan bau tengik, pencoklatan minyak dan kemungkinan menimbulkan keracunan (Ketaren 2005). Mekanisme reaksi oksidasi dapat dilihat pada Gambar 4.
Gambar 4 Mekanisme reaksi oksidasi (Ketaren 2005).
Bleaching
Bleaching merupakan salah satu tahapan proses pemurnian minyak yang bertujuan untuk menghilangkan zat warna minyak khususnya peopitin/klorofil dan karotenoid dalam minyak dengan menggunakan bleaching earth atau bleaching clay (Taylor 2005). Bleaching clay dapat berinteraksi dengan konstituen non colored seperti sabun, asam lemak bebas, fosfolipid dan peroksida. Bleaching clay diperlukan untuk menghilangkan color bodies, peroksida dan aldehid serta sisa-sisa logam, sabun, dan fosfolipid pada tahap bleaching (Akoh dan Min 2002; Wei et al. 2004; Taylor 2005).
Bleaching dengan proses batch dilakukan pada tekanan atmosfer. Pada proses ini, minyak sawit yang dimurnikan ditambahkan bleaching clay (0.8-2%) dan dipanaskan sampai suhu 100-120oC dengan periode waktu 30-45 menit. Apabila proses telah selesai, minyak panas dan clay dipisahkan dengan filtrasi (Taylor 2005).
Deodorisasi
Deodorisasi merupakan proses untuk memisahkan rasa dan bau dari minyak. Prinsip dari proses deodorisasi yaitu destilasi minyak oleh uap dalam keadaan hampa udara. Pada suhu tinggi, komponen-komponen yang menimbulkan bau mudah diuapkan, kemudian melalui aliran uap komponen-komponen tersebut dipisahkan dari minyak. Komponen-komponen yang dapat menimbulkan rasa dan bau dari minyak antara lain asam lemak bebas, aldehida, keton dan hidrokarbon (Djatmiko dan Widjaja 1985). Deodorisasi dilakukan dengan cara menguapkan
komponen-komponen volatil. Proses ini dilakukan secara kontinyu pada suhu 245-265oC dalam keadaan vakum 1-2 mmHg (Siswanto 2000).
Sifat Fisiko-Kimia Minyak Sawit
Minyak sawit bentuknya semi padat pada suhu ruang (28oC) dengan titik leleh sekitar 32-40oC (Lin 2002), berwarna kuning jingga karena mengandung pigmen karotenoid, sebaliknya minyak inti sawit bersifat cair pada suhu kamar. Perbedaan sifat ini disebabkan oleh perbedaan jenis dan jumlah rantai asam lemak yang membentuk trigliserida dalam kedua minyak tersebut (Budiman 1987; Goh et al. 1987).
Minyak sawit seperti minyak dan lemak lainnya terbentuk oleh sebagian besar trigliserida dan beberapa nongliserida dalam jumlah yang kecil. Komposisi kimia ini menggambarkan karakteristik fisiko kimia minyak sawit (Basiron 2005).
Beberapa karakteristik komponen lemak dalam minyak sawit dapat dilihat pada Tabel 5. Tabel ini menunjukkan stearin sawit mempunyai titik cair yang tertinggi, berat jenis dan indeks refraksi tidak banyak berbeda, bilangan iod yang tertinggi ditemukan pada olein dan bilangan penyabunan tertinggi pada minyak inti sawit. Asam lemak dengan C6 dan C8 hanya terdapat minyak inti sawit (PORIM 1988).
Tabel 5 Sifat fisiko kimia komponen minyak sawit*)
Sifat
Jenis Minyak
sawit (CPO) Olein Stearin
Minyak inti sawit (PKO) Titik cair, oC 34.2 21.6 44.5 27.3 Berat jenis (50oC/air 25oC) 0.892 0.902 0.882 0.902 Indek refraksi (nD, 50oC) 1.455 1.459 1.477 1.451 Bilangan iod (Wijs) 53.3 58.0 21.6 17.8 Bilangan penyabunan
(mg KOH/g minyak) 195.7 198.0 193.0 245.0 Bahan tak tersabunkan, (%) 0.5 0.5 0.2 0.3 *)
PORIM (1988)
Warna minyak ditentukan oleh adanya pigmen karoten yang larut dalam minyak, sebab asam-asam lemak dan gliserida tidak berwarna. Bau dan flavor terdapat secara alami, bau khas minyak sawit ditimbulkan oleh persenyawaan
β-ionone. Bau juga terjadi akibat adanya asam-asam lemak berantai pendek akibat kerusakan minyak (Ketaren 2005).
Komposisi Minyak Sawit
Unsur utama dalam minyak sawit adalah trigliserida, yaitu molekul gliserol yang teresterifikasi dengan tiga asam lemak. Selama ekstraksi minyak dari mesokarp, trigliserida menarik komponen seluler larut minyak atau lemak lainnya (Sundram 2007).
Unsur-unsur minor yang terdapat dalam minyak sawit dapat dikelompokan menjadi dua kelompok. Kelompok pertama terdiri dari derivat asam lemak, seperti monogliserol (MG), digliserol (DG), asam lemak bebas, fosfatida, ester dan sterol. Kelompok kedua meliputi kelas yang secara kimia tidak berhubungan dengan asam lemak seperti hidrokarbon, alkohol alifatik, tokoferol, tokotrienol, pigmen dan sedikit logam-logam. Sebagian besar komponen minor ditemukan dalam fraksi yang tidak tersabunkan (unsaponifiable) pada minyak sawit adalah sterol, alkohol alifatik yang lebih tinggi, pigmen dan hidrokarbon (Sundram 2007).
Menurut Morad et al. (2006) fosfolipid nonhidrat dapat dihidrasi, biasanya dilakukan dengan asidulasi diikuti dengan netralisasi. Komponen utama dari fosfolipid adalah fosfatida yang dapat membentuk komplek dengan logam-logam yang dapat mengkatalis reaksi oksidasi. Fosfolipid berada dalam jumlah yang relatif kecil sekitar 5 – 130 ppm dalam minyak sawit dibandingkan minyak sayur lainnya.
Fraksinasi minyak sawit akan menghasilkan dua fraksi yang unik, yakni fraksi olein yang mempunyai bilangan iod tinggi dan titik leleh rendah dan fraksi stearin yang mempunyai bilangan iod lebih rendah dan titik leleh yang tinggi (Lin 2002). Menurut Gunstone (2005) minyak sawit dapat difraksinasi menghasilkan fraksi padat (palm stearin, 30-35%, titik leleh 48-50oC dan fraksi cair (palm olein, 65–70%, titik leleh 18–20oC).
Trigliserida minyak sawit
Basiron (2005) mengatakan bahwa trigliserida merupakan komponen utama dalam minyak sawit. Menurut Morad et al. (2006) komponen trigliserida dalam
minyak sawit kasar mencapai 95 persen. Rantai asam lemak yang terdapat pada trigliserida minyak sawit dapat bervariasi jumlah atom karbon dan strukturnya (adanya ikatan rangkap seperti ketidakjenuhan). Variasi struktur dan jumlah karbon pada rantai asam lemak menggambarkan sifat fisik dan kimia minyak sawit (Basiron 2005).
Terdapat 7 sampai 10 persen trigliserida jenuh, sebagian besar adalah tripalmitin. Trigliserida tidak jenuh terdiri dari 6 sampai 12 persen. Posisi Sn-2 mempunyai spesifisitas untuk asam lemak tidak jenuh. Untuk itu, lebih dari 85 persen asam lemak tidak jenuh berada dalam posisi Sn-2 pada molekul gliserol (Sundram 2007). Menurut Winarno (1999) trigliserida minyak sawit seperti trigliserida alami pada umumnya, mengandung asam lemak jenuh pada posisi 1 dan/atau 3 serta asam lemak tidak jenuh pada posisi 2, namun ada juga beberapa trigliserida yang ketiga asam lemak penyusunnya asam lemak jenuh. Perbedaan penempatan asam lemak dan jenis asam lemak pada molekul gliserol menghasilkan sejumlah perbedaan trigliserida. Trigliserida dalam minyak sawit mendefinisikan secara parsial sebagian besar karakteristik fisik minyak sawit seperti titik cair (melting point) dan sifat kristalisasi (Sundram 2007).
Basiron (2005) melaporkan terdapat empat jenis gliserida utama dalam minyak sawit, yaitu gliserida dengan tiga asam lemak jenuh (trisaturated, 10.2%), gliserida dengan dua asam lemak jenuh (disaturated, 48.0%), gliserida dengan satu asam lemak jenuh (monosaturated, 34.6%) dan gliserida dengan tiga asam lemak tidak jenuh (triunsaturated, 6.8%).
Komposisi minyak sawit di Indonesia rata-rata mengandung PPP : 10.5%, PPO: 8.6%, POP: 40.0%, POO : 34.0%, dan OOO : 6.6 % (Hamilton dan Han 1980). Asam palmitat bentuk bebas dan bentuk terikat sebagai monopalmitin, dipalmitin dan tripalmitin memiliki titik leleh yang relatif tinggi (diatas 60oC), sehingga pada suhu ruang senyawa tersebut berbentuk padat (Belitz dan Grosh 1999).
Asam lemak minyak sawit
Minyak sawit tersusun dari unsur-unsur C, H, dan O. Minyak sawit mengandung asam lemak dalam jumlah cukup banyak dan asam lemak tersebut
berikatan dengan gliserol membentuk trigliserida. Asam-asam lemak yang terdapat pada trigliserida, fosfolipid, dan glikolipid minyak sawit dapat berupa asam lemak jenuh atau asam lemak tidak jenuh atau keduanya (Winarno 1999). Sifat minyak sawit sangat dipengaruhi oleh panjang rantai karbon dan jumlah ikatan rangkapnya. Asam lemak tanpa ikatan rangkap disebut asam lemak jenuh, dengan satu ikatan rangkap disebut asam lemak tidak jenuh tunggal dan bila dua atau lebih ikatan rangkap disebut asam lemak tak jenuh majemuk (Mayes 2003).
Adapun kandungan minyak sawit dibandingkan minyak nabati lainnya serta komposisi asam-asam lemak yang terdapat dalam minyak sawit dapat dilihat pada Tabel 6 dan Tabel 7.
Tabel 6 Kandungan minyak sawit dibandingkan minyak nabati lainnya*) No. Komponen minyak Minyak sawit Minyak kelapa Minyak jagung Minyak kedelai 1. Karotenoid (ppm) 800 - - - 2. Vitamin E (ppm) - Tokoferol - Tokotrienol 642 530 11 25 782 - - - 3. Lemak (%) - Jenuh - Tidak jenuh 50 49 94 5.9 16 83 14 85 4. Fitosterol (ppm) 18 14 50 28 *)
De Witt dan Chong (1988)
Karotenoid
Karotenoid merupakan kelompok pigmen yang berwarna kuning, orange, merah orange, serta larut dalam minyak (lipida). Karotenoid terdapat dalam kloroplas (0.5%) bersama-sama dengan klorofil (9.3%), terutama pada bagian permukaan atas daun, dekat dengan dinding sel-sel palisade. Karena itu pada dedaunan hijau selain klorofil terdapat juga karotenoid (Winarno 1992).
Karotenoid adalah bentuk linier hidrokarbon C40 tetraterpenoid yang terdiri dari delapan unit C5 isopren dengan rantai poliene terkonjugasi sebagai chromophore yang menangkap cahaya yang menyebabkan sifat warna terang (Bonnie dan Choo 1999).
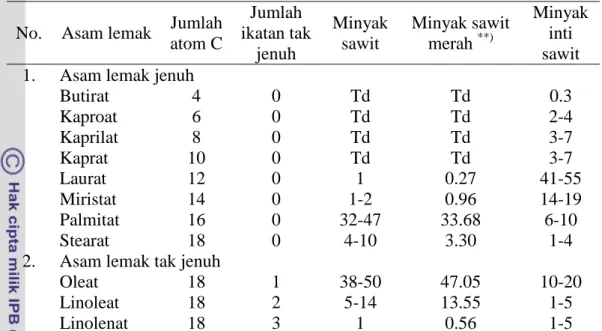
Tabel 7 Komposisi asam-asam lemak (%) yang terdapat dalam minyak sawit*)
No. Asam lemak Jumlah atom C Jumlah ikatan tak jenuh Minyak sawit Minyak sawit merah **) Minyak inti sawit 1. Asam lemak jenuh
Butirat 4 0 Td Td 0.3 Kaproat 6 0 Td Td 2-4 Kaprilat 8 0 Td Td 3-7 Kaprat 10 0 Td Td 3-7 Laurat 12 0 1 0.27 41-55 Miristat 14 0 1-2 0.96 14-19 Palmitat 16 0 32-47 33.68 6-10 Stearat 18 0 4-10 3.30 1-4
2. Asam lemak tak jenuh
Oleat 18 1 38-50 47.05 10-20
Linoleat 18 2 5-14 13.55 1-5
Linolenat 18 3 1 0.56 1-5
*)
Palm Oil Research Institute Malaysia (PORIM) (1988) - : tidak terdeteksi
**)
Kritchevsky et al. (2001)
Karotenoid merupakan senyawa yang tersebar luas di dalam tanaman dan buah-buahan. Karotenoid tidak selalu berdampingan dengan klorofil, tetapi sebaliknya klorofil selalu disertai dengan karotenoid. Disamping pada daun dan batang tanaman, karotenoid juga terdapat pada bagian-bagian lain tanaman misalnya pada umbi dan buah. Pada umumnya umbi-umbian mengandung sedikit karotenoid, kecuali ubi jalar atau wortel (Kumalaningsih 2006). Kandungan karotenoid beberapa jenis bahan pangan dapat dilihat pada Tabel 8.
Tabel 8 Kandungan karotenoid berbagai jenis bahan pangan*) Bahan Pangan μg RE/g
Jeruk Pisang Tomat Wortel
Minyak Merah Minyak Sawit Kasar
21 50 130 400 5000 6700 *) Hariyadi (2006)
β-karoten merupakan molekul simetri, yaitu separuh bagian kiri merupakan bayangan cermin dari kanannya. β-karoten mempunyai 40 atom karbon, yang
terdiri dari 8 unit isopren dan 11 ikatan rangkap, serta mempunyai 2 cincin β-ionon yang terletak masing-masing satu cincin pada ujung molekulnya. β-karoten mempunyai aktivitas provitamin A paling tinggi. Struktur isoprena dan β-karoten dapat dilihat pada Gambar 5 dan Gambar 6.
Gambar 5 Struktur isoprena (Winarno 1992).
Gambar 6 Struktur β-karoten (Gross 1991).
β-karoten mempunyai sifat dapat membentuk isomer geometri. Isomer cis- β-karoten mempunyai aktivitas provitamin A yang lebih rendah bila dibandingkan bentuk all trans-nya. Perubahan geometri β-karoten dapat disebabkan oleh cahaya, proses oksidasi, atau autooksidasi. Oksidasi akan membuka cincin β-ionon β-karoten dan menyebabkan kerusakan aktifitas β-karoten (Bauernfeind dan Klaul 1981).
Karotenoid minyak sawit. CPO adalah salah satu sumber alami yang
paling kaya akan karotenoid. Konsentrasi karotenoid bervariasi dari 400-3.500 ppm tergantung spesies dari kelapa sawit. CPO dari jenis Tenera mengandung 500-700 ppm (Ping dan Lian 2005).
Dibandingkan dengan sumber karoten lainnya, minyak sawit mempunyai retinol ekivalen 15 kali lebih besar daripada wortel dan 300 kali lebih besar daripada tomat (Tan 1987; Sundram 2007). Menurut Winarno (1999) karotenoid dalam minyak sawit terutama mencakup α-karoten dan β- karoten dan sejumlah kecil γ-karoten, likopen dan xantofil. Ooi et al. (1996) mengatakan α-karoten dan β- karoten jumlahnya mencapai 90 persen dari total karotenoid yang ada dalam minyak sawit. Komposisi karotenoid minyak sawit dapat dilihat pada Tabel 9.
CH2 = C – C = CH2 CH3
Tabel 9 Komposisi karotenoid minyak sawit*)
No. Komponen Jumlah (%)
1 α-karoten 35.16 2 β- karoten 56.02 3 γ-karoten 0.33 4 δ-karoten 0.83 5 δ-karoten 0.69 6 cis- α-karoten 2.49 7 cis- β- karoten 0.68 8 Phytoene 1.27 9 Lycopen 1.30 *) Basiron (2005)
Manfaat karotenoid. Karotenoid mengandung ikatan rangkap dua yang
menyebabkan karotenoid peka terhadap oksidasi. Kepekaannya terhadap oksidasi membuat karotenoid digunakan sebagai antioksidan yang kekuatannya menyamai vitamin C dan tokoferol (Muchtadi 1992). Oleh karena itu, karotenoid mempunyai peran essensial dalam melindungi sel dan organisme terhadap peroksidasi lipida. Sistem poliene yang terkonjugasi sangat efisien bagi molekul oksida tunggal dan jenis radikal bebas pada fase lipida dan telah dikaitkan dengan penurunan resiko kanker, atherosklerosis dan katarak (Bonnie dan Choo 1999; Kritchevsky et al. 2001).
β-karoten mempunyai potensi biologis paling besar. β-karoten berperan sebagai antioksidan dan anti-karsinogen karena kemampuannya untuk menangkap singlet oxygen (Manorama et al. 1999). Ziegler et al. (1996) melaporkan hasil studi epidemologis yang menunjukkan kecendrungan rendahnya resiko penyakit kanker dengan tingginya konsumsi makanan yang mengandung vitamin A dan β-karoten. Lebih lanjut dikatakan bahwa konsentrasi β-karoten plasma yang tinggi dapat menurunkan resiko penyakit kanker paru-paru dan penyakit jantung.
Menurut Kumalaningsih (2006), tubuh akan mengonversi β-karoten menjadi vitamin A dalam jumlah secukupnya saja. Selebihnya akan tetap tersimpan sebagai β-karoten. Sifat inilah yang menyebabkan β-karoten berperan sebagai sumber vitamin A yang aman. Jadi, tidak seperti suplemen vitamin A yang bisa menyebabkan keracunan, jika diberikan secara berlebihan. Aktivitas provitamin A berbagai jenis kelompok karoten terdapat pada Tabel 10.
Tabel 10 Beberapa jenis karotenoid dengan aktivitas provitamin A-nya*)
No. Jenis Karotenoid Aktivitas provitamin A (%)
1 2 3 4 5 6 7 All-trans-β-karoten All-trans-α- karoten All-trans-kriptoxantin γ-karoten β-Zeakaroten β-karoten-5,6-epoksi β-karoten-5,8-epoksi (mutakrom) 100 53 57 42-50 20-40 21 50 *) Gross (1991)
Minyak sawit merah dapat diaplikasikan pada beberapa area seperti pewarna alami, sebagai komponen atau ingridien dalam industri pangan sebagai pangan fungsional atau sebagai sumber provitamin A, substrat untuk neutrasetikal, pengganti lemak hewani, dan salad oil (Unnithan dan Foo 2001).
Manorama et al. (1993) diacu dalam Ping dan May (2007) mengatakan bahwa minyak sawit merah (red palm oil) lebih efektif sebagai pencegahan karsinogenesis dalam tikus dibandingkan dengan refined bleached deodorized palm olein (RBDPOo).
Minyak sawit merah kaya β-karoten yang digunakan dalam studi intervensi dietary untuk meningkatkan kemungkinan peranannya dalam pencegahan defisiensi vitamin A. Di India, anak-anak 5-10 tahun dengan keratomalacia diberikan 2 kali sehari emulsi yang mengandung minyak sawit merah. Setiap dosis mengandung 0.6 ml minyak sawit merah dan terapi dilanjutkan selama 15 hari. Perlakuan minyak sawit merah menunjukkan hasil yang baik dibandingkan hasil yang diperoleh dari perlakuan kelompok pasien lain dengan menggunakan minyak hati ikan yang mengandung dosis vitamin A yang serupa. Berdasarkan hasil yang diperoleh telah direkomendasikan bahwa negara berkembang seharusnya tidak ada keraguan dalam membuat strategi untuk meningkatkan penggunaan minyak sawit merah dalam menghadapi defisiensi vitamin A (Sundram 2007).
Jacques et al. (1991) melaporkan hasil penelitiannya tentang orang yang mempunyai konsentrasi karoten plasma yang tinggi yaitu lebih dari 3.3 μmol/L mempunyai prevalensi katarak lebih rendah 20 persen dibandingkan dengan orang yang memiliki persentase karoten plasma kurang dari 1.7 μmol/L.
Salah satu masalah gizi utama yang diderita oleh anak balita Indonesia adalah kekurangan Vitamin A (KVA). Untuk penanggulangan KVA tersebut, setiap tahunnya, dua kali setahun kepada anak balita diberikan kapsul vitamin A dosis tinggi (200.000 IU). Bila jumlah anak balita diperkirakan sekitar 7 persen dari jumlah penduduk, maka berarti setiap tahunnya dibutuhkan vitamin A sebesar kurang lebih 7% x 220 juta x 200.000 IU = 6.2 x 1012 IU (6,2 triliun IU) = 3700 kg β-karoten (1 IU vitamin A = 0.6 μg β-karoten). Pada awal penerapan program, kapsul tersebut disuplai dari UNICEF, namun sejak tahun 1997 bantuan tersebut dihentikan (Direktorat Jendral Pengawasan Obat dan Makanan 1998). Oleh karena itu untuk memenuhi kebutuhan vitamin A, dirasa perlu dilakukan upaya diversifikasi produk olahan yang diharapkan dapat membantu memenuhi kebutuhan ini.
Stabilitas β-karoten. Secara umum karotenoid mempunyai sifat fisik dan
kimia sebagai berikut : larut dalam lemak, larut dalam kloroform, karbon disulfida, petroleum eter, tidak larut dalam etanol dan metanol dingin, sensitif terhadap oksidasi, autooksidasi, cahaya, dan mempunyai spektrum serapan yang spesifik (Meyer 1982). Menurut Gross (1991) saponifikasi pada proses pemurnian minyak tidak mempengaruhi karotenoid yang umumnya stabil terhadap alkali.
β-karoten sebagaimana karotenoid di alam, sebagian besar berupa hidrokarbon yang larut dalam lemak, serta berikatan dengan senyawa yang strukturnya menyerupai lemak. Adanya struktur ikatan rangkap pada molekul β-karoten (11 ikatan rangkap pada 1 molekul β-β-karoten) menyebabkan bahan ini mudah teroksidasi ketika terkena udara. Menurut Sundram (2007) karoten sensitif terhadap oksigen dan cahaya. Oksidasi karoten dipicu oleh hidroperoksida yang dihasilkan dari oksidasi lipid, mengakibatkan diskolorisasi dan bleaching.
Oksidasi karotenoid akan lebih cepat dengan adanya sinar dan katalis logam, khususnya tembaga, besi dan mangaan. Oksidasi dapat terjadi secara acak pada rantai karbon yang mengandung ikatan ganda (Bonnie dan Choo 1999). Pengaruh suhu terhadap oksidasi pada karotenoid dikemukakan oleh Worker (1957) diacu dalam Muchtadi (1992) yaitu bahwa karotenoid belum mengalami kerusakan karena pemanasan pada suhu 60oC, sedangkan Gross (1991) mengatakan bahwa laju oksidasi β-karoten meningkat dengan peningkatan suhu.
Menurut Alyas et al. (2006), peningkatan waktu pemanasan dari 30 menit sampai 120 menit mengakibatkan reduksi β-karoten sebesar 3 persen pada suhu 50oC dan 6 persen pada suhu 100oC dalam red palm olein (RPOo). Pemanasan RPOo pada suhu yang sangat tinggi 200oC selama 30 menit mengakibatkan kehilangan β-karoten hanya 15 persen. Namun, peningkatan waktu pada suhu 200oC menyebabkan reduksi sebesar 59 persen kandungan β-karoten. Penurunan yang signifikan dari β-karoten terjadi pada suhu yang lebih tinggi untuk waktu pemanasan yang lebih lama. Hal ini sesuai dengan penemuan Lin dan Chen (2005) yang mengatakan bahwa kecendrungan penurunan β-karoten seiring dengan peningkatan suhu penyimpanan pada jus tomat yang di simpan pada suhu yang berbeda. Menurut Rianto (1995) penurunan karoten total minyak sawit
merah mencapai 97.94 persen pada suhu 180oC selama 120 menit.
Mac Dougall (2002) menyebutkan bahwa warna kuning, orange, merah karotenoid adalah terkait dengan sistem konjugasi ikatan rangkap karbon-karbon. Semua struktur trans dapat diubah menjadi isomer cis. Isomerisasi cis-trans menghasilkan perubahan warna produk yang ditunjukkan oleh sifat spektral karotenoid cis yang berbeda dengan karotenoid trans.
Rantai poliene yang berperan dalam penyerapan cahaya dan ikatan rangkap terkonjugasinya yang berperan sebagai antioksidan, disisi lain justru membuat karotenoid menjadi tidak stabil. Strukturnya mudah rusak dengan adanya serangan radikal bebas seperti molekul oksigen tunggal dan senyawa lain yang reaktif. Panas, sinar dan asam memacu isomerisasi bentuk trans karotenoid ke bentuk cis. Cahaya, enzim, dan prooksidan logam disisi lain memacu oksidasi (Bonnie dan Choo 1999).
Perubahan struktur β-karoten khususnya maupun karotenoid pada umumnya selama pengolahan dan penyimpanan dapat terjadi melalui beragam jalur, tergantung pada kondisi proses reaksinya. Jalur degradasi yang umum adalah isomerisasi, oksidasi, dan fragmentasi karotenoid (Bonnie dan Choo 1999).
Menurut Bonnie dan Choo (1999), isomerisasi, oksidasi dan kerusakan molekul karotenoid terjadi sebagai akibat degradasi termal. Dua jenis produk degradasi thermal yang terbentuk adalah volatil dan non-volatil. Fraksi volatil
terdiri dari molekul dengan berat molekul yang rendah yang mudah menguap. Fraksi non-volatil adalah fraksi residual setelah penguapan fraksi volatil.
Eskin (1979) menyebutkan pula bahwa oksidasi juga dapat menyebabkan kerusakan karotenoid. Oksidasi dapat dikelompokan menjadi 2 yaitu oksidasi enzimatis dan oksidasi non enzimatis. Oksidasi enzimatis dikatalis oleh enzim lipoksigenase. Hasil proses oksidasi ini menyebabkan penyimpangan rasa.
Provitamin A (β-karoten) lebih stabil terhadap cahaya dan oksidasi dibandingkan vitamin A. Hal ini disebabkan oleh lokasi karotenoid dalam jaringan tanaman. Namun, perlakuan panas yang merusak jaringan jika dipaparkan dengan oksigen, cahaya, dan asam dapat mengakibatkan kerusakan provitamin A (β-karoten). Lebih lanjut, panas dan cahaya dilaporkan menyebabkan isomerisasi vitamin A dan karotenoid. Faktor yang tidak menguntungkan ini dapat menyebabkan isomerisasi bentuk all trans ke bentuk cis yang secara biologis kurang baik (Gayathri et al. 2003).
Vitamin E minyak sawit. Vitamin E terjadi secara alami dan dengan luas
didistribusikan di alam. Minyak sawit mengandung 600-1000 ppm vitamin E. Komposisi vitamin E pada minyak sawit dikarakterisasi oleh adanya α−tokoferol (20%), α−tokotrienol (22%), γ−tokotrienol (46%) and δ−tokotrienol (12%). Keunikan minyak sawit dibandingkan vegetable oil lainnya adalah kandungan tokotrienol yang tinggi (Puah et al. 2007).
Puah et al. (2007) mengatakan bahwa hanya pada suhu tinggi yaitu diatas 260°C, vitamin E mengalami dekomposisi termal. Komposisi vitamin E (%) selama pemurnian minyak sawit secara fisik dapat dilihat pada Tabel 11.
Tabel 11 Komposisi vitamin E (%) selama pemurnian minyak sawit secara fisik*)
Sampel Komposisi (%)
α-T α-T3 γ-T3 δ-T3 α−tokomonoenol
Crude palm oil 17 24 49 7 3
Degummed palm oil 15 23 52 7 3
Bleached palm oil 14 22 53 7 3
Deodorized palm oil 15 24 52 6 3
*)
Puah et al. (2007)
Winarno (1999) mengatakan bahwa karotenoid dan tokoferol dapat berfungsi sebagai antioksidan, maka keduanya berperan penting dalam menjaga stabilitas minyak sawit dari proses oksidasi yang mengakibatkan ketengikan.
Peningkatan Skala
Peningkatan skala adalah suatu studi yang mengolah dan menggunakan data hasil percobaan laboratorium atau percobaan skala pilot plant untuk merancang proses alat/mesin yang akan digunakan dengan skala pabrik (Aiba 1973).
Menurut Smith (1990) percobaan pada peningkatan skala merupakan percobaan pada laboratorium ukuran besar yang dirancang untuk bersifat luwes bagi penggunaan peralatan dan penyesuaian operasi proses.
Peningkatan skala (scale up) merupakan salah satu target penelitian yang mempunyai arah industri, selain itu juga merupakan kunci penghubung antar lab dengan industri. Peningkatan skala pada proses deasidifikasi minyak sawit merah adalah suatu tindakan untuk membuat hasil proses yang identik pada laju tingkat produksi yang lebih besar dari perencanaan yang sebelumnya telah teruji baik. Dalam hal ini tersirat peningkatan produksi akan dilakukan dengan peralatan yang secara fisik lebih besar dari pada yang digunakan sebelumnya (Valentas et al. 1991).
Penentuan faktor fisik untuk skala yang lebih besar ditentukan berdasarkan metode kesamaan geometri. Menurut Valentas et al. (1991), dua benda dinyatakan mirip secara geometri jika setiap titik pada benda yang satu terwakili keberadaanya pada benda yang lain dan sebaliknya. Kemiripan atau kesamaan geometri ini juga ditunjukkan bahwa jika benda tersebut mempunyai kemiripan geometri maka rasio dua garis (atau kedudukan) dalam benda pertama akan sama dengan rasio garis (kedudukan) yang terwakili pada benda kedua dan sebaliknya, prinsip kemiripan ini pada umumnya merupakan landasan peningkatan skala yang paling banyak digunakan (Wirakartakusumah et al. 1991).
Kriteria peningkatan skala yang utama adalah parameter atau sekumpulan parameter proses yang bersifat bebas, tidak terpengaruh oleh ukuran (skala) proses, yang pada umumnya melibatkan lebih dari satu skala proses. Kriteria utama melibatkan parameter proses dan hasil proses secara kuantitas, sedangkan
kriteria tambahan adalah adanya perubahan secara fisik dan mekanik yang berkaitan dengan perubahan skala, misalnya pengaruh skala terhadap transfer panas atau terhadap tenaga. Sistem secara fisik dan obyek material pada dasarnya dicirikan oleh 3 kualitas, yaitu ukuran, bentuk dan komposisi. Kemiripan yang penting dalam peningkatan skala proses dan peralatan pangan adalah : kemiripan geometri, mekanika, termal dan kimiawi (Valentas et al. 1991).
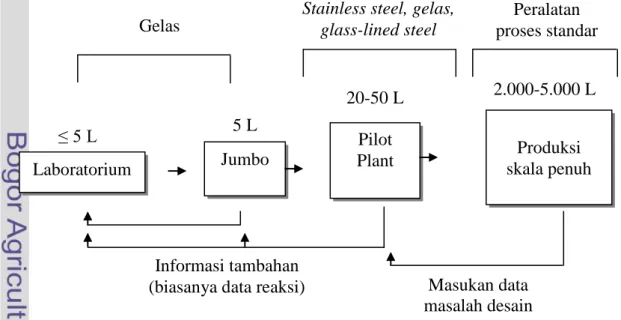
Peningkatan skala dilalui dengan 3 tahap yaitu : (1) skala laboratorium, (2) skala pilot plant, (3) skala industri. Skala pilot plant merupakan skala untuk mendapatkan operasi optimal dan kontrol yang tepat sebelum menuju ke produksi secara komersial atau industrialisasi (Valentas et al. 1991). Menurut Lowenstein (1985), peningkatan skala dijalankan melalui 4 tahapan yaitu : (1) skala laboratorium, (2) skala jumbo, (3) skala pilot plant, (4) skala produksi penuh. Tahapan peningkatan skala dapat dilihat pada Gambar 7.
Pada dasarnya apapun yang terdapat dalam proses dapat dijadikan parameter ataupun hasil proses, tergantung jenis dan tujuan proses. Dalam proses peningkatan skala ini memang diusahakan untuk menghindari parameter-parameter dan hasil proses yang tidak terukur secara efektif, namun sebenarnya tidak ada alasan untuk menyingkirkan parameter hasil/hasil subyektif, kecuali jika penilaiannya tidak dijamin ketepatannya (Valentas et al. 1991).
Gambar 7 Tahapan peningkatan skala (Lowenstein 1985).
2.000-5.000 L
Laboratorium Jumbo
Pilot
Plant skala penuh Produksi Gelas
Stainless steel, gelas, glass-lined steel Peralatan proses standar 5 L 20-50 L ≤ 5 L Informasi tambahan
(biasanya data reaksi) Masukan data masalah desain