PENGARUH VARIASI RASIO MOL SIKLOHEKSANON-BENZALDEHIDA PADA SINTESIS
BENZILIDINSIKLOHEKSANON
SKRIPSI
Diajukan kepada
Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta Guna
Memperoleh Gelar Sarjana Sains Kimia
OLEH:
NUR RAHMA YULIYANI 1230714120
PROGRAM STUDI KIMIA JURUSAN PENDIDIKAN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI YOGYAKARTA
HALAMAN PERNYATAAN
Yang bertanda tangan di bawah ini saya:
Nama : Nur Rahma Yuliyani
NIM : 12307141020
Program Studi : Kimia
Fakultas : Matematika dan Ilmu Pengetahuan Alam Universitas
Negeri Yogyakarta
Judul Penelitian : Pengaruh Variasi Rasio Mol Sikloheksanon-Benzaldehida
pada Sintesis Benzilidinsikloheksanon
Dengan ini menyatakan bahwa skripsi ini adalah karya saya sendiri. Tidak
terdapat pendapat atau karya yang ditulis maupun diterbitkan oleh orang lain,
kecuali bagian acuan atau kutipan yang telah mengikuti prosedur penulisan karya
ilmiah yang benar.
Yogyakarta, Juni 2016
Yang menyatakan,
Nur Rahma Yuliyani
MOTTO
Jika kesempatan tidak pernah datang, maka buatlah!
Tetaplah merasa bodoh agar kita belajar. Tetaplah merasa lapar agar kita
berusaha.
Waktu itu bagaikan pedang, jika kamu tidak memanfaatkannya untuk memotong
maka ia akan memotongmu–H.R.
Muslim-Ada masa lalu, masa sekarang dan masa depan. Ketiganya adalah perjalanan yang
harus dilalui dengan penuh kesabaran–Sura
Dananjaya-Jangan tunggu hingga besok, apa yang bisa kamu lakukan hari ini lakukanlah!
Ketika engkau bersedih, Tuhan sedang memelukmu erat meski kau tak pernah
merasakannya.
Bahagia secukupnya, sedih seperlunya, mencintai sewajarnya, membenci
sewajarnya, tetapi bersyukur sebanyak-banyaknya.
Hidup adalah soal keberanian menghadapi yang tanda tanya. Tanpa kita bisa
Gie-HALAMAN PESEMBAHAN
Saya persembahkan karya ini untuk:
1. Kedua orangtua, Bapak Purwanto dan Ibu Sri Andayani yang telah
membesarkanku hingga kini dan selalu memberikan dukungan, serta doanya.
2. Adik-adikku (Rahmi, Ningrum, dan Azzah) yang selalu mewarnai hari-hariku
dan semoga kita dapat menjadi anak-anak sholehah yang membanggakan
orang tua.
3. Nanda Abdi Wiguna yang selalu memberikan masukan, semangat dan
dukungan hingga menyelesaikan skripsi ini. Terima kasih atas waktu yang
selalu diluangkan selama ini dan segala hal baru yang diberikan.
4. Meita dan Rahma Dewi yang selalu mendengarkan keluh kesah dan
memberikan masukan selama ini.
5. Mareta dan Mila yang selalu memberikan nasehat dan dukungan, serta
semangat. Terima kasih telah menjadi sahabatku selama 6 tahun ini dan selalu
mendengarkan keluh kesahku.
6. Eti, Ellen, Leni, Rika, Winarni, Hamida, Karyanto, dan Yoga yang telah
mewarnai hari-hariku di kampus. Terima kasih telah mengenalkanku dengan
hal-hal baru yang gokil selama ini.
7. Ibu Dr. Sri Handayani yang telah banyak membantu dalam berlangsungnya
penelitian ini dan masukan yang diberikan, serta Erika, Rani, dan Winarni
yang telah membantu dalam penelitian.
8. Teman-teman Kimia (B) 2012, terima kasih atas kebersamaanya selama
masa-masa kuliah.
9. Seluruh keluarga besar yang selalu memberikan dukungan dan semangat,
KATA PENGANTAR
Puji syukur senantiasa penulis panjatkan ke hadirat Allah SWT yang telah
memberikan karunia, taufik, dan hidayah-Nya. Dengan anugerah yang telah
diberikan, penulis dapat menyelesaikan skripsi dengan judul “Pengaruh Variasi
Rasio Mol Sikloheksanon-Benzaldehida pada Sintesis Benzilidinsikloheksanon”.
Penulisan skripsi ini merupakan syarat untuk mendapatkan gelar Sarjana Sains
Kimia.
Penulisan skripsi ini dapat berjalan lancar atas bimbingan, arahan, dan
bantuan dari berbagai pihak. Pada kesempatan ini, penulis mengucapkan terima
kasih kepada:
1. Bapak Prof. Dr. Rochmat Wahab, M.Pd, M.A selaku Rektor Universitas
Negeri Yogyakarta.
2. Bapak Dr. Hartono selaku Dekan Fakultas Matematika dan Ilmu Pengetahuan
Alam Universitas Negeri Yogyakarta.
3. Bapak Jaslin Ikhsan, Ph.D selaku Ketua Jurusan Pendidikan Kimia dan Ketua
program Studi Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Negeri Yogyakarta.
4. Ibu Dr. Sri Handayani selaku Dosen Pembimbing yang telah membantu dan
membimbing dengan penuh kesabaran.
5. Ibu C. Budimarwanti, M.Si selaku Dosen Penguji Utama, Bapak Karim
Theresih, SU selaku Dosen Penguji Pendamping dan Ibu Dr. Das Salirawati,
6. Seluruh Dosen, staf laboratorium kimia, dan karyawan Prodi Kimia, terima
kasih atas bimbingan dan bantuannya selama ini.
7. Kedua orangtua, Bapak Purwanto dan Ibu Sri Andayani, serta adik saya
Rahmi, Ningrum, dan Azzah terima kasih atas doa, dukungan dan kasih
sayangnya.
8. Teman-teman Prodi Kimia angkatan 2012 yang selama ini memberikan
dorongan dan semangat.
9. Semua pihak yang telah membantu penelitian dan penyusunan laporan Tugas
Akhir Skripsi ini.
Penulis menyadari bahwa selama pelaksanaan dan penyusunan laporan ini
masih terdapat kekurangan. Kritik dan saran membangun dari semua pihak sangat
diharapkan. Penulis berharap penelitian ini dapat bermanfaat bagi pembaca.
Yogyakarta, Juni 2016
DAFTAR ISI A. Latar Belakang Masalah ... 1
B. Identifikasi Masalah ... 4
C. Pembatasan Masalah ... 5
D. Rumusan Masalah ... 5
E. Tujuan Penelitian ... 5
F. Manfaat Penelitian ... 6
BAB II KAJIAN PUSTAKA A. Deskripsi Teori 1. Benzilidinsikloheksanon ... 7
2. Benzaldehida ... 7
3. Sikloheksanon ... 8
4. Natrium Hidroksida ... 9
5. Kondensasi Aldol Silang ... 10
7. Spektroskopi IR ... 15
8. Spektroskopi1H-NMR ... 17
B. Penelitian yang Relevan ... 19
C. Kerangka Berfikir ... 21
BAB III METODE PENELITIAN A. Subjek dan Objek Penelitian ... 23
1. Subjek Penelitian ... 23
2. Objek Penelitian ... 23
B. Variabel Penelitian ... 23
C. Instrumen Penelitian ... 23
1. Alat Penelitian ... 23
2. Bahan Penelitian ... 24
D. Prosedur Penelitian ... 25
1. Sintesis Benzilidinsikloheksanon ... 25
2. Rekristalisasi ... 25
3. Karakterisasi Senyawa Hasil Sintesis ... 25
E. Teknik Analisis ... 26
BAB IV HASIL DAN PEMBAHASAN A. Hasil Penelitian ... 27
1. Hasil Pengamatan Pengaruh Variasi Rasio Mol Sikloheksanon-Bnezaldehida pada Sintesis Benzilidinsikloheksanon ... 27
2. Hasil Identifikasi Produk Sintesis menggunakan KLT dan KLT Scanner... 28
3. Hasil Identifikasi Produk Sintesis menggunakan Spektroskopi IR ... 32
4. Hasil Identifikasi Produk Sintesis menggunakan Spektroskopi1 H-NMR ... 33
B. Pembahasan ... 34
1. Identifikasi dan Karakterisasi Produk Sintesis Benzilidinsiklohek-sanon ... 34
Mengguna-kan KLT dan KLTScanner... 34
Identifikasi Produk Sintesis Benzilidinsikloheksanon Mengguna-kan Spektroskopi IR ... 35
Identifikasi Produk Sintesis Benzilidinsikloheksanon Mengguna-kan Spektroskopi1H-NMR ... 36
2. Mekanisme Reaksi Sintesis Benzilidinsikloheksanon ... 40
3. Mekanisme Pembentukan Dibenzilidinsikloheksanon ... 42
4. Pengaruh Variasi Rasio Mol Sikloheksanon-Benzaldehida pada Sintesis Benzilidinsikloheksanon ... 43
BAB V PENUTUP A. Kesimpulan ... 46
B. Saran ... 46
DAFTAR PUSTAKA ... 47
DAFTAR GAMBAR
Gambar 1. Struktur benzilidinsikloheksanon ... 7
Gambar 2. Struktur benzaldehida ... 8
Gambar 3. Struktur sikloheksanon ... 9
Gambar 4. Mekanisme reaksi pembentukan benzalaseton ... 12
Gambar 5. Mekanisme rekasi pembentukan dibenzalaseton ... 13
Gambar 6. Produk hasil sintesis ... 27
Gambar 7. Kromatrogram KLT hasil sintesis dengan eluen kloroform:n-heksana (1:2) ... 28
Gambar 8. Hasil KLTscanner ... 28
Gambar 9. Hasil KLTscannersintesis dengan rasio mol sikloheksanon : benzaldehida (1 : 1) selama 4 jam, eluen kloroform : n-heksana (1 : 2) ... 29
Gambar 10. Hasil KLTscannersintesis dengan rasio mol sikloheksanon: benzaldehida (2 : 1) selama 4 jam, eluen kloroform : n-heksana (1 : 2) ... 29
Gambar 11. Hasil KLTscannersintesis dengan rasio mol sikloheksanon: benzaldehida (4 : 1) selama 4 jam, eluen kloroform : n-heksana (1 : 2) ... 30
Gambar 12. Hasil KLTscannersintesis dengan rasio mol sikloheksanon: benzaldehida (6 : 1) selama 4 jam, eluen kloroform : n-heksana (1 : 2) ... 30
Gambar 13. Hasil KLTscannersintesis dengan rasio mol sikloheksanon: benzaldehida (8 : 1) selama 4 jam, eluen kloroform : n-heksana (1 : 2) ... 31
Gambar 14. Hasil KLTscannersenyawa standar dibenzilidinsikloheksanon, eluen kloroform : n-heksana (1 : 2) ... 31
Gambar 15. Spektra IR hasil sintesis ... 32
Gambar 16. Spektra1H-NMR hasil sintesis ... 33
Gambar 18. Perkiraan posisi proton dibenzilidinsikloheksanon ... 38
Gambar 19. Spektra1H-NMR dan daerah serapan senyawa
benzilidinsikloheksanon menggunakanchemdraw... 39
Gambar 20. Mekanisme reaksi sintesis benzilidinsikloheksanon ... 41
Gambar 21. Mekanisme reaksi sintesis dibenzilidinsikloheksanon ... 42
Gambar 22. Grafik perbandingan rasio mol sikloheksanon : benzaldehida
DAFTAR TABEL
Tabel 1. Daerah serapan gugus fungsi pada spektoskopi IR ... 16
Tabel 2. Data hasil sintesis senyawa benzilidinsikloheksanon dengan variasi
rasio mol sikloheksanon dan benzaldehida ... 27
Tabel 3. Data daerah serapan gugus fungsi spektroskopi IR menurut teori dan
hasil sintesis ... 32
Tabel 4. Data daerah pergeseran dan perkiraan proton hasil sintesis ... 33
Tabel 5. Perbandingan daerah serapan antara hasil sintesis dengan perkiraan
DAFTAR LAMPIRAN
Lampiran 1. Perhitungan Jumlah Bahan dan Rendemen ... 49
Lampiran 2. Prosedur Sintesis Benzilidinsikloheksanon ... 54
Lampiran 3. Hasil TLCScannerSenyawa Hasil Sintesis ... 59
Lampiran 4. Hasil IR Sintesis Senyawa Benzilidinsikloheksanon ... 63
Lampiran 5. Hasil1H-NMR Sintesis Senyawa Benzilidinsikloheksanon ... 66
PENGARUH VARIASI RASIO MOL SIKLOHEKSANON-BENZALDEHIDA PADA SINTESIS BENZILIDINSIKLOHEKSANON
Oleh:
Nur Rahma Yuliyani 12307141020
Pembimbing : Dr. Sri Handayani
ABSTRAK
Tujuan penelitian ini untuk menentukan pengaruh variasi rasio mol sikloheksanon : benzaldehida pada sintesis benzilidinsikloheksanon. Selain itu, untuk menentukan rasio mol sikloheksanon : benzaldehida yang dapat menghasil-kan rendemen maksimum. Sintesis benzilidinsikloheksanon menggunamenghasil-kan reaksi kondensasi aldol silang dengan katalis NaOH.
Sintesis benzilidinsikloheksanon menggunakan metode stirring pada suhu 5oC. Pelarut yang digunakan akuades : etanol (1 : 1) dengan waktu sintesis selama
4 jam. Variasi rasio mol sikloheksanon : benzaldehida yang digunakan adalah 1 : 1, 2 : 1, 4 : 1, 6 : 1 dan 8 : 1. Hasil sintesis diidentifikasi menggunakan KLT, KLT scanner, spektroskopi IR dan spektroskopi 1H-NMR. Sintesis benzilidinsiklo-heksanon dengan variasi rasio mol siklobenzilidinsiklo-heksanon : benzaldehida secara berurutan menghasilkan rendemenen sebesar 4,54; 8,52; 9,95; 12,73 dan 2,79%.
Kesimpulan dari penelitian ini adalah variasi rasio mol sikloheksanon : benzaldehida berpengaruh pada sintesis benzilidinsikloheksanon. Hal tersebut ditunjukkan dari hasil rendemen benzilidinsikloheksanon yang mengalami peningkatan pada rasio mol sikloheksanon : benzaldehida 1 : 1 sampai dengan 6 : 1, tetapi mengalami penurunan pada rasio 8 : 1. Rasio mol sikloheksanon : benzaldehida yang memberikan rendemen maksimum adalah 6 : 1.
EFFECT OF VARIATION CYCLOHEXANONE-BENZALDEHYDE MOLE RATIO ON BENZYLIDENECYCLOHEXANONE SYNTHESIS
Oleh:
Nur Rahma Yuliyani 12307141020
Adviser : Dr. Sri Handayani
ABSTRACT
The purpose of this research was to determine effect of variation cyclo-hexanone : benzaldehyde mole ratio on benzylidenecyclocyclo-hexanone synthesis. Moreover, to determined mole ratio of cyclohexanone : benzaldehyde which produced maximum rendemen. Synthesis benzylidenecyclohexanone using crossed aldol condensation reaction with NaOH catalyst.
Synthesis benzylidenecyclohexanone was done by strirring methode with temperature 5oC. Solvent were aquades : ethanol (1 : 1) with synthesis time 4 hours. Mole ratio variation cyclohexanone : benzaldehyde were 1 : 1, 2 : 1, 4 : 1, 6 : 1, and 8 : 1. Identification of synthesis product using TLC, TLC scanner, spectroscopy IR and spectroscopy1H-NMR. Synthesis benzylidenecyclohexanone with variation cyclohexanone: benzaldehyde mole ratio produce rendemen 4.54, 8.52, 9.95, 12.73, and 2.79%.
The conclusion of this research is variation cyclohexanone : benzaldehyde mole ratio influential on benzylidenecyclohexanone synthesis. Those things
showed from rendemen’s result of benzylidenecyclohexanone which experiencing an excalation on mole ratio of cyclohexanone : benzaldehyde 1 : 1 until 6 : 1, but descending on ratio 8 : 1. Mole ratio of cyclohexanone : benzaldehyde which give maximum rendemen is 6 : 1.
BAB I PENDAHULUAN
A. Latar Belakang Masalah
Sebagian besar molekul-molekul organik mempunyai kompleksitas yang
tinggi, sehingga diperlukan metode sintesis untuk pembuatan molekul organik
tersebut. Sintesis senyawa organik merupakan suatu teknik untuk memperoleh
suatu senyawa yang mempunyai kemiripan dengan senyawa yang berasal dari
alam, tetapi pada teknik ini menggunakan bahan kimia atau buatan. Pada saat ini
sejumlah senyawa organik telah berhasil disintesis dalam skala laboratorium
sampai dengan industri kimia.
Benzilidinsikloheksanon merupakan senyawa yang diperoleh dari reaksi
kondensasi aldol antara sikloheksanon dan benzaldehida dengan katalis larutan
NaOH (Pudjono, 2010). Senyawa analog kurkumin mempunyai aktivitas biologi
sebagai antiinflamasi, antioksidan, antikanker, dan anti-HIV (Da’i, 2010). Sintesis
analog benzalaseton menggunakan NaOH/ZrO2-Montmorilonit menghasilkan
senyawa yang bersifat antioksidan (Handayani, 2012).
Metode sintesis dapat diketahui keberhasilannya dengan memperhatikan
ketepatan perbandingan rasio mol reaktan. Ketepatan perbandingan rasio mol dari
reaktan tersebut berpengaruh terhadap terbentuknya senyawa target. Hal ini
diperkuat dengan adanya penelitian mengenai sintesis benzalaseton atau
turunannya dengan menggunakan rasio mol reaktan antara aseton : benzaldehida
turunannya menggunakan rasio mol reaktan antara aseton : benzaldehida
(turunannya) adalah 1 : 2 (Handayani dan Arty, 2008).
Oktovianto (2015) telah berhasil mensintesis 2,6-bis-(4’-metoksibenzilidn)
sikloheksanon. Sintesis ini menggunakan variasi NaOH yaitu 0,0025; 0,005; 0,01;
0,02; dan 0,04 mol. Bahan yang digunakan adalah
sikloheksanon:4-metoksibenzaldehida 1 : 2 dengan pelarut akuades : etanol (2 : 3). Sintesis ini
dilakukan melalui reaksi Claisen-Schmidtselama 120 menit. Rendemen maksimal
adalah pada 0,04 mol NaOH.
Hasanah et al.(2014) telah berhasil melakukan sintesis senyawa kurkumin
(3E,5E)-3,5-bis(2’-hidroksibenzilidin)-1-metilpiperidin-4-on. Pada sintesis ini
menggunakan senyawa 1-metil-4-piperidinon : 2-hidroksibenzaldehida (1 : 2).
Katalis yang digunakan adalah basa NaOH 20% dan pelarut etanol. Sintesis ini
menggunakan irradiasi microwave. Reaksi ini dilakukan selama 1 menit dengan
menggunakan daya 180 watt. Hasil rendemen yang diperoleh dari sintesis ini
sebesar 72%.
Triono dan Haryadi (2014) telah berhasil melakukan sintesis senyawa
1,7-difenil-1,4,6-heptatrien-3-on. Bahan yang digunakan adalah sinamalaseton dan
benzaldehida 1 : 1. Katalis yang digunakan adalah NaOH dengan pelarut akuades
dan etanol. Sintesis ini dilakukan selama 30 menit. Hasil reaksi kondensasi aldol
silang ini menghasilkan rendemen 71,26%.
Dewanti (2011) telah berhasil mensintesis 4-hidroksidibenzalaseton.
Sintesis ini dilakukan melalui reaksi kondensasi aldol silang. Bahan yang
yang digunakan adalah NaOH dengan pelarut akuades : etanol (1 : 1) sintesis ini
dilakukan dengan membuat variasi teknik sintesis. Teknik pertama katalis NaOH
yang telah siap dicampur dengan semua bahan, lalu disintesis. Teknik kedua
4-hidroksibenzaldehida dimasukkan, lalu berurutan dimasukkan benzaldehida dan
aseton. Teknik ketiga, aseton dimasukkan terlebih dahulu kemudian benzaldehida.
Etanol 15 ml dimasukkan lalu 4-hidroksibenzaldehida, dilanjutkan NaOH dalam
15 ml akuades. Hasil menjelaskan bahwa sintesis menggunakan teknik 1 dan 2
mempunyai perbedaan dari senyawa asal. Rendemen yang dihasilkan 0,145%
dengan kemurnian 87,09%.
Apriyansah (2010) telah berhasil mensintesis 3-hidroksidibenzalaseton.
Sintesis ini menggunakan benzaldehida : aseton : 3-hidroksibenzaldehida 1 : 1 : 1.
Katalis yang digunakan adalah NaOH 0,05 mol dengan pelarut akuades : etanol 1
: 1. Sintesis dilakukan melalui reaksi kondensasi aldol silang selama 6 jam.
Rendemen yang dihasilkan adalah 0,82%.
Pada penelitian ini diinginkan senyawa benzilidinsikloheksanon karena
dimungkinkan mempunyai sifat sebagai antioksidan, antikanker, dan anti-HIV.
Pembentukan senyawa benzilidinsikloheksanon sangatlah sulit karena bahan yang
digunakan adalah sikloheksanon yang mempunyai 4Hα. Benzilidinsikloheksanon
kurang stabil karena masih mempunyai Hα sehingga produk sintesis akan lebih
mudah membentuk dibenzilidinsikloheksanon. Dengan melakukan variasi rasio
mol reaktan, diharapkan dapat berhasil memperoleh senyawa target, yaitu
Tujuan variasi mol reaktan untuk menentukan rasio mol yang menghasilkan
rendemen maksimum. Secara teori, rasio mol antara sikloheksanon dan
benzaldehida 1 : 1 akan menghasilkan senyawa benzilidinsikloheksanon.
Penggu-naan variasi rasio mol sikloheksanon : benzaldehida dapat memberikan pengaruh
terbentuknya hasil samping, berupa dibenzilidinsikloheksanon. Secara teori,
senyawa dibenzilidinsikloheksanon dapat terbentuk dengan perbandingan rasio
mol sikloheksanon : benzaldehida 1 : 2.
Identifikasi senyawa senyawa benzilidinsikloheksanon hasil sintesis
dilakukan dengan menggunakan KLT dan KLT scanner. Karakterisasi gugus
fungsi dan struktur dari senyawa benzilidinsikloheksanon hasil sintesis dilakukan
dengan menggunakan spektrofotometer inframerah dan spektrofotometer 1
H-NMR.
B. Identifikasi Masalah
Berdasarkan latar belakang masalah yang telah diuraikan, maka dapat
diidentifikasikan beberapa masalah sebagai berikut:
1. Ada berbagai rasio mol sikloheksanon : benzaldehida yang digunakan untuk
sintesis benzilidinsikloheksanon yang dapat mempengaruhi banyak sedikitnya
rendemen yang diperoleh.
2. Ada berbagai katalis yang dapat digunakan untuk sintesis
benzilidin-sikloheksanon seperti katalis basa NaOH, katalis asam HCl dan H2SO4.
3. Ada berbagai metode identifikasi dan karakterisasi benzilidinsikloheksanon
yang dapat digunakan, seperti KLT, KLT scanner, GC-MS, spektroskopi IR,
C. Pembatasan Masalah
Penelitian ini mempunyai pembatasan masalah sebagai berikut:
1. Rasio mol sikloheksanon : benzaldehida yang digunakan untuk sintesis
benzili-dinsikloheksanon adalah 1 : 1; 2 : 1; 4 : 1, 6 : 1, dan 8 : 1.
2. Katalis yang digunakan untuk sintesis benzilidinsikloheksanon adalah katalis
basa kuat NaOH 0,2 gram.
3. Metode identifikasi dan karakterisasi senyawa benzilidinsikloheksanon
menggunakan KLT, KLT scanner, spektroskopi IR dan spektroskopi 1
H-NMR.
D. Rumusan Masalah
Berdasarkan identifikasi dan pembatasan masalah, maka dapat disusun
rumusan masalah sebagai berikut:
1. Berapa rendemen dari tiap variasi rasio mol sikloheksanon : benzaldehida pada
sintesis benzilidinsikloheksanon?
2. Berapa rasio mol sikloheksanon : benzaldehida yang menghasilkan
benzilidin-sikloheksanon maksimum?
3. Bagaimana pengaruh variasi rasio mol sikloheksanon : benzaldehida pada
sintesis benzilidinsikloheksanon?
E. Tujuan Penelitian
Tujuan penelitian ini adalah untuk menentukan:
1. rendemen dari tiap variasi rasio mol sikloheksanon : benzaldehida pada sintesis
2. rasio mol antara sikloheksanon dan benzaldehida yang menghasilkan
benzilidinsikloheksanon dengan rendemen maksimal.
3. pengaruh variasi rasio mol antara sikloheksanon dan benzaldehida pada sintesis
benzilidinsikloheksanon.
F. Manfaat Penelitian
Berdasarkan hasil penelitian ini diharapkan dapat memberikan manfaat:
1. Bagi masyarakat, yaitu hasil sintesis senyawa benzilidinsikloheksanon dapat
digunakan, khususnya pada bidang kimia.
2. Bagi peneliti, yaitu dapat mengetahui konsep reaksi kondensasi aldol silang
dan pengaruh variasi rasio mol reaktan (sikloheksanon dan benzaldehida) pada
sintesis senyawa benzilidinsikloheksanon.
3. Bagi lembaga atau institut pendidikan, yaitu sebagai bahan informasi dan
BAB II
KAJIAN PUSTAKA
A. Deskripsi Teori
1. Benzilidinsikloheksanon
Benzilidinsikloheksanon merupakan senyawa turunan dari benzilidinketon.
Benzilidinsikloheksanon dapat diperoleh melalui reaksi kondensasi aldol antara
sikloheksanon dan benzaldehida dengan katalis larutan NaOH. Senyawa turunan
benzilidinketon ini mempunyai peran sebagai antioksidan, antiinflamasi,
antibakteri, dan antikanker.
Senyawa benzilidinketon dapat diperoleh dengan mengisolasi kunyit, yaitu
terletak pada bagian pigmen kuning dari kunyit (Curcuma sp). Senyawa hasil
isolasi dari kunyit (Curcuma sp) disebut dengan kurkumin (Pudjono, 2010).
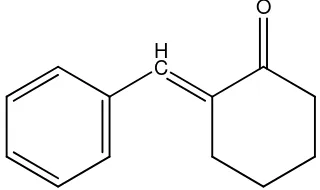
Benzilidinsikloheksanon mempunyai rumus struktur molekul C13H14O.
Struktur molekul benzilidinsikloheksanon ditunjukkan pada Gambar 1.
H C
O
Gambar 1. Struktur benzilidinsikloheksanon
2. Benzaldehida
Benzaldehida merupakan senyawa turunan benzena yang salah satu atom
hidrogennya tersubstitusi gugus aldehida (-CHO). Gugus karbonil (C=O) pada
rangkap terkonjugasi. Benzaldehida mempunyai rumus struktur molekul
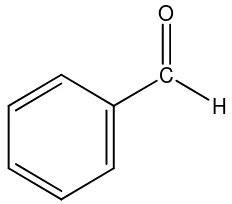
C6H5CHO seperti pada Gambar 2.
C H O
Gambar 2. Struktur benzaldehida
Benzaldehida banyak dimanfaatkan dalam pembuatan perisa almond pada
makanan dan minuman. Benzaldehida mempunyai bau yang khas sehingga
banyak digunakan sebagai bahan baku pembuatan parfum. Penggunaan lainnya
dari benzaldehida adalah sebagai bahan pestisida dan sebagai intermediet dalam
sintesis senyawa organik.
Hasil penelitian Handayani dan Arty (2008) menunjukkan bahwa
benzaldehida atau turunan benzaldehida yang direaksikan dengan aseton dapat
menghasilkan senyawa benzalaseton atau turunannya. Senyawa benzalaseton
adalah senyawa hasil sintesis antara aseton : benzaldehida (1 : 1). Senyawa
anisalaseton adalah hasil sintesis antara p-anisaldehida : aseton (1 : 1). Senyawa
veratralaseton adalah hasil sintesis antara veratraldehida : aseton (1 : 1).
3. Sikloheksanon
Sikloheksanon merupakan senyawa keton yang memilikiHα. Sikloheksanon
menguap. Sikloheksanon mempunyai sifat yang sedikit larut dalam air. Rumus
struktur molekul dari sikloheksanon adalah C6H10O seperti pada Gambar 3.
O
Gambar 3. Struktur sikloheksanon
Sikloheksanon digunakan dalam sintesis benzilidinsikloheksanon.
Berdasarkan hasil penelitian Pudjono et al. (2010) menunjukkan bahwa sintesis
melalui reaksi multistep kondensasi aldol antara p-nitrobenzaldehida dan
sikloheksanon dengan katalis asam klorida pekat menghasilkan
2-sikloheksilidin-6-(4’-nitrobenzilidin)sikloheksanon dan 2-(4’-nitrobenzilidin)sikloheksanon.
4. Natrium Hidroksida (NaOH)
Natrium hidroksida (NaOH) merupakan senyawa basa kuat yang juga
dikenal dengan istilah sodium hidroksida atau soda kaustik. NaOH murni
biasanya berbentuk padat berwarna putih. NaOH mempunyai sifat mudah larut
dalam air dan melepaskan panas ketika dilarutkan karena sifat dasarnya yang
merupakan golongan basa kuat. NaOH berperan sebagai katalis basa homogen,
yaitu katalis yang mempunyai fase yang sama dengan reaktan.
Katalis merupakan suatu senyawa yang mempunyai fungsi meningkatkan
laju reaksi untuk mencapai suatu kesetimbangan. Dengan adanya katalis, maka
dibandingkan reaksi tanpa menggunakan katalis. Penambahan katalis
mengakibatkan adanya interaksi antara reaktan dengan katalis tersebut tetapi pada
akhir reaksi akan terbentuk kembali seperti keadaan semula.
Katalis secara umum dapat dibedakan menjadi tiga, yaitu katalis homogen,
heterogen, dan enzim. Katalis homogen adalah katalis yang mempunyai fase yang
sama dengan reaktannya. Katalis heterogen adalah katalis yang fasenya berbeda
dengan reaktannya. Katalis enzim adalah katalis yang digunakan pada
reaksi-reaksi biokimia (Helwaniet al.,2009).
Katalis homogen terdiri dua jenis, yaitu asam dan basa. Katalis homogen
asam dapat berupa H2SO4, HCl dan H3PO4. Penggunaan katalis asam ini
membutuhkan waktu reaksi yang lama dan menyebabkan korosi pada reaktor
yang digunakan. Katalis homogen basa dapat berupa KOH dan NaOH.
Penggunaan katalis basa ini menghasilkan limbah pencucian dalam jumlah yang
besar (Helwaniet al.,2009).
NaOH berperan sebagai katalis dalam reaksi kondensasi aldol silang.
Dengan adanya suasana basa, maka ion enolat dapat terbentuk dengan syarat
senyawa aldehida atau keton mempunyai Hα.
5. Kondensasi Aldol Silang
Kondensasi aldol adalah reaksi pembentukan ikatan karbon-karbon melalui
adisi nukleofil dari enolat keton terhadap suatu aldehida. Reaksi ini biasanya
melepaskan satu molekul air untuk membentuk suatu senyawa karbonil tak jenuh
enolat dan senyawa karbonil lain. Jika nukleofil dan elektrofil yang digunakan
berbeda maka reaksi ini disebut reaksi kondensasi aldol silang (Bruice, 2007).
Reaksi kondensasi aldol mempunyai dua macam mekanisme reaksi berbeda
yang tergantung pada katalis yang digunakan. Apabila reaksi berlangsung dalam
suasana asam, maka menggunakan mekanisme enol. Apabila reaksi berlangsung
dalam suasana basa, maka menggunakan mekanisme enolat.
Reaksi kondensasi aldol silang dengan katalis basa akan menggunakan
mekanisme enolat. Basa yang digunakan biasanya ion hidroksida atau alkoksida.
Reaksi kondensasi aldol silang yang berlangsung dimulai dengan serangan
nukleofilik oleh resonansi enolat pada gugus karbonil terhadap molekul karbonil
yang lainnya. Produk yang dihasilkan pada reaksi ini adalah garam alkoksida.
Senyawa keton dalam suasana basa (NaOH) akan membentuk ion enolat
yang dapat bereaksi dengan gugus karbonil dari senyawa aldehida. Ion enolat
yang bereaksi dengan molekul aldehida lain akan mengadisi karbon karbonil,
sehingga terbentuk ion alkoksida. Ion alkoksida yang bereaksi dengan air akan
menghasilkan senyawa aldol.
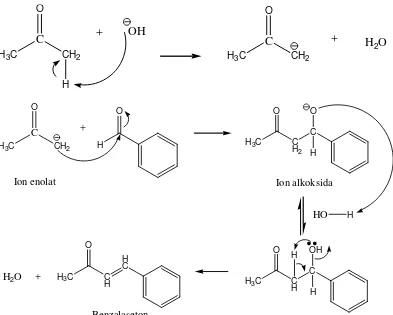
Handayani (2009) menjelaskan mekanisme reaksi yang terjadi pada
pembentukan benzalaseton. Reaktan yang digunakan adalah aseton : benzaldehida
1:1. Reaksi kondensasi aldol silang ini diawali dengan pembentukan ion enolat,
Hα pada senyawa aseton bereaksi dengan katalis NaOH. Ion enolat yang tebentuk
bertindak sebagai nukleofil. Nukleofil ini akan menyerang karbon karbonil dari
benzaldehida kemudian membentuk senyawa aldol. Mekanisme reaksinya
C
Gambar 4. Mekanisme reaksi pembentukan benzalaseton
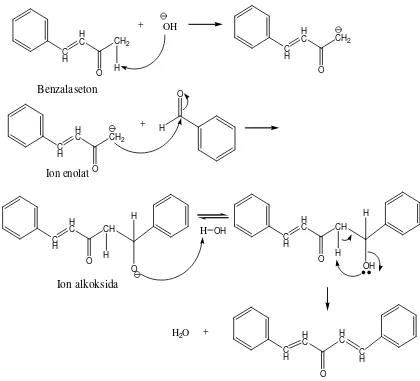
Senyawa benzalaseton masih mempunyai Hα, sehingga cenderung mudah
bereaksi membentuk senyawa dibenzalaseton. Hal tersebut dapat terjadi apabila
jumlah benzaldehida ditambahkan, sehingga rasio mol antara sikloheksanon :
benzaldehida menjadi 1 : 2. Benzalaseton yang masih mempunyai Hα berperan
ssebagai nukleofil menyerang karbon karbonil dari benzaldehida. Hasil reaksi
tersebut mengalami dehidrasi, sehingga membentuk senyawa dibenzalaseton.
C
Gambar 5.Mekanisme reaksi pembentukan dibenzalaseton
6. Kromatografi Lapis Tipis
Kromatografi lapis tipis merupakan metode pemisahan suatu komponen dari
senyawa dalam suatu medium yang secara prinsip memiliki persamaan dengan
kromatrografi kertas. Kromatografi lapis tipis (KLT) mempunyai beberapa
keunggulan, yaitu mudah dilakukan, mempunyai waktu yang efisien dan sampel
yang dihasilkan sangat rapat sehingga dapat mendeteksi senyawa dalam
komponen-komponen dari senyawa campuran dengan menentukan nilai Rf dari
masing-masing komponen tersebut sehingga dapat diketahui persentase
kemurnian senyawa tersebut. Nilai Rf yang baik 0,2 - 08 (Sastrohamidojo, 2005).
Pada metode KLT, nilai Rf dipengaruhi oleh ketebalan lapisan. Proses
pemisahan komponen suatu senyawa biasanya menggunakan ketebalan lapisan
250 µm dan untuk analisis preparatif digunakan ketebalan sampai 5 mm. Dalam
suatu analisis terkadang digunakan kalsium sulfat sebagai adsorben untuk
mengikat lapisan pada lempeng. Adsorben yang paling banyak digunakan untuk
pemisahan komponen dari suatu senyawa adalah silika gel (Bintang, 2008).
Fasa bergerak yang digunakan sebaiknya adalah campuran pelarut organik.
Hal ini disebabkan pelarut organik mempunyai polaritas yang rendah. Penggunaan
campuran pelarut organik ini akan mengurangi serapan dari setiap komponen dari
campuran pelarut (Sastrohamidjojo, 2005).
Prinsip kerja dari metode KLT adalah sampel yang berupa senyawa organik
ditotolkan pada suatu lempengan. Sampel yang digunakan sebaiknya dalam
jumlah yang kecil dan encer agar tidak menimbulkan noda yang melebar.
Lempengan berperan sebagai fasa diam dan pelarut non polar yang mempunyai
sifat mudah menguap sebagai fasa gerak atau eluen. Eluen berfungsi untuk
memisahkan komponen-komponen dalam sampel senyawa organik. Eluen yang
baik adalah campuran pelarut yang mempunyai tingkat kemurnian tinggi.
Lempengan yang tercelup pada eluen akan menunjukkan pergerakan hingga batas
tertentu (Day, 2002). Pada metode ini, nilai Retordation factor (Rf) dinyatakan
Rf =
Hal yang perlu diperhatikan dalam proses analisis menggunakan metode ini
adalah kondisi lingkungan karena pemisahan harus jenuh dengan pelarut sehingga
besar kecilnya nilai Rf dapat ditentukan. Hal ini dapat dilakukan dengan wadah
sekecil mungkin dan menghubungkan dinding dengan kertas yang terendam
dalam pelarut. Pengembangan pelarut pada lempengan biasanya menggunakan
teknik ascending yang berlangsung lebih lambat dibandingkan dengan teknik
descending. Teknik ascending merupakan teknik yang dilakukan dengan cara
menunggu fase gerak merambat ke atas hingga batas tertentu, sedangkan
descendingsebaliknya.
7. Spektroskopi IR
Spektroskopi inframerah merupakan metode spektroskopi yang berperan
untuk menentukan gugus fungsional pada suatu senyawa organik. Radiasi
inframerah menghasilkan energi yang dapat memberikan efek vibrasi (getaran)
pada gugus yang terkena radiasi tersebut. Efek vibrasi yang dihasilkan akan
memberikan informasi spesifik untuk masing-masing gugus fungsi yang terkena
radiasi inframerah.
Spektrum inframerah dari suatu molekul merupakan hasil transisi antara
tingkat energi getaran yang berlainan. Spektrum inframerah dari senyawa organik
mempunyai sifat fisik yang khas sehingga dari dua senyawa akan kecil
berasal dari kompleks, karena adanya overtone kombinasi dan perbedaan serapan
yang lemah.
Pada spektrum inframerah terdapat pita-pita yang letaknya dapat
dikelompokkan berdasarkan intensitas absorpsinya: kuat, medium dan lemah
dengan pita spektrum tajam, sedang ataupun melebar. Pita-pita pada spektrum
tersebut berada pada daerah serapan inframerah. Daerah finger print merupakan
daerah yang mengandung spektrum tertentu yang tidak dapat dijelaskan, yaitu
pada daerah serapan 1400-900 cm-1. Hampir sebagian ikatan tunggal akan
memberikan serapan pada daerah ini. Hal ini disebabkan energi vibrasi berbagai
ikatan tunggal hampir sama besarnya, sehingga akan terjadi interaksi kuat antara
ikatan tunggal yang berdekatan (Sastrohamidjojo, 2001).
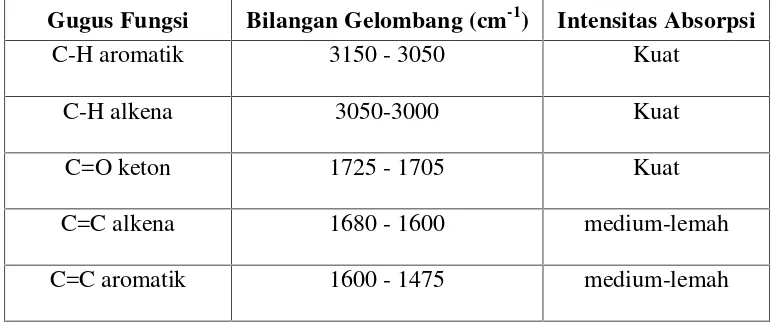
Beberapa daerah serapan inframerah penting ditunjukkan pada Tabel 1
berikut (Paviaet al., 2009).
Tabel 1. Daerah serapan gugus fungsi pada spektroskopi IR
Gugus Fungsi Bilangan Gelombang (cm-1) Intensitas Absorpsi
C-H aromatik 3150 - 3050 Kuat
C-H alkena 3050-3000 Kuat
C=O keton 1725 - 1705 Kuat
C=C alkena 1680 - 1600 medium-lemah
C=C aromatik 1600 - 1475 medium-lemah
Dengan melakukan pengujian sejumlah senyawa yang telah diketahui gugus
fungsinya, maka dapat diketahui serapan frekuensi dari senyawa tersebut. Selain
gugus fungsi akan terlihat pada daerah-daerah tertentu. Serapan dari gugus fungsi
dengan kisaran kecil dapat digunakan untuk menentukan tipe ikatan.
8. Spektroskopi1H-NMR
Spektroskopi resonansi magnetik inti (NMR) merupakan metode yang
digunakan untuk menentukan struktur suatu senyawa dengan spektrum NMR
yang menginformasikan tentang lingkungan kimia dari atom hidrogen, jumlah
atom hidrogen pada tiap lingkungan kimia dan struktur dari gugus yang
berdekatan dengan atom hidrogen. Prinsip dasar dari spektroskopi NMR adalah
penyerapan gelombang radio oleh inti-inti dalam suatu molekul organik yang
berada pada medan magnet yang kuat.
Inti atom hidrogen atau proton mempunyai sifat-sifat magnet. Bila suatu
senyawa yang mengandung atom hidrogen diletakkan pada bidang magnet yang
sangat kuat dan dipancarkan radiasi elektromagnetik, maka inti atom hidrogen
dari senyawa tersebut akan menyerap energi melalui proses absorbsi yang disebut
dengan resonansi magnet. Absorpsi radiasi dapat terjadi apabila kekuatan medan
magnet sesuai dengan frekuensi radiasi elektromagnet.
Senyawa yang berperan sebagai larutan standar adalah tetrametilsilan
(CH3)4Si atau TMS. Senyawa TMS yang digunakan mempunyai keunggulan,
yaitu protonnya dapat beresonansi pada medan magnet yang lebih besar daripada
medan magnet untuk resonansi proton senyawa organik lainnya. Hal tersebut
menyebabkan proton-proton dari gugus metil jauh lebih terlindungi dibandingkan
Tiap proton dalam suatu molekul akan beresonansi pada frekuensi yang
sama. Hal ini disebabkan karena proton dalam molekul tersebut dikelilingi oleh
elektron yang menunjukkan perbedaan lingkungan elektronik dari satu proton
terhadap proton lainnya. Konsep dasar atom menerangkan bahwa proton akan
dilindungi oleh elektron-elektron yang mengelilinginya. Semakin besar kerapatan
elektron yang mengelilingi proton (inti), semakin besar pula medan yang
dihasilkan berlawanan dengan medan yang digunakan.
Dalam suatu molekul, tiap proton berada dalam lingkungan kimia yang
berbeda. Hal ini memberikan shielding elektronik yang tingkatannya juga sedikit
berbeda. Beberapa substituen elektronegatif yang terikat pada atom karbon
mengakibatkan penarikan elektron. Penarikan ini akan mereduksi kerapatan dari
elektron valensi sekitar proton yang terikat pada karbon tersebut. Semakin banyak
substituen yang bersifat elektronegatif, semakin banyak pula proton yang tidak
terlindungi, sehingga akan terjadi pergeseran kimia dari proton-proton tersebut
(Sastrohamidjojo, 2007).
Spektra NMR dapat digambarkan dengan grafik yang menunjukkan
kekuatan medan magnet yang digunakan meningkat dari kiri ke kanan. Pada
bagian kiri dari grafik merupakan bagian medan magnet rendah (down field) dan
bagian kanan dari grafik merupakan bagian medan magnet tinggi (up field).
Pergeseran kimia TMS dapat dinyatakan sebagai titik nol dan absorpsi lainnya
Pergeseran kimia untuk jenis proton C-H aromatis berada pada daerah (δ)
sekitar 6,5 - 8 ppm, C=CH berada pada daerah (δ) sekitar 4,5 - 6,5 ppm dan C-H
alifatik berada pada daerah pergeseran kimia (δ) 2,1- 2,4 ppm (Paviaet al., 2009).
B. Penelitian yang Relevan
Pudjono et al. (2010) melaporkan bahwa telah berhasil melakukan sintesis
senyawa 2-sikloheksilidin-6-(4’-nitrobenzilidin)sikloheksanon dan senyawa 2-(4’
-nitrobenzilidin)sikloheksanon. Sintesis ini melalui reaksi multistep kondensasi
aldol antara p-nitrobenzaldehida dan sikloheksanon (1 : 1) dengan katalis HCl
pekat. Proses sintesis dilakukan selama 2 jam dan didiamkan selama 2 hari. Hasil
senyawa 2-sikloheksilidin-6-(4’-nitrobenzilidin)sikloheksanon mempunyai rumus
molekul C19H21NO3 kadarnya 12,53%. Senyawa 2-(4’
-nitrobenzilidin)-sikloheksanon mempunyai rumus molekul C13H12NO3dengan kadar 16,42%.
Pudjono et al. (2008) melaporkan bahwa telah berhasil melakukan sintesis
2,5-bis-(4’-hidroksi benzilidin)siklopentanon dan 2,5-bis-(4’
-klorobenzilidin)-siklopentanon. Sintesis ini melalui reaksi kondensasi Claisen-Schmidt antara
4-hidroksibenzaldehida dan 4-klorobenzaldehida:siklopentanon 1:2. Reaksi ini
menggunakan asam sulfat sebagai katalis dalam pelarut metanol dan 2-butanol.
Campuran ini didiamkan selama 30 menit. Proses sintesis dilakukan dengan cara
merefluks selama 2 jam pada suhu kamar. Hasil sintesis menggunakan pelarut
metanol menghasilkan 2,5-bis-(4’-hidroksi benzilidin)siklopentanon 23,36%.
Hasil sintesis menggunakan pelarut 2-butanol menghasilkan 2,5-bis-(4’-hidroksi
benzilidin)siklopentanon 82,87% dan 2,5-bis-(4’-klorobenzilidin)siklopentanon
Handayani and Arty (2008) melaporkan bahwa telah berhasil melakukan
sintesis benzalaseton serta turunannya melalui reaksi kondensasi aldol silang.
Sintesis menggunakan benzaldehida : aseton dengan rasio mol 1 : 1 menghasilkan
benzalaseton. Sintesis dengan rasio mol benzaldehida:aseton 2 : 1 menghasilkan
dibenzalaseton. Sintesis dilakukan selama 40 menit, 10 menit pertama larutan
NaOH (dalam akuades:etanol 1 : 1) dan benzaldehida diaduk. Aseton
ditambahkan dan pengadukan dilanjutkan selama 30 menit.
Da’i et al. (2010) melaporkan bahwa telah berhasil melakukan sintesis
senyawa analog kurkumin 3,5-bis-(4’-hidroksi-3’-metoksi
benzilidin)-piperidin-4-on (mbenzilidin)-piperidin-4-onohidrat hidroklorida). Sintesis ini dilakukan melalui reaksi kbenzilidin)-piperidin-4-ondensasi
aldol menggunakan katalis HCl. Piperidin-4-on monohidrat hidroklorida:vanilin
dengan rasio mol 1 : 2 digunakan dalam sintesis. Proses sintesis dilakukan dengan
variasi suhu, yaitu pada suhu kamar, pemanasan pada suhu 50 - 80oC dan refluks
pada suhu > 80oC. Sintesis ini berlangsung selama 2 jam dan didinginkan selama
2 hari. Hasil sintesis ini berupa pH optimal pembentukan senyawa analog
kurkumin 3,5-bis-(4’-hidroksi-3’-metoksi benzilidin)-piperidin-4-on (monohidrat
hidroklorida), yaitu pada pH 2.
Prabawati et al. (2014) telah berhasil melakukan sintesis senyawa
4-dimetilaminodibenzalaseton. Katalis yang digunakan adalah katalis basa kuat
NaOH 10%. Reaksi dilakukan pada kondisi di bawah suhu kamar. Bahan yang
digunakan adalah senyawa 4-dimetilamino-benzeldehida, benzaldehida dan aseton
dengan rasio mol 1 : 1 : 1. Reaksi dilakukan dengan variasi waktu sintesis, yaitu 3,
selama 3 jam. Hasil yang diperoleh berupa padatan kristal berwarna orange
dengan rendemen 66,87%.
Masyithoh (2014) telah berhasil mensintesis 6-fenil-3,5-heksadiena-2-on.
Pada sintesis ini menggunakan variasi rasio mol sinamaldehida:aseton yaitu 1 : 1,
1 : 3, 1 : 5, 1 : 10 dan 1 : 20. Katalis yang digunakan adalah NaOH dengan pelarut
akuades:etanol 2 : 1. Sintesis dilakukan selama 20 menit menggunakan reaksi
kondensasi aldol silang. Rasio mol sinamaldehida:aseton yang menghasilkan hasil
maksimum rendemen sebesar 30,59% adalah 1 : 3.
Penelitian sintesis benzilidinsikloheksanon mempunyai konsep yang sama
dengan beberapa penelitian yang telah dijabarkan di atas, yaitu menggunakan
reaksi kondesasi aldol silang. Perbedaan dari penelitian sebelumnya adalah
senyawa yang akan disintesis dan variasi rasio mol reaktan yang digunakan dalam
sintesis.
C. Kerangka Berfikir
Benzilidinsikloheksanon merupakan senyawa yang diperoleh dari reaksi
kondensasi aldol antara sikloheksanon dan benzaldehida dengan katalis larutan
NaOH. Senyawa turunan benzilidinketon ini mempunyai peran sebagi
antioksidan, antiinflamasi, antibakteri dan antikanker.
Sintesis benzilidinsikloheksanon dilakukan melalui reaksi kondensasi aldol
silang antara sikloheksanon dan benzaldehida. Katalis yang digunakan berupa
basa NaOH. Katalis basa NaOH ini berperan dalam mekanisme enolat. Ion enolat
sikloheksanon berperan sebagai nukleofil dan menyerang atom C karbonil pada
proton dari molekul air membentuk β-hidroksiketon yang mudah mengalami
dehidrasi menghasilkan ikatan rangkap yang terkonjugasi dengan gugus karbonil.
Sintesis benzilidinsikloheksanon ini dilakukan dengan variasi rasio mol
sikloheksanon-benzaldehida. Secara teori, senyawa benzilidinsikloheksanon akan
terbentuk pada perbandingan rasio mol sikloheksanon : benzaldehida 1 : 1. Variasi
rasio mol antara sikloheksanon : benzaldehida dimaksudkan untuk menentukan
rasio mol dengan rendemen maksimal. Hasil dari sintesis dengan reaksi
kondensasi aldol silang ini berupa senyawa berbentuk serbuk yang akan
diidentifikasi dan karakterisasi menggunakan KLT, KLTscanner, spektroskopi IR
BAB III
METODE PENELITIAN
A. Subjek dan Objek Penelitian 1. Subjek Penelitian
Subjek dalam penelitian ini adalah senyawa benzilidinsikloheksanon.
2. Objek Penelitian
Objek dalam penelitian ini adalah hasil rendemen yang berupa serbuk
berwarna kuning dan karakteristik senyawa benzilidinsikloheksanon.
B. Variabel Penelitian 1. Variabel Bebas
Variabel bebas dalam penelitian ini adalah rasio mol senyawa benzaldehida
dan sikloheksanon.
2. Variabel terikat
Variabel terikat dalam penelitian ini adalah rendemen senyawa
benzilidin-sikloheksanon.
3. Variabel Kendali
Variabel kendali dalam penelitian ini adalah jumlah katalis NaOH, jumlah
pelarut dan lama waktu sintesis.
C. Instrumen Penelitian 1. Alat-Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini meliputi:
b. Neraca analitik
c. Penyaring Buchner
d. Alat-alat gelas meliputi: erlenmeyer, corong gelas, gelas beker, gelas arloji,
pipet tetes, pipet volum, pipet ukur, mikro pipet, spatula dan pengaduk.
e. Plat KLT Silica Gel
f. Chamber
p. Spektrometer1H-NMR 500 MHz
2. Bahan-Bahan Penelitian
Bahan-bahan yang digunakan dalam penelitian ini meliputi:
D. Prosedur Penelitian
1. Sintesis benzilidinsikloheksanon
NaOH sejumlah 0,2 gram (0,005 mol) dilarutkan ke dalam akuades : etanol
(1 : 1), lalu dimasukkan ke dalam erlenmeyer yang dilengkapi dengan pengaduk
magnetik. Erlenmeyer dimasukkan ke dalam icebath, lalu benzaldehida sejumlah
0,53 gram (0,005 mol) dan sikloheksanon sejumlah 0,49 gram (0,005 mol)
dimasukkan ke dalam erlenmeyer secara berurutan. Campuran tersebut diaduk
selama ± 4 jam. Endapan yang terbentuk disaring menggunakan corong Buchner.
Endapan hasil yang tersaring dikeringkan di bawah lampu selama 24 jam.
Endapan yang telah kering ditimbang dan ditentukan sifat fisiknya.
Langkah kerja di atas diulangi dengan menggunakan perbandingan rasio
mol sikloheksanon-benzaldehida 2 : 1, 4 : 1, 6 : 1, dan 8 : 1, serta katalis NaOH
yang digunakan tetap yaitu 0,005 mol untuk tiap-tiap sintesis dengan waktu 4 jam.
Setelah diperoleh senyawa hasil sintesis tersebut dilanjutkan dengan
mengidentifikasi menggunakan KLT dan KLTscanner.
2. Rekristalisasi
Berdasarkan hasil KLT Scanner, produk I dimungkinkan sebagai senyawa
target, sehingga sampel B digunakan untuk analisis lebih lanjut. Hal tersebut
dikarenakan sampel B memiliki kemurnian paling tinggi dan berat hasil yang
besar jika dibandingkan dengan sampel lainnya. Memilih pelarut yang sesuai
untuk rekristalisasi. Pelarut yang diujikan adalah metanol dan etanol, namun
sampel hanya dapat mengkristal dengan pelarut metanol. Sampel B sebanyak
sampel larut sempurna. Kemudian disaring menggunakan corong panas. Hasil
filtrat didinginkan dalam wadah berisi es. Setelah terbentuk kristal disaring
menggunakan penyaring Buchner. Hasil kristal tersebut dikeringkan selama
semalam.
3. Karakterisasi Senyawa Hasil Sintesis
Hasil rekristalisasi tersebut digunakan untuk analisis menggunakan
spektroskopi IR dan spektroskopi1H-NMR.
E. Teknik Analisis Data 1. Analisis Kualitatif
a. KLT untuk mengetahui pemisahan senyawa hasil proses sintesis dengan
membandingan dengan senyawa pereaksi. KLT Scanner untuk mengetahui
nilai Rf dan kemurnian senyawa hasil sintesis yang telah dipisahkan.
b. Spektroskopi Inframerah untuk memgetahui gugus fungsi pada senyawa.
c. Spektroskopi NMR untuk mengetahui jenis, jumlah dan lingkungan proton
Hidrogen.
2. Analisis Kuantitatif
Analisis kuantitatif diperlukan untuk menghitung persentase rendemen
senyawa yang dihasilkan dari proses sintesis ini. Persentase rendemen dapat
dihitung menggunakan persamaan sebagai berikut:
BAB IV
HASIL DAN PEMBAHASAN
A. Hasil Penelitian
1. Hasil Pengamatan Pengaruh Variasi Rasio Mol Sikloheksanon : Benzalde-hida pada Sintesis Benzilidinsikloheksanon
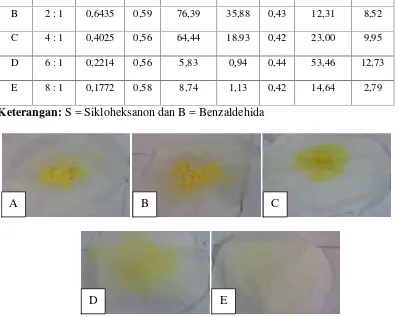
Data pengamatan hasil sintesis senyawa benzilidinsikloheksanon disajikan
pada Tabel 2 dan produk hasil sintesis disajikan pada Gambar 6 berikut.
Tabel 2. Data hasil sintesis senyawa benzilidinsikloheksanon dengan variasi rasio mol sikloheksanon dan benzaldehida
Keterangan:S = Sikloheksanon dan B = Benzaldehida
Gambar 6. Produk hasil sintesis C B
A
2. Hasil Identifikasi Produk Sintesis Menggunakan KLT dan KLTScanner Hasil kromatogram KLT produk sintesis menggunakan lampu UV disajikan
pada Gambar 7 berikut.
Gambar 7. Kromatogram KLT hasil sintesis dengan eluen kloroform : n-heksana (1 : 2)
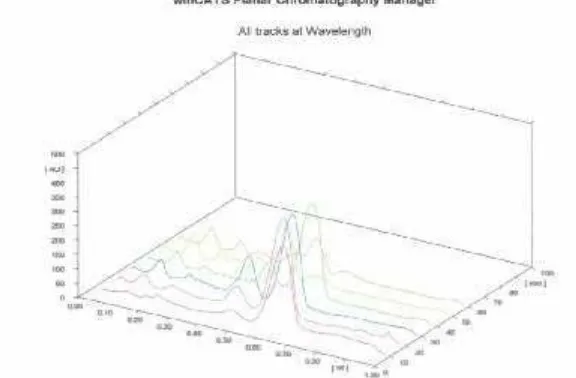
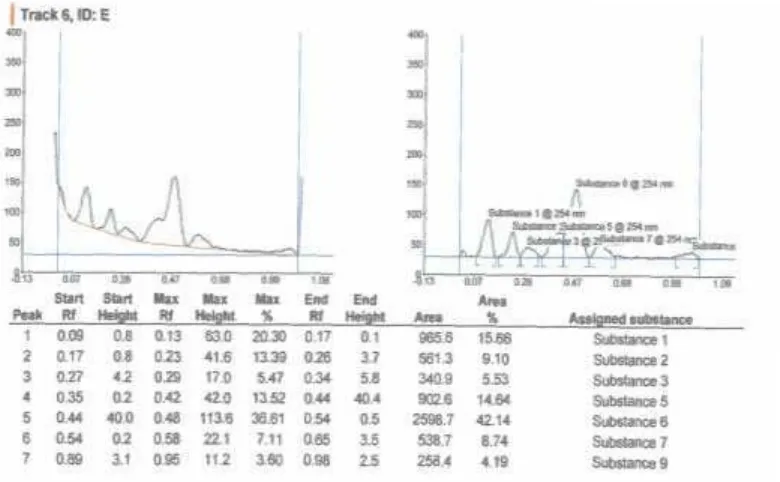
Hasil KLTScannerproduk sintesis dengan variasi rasio mol sikloheksanon
dan benzaldehida disajikan pada Gambar 8, 9, 10, 11, 12, 13, dan 14 berikut.
Gambar 8. Hasil KLTscanner
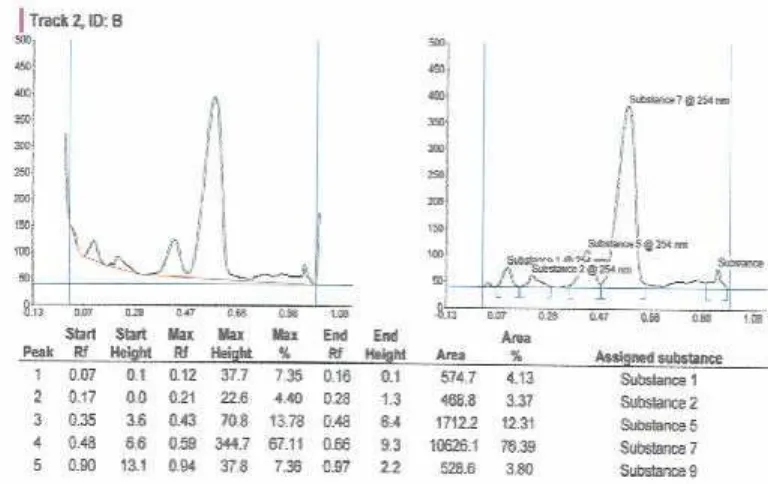
B C F D E
Gambar 9. Hasil KLTscannersintesis dengan rasio mol sikloheksanon : benzaldehida (1 : 1) selama 4 jam, eluen kloroform : n-heksana (1 : 2)
Gambar 11. Hasil KLTscannersintesis dengan rasio mol sikloheksanon : benzaldehida (4 : 1) selama 4 jam, eluen kloroform : n-heksana (1 : 2)
Gambar 13. Hasil KLTscannersintesis dengan rasio mol sikloheksanon : benzaldehida (8 : 1) selama 4 jam, eluen kloroform : n-heksana (1 : 2)
3. Hasil Identifikasi Produk Sintesis menggunakan Spektroskopi IR Spektra IR hasil sintesis ditunjukkan pada Gambar 15 berikut.
Gambar 15. Spektra IR hasil sintesis
Daerah serapan menurut teori dan hasil sintesis disajikan pada Tabel 3
berikut.
Tabel 3. Data daerah serapan gugus fungsi spektroskopi IR menurut teori dan hasil sintesis
No. Gugus Fungsi Daerah Serapan Menurut Teori (cm-1)
Daerah Serapan Menurut Hasil Sintesis (cm-1)
1 C-H aromatik 3150-3050 3082,02–3058,88
2 C-H alkena 3050-3000 3024,16
3 C=O keton 1725-1705 1658,66
4 C=C alkena 1680-1600 1604,66-1573,80
5 C=C aromatik 1600-1475 1485,08
4. Hasil Identifikasi Produk Sintesis Benzilidinsikloheksanon Menggunakan Spektroskopi1H-NMR
Spektra1H-NMR hasil sintesis disajikan pada Gambar 16 berikut. 1
2
3
Gambar 16. Spektra1H-NMR hasil sintesis
Daerah pergeseran kimia dan perkiraan proton hasil sintesis berdasarkan
spektra1H-NMR disajikan pada Tabel 4 berikut.
Tabel 4. Data daerah pergeseran dan perkiraan proton hasil sintesis
No. Hasil Sintesis δ(ΣH; m;J (Hz) Perkiraan Proton 1 7,45-7,49 (2H; dd; 7)
-CH aromatis 2 7,39-7,43 (2H; dt; 7,5)
3 7,32-7,36 (1H; t; 7,5)
4 7,79-7,82 (1H; s; 22) -CH alkena
5 2,96 (2H; dt; 11,5)
-CH2
6 1,80 (1H; m; 6,5)
7,26 (1H; s; -) CDCl3
4 5
3 2 1
B. Pembahasan
1. Identifikasi dan Karakterisasi Produk Sintesis Benzilidinsikloheksanon
a.
Identifikasi Produk Sintesis Benzilidinsikloheksanon Menggunakan KLT dan KLTScannerIdentifikasi senyawa menggunakan KLT bertujuan untuk memisahkan suatu
komponen dalam senyawa yang terkandung dalam produk sintesis. Identifikasi
menggunakan KLT ini dilakukan dengan menotolkan sampel pada plat KLT yang
berjarak masing-masing totolan 1 cm. Penotolan sampel dilakukan pada jarak 1
cm berfungsi untuk mencegah terjadinya tumbukan sampel pada saat dielusi.
Eluen yang digunakan pada kromatografi lapis tipis ini adalah campuran pelarut
organik yang memiliki tingkat polaritas rendah karena untuk mengurangi serapan
pada tiap komponen, sehingga sampel tersebut akan lebih terikat pada fasa diam
daripada geraknya. Eluen yang digunakan pada penelitian ini adalah kloroform:
n-heksan (1:2). Plat KLT yang telah diberi totolan sampel dimasukkan ke dalam
chamber yang berisi eluen tersebut. Laju eluen dapat diamati dari luar chamber,
laju eluen akan membawa zat terlarut dari sampel, sehingga akan terlihat sebagai
noda. Laju dihentikan pada saat eluen telah mencapai garis batas atas. Plat KLT
tersebut selanjutnya dikeringkan dan sampel diamati menggunakan lampu UV
dengan panjang gelombang 366 nm.
Hasil identifikasi menggunakan KLT menunjukkan pemisahan yang baik.
Hal tersebut ditunjukkan dengan noda yang terpisah, baik tunggal maupun ganda.
Setelah diperoleh hasil KLT dilanjutkan dengan KLT scanner untuk mengetahui
tingkat kemurnian dan nilai Rf dari senyawa hasil sintesis. Nilai Rf yang baik
Berdasarkan hasil identifikasi menggunakan KLT scanner diperoleh hasil
produk I dan II. Pengelompokan ini berdasarkan nilai Rf dengan puncak yang
bersebelahan. Produk I mempunyai nilai Rf 0,56 - 0,64. Produk II mempunyai
nilai Rf 0,42 - 0,47. Berdasarkan hasil pengelompokan hasil produk I dan II
tersebut dapat diketahui bahwa nilai Rf keduanya berbeda. Hasil produk I
mempunyai nilai Rf lebih tinggi dibandingkan dengan hasil II, sehingga produk I
bersifat lebih non polar dibandingkan dengan produk II. Produk yang mempunyai
tingkat kemurnian tinggi ditandai dengan persen area yang tinggi. Produk B
dengan rasio mol sikloheksanon : benzaldehida (2 : 1) mengandung produk I
dengan tingkat kemurnian tertinggi dibandingkan produk I lainnya. Produk D
dengan rasio mol sikloheksanon : benzaldehida (6 : 1) mengandung produk II
dengan tingkat kemurnian tertinggi dibandingkan produk II lainnya.
Hasil nilai Rf produk I apabila dibandingkan dengan nilai Rf dari senyawa
standar dibenzilidinsikloheksanon mempunyai kesamaan. Keduanya mempunyai
kesamaan pada nilai Rf yaitu berada pada daerah 0,56 - 0,64. Apabila nilai Rf
tersebut dibandingkan dengan produk II, keduanya mempunyai perbedaan. Hal
tersebut dikarena nilai Rf dari produk II berada pada daerah 0,42 - 0,47. Hasil ini
masih harus dilakukan analisis lebih lanjut menggunakan spektroskopi IR dan
spektroskopi1H-NMR.
b.
Identifikasi Produk Sintesis Benzilidinsikloheksanon Menggunakan Spektroskopi IRBerdasarkan spektra IR hasil sintesis pada Gambar 15 dapat dijabarkan
menunjukkan adanya gugus C-H aromatis. Hal ini diperkuat dengan adanya
serapan dengan intensitas medium pada daerah 1485,08 cm-1yang menunjukkan
adanya gugus C=C aromatik. Serapan pada daerah 3024,16 cm-1 menunjukkan
adanya gugus C-H alkena. Serapan pada daerah 1658,66 cm-1 menunjukkan
adanya gugus C=O keton. Menurut Paviaet al. (2009) gugus C=O keton biasanya
berada pada daerah sekitar 1725-1705 cm-1, namun pada hasil daerah serapannya
bergeser ke kiri. Hal ini dapat disebabkan adanya resonansi pada senyawa kimia
sehingga memperpanjang jarak ikatan dengan gugus C=O. Hal ini dipengaruhi
oleh lingkungan sekitar, yaitu adanya ikatan C=C alkena sehingga terjadi
pergeseran. Serapan pada daerah 1604,66 - 1573,80 cm-1 dengan intesitas
medium-lemah menunjukkan adanya gugus C=C alkena.
Hasil identifikasi tersebut menunjukkan bahwa senyawa hasil sintesis dapat
berupa senyawa benzilidinsikloheksanon ataupun dibenzilidinsikloheksanon. Hal
ini disebabkan gugus fungsi yang dimiliki keduanya sama. Dengan demikian
perlu identifikasi lebih lanjut menggunakan spektroskopi 1H-NMR.
c.
Identifikasi Produk Sintesis Benzilidinsikloheksanon Menggunakan Spektroskopi1H-NMRPerkiraan jumlah dan jenis proton ditampilkan pada Gambar 17 berikut:
O
Spektra 1H-NMR pada Gambar 16 menunjukkan bahwa terdapat serapan
pada daerah 1,80 ppm muncul 1 proton dengan splitting quintet yang
menggambarkan proton pada H6. Serapan pada daerah 2,96 ppm muncul 1 proton
dengan splitting quintet yang menggambarkan proton pada H7. Proton pada H6
dan H7 menunjukkan jenis proton –CH2 yang dipengaruhi oleh 4 proton
tetangganya sehingga terjadisplitting quintet. Kedudukan H7 lebih jauh dari TMS
dibandingkan dengan H6 karena posisi H7 lebih dekat dengan gugus karbonil,
sehingga lebih tidak terlindungi akibatnya bergeser menjauhi TMS. Proton H5
dan H8 merupakan jenis proton –CH2 yang apabila dipengaruhi oleh proton
tetangga akan mengalamisplitting triplet. Pada proton H8 masih mengandung Hα
dan lingkungannya dekat dengan gugus karbonil, sehingga daerah serapannya
akan lebih menjauhi TMS. Serapan pada daerah 7,26 ppm menunjukkan
munculnya 1 proton dengan splitting singlet yang merupakan pelarut CDCl3.
Pelarut kloroform yang digunakan dalam analisis ini telah mengalami deuterisasi,
sehingga menyebabkan munculnya puncak pada daerah serapan tersebut.
Serapan pada daerah 7,32-7,36 ppm muncul 1 proton dengansplitting triplet
yang menggambarkan proton pada H3. Serapan pada daerah 7,39-7,43 ppm
muncul 1 proton dengan splitting triplet yang menggambarkan proton pada H2.
Proton pada H2 dan H3 menunjukkan jenis proton –CH aromatis yang
dipengaruhi oleh 2 proton tetangganya, sehingga terjadi splitting triplet.
Kedudukan H2 lebih jauh dari TMS karena posisi H2 lebih dekat dengan gugus
alkena, sehingga lebih tidak terlindungi akibatnya bergeser menjauhi TMS.
menggambarkan proton pada H1. Puncak duplet pada H1 dipengaruhi oleh 1
proton tetangga, sehingga terjadi splitting duplet. Posisi H1 lebih jauh dari TMS
dibandingkan H2 dan H3 karena posisi H1 lebih dekat dengan gugus alkena,
sehingga proton di sekitarnya menjadi kurang terlindungi dan bergeser menjauhi
TMS. Serapan pada daerah 7,79-7,82 ppm muncul 1 proton dengan splitting
singlet yang menggambarkan proton pada H4. Puncak singlet ini menunjukkan
jenis proton–CH alkena.
Berdasarkan penjelasan tersebut, struktur produk I tersebut diperkirakan
dibenzilidinsikloheksanon yang ditunjukkan pada Gambar 18 berikut.
Gambar 18. Perkiraan posisi proton dibenzilidinsikloheksanon
Spektra1H-NMR senyawa hasil sintesis mempunyai kemiripan dengan hasil
estimasi menggunakan chemdraw. Apabila daerah serapan antara keduanya
dibandingkan mempunyai sedikit kemiripan. Daerah serapan senyawa hasil
sintesis mengalami sedikit pergeseran jika dibandingkan dengan hasil estimasi.
Hal ini disebabkan adanya pengotor yang ditandai dengan munculnya puncak
pada daerah 1,58 ppm. Adanya pengotor ini mengakibatkan pergeseran daerah
serapan yang menjauhi TMS. Pengotor yang muncul ini dapat disebabkan
Hasil sintesis merupakan senyawa dibenzilidinsikloheksanon diperkuat
dengan hasil estimasi menggunakan chemdraw. Hasilnya disajikan pada Gambar
19 berikut.
Gambar 19. Spektra 1H-NMR dan daerah serapan senyawa dibenzilidinsiklo-heksanon menggunakanchemdraw
Perbandingan daerah serapan antara hasil sintesis dengan perkiraan
Tabel 5. Perbandingan daerah serapan antara hasil sintesis dengan perkiraan chemdraw
Kode Hasil Sintesisδ (ΣH; m;J (Hz)
Perkiraan ini juga diperkuat dengan data banyaknya puncak yang muncul
pada spektra 1H-NMR. Pada spektra senyawa hasil sintesis terdapat 6 puncak
yang artinya terdapat 6 jenis proton pada senyawa tersebut.
Benzilidinsiklohek-sanon mempunyai 8 jenis proton, sedangkan dibenzilidinsiklohekBenzilidinsiklohek-sanon
mem-punyai 6 jenis proton. Berdasarkan data spektra 1H-NMR ini, senyawa hasil
sintesis adalah dibenzilidinsikloheksanon. Banyaknya proton pada senyawa hasil
sintesis juga sama dengan dibenzilidinsikloheksanon, yaitu 18 proton.
2. Mekanisme Reaksi Sintesis Benzilidinsikloheksanon
Sintesis senyawa benzilidinsikloheksanon menggunakan reaksi kondensasi
aldol silang antara sikloheksanon dan benzaldehida dengan katalis basa NaOH.
Sintesis ini berlangsung dalam suasana basa sehingga menggunakan mekanisme
Reaksi kondensasi aldol silang pada sintesis benzilidinsikloheksanon terjadi
karena adanya reaksi antara benzaldehida dengan sikloheksanon yang mempunyai
Hα dengan menggunakan katalis basa NaOH. Pada tahap awal terjadi
pemben-tukan karbanion dari sikloheksanon yang direaksikan dengan larutan basa NaOH.
Reaksi ini terjadi melalui serangan ion OH- ke Hα pada senyawa sikloheksanon
yang menghasilkan ion enolat. Ion enolat berperan sebagai nukleofil yang
bereaksi dengan gugus karbonil dari benzaldehida membentuk ion alkoksida.
Hasil reaksi tersebut mengalami dehidrasi, sehingga terbentuk
benzilidinsiklo-heksanon. Mekanisme reaksinya ditunjukkan pada Gambar 20 berikut.
C
Gambar 20. Mekanisme reaksi sintesis benzilidinsikloheksanon
Reaksi kondensasi aldol silang antara sikloheksanon dan benzaldehida
dengan katalis NaOH menghasilkan senyawa benzilidinsikloheksanon. Senyawa
reaksi lebih lanjut. Pada penelitian ini mol sikloheksanon diperbanyak dengan
variasi rasio mol sikloheksanon : benzaldehida yang digunakan 1 : 1, 2 : 1, 4 : 1, 6
: 1, dan 8 : 1 untuk menghalangi terbentuknya dibenzildinsikloheksanon.
3. Mekanisme Pembentukan Dibenzilidinsikloheksanon
Senyawa benzilidinsikloheksanon masih memiliki Hα, sehingga dapat
terjadi reaksi lebih lanjut melalui serangan ion OH-ke Hα pada
benzilidinsiklo-heksanon, kemudian terbentuk ion enolat. Ion enolat berperan sebagai nukleofil
yang bereaksi dengan gugus karbonil dari benzaldehida membentuk ion alkoksida.
Hasil reaksi tersebut mengalami dehidrasi, sehingga terbentuk
dibenzilidinsiklo-heksanon. Mekanisme reaksi dibenzilidinsikloheksanon disajikan pada Gambar 21
berikut.
4. Pengaruh Variasi Rasio Mol Sikloheksanon : Benzaldehida pada Sintesis Benzilidinsikloheksanon
Pada sintesis senyawa benzilidinsikloheksanon ini menggunakan variasi
rasio mol sikloheksanon:benzaldehida 1 : 1, 2 : 1, 4 : 1, 6 : 1, dan 8 : 1. Tujuan
dari variasi rasio mol untuk mengetahui hasil maksimum pada rasio mol tertentu.
Proses sintesis dilakukan selama 4 jam dengan metode ice bath menggunakan
reaksi kondensasi aldol silang dengan katalis basa NaOH dan pelarut akuades:
etanol (1 : 1).
Berdasarkan hasil penelitian diperoleh data seperti pada Tabel 2. Pada Tabel
2 tersebut dicantumkan bahwa terdapat produk I dan produk II. Berdasarkan hasil
identifikasi, dapat dijabarkan lebih lanjut bahwa produk I merupakan senyawa
dibenzilidinsikloheksanon dan produk II merupakan benzilidinsikloheksanon.
Tiap produk tersebut dapat dibuat grafik hubungan antara variasi rasio mol
sikloheksanon : benzaldehida dengan persen rendemen hasil sebagai berikut:
Gambar 22. Grafik perbandingan rasio mol sikloheksanon : benzaldehida terhadap rendemen
Rasio Mol Sikloheksanon : Benzaldehida
Dibenzilidinsikloheksano n (Produk I)
Berdasarkan Gambar 22 tersebut, senyawa benzilidinsikloheksanon
mempunyai kondisi maksimum yaitu pada rasio mol sikloheksanon : benzaldehida
(6 : 1) dengan persen rendemen 12,73%. Pada rasio mol sikloheksanon :
benzaldehida (6 : 1), hasil akhir produknya masih berbentuk minyak kuning.
Senyawa dibenzilidinsikloheksanon mempunyai kondisi maksimum yaitu pada
rasio mol sikloheksanon : benzaldehida (2 : 1) dengan kode 2 dengan rendemen
35,88%. Pada rasio mol sikloheksanon : benzaldehida (2 : 1) ini, hasil akhir
produknya berbentuk serbuk kuning.
Berdasarkan grafik rendemen pada Gambar 21 dapat dijabarkan bahwa
rendemen benzilidinsikloheksanon mengalami peningkatan dari rasio mol
sikloheksanon : benzaldehida 1 : 1 sampai 6 : 1, tetapi mengalami penurunan pada
rasio 8 : 1. Dengan demikian diperoleh rasio mol sikloheksanon : benzaldehida 6 :
1 memberikan rendemen paling besar.
Produk samping dibenzilidinsikloheksanon lebih banyak terbentuk jika
dibandingkan dengan benzilidinsikloheksanon. Hal ini disebabkan lamanya waktu
sintesis sehingga senyawa dibenzilidinsikloheksanon dapat mudah terbentuk dan
masih terdapatnya Hα mudah bereaksi dalam suasana basa. Dengan penambahan
mol sikloheksanon dapat mengurangi terbentuknya dibenzilidinsikloheksanon.
Benzilidinsikloheksanon bersifat lebih polar jika dibandingkan dengan
dibenzilidinsikloheksanon karena nilai Rf benzilidinsikloheksanon lebih rendah
dibandingkan dengan dibenzilidinsikloheksanon.
Pada awalnya diduga produk I adalah senyawa target, maka sampel B
lebih lanjut. Hal tersebut dikarenakan sampel B memiliki kemurnian produk I
(dibenzilidinsikloheksanon) paling besar jika dibandingkan dengan sampel
lainnya. Setelah diketahui bahwa produk II adalah benzilidinsikloheksanon,
seharusnya sampel D dengan rasio mol sikloheksanon : benzaldehida 6 : 1 yang
digunakan untuk analisis lebih lanjut. Hal tersebut dikarenakan sampel D
memiliki kemurnian produk II (benzilidinsikloheksanon) paling besar. Dengan
demikian, untuk penelitian senyawa benzilidinsikloheksanon lebih lanjut dapat
BAB V PENUTUP
A. Kesimpulan
Berdasarkan hasil penelitian dan pembahasan dapat disimpulkan bahwa:
1. Rendemen dari variasi rasio mol sikloheksanon : benzaldehida 1 : 1, 2 : 1, 4 : 1,
6 : 1, dan 8 : 1 pada sintesis benzilidinsikloheksanon secara berurutan adalah
4,54; 8,52; 9,95; 12,73; dan 2,79%.
2. Rasio mol sikloheksanon : benzaldehida yang menghasilkan hasil rendemen
maksimum adalah 6 : 1.
3. Variasi rasio mol sikloheksanon : benzaldehida berpengaruh pada sintesis
ben-zilidinsikloheksanon. Hal tersebut ditunjukkan dari hasil rendemen
benzilidin-sikloheksanon yang meningkat dari rasio mol benzilidin-sikloheksanon : benzaldehida 1 :
1 sampai dengan 6 : 1, tetapi mengalami penurunan pada rasio 8 : 1.
B. Saran
Berdasarkan penelitian yang telah dilakukan dapat diajukan saran untuk
penelitian selanjutnya:
1. Perlu dilakukan penelitian lebih lanjut dengan memperhatikan waktu sintesis
agar diperoleh hasil yang maksimal.
2. Metode stirring ini kurang cocok untuk sintesis senyawa
benzilidin-sikloheksanon, dimana produk yang dihasilkan masih berupa minyak berwarna
kuning sehingga perlu adanya penanganan akhir yang sesuai ataupun
pengembangan metode yang lebih cocok untuk melakukan sintesis senyawa