LAPORAN PRAKTIKUM FISIOLOGI TUMBUHAN LAPORAN PRAKTIKUM FISIOLOGI TUMBUHAN
DIFUSI-OSMOSIS DAN ZAT PENYERAPANNYA DIFUSI-OSMOSIS DAN ZAT PENYERAPANNYA
OLEH OLEH
KELOMPOK VII KELOMPOK VII
JURUSAN PENDIDIKAN BIOLOGI JURUSAN PENDIDIKAN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PE
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAMNGETAHUAN ALAM
UNIVERSITAS NEGERI YOGYAKARTA UNIVERSITAS NEGERI YOGYAKARTA
2013 2013
HALAMAN PENGESAHAN HALAMAN PENGESAHAN
PRAKTIKUM DIFUSI-OSMOSIS DAN PENYERAPAN ZAT PRAKTIKUM DIFUSI-OSMOSIS DAN PENYERAPAN ZAT
OLEH: OLEH: KELOMPOK VII KELOMPOK VII Yogyakarta, 10 Septembr 2013 Yogyakarta, 10 Septembr 2013 Anggota: Anggota: Nama
Nama NIM NIM Tanda TanganTanda Tangan
___________
______________________________________________________________________________________________________________ ___________
Anggun
Anggun Andreyani Andreyani `1230814100`123081410011
Ditya farastuti Ditya farastuti
Nurfitriana Dewi Nurfitriana Dewi
Dwiana Muflihah Yulianti Dwiana Muflihah Yulianti
Ika Pratiwi Ika Pratiwi
Mengetahui, Mengetahui,
Dosen Pembimbing/ Asisten Praktikum Dosen Pembimbing/ Asisten Praktikum
(...
(...)..) Diserahkan pada tanggal 17 September 2013,
Diserahkan pada tanggal 17 September 2013, pukul 13.00 WIB
DIFUSI-OSMOSIS DAN PENYERAPAN ZAT
Kegiatan 1
„DAPATKAH AIR BEROSMOSIS MENEMBUS MEMBRAN SEL JARINGAN TUMBUHAN‟
I. Tujuan penulisan
Setelah melakukan percobaan dapat:
1. Menemukan fakta mengenai gejala difusi-osmosis
2. Mengamati efek konsentrasi larutan terhadap kecepatan difusi 3. Menunjukkan arah gerakan air pada peristiwa difusi osmosis 4. Mendeskripsikan pengertian difusi osmosis
II. Tinjauan pustaka
1. Difusi
Difusi merupakan proses perpindahan atau pergerakan molekul zat atau gas dari konsentrasi tinggi ke konsentrasi rendah. Difusi melalui membran dapat berlangsung melalui tiga mekanisme, yaitu difusi sederhana (simple difusion), difusi melalui saluran yang terbentuk oleh protein transmembran (simple difusion by chanel formed), dan difusi difasilitasi (fasiliated difusion). Difusi melalui
membrane berlangsung karena molekul -molekul yang berpindah atau bergerak melalui membran bersifat larut dalam lemak (lipid) sehingga dapat menembus lipid bilayer pada membran secara langsung. Membran sel permeabel terhadap molekul larut lemak seperti hormon steroid, vitamin A, D, E, dan K serta bahan- bahan organik yang larut dalam lemak, Selain itu membran sel juga sangat permeabel terhadap molekul anorganik seperti O,CO2, HO, dan H2O. Beberapa
molekul kecil khusus yang terlarut dalam serta ion-ion tertentu, dapat menembus membran melalui saluran atau chanel. Saluran ini terbentuk dari protein transmembran, semacam pori dengan diameter tertentu yang memungkinkan molekul dengan diameter lebih kecil dari diameter pori tersebut dapat melaluinya. Sementara itu, molekul – molekul berukuran besar seperti asam amino, glukosa, dan beberapa garam – garam mineral , tidak dapat menembus membrane secara langsung, tetapi memerlukan protein pembawa atau transporter untuk dapat menembus membrane.
Ada beberapa faktor yang mempengaruhi kecepatan difusi, yaitu :
a. Ukuran partikel. Semakin kecil ukuran partikel, semakin cepat partikel itu akan bergerak, sehinggak kecepatan difusi semakin tinggi.
b. Ketebalan membran. Semakin tebal membran, semakin lambat kecepatan difusi.
c. Luas suatu area. Semakin besar luas area, semakin cepat kecepatan difusinya. d. Jarak. Semakin besar jarak antara dua konsentrasi, semakin lambat kecepatan difusinya.
e. Suhu. Semakin tinggi suhu, partikel mendapatkan energi untuk bergerak dengan lebih cepat. Maka, semakin cepat pula kecepatan difusinya.
Dalam mengambil zat-zat nutrisi yang penting dan mengeluarkan zat-zat yang tidak diperlukan, sel melakukan berbagai jenis aktivitas, dan salah satunya adalah difusi. Ada dua jenis difusi yang dilakukan, yaitu difusi biasa dan difusi khusus. Difusi biasa terjadi ketika sel ingin mengambil nutrisi atau molekul yang hydrophobic atau tidak berpolar / berkutub. Molekul dapat langsung berdifusi ke dalam membran plasma yang terbuat dari phospholipids. Difusi seperti ini tidak memerlukan energi atau ATP(Adenosine Tri-Phosphate). Difusi khusus terjadi ketika sel ingin mengambil nutrisi atau molekul yang hydrophilic atau berpolar dan ion. Difusi seperti ini memerlukan protein khusus yang memberikan jalur kepada partikel-partikel tersebut ataupun membantu dalam perpindahan partikel. Hal ini dilakukan karena partikel-partikel tersebut tidak dapat melewati membran plasma dengan mudah. Protein-protein yang turut campur dalam difusi khusus ini biasanya berfungsi untuk spesifik partikel.
2. Osmosis
Osmosis adalah proses perpindahan atau pergerakan molekul zat pelarut, dari larutan yang konsentrasi zat pelarutnya tinggi menuju larutan yang konsentrasi zat pelarutya rendah melalui selaput atau membran selektif permeabel atau semi permeabel. Jika di dalam suatu bejana yang dipisahkan oleh selaput semipermiabel, jika dalam suatu bejana yang dipisahkan oleh selaput semipermiabel ditempatkan dua Iarutan glukosa yang terdiri atas air sebagai pelarut dan glukosa sebagai zat terlarut dengan konsentrasi yang berbeda dan dipisahkan oleh selaput selektif permeabel, maka air dari larutan yang berkonsentrasi rendah akan bergerak atau berpindah menuju larutan glukosa yang konsentrasinya tinggi melalui selaput permeabel. Jadi, pergerakan air berlangsung dari larutan yang konsentrasi airnya tinggi menuju kelarutan yang konsentrasi airnya rendah melalui selaput selektif permiabel. Larutan vang konsentrasi zat terlarutnya lebih tinggi dibandingkan dengan larutan di dalam sel dikatakan sebagai larutan hipertonis. Sedangkan larutan yang konsentrasinya sama dengan larutan di dalam sel disebut larutan isotonis. Jika larutan yang terdapat di luar sel, konsentrasi zat terlarutnya lebih rendah daripada di dalam sel dikatakan sebagai larutan hipotonis. Apakah yang terjadi jika sel tumbuhan atau hewan, misalnya sel darah merah ditempatkan dalam suatu tabung yang berisi larutan dengan sifat larutan yang berbeda-beda? Pada larutan isotonis, sel tumbuhan dan sel darah merah akan tetap normal bentuknya. Pada larutan hipotonis, sel tumbuhan akan mengembang dari ukuran normalnya dan mengalami peningkatan tekanan turgor sehingga sel menjadi keras. Pada larutan hipertonis, sel tumbuhan akan kehilangan tekanan turgor dan mengalami plasmolisis (lepasnya membran sel dari dinding sel). (http://kireidwi.blog.friendster.com/2008/09/mekanisme-difusi-dan-osmosis-dalam-sel/).
Osmosis merupakan suatu fenomena alami, tapi dapat dihambat secara buatan dengan meningkatkan tekanan pada bagian dengan konsentrasi pekat menjadi melebihi bagian dengan konsentrasi yang lebih encer. Gaya per unit luas yang dibutuhkan untuk mencegah mengalirnya pelarut melalui membran
permeabel selektif dan masuk ke larutan dengan konsentrasi yang lebih pekat sebanding dengan tekanan turgor. Tekanan osmotik merupakan sifat koligatif, yang berarti bahwa sifat ini bergantung pada konsentrasi zat terlarut, dan bukan pada sifat zat terlarut itu sendiri.Osmosis terbalik adalah sebuah istilah teknologi
yang berasal dari osmosis. Osmosis adalah sebuah fenomena alam dalm sel hidup di mana molekul solvent (biasanya air) akan mengalir dari daerah solute rendah ke daerah solute tinggi melalui sebuah membran semipermeable. Membran semipermeable ini menunjuk ke membran sel atau membran apa pun yang memiliki struktur yang mirip atau bagian dari membran sel. Gerakan dari solvent berlanjut sampai sebuah konsentrasi yang seimbang tercapai di kedua sisi membran.Dua faktor penting yang mempengaruhi osmosis adalah: Kadar air dan materi terlarut yang ada di dalam sel serta Kadar air dan materi terlarut yang ada di luar sel. (http://nurmaatus.blogdetik.com/category/biologi/)
III. Metode praktikum
1) Waktu dan tempat pelaksanaan
Waktu : Selasa, 9 September 2013 Tempat : Laboratorium Biokimia
2) Alat dan bahan
Alat
1. Pelubang 2. Cawan petri 3. Pisau tajam
4. Pipa kaca berskala 5. Serbet
6. Karet penyumbat 7. Penggaris
Bahan
1. Kentang
2. Larutan gula sukrosa (50% dan 100%)
3) Prosedur percobaan
Osmosis dengan membran kentang
Memotong kentang berbentuk kubus
Memasukkan larutan gula pada sumuran sampai sampai setengah dari lubang sumuran
Membuat dua sumuran dengan pelubang sampai setengah dari ketinggiaan kubus
Menutup lubang sumuran dengan karet penyumbat sampai ketinggian pada skala terlihat
IV. Hasil dan pembahasan
Tabel data praktikum kelompok VII
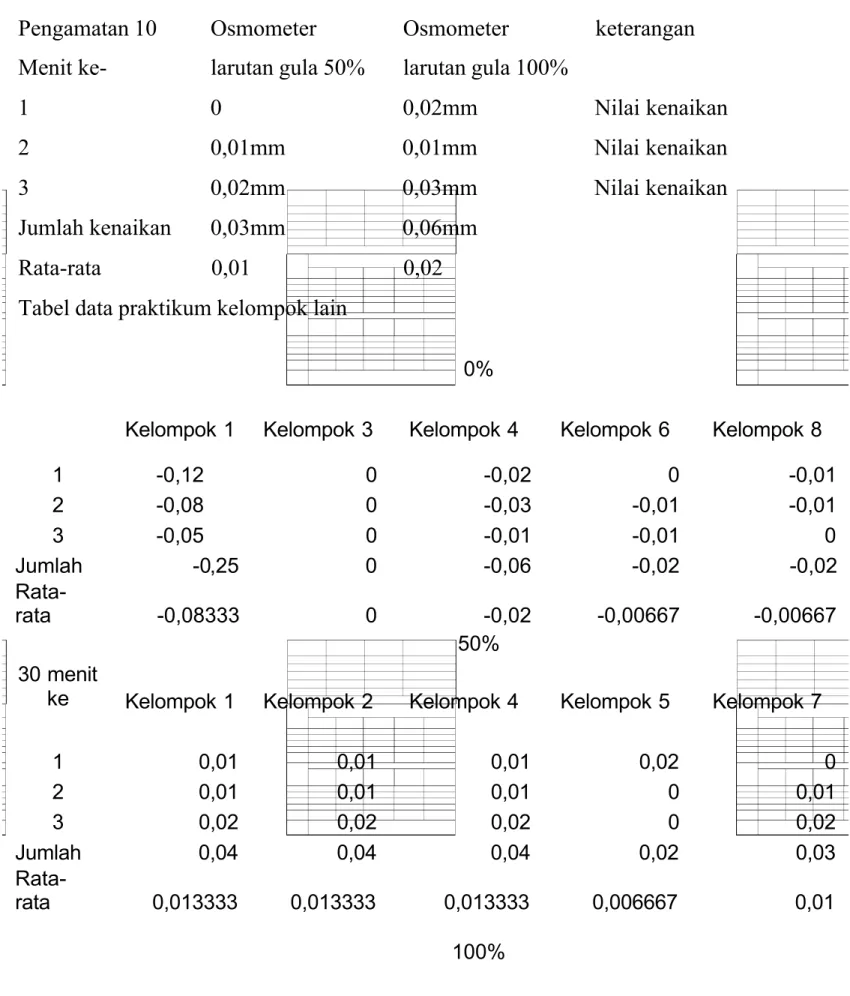
Pengamatan 10 Menit ke-Osmometer larutan gula 50% Osmometer larutan gula 100% keterangan 1 0 0,02mm Nilai kenaikan 2 0,01mm 0,01mm Nilai kenaikan 3 0,02mm 0,03mm Nilai kenaikan Jumlah kenaikan 0,03mm 0,06mm Rata-rata 0,01 0,02
Tabel data praktikum kelompok lain
0%
Kelompok 1 Kelompok 3 Kelompok 4 Kelompok 6 Kelompok 8
1 -0,12 0 -0,02 0 -0,01 2 -0,08 0 -0,03 -0,01 -0,01 3 -0,05 0 -0,01 -0,01 0 Jumlah -0,25 0 -0,06 -0,02 -0,02 Rata-rata -0,08333 0 -0,02 -0,00667 -0,00667 30 menit ke 50%
Kelompok 1 Kelompok 2 Kelompok 4 Kelompok 5 Kelompok 7
1 0,01 0,01 0,01 0,02 0 2 0,01 0,01 0,01 0 0,01 3 0,02 0,02 0,02 0 0,02 Jumlah 0,04 0,04 0,04 0,02 0,03 Rata-rata 0,013333 0,013333 0,013333 0,006667 0,01 100%
30 menit ke Kelompok 2 Kelompok 3 Kelompok 5 Kelompok 6 Kelompok 7 Kelompok 8 1 0,01 0 0,01 0,06 0,02 -0,01 2 0,005 0 0,01 0,02 0,01 0 3 0,005 0,01 0,01 0,02 0,03 0,02 Jumlah 0,02 0,01 0,03 0,1 0,06 0,01 Rata-rata 0,006667 0,003333 0,01 0,033333 0,02 0,003333
Pada percobaan osmosis-difusi dan penyerapan zat yang dilakukan melalui beberapa prosedur untuk menemukan semua fakta yang berhubungan dengan gejala difusi-osmosis yaitu kentang dipotong berbentuk kubus kemudian diberi lubang dan diisi dengan larutan gula yang konsentrasinya berbeda yaitu 0%, 50%, dan 100%. Masing-masing kentang yang beisi larutan gula dalam lubangnya direndam dalam preparat yang berisi air, tak lupa dipasang juga osmometer pada lubang kentang, kemudian dihitung ketinggian skala osmometer setiap 10 menit selama 3 kali.
Dari percobaan kelompok kami (kelompok VII) didapatkan data rata-rata kenaikan skala dengan larutan gula 50% adalah 0,01 dan rata-rata dari kenaikan skala dengan larutan gula 100% adalah 0,02 . Sedangkan bila dirata rata dengan hasil praktikum kelompok lain didapat rata-rata kenaikan skala dengan larutan 0% adalah 0.03543. Rata – rata dengan konsentrasi 50% adalah 0,02333, dan rata-rata untuk konsentrasi 100% adalah 0,02277. setelah dilakukan analisis ternyata rata-rata skala yang mengalami kenaikan paling tinggi ada pada konsentrasi 100% dan rata-rata skala paling rendah ada pada konsentrasi 0%.
Berdasarkan hasil praktikum kelompok kami (kelompok VII) ditmukan data yang sesuai dengan teori yaitu bila kita merujuk pada teori yang menyatakan bahwa perpindahan molekul melalui membran semi permeabel dari konsentrasi pelarut tinggi (encer) menuju konsentrasi pelarut rendah dikatakan sebagai peristiwa osmosis. Hal ini sesuai dengan percobaan yang dilakukan terhadap kentang yang dilubangi dan diberi gula dengan konsentrasi pelarut rendah dan
direndam dalam cawan petri yang diisi denga air biasa. Dalam hal ini larutan gula yang dimasukkan ke dalam lubang kentang berperan sebagai bagian yang memiliki konsentrasi pelarut rendah sedangkan air biasa berperan sebagai konsentrasi pelarut tinggi. Sehingga adanya perbedaan konsentrasi pelarut tersebut menyebabkan terjadinya peristiwa osmosis pada percobaan ini.
Perbedaan skala yang ditunjukkan dari masing-masing cawan petri dengan konsentrasi gula pada lubang kentang yang berbeda-beda menuntun kita untuk mengetahui faktor apa yang menyebabkannya dan bagaimana prosesnya. Setelah dilakukan percobaan dan menganalisis dengan referensi yang ada ditemukan satu faktor penting yang menyebabkan skala semakin meningkat mengikuti kenaikan konsentrasi gula. Hal ini sesuai dengan pernyataan Frank B Salisbury dan Cleon W Ross pada bukunya fisiologi tumbuhan jilid I yang menyatakan bahwa “Jika air murni berada di satu sisi membran dan larutan di sisi lainnya (dalam sel), maka potensial-air-larutan akan lebih rendah daripada potensial-air murni. Potensial air
murni pada tekanan atmosfer dan pada suhu yang sama dengan larutn tersebut sama dengan nol, maka karena itu molekul air akan berdifusi dari potensial air lebih tinggi di luar menuju potensial air yang lebih rendah dalam larutan sel. Artinya, air akan berdifusi menurui gradien potensial air ke dalam larutan. Akibatnya tekanan ke dalam sistem menbesar yang menyebabkan naiknya cairan dalam tabung osmometer atau naiknya tekanan pada dinding sel.” Pernyataan tersebut menghasilkan sebuah kesimpulan berdasarkan hasil percobaan yang dilakukan yaitu semakin tinggi konsentrasi gula maka air (di luar sel) akan memberikan tekanan yang lebih besar pula terhadap dinding sel sehingga skalanya pun semakin cepat naik, atau secara ringkasnya semakin tinggi konsentrasi larutan
maka semakin cepat pula naiknya cairan ke dalam tabung osmometer.
Hasil rata-rata praktikum dari setiap kelompok bila dianalisis, terjadi perbedaan hasil dan teori pada rata-rata praktikum kelas kenaikan skala pada
tabung osmometer dengan konsentrasi 0,0% justru mengalami kenaikan yang paling tinggi sebaliknya kenaikan pada konsentrasi 100% mengalami kanaikan yang paling kecil. Hal ini diduga karena terjadi kesalahan pada saat prktikum yaitu
mungkin saja trjadi kebocoroan pada lubang kentang akibat kurang teliti dan kurang terampilnya praktikan dalam melubangi kentang.
V. Kesimpulan dan saran
a. kesimpulan
1. pada percobaan tersebut menunjukkan peristiwa osmosis
2. semakin tinggi konsentrasi larutan, maka kecepatan difusi semakin tinggi
3. arah gerakan air pada peristiw osmosis adalah dari konsentrasi pelarut tinggi menuju ke konsentrasi pelarut rendah.
4. osmosis adalah peristiwa berpndahnya molekul-molekul air dari konsentrasi pelarut tinggi menuju ke konsentrasi pelarut rendah.
5. difusi adalah peristwa berpindahnya molekul-molekul zat (padat, cair, gas) dari konsentrasi lartan tinggi menuju konsentrasi larutan rendah.
b. Saran
Pada percobaan Difusi-Osmosis dan Penyerapan Zat saran yang dapat kami kemukakan demi meningkatnya kualitas praktikum dikemudian hari yaitu bahan yang disediakan khususnya kentang hendaknya lebih dari dua. Hal ini sebagai salah satu antisipasi jika terjadikesalahan. Koordinasi hasil praktikum dari masing-masing kelompok lebih ditekankan demi mempermudah penyelesaian pembuatan laporan resmi.
VI. Diskusi
1. Apakah potensial air 1 mol larutan garam (NaCl) sama dengan 1 mol larutan Glukosa?
Jawab: tidak, karena potensial air merupakan tingkat kemampuan molekul-molekul air untuk melakukan difusi , yang mana bergerak da ri potensial tinggi ke potensial rendah(encer menuju ke larutan pekat)
sehingga berkaitan erat dengan potensial osmotik. Potensial osmotik
= n.M.R.T. Maka potensial osmotik NaCl tidak sama dengan glukosa karna ion (n) berbedapada NaCl jumlah ion sebanyak 2 dan glukosa tidak memilki ion (n). Oleh sebab itu tekanan osmotik NaCl lebih besar dari pada tekan osmotik glukosa dan hal ini juga menyeababkan terjadinya perbedaan potensial osmotik diantara keduanya.
2. Apakah laju difusi air dari jaringan kentang dipengaruhi oleh jenis larutan perendamanya?
Jawab: iya, karena jenis larutan perendamnya memiliki konsentrasi zat(potensial kimia) yang berbeda. Hala ini lah yang akan memepengaruhi kecpatan difusi-osmosis.
3. Apa yang akan terjadi bila jaringan kentang ditempatkan pada larutan dengan potensial osmotiknya lebih rendah dari potensial osmotik cairan jaringannya?
Jawab: maka akan terjadi pergerakn molekul air dari jaringan kentang menuju sistem yang merendamnya. Larutan yang ada dalam kentang akan berkurang bahkan habis sehingga akan mengalami dehidrasi, dan terjadi pristiwa lpasnya plasmalema atau membran plasma dari dinding sel atau yang lebih dikenal dengan plasmolisis.
VII. Daftar Pustaka
Dwijoseputro.1986. Pengantar Fisiologi Tumbuhan. Jakarta : Gramedia
Lakitan, Benyamin.1993. Dasar-Dasar Fisiologi Tumbuhan. Jakarta : PT Raja Garafindo Persada
Salisbury,F.B. dan Cleon W.R. 1995. Fisiologi Tumbuhan, jilid 1. Bandung: ITB http://kireidwi.blog.friendster.com/2008/09/mekanisme-difusi-dan-osmosis-dalam-sel/
Kegiatan 2
“MENGUKUR POTENSIAL OSMOTIK DAN POTENSIAL AIR JARINGAN”
I. Tujuan Praktikum
Mengetahui nilai potensial air pada umbi kentang
II. Tinjauan Pustaka
Dalam tanah dan tubuh tumbuhan tingkah laku dan pergerakan air didasarkan atas suatu hubungan energi potensial. Air mempunyai kapasitas untuk melakukan kerja, yaitu akan bergerak dari daerah dengan energi potensial tinggi ke daerah dengan energi potensial rendah. Energi potensial dalam sistem cairan dinyatakan dengan cara membandingkannya dengan energi potensial air murni. Secara kimia, air dalam tumbuhan dan tanah biasanya tidak murni itu disebabkan oleh adanya bahan terlarut dan secara fisik dibatasi oleh berbagai gaya, seperti gaya tarik-menarik yang berlawanan, gravitasi, dan tekanan. Maka dari itu energi potensialnya lebih
kecil dari pada energi potensial air murni (Gardner, 1991).
Potensial Air merupakan energi yang dimiliki air untuk bergerak atau untuk mengadakan reaksi. Dengan kata lain, potensial air merupakan tingkat kemampuan molekul-molekul air untuk melakukan difusi. Pada potensial air, air bergerak dari potensial tinggi ke potensial rendah (dari
larutan encer ke larutan pekat, larutan encer lebih banyak mengandung air daripada larutan pekat).
Dalam fisiologi tumbuhan, potensial kimia air atau potensial air (PA) merupakan konsep yang sangatpenting. Ralph O. Slatyer (Australia) dan Sterling A Taylor (Utah State University) pada tahun 1960, mengusulkan
bahwa potensial air digunakan sebagai dasar untuk sifat air dalam sistem tumbuhan-tanah-udara. Potensial air merupakan sesuatu yang sama dengan potensial kimia air dalam suatu sistem, dibandingkan dengan potensial
kimia air murni pada tekanan atmosfir dan suhu yang sama. Mereka menganggap bahwa PA air murni dinyatakan sebagai (0) nol (merupakan konvensi) dengan satuan dapat berupa tekanan (atm, bar) atau satuan energi. Difusi air melintasi membran semipermeabel dinamakan osmosis. Molekul air dapat berdifusi secara bebas melintasi membran, dari larutan dengan gradien konsentrasi larutan rendah ke larutan dengan gradien konsentrasi larutantinggi (Ismail, 2006).
Status energi bebas air adalah suatu pernyataan Potensial air, suatu ukuran daya yang menyebabkan air bergerak kedalam suatu sistem, seperti jaringan tumbuhan, jaringan tumbuhan, tanah atau atmosfir, atau suatu bagian dari bagian lain dalam suatu sistem. (Ismail, 2009).
Osmosis merupakan difusi air yang melintasi membran semipermeabel dari daerah dimana air lebih banyak ke daerah yang lebih sedikit . Osmosis sangat ditentukan oleh potensial kimia air atau potensial air , yang menggambarkan kemampuan molekul air untuk dapat melakukan difusi. Sejumlah besar volume air akan memiliki kelebihan energi bebas daripada volume yang sedikit, di bawah kondisi yang sama. Energi bebas zuatu zat per unit jumlah, terutama per berat gram molekul (energi bebas mol-1) disebut potensial kimia. Potensial kimia zat terlarut kurang lebih sebanding dengan konsentrasi zat terlarutnya. Zat terlarut yang berdifusi cenderung untuk bergerak dari daerah yang berpotensi kimia lebih
tinggi menuju daerah yang berpotensial kimia lebih kecil (Ismail, 2006). Osmosis adalah difusi melalui membran semipermeabel. Contoh proses osmosis adalah masuknya larutan ke dalam sel-sel endodermis. Dalam tubuh organisme multiseluler, air bergerak dari satu sel ke sel lainnya dengan bebas. Selain air, molekul-molekul yang berukuran kecil seperti
O2 dan CO2juga mudah melewati membran sel. Molekul-molekul tersebut akan berdifusi dari daerah dengan konsentrasi tinggi ke konsentrasi rendah. Jika telah mencapai keseimbangan konsentrasi zat di kedua sisi membran maka proses osmosis akan berhenti. (Anonim, 2009).
Prinsip osmosis: transfer molekul solvent dari lokasi hypotonic (potensi rendah) solution menuju hypertonic solution, melewati membran. Jika lokasi hypertonic solution kita beri tekanan tertentu, osmosis dapat berhenti, atau malah berbalik arah (reversed osmosis).Besarnya tekanan yang dibutuhkan untuk menghentikan osmosis disebut sebagai osmotic press.Jika dijelaskan sebagai konseptermodinamika, osmosis dapat
dianalogikan sebagai proses perubahan entrropi. Komponen solvent murni memiliki entropi rendah, sedangkan komponen berkandunagn solut tinggi memiliki entropi yg tinggi juga. Mengikuti Hukum Termo II: setiap perubahan yang terjadi selalu menuju kondisi entropi maksimum, maka solvent akan mengalir menuju tempat yg mengandung solut lebih banyak, sehinggatotal entropi akhir yang diperoleh akan maksimum. Solvent akan kehilangan entropi, dan solut akan menyerap entropi. "Orang miskin akan semakin miskin, sedang yang kaya akan semakin kaya". Saat kesetimbangan tercapai, entropi akan maksimum, atau gradien (perubahan entropi terhadap waktu) = 0. Ingat: pada titik ekstrim, dS/dt = 0 (Wibosono, 2009).
Plasmolisis adalah suatu proses lepasnya protoplasma dari dinding sel yang diakibatkan keluarnya sebagian air dari vakuola (Salisbury and Ross, 1992). Menurut Tjitrosomo (1987), jika sel dimasukan ke dalam larutan gula, maka arah gerak air neto ditentukan oleh perbedaan nilai potensial air larutan dengan nilainya didalam sel. Jika potensial larutan lebih tinggi, air akan bergerak dari luar ke dalam sel, bila potensial larutan lebih rendah maka yang terjadi sebaliknya, artinya sel akan kehilangan air. Apabila kehilangan air itu cukup besar, maka ada kemungkinan bahwa volum sel akan menurun demikian besarnya sehingga tidak dapat mengisi seluruh ruangan yang dibentuk oleh dinding sel. Membran dan sitoplasma akan
terlepas dari dinding sel, keadaan ini dinamakan plasmolisis. Semakin tinggi konsentrasi larutan maka semakin banyak sel yang mengalami plasmolisis.
Membran protoplasma dan sifat permeabel deferensiasinya dapat diketahui dari proses plasmolisis. Permeabilitas dinding sel terhadap larutan gula diperlihatkan oleh sel-sel yang terplasmolisis. Apabila ruang bening diantara dinding dengan protoplas diisi udara, maka dibawah mikroskop akan tampak di tepi gelembung yang berwarna kebiru-biruan. Jika isinya air murni maka sel tidak akan mengalami plasmolisis. Molekul gula dapat berdifusi melalui benang-benang protoplasme yang menembus lubang-lubang kecil pada dinding sel. Benang-benang tersebut dikenal dengan sebutan plasmolema, dimana diameternya lebih besar daripada molekul tertentu sehingga molekul gula dapat masuk dengan mudah (Salisbury, 1995).
Keadaan volume vakuola dapat untuk menahan protoplsma agar tetap menempel pada dinding sel sehingga kehilangan sedikit air saja akan berakibat lepasnya protoplasma dari dinding sel. Peristiwa plasmolisis seperti ini disebut plasmolisis insipien. Plasmolisis insipien terjadi pada jaringan yang separuh jumlahnya selnya mengalami plasmolisis. Hal ini terjadi karena tekanan di dalam sel = 0. potensial osmotik larutan penyebab plasmolisis insipien setara dengan potensial osmotik di dalam sel setelah
keseimbangan dengan larutan tercapai (Salisbury and Ross, 1992). Untuk menghitung nilai potensial osmotiknya menggunakan rumus
keterangan:
M: molaritas larutan sukrosa
I: kostanta ionisasi, untuk sukrosa =1 R: kontanta gas
III. Metode praktikum
1. Waktu dan tempat pelaksanaan
Waktu : Selasa, 9 September 2013 Tempat : Laboratorium Biokimia
2. Alat dan Bahan
Alat : 1. Pelubang gabus 2. Cawan petri 3. Pisau tajam 4. Label 5. penggaris Bahan 1. Kentang
2. Larutan sukrosa (0,0 ;0,4 ;0,8; 1,2; 1,6; dan 2 molar)
3. Prosedur
Mengukur potensial osmotik
Memasukkan masing-masing 3 potong kentang kedalam larutan sukrosa 0 ,0 M dan 2,0 M
IV. Hasil dan Pembahasan
Data Hasil Praktikum Klompok VII
NO PANJANG KENTANG
0,0M 2,0 M
1 0,3CM 0,4 CM
2 0,3CM 0,1 CM
3 0,3CM 0 CM
RATA-RATA 0,3CM 0,16 CM
Data hasil praktikum kelompok lain
KELOMPOK PERTAMBAHAN PANJANG
0 M 0,4 M 0,8 M 1,2 M 1,6 M 2 M 1 0,2 0,4 - - - -0,3 0,4 - - - -0 0,2 - - - -2 - - 0,1 0,2 - -- - 0,1 0,2 - -- - 0,1 0,2 - -3 - - - - 0,2 0,3 - - - - 0,1 0,2 - - - - 0,2 0,2 4 0 0,1 - - - -0,1 0,1 - - - -0,2 0,1 - - - -5 - - 0,1 0,2 - -- - 0,1 0,2 - -- - 0,1 0,2 - -6 - - - - 0,4 0,4
Menutup rapat cawan petri dengan cover glass selama 30 menit
- - - - 0,2 0,3 - - - - 0,1 0,4 7 0,3 - - - - 0,4 0,3 - - - - 0,1 0,3 - - - - 0 8 - 0,3 - -0,2 - -- 0,1 - -0,1 - -Rata-rata - 0,1 - 0 - -0,188889 0,2 0,1 0,1 0,2 0,255556
Menghitung potensial osmotik rumus
keterangan:
M: molaritas larutan sukrosa
I: kostanta ionisasi, untuk sukrosa =1 R: konstanta gas(0,0831 bar/drajat)
T: suhu absolute (celcius +273)) suhu kamar=27
1. Potensial osmotik pada konsentrasi 0,0 M
= 0 atm
2. Potensial osmotik pada konsntrasi 0,4M
= 9,972 atm 3. Potensial osmotik pada konsntrasi 0,8M
= 19,944atm 4. Potensial osmotik pada konsntrasi 1,2 M
= 29,916atm 5. Potensial osmotik pada konsntrasi 1,6M
= 39,888atm 6. Potensial osmotik pada konsntrasi 2,0M
= 49,86atm
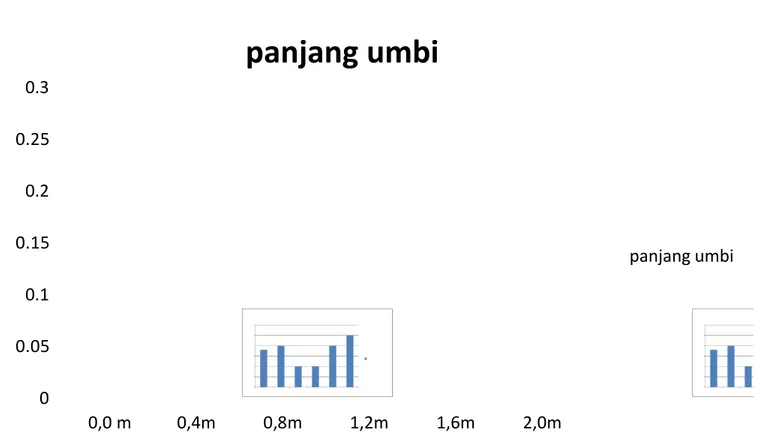
Grafik hubungan antara ukuran panjang umbi (sumbu y) dengan konsentrasi sukrosa (sumbu x) 0 0.05 0.1 0.15 0.2 0.25 0.3 0,0 m 0,4m 0,8m 1,2m 1,6m 2,0m
panjang umbi
panjang umbiPada percobaan mengukur potensial osmotik dan potensial air jaringan yang dilakukan melalui beberapa prosedur untuk mengetahui nilai potensial air pada umbi kentang yaitu membuat silinder umbi kentang dengan menggunakan pelubang gabus dengan ukuran 4 cm, kemudian masing-masing 3 potong silinder
kentang dimasukkan ke dalam cawan petri yang berisi larutan sukrosa : 0,0 M ; 0,4 M ; 0,8 M ; 1,2 M ; 1,6 M ; 2,0 M (kelompok VII hanya mengerjakan pada konsentarsi 0,0 M dan 2,0 M). Selanjutnya menutup cawan petri selama 30 menit. Setelah itu mengambil silinder kentang dan mengukur panjangnya.
Dari percobaan tersebut didapatkan data rata-rata panjang kentang setelah direndam di dalam cawan petri yang berisi larutan sukrosa yang berbeda-beda molaritasnya. Pada praktikum yang dilakukan kelompok VII didapat hasil yaitu terjadi perubahan panjang umbi kentang dari kelompok kontrol yaitu larutan dengan konsentrasi sukrosa 0,0 M . Perubahan panjang umbi kentang dengan larutan sukrosa 0,0 M adalah 0,3 cm. Sedangkan rata-rata penambahan panjang umbi kentang dari hasil praktikum setiap kelompok di kelas yaitu, 0,188889 untuk konsentrasi larutan 0,0M, pada konsentrasi 0,4 M rata-rata perubahan panjangnya 0,2, larutan dengan konsentrasi 0,8 adalah 0,1, perubahan panjang pada larutan dengan konsentrasi 1,2 M panjangnya 0,1, rata-rata pada larutan 1,6 M adalah 0,2 serta panjang umbi kentang dengan konsentrasi 2,0 M sebesar 0,25. Jadi terjadi perubahan panjang potongan kentang pada kelompok kontrol dan perlakuan srta
terjadi perubahan juga pada setiap perlakuan.
Setelah dianalisis, ternyata hasil percobaan menunjukkan kentang mengalami pemanjangan yang lebih panjang pada konsentrasi 0,0 M atau konsntrasi kimia rendah. Hal ini sesuai dengan teori yang menyatakan bahwa komponen potensial dalam potensial air mengacu pada energi potensial, yaitu kapasitas untuk melakukan kerja ketika air bergerak dari daerah dengan potensial air lebih tinggi ke daerah dengan potensial air lebih rendah . Hal ini mnunjukkan bahwa potensial air pada larutan sukrosa lebih tinggi daripada potensial air pada kentang, sehingga peristiwa yang terjadi adalah peristiwa osmosis bahwa air pada larutan sukrosa mengalir masuk pada jaringan. Sehingga kentang tersebut dapat menyerap larutan sukrosa saat perendaman dan bertambah panjang. Adanya
peristiwa osmosis berhubungan erat dengan potensial osmotik yaitu kemampuan molekul air untuk melakukan pristiwa osmosis. Penambahan panjang terbesar dialami oleh kentang yang dirndam pada konsentrasi 0,0 M dan penambahan panjang kentang paling rendah pada konsntrasi 2,0 M. Hal ini tentunya dipengaruhi oleh potensial osmotik dari masing-masing larutan. Pada larutan sukrosa 0,0 M tentunya potensial airnya lebih tinggi dan tekanan osmotiknya pun demikian. Pada setiap perlakuan terjadi prubahan panjang jika tidak terjadi perubahan volume atau panjang maka status potensial air pada jaringan kentang terhadap larutan perendam sama, sehingga terjadi kondisi isotonik dan mencapai kesetimbangan. Bila potnsial osmotik jaringan ditaksir dari larutan perendamnya, dimana tidak menimbulkan perubahan panjang potongan kentang, maka nilai potensial osmotik jaringan tersebut sama dengan nol. Jadi kesimpulan semakin
tinggi konsentrasi zat nya maka penambahan panjang atau penamahan volume kentang semakin kecil .
V. Kesimpulan dan Saran a. Kesimpulan
Nilai potensial air =potensial tekanan+potensial osmotik. Potensial tekanan ditetapkan samadengan nol pada tekanan atmosfer dan potensial osmotik selalu negatif atau nol pada air murni. Sehingga nilai potensial air sama dngan potnsial osmotiknya, yaitu pada konsentari 0,0 M sebesar 0 atm, potensial osmotik pada konsntrasi 0,4M sama dengan 9,972 atm, potensial osmotik pada konsntrasi 0,8M samadengan 19,944atm, potensial osmotik pada konsntrasi 1,2 M sama dngan 29,916atm, potensial osmotik pada konsntrasi 1,6M samadengan 39,888atm dapotensial osmotik pada
konsntrasi 2,0M samadengan 49,86atm. b.Saran
saran yang dapat praktikan sampaikan pada praktikum ini adalah koordinasi untuk penyerahn hasil praktikum lebih ditingkatkan agar penyelesaian laporan juga bisa lancar.
VI. Diskusi
1. Berapakah potensial osmotik larutan sukrosa pada suhu yang percobaan saudara?
Jawab:
Potensial osmotik pada konsentrasi 0,0 M
= 0 atm
Potensial osmotik pada konsntrasi 0,4M
= 9,972 atm
Potensial osmotik pada konsntrasi 0,8M
= 19,944atm
Potensial osmotik pada konsntrasi 1,2 M
= 29,916atm
Potensial osmotik pada konsntrasi 1,6M
= 39,888atm
Potensial osmotik pada konsntrasi 2,0M
= 49,86atm
2. Apa yang akan terjadi bila jaringan kentang ditempatkan pada larutan yang potensial osmotiknya rendah lebih rendah dari potensial osmotik jaringannya?
Jawab: larutan yang ada didalam kentang akan mennglami dehidrasi dan menjurus pada pristiwa plasmolisis.
VIII. Daftar Pustaka
Dwijoseputro.1986. Pengantar Fisiologi Tumbuhan. Jakarta : Gramedia
Lakitan, Benyamin.1993. Dasar-Dasar Fisiologi Tumbuhan. Jakarta : PT Raja Garafindo Persada
Salisbury,F.B. dan Cleon W.R. 1995. Fisiologi Tumbuhan, jilid 1. Bandung: ITB http://kireidwi.blog.friendster.com/2008/09/mekanisme-difusi-dan-osmosis-dalam-sel/