i
PEMANFAATAN PEKTIN KULIT PISANG KEPOK
(Musa paradisiaca Linn) UNTUK PEMBUATAN
EDIBLE FILM
Skripsi
disajikan sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains Program Studi Kimia
oleh Rofikah 4350408018
JURUSAN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS NEGERI SEMARANG
ii
karya sendiri, bukan jiplakan dari karya orang lain, baik sebagian maupun seluruhnya. Pendapat atau temuan orang lain yang terdapat dalam Skripsi ini dikutip atau dirujuk berdasarkan kode etik ilmiah.
Semarang, Maret 2013 Penyusun,
Rofikah
iii
PERSETUJUAN PEMBIMBING
Skripsi dengan judul “Pemanfaatan Pektin dari Kulit Pisang Kepok (Musa Paradisiaca Linn) Untuk Pembuatan Edible Film” telah disetujui oleh dosen pembimbing untuk diajukan ke sidang Panitia Ujian Skripsi Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Semarang.
Semarang, Maret 2013
Pembimbing I Pembimbing II
Ir. Winarni Pratjojo, M.Si Dra. Woro Sumarni, M.Si
iv
PENGESAHAN
Skripsi yang berjudul
Pemanfaatan Pektin dari Kulit Pisang Kepok (Musa paradisiaca Linn) Untuk Pembuatan Edible Film
disusun oleh
Nama : Rofikah NIM : 4350408018
telah dipertahankan di hadapan sidang Panitia Ujian Skripsi Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Semarang pada tanggal 15 Maret 2013.
Panitia Ujian :
Ketua Sekretaris
Prof. Dr. Wiyanto, M.Si. Dra. Woro Sumarni, M.Si.
NIP. 196310121988031001 NIP. 196507231993032001
Ketua Penguji
Dra. Sri Mantini Rahayu S, M.Si
NIP. 195010171976032001
Anggota Penguji/ Anggota Penguji/
Pembimbing Utama Pembimbing Pendamping
Ir. Winarni Pratjojo, M.Si Dra. Woro Sumarni, M.Si. NIP. 194808211976032001 NIP. 196507231993032001
v
MOTTO DAN PERSEMBAHAN
Motto:
Jangan pernah lelah untuk bangun dari setiap jatuhmu, dan Jangan pernah lelah untuk belajar dan menjadi lebih baik.
Ketika kamu membuka matamu pagi ini kamu punya 2 pilihan: 1. Kembali tidur dan bermimpi; atau 2. Bangun & mengejar mimpimu.
Sukses bukan datang dari uang atau ketenaran, tapi dari arti hidupmu, lakukan yang kamu senangi, & tekun menjalaninya.
Kenanglah masa lalu, persiapkan rencana masa depan tapi hiduplah untuk hari ini.
Persembahan:
Dari hati terdalam, karya kecil ini kupersembahkan pada :
Ibu dan Bapak untuk setiap lantunan doa, kesabaran dan perjuangan yang tak henti untukku.
Mas-Mbak-adekku dan segenap keluarga besarku untuk segala bentuk perhatian dan cinta.
Orang yang aku sayang Mahardika Sukma Pribadi, S.Kep untuk perhatian, kesabaran dan kasih sayang hingga karya ini tersusun.
Sahabat-sahabatku di “YEOJA KOST” untuk semangat dan motivasi yang diberikan.
Teman-teman seperjuanganku Big Family of Chemistry „08 untuk pengalaman yang sangat berharga.
vi
KATA PENGANTAR
Alhamdulillah, puji syukur penulis haturkan kepada Allah SWT atas limpahan rahmat dan karunia-Nya, sehingga penulis dapat menyelesaikan Skripsi dengan judul ”Pemanfaatan Pektin Kulit Pisang Kepok (Musa pradisiaca Linn) Untuk Pembuatan Edible Film”.
Penulis mengucapkan terima kasih kepada semua pihak yang telah membantu, baik dalam penelitian maupun penyusunan Skripsi ini. Ucapan terima kasih terutama disampaikan kepada:
1. Rektor Universitas Negeri Semarang
2. Dekan FMIPA UNNES untuk arahan dan bimbingan sehingga Skripsi ini dapat terselesaikan.
3. Ketua Jurusan Kimia, FMIPA UNNES untuk petunjuk dan arahan sehingga Skripsi ini dapat terselesaikan.
4. Ibu Ir. Winarni Pratjojo, M.Si., Dosen Pembimbing I untuk masukan dan arahan dalam penyusunan Skripsi ini.
5. Ibu Dra. Woro Sumarni, M.Si., Dosen Pembimbing II yang telah memberikan ilmu, petunjuk, bimbingan dengan sabar dalam pelaksanaan penelitian dan penyusunan Skripsi ini.
6. Ibu Dra. Sri Mantini Rahayu S, M.Si., Dosen Penguji utama yang telah memberikan pengarahan, kritikan membangun sehingga Skripsi ini menjadi lebih baik.
vii
7. Bapak Ibu Dosen Jurusan Kimia FMIPA UNNES yang telah memberikan bekal ilmu kepada penulis.
8. Segenap Karyawan dan Staf Laboratorium untuk bantuan tenaga maupun pikiran, diskusi selama penelitian.
9. Semua pihak yang tidak dapat penulis sebutkan satu per satu, yang telah membantu dalam penelitian, penyusunan Skripsi dan segala hal kepada penulis.
Demikian ucapan terima kasih dari penulis, mudah-mudahan Skripsi ini dapat bermanfaat dan dapat memberikan kontribusi positif bagi khazanah perkembangan ilmu pengetahuan khususnya dalam bidang katalis dan katalisis.
Semarang, Maret 2013
viii
ABSTRAK
Rofikah. 2013. Pemanfaatan Pektin Kulit Pisang Kepok (Musa paradisiaca Linn) Untuk Pembuatan Edible Film. Skripsi, Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Semarang. Pembimbing Utama Ir. Winarni Pratjojo, M.Si. dan Pembimbing Pendamping Dra. Woro Sumarni, M.Si.. Kata kunci: Edible film, Pektin Kulit Pisang Kepok, Gliserol, Tepung Tapioka
Bahan makanan pada umumnya sensitif dan mudah mengalami penurunan kualitas karena faktor lingkungan, sehingga perlu dilakukan upaya pengemasan. Bahan pengemas dari plastik banyak digunakan dengan pertimbangan ekonomis dan memberikan perlindungan yang baik dalam pengawetan. Umumnya plastik kemasan makanan yang digunakan berbahan dasar polimer sintetik polipropilen (PP). Penggunaan polipropilen tersebut berdampak pada pencemaran lingkungan. Oleh karena itu, dibutuhkan produk kemasan yang dapat diuraikan (degradable) untuk dapat menggantikan polipropilen. Salah satu solusinya adalah penggunaan edible film. Edible film dapat disintesis dari bahan baku biopolimer pektin. Pektin dapat diperoleh dari proses ekstraksi kulit pisang kepok. Penambahan plasticizer gliserol dan variasi konsentrasi tepung tapioka dilakukan untuk memperbaiki karakter mekanik edible film pektin kulit pisang kepok, sehingga memenuhi karakter mekanik polipropilen. Pengukuran sifat mekanik edible film pektin kulit pisang kepok digunakan standar ASTM. Hasil rendemen tertinggi ekstraksi pektin kulit pisang kepok adalah 0,8752 g pada suhu 70 oC selama 120 menit (2 jam). Karakterisasi sifat mekanik edible film pektin kulit pisang kepok menunjukkan bahwa penambahan tepung tapioka 0 gram lebih berpengaruh terhadap penambahan nilai persen elongasi dari edible film pektin kulit pisang kepok, sedangkan penambahan tepung tapioka 2,4 gram berpengaruh terhadap nilai kuat tarik edible film pektin kulit pisang kepok. Edible film pektin kulit pisang kepok yang memiliki nilai kuat tarik tertinggi, yaitu 10,53 MPa ditunjukkan oleh edible film pektin kulit pisang kepok dengan penambahan 2,4 gram tepung tapioka dan nilai persen elongasi tertinggi yaitu 20,47% dimiliki oleh edible film pektin kulit pisang kepok dengan penambahan 0 gram tepung tapioka dalam 100 mL larutan pektin. Hasil gugus fungsional FT-IR menunjukkan bahawa ekstraksi yang dihasilkan adalah pektin.
ix
ABSTRACT
Rofikah. 2013. Pectin Utilization Banana Skin kepok (Musa paradisiaca Linn) For Making Edible Films. Thesis, Department of Chemistry Faculty of Mathematics and Natural Sciences Semarang State University. Supervisor I : Ir. Winarni Pratjojo, M.Si. and Supervisor II : Dra. Woro Sumarni, M.Si.
Keywords: Edible films, Pectin kepok Banana Skin, Glycerol, Tapioca Starch Raw foods are generally sensitive and susceptible to degradation due to environmental factors, so we need the effort of packing. Packaging materials of plastic widely used by economic considerations and provides good protection in preservation. Commonly used food packaging made from synthetic polymers polypropylene (PP). The use of polypropylene impact on environmental pollution. Therefore, the required product packaging that can be described (degradable) to replace polypropylene. One solution is the use of edible films. Edible films can be synthesized from raw materials pectin biopolymers. Pectin can be obtained from the extraction process kepok banana peel. The addition of plasticizer glycerol and starch concentration variations made to improve the mechanical character of the banana peel pectin edible film kepok, thus meeting the mechanical character of polypropylene. Measuring mechanical properties of banana peel pectin edible film kepok used ASTM standards. The results of the highest yield of banana peel pectin extraction kepok is 0.8752 g at 70 ° C for 120 minutes (2 hours). Characterization of the mechanical properties of banana peel pectin edible film kepok showed that the addition of starch 0 grams more influence on the value addition per cent elongation of edible film kepok banana peel pectin, whereas the addition of 2.4 grams of tapioca starch affect the value of the tensile strength peel pectin edible film kepok . Edible films kepok banana peel pectin that has the highest tensile strength values, ie 10.53 MPa indicated by a banana peel pectin edible film kepok by the addition of 2.4 grams of tapioca starch and percent elongation highest value 20.47% owned by the skin pectin edible film kepok bananas with the addition of 0 grams of starch in 100 mL of pectin. The results of FT-IR functional group shows that the extraction of pectin is produced.
x
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
PERNYATAAN ... ii
PERSETUJUAN PEMBIMBING ... iii
PENGESAHAN ... iv
MOTTO DAN PERSEMBAHAN ... v
KATA PENGANTAR ... vi
ABSTRAK ... viii
ABSTRACT ... ix
DAFTAR ISI ... x
DAFTAR GAMBAR ... xii
DAFTAR TABEL ... xiii
DAFTAR LAMPIRAN ... xiv
BAB I PENDAHULUAN 1.1 Latar Belakang Masalah ... 1
1.2 Permasalahan ... 6
1.3 Tujuan Penelitian... 6
1.4 Manfaat Penelitian... 7
BAB II TINJAUAN PUSTAKA 2.1 Tinjauan Umum Pisang (Musa paradisiaca) ... 8
2.2 Pisang Kepok (Musa paradisiaca Linn) ... 10
2.3 Pektin ... 11
2.4 Edible Film ... 18
2.5 Ekstraksi Padat-Cair ... 22
2.6 Metode Analisis Spektroskopi FT-IR ... 24
2.7 Karakterisasi Edible Film ... 26
2.8 Penelitian Terdahulu ... 30
BAB III METODE PENELITIAN 3.1 Sampel Penelitian ... 32
xi
3.2 Variabel Penelitian ... 32
3.3 Alat dan Bahan ... 33
3.4 Prosedur Kerja ... 33
3.5 Metode Analisis Data ... 37
BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1 Penyiapan Bahan Baku Kulit Pisang Kepok ... 40
4.2 Ekstraksi Pektin Kulit Pisang Kepok ... 41
4.3 Hasil Ekstraksi Pektin Kulit Pisang Kepok ... 42
4.4 Hasil Uji Gugus Fungsional Pektin ... 44
4.5 Hasil Sintesis Edible Film ... 45
4.6 Hasil Uji Sifat Fisik-Mekanik Edible Film Pektin dari Kulit Pisang Kepok . ………... 47
4.6.1 Hasil Uji Ketebalan Edible Film Pektin Kulit Pisang Kepok . 47 4.6.2 Hasil Uji Kuat Tarik Edible Film Pektin Kulit Pisang Kepok 48 4.6.3 Hasil Uji Persen Elongasi Edible Film Pektin Kulit Pisang Kepok... 50
4.6.4 Hasil Uji Kelarutan Edible Film Pektin Kulit Pisang Kepok .. 52
4.7 Pembahasan ... 54 BAB V PENUTUP 5.1 Simpulan ... 57 5.2 Saran ... 58 DAFTAR PUSTAKA ... 59 LAMPIRAN ... 63
xii
2.1. Pisang kepok ... 10
2.2. Struktur kimia pektin (Asam Poligalakturonat) ... 14
2.3. Perkiraan reaksi tepung tapioka dan gliserol ... 15
2.4. Perkiraan hasil reaksi pektin, gliserol,dan tepung tapioka ... 16
2.5. Struktur gliserol ... 20
4.1. Kurva hubungan suhu dan rendemen ekstraksi pektin ... 43
4.2. Spektrum FT-IR pektin ... 45
4.3. Hasil sintesis edible film pektin ... 46
4.4. Kurva nilai ketebalan edible film pektin ... 48
4.5. Kurva nilai kuat tarik edible film pektin ... 50
4.6. Kurva nilai elongasi edible film pektin ... 52
xiii
DAFTAR TABEL
Tabel Halaman
2.1. Kandungan senyawa dalam pisang ... 9
2.2. Kandungan senyawa dalam kulit pisang ... ... 11
2.3. Komposisi pektin berbagai sayuran dan buah-buahan ... 13
2.4. Kandungan pati pada beberapa bahan pangan ... 22
2.5. Karakteristik rentang frekuensi pada spektrofotometri IR ... 25
2.6. Sifat mekanik dan fisik polipropilen (PP). ... 27
4.1. Ekstraksi pektin dari bubuk kulit pisang kepok ... 44
4.2. Nilai ketebalan edible film pektin ... 47
4.3. Nilai kuat tarik edible film pektin ... 49
4.4. Nilai persen elongasi edible film pektin ... 51
xiv
DAFTAR LAMPIRAN
Lampiran Halaman
1. Diagram alur kerja pembuatan bubuk kulit pisang kepok ... .63
2. Diagram alur kerja ekstraksi pektin dari bubuk kulit pisang kepok.. 64
3. Diagram alur kerja pembuatan edible film dari pektin kulit pisang kepok ... 65
4. Hasil uji FT-IR edible film pektin ... 66
5. Data uji kuat tarik edible film pektin ... 67
6. Data uji elongasi edible film pektin ... 68
7. Perhitungan nilai kuat dan persen elongasi edible film pektin ... 69
1
Bahan makanan pada umumnya sangat sensitif dan mudah mengalami penurunan kualitas karena faktor lingkungan, kimia, biokimia, dan mikrobiologi. Penurunan kualitas tersebut dapat dipercepat dengan adanya oksigen, air, cahaya, dan temperatur. Salah satu cara untuk mencegah atau memperlambat fenomena tersebut adalah dengan pengemasan yang tepat (Wahyu, 2009).
Pengemasan makanan yaitu suatu proses pembungkusan makanan dengan bahan pengemas yang sesuai. Pengemasan dapat dibuat dari satu atau lebih bahan yang memiliki kegunaan dan karakteristik yang sesuai untuk mempertahankan dan melindungi makanan sampai ke tangan konsumen, sehingga kualitas dan keamanannya dapat dipertahankan. Menurut Komolprasert (2006) dalam Wahyu (2009), bahan pengemas yang dapat digunakan antara lain plastik, kertas, logam, dan kaca.
Fungsi dari pengemas pada bahan pangan adalah mencegah atau mengurangi kerusakan, melindungi bahan pangan dari bahaya pencemaran serta gangguan fisik seperti gesekan, benturan dan getaran. Disamping itu pengemasan berfungsi sebagai wadah agar memudahkan dalam penyimpanan, pengangkutan dan pendistribusiannya (Syarief et al.,1988, dalam Harris: 2001).
Bahan pengemas dari plastik banyak digunakan dengan pertimbangan ekonomis dan memberikan perlindungan yang baik dalam pengawetan. Material sintetis yang terdiri dari sekitar 60% polietilen dan 27% dari poliester diproduksi untuk membuat bahan pengemas plastik yang digunakan dalam produk makanan (Wahyu, 2009). Penggunaan material sintetis tersebut berdampak pada pencemaran lingkungan. Plastik akan menjadi sampah yang sulit terurai. “Plastik sintetis yang sering digunakan untuk bahan pengemas makanan adalah produk non-biodegrable sehingga sulit untuk diuraikan,” pakar Ahli Teknologi Pangan dari Institut Pertanian Bogor (IPB), Arif Hartoyo. Limbah plastik baru bisa terurai setelah 1.000 tahun. Dibandingkan dengan limbah kertas yang membutuhkan waktu sebulan untuk terurai.
Perkembangan jenis kemasan telah mengarah ke kemasan baru yang memiliki kemampuan yang baik dalam mempertahankan mutu bahan pangan dan bersifat ramah lingkungan. Salah satu alternatif yang dapat dipertimbangkan untuk tujuan tersebut adalah bahan kemasan edible film (Gontard et al., 1996, dalam Irianto dkk: 2006).
Penggunaan edible film untuk produk pangan dan penguasaan teknologinya masih terbatas. Oleh karena itu perlu dikembangkan penelitian yang lebih intensif, karena edible film sangat potensial digunakan sebagai pembungkus dan pelapis produk-produk pangan, industri, farmasi, maupun hasil pertanian segar.
Edible film merupakan pengemas yang mampu bertindak sebagai penghambat perpindahan uap air dan pertukaran gas (CO2 dan O2),
mempertahankan integrasi struktur bahan, menahan komponen flavor yang muda menguap, dan dapat pula digunakan sebagai pembawa bahan tambahan pangan seperti agensia antimikrobia, antioksidan, dan sebagainya (Baldwin, 1994). Dengan kemampuan yang dimilikinya maka biodegradable film/edible film telah banyak digunakan untuk meningkatkan umur simpan buah-buahan dan sayur-sayuran. Kelebihan lain dari pengemas edible film adalah kemampuannya untuk didegradasi mudah sehingga tidak menimbulkan permasalahan lingkungan seperti sampah plastik yang dapat mencemari lingkungan (Lestari dan Yohana, 2008).
Edible film dapat dibuat dari tiga jenis bahan penyusun yang berbeda yaitu hidrokoloid, lipid, dan komposit dari keduanya (Donhowe & Fennema, 1994, dalam Irianto,dkk: 2006). Beberapa jenis hidrokoloid yang dapat dijadikan bahan pembuat edible film adalah protein (gelatin, kasein, protein kedelai, protein jagung, dan gluten gandum) dan karbohidrat (pati, alginat, pektin, gum arab, dan modifikasi karbohidrat lainnya), sedangkan lipid yang digunakan adalah lilin/wax, gliserol dan asam lemak (Irianto dkk: 2006).
Karbohidrat seperti pektin salah satunya dapat dibuat dari kulit pisang (Musaceaea sp.). Pengembangan pektin kulit pisang sebagai bahan dasar edible film merupakan salah satu upaya meningkatkan pemanfaatan kulit pisang. Selain itu, pemanfaatan kulit pisang sebagai bahan dasar edible film juga merupakan salah satu alternatif untuk menciptakan suatu kemasan makanan dan produk pangan yang ramah lingkungan, mengingat sebagian
besar produk pangan pada saat ini masih menggunakan bahan kemasan sintetis yang dapat menimbulkan pencemaran lingkungan.
Pektin digunakan secara luas sebagai komponen fungsional pada makanan karena kemampuannya membentuk gel encer dan menstabilkan protein (May, 1990 dalam Hariyati, 2006). Penambahan pektin pada makanan akan mempengaruhi proses metabolisme dan pencernaan khususnya pada adsorpsi glukosa dan tingkat kolesterol (Baker, 1994 dalam Hariyati, 2006). Selain itu, pektin juga dapat membuat lapisan yang sangat baik yaitu sebagai bahan pengisi dalam industri kertas dan tekstil, serta sebagai pengental dalam industri karet (Hariyati, 2006).
Beberapa penelitian berkaitan dengan pektin telah dilakukan. Ahda dan Berry (2008), menyatakan kandungan pektin dalam pisang kepok berkisar antara 10,10%-11,93%. Kandungan pektin dalam kulit jeruk lemon sebanyak 32,61% (Fitriani, 2003). Pada penelitian ekstraksi dan karakterisasi pektin dari limbah proses pengolahan jeruk Pontianak yang dilakukan Hariyati (2006) mendapatkan rendemen pektin berkisar antara 4,87%-6,95%.
Pektin lebih banyak digunakan pada industri makanan terutama produk jeli, selai, makaroni, makanan coklat, kembang gula dan industri minuman seperti produk susu dan pengalengan buah-buahan. Hal tersebut disebabkan oleh karena pektin memiliki kemampuan gel yang lebih optimum dan gel tersebut memiliki tekstur yang lebih baik, kuat dan stabil (Fitriani, 2003).
Polisakarida seperti pati dapat digunakan sebagai bahan tambahan pembuatan edible film. Pati sering digunakan dalam industri pangan sebagai biodegradable film untuk menggantikan polimer plastik karena ekonomis, dapat diperbaharui, dan memberikan karakteristik fisik yang baik (Bourtoom, 2007 dalam Wahyu, 2009).
Menurut Yoshida et al. (2009), plastik edible yang dibentuk dari polimer murni bersifat rapuh sehingga perlu digunakan plasticizer untuk meningkatkan fleksibilitasnya. Edible film pektin dengan penambahan bahan tambahan plastisizer mempunyai sifat lebih fleksibel daripada film tanpa plastisizer. Nilai persen elongasi semakin besar dengan penambahan plastisizer gliserol. Plasticizer merupakan bahan yang sering ditambahkan pada pembuatan edible film. Menurut Gontard et al (1993), plasticizer ditambahkan pada pembuatan edible film untuk mengurangi sifat rapuh film selain itu juga untuk meningkatkan permeabilitas terhadap gas, uap air, dan zat terlarut serta meningkatkan elastisitas film. Plasticizer seperti gliserol, sorbitol dan polietilen glikol memiliki viskositas rendah yang bila ditambahkan akan memberikan sifat fleksibilitas (Tamaela dan Sherly, 2007).
Beberapa penelitian yang berkaitan dengan uji kuat tarik (tensile strenght) dan persen elongasi edible film pektin telah dilakukan. Rachmawati (2009), menyatakan edible film pektin cincau hijau memiliki persen pemanjangan sebesar 13,7%-19,5%. Sedangkan kuat tarik edible film pektin cincau hijau adalah 0,70 MPa-2,53 MPa. Persentase elongasi dikatakan baik jika nilainya lebih dari 50% dan dikatakan jelek jika nilainya kurang dari
10%. Penelitian ini bertujuan untuk mengetahui karakteristik dan konsentrasi pektin terbaik dari pektin kulit pisang kepok dalam pembuatan edible film.
1.2 Permasalahan
Berdasarkan uraian pada latar belakang, permasalahan yang akan diselesaikan dalam penelitian ini adalah :
1. Bagaimana karakteristik edible film berbahan dasar pektin dari kulit pisang kepok (Musa paradisiaca Linn) ditinjau dari sifat fisik-mekanik?
2. Berapa konsentrasi pektin dari kulit pisang kepok (Musa paradisiaca Linn) yang menghasilkan edible film terbaik?
1.3 Tujuan Penelitian
Penelitian ini bertujuan untuk :
1. Mengetahui karakteristik edible film berbahan dasar pektin dari kulit pisang kepok (Musa paradisiaca Linn) ditinjau dari sifat fisik-mekanik. 2. Mengetahui konsentrasi pektin dari kulit pisang kepok (Musa paradisiaca
1.4 Manfaat Penelitian
Penelitian ini diharapkan mampu :
1. Menjadi salah satu teknologi alternatif dalam mengolah pektin sebagai bahan dasar pembuatan plastik biodegradable yang dapat dimakan (edible film) untuk skala industri maupun pada pemenuhan kebutuhan manusia lainnya.
2. Memberikan informasi mengenai karakteristik edible film pektin dari kulit pisang kepok (Musa paradisiaca Linn).
3. Menjadi dasar penelitian lebih lanjut dengan menggunakan variabel-variabel lain.
8
2.1 Tinjauan Umum Pisang (Musa paradisiaca)
Pisang merupakan tanaman asli daerah Asia Tenggara termasuk Indonesia, nama latinnya adalah Musa paradisiaca. Nama ini diberikan sejak sebelum Masehi, diambil dari nama dokter kaisar Romawi Octavianus Augustus (63 SM–14 M) yang bernama Antonius Musa (Munadjim,1988 dalam Dewati, 2008). Tanaman pisang ini oleh masyarakat dapat dimanfaatkan mulai dari bunga, buah, daun, batang sampai bonggolpun dapat dibuat sayur. Pisang merupakan tanaman hortikultura yang penting karena potensi produksinya yang cukup besar dan produksi pisang berlangsung tanpa mengenal musim (Dewati: 2008).
Dalam proses pengolahan buah pisang tentunya terdapat limbah kulit pisang. Masyarakat pedesaan memanfaatkan kulit pisang sebagai pakan ternak. Padahal kulit pisang mengandung 18,90 g karbohidrat pada setiap 100 g bahan (Susanto dan Saneto,1994 dalam Dewati: 2008).
Secara umum pisang mempunyai kandungan gizi yang baik. Buah ini kaya karbohidrat, mineral, dan vitamin. Mengacu dari Wikipedia, 100 gr pisang memasok 136 kalori. Ini berarti kandungannya 2 kali lipat dibandingkan apel. Kandungan energi pisang merupakan energi instan,
yang mudah tersedia dalam waktu singkat, sehingga bermanfaat dalam menyediakan kebutuhan kalori sesaat.
Sedangkan kandungan protein dan lemak pisang sangat rendah, yaitu hanya 2,3 persen dan 0,13 persen. Karena itu, tidak perlu takut kegemukan walau mengonsumsi pisang dalam jumlah banyak (Rumpis, 2011).
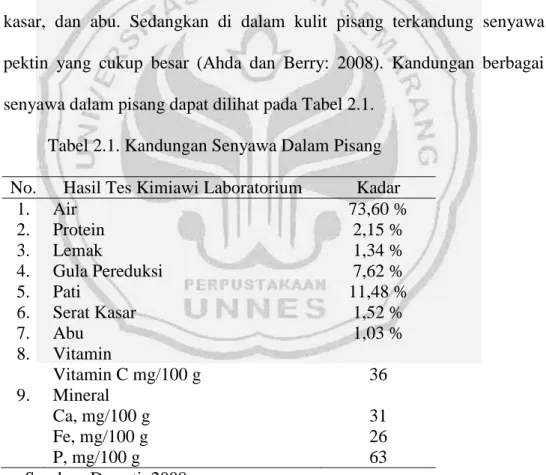
Menurut hasil penelitian dari Balai Penelitian dan Pengembangan Industri, tanaman pisang mengandung berbagai macam senyawa seperti air, gula pereduksi, sukrosa, pati, protein kasar, pektin, lemak kasar, serat kasar, dan abu. Sedangkan di dalam kulit pisang terkandung senyawa pektin yang cukup besar (Ahda dan Berry: 2008). Kandungan berbagai senyawa dalam pisang dapat dilihat pada Tabel 2.1.
Tabel 2.1. Kandungan Senyawa Dalam Pisang No. Hasil Tes Kimiawi Laboratorium Kadar
1. 2. 3. 4. 5. 6. 7. 8. 9. Air Protein Lemak Gula Pereduksi Pati Serat Kasar Abu Vitamin Vitamin C mg/100 g Mineral Ca, mg/100 g Fe, mg/100 g P, mg/100 g 73,60 % 2,15 % 1,34 % 7,62 % 11,48 % 1,52 % 1,03 % 36 31 26 63 Sumber: Dewati, 2008.
2.2 Pisang Kepok (Musa paradisiacal Linn)
Pisang adalah buah yang tumbuh berkelompok. Tanaman dari keluarga Musaceae ini hidup di daerah tropis dengan jenis yang berbeda-beda. Sebut saja pisang ambon, pisang sereh, pisang raja, pisang tanduk, pisang sunrise, dan pisang kepok.
Pisang kepok merupakan pisang berbentuk agak gepeng dan bersegi seperti terlihat pada Gambar 2.1. Karena bentuknya gepeng, ada yang menyebutnya pisang gepeng. Ukuran buahnya kecil, panjangnya 10-12 cm dan beratnya 80-120 g. Kulit buahnya sangat tebal dengan warna kuning kehijauan dan kadang bernoda cokelat.
Gambar 2.1. Pisang Kepok
Ada dua jenis pisang kepok, yaitu pisang kepok kuning dan pisang kepok putih. Secara kasat mata dari luar bentuk pisang hampir sama. Hanya daging buah pisang kepok kuning berwarna kekuningan, sedangkan kepok putih lebih pucat. Rasa kepok kuning lebih manis, sedangkan yang kepok putih lebih asam. Padahal nilai gizi yang terkandung dalam pisang kepok putih sama dengan pisang kepok kuning. Dunia industri membudidayakan pisang kepok ini untuk tepung, kripik, cuka, bir, dan
puree (Rumpis: 2011). Kandungan senyawa dalam kulit pisang dapat dilihat pada Tabel 2.2.
Tabel 2.2. Kandungan Senyawa Dalam Kulit Pisang No. Senyawa Kandungan (g/100 g berat kering)
1. 2. 3. 4. 5. Protein Lemak Pati Abu Serat total 8,6 13,1 12,1 15,3 50,3 Sumber: Yosephine, dkk, 2012.
2.3 Pektin
2.3.1 Pengertian dan Sumber Pektin
Pektin adalah substansi alami yang terdapat pada sebagian besar tanaman pangan. Selain sebagai elemen struktural pada pertumbuhan jaringan dan komponen utama dari lamella tengah pada tanaman, pektin juga berperan sebagai perekat dan menjaga stabilitas jaringan dan sel (Herbstreith dan Fox, 2005).
Pektin merupakan senyawa polisakarida dengan bobot molekul tinggi yang banyak terdapat pada tumbuhan. Pektin digunakan sebagai pembentuk gel dan pengental dalam pembuatan jelly, marmalade, makanan rendah kalori dan dalam bidang farmasi digunakan untuk obat diare (National Research Development Corporation, 2004).
Kata pektin berasal dari bahasa Latin “pectos” yang berarti pengental atau yang membuat sesuatu menjadi keras/padat. Pektin ditemukan oleh Vauquelin dalam jus buah sekitar 200 tahun yang lalu.
Pada tahun 1790, pektin belum diberi nama. Nama pektin pertama kali digunakan pada tahun 1824, yaitu ketika Braconnot melanjutkan penelitian yang dirintis oleh Vauquelin. Braconnot menyebut substansi pembentuk gel tersebut sebagai asam pektat (Herbstreith dan Fox, 2005).
Pektin yang dimanfaatkan untuk makanan merupakan suatu polimer yang berisi unit asam galakturonat (sedikitnya 65%). Kelompok asam tersebut bisa dalam bentuk asam bebas, metil ester, garam sodium, kalium, kalsium atau ammonium, dan dalam beberapa kelompok pektin amida (IPPA, 2002).
Komposisi kandungan protopektin, pektin, dan asam pektat di dalam buah sangat bervariasi tergantung pada derajat kematangan buah. Pada umumnya, protopektin yang tidak larut itu lebih banyak terdapat pada buah-buahan yang belum matang (Winarno, 1997).
Semua tanaman yang berfotosintesis tanpa kecuali mengandung pektin. Kertesz (1951) menyatakan bahwa pektin dijumpai pada buah-buahan dan sayur-sayuran serta dalam jumlah kecil ditemukan pada serelia. Kandungan pektin dari beberapa sayuran dan buah-buahan dapat dilihat pada Tabel 2.3. (Fitriani, 2003).
Tabel 2.3. Komposisi pektin berbagai sayuran dan buah-buahan Sumber Rendemen (% bobot kering)
Apel - kulit - daging Jeruk -Albedo -Flavedo Jambu biji Terong Bawang bombay Tomat -Hijau -Kuning -Merah Kubis Wortel Bayam Pisang 17,44 17,63 16,4 14,2 3,4 11 4,8 3,43 4,65 4,63 4,57 7,14 11,58 52,4 Sumber : Kertesz (1951) dalam Fitriani (2003).
Beberapa penelitian yang berkaitan dengan ekstraksi pektin dari kulit pisang telah dilakukan. Kaban, dkk (2012), menyatakan ekstraksi pektin dari kulit pisang raja mengandung pektin sebanyak 4,43%, dan pada penelitian ekstraksi pisang kepok oleh Tarigan, dkk (2012) dihasilkan pektin sebanyak 3,72%. Sedangkan pada penelitian Ahda dan Berry (2008), menyatakan ekstraksi pektin pada kulit pisang kepok mengandung pektin sebanyak 11,93%.
2.3.2 Struktur dan Komposisi Kimia Pektin
Pada tahun 1924, Smolenski adalah yang pertama kali berasumsi bahwa pektin merupakan polimer asam galakturonat. Pada tahun 1930, Meyer dan Mark menemukan formasi rantai dari molekul pektin, dan Schneider dan Bock pada tahun 1937 membentuk formula tersebut (Herbstreith dan Fox,
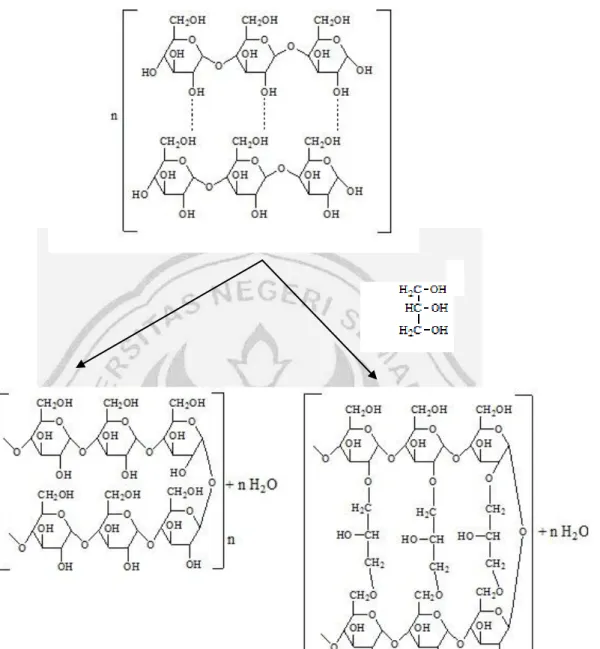
2005). Pektin tersusun atas molekul asam galakturonat yang berikatan dengan ikatan α-(1-4)-glikosida sehingga membentuk asam poligalakturonat seperti ditunjukkan pada Gambar 2.2. Gugus karboksil sebagian teresterifikasi dengan metanol dan sebagian gugus alkohol sekunder terasetilasi (Herbstreith dan Fox, 2005 dalam Hariyati: 2006).
Menurut Hoejgaard (2004) dalam Hariyati (2006), pektin merupakan asam poligalakturonat yang mengandung metil ester. Masing-masing cincin merupakan suatu molekul dari asam poligalakturonat, dan ada 300–1000 cincin seperti itu dalam suatu tipikal molekul pektin, yang dihubungkan dengan suatu rantai linier.
Gambar 2.2. Struktur Kimia Pektin (Asam Poligalakturonat) Pada umumnya senyawa-senyawa pektin dapat diklasifikasi menjadi tiga kelompok senyawa yaitu asam pektat, asam pektinat (pektin), dan protopektin. Pada asam pektat, gugus karboksil asam galakturonat dalam ikatan polimernya tidak teresterkan. Asam pektat dapat membentuk garam seperti halnya asam-asam lain. Asam pektat terdapat dalam jaringan tanaman sebagai kalsium atau magnesium pektat (Winarno, 1997).
Gambar 2.3. Perkiraan reaksi tepung tapioka dan gliserol (Yusmarlela, 2009)
Gambar 2.4. Perkiraan hasil reaksi pektin, gliserol dan tepung tapioka (Yusmarlela, 2009)
Dari Gambar 2.3 dan Gambar 2.4 diatas dapat diketahui bahwa dalam edible film pektin kulit pisang kepok terdapat ikatan hidrogen. Ikatan hidrogen adalah sejenis gaya tarik antar molekul yang terjadi antara dua muatan listrik persial dengan polaritas yang berlawanan. Kekuatan ikatan hidrogen ini dipengaruhi oleh perbedaan elektronegativitas antara atom-atom dalam molekul tersebut. Semakin besar perbedaannya, semakin besar ikatan hidrogen yang terbentuk (Yusmarlela, 2009).
2.3.3 Sifat-Sifat Pektin
Commite on Food Chemical Codex (1996), menyatakan bahwa pektin sebagian besar tersusun atas metil ester dari asam poligalakturonat dan sodium, potasium, kalsium dan garam ammonium. Pektin merupakan zat
berbentuk serbuk kasar hingga halus yang berwarna putih, kekuningan, kelabu atau kecoklatan dan banyak terdapat pada buah-buahan dan sayuran matang. Gliksman (1969) dalam Hariyati (2006) menyatakan bahwa pektin kering yang telah dimurnikan berupa kristal yang berwarna putih dengan kelarutan yang berbeda-beda sesuai dengan kandungan metoksilnya (Hariyati, 2006).
Faktor yang mempengaruhi pembentukan gel dengan tingkat kekenyalan dan kekuatan tertentu meliputi pH, konsentrasi pektin, suhu, ion kalsium, dan gula (Chang dan Miyamoto, 1992 dalam Hariyati, 2006). Kekentalan larutan pektin mempunyai kisaran yang cukup lebar tergantung pada konsentrasi pektin, dan ukuran rantai asam poligalakturonat (Rouse, 1977 dalam Hariyati: 2006).
2.3.4 Kegunaan Pektin
Pektin digunakan secara luas sebagai komponen fungsional pada industri makanan karena kemampuannya membentuk gel encer dan menstabilkan protein (May, 1990 dalam Hariyati, 2006). Penambahan pektin pada makanan akan mempengaruhi proses metabolisme dan pencernaan khususnya pada adsorpsi glukosa dan kolesterol (Baker, 1994 dalam Hariyati, 2006). Dalam industri makanan dan minuman, pektin dapat digunakan sebagai bahan pemberi tekstur yang baik pada roti dan keju, bahan pengental dan stabilizer pada minuman sari buah. Selain itu pektin juga berperan sebagai bahan pokok pembuatan jeli, jam, dan marmalade (Herbstreith dan Fox, 2005).
Pektin memiliki potensi yang baik dalam bidang farmasi. Towle dan Christensen (1973) dalam Hariyati (2006) menyatakan bahwa sejak dahulu pektin digunakan dalam penyembuhan diare dan menurunkan kandungan kolesterol darah. Pada industri farmasi, pektin digunakan sebagai emulsifier bagi preparat cair dan sirup, obat diare pada bayi dan anak-anak, obat penawar racun logam, dan bahan penyusut kecepatan penyerapan bermacam-macam obat. Selain itu, pektin juga berfungsi sebagai bahan kombinasi untuk memperpanjang kerja hormon dan antibiotika, bahan pelapis perban (pembalut luka) untuk menyerap kotoran dan jaringan rusak atau hancur sehingga luka tetap bersih dan cepat sembuh, serta bahan injeksi untuk mencegah pendarahan (Hoejgaard, 2004 dalam Hariyati: 2006).
2.4 Edible film
2.4.1 Pengertian Edible film
Edible film adalah suatu lapisan tipis yang dibuat dari bahan yang dapat dimakan, yang dapat digunakan untuk melapisi makanan (coating) atau diletakkan diantara komponen makanan (film) yang berfungsi sebagai penghalang terhadap perpindahan massa misalnya kelembaban, oksigen, dan cahaya (Krochta 1992, dalam Harris: 2001).
Menurut Arpah (1997) yang dikutip dari Wahyu (2009), edible packaging pada bahan pangan pada dasarnya dibagi menjadi tiga jenis bentuk, yaitu : edible film, edible coating, dan enkapsulasi. Hal yang membedakan edible coating dengan edible film adalah cara pengaplikasiannya. Edible
coating langsung dibentuk pada produk, sedangkan pada edible film pembentukkannya tidak secara langsung pada produk yang akan dilapisi/dikemas. Enkapsulasi adalah edible packaging yang berfungsi sebagai pembawa zat flavor berbentuk serbuk (Hui, 2006).
Fungsi dari edible film sebagai penghambat perpindahan uap air, menghambat pertukaran gas, mencegah kehilangan aroma, mencegah perpindahan lemak, meningkatkan karakteristik fisik, dan sebagai pembawa zat aditif. Jumlah karbondioksida dan oksigen yang kontak dengan produk merupakan salah satu yang harus diperhatikan untuk mempertahankan kualitas produk dan akan berakibat pula terhadap umur simpan produk. Film yang terbuat dari protein dan polisakarida pada umumnya sangat baik sebagai penghambat perpindahan gas, sehingga efektif untuk mencegah oksidasi lemak. Komponen volatil yang hilang atau yang diserap oleh produk dapat diatur dengan melakukan pelapisan edible coating atau film (Hui, 2006).
2.4.2 Bahan Tambahan Edible film 2.4.2.1 Gliserol
Menurut Syarief, et.al,. (1989), untuk memperbaiki sifat plastik maka ditambahkan berbagai jenis tambahan atau aditif. Bahan tambahan ini sengaja ditambahkan dan berupa komponen bukan plastik yang diantaranya berfungsi sebagai plasticizer, penstabil pangan, pewarna, penyerap UV dan lain-lain. Bahan itu dapat berupa senyawa organik maupun anorganik yang biasanya mempunyai berat molekul rendah.
Plasticizer merupakan bahan tambahan yang diberikan pada waktu proses agar plastik lebih halus dan luwes. Fungsinya untuk memisahkan bagian-bagian dari rantai molekul yang panjang. Plasticizer adalah bahan non volatile dengan titik didih tinggi yang apabila ditambahkan ke dalam bahan lain akan merubah sifat fisik dan atau sifat mekanik dari bahan tersebut (Krochta, et.al., 1994). Plasticizer ditambahkan untuk mengurangi gaya intermolekul antar partikel penyusun pati yang menyebabkan terbentuknya tekstur edible film yang mudah patah (getas).
Gliserol adalah senyawa golongan alkohol polihidrat dengan 3 buah gugus hidroksil dalam satu molekul (alkohol trivalent). Rumus kimia gliserol adalah C3H8O3, dengan nama kimia 1,2,3 propanatriol seperti pada Gambar
2.3. Berat molekul gliserol adalah 92,1 massa jenis 1,23 g/cm2 dan titik
didihnya 209°C (Winarno, 1992). Gliserol ialah suatu trihidroksi alkohol yang
terdiri atas 3 atom karbon. Jadi tiap atom karbon mempunyai gugus –OH. Satu molekul gliserol dapat mengikat satu, dua, tiga molekul asam lemak dalam bentuk ester, yang disebut monogliserida, digliserida dan trigliserida. Peran gliserol sebagai plasticizer dan konsentrasinya meningkatkan fleksibilitas film (Bertuzzi et al, 2007).
Gambar 2.5. Struktur Gliserol
Gliserol ini bermanfaat sebagai anti beku (anti freeze) dan juga merupakan senyawa yang higroskopis sehingga banyak digunakan untuk
mencegah kekeringan pada tembakau, pembuatan parfum, tinta, kosmetik, makanan dan minuman lainnya (Austin, 1985 dalam Yusmarlela, 2009).
2.4.2.2 Tepung Tapioka
Pati secara kimia adalah merupakan suatu polisakarida (C6H10O5)n.
pati sukar larut dalam air dingin tetapi dalam air panas butir-butir pati akan menyerap air dan akhirnya membentuk pasta.
Semua pati yang terdapat secara alami tersusun dari dua macam molekul pektin (amilosa dan amilopektin). Amilosa merupakan polimer berantai lurus, α-1-4 glukosidik, sedangkan amilopektin mempunyai cabang dengan ikatan α-1-6 glukosidik. Molekul-molekul berantai lurus, yaitu amilosa yang berdekatan dan bagian rantai lurus pada bagian luar atau ujung-ujung amilopektin tersusun dengan arah sejajar (Whistler, et. al. 1984 dalam Rachmawati, 2009).
Pati singkong sering digunakan sebagai bahan tambahan dalam industri makanan dan industri yang berbasis pati karena kandungan patinya yang cukup tinggi. Kandungan pati pada beberapa bahan pangan dapat dilihat pada Tabel 2.4.
Tabel 2.4. Kandungan Pati pada Beberapa Bahan Pangan No. Bahan Pangan Pati (% dalam basis kering)
1. 2. 3. 4. 5. 6. 7. Biji gandum Beras Jagung Biji sorghum Kentang Ubi jalar Singkong 67 89 57 72 75 90 90 Sumber: Wahyu, 2009.
2.5 Ekstraksi Padat-Cair
Ekstraksi merupakan salah satu metode pemisahan dua atau lebih komponen dengan menambahkan suatu pelarut yang tepat. Ekstraksi meliputi distribusi zat terlarut diantara dua pelarut yang tidak saling bercampur. Pelarut yang umum dipakai adalah air, dan pelarut organik lain seperti kloroform, eter, dan alkohol.
Dalam prosedur ekstraksi, zat-zat terlarut akan terdistribusi diantara lapisan air dan lapisan organik sesuai dengan perbedaan kelarutannya. Ekstraksi lebih efisien bila dilakukan berulang kali dengan jumlah pelarut yang lebih kecil daripada bila jumlah pelarutnya banyak tetapi ekstraksinya hanya sekali. Pemisahan secara ekstraksi ada dua macam yaitu ekstraksi padat-cair dan ekstraksi cair-cair atau dikenal sebagai ekstraksi pelarut (Sudjadi, 1988).
Ekstraksi yang akan digunakan pada penelitian ini yaitu ekstraksi padat-cair. Ekstraksi padat-cair adalah suatu metode pemisahan campuran terlarut yang terdapat dalam sampel padat (misalnya bahan alam, daun,
rimpang, kayu, dan sebagainya) dengan menggunakan pelarut organik (Winarni, 2007).
Tahapan-tahapan dalam pembuatan pektin yaitu persiapan bahan, ekstraksi, penggumpalan, pencucian, dan pengeringan. Metode yang digunakan untuk mengekstrak pektin dari jaringan tanaman sangat beragam. Akan tetapi pada umumnya ekstraksi pektin dilakukan dengan menggunakan ekstraksi asam, seperti asam natrium heksametafosfat (Ranggana, 1977 dalam Fitriani, 2003), asam sulfat (Cruess, 1958 dalam Fitriani, 2003), asam khlorida (Suradi, 1984 dalam Fitriani, 2003), asam nitrat (Rouse dan Crandall, 1978, dalam Fitriani, 2003).
Beberapa penelitian yang berkaitan dengan pelarut yang digunakan untuk ekstraksi pektin telah dilakukan. Ahda dan Berry (2008), menyatakan penggunaan pelarut asam klorida 0,05 N pada proses ekstraksi kulit pisang kepok lebih banyak menghasilkan rendemen pektin sebesar 11,93% dibandingkan dengan menggunakan pelarut asam asetat 0,05 N yang menghasilkan rendemen pektin sebesar 10,10% dengan suhu ekstraksi 80oC untuk waktu operasi selama 1,5 jam. Hal ini menunjukan bahwa pelarut asam klorida lebih optimal dibandingkan pelarut asam asetat. Untuk proses pemanasan Towle dan Christensen (1973) dalam Fitriani (2003) menyatakan bahwa pemanasan dapat menyebabkan degradasi senyawa pektin. Rendemen pektin yang dihasilkan semakin meningkat seiring dengan peningkatan suhu ekstraksi namun akan semakin menurun seiring dengan waktu ekstraksi (Fitriani, 2003).
2.6 Metode Analisis Spektroskopi FT-IR
Alasan suatu senyawa atau molekul diuji menggunakan FT-IR adalah karena senyawa atau molekul tersebut mampu menyerap radiasi inframerah yaitu yang terletak pada panjang gelombang 10-6 – 10-4 nm. Spektrum serapan inframerah suatu material mempunyai pola yang khas, sehingga berguna untuk identifikasi material dan identifikasi keberadaan gugus-gugus fungsi yang ada. Pada penampakan spektrum inframerah, posisi pita dalam analisa inframerah dinyatakan dalam satuan frekuensi. Frekuensi sering dinyatakan sebagai bilangan gelombang, yakni jumlah gelombang atau panjang gelombang per centimeter (cm-1). Hubungan antara frekuensi (bilangan gelombang) dengan panjang gelombang dinyatakan sebagai :
v = 104 / λ
dengan v menyatakan bilangan gelombang (cm-1) dan λ sebagai panjang gelombang dalam µm.
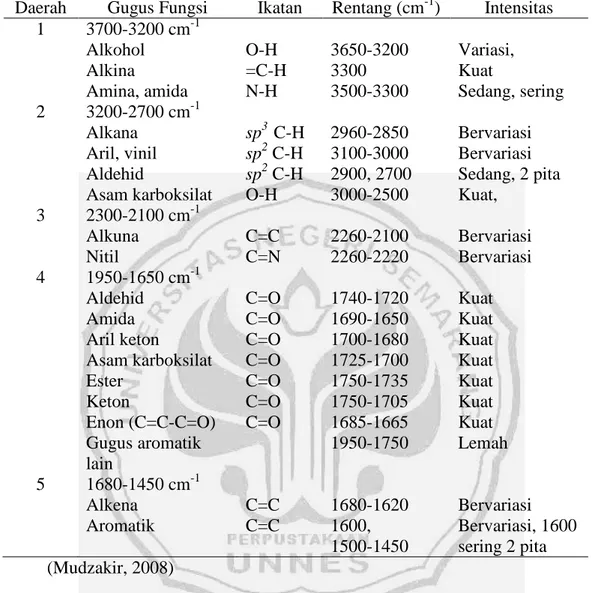
Daerah yang sering dianalisa dengan spektroskopi inframerah adalah dalam kisaran 4000-600 cm-1 (setara dengan 2,5 – 5 µm) atau lebih rendah. Hasil analisa dicatat dalam modus pemancar (%T) atau serapan (Abs). Tabel 2.2. menunjukkan karakteristik rentang frekuensi pada IR untuk tiap gugus fungsional.
Tabel 2.5. Karakteristik rentang frekuensi pada spektrofotometri IR
Daerah Gugus Fungsi Ikatan Rentang (cm-1) Intensitas 1 3700-3200 cm-1 Alkohol Alkina Amina, amida O-H =C-H N-H 3650-3200 3300 3500-3300 Variasi, Kuat Sedang, sering 2 3200-2700 cm-1 Alkana Aril, vinil Aldehid Asam karboksilat sp3 C-H sp2 C-H sp2 C-H O-H 2960-2850 3100-3000 2900, 2700 3000-2500 Bervariasi Bervariasi Sedang, 2 pita Kuat, 3 2300-2100 cm-1 Alkuna Nitil C=C C=N 2260-2100 2260-2220 Bervariasi Bervariasi 4 1950-1650 cm-1 Aldehid Amida Aril keton Asam karboksilat Ester Keton Enon (C=C-C=O) Gugus aromatik lain C=O C=O C=O C=O C=O C=O C=O 1740-1720 1690-1650 1700-1680 1725-1700 1750-1735 1750-1705 1685-1665 1950-1750 Kuat Kuat Kuat Kuat Kuat Kuat Kuat Lemah 5 1680-1450 cm-1 Alkena Aromatik C=C C=C 1680-1620 1600, 1500-1450 Bervariasi Bervariasi, 1600 sering 2 pita (Mudzakir, 2008)
Dibandingkan sistem dispersi pada spektrofotometer IR biasa yang menggunakan grating atau prisma, maka FT-IR yang menggunakan “Michelson Interferometer” mengukur lebih cepat dan lebih sensitif yang ditunjukkan pada Gambar 2.6. “Cermin Gerak” digerakkan pada kecepatan tetap oleh motor yang diatur oleh komputer. Kecepatan gerak cermin dimonitori oleh sistem laser He-Ne (pada 632,8 nm). Komputer akan merubah
signal dari interferometer (interferogram) ke dalam spektrum sinar tunggal melalui transformasi Fourier (Mudzakir, 2008).
2.7 Karakterisasi Edible film
Sifat fisik film meliputi sifat mekanik dan penghambatan. Sifat mekanik menunjukan kemampuan kekuatan film dalam menahan kerusakan bahan selama pengolahan, sedangkan sifat penghambatan menunjukan kemampuan film melindungi produk yang dikemas dengan menggunakan film tersebut. Beberapa sifat film meliputi kekuatan renggang putus, ketebalan, laju transmisi uap air, dan kelarutan film (Gontard,dkk, 1993 dalam Rachmawati: 2009).
Berdasarkan standar ASTM (American Standard Testing Method) parameter penting karakteristik mekanik yang diukur dan diamati dari sebuah material plastik adalah kuat tarik (tensile-strength at yield), kuat tusuk (puncture strength), elastisitas (elastic modulus/young modulus), kekakuan (flexural modulus), ketahanan benturan (notched izod impact strength), kekerasan (hardness), dan persen elongasi (tensile elongation at yield). Karakteristik mekanik menunjukkan indikasi integrasi film pada kondisi tekanan (stress) yang terjadi selama proses pembentukan film tersebut.
Keseluruhan parameter tersebut digunakan untuk menjelaskan karakteristik mekanik dari bahan plastik pada umumnya yang berkaitan dengan struktur kimia plastik. Beberapa parameter utama yang sangat penting dalam penentuan kualitas plastik khususnya edible film adalah nilai kuat tarik
dan persen elongasi. Sebagai bahan kemasan makanan, edible film pektin ini dimaksudkan untuk dapat menggantikan polipropilen (PP). Polipropilen merupakan material sintetis yang umumnya digunakan sebagai bahan pembuat plastik pembungkus makanan yang tidak dapat diuraikan. Oleh karena itu, karakter mekanik edible film pektin harus memenuhi kriteria polipropilen yang ditunjukkan pada Tabel 2.6.
Tabel 2.6. Sifat mekanik dan fisik polipropilen (PP). No. Sifat Mekanik & Fisik PP
1. Tensile stength (MPa) 24,7 – 302
2. Elongation (%) 21 – 220
3. Modulus Young (MPa) 1430
4. Densitas (g/cm3) 0,90 – 0,914
5. Water Uptake (%) 0,01
Sumber : Boedeker plastics dalam Darni, dkk (2009). 2.7.1 Ketebalan Film (mm)
Ketebalan film merupakan sifat fisik yang dipengaruhi oleh konsentrasi padatan terlarut dalam larutan film dan ukuran plat pencetak. Ketebalan film akan mempengaruhi laju transmisi uap air, gas dan senyawa volatil (Mc Hugh, et. al., 1993).
Ketebalan film diukur dengan menggunakan mikrometer. Mikrometer adalah suatu alat ukur yang berfungsi mengukur benda dengan satuan yang memiliki ketelitian 0,01mm (Kosim, 2005).
Ketebalan merupakan parameter penting yang berpengaruh terhadap penggunaan film dalam pembentukan produk yang akan dikemasnya. Ketebalan film akan mempengaruhi permeabilitas gas. Semakin tebal edible film maka permeabilitas gas akan semakin kecil dan melindungi produk yang
dikemas dengan lebih baik. Ketebalan juga dapat mempengaruhi sifat mekanik film yang lain, seperti tensile strength dan elongasi. Namun dalam penggunaannya, ketebalan edible film harus disesuaikan dengan produk yang dikemasnya (Kusumasmarawati, 2007 dalam Rachmawati, 2009).
2.7.2 Tensile-Strength/Kuat Tarik (MPa)
Kuat tarik atau kuat renggang putus (tensile-strength) merupakan tarikan maksimum yang dapat dicapai sampai film dapat tetap bertahan sebelum putus. Pengukuran tensile-strength dimaksudkan untuk mengetahui besarnya gaya yang dicapai untuk mencapai tarikan maksimum pada setiap satuan luas area film untuk merenggang atau memanjang. Hasil pengukuran ini berhubungan erat dengan jumlah plastisizer yang ditambahkan pada proses pembuatan film. Sedangkan persentase pemanjangan merupakan representasi kuantitatif kemampuan film untuk merenggang yaitu didefinisikan sebagai fraksi perubahan panjang bahan sebagai efek dari deformasi. (Alyanak, 2004).
Uji tarik (tensile test) merupakan prosedur paling umum digunakan untuk mempelajari hubungan tegangan-regangan (stress-strain). Uji tarik dilakukan dengan benda uji ditarik dari dua arah, sehingga panjangnya bertambah dan diameternya mengecil. Besarnya beban dan pertambahan panjang dicatat selama pengujian.
Tensile-strength adalah beban maksimum yang mampu diterima bahan uji (Huda, 2009).
TS = Fmax / A0
Fmax = gaya maksimum
A0 = luas permukaan awal
2.7.3 Pemanjangan/Elongasi (%)
Persen pemanjangan merupakan keadaan dimana edible film patah setelah mengalami perubahan panjang dari ukuran yang sebenarnya pada saat mengalami peregangan. Sifat tersebut sangat penting dan mengindikasikan kemampuan edible film dalam menahan sejumlah beban sebelum edible film tersebut putus. Persen pemanjangan dapat dihitung dengan membandingkan panjang film saat putus dan panjang film sebelum ditarik oleh Tensile Strength and Elongation Tester. Adapun secara matematis persen pemanjangan (elongasi) dapat dihitung dengan menggunakan rumus:
Persentase perpanjangan (Elongation) : e (%) = [(L1-L0 )/ L0] x 100%
dimana : L1= panjang akhir benda uji
L0= panjang awal benda uji
Perubahan panjang dapat dilihat dari film robek, semakin tinggi konsentrasi tepung tapioka yang digunakan, maka semakin menurunkan elongasi (pemanjangan) edible film yang dihasilkan.
,
2.7.4 Kelarutan Film (%)
Persen kelarutan edible film adalah persen berat kering dari film yang terlarut setelah dicelupkan di dalam air selama 24 jam (Gontard, dkk. 1993).
Kelarutan film merupakan faktor yang penting dalam menentukan biodegradibilitas film ketika digunakan sebagai pengemas. Ada film yang dikehendaki tingkat kelarutannya tinggi atau sebaliknya tergantung jenis produk yang dikemas (Nurjannah, 2004, dalam Rachmawati, 2009).
2.8 Penelitian Terdahulu
Penelitian ini selain menggunakan buku-buku, artikel dan jurnal penelitian sebagai literatur, juga merujuk pada beberapa penelitian terdahulu yang berkaitan. Adapun penelitian terdahulu yang dijadikan sebagai rujukan yaitu penelitian Rachmawati (2009) ekstraksi dan karakteristik pektin cincau hijau untuk pembuatan edible film menyatakan ketebalan pada edible film pektin cincau hijau yang dihasilkan berkisar antara 0,127 mm-0,145 mm, nilai elongasi sebesar 13,7%-19,5%, kelarutan film sebesar 64,9%-77,4% sedangkan untuk nilai kuat tarik yang dihasilkan berkisar antara 0,70 MPa-2,53 MPa. Pada penelitian Murdianto, dkk (2005) edible film ekstrak daun janggelan memiliki ketebalan film antara 0,073 mm-0,085 mm, nilai kuat tarik 3,10 MPa-5,70 MPa, nilai elongasi 0,14%-0,26% dan untuk nilai kelarutan film sebesar 44,94%-72,86%. Pada penelitian edible film yang dibuat dari komposit protein biji kecipir dan tapioka oleh Poeloengasih dan Marseno (2003) memiliki karakteristik ketebalan film antara 0,096 mm-0,104 mm dan untuk nilai elongasi berkisar antara 1,68%-3,48%.
Beberapa penelitian yang berkaitan dengan ekstraksi pektin telah dilakukan. Ahda dan Berry (2008), menyatakan pada penggunaan pelarut
asam klorida 0,05 N proses ekstraksi kulit pisang kepok menghasilkan rendemen pektin sebesar 11,93% sedangkan menggunakan pelarut asam asetat 0,05 N yang menghasilkan rendemen pektin sebesar 10,10% dengan suhu ekstraksi 80oC untuk waktu operasi selama 1,5 jam. Pada penelitian ekstraksi pektin dari kulit buah pisang raja oleh Kaban, dkk (2012) dihasilkan pektin sebanyak 4,43% pada suhu 90oC untuk waktu ekstraksi 80 menit dengan pelarut asam klorida. Tarigan, dkk (2012) ekstraksi pektin dari kulit pisang kepok dengan menggunakan pelarut asam klorida pada suhu 90oC dengan waktu ekstraksi 80 menit menghasilkan rendemen pektin sebanyak 3,72%.
32
Sampel dalam penelitian ini merupakan cuplikan pektin yang diproduksi di Laboratorium Kimia Organik, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Negeri Semarang.
3.2 Variabel Penelitian
3.2.1 Variabel bebas
Variabel bebas adalah variabel yang akan diteliti pengaruhnya terhadap variabel terikat. Variabel bebas dalam penelitian ini adalah konsentrasi tepung tapioka.
3.2.2 Variabel terikat
Variabel terikat adalah variabel yang menjadi titik pusat penelitian. Variabel terikat pada penelitian ini adalah kuat tarik (tensile-srength), pemanjangan (elongasi), ketebalan film, dan kelarutan edible film dari pektin kulit pisang kepok.
3.2.3 Variabel kontrol
Variabel kontrol adalah faktor-faktor lain yang dapat mempengaruhi hasil selama penelitian. Variabel kontrol dalam penelitian ini adalah konsentrasi pektin, konsentrasi gliserol, jenis pelarut dan volume.
3.3 Alat dan Bahan
3.3.1 Alat yang digunakan dalam penelitian
Alat yang digunakan dalam penelitian ini meliputi : Gelas ukur, Beker gelas, Ayakan ukuran 100 mesh, Ayakan ukuran 50 mesh, Termometer, Neraca analitik merek Mettler Toledo AL204, Oven pengering, Hot plate merek Ceramag Midi IKA® Works USA, Cetakan / plat plastik, Magnetic stirer, Alat ekstraksi 1 set, Mikrometer Mitutoya, Blender, Spatula, Pengaduk, FT-IR merek Shimadzu .
3.3.2 Bahan yang digunakan dalam penelitian
Bahan yang digunakan dalam penelitian ini meliputi : Pektin kulit pisang kepok, Asam klorida (HCl) 0,05 N, Gliserol, Kertas saring, Aquades, Tepung tapioka, Etanol 96%.
3.4 Prosedur kerja
3.4.1 Tahap Persiapan Bahan
Pembuatan bubuk kulit pisang kepok
Bahan yang dipakai adalah kulit pisang kepok yang sudah diambil daging kulitnya, dicuci bersih dengan air kemudian dipotong kecil-kecil. Kemudian dikeringkan dibawah sinar matahari langsung. Kulit pisang yang sudah kering lalu dihancurkan dengan menggunakan blender hingga menjadi serbuk, setelah itu diayak dengan ayakan 50 mesh (Ahda dan Berry, 2008). Bubuk kulit pisang ini yang kemudian digunakan untuk proses ekstraksi.
3.4.2 Tahap Ekstraksi Pektin dari Serbuk Kulit Pisang Kepok
Sebanyak 6 gram serbuk kulit pisang kepok yang sudah diayak dimasukkan ke dalam labu, sebagai pelarut digunakan asam klorida 0,05 N 200 mL. Pemanas listrik dihidupkan dengan variasi suhu 70oC, 75oC, 80oC, 85oC dan 90oC lalu pengaduk magnetik dijalankan. Waktu ekstraksi selama 120 menit. Setelah diekstraksi, bahan disaring dengan kertas saring dalam keadaan panas. Filtrat dari hasil penyaringan ditambah dengan etanol 96% dengan perbandingan volume 1:1 sambil diaduk-aduk sehingga terbentuk endapan. Presipitat dipisahkan dari larutannya dengan cara disaring dengan menggunakan kertas saring. Pemurnian presipitat dilakukan dengan menggunakan etanol secara berulang-ulang. Setelah itu keringkan dibawah sinar matahari langsung sampai diperoleh berat yang konstan. Kemudian diayak dengan ayakan 100 mesh. Selama proses ekstraksi dilakukan pengadukan dengan magnetic stirrer. Hasil optimum rendeman pektin kering digunakan untuk pembuatan edible film dan dilakukan analisis uji FT-IR (Ahda dan Berry, 2008).
3.4.3 Tahap pembuatan edible film
Pembuatan edible film dua jenis larutan awalnya disiapkan terlebih dahulu, yaitu pertama adalah larutan pektin kulit pisang kepok sebanyak 6 gram dilarutkan dalam 150 mL aquades. Bahan kedua berupa larutan yang berisi tepung tapioka dengan variasi penambahan 0 gram, 0,6 gram, 1,2 gram, 1,8 gram dan 2,4 gram yang dilarutkan dalam 150 mL aquades, dipanaskan dengan hot plate selama 30 detik (sampai warnanya berubah
menjadi bening) dan dilanjutkan dengan pengadukan menggunakan magnetic stirrer selama 30 detik. Kemudian larutan tapioka dituang ke dalam beker gelas yang telah berisi larutan pektin kulit pisang. Selanjutnya tambahkan gliserol sebanyak 1 mL, kemudian diaduk dan dipanaskan terus sampai suhu 75ºC (selama 5 menit). Pemanasan dilanjutkan sambil diaduk hingga suhu 80ºC-85ºC (selama 10 menit). Larutan dituang ke dalam cetakan dan dikeringkan menggunakan oven pada suhu 60ºC selama 6 jam. Edible film yang dihasilkan dilakukan analisis dengan parameter uji ketebalan film, uji kuat tarik, uji pemanjangan (elongasi), dan uji kelarutan edible film (Rachmawati, 2009).
3.4.4 Analisis Gugus Fungsional Pektin
Data hasil FT-IR kemudian dianalisis dengan memperhatikan bilangan gelombang pada spektra dan intensitasnya masing-masing. Bilangan gelombang inilah yang mencirikan gugus fungsi yang ada pada pektin.
3.4.5 Tahap Pengujian Produk Edible film 3.4.5.1 Uji Ketebalan Edible film
Ketebalan film merupakan sifat fisik yang dipengaruhi oleh konsentrasi padatan terlarut dalam larutan film dan ukuran plat pencetak. Ketebalan film akan dipengaruhi laju transmisi uap air, gas, dan senyawa volatil (Mc Hugh, et. al., 1993).
Ketebalan film diukur menggunakan mikrometer (ketelitian 0,01 mm) dengan cara menempatkan film diantara rahang mikrometer. Untuk setiap sampel film yang akan diuji, ketebalan diukur pada lima titik yang berbeda, kemudian dihitung reratanya dan digunakan untuk menghitung kuat tarik (Poeloengasih dan Marseno, 2003).
3.4.5.2 Uji Kuat Tarik/Tensile Strength (MPa)
Kekuatan regang putus merupakan tarikan yang dapat dicapai sampai film dapat tetap bertahan sebelum film putus atau robek. Pengukuran kekuatan regang putus berguna untuk mengetahui besarnya gaya yang dicapai untuk mencapai tarikan maksimum pada setiap satuan luas area film untuk merenggang atau memanjang (Krochta dan Mulder Jhonston, 1997 dalam Rachmawati: 2009).
Tensile-strength adalah beban maksimum yang mampu diterima bahan uji (Huda, 2009).
TS = Fmax / A0
dimana : TS = tensile-strength Fmax = gaya maksimum
A0 = luas permukaan awal
Kuat regang diuji dengan menggunakan mesin uji tarik Lioyd’s Universal Testing Instrument. Kuat regang putus dinyatakan sebagai gaya maksimum yang diberikan pada film sampai sobek (Newton) dibagi luas penampang film (m2) (Murdianto, dkk. 2005).
3.4.5.3 Uji Pemanjangan/Elongasi (%)
Persen elongasi dari edible film diperoleh dari hasil uji kuat tarik produk tersebut, sehingga diperoleh 2 data, yaitu panjang awal (sebelum uji kuat tarik) dan panjang akhir (setelah uji kuat tarik) dari edible film, yang dihitung dengan rumus :
e (%) = [(L1-L0 )/ L0] x 100%
dimana : L1= panjang akhir benda uji
L0= panjang awal benda uji
3.4.5.4 Uji Kelarutan Edible film (%)
Persen kelarutan edible film adalah persen berat kering dari film yang terlarut setelah dicelupkan di dalam air selama 24 jam (Murdianto, dkk. 2005).
3.5
Metode Analisis Data
Data yang diperoleh dari prosedur kerja diatas belum dapat memberikan informasi tentang hasil penelitian sehingga perlu dianalisis baik secara kualitatif maupun kuantitatif. Seluruh data yang didapat dimasukkan dalam tabel, kemudian dibuat kurva/grafik untuk mengetahui massa tepung tapioka dalam sintesis edible film pektin dengan kuat tarik dan persen elongasi optimum..
3.5.1 Analisis Ketebalan Edible film Pektin
Ketebalan diukur menggunakan mikrometer Mitutoyo (ketelitian 0,01 mm) dengan cara menempatkan film diantara rahang mikrometer. Untuk setiap sampel yang akan diuji, ketebalan diukur pada tiga titik yang berbeda, kemudian dihitung reratanya dan digunakan untuk menghitung kuat tarik.
3.5.2 Analisis Kuat Tarik Edible film Pektin
Uji kuat tarik dilakukan pada edible film pektin yang telah disintesis dengan penambahan massa gliserol dan tepung tapioka. Data yang diperoleh dari uji kuat tarik digunakan untuk menganalisis karakteristik mekanik yaitu nilai kuat tarik dan persen elongasi dari edible film pektin. Besarnya gaya yang digunakan untuk memutuskan edible film pektin terukur dalam satuan Kg. Selanjutnya gaya tersebut harus dibagi dengan besarnya luas permukaan benda uji untuk mendapatkan nilai kuat tarik edible film pektin dalam satuan Kg/cm2. Nilai yang didapat harus di konversi terlebih dahulu dalam satuan baku nilai kuat tarik yaitu MPa dengan cara dibagi dengan bilangan 10,2. Secara matematis, dapat dirumuskan sebagai berikut :
Kuat Tarik = Kg/cm2 : 10,2
3.5.3 Analisis Elongasi Edible film Pektin
Berdasarkan data hasil uji kuat tarik, dapat diukur pula pertambahan panjang (kemuluran) edible film pektin dengan mistar. Besarnya selisih antara panjang awal dan panjang akhir dibagi panjang awal edible film
pektin menghasilkan nilai persen elongasi dari edible film pektin tersebut, secara matematis dirumuskan :
Persen elongasi = x 100 %
3.5.4 Analisis Kelarutan Edible film Pektin
Uji kelarutan edible film merupakan persen berat kering dari film yang terlarut setelah dicelupkan di dalam air. Untuk menentukan edible film dalam penelitian ini dihitung dengan melihat berapa lama waktu yang diperlukan edible film tersebut larut dalam air.
40
4.1
Penyiapan Bahan Baku Kulit Pisang Kepok
Dalam penelitian ini pektin yang dipakai diperoleh dari proses ekstraksi yang dilakukan di Laboratorium Kimia Organik, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Negeri Semarang.
Bahan utama yang digunakan dalam penelitian ini adalah kulit pisang kepok (Musa paradisiaca Linn) yang terlebih dahulu dikeringkan menjadi serbuk sebelum diekstrak pektinnya. Setelah kering kulit pisang dihancurkan dengan blender dan diayak. Serbuk kulit pisang kepok yang dihasilkan berwarna coklat kehitaman yang selanjutnya digunakan untuk proses ekstraksi.
Proses pengeringan ini bertujuan untuk mengurangi kadar air yang terkandung dalam kulit pisang kepok. Menurut Fitriani (2003) pektin yang dihasilkan dengan menggunakan metode pengeringan pada persiapan bahan memiliki rendemen yang lebih besar dibandingkan dengan yang tidak dikeringkan lebih dahulu (bahan yang masih dalam keadaan segar). Hal ini disebabkan pengeringan bahan baku akan mempengaruhi difusi larutan ke bahan akan lebih baik dibandingkan dalam keadaan segar, karena bahan segar memiliki kadar air yang tinggi yang menyulitkan difusi larutan asam untuk mengekstrak pektin dari bahan.
4.2 Ekstraksi Pektin Kulit Pisang Kepok
Setelah diperoleh serbuk kulit pisang kepok, selanjutnya dilakukan ekstraksi pektin kulit pisang kepok. Suhu yang digunakan untuk proses ekstraksi bervariasi yaitu 70oC, 75oC, 80oC, 85oC dan 90oC dengan waktu ekstraksi 120 menit (2 jam).
Ekstraksi pektin merupakan usaha untuk melepaskan pektin yang terikat dalam suatu bahan dengan bantuan pelarut, dalam hal ini berupa air yang telah diasamkan dengan menggunakan asam klorida. Penggunaan asam klorida ini didasarkan pada penelitian Ahda dan Berry (2008) yang menghasilkan rendemen lebih banyak (11,93%) dibandingkan dengan menggunakan asam asetat (10,10%). Penggunaan asam dalam ekstraksi pektin adalah untuk menghidrolisis protopektin menjadi pektin yang larut dalam air ataupun membebaskan pektin dari ikatan dengan senyawa lain, misalnya selulosa (Fitriani, 2003).
Campuran yang telah diekstrak kemudian disaring dengan menggunakan kertas saring untuk memisahkan filtrat dari ampasnya. Filtrat yang telah didapat kemudian dilakukan pengendapan dengan etanol 96%.
Penggumpalan/pengendapan pektin dapat dilakukan dengan alkohol, aseton, garam metal kalium sulfat dan aluminium sulfat (Morris, 1951 dalam Fitriani, 2003). Untuk proses pencucian pektin dari kulit pisang kepok Ahda dan Berry (2008) menggunakan etanol 96%. Salah satu tujuan pencucian pektin adalah untuk menghilangkan khlorida yang ada pada pektin. Untuk mengetahui adanya khlorida, dapat dilakukan dengan
menambahkan beberapa tetes larutan perak nitrat (AgNO3) pada cairan
bekas cucian. Apabila khlorida masih ada, maka akan terbentuk endapan putih (AgCl).
Tahap akhir dari ekstraksi pektin adalah pengeringan dan pengayakan endapan pektin. Ranganna (1977) dalam Hariyati (2006) menganjurkan pengeringan dilakukan pada tekanan rendah agar pektin tidak terdegradasi. Pengeringan pektin dilakukan pada suhu kamar dengan sinar matahari sampai berat konstan lalu lakukan pengayakan dengan ayakan 100 mesh.
4.3 Hasil Ekstraksi Pektin Kulit Pisang Kepok
Pada Gambar 4.1. menunjukan grafik hubungan antara suhu dan rendemen pektin yang dihasilkan semakin menurun seiring dengan peningkatan suhu ekstraksi. Hal ini dikarenakan terlalu tingginya suhu ekstraksi yang digunakan mengakibatkan pektin menjadi senyawa lain. Penggunaan suhu ekstraksi yang terlalu tinggi akan menghasilkan pektin yang tidak jernih, sehingga gel yang diperoleh akan keruh dan kekuatan gel berkurang.
0.8752 0.8313 0.7984 0.7638 0.7435 0.65 0.7 0.75 0.8 0.85 0.9 70 75 80 85 90 R e m d e m e n (g r am ) Suhu (oC)
Grafik Hubungan Suhu Dan Rendemen
Ekstraksi Pektin Kulit Pisang Kepok
Series 1
Gambar 4.1. Kurva hubungan suhu dan rendemen ekstraksi pektin Rendemen pektin yang diperoleh pada penelitian ini berkisar antara 0,7435 - 0,8752 gram (12,39% - 14,59%) sesuai pada Tabel 4.1. Hasil ini lebih besar dibandingkan rendemen pektin kulit pisang kepok pada penelitian Ahda dan Berry (2008) yaitu sebesar 11,93% dengan suhu ekstraksi 80oC untuk waktu ekstraksi 1,5 jam. Pada penelitian ekstraksi pektin dari kulit pisang raja oleh kaban, dkk (2012) dihasilkan pektin sebanyak 4,43% pada suhu 90oC untuk waktu ekstraksi 80 menit dan penelitian yang dilakukan Tarigan, dkk (2012) ekstraksi pektin dari kulit pisang kapok pada suhu 90oC dengan waktu ekstraksi 80 menit menghasilkan rendemen pektin sebanyak 3,72%, maka ekstraksi pektin penelitian ini menghasilkan rendemen yang lebih banyak.
Tabel. 4.1 Ekstraksi pektin dari serbuk kulit pisang kepok No. Bubuk Kulit Pisang Kepok (gram) Asam Klorida (HCl) 0,05 N (mL) Suhu (oC) Waktu (menit) Rendemen (gram) Rendemen (%) 1. 2. 3. 4. 5. 6 6 6 6 6 200 200 200 200 200 70 75 80 85 90 120 120 120 120 120 0,8752 0,8313 0,7942 0,7638 0,7435 14,59 13,86 13,24 12,73 12,39 Sumber: Data Primer, 2012
Rendemen tertinggi diperoleh pada ekstraksi dengan suhu 70oC sebanyak 0,8752 gram (14,59%) dan rendemen terendah diperoleh pada ekstraksi suhu 90oC sebanyak 0,7435 gram (12,39%). Hasil rendemen pektin pada suhu 70oC yang diperoleh akan digunakan untuk pembuatan edible film sebagai hasil rendemen pektin optimum.
4.4 Hasil Uji Gugus Fungsional Pektin
Pengujian gugus fungsional pectin dilakukan dengan spektrofotometer Infra Merah (FT-IR). Analisa ini bertujuan untuk mengetahui perubahan gugus fungsi dari suatu bahan atau matriks yang dihasilkan. Pengujian ini dilakukan pada sampel edible film pektin tanpa penambahan tepung tapioka. Spektrum hasil analisa FT-IR dapat dilihat pada Gambar 4.2.