PENGARUH LOGAM ALUMINIUM DAN NIKEL PADA
KATALIS PENCAIRAN BATUBARA
SARIMAN DAN SITI ROCHANI
Pusat Penelitian dan Pengembangan Teknologi Mineral dan Batubara
Jalan Jenderal Sudirman No 623, Bandung 40211, Telp: 022-6030483, Fax: 022-6003373
Naskah masuk : 18 Juli 2007, revisi pertama : 27 Juli 2007, revisi kedua : 28 Agustus 2007, revisi terakhir : September 2007
SARI
Pengaruh logam nikel dan aluminium serta suhu terhadap katalis besi telah dikaji melalui uji sulfidasi tanpa batubara pada kondisi yang sama dengan proses pencairan batubara. Bahan katalis yang digunakan adalah campuran Fe-Ni dan Fe-Al dengan kadar Ni 0, 0,5, 1, 1,5, 2% dan Al 0, 3, 5, 7, 9, dan 11%. Parameter yang diamati adalah ukuran kristal pirhotit yang terbentuk dari hasil transformasi katalis besi dan belerang. Batas maksimum ukuran kristal pirhotit adalah 40 nm. Hasil terbaik yang diperoleh menunjukkan bahwa suhu sulfidasi yang optimal ádalah 400°C dan ukuran kristal pirhotit dapat diredam menjadi 35 nm dengan penambahan nikel 0,5% dari 58 nm dengan tanpa penambahan nikel. Untuk kadar aluminium yang sebaiknya terdapat dalam katalis besi adalah 4% dengan ukuran kristal pirhotit yang dihasilkan adalah 33,6 nm. Bila pada campuran kadar Al>4%, ukuran kristal pirhotit akan membesar. Ukuran kristal pirhotit yang diperoleh ini tidak berbeda jauh bila menggunakan katalis dari limonit sebesar 28,8 nm.
Kata kunci : Aluminium, pencairan batubara, katalis, sulfidasi
ABSTRACT
The effect of aluminum, nickel and temperature on the iron catalyst was investigated through sulfidation test in the absence of coal feed under liquefaction conditions. The Fe-Ni and Fe-Al were used as catalyst with the concentration of Ni and Al were 0, 0.5, 1, 1.5, 2% and Al 0, 3, 5, 7, 9, 11% respectively. The crystalite size of pyrrhotite, as an active phase formed due to iron-sulfur transformation was the main concern observed. It is suggested that the maximum size of crystallite is 40 nm. The results showed that the best condition of sulfiding temperature was 400°C. The lowest crystallite size 35 nm was achieved by adding 0.5% of nickel, while the 58 nm crystallite size of pyrrhotite was obtained without nickel addition. To get a 33.6-nm crystal- lite, the Al content within Fe catalyst should be 4%. In fact, the bigger the content, the bigger the crystallite size. Yet the experiment results show that the size of crystallite is similar with that of using limonite catalyst, i.e. 28.8 nm.
Keywords : Aluminium, coal liquefaction, catalyst, sulphidation
1. PENDAHULUAN
Batubara telah dijadikan sumber energi alternatif. Salah satu pemanfaatan batubara khususnya di bidang transportasi sebagai bahan bakar dalam fase
cair. Pada proses pencairan batubara yang banyak mendapat perhatian adalah proses pencairan batubara secara langsung (Hirano and Kanda 2001, BPPT dan Kobe Steel, 2000) melalui proses perengkahan batubara pada suhu tinggi. Proses tersebut dilakukan
dengan melarutkan batubara pada pelarut tertentu dan dipanaskan pada tekanan tinggi. Dengan proses ini, katalis sangat dibutuhkan agar diperoleh hasil cairan (yield) yang tinggi dengan kondisi reaksi yang tidak terlalu tinggi. Katalis yang yang telah umum dipakai pada proses pencairan batubara adalah katalis berbasis besi dan molibden. Namun karena pertimbangan harga serta kemudahan dalam operasional maka katalis berbasis besi nampaknya yang banyak dipakai di masa mendatang.
Peranan katalis dalam pencairan batubara adalah untuk membantu memasukkan atom hidrogen yang berasal dari disosiasi molekul hidrogen ke dalam batubara atau campuran batubara pelarut sehingga menaikkan ketersediaan hidrogen aktif. Kriteria pemilihan katalis antara lain adalah kereaktifannya tinggi, harganya murah dan mudah diproduksi. Beberapa katalis yang termasuk kriteria tersebut adalah katalis berbasis besi seperti pirit (FeS2),
limonit (FeOOH) dan hematit (Fe2O3). Katalis ini
bila bereaksi dengan sulfur pada kondisi pencairan batubara, strukturnya berubah menjadi pirhotit (Fe1-xS)
yang berperan aktif pada proses pencairan batubara (Cugini dkk., 1994, Ikenaga, dkk., 2000). Kandungan
Fetotal dalam senyawa besi tersebut >30%.
Diketahui bahwa katalis berbasis besi yang mendapat perhatian luas adalah limonit ditinjau dari cadangan dan kereaktifannya (Kaneko dkk, 2000). Kandungan limonit dari daerah Soroako terdiri dari campuran hematit (Fe2O3), goethit (FeOOH) dan gibsit
Al(OH)3 sebagai pengotor. Selain itu dalam limonit
terkandung banyak pengotor dalam jumlah yang lebih kecil antara lain Si, Mg, Ni, dan Cr. Unsur unsur ini umumnya terikat dalam struktur dari senyawa utamanya, sehingga sulit dipisahkan dari mineral utama. Sejauh ini belum banyak diketahui pengaruh dari unsur-unsur ini terhadap pertumbuhan kristal pirhotit. Kajian tentang faktor-faktor yang mempengaruhi pembentukan pirhotit sangat diperlukan untuk mendapatkan produk berupa batubara cair berjumlah banyak hasil dari pencairan batubara. Kereaktifan reaksi pencairan batubara sangat ditentukan oleh ukuran kristalnya. Semakin besar ukuran kristal pirhotit semakin rendah kereaktifannya, yang mengakibatkan rendahnya jumlah batubara yang dapat dicairkan. Batas maksimum ukuran kristal pirhotit adalah 40 nm. Ukuran kristal dapat membesar karena adanya aglomerasi antar partikel pirhotit. Literatur menyebutkan bahwa nikel dapat meredam perbesaran kristal pirhotit. Namun berapa kadar nikel yang diperlukan belum diketahui. Kajian lebih lanjut tentang pengaruh nikel dalam limonit dan unsur
unsur lainnya seperti aluminium, silika, serta krom perlu mendapat perhatian khusus.
Pada penelitian ini telah dikaji pengaruh dari unsur nikel dan aluminium terhadap pertumbuhan kristal pirhotit dengan menggunakan percontoh buatan yaitu dengan mencampur bahan oksida besi dengan variasi kandungan nikel dan aluminum. Sebagai pembanding digunakan limonit dari Soroako. Karakterisasi limonit dan hasil kristalisasi dilakukan dengan menggunakan difraksi sinar-x (XRD), mikroskopi dan mikroskop elektron (SEM). Penentuan kadar dari unsur-unsur tersebut yang mampu meredam pertumbuhan kristal pirhotit dilakukan dengan menghitung ukuran kristal pirhoit yang terbentuk.
2. METODOLOGI PENELITIAN
Bahan-bahan katalis alam yang digunakan adalah limonit yang didatangkan dari Soroako dan Pomala Sulawesi. Percontoh digiling dengan menggunakan
Planetary ball mill hingga mencapai kehalusan -200
mesh dan dikeringkan pada suhu 105 °C. Selanjutnya percontoh tersebut disimpan dalam desikator sebelum dianalisis. Sebagai bahan katalis buatan Fe+Ni dan Fe+Al disiapkan dari besi oksida (Fe2O3)
buatan/sintetis, serbuk logam nikel, dan serbuk logam aluminium masing-masing dengan kemurnian 99,4; 99,5; dan 90% produksi dari Merck. Berat total katalis adalah 0,6 g dengan variasi kandungan nikel 0, 0,5, 1, 1,5, 2% serta Al 0, 3, 5, 7, 9, dan 11%. Perbandingan atom sulfur dan katalis adalah 2. Minyak antrasen digunakan sebagai pelarut sebanyak 30 g untuk setiap percobaan.
Pelarut digunakan untuk membuat slurry katalis dan untuk menguraikan ikatan-ikatan hidrokarbon pada batubara sehingga mempercepat perolehan produk cair dari batubara. Tetrahidrofuran (THF) p.a digunakan untuk mencuci katalis yang telah mengalami sulfidasi.
Uji sulfidasi terhadap katalis alam dan buatan dilakukan dengan memasukkan bahan katalis beserta nikel atau aluminium, sulfur, dan 30g pelarut antrasen ke dalam otoklaf yang bervolum 500 ml. Udara yang terkandung dalam otoklaf dibilas dengan gas nitrogen sebanyak dua kali, selanjutnya dialirkan gas hidrogen sampai tekanannya mencapai 100 bar. Otoklaf tersebut dipanaskan dari suhu 25 sampai 400 °C dengan kecepatan pemanasan 5 °C/menit sambil digoyang dengan kecepatan konstan. Setelah mencapai suhu yang diinginkan, otoklaf didinginkan dengan cepat hingga suhu kamar, katalis dicuci
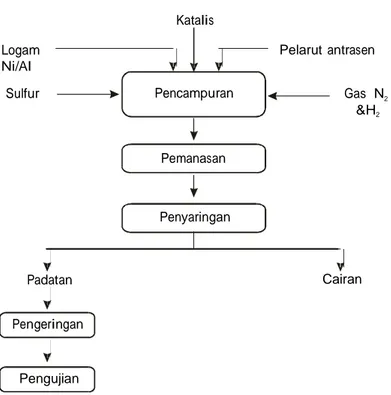
dengan THF dan diikuti dengan pengeringan pada suhu 100 °C selama 2 jam untuk menghilangkan THF. Gambar 1 menunjukkan diagram proses uji sulfidasi katalis.
Analisis mineralogi dan kimia digunakan untuk mengetahui komposisi mineral dan kimia bahan baku. Kristal pirhotit yang terbentuk dari uji sulfidasi diidentifikasi dengan menggunakan difraksi sinar x (XRD) dan SEM. Identifikasi fasa dilakukan dengan menggunakan perangkat lunak expertpro. Analisis image dan morphologi katalis dilakukan dengan Jeol JSM-6360. Resolusi mesin ini hingga 1,5 nm dengan detektor Robson backscattering. Unit dilengkapi dengan EDS yang digunakan untuk menganalisis unsur yang terkandung dalam parcontoh. Ukuran rata- rata kristal pirhotit (d) dihitung dengan persamaan Scherrer (Klug dan Alexander, 1978) dengan menggunakan lebar puncak difraksi pada setengah intensitas maksimum. 0,9 x x 57,3 d = x cos
Keterangan :d = ukuran kristal (nm) pada bidang kristal tertentu (hkl)
= panjang gelombang sinar – x = 1,542 °A
= lebar puncak pada setengah insensitas maksimum
= sudut difraksi
57,3 = faktor konversi derajat ke radian
3. HASIL DAN PEMBAHASAN 3.1. Karakterisasi Limonit
Komposisi oksida limonit dari Pomalaa, Soroako, dan oksida besi (Fe2O3) buatan/sintetis adalah seperti
tercantum pada Tabel 1. Oksida besi sintetis digunakan sebagai katalis buatan pada penelitian ini. Kandungan besi total, nikel, dan aluminium dalam kedua limonit tersebut berbeda. Perbedaan ini akan terlihat dari mengamati ukuran kristal pirhotit yang terbentuk pada proses sulfidasi. Dari data pada Tabel 1 ini dapat dinyatakan bahwa bahan baku yang digunakan untuk katalis pada proses pencairan batubara sudah memenuhi syarat, yaitu kandungan Fetot > 30%.
Gambar 2 menunjukkan komposisi mineral yang terdapat pada limonit Soroako dan Pomalaa. Pada limonit dari Soroako senyawa besi lainnya yang terdeteksi adalah magnetit, sedangkan pada limonit dari Pomalaa tidak teramati senyawa besi lainnya. Resume komposisi mineral limonit dari Pomalaa, Soroako, dan oksida besi buatan ditunjukkan pada Tabel 2.
Katalis Logam
Ni/Al
Pelarut antrasen
Sulfur Pencampuran Gas N2
&H2 Pemanasan Penyaringan Padatan Cairan Pengeringan Pengujian
In
te
n
si
tas
Tabel 1. Komposisi kimia (%) dari limonit Pomalaa dan Soroako serta oksida besi buatan/ sintetis
Sumber Fetot Fe2O3 SiO2 Al2O3 CaO MgO TiO2 Ni Cr LOI
Pomalaa Soroako Sintetis 41,88 45,40 69,86 59,84 64,85 99,8 18,47 15,36 -9,46 6,67 -0,10 0,01 -0,58 1,64 -0,45 0,35 -0,49 1,29 -1,26 1,56 -8,99 9,37 0,20
Tabel 2. Komposisi mineral limonit Pomalaa dan Soroako serta oksida besi buatan
Sumber Komposisi mineral
Pomalaa Limonit (goetit) Hematit Magnetit Kromit Gangue mineral
Soroako Limonit (goetit)
Magnetit Kromit Gangue mineral
Buatan Fe2O3 L
L
KrL
L
L
L
P
L
M KrL
L
L
L
A
B
Gambar 2. Fotomikrograf Limonit Soroako (A) dan Pomalaa (B). M= magnetit, Kr=kromit, L=limonit, P=piroksen Q Q= kuarsa G= goetit H=hematite G Q+G H H H 2 theta
C o u n ts C o u n ts Pc
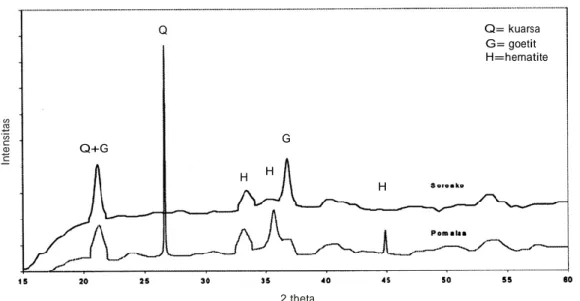
Pola difraksi sinar x percontoh limonit Pomalaa dan Soroako ditunjukkan pada Gambar 3. Kuarsa dan hematit (aFe2O3) terlihat sebagai mineral dominan
dalam limonit Pomalaa. Sedangkan kromit dan
gangue mineral, sebagaimana yang terdeteksi dengan
mikroskop tidak teramati. Limonit adalah senyawa hidroksida, salah satunya adalah goethit. Identifikasi goetit yang terdapat pada perconto ini dengan XRD tidak sejelas hasil identifikasi dengan metode mikroskop. Tidak teramatinya besi hidroksida ini dengan XRD kemungkinan disebabkan telah terjadinya dehidrasi pada percontoh untuk XRD, mengingat adanya selisih waktu yang lama antara analisis mikroskopi dengan XRD, seperti ditunjukkan oleh reaksi berikut: 2FeOOH -> Fe2O3 + H2O.
Terlepasnya molekul H2O (air) pada FeOOH
menghasilkan Fe2O3 sebagai hematit. Senyawa besi
yang dominan pada limonit asal Soroako adalah goethit dan hematit. Senyawa lainnya tidak teramati
pada difraktogram ini. Sedangkan menurut Kaneko dkk (2002) limonit Soroako mengandung goethit dan magnetit sebagai mineral besinya. Perbedaan ini memerlukan analisis lebih lanjut mungkin disebabkan sensitivitas alat yang digunakan berbeda.
3.2. Identifikasi Pirhotit
Identifikasi pirhotit sebagai hasil reaksi sulfidasi dilakukan dengan analisis difraksi sinar x (XRD) dan mikroskop elektron (SEM). Suhu sulfidasi yang digunakan adalah 400 °C. Pirhotit mempunyai rumus kimia Fe1-xS. Harga x berkisar antara 0 - 0,17. Besi
oksida (Fe2O3) yang digunakan sebagai katalis pada
pencairan batubara diharapkan dapat terubah seluruhnya menjadi pirhotit. Pada Gambar 4.A katalis tanpa penambahan nikel, bulatan-bulatan yang saling menempel (struktur asikular) masih terlihat jelas. Besi oksida telah terubah sebagian dicirikan oleh adanya
200 180 160 140 120 100 80 Pc 60 40 20 Mo Mo Mo 200 Pc Pc 0 0.00 0.80 1.00 2.40 3.20 4.00 4.80 5.00 6.40 7.20 keV
Element keV mass% error% At% Compound mass% Cation K
O 23.85 A FeK 6.398 66.66 0.71 92.34 FeO 85.75 19.22 89.7347 Mo L 2.293 9.50 0.48 7.66 MoO3 14.25 1.59 10.2653 Total 100.00 100.00 100.00 20.81 Katalis Fe + Ni; Ni = 0% 200 180 Pc 160 140 120 100 80 Pc 60 Cu Cu 40 Cu 20 Cu 0 0.00 1.00 2.00 3.00 4.00 5.00 6.00 7.00 8.00 keV 9.00 10.00
Element keV mass% error% At% Compound mass% Cation K C K 0.277 40.38 0.07 81.04 C 40.38 0.00 22.7040 O 23.83 B S K 2.307 11.27 0.20 8.48 SO3 28.15 5.66 26.8815 Fe K 6.398 22.60 0.68 9.75 FeO 29.07 6.52 46.7180 Cu K 8.040 1.92 1.71 0.73 CuO 2.40 0.49 3.6965 Total 100.00 100.00 100.00 12.67 Katalis Fe + Ni; Ni = 0,5%
C o u n ts C o u n ts C o un ts D 3600 S 3200 2800 2400 2000 1600 1200 800 400 O Pc C Pc S Pc 0 0.00 0.80 1.00 2.40 3.20 4.00 4.80 5.00 keV 6.40 7.20
Element keV mass% error% At% Compound mass% Cation K C K 0.277 25.69 0.05 68.51 C 25.69 0.00 10.9150 O 27.02 S K 2.307 11.32 0.15 11.31 SO3 28.26 5.02 22.6164 Fe K 6.398 19.56 0.46 11.22 FeO 29.07 6.52 36.8941 C Cu K 7.471 16.42 0.82 8.96 CuO 20.89 3.97 29.5745 Total 100.00 100.00 100.00 13.97 Katalis Fe + Ni; Ni = 1% 4600 3800 3200 Pc 2800 2400 2000 1600 Pc O 1200 C 800 S Pc 400 0 0.00 0.80 1.00 2.40 3.20 4.00 4.80 5.00 keV 6.40 7.20
Element keV mass% error% At% Compound mass% Cation K C K 0.277 11.37 0.06 44.75 C 11.37 0.00 3.8205 O 37.00 S K 2.307 18.35 0.13 27.07 SO3 45.82 5.94 36.7014 Fe K 6.398 33.28 0.42 28.18 FeO 42.81 6.18 59.4781 Total 100.00 100.00 100.00 12.12 Katalis Fe + Ni; Ni = 1,5%
Gambar 5. SEM mikrogram katalis Fe+Ni (A) Ni=1% dan (B) Ni=1,5%
5000 S 4800 4000 3200 Ni Pc 2400 1600 O C Zr S 800 Zr Pc Pc Ni Ni 0 0.00 1.00 2.00 3.00 4.00 5.00 6.00 7.00 keV 8.00 9.00
Element keV mass% error% At % Compound mass% Cation K C K 0.277 11.80 0.05 46.40 C 11.80 0.00 3.8433 O 35.72 S K 2.307 17.04 0.10 25.09 SO3 42.55 5.71 33.0416 Fe K 6.398 22.14 0.30 18.71 FeO 28.48 4.26 40.3805 E Ni K 7.471 10.14 0.54 8.16 NiO 12.90 1.86 17.9819 Zr L 2.042 3.16 0.17 1.63 ZrO2 4.26 0.37 4.7528 Total 100.00 100.00 100.00 12.20 Katalis Fe + Ni; Ni = 2%
In
te
n
si
ta
s
P
P
P
P
20
30
40
50
60
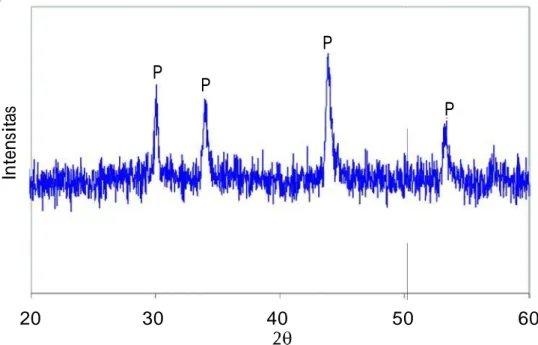
Gambar 7. Difraktogram kristal pirhotit yang terbentuk dari katalis Fe+Ni setelah proses sulfidasi
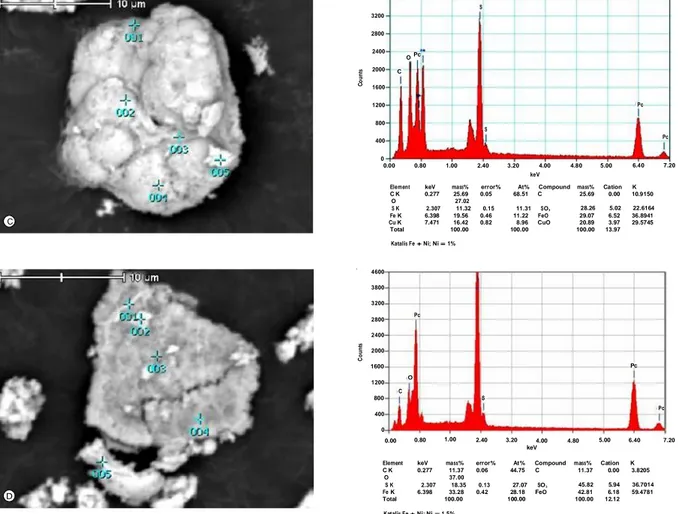
fragmen-fragmen pada partikel terdeteksi. Lima titik deteksi EDS menunjukkan pola spektrum yang mirip. Besi hadir sebagai unsur dominan di setiap titik deteksi. Belerang terdeteksi di titik 1-4 dan absen di titik 5. Dengan demikian pirhotit dapat dikatakan sudah terbentuk.
Struktur asikular Fe+Ni dengan Ni=0,5% (Gambar 4.B) terlihat sangat jelas dan umumnya masih utuh, selain itu partikel memperlihatkan pori-pori yang hampir merata di seluruh permukaan partikel. Pola spektrum titik 1-3 terlihat hampir sama didominasi oleh unsur besi dan belerang, sedangkan titik 4 dan 5 menampilkan pola spektrum sangat mencolok - yang dimungkinkan karena adanya logam Cu, walaupun pada titik deteksi 5 Cu tidak terdeteksi tetapi melihat penampilan partikelnya dengan tona lebih terang dibandingkan partikel sekitarnya, diasumsikan partikel tersebut mengandung logam (Cu) seperti partikel titik deteksi 4 yang juga memperlihatkan tona lebih terang. Seperti pada katalis dengan Ni=0% dan Ni=0,5% juga tidak memperlihatkan rasio 1:1 antara massa Fe dan S. Diasumsikan pada percontoh inipun besi oksida sudah terubah menjadi pirhotit.
Katalis dengan Ni=1% (Gambar 5.A) dan Ni=1,5% (Gambar 5.B) memperlihatkan pola spektrum yang serupa. Pada percontoh ini perbandingan Fe dan S dapat memenuhi rasio untuk rumus empiris pirhotit
(FeS) Pada katalis Fe+Ni dengan Ni=1%, titik deteksi 1 menunjukkan adanya Fe dan S. Fe terlihat lebih dominan pada partikel ini seperti ditunjukkan oleh titik deteksi 2, 3 dan 4. Unsur-unsur terdeteksi pada titik deteksi 1 pada katalis dengan Ni=0% terlihat lebih bervariasi, namun secara keseluruhan besi dan belerang mendominasi partikel ini, sehingga dapat dikatakan besi oksida telah terubah menjadi pirhotit. Nikel terdeteksi pada katalis dengan Ni=1%, namun tidak teramati pada katalis dengan Ni=1,5%. Ini menunjukkan katalis yang disiapkan belum homogen.
Lima titik deteksi pada katalis dengan Ni=2% (Gambar 6) menunjukkan kandungan besi dan belerang yang hampir mendekati rasio untuk rumus empiris pirhotit (1:1). Rasio massa Fe dan yang terdeteksi memang tidak sepenuhnya memperlihatkan perbandingan 1:1. Pada partikel ini teramati unsur nikel. Berdasarkan identifikasi SEM dapat disimpulkan bahwa kristal pirhotit telah terbentuk dan Ni selalu berada dekat kristal tersebut.
Untuk memperkuat hasil analisis EDS terhadap dugaan terbentuknya kristal pirhotit tersebut, maka analisis difraksi sinar x dilakukan. Hasil yang diperoleh menunjukkan bahwa keseluruhan katalis telah membentuk kristal pirhotit. Gambar 7 menunjukkan salah satu katalis Fe+Ni yang telah mengalami perubahan struktur menjadi kristal pirhotit.
U k u ra n kr is ta l F e 1 -x S ( n m )
3.3. Pengaruh Suhu, Ni, dan Al terhadap Pertumbuhan Kristal Pirhotit
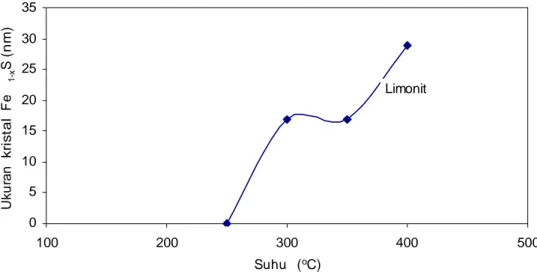
Pada Gambar 8 juga ditunjukkan pengaruh suhu terhadap pertumbuhan kristal pirhotit dari limonit asal Soroako. Ukuran kristal membesar dengan kenaikan suhu operasi. Kristal pirhotit pada suhu 250 °C belum teramati dan mulai teramati pada suhu 300 °C dengan ukuran kristal pirhotit yang terbentuk adalah 16 nm, dan pada suhu 400 °C membesar menjadi 28,8 nm. Data ini menunjukkan bahwa suhu reaksi pencairan batubara yang terbaik adalah pada 400 °C. Oleh karena itu, untuk percobaan tentang pengaruh Ni dan Al digunakan suhu 400 °C.
0,5% adalah rentang kadar Ni yang sebaiknya digunakan agar proses aglomerasi dapat dicegah. Sebagai rujukan pada Gambar 9 limonit (Soroako) dengan kadar Ni 0,5% memberikan ukuran kristal 28,8 nm. Variasi kandungan aluminium dalam limonit beragam, seperti yang ditunjukkan pada Gambar 10 (BPPT and Kobe Steel, 2000). Atas dasar itu maka disiapkan campuran biner besi aluminium dengan variasi kadar aluminium mulai dari 0, 3, 5, 7, 9, dan 11%.
Campuran biner Fe-Al ini digunakan untuk mengetahui pengaruh kandungan aluminium terhadap pertumbuhan kristal pirhotit. Keberadaan
35 30 25 Limonit 20 15 10 5 0 100 200 300 400 500 Suhu (oC)
Gambar 8. Pengaruh suhu terhadap peningkatan ukuran kristal pirhotit
Gambar 9 menunjukkan pengaruh dari nikel terhadap ukuran kristal pirhotit. Puncak difraksi yang digunakan untuk menentukan ukuran kristal adalah pada bidang miller d200. Puncak ini dipilih karena
intensitasnya relatif tinggi dan tidak bersekutu dengan puncak senyawa lainnya.
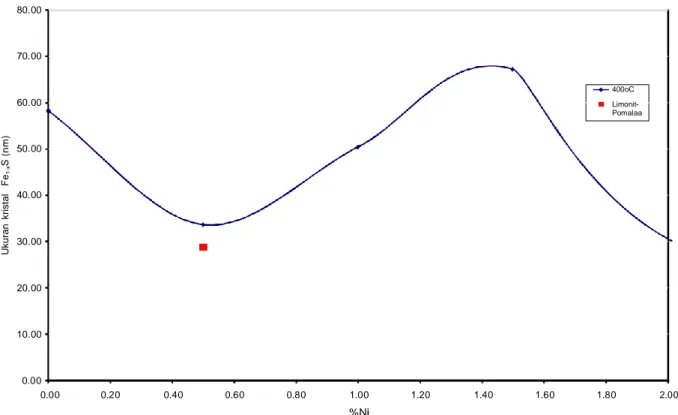
Kadar Ni dalam limonit yang menjadi perhatian pada penelitian ini maksimum adalah 1,5%, karena belum banyak dimanfaatkan. Pada Gambar 9 katalis Fe tanpa penambahan nikel, diperoleh ukuran kristal pirhotit 58 nm. Bila kadar Ni 0,5% ukuran kristal menurun hingga 35 nm, namun bila kadar Ni ditingkatkan hingga 1,5% ukuran kristal makin membesar. Ini berarti Ni dengan kadar di atas 0,5% membentuk aglomerasi antar partikel pirhotit yang tidak dapat dicegah. Dengan demikian kadar 0 <Ni<
alum inium dalam besi akan menghambat pertumbuhan kristal pirhotit yang terbentuk. Dengan melakukan hal yang sama seperti pada campuran biner besi nikel, maka pengaruh aluminium terhadap pertumbuhan kristal pirhotit dapat ditentukan, seperti terlihat pada Gambar 11. Kadar aluminium dalam campuran mulai dari 0%-11% dan suhu reaksi sulfidasi pada T 400 °C.
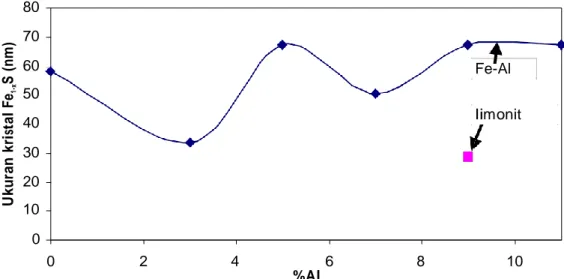
Pada Gambar 11 menunjukkan bahwa meskipun terjadi fluktuasi sinusoidal ukuran kristal pirhotit, namun ada kecenderungan terjadi kenaikan ukuran kristal tersebut terhadap bertambahnya kadar alu- minium dalam campuran. Pada Al<4%, ukuran kristal yang dihasilkan adalah 33,6 nm. Al 11% menghasilkan ukuran kristal pirhotit 67 nm, hampir sama nilainya bila hanya menggunakan oksida besi
U kur a n kr is ta l Fe 1 -x S ( n m ) 80.00 70.00 60.00 400oC Limonit- Pomalaa 50.00 40.00 30.00 20.00 10.00 0.00 0.00 0.20 0.40 0.60 0.80 1.00 1.20 1.40 1.60 1.80 2.00 %Ni
Gambar 9. Pengaruh kadar nikel dalam katalis terhadap ukuran kristal pirhotit.
Gambar 10. Komposisi logam pada limonit Soroako berdasarkan lapisannya (BPPT and Kobe Steel, 2000)
saja (Al 0%). Dari gambar tersebut kelihatannya aglomerasi partikel pirhotit tidak dapat dicegah ketika Al>4%. Namun, ketika menggunakan limonit dengan kadar Al 9% menghasilkan ukuran kristal pirhotit hanya 28,8 nm (Gambar 11), menunjukkan tidak terjadinya aglomerasi. Ukuran kristal seperti
ini tidak diperoleh dari katalis dari campuran Fe+Al untuk seluruh rentang kadar Al yang digunakan. Dengan demikian bila dibandingkan dengan nikel, aluminium memiliki kemampuan menghambat aglomerasi yang lebih kecil dibandingkan dengan nikel.
U k u ra n k ri st a l Fe 1 -x S ( n m ) 80 70 60 Fe-Al 50 40 limonit 30 20 10 0 0 2 4 6 8 10 %Al
Gambar 11. Pengaruh kadar aluminium dalam katalis terhadap ukuran kristal pirhotit
Dari data tersebut, dapat dinyatakan bahwa ukuran kristal limonit yang relatif kecil itu dominan hanya disebabkan oleh keberadaan nikel saja, tidak oleh aluminium. Aluminium berperan untuk meredam pertumbuhan kristal pirhotit bila kadarnya <4%. Percobaan ini baru menjawab pengaruh unsur nikel dan aluminium dalam campuran biner. Bila dalam campuran tersier, besi aluminium dan nikel belum dapat diketahui dengan pasti.
4. KESIMPULAN
Dari hasil percobaan ini dapat disimpulkan sebagai berikut:
– Kadar nikel yang dianjurkan untuk pencairan batubara tidak lebih dari 0,5%, karena tidak memberikan perbesaran ukuran kristal melebihi 40 nm. Kadar nikel lebih dari 0,5% mengakibatkan ukuran kristal pirhotit membesar hingga 67 nm. – Kadar aluminium yang dapat digunakan pada
campuran biner adalah di bawah 4%.
UCAPAN TERIMAKASIH
Penulis mengucapkan terimakasih kepada Hermanu Prijono, Manik Astiti, Tatang Wahyudi dan rekan lainnya yang telah membantu dalam proses pengujian sulfidasi dan analisis XRD maupun SEM dan EDS.
DAFTAR PUSTAKA
BPPT dan Kobe Steel, 2000. Research Cooperation on Coal Liquefaction Technology, Report. Cugini, A.V., Krastman, D., Lett, R. G., dan Balsone,
V. D., 1994. Development of a dispersed iron catalyst for first stage coal liquefaction, Cataly-
sis Today 19, 395-408.
Hirano, K. and Kanda, Y., 2001. Study on industrial catalyst for Bituminous Coal Liquefaction, Fuel
Processing Technology 72, 35-45.
Ikenaga, N., Taniguchi, H., Watanabe, A., Suzuki, dan T., 2000. Sulfiding Behavior of Iron Based Coal Liquefaction Catalyst, Fuel 79, 273-283. Kaneko, T., Sugita, S., Tamura, M., Shimasaki, K.,
Makino, E., and Silalahi, L. H., 2000. Effect of Highly Dispersed Iron Catalyst on Direct Liq- uefaction of Coal, Fuel 79, 263-271.
Kaneko, T., Tazawa, K., Okuyama, N., Tamura, M., and Shimasaki, K., 2002. Highly Active Limo- nite Catalysts for Direct Coal Liquefaction, Fuel
81, 1541-1549.
Klug, H.P. and Alexander, L.E., 1978. X-Ray Dif-
fraction Procedures for Polycrystalline and Amor- phous Materials, New York, John Wiley & Sons