Nurbayani, Asriyani. 2014
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA BAKTERIAL DARI LIMBAH KULIT NANAS
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA
BAKTERIAL DARI LIMBAH KULIT NANAS
SKRIPSI
Diajukan untuk Memenuhi Sebagian dari Syarat Memperoleh
Gelar Sarjana Sains Program Studi Kimia
Oleh
Asriyani Nurbayani
1001119
PROGRAM STUDI KIMIA JURUSAN PENDIDIKAN KIMIA
FAKULTAS PENDIDIKAN MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS PENDIDIKAN INDONESIA
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA
BAKTERIAL DARI LIMBAH KULIT NANAS
Oleh
Asriyani Nurbayani
Sebuah skripsi yang diajukan untuk memenuhi salah satu syarat
memperoleh gelar Sarjana Sains pada
Fakultas Pendidikan Matematika dan Ilmu Pengetahuan Alam
© Asriyani Nurbayani 2014
Universitas Pendidikan Indonesia
Oktober 2014
Hak Cipta dilindungi undang-undang.
Skripsi ini tidak boleh diperbanyak seluruhnya atau sebagian, dengan dicetak
ASRIYANI NURBAYANI
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA
BAKTERIAL DARI LIMBAH KULIT NANAS
DISETUJUI DAN DISAHKAN OLEH :
Pembimbing I
H. Budiman Anwar, S.Si, M.Si NIP. 197003131997031004
Pembimbing II
Dr.rer.nat. Ahmad Mudzakir, M.Si NIP. 1966112111991031002
Mengetahui,
Ketua Jurusan Pendidikan Kimia FPMIPA UPI
Nurbayani, Asriyani. 2014
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA BAKTERIAL DARI LIMBAH KULIT NANAS
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
ABSTRAK
Penelitian ini bertujuan untuk mengetahui waktu optimum isolasi nanokristalin selulosa bakterial dari limbah kulit nanas dan memperoleh nanokristalin selulosa bakterial serta karakterisasinya berdasarkan interpretasi data spektroskopi Fourier Transform InfraRed (FTIR), Transmission Electron Microscopy (TEM), dan X-Ray Diffraction (XRD). Sumber selulosa bakterial yang digunakan berasal dari hasil fermentasi bakteri Acetobacter xylinum. Metode yang digunakan untuk isolasi nanokristalin selulosa bakterial dengan cara hidrolisis menggunakan asam sulfat. Beberapa faktor yang mempengaruhi proses hidrolisis diantaranya konsentrasi asam, waktu hidrolisis, rasio selulosa bakterial/asam dan suhu. Variasi waktu hidrolisis selama yaitu 5; 15; 25; 35; dan 45 menit. Hasil penelitian menunjukkan bahwa waktu hidrolisis optimum untuk isolasi nanokristalin selulosa bakterial dari limbah kulit nanas adalah 25 menit. Volume sol koloid nanokristalin selulosa bakterial yang dihasilkan sebanyak 70,20 mL. Hasil FTIR nanokristalin selulosa bakterial menunjukkan kemiripan gugus fungsi dengan selulosa bakterial limbah kulit nanas serta adanya sedikit perubahan struktur akibat perlakuan hidrolisis yaitu munculnya puncak serapan gugus fungsi C=C pada bilangan gelombang 1656,85 – 1627,92 cm-1 dan diperkuat dengan munculnya puncak serapan C-H sp2 vibrasi ulur pada bilangan gelombang 3132,40 cm-1 karena terjadinya proses eliminasi. Hasil TEM menunjukkan ukuran nanokristalin selulosa bakterial yang dihasilkan mempunyai dimensi rerata panjang 200 – 750 nm, lebar 10 – 25 nm dan aspek rasio 10 – 30 dengan bentuk partikel jarum. Besarnya aspek rasio yang didapatkan berpotensi untuk dijadikan reinforcing nanofiller pada polimer. Hasil pengukuran XRD diperoleh derajat kristalinitas sebesar 63,70%.
Kata Kunci : nanokristalin bakterial selulosa, bakterial selulosa, hidrolisis asam
ABSTRACT
Nurbayani, Asriyani. 2014
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA BAKTERIAL DARI LIMBAH KULIT NANAS
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
nanocrystalline can be use as a reinforcing nano-filler for various composite. Result of XRD pattern showed that degree of crystallinity bacterial cellulose nanocrystalline were 63.70%.
Nurbayani, Asriyani. 2014
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA BAKTERIAL DARI LIMBAH KULIT NANAS
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
DAFTAR ISI
ABSTRAK ... i
KATA PENGANTAR ... ii
UCAPAN TERIMA KASIH ... iii
DAFTAR ISI ... v
DAFTAR GAMBAR ... viii
DAFTAR TABEL ... ix
DAFTAR LAMPIRAN ... x
BAB I PENDAHULUAN 1.1. Latar Belakang ... 1
1.2. Perumusan Masalah ... 4
1.3. Tujuan Penelitian ... 4
1.4. Pembatasan Penelitian ... 4
1.5. Manfaat Penelitian. ... 5
1.6. Struktur Organisasi ... 5
BAB II TINJAUAN PUSTAKA 2.1. Limbah Kulit Nanas ... 6
2.2 . Selulosa ... 7
2.2.1. Selulosa Bakterial ... 8
2.2.2. Selulosa Bakterial Nata de Pina ... 11
2.3. Isolasi Nanokristalin Selulosa Bakterial ... 12
2.4. Uji Karakterisasi ... 16
2.4.1. Fourier Transform Infra Red (FTIR) ... 16
2.4.2. Scanning Electron Microscopy (SEM) dan Transmission Electron Microscopy (TEM) ... 17
2.4.3. X-Ray Diffraction (XRD) ... 17
BAB III METODOLOGI PENELITIAN 3.1. Waktu dan Lokasi Penelitian ... 19
3.2. Desain Penelitian ... 19
3.3. Alat dan Bahan ... 22
3.3.1. Alat ... 22
Nurbayani, Asriyani. 2014
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA BAKTERIAL DARI LIMBAH KULIT NANAS
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
3.4. Prosedur Penelitian ... 22
3.4.1. Sintesis Selulosa Bakterial dari Limbah Kulit Nanas ... 22
3.4.1.1. Pembuatan Sari Limbah Kulit Nanas ... 22
3.4.1.2. Fermentasi Sari Limbah Kulit Nanas Menggunakan Bakterial (Susanto, et.al., 2000) ... 23
3.4.1.3. Pemurnian Selulosa Bakterial dari Limbah Kulit Nanas 23 3.4.2. Karakterisasi Selulosa Bakterial Limbah Kulit Nanas ... 23
3.4.2.1. Randemen ... 23
3.4.2.2. Analisis Gugus Fungsi dengan FTIR ... 24
3.4.2.3. Kadar Selulosa (Chesson A, 1981) ... 24
3.4.2.4. Analisis Morfologi Permukaan dengan SEM ... 24
3.4.3. Isolasi Nanokristalin Bakterial Selulosa dari LimbahKulitNanas ... 25
3.4.3.1. Hidrolisi Selulosa Bakterial Menggunakan Asam ... 25
3.4.3.2. Proses Sentrifugasi ... 25
3.4.3.3. Dialisis ... 25
3.4.3.4. Sonikasi ... 25
3.4.3.5. Penentuan Kondisi Optimum ... 26
3.4.4. Karakterisasi Nanokristalin Selulosa Bakterial dari Limbah Kulit Nanas ... 26
3.4.4.1. Analisis Gugus Fungsi Menggunakan FTIR ... 26
3.4.4.2. Efek Tyndall ... 26
3.4.4.3. Analisis Morfologi Permukaan dan Ukuran Partikel dengan TEM ... 26
3.4.4.4. Analisis Penentuan Derajat Kristalinitas Menggunakan XRD ... 27
BAB IV HASIL PENELITIAN DAN PEMBAHASAN 4.1. Sintesis Selulosa Bakterial dari Limbah Kulit Nanas ... 28
4.2. Karakterisasi Selulosa Bakterial dari Limbah Kulit Nanas ... 31
4.2.1. Randemen ... 31
4.2.2. Analisis Gugus Fungsi Menggunakan FTIR ... 32
4.2.3. Kadar Selulosa ... 33
4.2.4. Analisis Morfologi Permukaan Menggunakan SEM ... 33
4.3. Isolasi Nanokristalin Selulosa Bakterial dari Limbah Kulit Nanas ... 33
4.3.1. Hidrolisis Selulosa Bakterial Menggunakan Asam ... 33
4.3.2. Sentrifugasi ... 34
4.3.3. Dialisis ... 35
4.3.4. Sonikasi ... 35
4.3.5. Penentuan Kondisi Optimum ... 35
4.4. Karakterisasi Selulosa Bakterial ... 36
4.4.1. Efek Tyndall... 36
Nurbayani, Asriyani. 2014
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA BAKTERIAL DARI LIMBAH KULIT NANAS
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
4.4.3. Analisis Gugus Fungsi Menggunakan FTIR ... 38
4.4.4. Analisis Penentuan Derajat Kristalinitas Menggunakan XRD .... 40
BAB V KESIMPULAN DAN SARAN 5.1. Kesimpulan ... 41
5.2. Saran. ... 41
DAFTAR PUSTAKA ... 42
Nurbayani, Asriyani. 2014
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA BAKTERIAL DARI LIMBAH KULIT NANAS
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
BAB I
PENDAHULUAN
1.1. Latar Belakang Masalah
Polimer bahan baku berbasis petroleum semakin hari semakin dibatasi
penggunaannya disebabkan polimer berbahan baku petroleum bersifat tidak
terbarukan, tidak dapat terbiodegradasi, tidak berkelanjutan, dan mencemari
lingkungan. Akhir-akhir ini kimiawan melakukan penelitian tentang pemanfaatan
biomassa selulosa sebagai kandidat material biopolimer berbasis non-petroleum
yang mempunyai kelebihan diantaranya terbarukan, dapat terbiodegradasi, tidak
beracun, ramah lingkungan, berkelanjutan dan biocompatible (Eichhorn, 2010).
Indonesia merupakan paru-paru dunia karena hutannya yang begitu luas
sehingga Indonesia memiliki tanaman tinggi sebagai sumber kekayaan alam
selulosa yang melimpah, pengguaan tanaman tingkat tinggi sebagai sumber
selulosa secara terus menerus berpotensi mengakibatkan kerusakan alam seperti
pemanasan global, bencana banjir, dan tanah longsor. Upaya mengurangi dampak
negatif tersebut diperlukan alternatif lain penghasil serat selulosa.
Buah nanas (Ananas comocus) merupakan salah satu tanaman buah yang
banyak dibudidayakan di daerah tropis dan subtropis. Produksi buah nanas
mengalami pertumbuhan yang sangat pesat untuk setiap tahunnya. Satu buah
nanas yang dapat dikonsumsi hanya 53%-nya saja, sedangkan sisanya berupa
limbah. Apabila limbah tersebut dibiarkan menumpuk begitu saja tanpa
mengalami pengolahan lebih lanjut maka akan menimbulkan permasalahan
terhadap lingkungan, sehingga diperlukan upaya pemanfaatan limbah kulit nanas.
Telah dilakukan berbagai usaha untuk mengolah limbah kulit nanas
tersebut, seperti diolah menjadi pupuk organik dan pakan ternak. Limbah kulit
nanas juga dapat diolah lebih lanjut menjadi produk nata de pina. Adanya
kandungan gula dalam limbah kulit nanas dapat dimanfaatkan sebagai media
2
Nata merupakan biomassa selulosa yang berasal dari mikrobakterial,
berbentuk agar, dan berwarna putih. Selulosa ini dikenal dengan istilah selulosa
bakterial (Bacterial cellulose atau BC). Nata dihasilkan dari hasil sekresi
Acetobacter xylinum sebagai metabolit sekunder. Selain itu, selulosa bakterial
diproduksi untuk melindingi sel-sel bakteri dari sinar ultraviolet dan udara
lembab. Penelitian produksi nata de pina telah dibahas tuntas sebelumnya oleh
Susanto et al., (2000) dan Rulianah (2002). Bakterial selulosa mempunyai
beberapa keunggulan antara lain : kemurnian dan kristalinitas yang tinggi, sifat
mekanik dan termal yang baik, kapasitas penyerapan air yang tinggi, sifat
hidrofilik yang sangat tinggi, dan dapat diproduksi dari berbagai macam susbstrat
yang relatif mudah serta murah (Tresnawati, 2006). Bakterial selulosa juga
mempunyai kelebihan yaitu mudah untuk dimurnikan, karena tidak melibatkan
biomassa yang lain seperti lignin, pektin dan hemiselulosa.
Jika dibandingkan dengan selulosa, nanokristalin selulosa mempunyai
beberapa kelebihan diantaranya: kekuatan tarik dan modulus yang tinggi, luas
permukaan yang tinggi, sifat optik yang unik, dan lain-lain (Peng, B.L., et.al.,
2011). Beberapa peneliti sebelumnya telah melakukan isolasi nanokristalin
selulosa dengan cara hidrolisis asam dari berbagai sumber selulosa seperi kain
katun (Chang, et.al., 2010), ramie (de Menezes, et.al., 2009), bambu (Brito, et.al.,
2012), bakteri (Roman dan Winter, 2004), microcrystalline cellulose (Panger and
Tannenbaum, 2008), tunicate (de Souza Lima, et.al., 2003). Pada penelitian
sebelumnya Hestrin-Scharmm, et.al. (1954) telah mensintesis selulosa bakterial
dengan medium yang mengandung peptone dan ekstrak ragi. Akan tetapi
penggunaan medium tersebut dalam skala besar akan meningkatkan biaya
produksi sehingga diperlukan medium yang mempunyai biaya produksi yang
lebih murah untuk menghasilkan selulosa bakterial. Castro et.al (2010) telah
berhasil membandingkan karakteristik struktur selulosa bakterial dari medium
Hestrin-Scharmm, et.al. (1954) dengan medium limbah agroindustri yang
bersumber dari media limbah tebu dan kulit nanas. Penelitian isolasi nanokristalin
selulosa dari limbah kulit nanas belum dilakukan sehingga peneliti akan
3
Penerapan nanokristalin selulosa pada umumnya digunakan dalam
berbagai keperluan khususnya perkembangan ilmu pengetahuan nano teknologi.
Hasil perkembangan ilmu pengetahuan nano teknologi dapat diaplikasi dibeberapa
industri seperti industri cat, film, perekat, material penguat dalam biopolimer,
sintetik fiber, kosmetik, obat-obatan, alat optik, katalis, hidrogel, dan lainnya.
Nanokristalin selulosa dapat diisolasi dengan menggunakan berbagai
metode. Berbagai peneliti telah melakukan isolasi dengan metode mekanik
maupun kimia. Metode mekanik seperti homogenizer (T. Zimmermann, et.al.,
2010) penggiling (S. Iwamoto, et.al., 2009), cryocrushing (Chakraborty, et.al.,
2005), high-pressure homogenization (Nikmatin, et.al., 2010), dan ultrasonikasi.
Sementara, metode kimia meliputi hidrolisis menggunakan asam kuat (Roman,
et.al., 2004; Wang, et.al., 2007), hidrolisis menggunakan enzim (George, et.al.,
2010), dan hidrolisis menggunakan cairan ionik (Man, et.al., 2011). Sebagian
peneliti menggabungkan beberapa metode seperti penggabungan antara metode
kimia dengan mekanik yang dilakukan oleh Ioelovich (2010) dan Bondenson
et.al., (2006).
Penggunaan metode mekanik memiliki kekurangan, untuk menghasilkan
ukuran partikel kurang dari 100 nm membutuhkan frekuensi tinggi dan waktu
yang cukup lama (Nikmatin, et.al., 2010). Hidrolisis menggunakan enzim
memiliki kelemahan seperti sulitnya isolasi enzim yang sesuai, tidak dapat
digunakan kembali, dan stabilitas termal yang rendah sehingga akan menaikan
biaya produksi (Rodiansono, et.al., 2013). Sama halnya dengan hidrolisis
menggunakan enzim, hidrolisis menggunakan cairan ionik memiliki kekurangan
seperti mahalnya cairan ionik yang dapat meningkatkan biaya produksi. Maka,
alternatif lain untuk isolasi nanokristalin selulosa dalam menyelesaikan
permasalahan tersebut adalah hidrolisis menggunakan asam yang mempunyai
biaya produksi yang lebih murah.
Isolasi nanokristalin selulosa dengan metode hidrolisis asam dipengaruhi
beberapa faktor, seperti: konsentrasi asam, waktu hidrolisis, rasio bakterial
selulosa/asam, suhu, dan kecepatan pengadukan (Pang, et.al., 2011). Pada
4
selulosa dari limbah kulit nanas dengan variasi waktu hidrolisis selama 5 menit,
15 menit, 25 menit, 35 menit, dan 45 menit.
1.2. Perumusan Masalah
Berdasarkan uraian yang telah dikemukan di atas, rumusan masalah
penelitian ini adalah sebagai berikut:
1. Berapa waktu hidrolisis optimum untuk isolasi nanokristalin selulosa bakterial
dari limbah kulit nanas dengan hidrolisis asam?
2. Bagaimana karakteristik nanokristalin selulosa bakterial dari limbah kulit
nanas yang didapat berdasarkan interpretasi data FTIR, TEM, dan XRD?
1.3. Tujuan Penelitian
Tujuan penelitian ini adalah :
1. Mengetahui waktu hidrolisis optimum untuk isolasi nanokristalin selulosa
bakterial dari limbah kulit nanas dengan hidrolisis asam.
2. Memperoleh nanokristalin selulosa bakterial beserta karakteristiknya
berdasarkan interpretasi data FTIR, TEM, dan XRD.
1.4. Batasan Penelitian
Agar tujuan penelitian ini dapat tercapai maka perlu dijelaskan tentang
pembatasan masalah yang akan diteliti. Pembatasan masalah yang terdapat dalam
penelitian ini adalah:
1. Bakteri yang digunakan adalah Acetobakter xylinum untuk menghasilkan
bahan baku selulosa bakterial.
2. Larutan asam yang digunakan yaitu H2SO4 dengan konsentrasi 50%, rasio bakterial selulosa/asam 1:50, dan suhu 50oC.
3. Variasi waktu hidrolisis yaitu 5 menit, 15 menit, 25 menit, 35 menit, dan 45
menit
4. Waktu hidrolisis optimum ditentukan dari hasil nanokristalin selulosa yang
diperoleh (volume) dan ukuran partikelnya.
5. Pada penelitian ini limbah kulit nanas yang digunakan berasal dari perkebunan
5
1.5. Manfaat Penelitian
1. Memperoleh nanomaterial dari sumber yang murah dan ramah lingkungan.
2. Hasil yang diperoleh dari penelitian ini diharapkan mampu memberikan
sumbangan pada perkembangan ilmu pengetahuan teknologi industri
nanokomposit biopolimer di Indonesia khususnya dalam bidang
nanoteknologi.
1.6. Struktur Organisasi Skripsi
Struktur organisasi skripsi terdiri dari lima bab yaitu bab I berisi tentang
pendahuluan, bab II berisi tentang tinjauan pustaka, bab III berisi tentang metode
penelitian, bab IV berisi tentang hasil dan pembahasan, dan bab V berisi tentang
kesimpulan dan saran. Sistematika penulisan skripsi ini adalah sebagai berikut:
BAB I PENDAHULUAN
Terdiri dari latar belakang, perumusan masalah, tujuan
penelitian, batasan penelitian, manfaat penelitian, dan
struktur organisasi skripsi.
BAB II TINJAUAN PUSTAKA
Berisi tinjauan pustaka yang membahas tentang limbah
kulit nanas, selulosa, isolasi nanokristalin selulosa bakterial,
dan uji karakterisasi.
BAB III METODOLOGI PENELITIAN
Terdiri dari waktu dan lokasi penelitian, desain penelitian,
alat dan bahan, serta prosedur penelitian.
BAB IV HASIL DAN PEMBAHASAN
Berisi hasil sintesis dan karakterisasi selulosa bakterial dari
limbah kulit nanas, dan hasil isolasi dan karakterisasi
nanokristalin selulosa bakterial dari limbah kulit nanas.
6
Berisi kesimpulan yang dapat diambil dari penelitian serta
Nurbayani, Asriyani. 2014
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA BAKTERIAL DARI LIMBAH KULIT NANAS
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
BAB III
METODOLOGI PENELITIAN
3.1. Waktu dan Lokasi Penelitian
Pelaksanaan penelitian dimulai dari bulan Februari sampai Juni 2014.
Sintesis selulosa bakterial dan isolasi nanokristalin selulosa bakterial dari limbah
kulit nanas di Laboratorium Riset Kimia Material dan Hayati Jurusan Pendidikan
Kimia FPMIPA Universitas Pendidikan Indonesia. Pengujian Fourier Transform
Infra Red (FTIR), dan Scanning Electron Microscopy (SEM) dilakukan di
Laboratorium Kimia Material Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Teknologi Bandung, X-ray Diffraction (XRD) dilakukan di Laboratorium
Teknik Kimia Institut Teknologi Bandung, dan pengujian Transmission Electron
Microscopy (TEM) dilakukan di Laboratorium Kimia Universitas Gajah Mada.
3.2. Desain Penelitian
Penelitian dibagi dalam empat tahap, yaitu sintesis dan karakterisasi
selulosa bakterial dari limbah kulit nanas, isolasi nanokristalin selulosa bakterial
dan karakterisasi nanokristalin selulosa bakterial.
Sintesis selulosa bakterial terdiri dari pembuatan sari limbah kulit nanas,
fermentasi sari limbah kulit nanas menggunakan bakteri, pemurnian selulosa
bakterial limbah kulit nanas. Karakterisasi selulosa bakterial meliputi randemen
dan kadar selulosa, gugus fungsi (FTIR), dan morfologi permukaan dan ukuran
partikel (SEM). Isolasi nanokristalin selulosa bakterial limbah kulit nanas terdiri
dari hidrolisis selulosa bakterial menggunakan asam, sentrifugasi, dialisis, dan
sonikasi. Karakterisasi isolasi nanokristalin bakterial selulosa meliputi analisis
gugus fungsi (FTIR), morfologi permukaan dan ukuran partikel (TEM), dan
20
Secara keseluruhan penelitian yang dilakukan berdasarkan desain pada
bagan alir berikut :
Dipotong menjadi bagian kecil Direbus selama ± 20 menit
Direndam dalam larutan NaOH 1% selama 24 jam
Direndam dalam larutan CH3COOH 1% selama 24 jam Direndam dalam aquades selama
24 jam
Dkeringkan dengan oven pada suhu 50oC
Dihancurkan hingga 100 mesh Dicuci dengan air hingga bersih Dipotong menjadi bagian kecil Dihancurkan dengan blender Diperas dan disaring
Diencerkan 1:4 (sari nanas : air) Dididihkan
Ditambahkan gula pasir 7,5%, ammonium sulfat 0,5%
Didinginkan pada suhu kamar selama 24 jam
Ditambahkan starter Acetobacter xylinum 10%
Difermentasi selama 10 hari
Selulosa bakterial Limbah kulit nanas
Sari kulit nanas
Uji randemen dan kadar selulosa Karakterisasi
FTIR, SEM
21
Gambar 3.1. Diagam Alir Sintesis Selulosa Bakterial Limbah Kulit Nanas
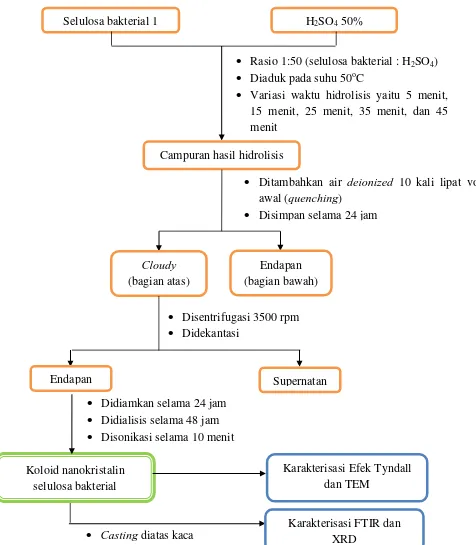
Rasio 1:50 (selulosa bakterial : H2SO4) Diaduk pada suhu 50oC
Variasi waktu hidrolisis yaitu 5 menit, 15 menit, 25 menit, 35 menit, dan 45 menit
Disentrifugasi 3500 rpm Didekantasi
Didiamkan selama 24 jam Didialisis selama 48 jam Disonikasi selama 10 menit
Ditambahkan air deionized 10 kali lipat volume awal(quenching)
Disimpan selama 24 jam
Koloid nanokristalin selulosa bakterial
Karakterisasi Efek Tyndall dan TEM
H2SO4 50% Selulosa bakterial 1
Campuran hasil hidrolisis
Endapan Supernatan
Endapan (bagian bawah) Cloudy
(bagian atas)
Casting diatas kaca
[image:17.595.66.542.215.760.2]22
Gambar 3.2. Diagam Alir Isolasi Nanokristalin Selulosa Bakterial dari Limbah Kullit
23
3.3. Alat dan Bahan
3.3.1. Alat
Peralatan yang digunakan untuk tahapan preparasi selulosa bakterial dan
isolasi nanokristalin selulosa bakterial dari limbah kulit nanas antara lain: pisau,
blender, panci aluminium, kompor listrik, wadah plastik ukuran 30 cm x 50 cm
dan tinggi 5 cm, alat-alat gelas, kaca arloji, spatula, oven, neraca analitik,
saringan 100 mesh, satu set alat refluks, corong buchner, pengaduk magnetik,
botol vial, pemanas listrik, termometer raksa, wrapping plastic, satu set pompa
vacuum, satu set sentrifugator, dan satu set reaktor hidrolisis. Instrumen untuk
karakterisasi digunakan FTIR, SEM, TEM dan XRD.
3.3.2. Bahan
Bahan-bahan yang digunakan untuk tahapan preparasi selulosa bakterial
dan isolasi nanokristalin selulosa bakterial dari limbah kulit nanas antara lain:
limbah kulit nanas yang didapatkan dari pedagang di depan kampus Universitas
Pendidikan Indonesia, gula pasir, amonium sulfat ((NH4)2SO4) (E. Merck), alkohol 95%, NaOH 1% (E. Merck), CH3COOH glasial (E. Merck), H2SO4 97% (E.Merck), biakan bakteri Acetobacter xylinum, kertas saring whatmann, pH
indicator, air, aquades, air deionized (E.Merck), dan membran semipermeabel
(Cellu-Sep®; MWCO 12,000-14,000. Membrane Filtration Products, Inc. TXS,
USA).
3.4. Prosedur Penelitian
3.4.1. Sintesis Selulosa Bakterial dari Limbah Kulit Nanas
Sintesis selulosa bakterial terdiri dari beberapa tahap diantaranya:
pembuatan sari limbah kulit nanas, fermentasi dengan bakteri, serta pemurnian
selulosa bakterial limbah kulit nanas.
3.4.1.1. Pembuatan Sari Limbah Kulit Nanas
Sebanyak 5 kg limbah kulit nanas dicuci menggunakan air bersih,
dipotong menjadi bagian kecil, diblender, dan disaring menggunakan kain hingga
24
3.4.1.2. Fermentasi Sari Limbah Kulit Nanas Menggunakan Bakteri
(Susanto, et.al 2000)
Sari limbah kulit nanas yang diperoleh sebanyak 5 liter. Diencerkan
hingga perbandingan sari kulit nanas: air (1:4). Larutan direbus sampai mendidih,
kemudian ditambahkan gula pasir 7,5% (b/v) dan (NH4)2SO4 0,5% (b/v). Larutan medium nata ini dimasukkan ke dalam wadah plastik berukuran 30 cm x 50 cm
dan tinggi 5 cm yang telah disterilkan terlebih dahulu dengan alkohol dan sinar
UV. Larutan medium nata ini segera ditutup menggunakan koran yang telah
disterilkan dan diikat dengan karet, kemudian disimpan selama 24 jam pada suhu
ruangan dan ditambahkan starter Acetobacter xylinum sebanyak 10% (v//v)
kedalam medium nata yang benar-benar telah dingin. Bakteri dibiarkan
berfermentasi selama 10 hari.
3.4.1.3. Pemurnian Selulosa Bakterial dari Limbah Kulit Nanas (Safriani,
2000)
Selulosa bakterial dipotong-potong menjadi bagian kecil kemudian direbus
selama ±20 menit. Selulosa bakterial yang telah direbus kemudian direndam
dalam larutan NaOH 1% (v/v) selama 24 jam. Setelah itu, direndam kembali
menggunakan larutan CH3COOH 1% (v/v) selama 24 jam pada suhu ruangan, dan aquades selama 24 jam. Setelah proses perendaman selesai selulosa bakterial
disaring menggunakan vacuum evaporator untuk menghilangkan air hingga
diperoleh lembaran selulosa bakterial yang tipis. Lembaran tipis tersebut
dikeringkan dalam oven pada suhu 50oC dan dihancurkan dengan blender, dan disaring dengan saringan 100 mesh hingga didapatkan serbuk selulosa bakterial.
3.4.2. Karakterisasi Selulosa Bakterial dari Limbah Kulit Nanas
3.4.2.1. Randemen
Randemen selulosa bakterial yang dihasilkan terhadap 5 kg kulit nanas
dihitung dengan cara menimbang serbuk selulosa kering. Persen randemen yang
diperoleh dihitung menggunakan persamaan berikut :
25
3.4.2.2. Analisis Gugus Fungsi Menggunakan FTIR
Sampel selulosa bakterial yang dihasilkan dilakukan identifikasi gugus
fungsi menggunakan instrumen FTIR. Sampel berbentuk padatan dibuat pelet.
Pelet KBr dibuat dengan menggerus sampel dan kristal KBr (0.1-2.0 % berdasar
berat) sehingga merata kemudian ditekan (hingga 8 ton) sampai diperoleh pelet.
Pelet siap untuk dianalisis.
3.4.2.3. Kadar Selulosa (Chesson A, 1981)
Disiapkan satu gram selulosa kering (Berat A) ditambahkan aquades 150
mL, direfluks pada suhu 100oC selama satu jam. Hasil refluks disaring menggunakan pompa vacuum dan dicuci menggunakan air panas 300 mL,
dikeringkan menggunakan oven hingga diperoleh berat konstan (Berat B). Residu
B ditambahkan H2SO4 1N sebanyak 150 mL direfluks selama satu jam pada suhu 100oC. Hasil refluks disaring menggunakan pompa vacuum dan dicuci menggunakan aquades hingga diperoleh pH netral, kemudian dikeringkan
menggunakan oven hingga diperoleh berat konstan (Berat C). Residu C yang
diperoleh ditambahkan H2SO4 72% sebanyak 100 mL dan direndam pada suhu ruangan selama 4 jam. Selanjutnya residu ditambahkan H2SO4 1N sebanyak 150 mL selama satu jam. Hasil refluks disaring menggunakan pompa vacuum dan
dicuci menggunakan aquades hingga diperoleh pH netral, kemudian dikeringkan
menggunakan oven pada suhu 60oC hingga diperoleh berat konstan (Berat D). Kadar selulosa yang dihasilkan dihitung menggunakan persamaan berikut :
3.4.2.4. Analisis Morfologi Permukaan Menggunakan SEM
Sampel yang akan dipelajari dan akan diambil gambarnya dengan SEM
harus bersifat konduktif, dan arena pengoperasian SEM berlangsung dalam
vacuum maka sampel harus bebas air dan lemak. Untuk sampel yang tidak
26
Prosedur sputtering sampel nonkonduktif ini adalah sebagai berikut: Sampel
dibersihkan, dikeringkan dengan vacuum hingga bebas H2O, dan sampel ditempatkan pada sampel holder. Ukuran sampel holder adalah 12 mm atau 25
mm. Diperlukan double-side tape konduktif untuk menempelkan sampel dengan
area sudut 45 derajat.
3.4.3. Isolasi Nanokristalin Bakterial Selulosa dari Limbah Kulit Nanas
Proses isolasi nanokristalin bakterial selulosa terdiri dari beberapa tahap
diantarnya: proses hidrolisis menggunakan asam kuat H2SO4, sentrifugasi, dialisis, sonikasi, dan penentuan kondisi optimum
3.4.3.1. Hidrolisis Selulosa Bakterial Menggunakan Asam
Larutan H2SO4 50% dimasukan 50 mL kedalam reaktor, diaduk hingga campuran reaktor homogen pada suhu 50oC. Kemudian ditambahkan 1 gram serbuk selulosa hingga perbandingan selulosa bakterial/asam (1:50). Hasil
hidrolisis dilakukan quenching menggunakan air deionized 500 mL dan disimpan
dalam lemari pendingin selama 24 jam.
3.4.3.2. Proses Sentrifugasi
Hasil quenching terbentuk dua bagian yaitu cloudy (bagian atas) dan
endapan (bagian bawah). Cloudy yang dihasilkan dipisahkan kemudian
disentrifugasi dengan kecepatan 3500 rpm hingga diperoleh endapan. Endapan
dicuci dengan aquades ditampung ke dalam gelas kimia.
3.4.3.3. Dialisis
Endapan yang telah disentrifugasi dibiarkan selama 24 jam. Endapan yang
diperoleh didekantasi dan dimasukan ke dalam membran dialisis yang berisi air
deionized. Proses dialisis dilakukan selama 48 jam pada suhu ruangan.
3.4.3.4. Sonikasi
Endapan hasil dialisis kemudian disonikasi selama 10 menit. Sonikasi
27
3.4.3.5. Penentuan Kondisi Optimum
Penelitian isolasi nanokristalin selulosa bakterial dilakukan variasi wkatu
hidrolisis. Variasi waktu hidrolisis yaitu 5 menit, 15 menit, 25 menit, 35 menit,
dan 45 menit.
3.4.4. Karakterisasi Nanokristalin Selulosa Bakterial dari Limbah Kulit
Nanas
3.4.4.1. Analisis Gugus Fungsi Menggunakan FTIR
Sampel nanokristalin selulosa bakterial yang dihasilkan dilakukan
identifikasi gugus fungsi menggunakan instrumen FTIR. Sampel nanokristalin
di-casting di atas kaca sehingga diperoleh serbuk nanokristalin selulosa bakterial.
Sampel berbentuk padatan dibuat pelet. Pelet KBr dibuat dengan menggerus
sampel dan kristal KBr (0.1 - 2.0 % berdasar berat) sehingga merata kemudian
ditekan (hingga 8 ton) sampai diperoleh pelet. Pelet siap untuk dianalisis.
3.4.4.2. Efek Tyndall
Sejumlah sampel koloid nanokristalin selulosa bakterial disimpan di
tempat gelap, kemudian sampel disinari menggunakan laser dalam beberapa detik
hingga terlihat adanya hamburan cahaya dari sampel koloid nanokristalin selulosa
bakterial tersebut.
3.4.4.3. Analisis Morfologi Permukaan dan Ukuran Partikel dengan TEM
Morfologi permukaan dan bentuk nanokristalin selulosa bakterial
dianalisis menggunakan TEM. Sampel yang akan dianalisis dan akan diambil
gambarnya menggunakan TEM harus bersifat konduktif, dan arena pengoperasian
TEM berlangsung dalam vakum maka sampel harus bebas air dan lemak. Untuk
sampel yang tidak konduktif, sampel harus di sputtering (dilapisi secara tipis)
dengan Au atau Pt. Prosedur sputtering sampel non konduktif ini adalah sebagai
berikut: Sampel dibersihkan, dikeringkan dengan vakum hingga bebas H2O, dan sampel ditempatkan pada sampel holder. Ukuran sampel holder adalah 12 mm
atau 25 mm. Diperlukan double-side tape konduktif untuk menempelkan sampel
28
3.4.4.4. Analisis Penentuan Derajat Kristalinitas Menggunakan XRD
Derajat kristalinitas dari nanokristalin selulosa bakterial dapat diketahui
dari hasil pengukuran menggunakan XRD. Sampel yang sudah terbebas dari
pengotor yang tidak diinginkan disiapkan, kemudian sampel dihaluskan. Sampel
yang telah dihaluskan diletakan pada sampel holder secara merata dengan
Nurbayani, Asriyani. 2014
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA BAKTERIAL DARI LIMBAH KULIT NANAS
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
BAB V
KESIMPULAN DAN SARAN
5.1. Kesimpulan
Berdasarkan penelitian yang telah dilakukan, dapat disimpulkan bahwa:
1. Waktu hidrolisis optimum isolasi nanokristalin selulosa bakterial dari
limbah kulit nanas pada kondisi konsentrasi H2SO4 50%, rasio selulosa bakterial/asam 1:50, suhu 50oC adalah 25 menit.
2. Hasil FTIR nanokristalin selulosa bakterial menunjukan kemiripan gugus
fungsi dengan selulosa bakterial limbah kulit nanas. Hasil TEM
nanokristalin selulosa bakterial yang dihasilkan mempunyai dimensi rerata
panjang 200 – 750 nm, rerata lebar 10 – 25 nm, dan aspek rasio 10-30
dengan bentuk partikel jarum. Besarnya aspek rasio yang didaptkan
berpotensi untuk dijadikan reinforcing nanofiller pada polimer. Hasil
pengukuran XRD diperoleh harga derajat kristalinitas sebesar 63,70%.
5.2. Saran
1. Diperlukan studi lebih lanjut untuk mengetahui kondisi optimum isolasi
nanokristalin selulosa bakterial dari limbah kulit nanas untuk berbagai
faktor lainnya seperti konsentrasi, rasio, dan suhu.
2. Diperlukan studi lebih lanjut untuk mengaplikasikan nanokristalin selulosa
Nurbayani, Asriyani. 2014
WAKTU OPTIMUM ISOLASI NANOKRISTALIN SELULOSA BAKTERIAL DARI LIMBAH KULIT NANAS
Universitas Pendidikan Indonesia | repository.upi.edu | perpustakaan.upi.edu
DAFTAR PUSTAKA
[BPS] Biro Pusat Statistika. (2007). Productiction of Fruit per Province (Ton) 2007. Tersedia: [Online]. http://bps.go.id/sector/agri/horti/2006/table6.html. [21 Mei 2013].
AAK. (1998). Bertanam Pohon Buah-Buahan. Kanisius. Yogyakarta.
Brito B. S. L., Pereira F. V., Putaux J, dan Jean B. (2012). Preparation, Morphologr and Struture of Cellulose Nanocrystals From Bamboo fibers. Cellulose, 19 : 1527-1536.
Castro C, Robin Z, Jean-Luc P, Gloria C, Inaki M, dan Piedad G. (2011). Structural Characterization Of Bacterial Cellulose Produced by Gluconacetobacter Swingsii Sp. From Colombian Agroindustrial Wates. Carbohydrate Polumers, 84: 96-102.
Chakraborty, A., Sain, M., Kortschot, M. (2005). Cellulose microfibrils: A novel method of preparation using high shear refining and cryocrushing. Holzforschung, 59: 102-107.
Chang C, Wang I, Hung K, Perng Y. (2010). Preparation and Characterization of Nanocrystalline Cellulose by Acid Hydrolysis of Catton Linter. Taiwan J Dor Sci, 25(3): 251-64.
de Menezes A. Jr., G. Siqueira, A. A. S. Curvelo dan A. Dufresne. (2009). Extrusion and Characterisation of Functionalised Cellulose Whiskers Reinforced Polyethylene Nanocomposite. Polymer, 50: 4552-4563.
de Souza Lima, M. M., J. T. Wong, M. Paillet, R. Borsali dan R. Pecora. (2003). Tranlational and Rotational Dynamics of Rodlike Cellulose Whiskers. Langmuir, 19: 24-29.
Eichhorn, Stephen J. (2011). Cellulose nanowhiskes: promising materials for advanced application. The Royal Society of Chemistry, 7: 303-315.
Fessenden Ralp J. dan Fessenden Joan S. (1986). Kimia Organik Edisi Ketiga. Jakarta: Erlangga.
43
Hestrin, S., dan Schramm, M. (2002). Synthesis of cellulose by Acetobacter Xylinum. 2. Preparation of freeze-dried cells capable of polumerizing glucose to cellulose. Biochemical Jounal, 58(2): 345-352.
Iguchi M., Yamanaka S., dan Budhiono A. (2000). R eview Bacterial Cellulose–A Masterpiece of Nature’s Art. J. Mater. Sci, 35: 261-270
Ioelovich Michael. (2012). Optimal Conditions for Isolation of Nanocrystalline Cellulose Particles. Nanoscience and Nanotechnology, 2(2): 9-13.
Man, Z., Muhammad, N., Sarwono, A., Bustam, M. A., Kumar, M. V., Rafiq, S. (2011). Preparation of Cellulose Nanocrystals Using an Ionic Liquid. J. Polym. Environ., 19: 726–731.
Moon, J Robert, Ashlie Martini, John Nairn, John Simonsen dan Jeff Youngnlood. (2011). Cellulose nanomaterials review: structure, properties and nanocomposites. Chem. Soc. Rev, 40: 3941-3994.
Nikmatin Siti, P. Setyo, M. Akhiruddin, M. Tieneke, dan P. Aris. (2010). Analisis Struktur Selulosa Kulit Rotan Sebagai Filler Bionanokomposit dengan Difraksi Sinar-X. Jurnal Sains Material Indonesia, 13(2): 97-102.
Park, S., Baker, J.O., Himmel, M. E., Parilla, P.A., dan Johnson, D. K. (2010). Cellulose Crystalinity Index : Measurement Techniques and Their Impact on Interpreting Cellulose Performance. Biotechnology for Biofuels, 3(10): 1-10.
Peng B. L., Dhar, N., Liu, H. L., Tam, K. C. (2011). Chemistry and Applications of Nanocrystalline Cellulose and its Derivatives: a Nanotechnology Perspective. chemical engineering, 9999: 1-16.
Phillips., G.O., dan Williams, P.A., 2000. Handbook of hidrocolloids. CRC Press.
Poedjiadi Anna dan F.M. Titin Supriyanti. (2009). Dasar-Dasar Biokimia. UI-Press. Universitas Indonesia.
Pranger, L., dan R. Tannenbaum. (2008). Biobased Nanocomposite Prepared by In Situ Polymerisation of Furfuryl Alcohol with Cellulose Whiskers or Montmorillonite Clay. Macromolecules, 41: 86821-8687.
Rodiansono, Utami U. B. Lili, W. Nana, Wulandari P. Catur, dan R. Ina. (2013). Hidrolisis Lignoselulosa Dari Tandan Kosong Kelapa Sawit Menggunakan Katalis Asam Karboksilat. Jurnal Sains dan Terapan Kimia, 7(1): 60-71.
Roman, M. dan W. T. Winter. (2004). Effect of Sulfate Groups from Sulfuric Acid Hydrolysis on the Thermal Degradation Behaviour of Bacterial Cellulose. Biomacromolecules, 5: 1671-1677.
44
S. Beck-Candanedo, M. Roman and D. G. Gray. (2005). Biomacromolecules, 6: 1048–1054.
S. Iwamoto, W.H. Kai, A, Isogai dan T.Iwatta. (2009). Biomacromolecules, 10: 2571-1576.
Susanto, et.al. (2000). Pembuatan Nata De Pina dari Kulit Nenas Kajian Dari Sumber Karbon dan Pengenceran Medium Fermentasi. Jurnal Teknologi Pertanian :58-66.
T. Zimmermann, N. Bordeanu dan E. Strub. (2010). Carbohydrate. Polymer, 76: 2080-2092.
Tresnawati Astika. (2006). Kajian Spektroskopi Infra Mera Transformasi Fourier dan Mikroskop Susuran Elektron Membran Selulosa Asetat dari Limbah Nanas. Skripsi Sarjana. Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor: tidak diterbitkan.
Wang Neng, Ding Enyong dan Cheng Rongshi. (2008). Preparation and Liquid Crystalline Properties of Spherical Cellulose Nanocrystals. Langmuir, 24: 5-8.