UJI KARAKTERISTIK MINYAK BIJI KELOR
(Moringa oleifera L.)
KARYA TULIS ILMIAH
Oleh :
Maria Yohana M. Kedang
PO. 530333215670
Karya Tulis Ilmiah ini diajukan sebagai salah satu persyaratan dalam menyelesaikan program pendidikan Ahli Madya Farmasi
KEMENTERIAN KESEHATAN REPUBLIK INDONESIA
POLITEKNIK KESEHATAN KEMENKES KUPANG
PROGRAM STUDI FARMASI
KUPANG
ii
LEMBAR PERSETUJUAN
KARYA TULIS ILMIAH
UJI KARAKTERISTIK MINYAK BIJI KELOR
( Moringa oleifera L.)
Oleh :
Maria Yohana Merika Kedang
PO. 530333215670
Telah disetujui untuk mengikuti ujian
Kupang, 23 juli 2018 Pembimbing
Marce I. Taku Bessi, S.Farm., Apt., M.Sc NIP. 197901051999032001
iii
LEMBAR PENGESAHAN
KARYA TULIS ILMIAH
UJI KARAKTERISTIK MINYAK BIJI KELOR
( Moringa oleifera L.)
Oleh :
Maria Yohana M. Kedang
PO. 530333215670
Telah dipertahankan di depan Tim Penguji Pada tanggal 24 Juli 2018
Susunan Tim Penguji 1. Dra. Elisma, Apt., M.si
2. Marce I. Taku Bessi, S.Farm., Apt., M.Sc
Karya Tulis Ilmiah ini telah diterima sebagai salah satu persyaratan untuk memperoleh gelar Ahli Madya Farmasi
Kupang, 24 Juli 2018 Ketua Prodi
Dra. Elisma, Apt., M.si NIP. 196507221995022001
iv
PERNYATAAN
Dengan ini saya menyatakan bahwa Karya Tulis Ilmiah Ini tidak terdapat karya yang pernah diajukan untuk memperoleh gelar kesarjanaan di suatu perguruan tinggi, dan sepanjang pengetahuan saya juga tidak terdapat karya atau pendapat yang pernah dituliskan atau diterbitkan orang lain, kecuali yang secara tertulis diacu dalam naskah dan disebutkan dalam daftar pustaka.
Kupang, Juli 2018
v
KATA PENGANTAR
Syukur kepada Tuhan Yang Maha Esa karena kasih dan penyertaan-Nya sehingga penulis diberikan hikmat untuk menyelesaikan penelitian dan menyusun Karya Tulis Ilmiah dengan judul Uji Karakteristik Minyak Biji Kelor (Moringa
oleifera L.).
Tujuan dari penelitian ini yakni untuk memberikan informasi kepada masyarakat tentang karakteristik minyak biji kelor.
Karya Tulis Ilmiah ini dapat diselesaikan tidak terlepas dari dukungan berbagai pihak. Penulis mengucapkan terima kasih kepada :
1. Ibu Ragu Harming Kristina, S.KM., M.Kes selaku Direktur Politeknik
Kesehatan Kementerian Kesehatan Kupang.
2. Ibu Dra. Elisma, Apt., M.Si selaku Ketua Prodi Farmasi Politeknik Kesehatan Kementerian Kesehatan Kupang sekaligus penguji I.
3. Ibu Marce I. Taku Bessi, S.Farm., Apt., M.Sc selaku penguji II sekaligus pembimbing yang senantiasa membimbing, mengarahkan dan memotivasi penulis dalam menyelesaikan penyusunan Karya Tulis Ilmiah.
4. Ibu Dra. Fatmawati Blegur Apt., M.Si selaku dosen pembimbing akademik yang
telah membimbing, memberi masukan serta motivasi kepada penulis selama mengikuti perkuliahan di Prodi Farmasi Politeknik Kesehatan Kementerian Kesehatan Kupang.
5. Bapak Falentinus S. Duly, A.Md.F dan Ibu Asmaira Br. Tarigan, A.Md.F selaku
pembimbing di laboratorium yang setia membimbing dan mengarahkan selama proses penelitian.
vi
6. Orang tua tercinta Bapak dan Mama, kakak dan adik serta seluruh keluarga yang selalu memberikan cinta kasih, dan mendukung penulis dalam doa selama proses perkuliahan dan penyusunan Karya Tulis Ilmiah.
7. Sahabat-sahabat Meisha, Tia, Minda, Tasya, Aning, dan Icha yang selalu
memberi dukungan dan doa.
8. Teman-teman seperjuangan TIM Minyak biji kelor Nata dan Yedi yang selalu membantu, mendukung selama proses penelitian.
9. Teman-teman seperjuangan Reguler A angkatan 16 yang selalu memberikan
dukung dan doa.
10. Semua pihak yang telah membantu dalam menyelesaikan penelitian dan Karya Tulis Ilmiah ini yang tidak dapat penulis sebutkan satu persatu.
Akhirnya dengan segala kerendahan hati penulis menyadari masih banyak kekurangan baik materi maupun cakupan pembahasan dalam penulisan karya Tulis Ilmiah ini. Oleh karena itu, segala kritik dan saran yang bersifat membangun dari semua pihak sangat diharapkan guna meyempurnakan penulisan selanjutnya.
Kupang, Juli 2018
vii
INTISARI
Tumbuhan kelor (Moringa oleifera L.) merupakan tanaman yang termasuk famili moringaceae mudah tumbuh pada daerah tropis dan subtropis pada semua jenis tanah dan tahan terhadap musim kering termasuk Nusa Tenggara Timur (NTT). Minyak biji kelor dimanfaatkan sebagai bahan kosmetik. Pemanfaatan biji kelor oleh masyarakat NTT belum dilakukan secara maksimal. Karakteristik minyak biji kelor asal NTT perlu diketahui untuk menunjang penggunaanya dalam bidang kosmetik. Tujuan dari penelitian ini adalah untuk mengetahui karakteristik minyak biji kelor asal NTT berdasarkan parameter fisiko kimia . Karakteristik minyak biji kelor dalam hal ini sifat fisika kimia. Parameter fisika yang diuji berupa pengamatan fisik, berat jenis, kelarutan dan uji noda minyak.Parameter kimia yang diuji adalah bilangan saponifikasi, bilangan iodin dan bilangan asam Ekstraksi yang digunakan dalam penarikan minyak biji kelor adalah metode ekstraksi sokletasi dengan pelarut n- heksan.. Berdasarkan hasil penelitian minyak dihasilkan memiliki rendemen sebesar 13,31% berwarna kuning dan bau seperti kacang, larut dalam kloroform dan menimbulkan noda saat ditetesi di kertas saring dengan bobot jenis sebesar 0,9 ± 0,003 g/liter, bilangan saponifikasi, bilangan iodin dan bilangan asam berturut –turut adalah 52,705 ± 29,045, 8,772 ± 0,108, dan 124,309 ± 12,299
viii
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
LEMBAR PERSETUJUAN... ii
LEMBAR PENGESAHAN ... iii
LEMBAR PERNYATAAN ... iv
KATA PENGANTAR ... v
INTISARI ... vii
DAFTAR ISI ... viii
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xiii
BAB I PENDAHULUAN ... 1 A. Latar Belakang ... 1 B. Rumusan Masalah ... 2 C. Tujuan Penelitian ... 2 1. Tujuan Umum ... 2 2. Tujuan Khusus ... 2 D. Manfaat Penelitian ... 3 1. Bagi Peneliti ... 3 2. Bagi Institusi ... 3 3. Bagi Masyarakat ... 3
BAB II TINJAUAN PUSTAKA ... 4
A. Klasifikasi ... 4
1. Klasifikasi Tanaman Kelor ... 4
2. Nama Lain ... 5
3. Morfologi Tanaman Kelor ... 5
4. Tempat Tumbuh dan Distribusi Tanaman ... 5
ix B. Metode Ekstraksi ... 6 C. Parameter Fisika ... 8 1. Penampakan Fisik ... 8 2. Bobot Jenis ... 8 3. Kelarutan ... 8
4. Uji Noda Minyak ... 8
D. Parameter Kimia ... 8
1. Bilangan Saponifikasi ... 8
2. Bilangan Iodin ... 9
3. Bilangan Asam ... 9
BAB III METODE PENELITIAN ... 10
A. Jenis Penelitian ... 10
B. Tempat dan Waktu Penelitian ... 10
1. Tempat penelitian... 10
2. Waktu Penelitian ... 10
3. Sampel... 10
4. Variabel Penelitian ... 10
C. Defenisi Operasional ... 10
D. Alat dan Bahan ... 11
E. Prosedur Penelitian ... 11 1. Determinasi ... 11 2. Pengumpulan Biji... 11 3. Pembuatan Simplisia ... 11 4. Ekstraksi ... 12 5. Penentuan Parameter ... 13 F. Analisis data ... 16
x A. Sokletasi ... 18 B. Uji Karektaristik ... 18 1. Penampakan Fisik ... 18 2. Bobot Jenis ... 19 3. Kelarutan ... 19
4. Uji Noda Minyak Lemak ... 19
5. Bilangan Saponifikasi ... 19
6. Bilangan Iodin ... 21
7. Bilangan Asam ... 22
BAB V SIMPULAN DAN SARAN ... 22
A. Simpulan ... 23
B. Saran ... 23
DAFTAR PUSTAKA ... 23 LAMPIRAN
xi
DAFTAR TABEL
Halaman
Tabel 1. Uji Bobot Jenis ... 19
Tabel 2. Uji Bilangan Saponifikasi ... 20
Tabel 3. Uji Bilangan Iodin ... 21
Tabel 4. Uji Bilangan Asam ... 22
Tabel 5. Perhitungan Uji Bobot Jenis ... 28
Tabel 6. Hasil Uji Kelarutan ... 30
Tabel 7. Perhitungan Uji Bilangan Saponifikasi ... 35
Tabel 8. Perhitungan Uji Bilangan Iodin ... 39
xii
DAFTAR GAMBAR
Halaman
Gambar 1. Tanaman Kelor ... 4
Gambar 1. Warna Minyak Biji Kelor ... 27
Gambar 2. Piknometer dan Minyak ... 28
Gambar 3. Piknometer Kosong ... 28
Gambar 4. Minyak Dengan Pelarut Kloroform... 29
Gambar 5. Minyak Dengan Pelarut Air ... 29
Gambar 6. Kertas Saring ... 30
Gambar 7. Kertas Saring dan Minyak ... 30
Gambar 8. Sebelum Titrasi ... 35
Gambar 9.Sesudah Titrasi ... 35
Gambar 10. Sebelum Titrasi ... 39
Gambar 11.Sesudah Titrasi ... 39
Gambar 12. Sebelum Titrasi ... 42
xiii
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Surat Determinasi Tumbuhan Kelor ... 26
Lampiran 2. Perhitungan Rendemen ... 27
Lampiran 3. Hasil Uji Penampakan Fisik ... 27
Lampiran 4. Hasil Uji Bobot Jenis ... 28
Lampiran 5. Hasil Uji Kelarutan ... 29
Lampiran 6. Hasil Uji Noda Minyak Lemak ... 30
Lampiran 7. Hasil Uji Bilangan Saponifikasi ... 30
Lampiran 8. Hasil Uji Bilangan Iodin ... 35
Lampiran 9. Hasil Uji Bilangan Asam ... 39
Lampiran 10. Surat Ijin Penelitian ... 43
BAB I
PENDAHULUAN
A. Latar Belakang
Tanaman kelor (Moringa oleifera L.) merupakan tanaman yang termasuk
famili moringaceae. Tanaman kelor di Indonesia sudah banyak dijumpai di
Aceh, Kalimantan, Ujung Pandang dan Kupang (Fahey, 2005). Tanaman kelor mudah tumbuh karena Kelor dapat tumbuh pada daerah tropis dan subtropis pada semua jenis tanah dan tahan terhadap musim kering dengan toleransi terhadap kekeringan sampai 6 bulan (Mendeita Araicia dkk., 2013). Tanaman kelor umumnya dimanfaatkan sebagai tanaman pagar. Daunnya digunakan sebagai bahan makanan dan obat tradisional (Nasir dkk., 2010), Sedangkan biji kelor belum banyak dimanfaatkan oleh masyarakat.
Biji kelor memiliki kandungan minyak nabati 30,8 ± 2,19 % (Abdulkarim dkk., 2005). Berdasarkan penelitian yang dilakukan oleh (Barakat dan Ghazal, 2016) minyak biji kelor memiliki nilai bilangan saponifikasi, bilangan iodine, bilangan asam berturut-turut adalah 171,7 – 178,3 mg KOH g-1, 65,7 – 67,5, 0,29 – 0,37 mg.g-1. Biji kelor merupakan antioksidan yang baik karena mampu mengurangi kerusakan oksidatif disertai penuaan dan kanker (Singh dkk., 2009). Penelitian yang dilakukan oleh (Surdayanto dkk., 2016) minyak dari biji kelor dapat dijadikan sebagai bahan kosmetik karena memiliki aktivitas IC50 sebesar
2
zaitun dalam makanan dan produk bukan makanan seperti biodiesel dan kosmetik (Ndabigengesere dan Narasiah, 1998)
Minyak biji kelor dapat diperoleh dengan metode ekstraksi sokletasi. Pelarut yang digunakan adalah n-heksan karena bersifat nonpolar yang dapat menarik zat aktif ( minyak biji kelor ) yang juga bersifat non polar (Ketaren, 1985). Pengujian karakteristik minyak biji kelor yang diperoleh dari NTT belum pernah dilakukan. Karakteristik minyak biji kelor dalam hal ini sifat fisika kimia sebagai informasi awal berkaitan dengan pemanfaatannya sebagai kosmetik dan produk lainnya. Parameter-parameter yang diamati dalam penelitian ini adalah penampakan fisik, berat jenis, kelarutan dan uji noda minyak, bilangan saponifikasi, bilangan iodin dan bilangan asam
B. Rumusan Masalah
Bagaimana karakteristik minyak biji kelor asal NTT ?
C. Tujuan Penelitian
1. Tujuan Umum
Mengetahui karakteristik minyak biji kelor
2. Tujuan Khusus
a. Mengukur karakteristik minyak biji kelor berdasarkan parameter fisika
yaitu pengamatan fisik, berat jenis, kelarutan dan uji noda minyak.
b. Mengukur karakteristik minyak biji kelor berdasarkan parameter kimia
3
D. Manfaat Penelitian
1. Bagi Peneliti
Sebagai media pengembangan yang diperoleh selama proses perkuliahan di Prodi Farmasi Poltekkes Kemenkes Kupang.
2. Bagi Institusi
Sebagai bahan tambahan pustaka dan referensi untuk penelitian selanjutnya.
3. Bagi Masyarakat
Sebagai sumber informasi tambahan bagi masyarakat tentang
BAB II
TINJAUAN PUSTAKA
A. Klasifikasi
1. Klasifikasi Tanaman Kelor
Klasifikasi tanaman kelor adalah sebagai berikut
Kingdom : Plantae Superdivisi : Spermatophyta Divisi : Magnoliophyta Kelas : Magnoliopsida Bangsa : Brassicales Suku : Moringaceae Genus : Moringa
Spesies : Moringa oleifera Lam (Tilong, 2012)
5
2. Nama Lain
Tanaman kelor di indonesia memiliki banyak sebutan di berbgai daerah diantaranya murong (Aceh); Kelor (Melayu); Munggai (Minangkabau); Kilor (Lampung); Kelor (Sunda); Marongghi (Madura); Parongge (Bima); Kawona (Sumba); Kirol (Buru); Kelo (Ternate); Kelo (Tidore). (Depkes RI, 2001)
3. Morfologi Tanaman Kelor
Tanaman kelor tumbuh dalam bentuk pohon dengan tinggi ± 8 m. Batangnya berkayu bercabang berwarna putih kotor dengan bintik-bintik hitam. Daunnya merupakan daun majemuk, panjang 20-60 cm, anak daunyna berbentuk bulat telur dengan tepi yang rata, ujung berlekuk, menyirip ganjil, dan hijau. Memiliki bunga majemuk bentuk malai, letak di ketiak daun, panjang 10-30 cm, daun kelopak hijau, benang sari dan putik kecil, mahkota putih. Buahnya berupa polong dengan panjang 20-45 cm, berisi 15-25 biji, berwarna coklat kehitaman. Biji kelor berbentuk bulat , bersayap tiga dan hitam. Akar kelor merupakan akar tunggang berwarna putih kotor.(Depkes RI, 2001)
4. Tempat Tumbuh dan Distribusi Tanaman
Tanaman kelor tumbuh di dataran rendah maupun dataran tinggi sampai ketinggian ± 1000 m dpl, banyak ditanam sebagai tapal batas atau pagar di halaman rumah atau ladang. Spesies ini dibudidayakan secara luas sejak dahulu di Roma, Yunani kuno dan Mesir dan saat ini meluas di seluruh daerah tropis dan subtropis di dunia karena mempunyai toleransi rentang
6
iklim yang luas. Tanaman ini juga sangat banyak ditemukan di seluruh bagian dari negeri india dan pegununggan Himalaya.(Navie dan Csurhes, 2010; Qaiser, 1973)
5. Kandungan Kimia dan Khasiat
Akar, daun dan kulit batang Moringa oleifera mengandung saponin
dan polifenol, di samping itu kulit batangnya mengandung alkaloida (Depkes RI, 2001). Buah kelor akan menghasilkan biji yang dapat dibuat tepung atau minyak sebagai bahan baku pembuatan obat dan kosmetik bernilai tinggi (Aminah dkk., 2015). Biji kelor mengandung senyawa fenolik, flavonoid, saponin, terpenoid, proantosianidin dan glikosida jantung (Sharma dkk., 2012). Biji kelor merupakan antioksidan yang baik karena mampu mengurangi kerusakan oksidatif disertai penuaan dan kanker (Singh dkk., 2009). Biji kelor juga mengandung vitamin E (0,01%) dan beta karoten (0,014%) (Bhoomika dkk., 2007).
Minyak biji kelor bisa menjadi pengganti yang baik untuk minyak zaitun dalam makanan dan produk bukan makanan seperti biodiesel dan kosmetik (Ndabigengesere dan Narasiah, 1998). Biji kelor mengahasilkan minyak yang tahan terhadap ketengikan karena kandungan antioksidan sehingga minyak tidak mudah teroksidasi (Anwar dkk., 2006).
B. Metode Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan menggunakan pelarut cair. Senyawa aktif yang terdapat dalam berbagai simplisia dapat digolongkan
7
kedalam golongan minyak atsiri, alkaloida, falvonoida dan lain-lain. Dengan diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah pemilihan pelarut dan cara ekstraksi yang tepat (Depkes RI, 2000)
Metode yang digunakan dalam penelitian ini adalah metode ekstraksi sokletasi. Sokletasi adalah ekstraksi dengan menggunakan pelarut yang selalu baru dan yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstrak kontinu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik (Depkes RI, 2000) dengan pelarut yang digunakan adalah n-heksan. Heksana adalah suatu hidrokarbon alkana dengan rumus kimia CH3(CH2)4CH3. Awalan
"Hex" menunjukkan jumlah enam atom karbonnya, sedangkan akhiran “ana” menunjukkan bahwa atom karbonnya dihubungkan oleh ikatan tunggal. (Nasir dkk., 2010)
Isometri heksana umumnya bersifat tidak reaktif, dan sering digunakan sebagai pelarut inert dalam reaksi organik, karena heksana tidak polar. Umumnya heksana digunakan untuk mengekstrak minyak dari bijinya seperti pada kacang-kacangan dan flax. Hal ini karena heksana tidak reaktif dan inert dalam reaksi organik karena bersifat sangat non-polar dan memilki narrow distillation range dan selective power, sehingga tidak memerlukan tingkat pemanasan yang tinggi dan daya ekstraksinya tinggi, yang menjadikan heksana sebagai pelarut yang baik untuk mengekstrak minyak dari bijinya.(Nasir dkk., 2010)
8
C. Parameter Fisika
Berdasarkan (Sudamardji dkk., 2003) parameter fisika yang diuji meliputi :
1. Penampakan Fisik
Pengujian yang didasarkan pada proses penginderaan. Penilaian indera dengan cara uji organoleptik meliputi tekstur suatu bahan, faktor kenampakan berupa warna dan bau.
2. Bobot Jenis
Bobot jenis merupakan perbandingan berat dari volume minyak atau lemak pada suhu 25°C dengan berat air pada volume dan suhu yang sama
3. Kelarutan
Kelarutan adalah jumlah zat terlarut yang dapat larut dalam jumlah tertentu. Dalam larutan, zat terlarut adalah zat yang larut, dan pelarut adalah zat yang tidak larut kedalamnya.
4. Uji Noda Minyak
Minyak atau lemak dapat membentuk noda sehingga kertas yang tidak tembus pandang menjadi semi transparan. Sampel dengan kejenuhan yang tinggi akan meninggalkan noda pada kertas saring yang digunakan.
D. Parameter Kimia
Berdasarkan (Sudjadi dan Rohman, 2004) parameter kimia yang diuji meliputi:
1. Bilangan Saponifikasi
Bilangan saponifikasi didefenisikan sebagai banyaknya milligram KOH yang dibutuhkan untuk menyabunkan lemak secara sempurna dari 1 gram lemak atau minyak.
9
2. Bilangan Iodin
Bilangan iodin didefenisikan sebagai banyaknya iodium yang diserap oleh oleh 100 gram minyak, lemak, atau senyawa-senyawa lain. Bilangan ini merupakan pengukuran kuantitatif yang menyatakan banyaknya asam-asam lemak tidak jenuh baik dalam bentuk bebas atau dalam bentuk ester yang terdapat dalam minyak atau lemak karena asam lemak ini mempunyai sifat yang mampu menyerap iodium.
3. Bilangan Asam
Bilangan asam juga dikenal dengan indeks keasaman didefenisikan sebagai banyaknya milligram KOH yang dibutuhkan untuk menetralkan asam bebas dalam 1 gram minyak, lemak, resin, balsam atau senyawa organik serupa dengan komposisi yang kompleks.
BAB III
METODE PENELITIAN
A. Jenis Penelitian
Jenis penelitian ini adalah penelitian deskriptif
B. Tempat dan Waktu Penelitian 1. Tempat penelitian
Penelitian dilakukan di laboratorium Farmakognosi, laboratorium kimia, dan di laboratorium analisa instrument Prodi Farmasi Poltekkes Kemenkes Kupang.
2. Waktu Penelitian
Penelitian ini dilakukan pada bulan maret sampai juni tahun 2018.
3. Sampel
Sampel yang digunakan dalam penelitian ini adalah biji kelor yang diambil dari Kelurahan Liliba, Kota Kupang.
4. Variabel Penelitian
Variabel tunggal penelitian ini adalah karakteristik minyak biji kelor
C. Defenisi Operasional
1. Biji kelor adalah biji tua berwarna coklat
2. Minyak biji kelor adalah hasil dari proses ektraksi dengan metode sokletasi
biji kelor dengan pelarut n-heksan
3. Karakteristik Minyak Biji Kelor adalah dengan parameter fisika yaitu pengamatan fisik, bobot jenis, indeks bias dan dengan parameter kimia meliputi bilangan saponifikasi, bilangan iodine dan bilangan asam.
11
D. Alat dan Bahan
1. Alat yang digunakan dalam penelitian ini meliputi piknometer,
refraktometer, evaporator, soklet, buret, statif, desikator, beaker glass (Pyerx), erlenmeyer (Pyrex), timbangan digital ( Shimadzu type BL-3200H),
hot plate, waterbath (Memmert), batang pengaduk, kertas perkamen, tabung
reaksi (Pyrex) dan kertas saring.
2. Bahan yang digunakan meliputi aquades, asam asetat glacial, KOH 0,1 N, KOH 0,5 N, Alcohol netral 95%, Kloroform, natrium sulfat anhidrat, natrium karbonat, kalium biftalat, natrium tiosulfat, kalium bikarbonat, natrium bikarbonat, asam asesat glasial, iodine bromide, indicator amilum dan indicator phenolphthalein, indikator merah metil.
E. Prosedur Penelitian
1. Determinasi
Determinasi tanaman kelor dilakukan di UPT Materia Medika Malang.
2. Pengumpulan Biji
Biji kelor di ambil di kelurahan liliba kecamatan Oebobo kota Kupang dari buah yang sudah matang dengan ciri buah berwarna coklat.
3. Pembuatan Simplisia
Pengambilan dengan kriteria buah yang sudah tua. Buah kelor dikupas, dipisahkan serabut dengan bijinya. Biji kelor yang diperoleh disortasi basah dan dicuci dengan air.Selanjutnya biji kelor dikeringkan dengan pada sinar matahari langsung yang ditutupi plastik berwarna hitam dan disortasi kering untuk menjamin simplisia benar-benar bebas bebas dari bahan
12
asing.Selanjutnya simplisia diserbuk dan diayak dengan menggunakan ayakan no 45.
4. Ekstraksi
Serbuk simplisia biji kelor sebanyak 100 gram dimasukkan dalam timbel, dibungkus dengan kertas saring kemudian dimasukkan ke dalam tabung soklet.Labu diisi dengan pelarut kira-kira 2/3 bagiannya sampai badan soklet terisi sepenuhnya. Panaskan dalam waterbath dan refluks selama kurang lebih 4 jam hingga warna pelarut dalam wadah soklet pada saat kontak dengan cuplikan tidak berubah. Dipisahkan pelarut dengan zat yang diekstrak dengan destilasi secara langsung menggunakan alat soklet.Ulangi pemanasan sehingga dalam labu hanya terdapat zat sampel. Kemudian, hitung rendemen dengan menggunakan rumus:
Rendemen bobot minyak
bobot simplisia x
Minyak biji kelor yang diperoleh kemudian dipisahkan dari pelarut n-heksan dengan cara diuapkan diatas water bath 7 ˚C kemudian tambahkan air panas dikocok selama 12 menit, setelah dingin minyak disentrifius selama 10 menit. Tambahkan natrium sulfat anhidrat untuk menghilangkan sisa-sisa air diamkan selama 5 menit, saring dengan kertas saring. Masukkan hasil minyak dalam botol tertutup dan simpan dalam pendingin dengan suhu 0-4˚C.
13
5. Penentuan Parameter
Prosedur penentuan parameter fisik dan kimia berdasarkan (Sudamardji dkk., 2003)
a. Penampakan Fisik
Penampakan fisik dilihat warna dan bau minyak biji kelor
b. Bobot jenis
Timbang bobot piknometer 10 ml kosong. Dicatat berat piknometer. Minyak biji kelor dimasukkan kedalam piknometer hingga penuh kemudian ditutup, dibersihkan permukaan luar piknometer dan ditimbang. Piknometer dibersihkan dalam keadaan kering masukkan air dalam piknometer hingga penuh kemudian ditutup, bersihkan permukaan luar piknometer dan ditimbang. Direplikasi 3 kali.
obot jenis bobot piknometer dan minyak bobot piknometer kosong
bobot piknometer dan air bobot piknometer kosong
c. Uji kelarutan
Minyak ditimbang seberat 0,5 gram di masukkan dalam tabung reaksi. Kemudian tambahkan kloroform sebanyak 5 ml , kocok hingga larut . Amati kelarutan minyak dalam tabung.
d. Uji noda minyak lemak
Minyak diteteskan diatas kertas saring dan diamkan 5 menit. Amati noda yang terbentuk.
e. Bilangan saponifikasi
Minyak ditimbang seberat kurang lebih 1 gram dalam Erlenmeyer. Kemudian ditambahkan sebanyak 10 ml KOH 0,5 N
14
alkoholik. Sesudah ditutup dengan pendingin selanjutnya dididihkan sampai minyak tersabunkan secara sempurna ditandai dengan tidak terlihat butir-butir lemak atau minyak dalam larutan. Setelah didinginkan kemudian dititrasi dengan HCl 0,5 N menggunakan indicator/phenolphthalein. Titik akhir titrasi ditandai dengan tepat hilangnya warna merah, misalnya titrasi memerlukan (ts) ml.
Dibuat perlakuan blanko yaitu seperti perlakuan sebelumnya hanya tanpa sampel.Titrasi blanko ini menunjukkan KOH mula-mula yang digunakan dalam reaksi penyabunan, misalkan titrasi blanko memerlukan (tb) ml.Alkohol yang ada dalam KOH berfungsi untuk melarutkan asam lemak hasil hidrolisa agar supaya mempermudah reaksi dengan basa sehingga terbentuk sabun. Direplikasi 3 kali.
ngka penyabunan (tb ts) x Cl x berat contoh g Keterangan : tb = Titrasi blanko ts = Titrasi sampel N = Normalitas BM = Berat molekul f. Bilangan iodine
Minyak sebanyak 0,1-0,5 gram dilarutkan dalam 10 ml kloroform atau karbon tetra klorida kemudian ditambahkan 25 ml larutan iodine bromide dalam asam asetat glacial. Dibiarkan selama satu jam maka akan terjadi peningkatan iodine oleh minyak pada ikatan rangkapnya selama ini dibiarkan ditempat gelap. Iodine sisa dititrasi dengan natrium
15
tiosulfat 0,1 N menggunakan indicator amilum, akhir titrassi ditandai dengan hilangnya warna biru. Titrasi sampel missal ( =ts) ml. Untuk mengetahui iodine mula-mula dalam reagen maka dilakukan perlakuan blanko dengan jalan yang sama. Titrasi blanko misal tb ml. Direplikasi 3 kali.
ngka iodin (tb ts) x a S x iod x
bobot contoh (gram) x (tb ts) x a S x ,
bobot contoh gram Keterangan : tb = Titrasi blanko ts = Titrasi sampel N = Normalitas BA = Berat Atom g. Bilangan Asam
Minyak atau lemak sebanyak 1 gram ditambah 5 ml alcohol netral 95% kemudian dipanaskan 5 menit dalam penangas air sambil diaduk dan ditutup pendingin balik. Alkohol berfungsi untuk melarutkan asam lemak. Setelah didinginkan kemudian dititrasi dengan KOH 0,1 N menggunakan indikator fenolftalein sampai tepat warna merah jambu. Direplikasi 3 kali.
ngka asam ml x x
bobot contoh gram BM = Bobot molekul asam lemak
16
F. Analisis data
Data yang diperoleh akan dianalisis dengan cara deskriptif kualitatif
1. Pengamatan fisik yang diamati berupa warna, tekstur dan bau.
2. Nilai bobot jenis dilihat dengan alat piknometer lalu dihitung bobot jenis dengan rumus.
obot jenis minyak bobot piknometer dan minyak bobot piknometer kosong
bobot piknometer dan air bobot piknometer kosong
3. Kelarutan
Diamati kelarutan minyak dalam kloroform
4. Uji Noda Minyak
Diamati ada tidaknya noda di kertas saring.
5. Penentuan bilangan saponifaksi dilakukan dengan titrasi. Nilai dihitung dengan rumus
ngka penyabunan (tb ts) x Cl x
berat contoh g
6. Penentuan bilangan iodine dilakukan dengan titrasi. Nilai dihitung dengan
rumus
ngka iodin (tb ts) x a S x iod x
bobot contoh (gram) x (tb ts) x a S x ,
17
7. Penentuan bilangan asam dilakukan dengan titrasi. Nilai dihitung dengan rumus
ngka asam ml x x
BAB IV
HASIL DAN PEMBAHASAN
A. Determinasi
Determinasi tanaman kelor yang dilakukan di UPT Materia Medika Malang menunjukkan tanaman yang digunakan dalam penelitian adalah tanaman kelor
dengan nama latin Moringa oleifera L. dan suku moringaceae. (Lampiran 1)
B. Sokletasi
Ekstraksi metode sokletasi menggunakan simplisia sebanyak 100 gram dimasukkkan dalam tabung soklet, ditambah pelarut 300 ml. Sokletasi minyak biji kelor dilakukan sebanyak 10 siklus. Minyak yang dihasilkan dipisahkan dari pelarut n-heksan dengan cara diuapkan diatas waterbath 7 ˚C kemudian tambahkan air panas dikocok selama 12 menit, setelah dingin minyak disentrifius selama 10 menit. Ditambahkan natrium sulfat anhidrat untuk menghilangkan sisa-sisa air diamkan selama 5 menit, saring dengan kertas saring. Hasil minyak dimasukkan dalam botol tertutup dan disimpan dalam pendingin dengan suhu 0-4˚C Rendemen yang diperoleh pada ekstrasi ini sebesar 13,31%.( Lampiran 2)
C. Uji Karektaristik 1. Penampakan Fisik
Pengujian dengan penampakan fisik ini didasarkan pada proses penginderaan. Penampakan fisik yang dilihat pada minyak biji kelor yang dihasilkan adalah warna dan bau. Warna dari minyak biji kelor adalah kuning. Bau minyak biji kelor seperti bau kacang-kacangan.(Lampiran 3)
19
2. Bobot Jenis
Bobot jenis merupakan perbandingan berat dari volume minyak dengan berat air.
Tabel 1. Berat jenis minyak
No. Uji BJ Minyak
1 Replikasi 1 0,907
2 Replikasi 2 0,912
3 Replikasi 3 0,909
4 Rata-rata 0,909 ± 0,003
Data diatas menunjukkan BJ minyak kelor sebesar 0,907. Penelitian yang pernah dilakukan oleh (Surdayanto dkk., 2016) menunjukkan bahwa minyak biji kelor memiliki BJ 0,90.( Lampiran 4 )
3. Kelarutan
Kelarutan minyak lemak menurut farmakope edisi III kecuali dinyatakan lain mudah larut dalam kloroform p, dalam eter P dan dalam eter minyak tanah P. Penelitian ini minyak biji kelor dilarutkan dalam kloroform dan dapat larut sempurna ( Lampiran 5 )
4. Uji Noda Minyak Lemak
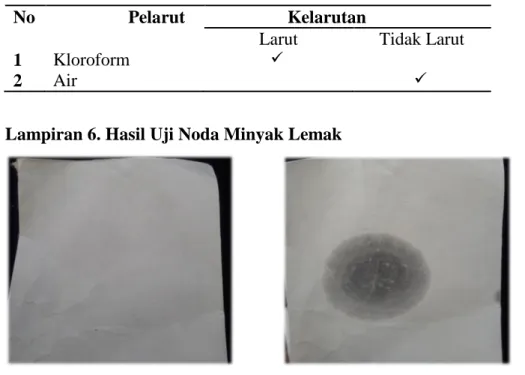
Minyak lemak yang diteteskan diatas kertas saring meniggalkan noda ( kertas menjadi semi transparan). Hal ini menunjukan bahwa kandungan lemak pada minyak biji kelor tinggi. (Lampiran 6 )
5. Bilangan Saponifikasi
Bilangan saponifikasi (penyabunan) dapat dipergunakan untuk menentukan berat molekul minyak dan lemak secara kasar. Minyak yang disusun oleh asam lemak berantai C pendek berarti mempunyai berat molekul relatif kecil akan mempunyai angka penyabunan yang besar dan
20
sebaliknya minyak dengan berat molekul yang besar mempunyai angka penyabunan yang relatif kecil.
Bilangan penyabunan dinyatakan sebagai banyaknya (mg) KOH yang dibutuhkan untuk menyabunkan satu gram lemak atau minyak. Alkohol yang ada dalam KOH berfungsi untuk melarutkan asam lemak hasil hidrolisa supaya mempermudah reaksi dengan basa sehingga terbentuk sabun.
Tabel 2. Uji Bilangan Saponifikasi
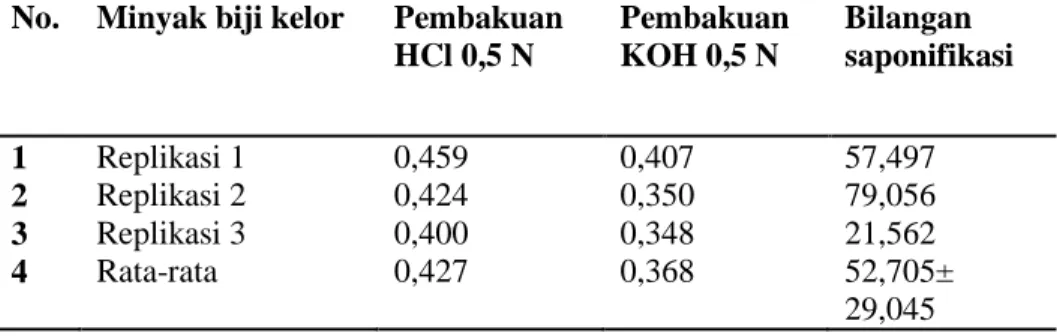
No. Minyak biji kelor Bilangan saponifikasi 1 Replikasi 1 57,497 2 Replikasi 2 79,056 3 Replikasi 3 21,562 4 Rata-rata 52,705± 29,045
Data hasil replikasi pada titrasi bilangan saponifikasi memiliki perbedaan volume titrasi karena adanya proses pemanasan pada prosedur penentuan bilangan saponifikasi. Pemanasan dilakukan di hotplate dan suhu pada hotplate yang tidak stabil.
Data diatas di dapat bilangan saponifikasi adalah 52,705 ± 29,045 dan penelitian yang pernah dilakukan oleh (Surdayanto dkk., 2016) menunjukkan bahwa minyak biji kelor memiliki bilangan saponifikasi 219,20. Hasil uji bilangan saponifikasi yang diteliti lebih kecil dari penelitian sebelumnya menunjukkan bahwa berat molekul dari minyak biji kelor asal NTT lebih besar. Hal ini berarti minyak disusun oleh asam lemak berantai panjang dan titik lebur yang lebih tinggi. (Lampiran 7)
21
6. Bilangan Iodin
Bilangan iodin mencerminkan ketidakjenuhan asam lemak penyusun minyak dan lemak. Asam lemak tidak jenuh mampu mengikat iod dan membentuk senyawaan yang jenuh. Banyaknya iod yang diikat menunjukkan banyaknya ikatan rangkap . Angka iod dinyatakan sebagai banyaknya gram iod yang diikat oleh 100 gram minyak atau lemak.
Tabel 3. Uji Bilangan Iodin
No. Minyak biji kelor Bilangan iodin 1 Replikasi 1 8,872 2 Replikasi 2 8,788 3 Replikasi 3 8,657 Rata-rata 8,772± 0,108
Reaksi adisi antara asam lemak dengan iodin dapat menentukan
derajat ketidakjenuhan asam lemak yang menyusun minyak
(Kusnandar,2010) .
Berdasarkan data diatas nilai bilangan iodine adalah 8,772 ± 0,108. Minyak biji kelor ini memiliki tingkat ketidakjenuhan yang rendah jika
dibandingkan dengan penelitian yang pernah dilakukan oleh
(surdayanto,dkk, 2016 ) menunjukkan bahwa minyak biji kelor memiliki bilangan iodine 13,19. Pada penelitian ini minyak biji kelor yang di teliti memiliki asam lemak jenuh lebih banyak karena minyak sukar menyerap iod lagi dibandingkan dengan penelitian yang dilakukan oleh (Surdayanto dkk., 2016). Minyak yang meiliki kandungan asam lemak jenuh yang memiliki rantai tunggal akibat adanya pemanasan yang membuat ikatan
22
rangkap menjadi ikatan tunggal sehingga mudah teroksidasi dan menjadi tengik.(Lampiran 8)
7. Bilangan Asam
Bilangan asam dinyatakan sebagai jumlah milligram KOH yang diperlukan untuk menetralkan asam lemak bebas yang terdapat dalam satu gram minyak atau lemak. Angka asam yang besar menunjukkan asam lemak bebas yang besar yang berasal dari hidrolisa minyak ataupun karena proses pengolahan yang kurang baik. Makin tinggi angka asam makin rendah kualitasnya.
Tabel 4. Uji Bilangan Asam
Data hasil replikasi pada titrasi bilangan asam memiliki perbedaan volume titrasi karena adanya proses pemanasan pada prosedur penentuan bilangan asam. Pemanasan dilakukan di penangas air dan suhu pada penagas air tidak stabil. Hasil uji bilangan asam menyatakan bahwa nilai bilangan asam pada minyak biji kelor adalah 124,309 ± 12,299. Data menunjukkan bahwa kandungan asam lemak bebas tinggi yang berpengaruh pada turunnya rendemen minyak. Tingginya kandungan asam lemak berarti banyaknya asam lemak yang telah lepas dari gliserol dimana gliserol dapat membantu asam lemak membentuk trigliserida. Asam lemak bebas yang tinggi juga menimbulkan rasa tidak enak dalam bahan pangan berlemak.(Lampiran 9)
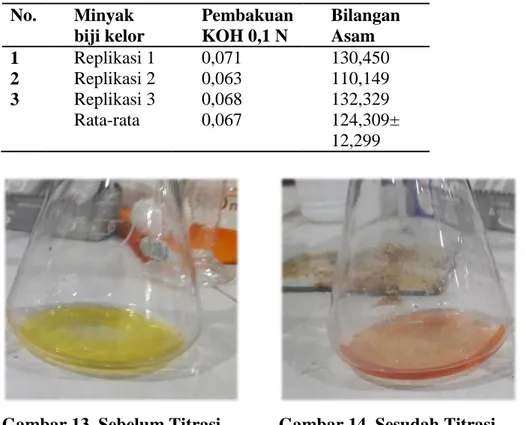
No. Minyak biji kelor Bilangan Asam 1 Replikasi 1 130,450 2 Replikasi 2 110,149 3 Replikasi 3 132,329 Rata-rata 124,309± 12,299
BAB V
SIMPULAN DAN SARAN
A. Simpulan
1. Karakteristik minyak biji kelor yang dihasilkan dengan metode ekstraksi sokletasi berwarna kuning dan bau khas seperti kacang-kacangan. Berat jenis dari minyak biji kelor adalah 0,9 ± 0,003. Larut dalam kloroform dan merupakan minyak lemak karena menimbulkan noda dikertas saring
2. Karakteristik minyak biji kelor berdasarkan parameter kimia nilai bilangan saponifikasi, bilangan iodin dan bilangan asam adalah masing-masing 52,705 ± 29,045, 8,772 ± 0,108, dan 124,309 ± 12,299.
B. Saran
Bagi peneliti selanjutnya dapat melakukan pengujian karekteristik minyak dilihat dari indeks bias, uji kadar air dan bilangan peroksida.
24
DAFTAR PUSTAKA
Abdulkarim, K, L., Muhammad, dan Ghazali, 2005. Some Physico-Chemical Properties of Moringa Oleifera Seed Oil Extracted Using Solvent and Aqueous Enzymatic Methods. Food Chem.
Aminah, S., Ramdhan, T., dan Yanis, M., 2015. Kandungan Nutrisi Dan Sifat Fungsional Tanaman Kelor (Moringa Oleifera). Buletin Pertanian Perkotaan. Anwar, farooq, nahid, syeda, dan rashid, umer, 2006. Characterization of Moringa
Oleifera Seed Oil from Drought and Irrigatedregions of Punjab, Pakistan. Grasass Y Aceites.
Barakat, H. dan Ghazal, G.A., 2016. Physicochemical Properties of Moringa Olifera Seeds and Their Edible Oil Cultivated at Different Regions in Egypt. Bhoomika, R.G., Agrawal, B.B., Goyal, R.K., dan Metha, A.A., 2007.
Phyto-Pharmacology of Moringa Oleifera Lam. Natural Product Radiance.
Day, R.A.J. dan A.L., U., 1996. Analisa Kimia Kuantitatif, 5th ed. Erlangga, Jakarta. Depkes RI, 2000. Parameter Standar Umum Ekstrak Tumbuhan Obat. Departemen
Kesehatan Republik Indonesia, Jakarta.
Depkes RI, 2001. Inventaris Tanaman Obat Indonesia (I) Jilid 2.
Fahey, J.W., 2005. Moringa Oleifera: A Review of the Medical Evidence for Its Nutritional, Therapeutik, and Prophylactic Properties, Part 1.
Ketaren, S., 1985. Pengantar Teknologi Minyak Atsiri. Balai Pustaka, Jakarta . Mendeita Araicia, B., Sporndly, Reyes sanchez, Salmeron Miranda, dan Halling,
2013. Biomas Production and Chemical Composition of Moringa Oleifera under Different Planting Densities and Levels of Nitrogen Fertilization. Agroforest.
Nasir, S., Soraya, D.F., dan Pratiwi, D., 2010. Pemanfaatan Ekstrak Biji Kelor (Moringa Oleifera L.) Untuk Pembuatan Bahan Bakar Nabati. Universitas Surabaya, Teknik Kimia.
avie, S dan Csurhes, S , orseradish Tree : oringa leifera Queensland Government.
25
Ndabigengesere, A. dan Narasiah, S., 1998. Quality of Water Treated by Coagulation Using Moringa Oleifera Seeds.
Nugraheni, D.T., 2011. Analisis Penurunan Bilangan Iod Terhadap Pengulangan Penggorengan Minyak Kelapa Degan Metode Titrasi Iodometri. Fakultas Tarbiyah dan Keguruan Universitas Islam Negeri Sultan Syarif Kasim Riau Pekanbaru, Pekanbaru.
Qaiser, , 7 oringaceae In : Flora of West Pakistan, E asir and SI li ed University of karachi, pakistan, Departement of Botany.
Sharma, V., Paliwal, R., Janmeda, P., dan Sharma, S., 2012. Chemopreventive Efficacy of Moringa Oleifera Pods Against 7,12-Dimethylbenz[a]Anthracene Induced Hepatic Carcinogenesis in Mice. Asian Pacific Journal of Cancer Prevention.
Singh, B.N., Singh, B.R., Singh, R.L., Prakash, Dhakarey, dan Upadhyay, 2009. Oxidative DNA Damage Protective Activity, Antioxidant and Anti-Quorum Sensing Potensials of Moringa Oleifera. Food Chem. Toxicol.
Sudamardji, S., Haryono, B., dan Suhardi, 2003. Analisa Bahan Makanan Dan Pertanian, 2nd ed. Liberty Yogyakarta, Yogyakarta.
Sudjadi dan Rohman, A., 2004. Analisis Obat Dan Makanan. Pustaka Pelajar, Yogyakarta.
Surdayanto, Herwanto, T., dan Harnesa Putri, S., 2016. Aktivitas Antioksiddan Pada Minyak Biji Kelor ( Moringa Oleifera L.) Dengan Metode Sokletasi Menggunakan Pelarut N-Heksan, Metanol Dan Etanol.
Tilong, A., 2012. Ternyata Kelor Penakluk Diabetes. DIVA Press, Yogyakarta. Winarno, F.G., 1984. Kimia Pangan Dan Gizi. PT. Gramedia, Jakarta.
26
LAMPIRAN
27
Lampiran 2. Perhitungan Rendemen
Bobot wadah = 58,68
Bobot wadah dan minyak = 113,93
Rendemen bobot wadah dan isi bobot wadah
gram simplisia x
, ,
4 gram x
= 13,31%
Lampiran 3. Hasil Uji Penampakan Fisik
28
Lampiran 4. Hasil Uji Bobot Jenis
Gambar 3. Piknometer dan minyak Gambar 4. Piknometer Kosong
A. Perhitungan
obot jenis bobot piknometer dan minyak bobot piknometer kosong
bobot piknometer dan air bobot piknometer kosong
obot jenis bobot minyak
bobot air
Tabel 5. Perhitungan Uji Bobot jenis
obot jenis bobot piknometer dan minyak bobot piknometer kosong
bobot piknometer dan air bobot piknometer kosong
obot jenis bobot minyak
bobot air
bobot jenis 4 ,
, 4 , 7
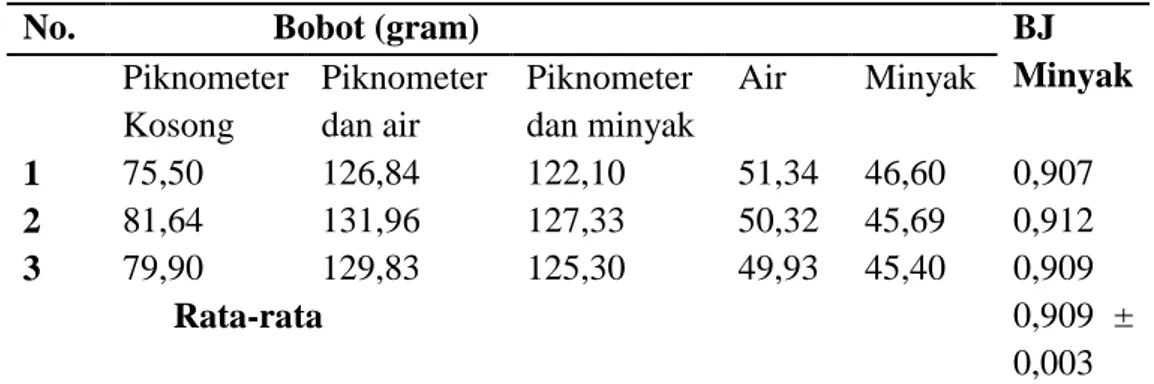
No. Bobot (gram) BJ
Minyak Piknometer Kosong Piknometer dan air Piknometer dan minyak Air Minyak 1 75,50 126,84 122,10 51,34 46,60 0,907 2 81,64 131,96 127,33 50,32 45,69 0,912 3 79,90 129,83 125,30 49,93 45,40 0,909 Rata-rata 0,909 ± 0,003
29 bobot jenis 4 , , , bobot jenis 4 ,4 4 , , Rata rata , 7 , , Rata-rata = 0,909 ± 0,003
Lampiran 5. Hasil Uji Kelarutan
Gambar 5. Minyak dengan pelarut Kloroform
30
Tabel 6. Hasil Uji Kelarutan
No Pelarut Kelarutan
Larut Tidak Larut
1 Kloroform
2 Air
Lampiran 6. Hasil Uji Noda Minyak Lemak
Gambar 7. Kertas Saring Gambar 8. Kertas Saring dan Minyak
Lampiran 7. Hasil Uji Bilangan Saponifikaisi
A. HCl 1. Pembuatan ml C ol x x mr , x , x , , = 20,35 ml
Pipet 20 ml HCl P masukkan dalam labu ukur 500 ml larutkan dengan aquades hingga tanda.
2. Pembakuan HCl 0,5 N
Ditimbang 0,264 gram natrium karbonat anhidrat P yang sebelumnya telah dikeringkan pada suhu 270° selama 1 jam, larutkan dalam 10 ml aquades. Titrasi dengan asam klorida menggunakan indikator merah metil.
31 Cl mg mr x E x t Replikasi 4 ,4 x x , 4 74, = 0,459 Replikasi 4 ,4 x x ,7 4 , 7 = 0,424 Replikasi 4 ,4 x x ,4 4 , 4 = 0,400 Rata rata ,4 ,4 4 ,4 ,4 7 B. KOH 0,5 N alkoholik 1. Pembuatan
Ditimbang 14,025 gram KOH dalam labu ukur 500 ml tambahkan etanol 95% hingga tanda.
2. Pembakuan
Lebih kurang 25 ml asam klorida 0,5 N yang diukur saksama encerkan dengan 50 ml air. Titrasi dengan larutan kalium hidroksida alkoholik menggunakan indikator fenolftalein.
32 V1 x N1 = V2 x N2 a. 25 x 0,427 = 26,2 x N2 10,675 = 26,2 x N2 , 7 , = 0,407 b. V1 x N1 = V2 x N2 25 x 0,427 = 30,5 x N2 10,675 = 30,5 x N2 , 7 , = 0,350 c. V1 x N1 = V2 x N2 25 x 0,427 = 30,6 x N2 10,675 = 30,6 x N2 , 7 , = 0,348 Rata rata ,4 7 , , 4 , C. Bilangan saponifikasi Replikasi a ( tb ts ) x Cl x erat sampel ( gram ) ( , 4, ) x ,4 7 x , , x , = 45,516 Repliakasi b ( tb ts ) x Cl x erat sampel ( gram ) ( , 4, ) x ,4 7 x ,
33 ,4 x ,
= 45,516
Replikasi c ( tb ts ) x Cl x erat sampel ( gram ) ( , , ) x ,4 7 x ,
, x ,
= 69,478
Rata rata replikasi 4 , 7,4 ,47
7,4 7
Replikasi a ( tb ts ) x Cl x erat sampel ( gram ) ( 7,4 4, ) x ,4 7 x , , x , = 79,054 Replikasi b ( tb ts ) x Cl x erat sampel ( gram ) ( 7,4 4, ) x ,4 7 x , , x , = 67,076 Replikasi c ( tb ts ) x Cl x erat sampel ( gram ) ( 7,4 , ) x ,4 7 x ,
, x ,
= 91,040
34
Rata rata replikasi 7, 7 , 4
7 ,
Replikasi a ( tb ts ) x Cl x erat sampel ( gram ) ( 4, ) x ,4 7 x , ,4 x , = 9,583 Replikasi b ( tb ts ) x Cl x erat sampel ( gram ) ( 4, ) x ,4 7 x , , x , = 21,562 Replikasi c ( tb ts ) x Cl x erat sampel ( gram ) ( , ) x ,4 7 x ,
,4 x ,
= 33,541
Rata rata replikasi , , 4
,
adar rata rata 7,4 7 7 , ,
35
Tabel 7. Perhitungan Uji Bilangan Saponifikasi
No. Minyak biji kelor Pembakuan
HCl 0,5 N Pembakuan KOH 0,5 N Bilangan saponifikasi 1 Replikasi 1 0,459 0,407 57,497 2 Replikasi 2 0,424 0,350 79,056 3 Replikasi 3 0,400 0,348 21,562 4 Rata-rata 0,427 0,368 52,705± 29,045
Gambar 9. Sebelum Titrasi Gambar 10. Sesudah Titrasi
Lampiran 8. Hasil Uji Bilangan Iodin
A. Natrium tiosulfat 0,1 N
1. Pembuatan
Larutkan 13 gram natrium tiosulfat dan 100 mg natrium karbonat dalam air bebas karbondioksida segar secukupnya hingga 500 ml.
2. Pembakuan
Timbang seksama 105 mg kalium bikromat yang sebelumnya telah dikeringkan pada suhu 120 selama 4 jam, larutkan dalam 50 ml air. goyangkan hingga larut tambahkan dengan cepat 1,5 gram kalium iodide, 1 gram natrium bikarbonat dan 2,5 ml HCl P. Sumbat labu, goyangkan hingga tercampur, biarkan ditempat gelap selama 10 menit. Titrasi dengan larutan natrium tiosulfat menggunakan indikator kanji.
36 a S mg mr x E x t Replikasi 4, x x , , = 0,033 Replikasi 4, x x ,7 44, = 0,034 Replikasi 4, x x , 7 , = 0,035 Rata rata , , 4 , , 4 B. Bilangan iodin ( tb ts ) x a S x Iod x erat sampel ( gram ) x
Replikasi a ( tb ts ) x a S x , erat sampel ( gram ) ( ,7 , ) x , 4 x , , x ,4 = 8,948 Replikasi b ( tb ts ) x a S x , erat sampel ( gram ) ( ,7 , ) x , 4 x ,
, x ,4
37 = 8,817
Replikasi c ( tb ts ) x a S x , erat sampel ( gram ) ( ,7 ,4 ) x , 4 x ,
, x ,4
= 8,861
Rata rata replikasi , 7 ,
, 7
Replikasi a ( tb ts ) x a S x , erat sampel ( gram ) ( , , ) x , 4 x , , x ,4 = 8,861 Replikasi b ( tb ts ) x a S x , erat sampel ( gram ) ( , , ) x , 4 x , x ,4 = 8,730 Replikasi c ( tb ts ) x a S x , erat sampel ( gram ) ( , ,4 ) x , 4 x ,
, x ,4
= 8,773
38 Rata rata replikasi ,7 ,77
,7
Replikasi a ( tb ts ) x a S x , erat sampel ( gram ) ( , , ) x , 4 x , x ,4 = 8,730 Replikasi b ( tb ts ) x a S x , erat sampel ( gram ) ( , , ) x , 4 x , ,7 x ,4 = 8,599 Replikasi c ( tb ts ) x a S x , erat sampel ( gram ) ( , ,4 ) x , 4 x ,
, x ,4
= 8,642
Rata rata replikasi , , 4
, 7
adar rata rata , 7 ,7 , 7
39
Tabel 8. Perhitungan Uji Bilangan Iodin
No. Minyak biji kelor Pembakuan Natrium tiosulfat Bilangan iodin 1 Replikasi 1 0,033 8,872 2 Replikasi 2 0,034 8,788 3 Replikasi 3 0,035 8,657 Rata-rata 0,034 8,772± 0,108
Gambar 11. Sebelum Titrasi Gambar 12. Sesudah Titrasi
Lampiran 9. Hasil Uji Bilangan Asam
A. HCl 0,1 N 1. Pembuatan ml C ol x x mr , x , x , , = 4,0700 ml
Pipet 20 ml HCl P masukkan dalam labu ukur 500 ml larutkan dengan aquades hingga tanda
2. Pembakuan HCl 0,1
Ditimbang 50 mg natrium karbonat anhidrat P yang sebelumnya telah dikeringkan pada suhu 270° selama 1 jam, larutkan dalam 10 ml aquades. Titrasi dengan asam klorida menggunakan indikator merah metil.
40 Cl mg mr x E x t Replikasi ,4 x x , ,7 = 0,089 Replikasi ,4 x x , 4 , = 0,102 Replikasi ,4 x x ,4 44 , 4 = 0,111 Rata rata , , , B. KOH0,1 N 1. Pembuatan
Ditimbang 2,805 gram KOH dalam labu ukur 500 ml tambahkan etanol 95% hingga tanda.
2. Pembakuan
Ditimbang 204,2 mg natrium karbonat anhidrat P yang sebelumnya telah dikeringkan pada suhu 270° selama 1 jam, larutkan dalam 10 ml aquades. Titrasi dengan asam klorida menggunakan indikator merah metil.
mg mr x E x t Replikasi 4, 4, x x , 4, ,
41 = 0,071 Replikasi 4, 4, x x , 4, , = 0,063 Replikasi 4, 4, x x 4, 4, , = 0,068 Rata rata , , , 7 C. Bilangan Asam ngka asam ml x x
erat sampel ( gram )
Replikasi 4,7 x , 7 x , = 130,450 Replikasi x , 7 x , = 110,149 Replikasi , x , 7 x , = 132,329 Rata rata , 4 , 4,
42
Tabel 9. Perhitungan Uji Bilangan Asam
Gambar 13. Sebelum Titrasi Gambar 14. Sesudah Titrasi No. Minyak biji kelor Pembakuan KOH 0,1 N Bilangan Asam 1 Replikasi 1 0,071 130,450 2 Replikasi 2 0,063 110,149 3 Replikasi 3 0,068 132,329 Rata-rata 0,067 124,309± 12,299
43
44