LAPORAN PRAKTEK KERJA PROFESI APOTEKER
DI DIREKTORAT STANDARDISASI OBAT TRADISIONAL,
KOSMETIK, DAN PRODUK KOMPLEMEN
BADAN PENGAWAS OBAT DAN MAKANAN RI
JL. PERCETAKAN NEGARA NO. 23 JAKARTA PUSAT
PERIODE 2 – 24 SEPTEMBER 2013
LAPORAN PRAKTEK KERJA PROFESI APOTEKER
ALI SYAIFULLOH MUNTHYA, S. Farm.
1206329335
ANGKATAN LXXVII
FAKULTAS FARMASI
PROGRAM PROFESI APOTEKER
DEPOK
JANUARI 2014
LAPORAN PRAKTEK KERJA PROFESI APOTEKER
DI DIREKTORAT STANDARDISASI OBAT TRADISIONAL,
KOSMETIK, DAN PRODUK KOMPLEMEN
BADAN PENGAWAS OBAT DAN MAKANAN RI
JL. PERCETAKAN NEGARA NO. 23 JAKARTA PUSAT
PERIODE 2 – 24 SEPTEMBER 2013
LAPORAN PRAKTEK KERJA PROFESI APOTEKER
ALI SYAIFULLOH MUNTHYA, S. Farm.
1206329335
ANGKATAN LXXVII
FAKULTAS FARMASI
PROGRAM PROFESI APOTEKER
DEPOK
JANUARI 2014
LAPORAN PRAKTEK KERJA PROFESI APOTEKER
DI DIREKTORAT STANDARDISASI OBAT TRADISIONAL,
KOSMETIK, DAN PRODUK KOMPLEMEN
BADAN PENGAWAS OBAT DAN MAKANAN RI
JL. PERCETAKAN NEGARA NO. 23 JAKARTA PUSAT
PERIODE 2 – 24 SEPTEMBER 2013
LAPORAN PRAKTEK KERJA PROFESI APOTEKER
ALI SYAIFULLOH MUNTHYA, S. Farm.
1206329335
ANGKATAN LXXVII
FAKULTAS FARMASI
PROGRAM PROFESI APOTEKER
DEPOK
LAPORAN PRAKTEK KERJA PROFESI APOTEKER
DI DIREKTORAT STANDARDISASI OBAT TRADISIONAL,
KOSMETIK, DAN PRODUK KOMPLEMEN
BADAN PENGAWAS OBAT DAN MAKANAN RI
JL. PERCETAKAN NEGARA NO. 23 JAKARTA PUSAT
PERIODE 2 – 24 SEPTEMBER 2013
LAPORAN PRAKTEK KERJA PROFESI APOTEKER
Diajukan sebagai salah satu syarat untuk memperoleh gelar Apoteker
ALI SYAIFULLOH MUNTHYA, S. Farm.
1206329335
ANGKATAN LXXVII
FAKULTAS FARMASI
PROGRAM PROFESI APOTEKER
DEPOK
JANUARI 2014
LAPORAN PRAKTEK KERJA PROFESI APOTEKER
DI DIREKTORAT STANDARDISASI OBAT TRADISIONAL,
KOSMETIK, DAN PRODUK KOMPLEMEN
BADAN PENGAWAS OBAT DAN MAKANAN RI
JL. PERCETAKAN NEGARA NO. 23 JAKARTA PUSAT
PERIODE 2 – 24 SEPTEMBER 2013
LAPORAN PRAKTEK KERJA PROFESI APOTEKER
Diajukan sebagai salah satu syarat untuk memperoleh gelar Apoteker
ALI SYAIFULLOH MUNTHYA, S. Farm.
1206329335
ANGKATAN LXXVII
FAKULTAS FARMASI
PROGRAM PROFESI APOTEKER
DEPOK
JANUARI 2014
LAPORAN PRAKTEK KERJA PROFESI APOTEKER
DI DIREKTORAT STANDARDISASI OBAT TRADISIONAL,
KOSMETIK, DAN PRODUK KOMPLEMEN
BADAN PENGAWAS OBAT DAN MAKANAN RI
JL. PERCETAKAN NEGARA NO. 23 JAKARTA PUSAT
PERIODE 2 – 24 SEPTEMBER 2013
LAPORAN PRAKTEK KERJA PROFESI APOTEKER
Diajukan sebagai salah satu syarat untuk memperoleh gelar Apoteker
ALI SYAIFULLOH MUNTHYA, S. Farm.
1206329335
ANGKATAN LXXVII
FAKULTAS FARMASI
PROGRAM PROFESI APOTEKER
DEPOK
Puji syukur kehadirat Tuhan Yang Maha Esa karena berkat rahmat dan karunia-Nya kami dapat menyelesaikan Laporan Praktek Kerja Profesi Apoteker (PKPA) di Badan Pengawas Obat dan Makanan, Jl. Percetakan Negara No.23, Jakarta Pusat, periode tanggal 2 - 24 September 2013 sebagai salah satu syarat untuk memperoleh gelar Apoteker pada Program Studi Profesi Apoteker Fakultas Farmasi Universitas Indonesia.
Penulis menyadari bahwa tanpa bantuan dari berbagai pihak yang penulis terima, sulit bagi penulis untuk dapat menyelesaikan laporan ini tepat pada waktunya. Oleh karena itu, dalam ruang yang terbatas ini dengan segala kerendahan hati, penulis ingin menyampaikan terima kasih dan rasa hormat kepada:
1. Ibu Dra. Kenik Sintawati, Apt., selaku pembimbing PKPA di Badan Pengawas Obat dan Makanan Republik Indonesia yang telah membimbing dan mengarahkan penulis.
2. Ibu Dr. Amarila Malik, M. S., Apt., selaku pembimbing PKPA di Fakultas Farmasi Universitas Indonesia yang telah membimbing, memberi saran, dan mendukung penulis.
3. Bapak Ir. Roy A. Sparringa, M. App. Sc., Ph.D, selaku Kepala Badan Pengawas Obat dan Makanan Republik Indonesia.
4. Bapak Drs. Hary Wahyu T., Apt., selaku Direktur Standardisasi Obat Tradisional, Kosmetik, dan Produk Komplemen Badan Pengawas Obat dan Makanan Republik Indonesia.
5. Bapak Dr. Mahdi Jufri, M. Si., Apt., selaku Dekan Fakultas Farmasi Universitas Indonesia.
6. Ibu Prof. Dr. Yahdiana Harahap, M. S., Apt., selaku Pj.S Fakultas Farmasi Universitas Indonesia sampai dengan 20 Desember 2013.
7. Bapak Dr. Harmita, Apt., selaku ketua Program Profesi Apoteker Universitas Indonesia.
Standardisasi Obat Tradisional, Kosmetik, dan Produk Komplemen.
9. Ibu Drh. Rachmi Setyorini, MKM., selaku Ka. Sub. Dir. Standardisasi Produk I Direktorat Standardisasi Obat Tradisional, Kosmetik, dan Produk Komplemen Badan Pengawas Obat dan Makanan Republik Indonesia.
10. Seluruh staf dan karyawan Badan Pengawas Obat dan Makanan Republik Indonesia, khususnya Standardisasi Obat Tradisional, Kosmetik, dan Produk Komplemen Badan Pengawas Obat dan Makanan Republik Indonesia, yang telah memberikan bantuan dan perhatian selama pelaksanaan Praktek Kerja Profesi Apoteker.
11. Seluruh staf pengajar dan tata usaha program Profesi Apoteker Universitas Indonesia atas bantuan yang telah diberikan kepada penulis.
12. Keluarga tercinta atas semua dukungan, kasih sayang, perhatian, kesabaran, dorongan, semangat dan doa yang tidak henti-hentinya.
13. Teman-teman Apoteker Angkatan 77 Fakultas Farmasi Universitas Indonesia atas dukungan dan kerja sama selama ini.
14. Semua pihak yang telah memberikan bantuan kepada penulis selama penyusunan laporan ini.
Penulis menyadari bahwa laporan PKPA ini masih jauh dari sempurna. Oleh karena itu penulis mengharapkan kritik dan saran untuk kesempurnaan laporan PKPA ini. Semoga laporan PKPA ini dapat memberikan manfaat bagi pengembangan ilmu pengetahuan dalam dunia farmasi khususnya dan masyarakat pada umumnya.
Penulis,
Nama : Ali Syaifulloh Munthya, S. Farm
NPM : 1206329335
Program Studi : Profesi Apoteker
Judul :Laporan Praktek Kerja Profesi Apoteker di Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen Badan Pengawas Obat dan Makanan Periode 2 – 24 September 2013
Praktek Kerja Profesi Apoteker di Badan Pengawas Obat dan Makanan Republik Indonesia bertujuan untuk mengetahui dan memahami peran dan fungsi Badan Pengawas Obat dan Makanan dan mengetahui dan memahami kegiatan pada Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen di Badan Pengawas Obat dan Makanan. Sedangkan tujuan dari tugas khusus adalah untuk menelaah dampak diberlakukannya kewajiban pencantuman nomor notifikasi pada penandaan kosmetik.
Kata kunci : Badan Pengawas Obat dan Makanan RI, Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen, Obat dan Makanan, Notifikasi Kosmetik, Penandaan Kosmetik
Tugas umum : x + 48 halaman; 5 lampiran Tugas khusus : iii + 14 halaman
Daftar Acuan Tugas Umum : 9 (2001-2013) Daftar Acuan Tugas Khusus : 8 (2003-2013)
Name : Ali Syaifulloh Munthya, S.Farm
NPM : 1206329335
Program Study : Apothecary profession
Title : Pharmacist Internship Program at BPOM RI Period October21st-November 26th2013
Pharmacists Professional Practice in BPOM RI aims to understand the duties and functions of Organization of BPOM RI and also to understand the duties and functions of the part of health personnel, parts standardization herbal medicine, cosmeutic, adan food suplement. While the purpose of the special task is to examine the impact of the inclusion of mandatory notification number on cosmetic labeling.
Keywords : Badan Pengawas Obat dan Makanan RI, Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen, Obat dan Makanan, Notifikasi Kosmetik, Penandaan Kosmetik
General Assignment : x + 48 pages; 5 appendices Specific Assignment : iii + 14 pages;
Bibliography of General Assignment: 9 (2001-2013) Bibliography of Specific Assignment: 8 (2003-2013)
HALAMAN JUDUL ... ii
LEMBAR PENGESAHAN ... iii
KATA PENGANTAR... iv
DAFTAR ISI... vi
DAFTAR LAMPIRAN ... viii
BAB 1 PENDAHULUAN ... 1
1.1 Latar Belakang... 1
1.2 Tujuan... 2
BAB 2 TINJAUAN UMUM BADAN POM... 3
2.1 Kedudukan... 3
2.2 Tugas Pokok, Fungsi dan Kewenangan... 3
2.2.1 Tugas Pokok Badan POM ... 3
2.2.2 Fungsi Badan POM ... 4
2.2.3 Wewenang Badan POM ... 4
2.3 Visi dan Misi Badan POM ... 5
2.3.1 Visi Badan POM... 5
2.3.2 Misi Badan POM ... 5
2.4 Budaya Organisasi... 5
2.5 Kebijakan dan Sasaran Strategi Badan POM ... 6
2.5.1 Sasaran Strategi ... 6
2.5.2 Arah Kebijakan dan Strategi ... 6
2.6 Struktur Organisasi Badan POM ... 8
2.6.1 Kepala Badan POM ... 9
2.6.2 Sekretariat Utama ... 9
2.6.3 Deputi ... 10
2.6.4 Inspektorat ... 16
2.6.5 Pusat Pengujian Obat dan Makanan Nasional... 16
2.6.9 Unit Pelaksanaan teknis Badan POM di Daerah ... 20
2.7 Sistem Pengawasan Obat dan Makanan Badan POM ... 21
2.8 Target kinerja Badan POM... 23
BAB 3 TINJAUAN KHUSUS DIREKTORAT STANDARDISASI OBAT TRADISIONAL, KOSMETIK DAN PRODUK KOMPLEMEN ... 24
3.1 Struktur Organisasi ... 24
3.2 Tugas Pokok ... 24
3.3 Fungsi ... 25
3.4 Sub Direktorat Standardisasi Produk I ... 26
3.5 Sub Direktorat Standardisasi Produk II ... 27
3.6 Sub Direktorat Standardisasi Sarana Produksi ... 28
BAB 4 PEMBAHASAN ... 29
BAB 5 KESIMPULAN DAN SARAN ... 36
5.1 Kesimpulan... 36
5.2 Saran ... 37
DAFTAR PUSTAKA ... 38
Lampiran 1. Struktur Organisasi Badan POM RI ... 39
Lampiran 2. Struktur Organisasi Deputi Bidang Pengawasan
Obat Tradisional, Kosmetik dan Produk Komplemen ... 40
Lampiran 3. Struktur Organisasi Struktur Organisasi Direktorat
Standardisasi Obat Tradisional, Kosmetik dan Produk
Komplemen ... 41
Lampiran 4. Tahapan Penyusunan Peraturan Kepala Badan ... 42
1.1 LATAR BELAKANG
Sejalan dengan meningkatnya laju pertumbuhan masyarakat di Indonesia yang diiringi dengan kesadaran akan kebutuhan konsumen terhadap suatu produk, maka semakin tinggi pula kebutuhan akan konsumsi masyarakat terhadap produk-produk tersebut. Hal tersebut ditandai dengan perubahan gaya hidup masyarakat termasuk pola konsumsinya. Gaya hidup konsumen tersebut pada kenyataanya dapat meningkatkan resiko dengan memberikan efek yang luas pada kesehatan dan keselamatan konsumen. Apabila konsumen menggunakan produk yang rusak atau terkontaminasi oleh bahan berbahaya, maka resiko yang terjadi akan berakibat buruk pada kesehatan tubuh serta berlangsung secara cepat. Sehingga dibutuhkan produk-produk yang aman, bermutu, berkhasiat agar tidak menganggu kesehatan dan keselamatan konsumen.
Sementara itu, pengetahuan masyarakat masih belum memadai untuk dapat memilih dan menggunakan produk secara tepat, benar dan aman. Di sisi lain banyaknya promosi produk mendorong konsumen untuk mengkonsumsi secara berlebihan dan seringkali tidak terjamin secara kemananan, kualitas dan keefektifannya. Oleh karena itu Badan Pengawas Obat dan Makanan (Badan POM) sebagai institusi pemerintah yang melakukan pengawasan terhadap obat, obat tradisional, makanan dan kosmetik di Indonesia perlu menerapkan sistem pengawasan yang efektif dan efisien untuk melindungi keamanan, keselamatan dan kesehatan konsumen.
Apoteker adalah salah satu profesi kesehatan dan merupakan sumber daya manusia yang berkompeten yang memiliki peran penting dalam pengawasan obat dan makanan untuk mendukung tugas Badan POM. Calon Apoteker tidak cukup hanya belajar dari teori melainkan perlu mengetahui dan memahami secara langsung mengenai pengawasan obat dan makanan
Apoteker. Menyadari pentingnya hal tersebut, maka diselenggarakan Praktek Kerja Profesi Apoteker (PKPA) di Badan POM RI Jakarta Pusat. Pelaksanaan tersebut berlangsung mulai tanggal 2 – 24 September 2013. Pendalaman kelompok dilaksanakan di Direktorat Standardisasi Obat Tradisional, Suplemen Makanan dan Kosmetik. Harapan yang ingin dicapai dalam program PKPA ini adalah calon mahasiswa Apoteker mampu menerapkan ilmu yang telah diperolehnya selama pelaksanaan PKPA dalam dunia kerja nantinya.
1.2 TUJUAN
1. Mengetahui dan memahami peran dan fungsi Badan Pengawas Obat dan Makanan.
2. Mengetahui dan memahami kegiatan pada Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen di Badan Pengawas Obat dan Makanan.
BADAN PENGAWAS OBAT DAN MAKANAN
2.1 KEDUDUKAN
Badan Pengawas Obat dan Makanan Republik Indonesia (Badan POM) adalah lembaga pemerintah yang mempunyai wewenang dalam pengawasan obat dan makanan yang beredar di Indonesia. Berdasarkan Keputusan Presiden Republik Indonesia Nomor 103 tahun 2001 yang beberapa kali diubah dengan Keppres No. 3 tahun 2002, Keppres No. 46 tahun 2002, Keppres No. 30 tahun 2003, Keppres No. 9 tahun 2004, Perpres No. 11 tahun 2005, Keppres No. 64 tahun 2005, dan Perpres No. 3 tahun 2013 tentang Kedudukan, Tugas, Fungsi, Kewenangan, Susunan Organisasi, dan Tata Kerja Lembaga Pemerintah Non Kementerian, Badan POM ditetapkan sebagai Lembaga Pemerintah Non Kementerian (LPNK) yang bertanggung jawab kepada Presiden dan dalam melaksanankan tugasnya dikoordinasi oleh Menteri Kesehatan. Struktur organisasi Badan POM dapat dilihat pada Lampiran 1.
2.2 TUGAS POKOK, FUNGSI DAN KEWENANGAN
Berdasarkan Keputusan Presiden Republik Indonesia No. 103 tahun 2001 tentang Kedudukan, Tugas, Fungsi, Kewenangan, Susunan Organisasi, dan Tata Kerja Lembaga Pemerintah Non Kementrian, Badan POM mempunyai tugas, fungsi, dan wewenang sebagai berikut:
2.2.1 Tugas Pokok Badan POM
Seperti yang tercantum dalam Keputusan Presiden Republik Indonesia Nomor 103 tahun 2001 pasal 67, tugas pokok Badan POM adalah melaksanakan tugas pemerintah di bidang pengawasan obat dan makanan sesuai dengan ketentuan peraturan perundang-undangan yang berlaku.
2.2.2 Fungsi Badan POM
Berdasarkan Keputusan Presiden Republik Indonesia Nomor 103 tahun 2001 pasal 68, fungsi Badan POM adalah:
a. Pengkajian dan penyusunan kebijakan nasional di bidang pengawasan obat dan makanan.
b. Pelaksanaan kebijakan tertentu di bidang pengawasan obat dan makanan.
c. Koordinasi kegiatan fungsional dalam pelaksanaan tugas Badan POM.
d. Pemantauan, pemberian bimbingan dan pembinaan terhadap kegiatan instansi pemerintah di bidang Pengawasan Obat dan Makanan.
e. Penyelenggaraan pembinaan dan pelayanan administrasi umum di bidang perencanaan umum, ketatausahaan, organisasi dan tata laksana, kepegawaian, keuangan, kearsipan, persandian, perlengkapan dan rumah tangga.
2.2.3 Wewenang Badan POM
Berdasarkan Keputusan Presiden Republik Indonesia Nomor 103 tahun 2001 pasal 69, wewenang Badan POM adalah:
a. Penyusunan rencana nasional secara makro di bidang pengawasan obat dan makanan.
b. Perumusan kebijakan di bidang pengawasan obat dan makanan untuk mendukung pengobatan secara makro.
c. Penetapan sistem informasi di bidang pengawasan obat dan makanan.
d. Penetapan persyaratan penggunaan bahan tambahan (zat aditif) tertentu untuk makanan dan penetapan pedoman pengawasan peredaran obat dan makanan.
e. Pemberian izin dan pengawasan peredaran obat serta pengawasan industri farmasi.
f. Penetapan pedoman penggunaan, konservasi, pengembangan dan pengawasan tanaman obat.
2.3 VISI DAN MISI BADAN POM
Seperti yang tercantum dalam Keputusan Kepala Badan Pengawas Obat dan Makanan Republik Indonesia No. HK.04.01.21.11.10.10509 Tahun 2010 tentang Penetapan Visi dan Misi Badan Pengawas Obat dan Makanan menyatakan bahwa visi dan misi Badan POM adalah sebagai berikut:
2.3.1 Visi Badan POM
Menjadi Institusi Pengawas Obat dan Makanan yang Inovatif, Kredibel, dan diakui Secara Internasional untuk melindungi masyarakat.
2.3.2 Misi Badan POM
a. Melakukan pengawasan pre-market dan post-market berstandar internasional.
b. Menerapkan sistem manajemen mutu secara konsisten.
c. Mengoptimalkan kemitraan dengan pemangku kepentingan di berbagai lini.
d. Memberdayakan masyarakat agar mampu melindungi diri dari obat dan makanan yang berisiko terhadap kesehatan.
e. Membangun organisasi pembelajaran (Learning Organization).
2.4 BUDAYA ORGANISASI
Sebagai suatu organisasi, Badan POM memiliki nilai – nilai yang diyakini dengan tujuan untuk dihayati dan diamalkan oleh seluruh anggota organisasi dalam melaksanakan tugas. Nilai-nilai luhur yang hidup dan tumbuh berkembang dalam organisasi menjadi semangat bagi seluruh anggota organisasi dalam berkarsa dan berkarya.
Pilar-pilar dari budaya organisasi Badan POM adalah sebagai berikut:
1. Profesional
Menegakkan profesionalisme dengan integritas, objektivitas, ketekunan dan komitmen yang tinggi.
2. Kredibel
Dapat dipercaya dan diakui oleh masyarakat luas, nasional dan internasional.
3. Cepat tanggap
Antisipatif dan responsif dalam mengatasi masalah. 4. Kerjasama tim
Mengutamakan keterbukaan, saling percaya dan komunikasi yang baik.
5. Inovatif
Mampu melakukan pembaruan sesuai ilmu pengetahuan dan teknologi terkini.
2.5 KEBIJAKAN DAN STRATEGI BADAN POM 2.5.1 Sasaran Strategi
Sasaran strategi Badan POM selama 5 tahun adalah sebagai berikut:
a. Pengawasan obat dan makanan terlaksana secara efektif untuk melindungi konsumen di dalam dan di luar negeri dengan sistem yang tergolong terbaik di ASEAN.
b. Terwujudnya laboratorium pengawasan obat dan makanan yang modern dengan jaringan kerja di seluruh Indonesia dengan kompetensi dan kapabilitas terunggul di ASEAN.
c. Meningtkatnya kompetensi, kapabilitas, dan jumlah modal insane yang unggul dalam melaksanakan pengawasan obat dan makanan. d. Diterapkannya sistem manajemen mutu di semua unit kerja Badan
POM.
2.5.2 Arah Kebijakan dan Strategi Nasional
Arah kebijakan dan strategi nasional bidang kesehatan yang menjadi acuan pembangunan bidang Pengawasan Obat dan Makanan.
1. Fokus 1: Peningkatan Kesehatan ibu, bayi, balita dan keluarga berencana
Peningkatan kesehatan ibu, bayi, balita dan Keluarga Berencana melalui upaya yang menjamin produk obat dan makanan yang memenuhi persyaratan keamanan dan mutu, yang digunakan dalam upaya:
a) Peningkatan cakupan peserta KB aktif
b) Pemberian makanan pemulihan bagi ibu hamil kekurangan energi kronis (KEK)
c) Pencapaian cakupan imunisasi yang tinggi, merata dan berkualitas pada bayi, anak sekolah dan wanita usia subur (WUS)
2. Fokus 2: perbaikan status gizi masyarakat
Perbaikan status gizi masyarakat, melalui pengujian laboratorium terhadap sampel-sampel produk yang digunakan untuk upaya:
a) Asupan zat gizi makro, dll, untuk memenuhi angka kecukupan gizi
b) Surveilans pangan dan gizi
c) Pemberian makanan pendamping ASI d) Fortifikasi
e) Pemberian makanan pemulihan balita gizi kurang f) Penanggulangan gizi darurat
3. Fokus 3: pengendalian penyakit menular serta penyakit tidak menular, diikuti penyehatan lingkungan
Pengendalian penyakit menular serta penyakit tidak menular, diikuti penyehatan lingkungan, melalui upaya pengawasan yang diarahkan untuk menurunkan proporsi obat dan makanan bermasalah di pasar, sebagai salahsatu faktor risiko timbulnya penyakit.
4. Fokus 4: peningkatan ketersediaan, keterjangkuan, pemerataan, mutu dan penggunaan obat serta pengawasan obat dan makanan
Peningkatan ketersediaan, keterjangkauan, pemerataan, mutu dan penggunaan obat, serta pengawasan Obat dan Makanan, yang dilaksanakan melalui pelaksanaan kegiatan-kegiatan:
a) Pengawasan produksi produk terapetik dan PKRT b) Pengawasan produk dan bahan berbahaya
c) Pengawasan obat dan makanan di 31 Balai Besar/ Balai POM d) Pemeriksaan secara laboratorium, pengujian dan penilaian
keamanan, manfaat dan mutu obat dan makanan serta pembinaan laboratorium POM
e) Standarisasi produk terapetik dan PKRT
f) Penyelidikan dan penyidikan terhadap pelanggaran di bidang obat dan makanan
g) Inspeksi dan sertifikasi makanan
h) Standarisasi obat tradisional, kosmetik dan produk komplemen i) Standarisasi makanan
j) Surveilan dan penyuluhan keamanan makanan k) Pengawasan distribusi produk terapetik dan PKRT
l) Pengawasan narkotika, psikotropika, prekursor dan zat adiktif m) Penilaian produk terapetik dan produk biologi
n) Penilaian obat tradisional, kosmetik dan produk komplemen o) Penilaian makanan
p) Riset keamanan, khasiat, mutu obat dan makanan q) Pengembangan Obat Asli Indonesia
2.6 STRUKTUR ORGANISASI BADAN POM
Berdasarkan Keputusan Presiden Republik Indonesia Nomor 103 tahun 2001 tentang Kedudukan, Tugas, Fungsi, Kewenangan, Susunan Organisasi, dan Tata Kerja Lembaga Pemerintah Non Departemen, Badan POM terdiri atas Kepala, Inspektorat, Sekretariat Utama, Deputi dan Unit Pelaksana Teknis Balai Besar/Balai POM. Deputi terdiri dari beberapa Direktorat yang mempunyai bagiannya masing-masing. Berikut ini merupakan struktur organisasi Badan POM:
2.6.1 Kepala Badan POM
Berdasarkan Keputusan Presiden Republik Indonesia Nomor 103 tahun 2001 Pasal 80, Badan POM adalah pemimpin dari Badan POM dan mempunyai tugas sebagai berikut:
a. Memimpin Badan POM sesuai dengan ketentuan peraturan perundang undangan yang berlaku.
b. Menyiapkan kebijakan nasional dan kebijakan umum sesuai dengan tugas Badan POM.
c. Menetapkan kebijakan teknis pelaksanaan tugas Badan POM yang menjadi tanggung jawabnya.
d. Membina dan melaksanakan kerjasama dengan instansi dan organisasi lain.
2.6.2 Sekretariat Utama
a. Tugas Sekretariat Utama
Berdasarkan Keputusan Presiden Republik Indonesia Nomor 103 tahun 2001 Bagian Ketiga Pasal 83, Sekretariat Utama ditujukan sebagai unsur pembantu pimpinan Badan POM yang berada di bawah dan bertanggungjawab kepada Kepala Badan POM. Dalam pelaksanaannya, Sekretariat Utama mempunyai tugas mengkoordinasi perencanaan, pembinaan, pengendalian terhadap program, administrasi, dan sumber daya di Badan POM, seperti perencanaan strategis dan organisasi, pengembangan pegawai, pengelolaan keuangan, bantuan hukum dan legislasi, hubungan masyarakat dan kerjasama internasional, serta akses masyarakat terhadap Badan POM melalui Unit Layanan Pengaduan Konsumen yang menerima dan menindaklanjuti berbagai pengaduan dari masyarakat di bidang obat dan makanan, serta dilakukan pembinaan administratif beberapa pusat yang ada di lingkungan Badan POM dan unit-unit pelaksana teknis yang tersebar di seluruh Indonesia.
b. Fungsi Sekretariat utama
Fungsi sekretariat utama, antara lain:
1) Pengkoordinasian, sinkronisasi dan integrasi perencanaan, penganggaran, penyusunan laporan, pengembangan pegawai termasuk pendidikan dan pelatihan serta perumusan kebijakan teknis di lingkungan Badan POM.
2) Pengkoordinasian, sinkronisasi, dan integrasi penyusunan peraturan perundang-undangan, kerjasama luar negeri, hubungan antarlembaga, kemasyarakatan, dan bantuan hukum yang berkaitan dengan tugas Badan POM.
3) Pembinaan dan pelayanan administrasi ketatausahaan, organisasi dan tata laksana, kepegawaian, keuangan, kearsipan, perlengkapan dan rumah tangga.
4) Pembinaan dan pengendalian terhadap pelaksanaan kegiatan pusat-pusat dan unit-unit pelaksana teknis di lingkungan Badan POM.
5) Pengkoordinasian administrasi pelaksanaan tugas Deputi di lingkungan Badan POM.
6) Pelaksanaan tugas lain yang ditetapkan oleh Kepala, sesuai dengan bidang tugasnya.
c. Struktur Sekretariat utama
Sekretariat utama terdiri dari: 1. Biro Perencanaan dan Keuangan 2. Biro Kerjasama Luar Negeri
3. Biro Hukum dan Hubungan Masyarakat 4. Biro Umum
2.6.3 Deputi
Berdasarkan Keputusan Presiden Republik Indonesia Nomor 103 tahun 2001 Bagian Ketiga, Deputi bertanggung jawab terhadap Kepala dan mempunyai tugas merumuskan dan
melaksanakan kebijakan di bidang tertentu. Deputi di Badan POM terdiri dari:
a. Deputi I Bidang Pengawasan Produk Terapetik, Narkotika, Psikotropika dan Zat Adiktif (NAPZA)
1) Tugas Deputi I
Deputi Bidang Pengawasan Produk Terapetik dan NAPZA bertugas melaksanakan perumusan kebijakan di bidang pengawasan produk Terapetik dan NAPZA dengan menyelenggarakan fungsi sebagai berikut:
a) Pengkajian dan penyusunan kebijakan nasional dan kebijakan umum di bidang pengawasan produk terapetik dan NAPZA.
b) Penyusunan rencana pengawasan produk terapetik dan NAPZA.
c) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan di bidang penilaian obat dan produk biologi.
d) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan di bidang penilaian alat kesehatan, produk diagnostik dan perbekalan kesehatan rumah tangga.
e) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan di bidang standardisasi produk terapetik.
f) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan di bidang inspeksi dan sertifikasi produk terapetik.
g) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan di bidang pengawasan NAPZA.
h) Pengawasan produk terapetik dan NAPZA.
i) Koordinasi kegiatan fungsional pelaksanaan kebijakan di bidang pengawasan produk terapetik dan NAPZA.
j) Evaluasi pelaksanaan kebijakan teknis pengawasan produk terapetik dan NAPZA.
k) Pelaksanaan tugas lain yang ditetapkan oleh Kepala, sesuai dengan bidang tugasnya.
2) Struktur Deputi I
Deputi Bidang Pengawasan Produk Terapetik dan NAPZA terdiri dari:
a) Direktorat Penilaian Obat dan Produk Biologi.
b) Direktorat Standardisasi Produk Terapetik dan PKRT. c) Direktorat Inspeksi dan Sertifikasi Produk Terapetik. d) Direktorat Pengawasan NAPZA.
b. Deputi II Bidang Pengawasan Obat Tradisional, Kosmetik, dan Produk Komplemen
1) Tugas Deputi II
Deputi Bidang Pengawasan Obat Tradisional, Kosmetik dan Produk Komplemen mempunyai tugas melaksanakan perumusan kebijakan dibidang pengawasan obat tradisional, kosmetik dan produk komplemen.
2) Fungsi Deputi II
Dalam melaksanakan tugas Deputi Bidang Pengawasan Obat Tradisional, Kosmetik dan Produk Komplemen menyelenggarakan fungsi sebagai:
a) Pengkajian dan penyusunan nasional dan kebijakan umum di bidang pengawasan obat tradisional, kosmetik dan produk komplemen.
b) Penyusunan rencana pengawasan obat tradisional, kosmetik dan produk komplemen.
c) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan di bidang penilaian obat tradisional, suplemen makanan dan kosmetik. d) Perumusan kebijakan teknis, penetapan pedoman, standar,
kriteria dan prosedur pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan dibidang pengaturan dan standardisasi obat tradisional, kosmetik dan produk komplemen.
e) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan dibidang inspeksi dan sertifikasi obat tradisional, kosmetik dan produk komplemen.
f) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan di bidang Obat Asli Indonesia.
g) Pengawasan obat tradisional, kosmetik dan produk komplemen.
h) Koordinasi kegiatan fungsional pelaksanaan kebijakan di bidang pengawasan obat tradisional, kosmetik dan produk komplemen.
i) Evaluasi pelaksanaan kebijakan teknis pengawasan obat tradisional, kosmetik dan produk komplemen
j) Pelaksanaan tugas lain yang ditetapkan oleh Kepala, sesuai dengan bidang tugasnya.
3) Struktur Deputi II
Deputi Bidang Pengawasan Obat Tradisional, Kosmetik dan Produk Komplemen, terdiri dari:
a) Direktorat Penilaian Obat Tradisional, Suplemen Makanan dan Kosmetik.
b) Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen.
c) Direktorat Inspeksi dan Sertifikasi Obat Tradisional, Kosmetik dan Produk Komplemen.
d) Direktorat Obat Asli Indonesia.
c. Deputi III Bidang Pengawasan Keamanan Pangan dan Bahan Berbahaya
1) Tugas Deputi III
Deputi Bidang Pengawasan Keamanan Pangan dan Bahan Berbahaya mempunyai tugas melaksanakan perumusan kebijakan di bidang pengawasan keamanan pangan dan bahan berbahaya.
2) Fungsi Deputi III
Dalam melaksanakan tugasnya, Deputi Bidang Pengawasan Keamanan Pangan dan Bahan Berbahaya menyelenggarakan fungsi sebagai berikut:
a) Pengkajian dan penyusunan kebijakan nasional dan kebijakan umum di bidang pengawasan keamanan pangan dan bahan berbahaya.
b) Penyusunan rencana pengawasan keamanan pangan dan bahan berbahaya.
c) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan di bidang penilaian keamanan pangan.
d) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan di bidang standarisasi produk pangan.
e) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan di bidang inspeksi dan sertifikasi pangan.
f) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan di bidang surveilan dan penyuluhan keamanan pangan.
g) Perumusan kebijakan teknis, penetapan pedoman, standar, kriteria dan prosedur, pengendalian pelaksanaan kebijakan teknis, pemantauan, pemberian bimbingan di bidang pengawasan produk dan bahan berbahaya.
h) Pengawasan keamanan pangan dan bahan berbahaya. i) Koordinasi kegiatan fungsional pelaksanaan kebijakan di
bidang pengawasan keamanan pangan dan bahan berbahaya.
j) Evaluasi pelaksanaan kebijakan teknis pengawasan keamanan pangan dan bahan berbahaya.
k) Pelaksanaan tugas lain yang ditetapkan oleh Kepala, sesuai dengan bidang tugasnya.
3) Struktur Deputi III
Deputi Bidang Pengawasan Keamanan Pangan dan Bahan Berbahaya terdiri dari:
a) Direktorat Penilaian Keamanan Pangan. b) Direktorat Standardisasi Produk Pangan.
c) Direktorat Inspeksi dan Sertifikasi Pangan Direktorat Surveilan dan Penyuluhan Keamanan Pangan.
2.6.4 Inspektorat
Inspektorat dipimpin oleh Inspektur yang berada di bawah dan bertanggung jawab kepada Kepala Badan POM. Dalam pelaksanaan tugas sehari-hari, Inspektorat dibina oleh Sekretaris Utama.
a. Tugas Inspektorat
Inspektorat memiliki tugas melaksanakan pengawasan fungsional di lingkungan Badan POM.
b. Fungsi Inspektorat
Dalam melaksanakan tugasnya, Inspektorat menyelenggarakan fungsi sebagai berikut:
1) Penyiapan perumusan kebijakan, rencana dan program pengawasan fungsional.
2) Pelaksanaan pengawasan fungsional sesuai dengan ketentuanperaturan perundang-undangan yang berlaku. 3) Pengusutan mengenai kebenaran laporan atau pengaduan
tentang hambatan, penyimpangan atau penyalahgunaan dalam pelaksanaan tugas yang dilakukan oleh unsur atau unit di lingkungan Badan POM.
4) Pelaksanaan urusan tata usaha Inspektorat.
2.6.5 Pusat Pengujian Obat dan Makanan Nasional
Pusat Pengujian Obat dan Makanan Nasional (PPOMN) merupakan rujukan dari 26 laboratorium pemeriksaan obat dan makanan di seluruh Indonesia yang telah diakreditasi oleh Komite Akreditasi Nasional, Badan Standardisasi Nasional, serta merupakan WHO Collaborating Center sejak tahun 1986 dan anggota International Certification Scheme. Fasilitas penunjang dari PPOMN adalah laboratorium bioteknologi, laboratorium baku pembanding, laboratorium kalibrasi, laboratorium hewan percobaan dan didukung dengan peralatan laboratorium canggih untuk analisis fisikokimia
seperti Kromatografi Cair Kinerja Tinggi, Kromatografi Gas, Spektrofotometer Absorpsi Atom, Spektrofotometer Infra Merah; analisis fisik seperti Alat Uji Disolusi Otomatis dan Smoking Machine serta peralatan untuk analisis mikrobiologi dan biologi.
Pusat Pengujian Obat dan Makanan Nasional adalah unsur pelaksana tugas Badan POM yang berada di bawah dan bertanggung jawab kepada Kepala Badan POM, dalam pelaksanaan tugas sehari-hari secara teknis dibina oleh Deputi dan secara administrasi dibina oleh Sekretariat Utama. Pusat Pengujian Obat dan Makanan Nasional dipimpin oleh seorang Kepala.
a. Tugas PPOMN
PPOMN mempunyai tugas melaksanakan pemeriksaan secara laboratorium, pengujian dan penilaian mutu Produk Terapetik, Narkotika, Psikotropika dan Zat Adiktif lain, Alat Kesehatan, Obat Tradisional, Kosmetik, Produk Komplemen, Pangan dan Bahan Berbahaya sesuai dengan peraturan perundang-undangan yang berlaku, serta melaksanakan pembinaan laboratorium pengawasan obat dan makanan.
b. Fungsi PPOMN
Dalam melaksanakan tugasnya, PPOMN menyelenggarakan fungsi:
1) Penyusunan rencana dan program pengujian obat dan makanan.
2) Pelaksanaan pemeriksaan secara laboratorium, pengujian dan penilaian mutu produk Terapetik, NAPZA, alat kesehatan, obat tradisional, kosmetik, produk komplemen, pangan dan bahan berbahaya.
3) Pembinaan mutu laboratorium Pengujian Obat dan Makanan di seluruh Indonesia.
4) Pelaksanaan sistem rujukan pengawasan obat dan makanan. 5) Penyediaan baku pembanding dan pengembangan metode
6) Pelatihan tenaga ahli di bidang pengujian obat dan makanan. 7) Evaluasi dan penyusunan laporan pengujian obat dan
makanan.
8) Pelaksanaan urusan tata usaha dan kerumahtanggaan pusat.
2.6.6 Pusat Penyidikan Obat dan Makanan
Pusat Penyidikan Obat dan Makanan adalah unsur pelaksana tugas Badan POM yang berada di bawah dan bertanggung jawab kepada Kepala Badan POM, dalam pelaksanaan tugas sehari-hari secara teknis dibina oleh Deputi dan secara administrasi dibina oleh Sekretariat Utama. Pusat Pengujian Obat dan Makanan Nasional dipimpin oleh seorang Kepala.
a. Tugas PPOM
Pusat Penyidikan Obat dan Makanan (PPOM) memiliki tugas melaksanakan kegiatan penyelidikan dan penyidikan terhadap perbuatan melawan hukum di bidang produk terapetik, narkotika, psikotropika dan zat adiktif, obat tradisional, kosmetik dan produk komplemen dan makanan serta produk sejenis lainnya.
b. Fungsi PPOM
Dalam melaksanakan tugasnya, PPOM menyelenggarakan fungsi:
1) Penyusunan rencana dan program penyelidikan dan penyidikan obat dan makanan.
2) Pelaksanaan penyelidikan dan penyidikan obat dan makanan. 3) Evaluasi dan penyusunan laporan pelaksanaan penyelidikan
dan penyidikan obat dan makanan.
2.6.7 Pusat Riset Obat dan Makanan
Pusat Riset Obat dan Makanan adalah unsur pelaksana tugas Badan POM yang berada di bawah dan bertanggung jawab kepada Kepala Badan POM, dalam pelaksanaan tugas sehari-hari secara
teknis dibina oleh Deputi dan secara administrasi dibina oleh Sekretariat Utama. Pusat Pengujian Obat dan Makanan Nasional dipimpin oleh seorang Kepala.
a. Tugas PROM
Pusat Riset Obat dan Makanan (PROM) mempunyai tugas melaksanakan kegiatan di bidang riset toksikologi, keamanan pangan dan produk terapetik.
b. Fungsi PROM
Dalam melaksanakan tugasnya, PROM menyelenggarakan fungsi:
1) Penyusunan rencana dan program riset obat dan makanan. 2) Pelaksanaan riset obat dan makanan.
3) Evaluasi dan penyusunan laporan pelaksanaan riset obat dan makanan.
2.6.8 Pusat Informasi Obat dan Makanan
Pusat Informasi Obat dan Makanan adalah unsur pelaksana tugas Badan POM yang berada di bawah dan bertanggung jawab kepada Kepala Badan POM, dalam pelaksanaan tugas sehari-hari secara teknis dibina oleh Deputi dan secara administrasi dibina oleh Sekretariat Utama. Pusat Pengujian Obat dan Makanan Nasional dipimpin oleh seorang Kepala.
a. Tugas PIOM
Pusat Informasi Obat dan Makanan (PIOM) mempunyai tugas melaksanakan kegiatan di bidang pelayanan informasi obat, informasi kemananan pangan, informasi keracunan dan teknologi informasi.
b. Fungsi PIOM
Dalam melaksanakan tugasnya, PIOM menyelenggarakan fungsi:
1) Penyusunan rencana dan program kegiatan pelayanan informasi obat dan makanan.
2) Pelaksanaan pelayanan informasi obat. 3) Pelaksanaan pelayanan informasi keracunan.
4) Pelaksanaan kegiatan di bidang teknologi informasi.
5) Evaluasi dan penyusunan laporan pelaksanaan pelayanan informasi obat dan makanan.
6) Pelaksanaan urusan tata usaha dan kerumahtanggaan pusat.
2.6.9 Unit Pelaksana Teknis Badan POM di Daerah
Organisasi dan Tata kerja Unit Pelaksana Teknis di Lingkungan Badan POM terdiri atas 19 (sembilan belas) Balai Besar Pengawas Obat dan Makanan dan 12 (dua belas) Balai Pengawas Obat dan Makanan.
a. Tugas Unit Pelaksana Teknis Badan POM
Unit Pelaksana Teknis Badan POM adalah unit organisasi yang melaksanakan tugas dan fungsi pengawasan obat dan makanan di wilayah kerjanya, diatur, dengan Keputusan Kepala Badan POM setelah mendapat persetujuan tertulis dari Menteri yang bertanggung jawab di bidang pendayagunaan aparatur Negara. Unit Pelaksana Teknis Badan POM mempunyai tugas melaksanakan kebijakan di bidang pengawasan produk terapeutik, narkotika, psikotropika dan zat adiktif lain, obat tradisonal, kosmetik, produk komplemen, keamanan pangan dan bahan berbahaya.
b. Fungsi Unit Pelaksana Teknis Badan POM
Unit Pelaksana Teknis memiliki fungsi yaitu:
1) Penyusunan rencana dan program pengawasan obat dan makanan.
2) Pelaksanaan pengujian dan penilaian mutu produk terapetik, narkotika, psikotropika dan zat adiktif lain, obat tradisional, kosmetik, produk komplemen, pangan dan bahan berbahaya. 3) Pelaksanaan pengujian laboratorium dan penilaian mutu
4) Pelaksanaan pemeriksaan setempat, pengambilan contoh dan pemeriksaan sarana produksi dan distribusi.
5) Pelaksanaan penyidikan dan penyelidikan pada kasus pelanggaran hukum.
6) Pelaksanaan sertifikasi produk, sarana produksi dan distribusi. Pelaksanaan kegiatan pelayanan informasi konsumen.
7) Evaluasi dan penyusunan laporan pengujian obat dan makanan.
8) Pelaksanaan urusan tata usaha dan kerumahtanggaan.
9) Pelaksanaan tugas lain yang ditetapkan oleh Kepala Badan Pengawas Obat dan Makanan, sesuai dengan bidang tugasnya.
2.7 SISTEM PENGAWASAN OBAT DAN MAKANAN BADAN POM
Proses mengawasi obat dan makanan mempunyai permasalahan dengan dimensi yang luas dan kompleks. Dari segi datangnya produk yang perlu diawasi, permasalahan datang dari 2 sisi yaitu dari luar dan dalam negeri. Produk luar akan masuk dengan mudah ke dalam Indonesia lewat perdagangan internasional yang tanpa/kurang perlindungan. Ini diakibatkan adanya globalisasi ekonomi yang memasuki era pasar bebas. Tidak hanya produk dari luar, tetapi produk dari dalam di pasar global. Penyebabnya akibat dari globalisasi komunikasi, teknologi, transportasi memudahkan memodernisasinya suatu industri.
Diperlukan suatu sistem pengawasan yang komprehensif, dimulai dari awal proses suatu produk hingga produk tersebut beredar di tengah masyarakat. Upaya yang dilakukan untuk menekan sekecil mungkin risiko yang bisa terjadi, dilakukan SISPOM tiga lapis, yang tak lain ditujukan untuk keamanan masyarakat Indonesia:
1. Sub-sistem pengawasan Produsen
Sistem pengawasan internal oleh produsen melalui pelaksanaan cara-cara produksi yang baik atau Good Manufacturing Practices (GMP) agar setiap bentuk penyimpangan dari standar mutu dapat dideteksi sejak awal. Secara hukum produsen bertanggung jawab atas mutu dan keamanan
produk yang dihasilkannya. Apabila terjadi penyimpangan dan pelanggaran terhadap standar yang telah ditetapkan maka produsen dikenakan sanksi, baik administratif maupun pro justitia.
2. Sub-sistem pengawasan Konsumen
Sistem pengawasan oleh masyarakat konsumen sendiri melalui peningkatan kesadaran dan pengetahuan mengenai kualitas produk yang digunakannya dan cara penggunaan produk yang rasional. Pengawasan oleh masyarakat sendiri sangat penting dilakukan karena pada akhirnya masyarakatlah yang mengambil keputusan untuk membeli dan menggunakan suatu produk.
Konsumen dengan kesadaran dan tingkat pengetahuan yang tinggi terhadap mutu dan kegunaan suatu produk di satu sisi dapat membentengi dirinya sendiri terhadap penggunaan produk-produk yang tidak memenuhi syarat dan tidak dibutuhkan, sedang pada sisi lain akan mendorong produsen untuk ekstra hati-hati dalam menjaga kualitasnya.
3. Sub-sistem pengawasan Pemerintah/ Badan POM
Sistem pengawasan oleh pemerintah melalui pengaturan dan standardisasi, penilaian keamanan, khasiat dan mutu produk sebelum diijinkan beredar di Indonesia; inspeksi, pengambilan sampel dan pengujian laboratorium produk yang beredar serta peringatan kepada publik yang didukung penegakan hukum. Untuk meningkatkan kesadaran dan pengetahuan masyarakat konsumen terhadap mutu, khasiat dan keamanan produk maka pemerintah juga melaksanakan kegiatan komunikasi, informasi dan edukasi.
Prinsip dasar Sistem Pengawasan Obat dan Makanan: a. Tindakan pengaman yang cepat, tepat, akurat dan profesional.
b. Tindakan dilakukan berdasarkan atas tingkat risiko dan berbasis bukti-bukti ilmiah.
c. Lingkungan pengawasan bersifat menyeluruh, mencakup seluruh siklus proses.
d. Berskala nasional/lintas provinsi, dengan jaringan kerja internasional. e. Otoritas yang menunjang penegakan supremasi hukum.
f. Memiliki jaringan laboratorium nasional yang kohesif dan kuat yang berkolaborasi dengan jaringan global. Memiliki jaringan sistem informasi keamanan dan mutu produk.
2.8 TARGET KINERJA BADAN POM
Target kinerja dari Badan POM yaitu:
1. Terkendalinya penyaluran produk Terapetik dan NAPZA.
2. Terkendalinya mutu, keamanan dan khasiat/kemanfaatan produk obat dan makanan termasuk klaim pada label dan iklan di peredaran.
3. Tercegahnya risiko penggunaan bahan kimia berbahaya sebagai akibat pengelolaan yang tidak memenuhi syarat.
4. Penurunan kasus pencemaran pangan.
5. Peningkatan kapasitas organisasi yang didukung dengan kompetensi dan keterampilan personel yang memadai.
6. Terwujudnya komunikasi yang efektif dan saling menghargai antara sesama dan pihak terkait.
DIREKTORAT STANDARDISASI OBAT TRADISIONAL, KOSMETIK DAN PRODUK KOMPLEMEN
3.1 STRUKTUR ORGANISASI
Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen dipimpin oleh seorang Direktur yang membawahi 3 (tiga) Sub Direktorat yaitu Sub Direktorat Standardisasi Produk I, Sub Direktorat Standardisasi Produk II dan Sub Direktorat Standardisasi Sarana Produksi. Produk I merupakan produk Obat Tradisional dan Suplemen Makanan sedangkan Produk II merupakan produk Kosmetik. Masing-masing Sub Direktorat dipimpin oleh seorang Kepala Sub Direktorat (Ka.Subdit) yang membawahi beberapa Seksi. Sub Direktorat Standardisasi Produk I membawahi Seksi Standardisasi Obat Tradisional dan Suplemen Makanan, Seksi Standardisasi Sediaan Galenik dan Seksi Tata Operasional.
Sub Direktorat Produk II membawahi Seksi Standardisasi Bahan Kosmetik dan Seksi Standardisasi Kosmetik. Sub Direktorat Standardisasi Sarana Produksi membawahi Seksi Standardisasi Sarana Produksi Obat Tradisional dan Suplemen Makanan dan Seksi Standardisasi Sarana Produksi Kosmetik. Seksi Tata Operasional berkoordinasi dengan seluruh Sub Direktorat.
3.2 TUGAS POKOK
Berdasarkan Keputusan Kepala BPOM RI No.02001/SK/KBPOM tanggal 26 Februari tahun 2001 Pasal 182, Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen mempunyai tugas penyiapan perumusan kebijakan, penyusunan pedoman, standar, kriteria dan prosedur, serta pelaksanaan pengendalian, bimbingan teknis dan evaluasi dibidang
pengendalian dan standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen.
3.3 FUNGSI
Fungsi Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen menurut Keputusan Kepala BPOM RI No.02001/SK/KBPOM tanggal 26 Februari tahun 2001 Pasal 183 adalah sebagai berikut:
1. Penyiapan bahan perumusan kebijakan teknis, penyusunan pedoman, standar, kriteria dan prosedur serta pelaksanaan pengendalian, pemantauan, pemberian bimbingan dan pembinaan di bidang pengaturan dan standardisasi Produk I.
2. Penyiapan bahan perumusan kebijakan teknis, penyusunan pedoman, standar, kriteria dan prosedur serta pelaksanaan pengendalian, pemantauan, pemberian bimbingan dan pembinaan di bidang pengaturan dan standardisasi Produk II.
3. Penyiapan bahan perumusan kebijakan teknis, penyusunan pedoman, standar, kriteria dan prosedur, serta pelaksanaan pengendalian, pemantauan, pemberian bimbingan dan pembinaan di bidang pengaturan dan standardisasi sarana produksi Obat Tradisional, Kosmetik dan Produk Komplemen.
4. Penyusunan rencana dan program standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen.
5. Koordinasi kegiatan fungsional pelaksanaan kebijakan teknis di bidang pengaturan dan standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen.
6. Evaluasi dan penyusunan laporan di bidang pengaturan dan standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen.
7. Pelaksanaan tugas lain sesuai dengan kebijakan yang ditetapkan oleh Deputi Bidang Pengawasan Obat Tradisional, Kosmetik dan Produk Komplemen.
3.4 SUB DIREKTORAT STANDARDISASI PRODUK I
1. Tugas
Melaksanakan penyiapan bahan perumusan kebijkan teknis, penyusunan pedoman, standar, kriteria dan prosedur, evaluasi dan pelaksanaan pengaturan dan standardisasi Produk I.
2. Fungsi
Sub Direktorat Standardisasi Produk I memiliki fungsi sebgai berikut:
a. Penyusunan rencana dan program standardisasi Produk I.
b. Pelaksanaan penyiapan bahan perumusan kebijakan teknis, penyusunan pedoman, standar, kriteria dan prosedur, serta pelaksanaan
pengaturan dan standardisasi Obat Tradisional dan Suplemen Makanan.
c. Pelaksanaan penyiapan bahan perumusan kebijakan teknis, penyusunan pedoman, standar, kriteria dan prosedur serta pelaksanaan
pengaturan dan standardisasi Sediaan Galenik.
d. Evaluasi dan penyusunan laporan standardisasi Produk I.
e. Pelaksanaan urusan tata operasional di lingkungan Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen. 3. Struktur Sub Direktorat Standardisasi Produk I
Sub Direktorat Standardisasi Produk I terdiri dari:
a. Seksi Standardisasi Obat Tradisional dan Suplemen Makanan, mempunyai tugas menyiapkan bahan perumusan kebijakan teknis, penyusunan perencanaan dan program, penyusunan pedoman, standar, kriteria dan prosedur, evaluasi dan penyusunan laporan, serta melakukan pengaturan dan standardisasi Obat Tradisional dan Suplemen Makanan.
b. Seksi Standardisasi Sediaan Galenik, mempunyai tugas menyiapkan bahan perumusan kebijakan teknis, penyusunan rencana dan program, penyusunan pedoman, standar, kriteria dan prosedur, evaluasi dan penyusunan laporan, serta melakukan pengaturan dan standardisasi Sediaan Galenik.
c. Seksi Tata Operasional mempunyai tugas melakukan urusan tata operasional di lingkungan Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen.
3.5 SUB DIREKTORAT STANDARDISASI PRODUK II
1. Tugas
Melaksanakan penyiapan bahan perumusan kebijakan teknis, penyusunan pedoman, standar, kriteria dan prosedur, evaluasi dan pelaksanaan pengaturan dan standardisasi Produk II.
2. Fungsi
Sub Direktorat Standardisasi Produk II memiliki fungsi sebagai berikut:
a. Penyusunan rencana dan program standardisasi Produk II.
b. Pelaksanaan penyiapan bahan perumusan kebijakan teknis, penyusunan pedoman, standar, kriteria dan prosedur, serta pelaksanaan pengaturan dan standardisasi Bahan Kosmetik.
c. Pelaksanaan penyiapan bahan perumusan kebijakan teknis, penyusunan pedoman, standar, kriteria prosedur serta pelaksanaan pengaturan dan Standardisasi Kosmetik.
d. Evaluasi dan penyusunan laporan standardisasi Produk II. 3. Struktur Sub Direktorat Standardisasi Produk II
Sub Direktorat Standardisasi Produk II terdiri dari:
a. Seksi Standardisasi Bahan Kosmetik mempunyai tugas menyiapkan bahan perumusan kebijakan teknis, penyusunan rencana dan program, penyusunan pedoman, standar, kriteria dan prosedur, evaluasi dan penyusunan laporan, serta melakukan pengaturan dan standardisasi Bahan Kosmetik.
b. Seksi Standardisasi Kosmetik, mempunyai tugas menyiapkan bahan perumusan kebijakan teknis, penyusunan rencana dan program, penyusunan pedoman, standar, kriteria dan prosedur, evaluasi dan penyusunan laporan serta melakukan pengaturan dan Standardisasi Kosmetika.
3.6 SUB DIREKTORAT STANDARDISASI SARANA PRODUKSI
1. Tugas
Melaksanakan penyiapan bahan perumusan kebijakan teknis, penyusunan pedoman, standar, kriteria dan prosedur, evaluasi dan pelaksanaan pengaturan dan standardisasi sarana produksi.
2. Fungsi
a. Penyusunan rencana dan program standardisasi sarana produksi Obat Tradisional, Kosmetik dan Produk Komplemen.
b. Pelaksanaan penyiapan bahan perumusan kebijakan teknis, penyusunan pedoman, standar, kriteria dan prosedur, serta pelaksanaan pengaturan dan standardisasi sarana produksi Obat Tradisional dan Suplemen Makanan.
c. Pelaksanaan penyiapan bahan perumusan kebijakan teknis, penyusunan pedoman, standar, kriteria dan prosedur, serta pelaksanaan pengaturan dan standardisasi sarana produksi Kosmetik.
d. Evaluasi dan penyusunan laporan standardisasi sarana produksi Obat Tradisional, Kosmetik dan Produk Komplemen.
3. Struktur Subdirektorat Standardisasi Sarana Produksi
Sub Direktorat Standardisasi Sarana Produksi terdiri dari:
a. Seksi Standardisasi Sarana Produksi Obat Tradisional dan Suplemen Makanan, mempunyai tugas menyiapkan bahan perumusan kebijakan teknis, penyusunan rencana dan program, penyusunan pedoman, standar, kriteria dan prosedur, evaluasi dan penyusunan laporan serta melakukan pengaturan dan standardisasi sarana produksi Obat Tradisional dan Suplemen Makanan.
b. Seksi Standardisasi Sarana Produksi Kosmetik mempunyai tugas menyiapkan bahan perumusan kebijakan teknis, penyusunan rencana dan program, penyusunan pedoman, standar, kriteria dan prosedur, evaluasi dan penyusunan laporan serta melakukan pengaturan dan standardisasi sarana produksi Kosmetik.
Badan Pengawas Obat dan Makanan (Badan POM) adalah sebuah lembaga di Indonesia yang bertugas mengawasi peredaran obat dan makanan di Indonesia. Badan POM memiliki beberapa fungsi yakni mengkaji dan menyusun kebijakan nasional di bidang Pengawasan Obat dan Makanan, melaksanaan kebijakan tertentu di bidang Pengawasan Obat dan Makanan, melakukan koordinasi kegiatan fungsional dalam pelaksanaan tugas Badan POM, memantau, memberi bimbingan dan pembinaan terhadap kegiatan instansi pemerintah di bidang Pengawasan Obat dan Makanan dan menyelenggarakan pembinaan dan pelayanan administrasi umum di bidang perencanaan umum, ketatausahaan, organisasi dan tata laksana, kepegawaian, keuangan, kearsipan, persandian, perlengkapan dan rumah tangga (Keppres RI No. 103, 2001).
Badan POM dalam menjalankan fungsi melakukan pengkajian dan penyusunan kebijakan nasional di bidang pengawasan obat dan makanan umumnya berdasarkan latar belakang kebutuhan masyarakat, perkembangangan ilmu pengetahuan dan teknologi (IPTEK) serta kondisi regional/global. Misalnya laporan-laporan pengaduan adanya efek berbahaya dari konsumsi sebuah produk di masyarakat tidak jarang menjadi salah satu yang berperan disusunnya peraturan, pedoman atau standar. Laporan-laporan tersebut selanjutnya dikaji berdasarkan perkembangan IPTEK terkini. Selain itu, sebagai anggota masyarakat regional/global, dalam beberapa hal Indonesia juga perlu menyusun peraturan, pedoman dan standar menyesuaikan kondisi regional/global.
Salah satu unit yang bertanggungjawab dalam pengkajian dan penyusunan kebijakan nasional di bidang pengawasan obat dan makanan adalah Direktorat Standardisasi Obat Tradisional, Kosmetik, dan Produk Komplemen. Direktorat ini berada di bawah Deputi II Bidang Pengawasan Obat Tradisional, Kosmetik dan Produk Komplemen yang membawahi Sub Direktorat Standardisasi Produk I, Sub Direktorat Standarisasi Produk II dan Standardisasi Sarana Produksi. Sub Direktorat Standardisasi Produk I bertanggungjawab melakukan penyusunan
peraturan, pedoman dan standar untuk produk obat tradisional dan suplemen makanan, sedangkan Sub Direktorat Standardisasi Produk II melakukan penyusunan peraturan, pedoman dan standar untuk produk kosmetika. Sementara itu, Sub Direktorat Standardisasi Sarana Produksi melakukan penyusunan peraturan, pedoman dan standar untuk sarana produksi obat tradisional, kosmetika dan produk komplemen.
Dalam menyusun peraturan, pedoman dan standar terkait Obat Tradisional, Kosmetik dan Suplemen Makanan, Direktorat Standardisasi Obat Tradisional, Kosmetik, dan Produk Komplemen memiliki dan menerapkan Standar Operasional Procedure (SOP) yang telah ditetapkan. Inisiatif penyusunan peraturan Kepala Badan POM dapat berasal dari Kepala Badan POM atau Unit Kerja. Dalam hal inisiatif berasal dari Kepala Badan POM, Sestama/Deputi ditugaskan oleh Kepala Badan POM untuk meneruskan perintah kepada Direktorat Standadrisasi Obat Tradisional, Kosmetik dan Produk Kompleman melakukan pembahasan dan penyusunan peraturan. Sedangkan jika inisiatif berasal dari Unit Kerja, usulan dilaporkan kepada Kepala badan POM melalui Deputi/Sestama. Bila usulan disetujui, Sestama/Deputi menugaskan Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Kompleman melakukan pembahasan dan penyusunan peraturan. Pembahasan dilakukan secara internal maupun eksternal melibatkan lintas unit dan/atau stakeholder terkait jika diperlukan. Hasil pembahasan dilaporkan kepada Sestama/Deputi. Bila diperlukan, Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen melakukan sounding kepada stakeholder. Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen melalui Biro Hukum dan Humas melakukan notifikasi ke WTO jika diperlukan. Pembahasan akhir peraturan dilakukan Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen bersama dengan Biro Hukum. Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen meminta persetujuan dari unit kerja di lingkungan Kedeputian terkait dan menyerahkan hasil persetujuan Peraturan Kepala Badan POM kepada Biro Hukum dan Humas yang selanjutnya diteruskan kepada Deputi/Sestama dan Kepala Badan POM. Jika disetujui, Kepala Badan POM menandatangani peraturan Kepala Badan POM. Namun jika tidak
disetujui, proses akan kembali ke posisi awal. Biro Hukum dan Humas melakukan penyelesaian akhir Peraturan Kepala Badan POM dan mengajukan pengundangan kepada Kementerian Hukum dan HAM untuk mendapatkan nomor Berita Negara RI. Biro Hukum dan Humas menyerahkan Peraturan Kepala Badan POM yang asli kepada Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen. Setelah Penyusunan Peraturan Kepala Badan POM selesai, Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen dengan Biro Hukum dan Humas melakukan sosialisasi kepada seluruh stakeholder terkait. Biro Hukum dan Humas menginformasikan kepada Pusat Informasi Obat dan Makanan (PIOM) untuk mengunggah Peraturan Kepala Badan POM dalam website Badan POM. Selanjutnya Peraturan Kepala Badan POM didokumentasikan oleh Biro Hukum dan Humas oleh Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen. Tahapan Penyusunan Peraturan Kepala Badan dapat dilihat pada lampiran 4.
Selain menyusun Peraturan Kepala Badan POM, Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen juga memiliki tugas menyusun Pedoman dan Standar. Inisiatif penyusunan Pedoman dan Rancangan Standar dapat berasal dari Deputi/ Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen/Unit kerja. Inisiatif dapat berasal dari Deputi/Unit Kerja. Semua usulan disampaikan kepada Deputi. Selanjutnya Deputi menugaskan kepada Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen untuk melakukan analisis dan menyusun materi untuk Pedoman dan Rancangan Standar. Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen melakukan pembahasan secara internal maupun eksternal melibatkan lintas unit dan/atau stakeholder terkait jika diperlukan. Hasil pembahasan dilaporkan kepada Deputi/Sestama. Jika disetujui oleh Deputi, dan jika diperlukan Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen melakukan sounding dengan stakeholder terkait. Pemberlakuan Pedoman dan Rancangan Standar agar memiliki kekuatan hukum mengikuti tata cara penyusunan peraturan. Selanjutnya Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen
mendokumentasikan Pedoman dan Rancangan Standar. Tahapan Penyusunan Pedoman dan Rancangan Standar dapat dilihat pada lampiran 5.
Badan POM sebagai Lembaga Pemerintah Non Kementerian yang mempunyai wewenang dalam melakukan pengawasan terhadap obat dan makanan, termasuk produk Obat Tradisional, Kosmetik dan Produk Komplemen, harus dapat menyesuaikan dengan Ilmu Pengetahuan dan Teknologi yang berkembang saat ini. Oleh sebab itu, diperlukan sumber daya manusia yang memiliki intelektualitas tinggi serta didukung oleh infrastruktur yang memadai dalam memperoleh informasi perkembangan Ilmu Pengetahuan yang berkaitan dengan perubahan peraturan.
Salah satu komoditi yang berada dalam pengawasan Badan POM dan perlu mendapat perhatian adalah Obat Tradisional. Pengembangan obat tradisional saat ini sangat meningkat dikarenakan masyarakat Indonesia mulai mengenal lebih jauh tanaman - tanaman untuk obat. Akhir-akhir ini, tampak adanya trend hidup sehat pada masyarakat untuk menggunakan produk yang berasal dari alam. Oleh karena itu, obat-obatan tradisional perlu didorong untuk menjadi salah satu pilihan pengobatan.
Obat tradisonal memang patut mendapatkan perhatian yang lebih besar bukan hanya disebabkan potensi pengembangannya yang terbuka, tetapi juga permintaan pasar akan bahan baku obat-obat tradisional ini terus meningkat untuk kebutuhan domestik maupun internasional. Sehingga perlu diperhatikan peraturan - peraturan dan standardisasi obat tradisional yang ada. Mengingat perkembangan obat tradisional yang pesat tersebut, pemerintah melalui Permenkes RI 006 tahun 2012 telah mengatur tentang Industri dan Usaha Obat Tradisional. Industri Obat Tradisonal dibagi dalam beberapa stratifikasi yaitu Industri Obat Tradisional (IOT) dan Industri Ekstrak Bahan Alam (IEBA). Sedangkan Stratifikasi Usaha Obat Tradisional terdiri dari Usaha Kecil Obat Tradisional (UKOT), Usaha Mikro Obat Tradisional (UMOT, Usaha Jamu Rajangan dan Usaha Jamu Gendong.
Berdasarkan PP 51 tahun 2009 tentang Pekerjaan Kefarmasian, Kosmetik termasuk ke dalam sediaan farmasi sehingga harus memenuhi persyaratan keamanan, kemanfaatan dan mutu. Untuk menghasilkan produk yang memenuhi persyaratan mutu, produsen kosmetika harus menerapkan Cara Pembuatan
Kosmetik yang Baik (CPKB). CPKB merupakan salah satu faktor penting untuk dapat menghasilkan kosmetika yang memenuhi standar mutu dan keamanan. Mengingat pentingnya penerapan CPKB maka pemerintah secara terus menerus memfasilitasi industri kosmetika agar dapat menerapkan CPKB melalui langkah-langkah dan tahapan yang terprogram.
Dalam upaya mendorong Industri Kosmetika agar dapat menerapkan CPKB, pemerintah melalui Permenkes 1175 tahun 2010 tentang Izin Produksi Kosmetika membuat klasifikasi izin produksi kosmetika menjadi dua yaitu golongan A dan golongan B. Izin produksi golongan A yaitu izin produksi untuk industri kosmetika yang dapat membuat semua bentuk dan jenis sediaan kosmetika dan izin produksi kosmetika golongan B yaitu izin produksi untuk industri kosmetika yang dapat membuat bentuk dan jenis sediaan kosmetika tertentu dengan menggunakan teknologi sederhana. Industri kosmetika yang telah memiliki izin produksi kosmetika golongan A diwajibkan memiliki apoteker sebagai penanggung jawab, memiliki fasilitas produksi sesuai dengan produk yang akan diproduksi, fasilitas laboratorium dan wajib menerapkan CPKB. Sedangkan Industri kosmetika yang memiliki izin produksi industri kosmetika Golongan B dipersyaratkan memiliki sekurang-kurangnya tenaga teknis kefarmasian sebagai penanggung jawab, memiliki fasilitas produksi dengan teknologi sederhana sesuai produk yang akan diproduksi, dan mampu menerapkan higiene sanitasi dan dokumentasi sesuai CPKB.
Penerapan CPKB merupakan persyaratan kelayakan dasar untuk menerapkan sistem jaminan mutu dan keamanan yang diakui dunia internasional. Terlebih lagi untuk mengantisipasi pasar bebas di era globalisasi maka penerapan CPKB merupakan nilai tambah bagi kosmetika Indonesia untuk bersaing dengan produk sejenis dari negara lain baik di pasar dalam negeri maupun internasional. Dalam pembuatan kosmetika, pengawasan yang menyeluruh disertai pemantauan sangat penting untuk menjamin agar konsumen memperoleh produk yang memenuhi persyaratan yang telah ditetapkan.
Selain hal tersebut di atas, dalam bidang kosmetika Indonesia telah berkomitmen untuk ikut serta dalam Harmonisasi ASEAN sejak 1 Januari 2011. Tujuan dari Harmonisasi ASEAN adalah:
Meningkatkan kerjasama antar Negara-negara anggota ASEAN dalam rangka menjamin mutu, keamanan, dan klaim manfaat dari semua kosmetika yang dipasarkan di ASEAN.
Menghapus hambatan perdagangan kosmetika melalui harmonisasi standar dan persyaratan teknis.
Meningkatkan daya saing produk-produk ASEAN.
Meningkatkan perekonomian ASEAN Member States (AMS).
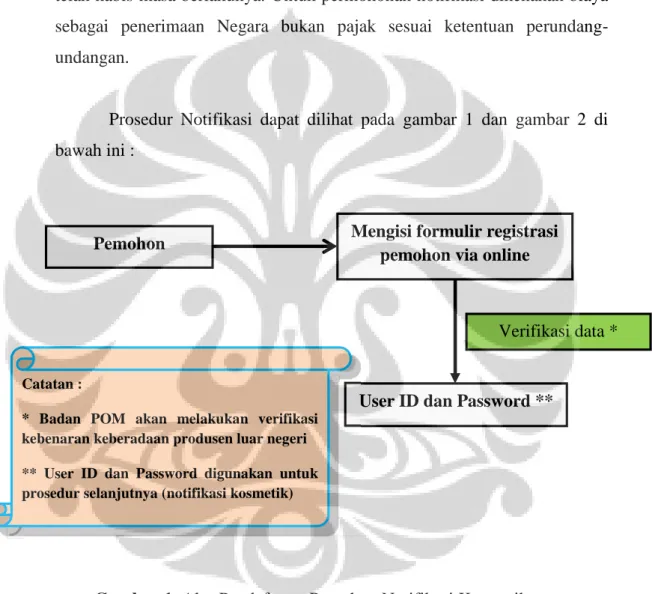
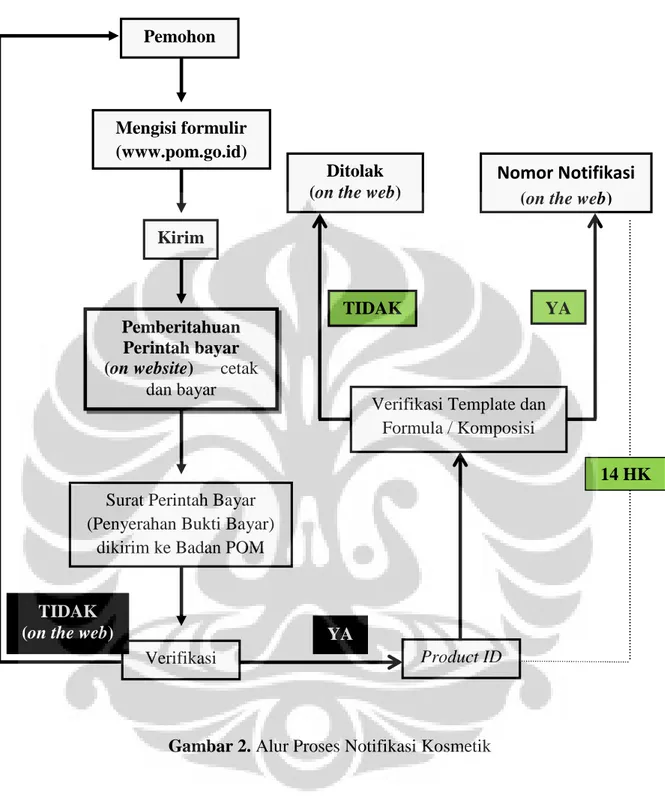
Implementasi dari Harmonisasi ASEAN yaitu penerapan Notifikasi Kosmetika. Persyaratan utama kosmetika yang boleh dinotifikasi adalah memenuhi persyaratan teknis, meliputi aspek keamanan, bahan, penandaan dan klaim sesuai peraturan perundang-undangan, dimana semua hal tersebut terangkum dalam Dokumen Informasi Produk (DIP). Perbedaan yang mendasar antara sistem ini dengan yang sebelumnya berlaku di Indonesia adalah perubahan dari sistem Registrasi (sistem pre market approval) menjadi Notifikasi (sistem pengawasan post market surveillance). Pada sistem Registrasi dilakukan penilaian terhadap keamanan, mutu, dan manfaat serta penandaan produk sebelum beredar melalui evaluasi dokumen yang diserahkan ke Badan POM, sedangkan Notifikasi dilakukan dengan cara pencatatan dan verifikasi terhadap formula dan data kosmetika sebelum produk beredar serta penilaian/evaluasi secara keseluruhan terhadap kosmetika dilakukan setelah produk beredar. Alasan utama diberlakukannya perubahan ini adalah karena kosmetika dinilai beresiko rendah sepanjang semua aturan dipatuhi oleh produsen. Selain itu, pada mekanisme Notifikasi prosesnya lebih cepat dibandingkan dengan Registrasi yaitu 14 hari kerja telah ada pemberitahuan secara elektronik bahwa kosmetika telah ternotifikasi atau ditolak Notifikasinya. Masa berlaku notifikasi selama 3 tahun. Notifikasi dapat dilakukan dimana saja dan kapan saja secara online.
Dengan telah disepakatinya Harmonisasi ASEAN maka pelaku usaha di bidang kosmetik dituntut agar mampu memenuhi standar ASEAN. Untuk itu pemerintah harus berupaya untuk mempersiapkan pelaku usaha di bidang kosmetik, termasuk industri dan UKM agar produk-produk yang dihasilkan sesuai dengan standar dari ASEAN dengan cara melakukan sosialisasi, pelatihan,
asistensi, dan bimbingan teknis baik dalam hal Notifikasi, CPKB maupun DIP. Selain itu pemerintah juga harus mempersiapkan diri dengan melakukan pelatihan terhadap petugas dari instansi terkait yang akan melakukan pengawasan dan sosialisasi kepada masyarakat mengenai penerapan Notifikasi Kosmetik.
Dewasa ini berbagai jenis suplemen makanan telah membanjiri pasaran, termasuk pasar Indonesia. Konsumsi suplemen makanan diperlukan untuk meningkankan asupan zat gizi yang tidak/belum tercukupi dengan makanan dan bukan digunakan sebagai obat/makanan. Budaya makanan instan yang sebagian kurang memperhatikan faktor gizi, menyebabkan banyak orang merasa perlu memenuhi kebutuhan gizi dengan cara mengkonsumsi suplemen makanan. Dari tahun ke tahun terus terjadi peningkatan permintaan akan kebutuhan tahun mendorong para produsen suplemen makanan berlomba-lomba memproduksi suplemen makanan. Produksi suplemen makanan yang dilakukan secara masal dan untuk kepentingan diperdagangkan memiliki dampak positif maupun negatif terhadap masyarakat. Sebagai salah satu bentuk pengawasan produk suplemen makanan, Badan POM telah mengeluarkan Peraturan Kepala Badan POM Nomor HK.00.05.41.1381 tahun 2005 Tentang Tata Laksana Pendaftaran Suplemen Makanan.
36 Universitas Indonesia
5.1 KESIMPULAN
Selama melaksanakan Praktek Kerja Profesi Apoteker (PKPA) di Badan POM, terutama Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen Badan Pengawas Obat dan Makanan Republik Indonesia (BPOM RI) dapat disimpulkan sebagai berikut:
1. Badan Pengawas Obat dan Makanan (Badan POM) adalah sebuah Lembaga Non Kementerian di Indonesia yang bertugas mengawasi peredaran obat-obatan dan makanan di Indonesia.
2. Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen mempunyai tugas menyiapkan perumusan kebijakan, penyusunan pedomanan, standar, kriteria prosedur, serta pelaksanaan pengendalian, bimbingan teknis, dan melakukan evaluasi di bidang pengendalian dan Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen.
3. Di bidang obat tradisional, Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen ikut serta berpartisipasi dengan membantu pemerintah dalam merancang peraturan, pedoman dan standar yang berkaitan dengan obat tradisional
4. Di bidang kosmetik, Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen ikut serta berpartisipasi dalam mensukseskan program Harmonisasi ASEAN antara lain dengan merancang peraturan, pedoman dan standar yang berkaitan dengan notifikasi kosmetik.
5. Di bidang suplemen makanan, Direktorat Standardisasi Obat Tradisional, Kosmetik dan Produk Komplemen ikut serta berpartisipasi