BAB II
TINJAUAN PUSTAKA
2.1 Tepung Terigu
Tepung terigu adalah tepung atau bubuk halus yang berasal dari bulir
gandum, dan digunakan sebagai bahan dasar pembuat kue kering, biskuit, mi,
cake, roti, dan lain-lain. Kata terigu dalam bahasa Indonesia diserap dari bahasa
Portugis, trigo, yang berarti “gandum”. Tepung terigu mengandung banyak zat
pati yaitu karbohidrat kompleks yang tidak larut dalam air. Tepung terigu juga
mengandung protein dalam bentuk gluten, yang berperan dalam menentukan
kekenyalan makanan yang terbuat dari bahan terigu (Salam, dkk., 2012).
2.2 Syarat Mutu Tepung Terigu
Yang digunakan sebagai pedoman dalam penentuan mutu tepung terigu
adalah Standar Nasional Indonesia (SNI) 01-3751-2009 tentang syarat mutu
tepung terigu sebagai bahan makanan (Tabel 1).
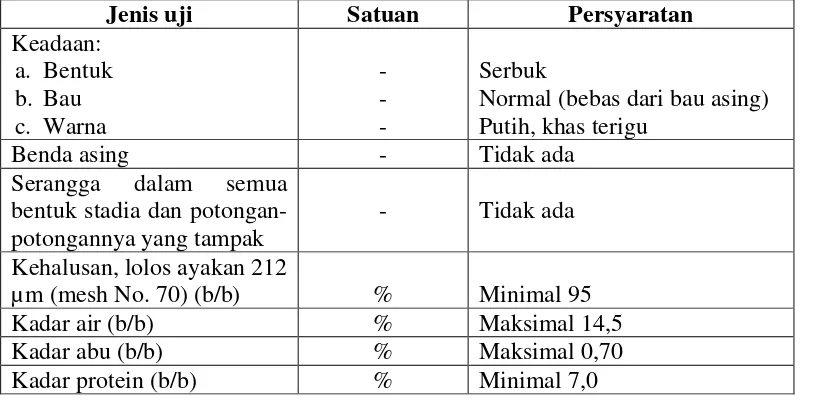
Table 1. Syarat mutu tepung terigu sebagai bahan makanan
Jenis uji Satuan Persyaratan
Keadaan:
Normal (bebas dari bau asing) Putih, khas terigu
Kehalusan, lolos ayakan 212
µm (mesh No. 70) (b/b) % Minimal 95
Kadar air (b/b) % Maksimal 14,5
Keasaman mg KOH/100g Maksimal 50
Falling number (atas dasar kadar air 14%)
detik Minimal 300
Besi (Fe) mg/kg Minimal 50
Seng (Zn) mg/kg Minimal 30
Vitamin B1 (tiamin) mg/kg Minimal 2,5 Vitamin B2 (riboflavin) mg/kg Minimal 4
Asam folat mg/kg Minimal 2
Cemaran arsen mg/kg Maksimal 0,50
Cemaran mikroba: a. Angka lempeng total b. Escherichia coli
2.3 Pengukuran Pertumbuhan Mikroorganisme
Pengukuran mikroorganisme dapat dilakukan dengan dua cara, yaitu
secara langsung dan tidak langsung. Pengukuran mikroorganisme secara langsung
dapat dilakukan dengan beberapa cara, yaitu:
a. Pengukuran Menggunakan Bilik Hitung (Counting Chamber)
Pada pengukuran ini, untuk bakteri digunakan bilik hitung
Petroff-Hausser, sedangkan untuk mikroorganisme eukariot digunakan hemositometer.
Keuntungan menggunakan metode ini adalah mudah, murah, dan cepat, serta bisa
diperoleh informasi tentang ukuran dan morfologi mikroorganisme. Kerugiannya
adalah populasi mikroorganisme yang digunakan harus banyak (minimum
berkisar 106 CFU/ml), karena pengukuran dengan volume dalam jumlah sedikit
tidak dapat membedakan antara sel hidup dan sel mati, serta kesulitan menghitung
b. Pengukuran Menggunakan Electronic Counter
Pada pengukuran ini, suspensi mikroorganisme dialirkan melalui lubang
kecil (orifice) dengan bantuan aliran listrik. Elektroda yang ditempatkan pada dua
sisi orifice mengukur tahanan listrik (ditandai dengan naiknya tahanan) pada saat
bakteri melalui orifice. Pada saat inilah sel terhitung. Keuntungan metode ini
adalah hasil bisa diperoleh dengan lebih cepat dan lebih akurat, serta dapat
menghitung sel dengan ukuran besar. Kerugiannya adalah metode ini tidak bisa
digunakan untuk menghitung bakteri karena adanya gangguan debris, filamen, dan
sebagainya, serta tidak dapat membedakan antara sel hidup dan mati (Pratiwi,
2008).
c. Pengukuran dengan Planting Technique
Metode ini merupakan metode penghitungan jumlah sel tampak (visible)
dan didasarkan pada asumsi bahwa bakteri hidup akan tumbuh, membelah, dan
memproduksi satu koloni tunggal. Satuan penghitungan yang dipakai adalah CFU
(colony forming unit) dengan cara membuat seri pengenceran sampel dan
menumbuhkan sampel pada media padat. Pengukuran dilakukan pada plate
dengan jumlah koloni berkisar 25-250 atau 30-300 (Pratiwi, 2008).
Keuntungan metode ini adalah sederhana, mudah, dan sensitif karena
menggunakan colony counter sebagai alat hitung dan dapat digunakan untuk
menghitung mikroorganisme pada sampel makanan, air, ataupun tanah.
Kerugiannya adalah kurang akurat karena satu koloni tidak selalu berasal dari satu
Uji Angka Lempeng Total (ALT) dilakukan untuk menentukan jumlah
atau angka bakteri mesofil aerob yang mungkin mencemari suatu produk, baik itu
makanan-minuman, obat tradisional ataupun kosmetika (Kusuma, 2009).
Pada prinsipnya angka lempeng total (ALT) yaitu pertumbuhan bakteri
mesofil aerob setelah sampel diinkubasikan dalam perbenihan yang cocok selama
24-48 jam pada suhu 35 ± 1ºC (SNI, 1992).
Cara inokulasi yang dipilih adalah cara tuang, dimana hal ini dimaksudkan
untuk melihat pertumbuhan bakteri mesofil aerob, yang membutuhkan oksigen
dalam pertumbuhannya, sehingga akan teramati bahwa pertumbuhan bakteri
mesofil aerob tersebut akan berada dipermukaan lempeng agar, karena
pertumbuhannya yang mencari oksigen. Oleh karena itu, pada pengamatan angka
lempeng total ini, dicari hanya koloni bakteri yang tumbuh di permukaan lempeng
agar. Masa inkubasi dilakukan dengan membalik cawan petri yang berisi biakan.
Hal ini dimaksudkan untuk menghindari jatuhnya butir air hasil pengembunan
disebabkan suhu inkubator. Apabila sampai terdapat air yang jatuh maka akan
merusak pembacaan angka lempeng total dari sampel yang diuji (Kusuma, 2009).
d. Pengukuran dengan Menggunakan Teknik Filtrasi Membran
Pada metode ini sampel dialirkan pada suatu sistem filter membran dengan
bantuan vacuum. Bakteri yang terperangkap selanjutnya ditumbuhkan pada media
yang sesuai dan jumlah koloni dihitung. Keuntungan metode ini adalah dapat
menghitung sel hidup dan system penghitungannya langsung, sedangkan
Metode pengukuran pertumbuhan mikroorganisme secara tidak langsung
dapat dilakukan dengan sebagai berikut:
a. Pengukuran Kekeruhan/Turbidity
Bakteri yang bermultiplikasi pada media cair akan menyebabkan media
menjadi keruh. Alat yang digunakan untuk pengukuran adalah spektrofotometer
atau kolorimeter dengan cara membandingkan densitas optik (optical density, OD)
antara media tanpa pertumbuhan bakteri dan media dengan pertumbuhan bakteri
(Pratiwi, 2008).
b. Pengukuran Aktivitas Metabolik
Metode ini didasarkan pada asumsi bahwa jumlah produk metabolik
tertentu, misalnya asam atau CO2, menunjukkan jumlah mikroorganisme yang
terdapat di dalam media. Misalnya pengukuran produksi asam untuk menentukan
jumlah vitamin yang dihasilkan mikroorganisme (Pratiwi, 2008).
c. Pengukuran Berat Sel Kering (BSK)
Metode ini umum digunakan untuk mengukur pertumbuhan fungi
berfilamen. Miselium fungi dipisahkan dari media dan dihitung sebagai berat
kotor. Miselium selanjutnya dicuci dan dikeringkan dengan alat pengering
(desikator) dan ditimbang beberapa kali hingga mencapai berat konstan yang
dihitung sebagai berat sel kering (BSK) (Pratiwi, 2008).
2.4 Pengaruh Faktor Lingkungan pada Pertumbuhan
Faktor-faktor yang mempengaruhi pertumbuhan mikroorganisme dapat
pH, tekanan osmotik, dan cahaya atau radiasi. Faktor kimia meliputi karbon,
oksigen, trace elements, dan faktor-faktor pertumbuhan organik, termasuk nutrisi
yang terdapat dalam media pertumbuhan (Pratiwi, 2008).
2.4.1 Pengaruh Faktor Fisik pada Pertumbuhan a. Temperatur
Temperatur menentukan aktivitas enzim yang terlibat dalam aktivitas
kimia. Peningkatan temperatur sebesar 10ºC dapat meningkatkan aktivitas enzim
sebesar dua kali lipat. Pada temperatur yang sangat tinggi akan terjadi denaturasi
protein yang tidak dapat balik (irreversible), sedangkan pada temperatur yang
sangat rendah aktivitas enzim akan berhenti. Pada temperatur optimal akan terjadi
kecepatan pertumbuhan optimal dan dihasilkan jumlah sel yang maksimal
(Pratiwi, 2008) (Tabel 2).
Tabel 2. Pembagian mikroorganisme berdasarkan kisaran temperatur tubuh Psikrofil Psikrofil Fakultatif
/ Psikotrof
Mesofil Termofil 1. Tumbuh pada
pH merupakan indikasi konsentrasi ion hidrogen. Peningkatan dan
dalam protein, amino, dan karboksilat. Hal ini dapat menyebabkan denaturasi
protein yang mengganggu pertumbuhan sel (Pratiwi, 2008).
c. Tekanan Osmosis
Osmosis merupakan perpindahan air melewati membran semipermeabel
karena ketidakseimbangan material terlarut dalam media. Dalam larutan hipotonik
air akan masuk ke dalam sel mikroorganisme, sedangkan dalam larutan hipertonik
air akan keluar dari dalam sel mikroorganisme sehingga membran plasma
mengkerut dan lepas dari dinding sel (plasmolisis), serta menyebabkan sel secara
metabolik tidakaktif. Mikroorganisme halofil mampu tumbuh pada lingkungan
hipertonik dengan kadar garam tinggi, umumnya NaCl 3%, contohnya adalah
bakteri laut. Mikroorganisme yang mampu tumbuh pada konsentrasi garam sangat
tinggi sebesar ≥ 33% NaCl disebut halofil ekstrem, contohnya adalah
Halobacterium halobium(Pratiwi, 2008).
d. Oksigen
Berdasarkan kebutuhan oksigen, dikenal mikroorganisme yang bersifat
aerob dan anaerob. Mikroorganisme aerob memerlukan oksigen untuk bernapas,
sedangkan mikroorganisme anaerob tidak memerlukan oksigen untuk bernapas.
Adanya oksigen pada mikroorganisme anaerob justru akan menghambat
pertumbuhannya. Energi pada mikroorganisme anaerob dihasilkan dengan cara
fermentasi (Pratiwi, 2008).
Bakteri aerob adalah bakteri yang membutuhkan oksigen bebas untuk
menumbuhkannya tidaklah jadi masalah, selama bakteri itu berhubungan dengan
udara (Volk dan Margaret, 1988).
e. Radiasi
Sumber utama radiasi di bumi adalah sinar matahari yang mencakup
cahaya tampak (visible light), radiasi UV (ultraviolet), sinar inframerah, dan
gelombang radio. Radiasi yang berbahaya untuk mikroorganisme adalah radiasi
pengionisasi (ionizing radiation), yaitu radiasi dari panjang gelombang yang
sangat pendek dan berenergi tinggi yang dapat menyebabkan atom kehilangan
elektron (ionisasi) (Pratiwi, 2008).
2.4.2 Pengaruh Faktor Kimia pada Pertumbuhan a. Nutrisi
Nutrisi merupakan substansi yang diperlukan untuk biosintesis dan
pembentukan energi. Berdasarkan kebutuhannya, nutrisi dibedakan menjadi dua
yaitu:
1. Makroelemen yaitu elemen-elemen nutrisi yang diperlukan dalam jumlah
banyak (gram). Meliputi karbon (C), oksigen (O), hidrogen (H), nitrogen
(N), sulfur (S), fosfor (P), kalium (K), magnesium (Mg), kalsium (Ca), dan
besi (Fe). CHONSP diperlukan dalam jumlah besar (takaran gram) untuk
pembentukan karbohidrat, lemak, protein, dan asam nukleat. P, K, Ca, dan
Mg diperlukan dalam jumlah yang lebih kecil (mg) dan berperan sebagai
kation dalam sel (Pratiwi, 2008).
2. Mikroelemen (trace element) yaitu elemen-elemen nutrisi yang diperlukan
(Mn), zinc (Zn), kobalt (Co), molybdenum (Mo), nikel (Ni), dan tembaga
(Cu). Mikroelemen kadang merupakan bagian enzim atau kofaktor yang
membantu katalisasi dan membentuk protein (Pratiwi, 2008).
b. Media Kultur
Pada pengujian mikrobiologi, bakteri dibiakkan dalam bahan berisi nutrisi
yang disebut media. Media dapat berupa cairan seperti kaldu dan dapat pula
berupa padatan seperti agar dan gelatin. Media pengkaya adalah media yang dapat
menunjang pertumbuhan bakteri yang memiliki persyaratan nutrisi yang rumit
agar dapat tumbuh dengan optimal (Kusuma, 2009).
Media padat yang paling banyak digunakan adalah agar-agar, karena bila
agar-agar sudah menjadi padat masih dapat dicairkan kembali untuk digunakan.
Selain itu, suspensi agar-agar 1,5% - 2% dalam air karena dapat larut pada suhu
100ºC dan tidak menjadi padat sebelum suhu turun di bawah 45ºC kemudian
media agar didinginkan dengan cepat sehingga menjadi padat tanpa merusak
sel-sel tersebut. Sekali menjadi padat, agar tidak dapat mencair kembali, kecuali jika
dipanaskan di atas 80ºC. Pada metode lempeng tuangan, suatu suspensi sel
dicampur dengan agar-agar cair pada suhu 50ºC dituang pada cawan petri. Bila
agar-agar telah mengeras, sel tidak akan bergerak lagi dan tumbuh menjadi koloni
sangat besar kemungkinannya berasal dari satu sel yang sama (Kusuma, 2009).
Media yang digunakan dalam pengujian, yaitu: 1. Pengencer Buffered Peptone Water (BPW)
Peptone 10 gram
Disodium hydrogen phosphate 3,5 gram
Kalium dihidrogen phosphate 1,5 gram
Air suling (akuades) 1 liter
Larutkan bahan-bahan dalam 1 liter air suling, atur pH 7,0, masukkan 250
ml ke dalam botol (labu) 500 ml dan 9 ml ke dalam tabung reaksi. Sterilkan pada
suhu 121ºC selama 15 menit (SNI, 1992).
2. Perbenihan (media) Plate Count Agar
Yeast extract 2,5 gram
Pancreatic digest of Caseine 5 gram
Glucose 1 gram
Agar 15-20 gram
Air suling 1 liter
Larutkan semua bahan-bahan, atur pH 7,0. Masukkan ke dalam labu,
sterilkan pada suhu 121ºC selama 15 menit (SNI, 1992).
3. Pereaksi Triphenyl Tetrazolium Chloride (TTC) 0,5%
TTC ini berfungsi sebagai indikator yang akan direduksi sehingga
mewarnai koloni bakteri yang hendak diamati, dengan demikian dapat dibedakan
dengan kotoran yang mungkin berasal dari sisa-sisa sampel yang dapat
mengganggu pengamatan koloni bakteri. TTC yang ditambahkan adalah 1 ml
dalam 100 ml media PCA. TTC akan direduksi dengan cepat menjadi formazan
yang berwarna merah dan tidak larut. Dalam pengujian untuk angka lempeng total
sering digunakan untuk indikator koloni karena kebanyakan bakteri mesofil aerob
keruh karena terdapat matriks sampel yang kompleks, koloni dapat terlihat jelas
(Kusuma, 2009).
2.5 Sterilisasi
Sterilisasi dalam mikrobiologi merupakan proses penghilangan semua
jenis organisme hidup, dalam hal ini adalah mikroorganisme (protozoa, fungi,
bakteri, mycoplasma, virus) yang terdapat pada suatu benda atau bahan (Pratiwi,
2008).
2.5.1 Sterilisasi Uap
Proses sterilisasi termal menggunakan uap jenuh di bawah tekanan
berlangsung di suatu bejana yang disebut autoklaf, dan mungkin merupakan
proses sterilisasi yang paling banyak digunakan (suatu siklus autoklaf yang
ditetapkan dalam farmakope untuk media atau pereaksi adalah selama 15 menit
pada suhu 121ºC kecuali dinyatakan lain). Prinsip dasar kerja alat adalah udara di
dalam bejana sterilisasi diganti dengan uap jenuh, dan hal ini dicapai dengan
menggunakan alat pembuka atau penutup khusus (Ditjen POM, 1995).
2.5.2 Sterilisasi Panas Kering
Proses sterilisasi termal untuk bahan yang tertera di Farmakope dengan
menggunakan panas kering biasanya dilakukan dengan suatu proses bets di dalam
suatu oven yang didesain khusus untuk tujuan itu. Oven modern dilengkapi
dengan udara yang dipanaskan dan disaring, didistribusikan secara merata ke
seluruh bejana dengan cara sirkulasi atau radiasi menggunakan sistem semprotan
sterilisasi panas uap. Unit yang digunakan untuk sterilisasi komponen seperti
wadah untuk larutan intravena, harus dijaga agar dapat dihindari akumulasi
partikel di dalam bejana sterilisasi. Rentang suhu khas yang dapat diterima di
dalam bejana sterilisasi kosong adalah lebih kurang 15 menit, jika alat sterilisasi
beroperasi pada suhu tidak kurang dari 250ºC (Ditjen POM, 1995).
Sebagai penambahan pada proses bets tersebut di atas, suatu proses
berkesinambungan digunakan untuk sterilisasi dan depirogenisasi alat kaca
sebagai suatu bagian sistem pengisian dan penutupan kedap secara aseptik yang
berkesinambungan terpadu (Ditjen POM, 1995).
2.5.3 Sterilisasi Gas
Pilihan untuk menggunakan sterilisasi gas sebagai alternatif dari sterilisasi
termal sering dilakukan jika bahan yang akan disterilkan tidak tahan terhadap
suhu tinggi pada proses sterilisasi uap atau panas kering. Bahan aktif yang
umumnya digunakan pada sterilisasi gas adalah etilen oksida dengan kualitas
mensterilkan yang dapat diterima. Keburukan dari bahan aktif ini antara lain
sifatnya yang sangat mudah terbakar, walaupun sudah dicampur dengan gas inert
yang sesuai, bersifat mutagenik, dan kemungkinan adanya residu toksik di dalam
bahan yang disterilkan, terutama yang mengandung ion klorida. Proses sterilisasi
pada umunya berlangsung di dalam bejana bertekanan yang didesain sama seperti
pada autoklaf, tetapi dengan tambahan bagian khusus yang hanya terdapat pada
alat sterilisasi yang menggunakan gas. Fasilitas yang menggunakan bahan
sterilisasi seperti ini harus didesain sedemikian rupa hingga mampu mengeluarkan
hidup, dan mengurangi paparan gas yang sangat berbahaya terhadap petugas yang
menangani alat tersebut (Ditjen POM, 1995).
2.5.4 Sterilisasi dengan Radiasi Ion
Perkembangan yang cepat alat kesehatan yang tidak tahan terhadap
sterilisasi panas dan kekhawatiran tentang keamanan etilen oksida mengakibatkan
peningkatan penggunaan sterilisasi radiasi. Tetapi cara ini juga dapat digunakan
pada bahan obat dan bentuk sediaan akhir. Keunggulan sterilisasi iradiasi meliputi
reaktivitas kimia rendah, residu rendah yang dapat diukur, dan kenyataan yang
membuktikan bahwa variabel yang dikendalikan lebih sedikit. Kenyataannya
sterilisasi radiasi adalah sesuatu kekhususan dalam dasar pengendalian yang
penting adalah dosis radiasi yang diserap, dan dapat diukur secara tepat. Oleh
karena sifat khas tersebut, banyak prosedur baru yang telah dikembangkan untuk
menetapkan dosis sterilisasi. Walaupun begitu, hal ini masih dalam peninjauan
dan pertimbangan, terutama mengenai kegunaannya, paling tidak, untuk
pengendalian tambahan dan tindakan keamanan. Iradiasi hanya menimbulkan
sedikit kenaikan suhu, tetapi dapat mempengaruhi kualitas dan jenis plastik atau
kaca tertentu (Ditjen POM, 1995).
Ada dua jenis radiasi ion yang digunakan, yaitu disintegrasi radioaktif dari
radioisotop (radiasi gamma) dan radiasi berkas elektron. Pada kedua jenis
tersebut, dosis radiasi yang dapat menghasilkan derajat jaminan sterilitas yang
diperlukan harus ditetapkan sedemikian rupa hingga dalam rentang satuan dosis
minimum dan maksimum, sifat bahan yang disterilkan dpat diterima (Ditjen
2.5.5 Sterilisasi dengan Penyaringan
Sterilisasi larutan yang labil terhadap panas sering dilakukan dengan
penyaringan menggunakan bahan yang dapat menahan mikroba, hingga mikroba
yang dikandung dapat dipisahkan secara fisika. Perangkat penyaring umumnya
terdiri dari suatu matriks berpori bertutup kedap atau dirangkaikan pada wadah
yang tidak permeabel. Efektivitas suatu penyaring media atau penyaring substrat
tergantung pada ukuran pori bahan dan dapat tergantung pada daya adsorpsi
bakteri pada atau di dalam matriks penyaring atau tergantung pada mekanisme
pengayakan. Ada beberapa bukti yang menyatakan bahwa pengayakan merupakan
komponen yang lebih penting dari mekanisme. Penyaring yang melepas serat,
terutama yang mengandung asbes, harus dihindarkan penggunaanya kecuali tidak
ada cara penyaringan alternatif lain yang mungkin digunakan. Jika penyaring yang
melepas serat memang diperlukan, merupakan keharusan, bahwa proses
penyaringan meliputi adanya penyaring yang tidak melepas serat diletakkan pada