TEKNIK EKSTRAKSI DENGAN MEKANISME PEMBENTUKAN KOMPLEKS PADA PENETAPAN NIKEL DALAM SAMPEL
I. TUJUAN
Dapat Memisahkan Nikel dalam sampel dengan mekanisme ekstraksi pembentukan senyawa kompleks nikel dimetilglioksima
Dapat menetapkan nikel secara spektrofotometri visible
II. PRINSIP
Nikel dalam larutan membentuk senyawa kompleks dimetilglioksim merah dalam suasana yang sedikit basa. Ekstraksi kompleks nikel ini optimum pada pH 7-12 dengan adanya sitrat. Kompleks ini dapat diukur absorbansinya pada panjang gelombang 465 nm.
III. REAKSI
merah pada Ni kons tinggi
+2H+
IV. DASAR TEORI
bercampur. Menurut Nernst, zat terlarut akan terdistribusi pada kedua solven sehingga perbandingan konsentrasi pada kedua solven tersebut tetap untuk tekanan dan suhu yang tetap (Christian, 1986).
Ekstraksi pelarut terutama digunakan, bila pemisahan campuran dengan cara destilasi tidak mungkin dilakukan (misalnya karena pembentukan azeotrop atau karena kepekaannya terhadap panas) atau tidak ekonomis. Seperti ekstraksi padat-cair, ekstraksi cair-cair selalu terdiri atas sedikitnya dua tahap, yaltu pencampuran secara intensif bahan ekstraksi dengan pelarut, dan pemisahan kedua fasa cair itu sesempurna mungkin.
Ekstraksi cair-cair dengan pengkelat logam adalah salah satu aplikasi utama ekstraksi cair-cair yaitu ekstraksi selektif ion logam menggunakan agen pengkelat. Sayangnya beberapa agen pengkelat memiliki keterbatasan kelarutan dalam air atau subyek untuk hidrolisis atau oksidasi udara dalam larutan (aqueous). Karena alasan ini agen pengkelat ditambahkan ke pelarut organik sebagai ganti fasa aqueous. Agen pengkelat diekstrak ke fasa cairan yang reaksinya membentuk kompleks logam-ligan yang stabil dengan ion logam. Kompleks logam-ligan kemudian terekstrak ke fasa organik. Efisiensi ekstraksi ion logam bergantung pada pH.
Pada umumnya ion-ion logam tidak larut dalam pelarut organik non polar. Ion logam harus diubah menjadi bentuk molekul yang tidak bermuatan dengan pembentukan kompleks agar ion logam tersebut dapat terekstrak ke dalam pelarut organik non polar. Senyawa kompleks adalah suatu senyawa dimana ion logam bersenyawa dengan ion atau molekul netral yang mempunyai sepasang atau lebih elektron bebas yang berikatan secara kovalen koordinasi (Moersid, 1989)
bilangan koordinasi. Pembentukan kompleks oleh ligan bergantung pada kecenderungan untuk mengisi orbital kosong dalam usaha mencapai konfigurasi elektron yang lebih stabil. Untuk memudahkan ekstraksi maka ion logam yang bermuatan harus dinetralkan oleh ion atau molekul netral menjadi kompleks tidak bermuatan (Khopkar, 1984).
Kompleks kelat merupakan asam lemah (HL) yang terionisasi dalam air dan terdistribusi dalam fase organik dan fase air, serta dengan ion logam dapat membentuk ion kompleks yang netral dan mudah larut dalam fase organik (Day dan Underwood, 1989). Sesuai dengan reaksi:
Salah satu keuntungan menggunakan agen pengkelat adalah derajat selektifitas tinggi. Efisiensi ekstraksi untuk kation divalent meningkat dari 0-100% disekitar 2 unit pH. lagipula konstanta pembentukan kompleks logam-ligan bervariasi diantara ion logam. Akibatnya, perbedaan signifikan muncul dalam range pH dimana ion logam yang berbeda menaikkan efisiensi ekstraksi dari 0-100%.
Penentuan kadar nikel dilakukan dengan metode spektrofotometri, dimana diketahui kompleks berwarna Ni(DMG)2 dalam kloroform mengikuti hukum Lambert-Beer dalam range konsentrasi yang lebar. Sebagaimana diketahui warna adalah salah satu kriteria untuk mengidentifikasi suatu objek. Pada analisis spektrokimia spektrum radiasi elektromagnetik digunakan untuk menganalisis spesies kimia dan menelaah interaksinya dengan radiasi elektromagnetik.
Proses absorpsi ini kemudian dapat dijelaskan bahwa suatu molekul/atom yang mengabsorpsi radiasi akan memanfaatkan energi radiasi tersebut untuk mengadakan eksitasi elektron. Eksitasi ini hanya akan terjadi bila energi radiasi yang diperlukan sesuai dengan perbedaan tingkat energi dari keadaan dasar ke keadaan tereksitasi dan sifatnya karakteristik.
Komponen-komponen yang mengabsorpsi dalam spektrofotometri UV-Vis dapat berupa absorpsi oleh senyawa-senyawa organik maupun anorganik. Senyawa-senyawa organik yang mengandung ikatan rangkap 2/ rangkap 3 akan menghasilkan puncak-puncak absorpsi yang penting terutama dalam daerah UV. Gugus-gugus fungsional organik tidak jenuh yang mengabsorpsi sinar tampak dan UV ini dinamakan kromofor/sering dikenal dengan pembawa warna. Contoh kromofor, -NH2, -C=C-, C=O, -CHO, -NO2, -N=N-dan lain-lain. Se-N=N-dangkan absorpsi oleh senyawa-senyawa anorganik, spektra dari hampir semua ion-ion kompleks dan molekul-molekul anorganik menghasilkan puncak absorpsi agak melebar. Untuk ion-ion logam transisi, pelebaran puncak disebabkan oleh faktor-faktor lingkungan kimianya. Suatu contoh larutan Cu (II) encer berwarna biru muda, tetapi warna akan berubah menjadi biru tua dengan adanya amonia. Bila unsur-unsur logam membentuk kompleks, maka faktor ligan sangat menentukan. Sebagian radiasi yang terabsorpsi oleh suatu larutan analit yang mengabsorpsi ternyata terdapat hubungan kuantitatif dengan konsentrasinya. Jumlah radiasi yang terabsorpsi oleh sampel dinyatakan dalam hukum Lambert-Beer dan dijadikan dasar pada analisis kuantitatif spektrofotometri.
V. Alat :
Labu takar 100 mL
Labu takar 1 L
Gelas piala
Pipet mohr
Corong pemisah
Botol semprot
Naraca analitik
Botol vial
Spektrofotometer UV-Visible
VI. Bahan : Larutan sampel
Asam sitrat (p.a)
NH4OH 4N
Kloroform
Air suling
Dimetilglioksima
VII. Cara Kerja: Ekstraksi sampel
absorbansinya pada spektrofotometer UV-Vis dengan panjang gelombang 465 nm
Ekstraksi deret standar
Dibuat deret standar nikel dengan konsentrasi masing-masing 5 ppm, 10 ppm, 15 ppm, 20 ppm, 25 ppm, dan blanko dalam labu takar 100 mL dari larutan baku 100 ppm. Masing-masing standar dipipet sebanyak 10 mL dimasukkan ke dalam piala gelas yang berisi 90 mL air suling dan ditambahkan 5 g asam sitrat (p.a). Kemudian ditambahkan amonia encer 4 N (di ruang asam) sampai pH larutan tersebut 7,5 menggunakan indikator universal dan didinginkan. Larutan dipindahkan ke dalam corong pemisah dan ditambahkan 20 mL larutan dimetilglioksim sampai larutan berwana merah muda, diamlan 1-2 menit, kemudian ditambahkan 12 mL kloroform. Larutan dalam corong pemisah dikocok selama 1 menit, setelah itu didiamkan sampai fase-fase saling memisah. Setelah fase-fase tersebut stabil dan terpisah, dipisahkan lapisan kloroform yang berwarna merah ke dalam botol vial. Diukur absorbansinya pada spektrofotometer UV-Vis dengan panjang gelombang 465 nm.
Pembuatan Dimetilglioksim (volume 250 mL)
0,25 g dimetilglioksim (p.a) ditimbang, kemudian dilarutkan dalam 125 mL amonia dan diencerkan dengan air suling sampai 250 mL.
VIII. Hasil Percobaan Identifikasi Bahan
No Nama Bahan Rumus Molekul Sifat Fisik
1 Asam Sitrat C6H8O7.H2O berbentuk serbuk kristal berwarna
putih pada temperatur kamar
asam organik lemah
Efek akut, menimbulkan iritasi kulit dan mata.
Efek kronik, tidak ada
2 Dimetilglioksim
Serbuk kristal putih
Sukar larut dalam asam,
mengendap dalam larutan basa lemah
3 Amonia NH4OH
larutan tidak berwarna
bau khas amonia dan bersifat basa lemah
4 Kloroform CHCl3
Berbentuk cairan pada suhu ruang
Tidak berwarna
Berbau khas,
berbahaya bagi tubuh,
mengiritasi, karsinogenik
mudah menguap
5 Air suling H2O Cairan tidak berwarna dan tidak berbau
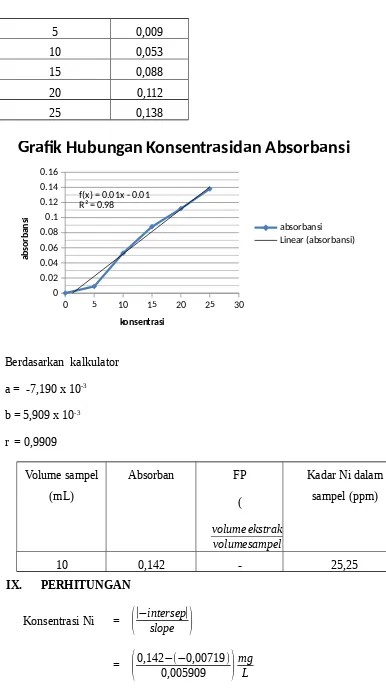
Tabel Data
Standar Ni (mg/L) Absorban
= 25,25 mg
L
X. PEMBAHASAN
Judul Percobaan kali ini adalah “Teknik Ekstraksi dengan Mekanisme Pembentukan Kompleks pada Penetapan Nikel dalam Sampel”, dimana yang dimaksud ekstraksi pelarut itu sendiri adalah suatu metode pemisahan berdasarkan transfer suatu zat terlarut dari suatu pelarut kedalam pelarut lain yang tidak saling bercampur. Tujuan dari percobaan kali ini adalah untuk memisahkan logam Ni dari campurannya dengan eksatraksi pelarut dan juga menentukan kadar Ni dalam sampel dengan metode spektrofotometri.
Suatu senyawa kompleks adalah suatu senyawa yang terdiri dari atom pusat dan sejumlah ligan yang terikat melalui ikatan koordinasi dengan erat dengan atom pusat. Untuk mengetahui apakah telah terjadi pembentukan kompleks, biasanya kedalam suatu senyawa ditambahkan reagen tertentu yang menyebabkan timbulnya warna pada larutan yang dianalisis. Pada penentuan nikel sebagai kompleks nikel - dimetilglioksim dilakukan dengan cara ekstraksi. Ekstraksi dilakukan dengan menggunakan corong pisah.
Ni merupakan ion logam yang tidak dapat larut dalam senyawa nonpolar, oleh karena itu Ni harus diubah menjadi senyawa non polar dengan cara membentuknya menjadi senyawa kelat. Agen pengkelat yang digunakan dalam percobaan ini adalah Dimetilglioksin. Ion logam Ni2+ dijadikan senyawa kompleks terlebih dahulu dengan DMG menjadi senyawa kompleks Ni(DMG)2 agar dapat terekstraksi ke fasa organik yang akhirnya dapat diukur pada panjang gelombang 465 nm.
mengekstrak Ni dalam sampel, kemudian ketika Ni tersebut sudah saling terpisah kita bias mengukur absorbansinya pada fase kloroform pada panjang gelombang 465 nm. Dan Ekstraksi kembali dengan 12 mL kloroform dan ukur absorban ekstrak pada 465 nm.
Pada hasil praktikum di dapat kadar Ni dalam sampel sebesar 25,25 mg
L .
Pada perhitungan juga di perlukan slope pada standar, slope kalkulator pada standar yang kita peroleh adalah 0,005909 dengan nilai intersep sebesar -0,00719 dan nilai r sebesar 0,9909
Pada saat pengukuran dengan menggunakan spektrofotometer kuvet yang digunakan haruslah kuvet kuarsa tidak boleh menggunakan kuvet plastik karena pelarut organik khloroform akan bereaksi dengan silikat pada kuvet plastik yang akan melelehkan kuvet tersebut dan tentunya akan membuat pemeriksaan menjadi terganggu dan menghasilkan absorbansi yang tidak sesuai dari seharusnya. Larutan blanko digunakan untuk mengkalibrasi spektrofotometer yang diseting dengan absorban nol atau nilai transmitan 100% dan meminimalkan kesalahan sistematik.
Faktor-faktor yang menyebabkan absorbansi vs konsentrasi tidak linear:
Adanya serapan oleh pelarut. Hal ini dapat diatasi dengan penggunaan blanko, yaitu larutan yang berisi selain komponen yang akan dianalisis termasuk zat pembentuk warna.
Serapan oleh kuvet. Kuvet yang ada biasanya dari bahan gelas atau kuarsa, namun kuvet dari kuarsa memiliki kualitas yang lebih baik.
Kesalahan fotometrik normal pada pengukuran dengan absorbansi sangat rendah atau sangat tinggi, hal ini dapat diatur dengan pengaturan konsentrasi, sesuai dengan kisaran sensitivitas dari alat yang digunakan (melalui pengenceran atau pemekatan).
XI. KESIMPULAN
ekstrasi Ni dapat dilakukan dengan menambahkan beberapa reagen yaitu asam sitrat, amonia encer, dimetilglioksim, dan kloroform.
Kadar Ni yang diperoleh dalam sampel sebesar 25,25 mg/L
XII. Daftar Pustaka:
Basset,J.Denney,R.C Jefry,G.H Mendhan,J.Buku Ajar Vogel Kimia
Analisis Kuantitatif Anorganik.Jakarta:Buku kedokteran EGC.
Day RA. Jr dan Al Underwood.1992. Analisis Kimia Kuantitatif. Edisi
Kelima. Jakarta : Erlangga
Harvey David. 2000. Modern Analytical Chemistry. New York: McGraw-Hill Comp.
Vogel, 1985, Buku Teks Analisis Anorganik Kualitatif Makro dan Semi
Mikro, Edisi V, diterjemahkan oleh: Setiono & Pudjaatmaka, PT Kalman
Media Pustaka, Jakarta