BIOAKUMULASI LOGAM BERAT KADMIUM (Cd) PADA AKAR KULIT BATANG DAN DAUN Avicennia marina DI KAWASAN MANGROVE
PERCUT SEI TUAN KABUPATEN DELI SERDANG SUMATERA UTARA
Bioaccumulation of Cadmium (Cd) on Avicennia marina roots, Leaf Bark and Leaves at Mangrove Area of Percut Sei Tuan Deli Serdang
District, North Sumatera
Keumala Hafni Munthe1), Yunasfi2), Ani Suryanti2)
1) Mahasiswa Program Studi Manajemen Sumberdaya Perairan, Fakultas Pertanian, Universitas Sumatera Utara, (Email : [email protected]) 2) Staff Pengajar Program Studi Manajemen Sumberdaya Perairan, Fakultas
Pertanian, Universitas Sumatera Utara, Medan, Indonesia, 20155 ABSTRACT
Sungai Percut merupakan sungai yang terdapat di Kabupaten Deli Serdang yang bermuara ke Selat Malaka. Air sungai Percut digunakan untuk, bahan baku air instalasi pengolahan air (WTP Mini) PDAM Tirtanadi, keperluan mandi cuci kakus (MCK) serta sebagai tempat pendaratan kapal nelayan Percut Sei Tuan. Penelitian ini bertujuan untuk mengetahui konsentrasi logam berat kadmium (Cd) pada akar, kulit batang, daun A.marina, mengetahui konsentrasi kadmium pada sedimen dan air, mengetahui hubungan antara konsentrasi logam berat di air dan sedimen. Pengambilan sampel A. marina (akar, kulit batang dan daun) dilakukan pada tiga stasiun dengan tiga kali ulangan. Analisis konsentrasi kadmium menggunakan metode Atomic Absorption Spectrophotometry (AAS). Hasil penelitian menunjukkan bahwa konsentrasi kadmium pada akar, kulit batang, daun A. marina memiliki konsentrasi berurutan sebesar 6,18 mg/kg, 3,92 mg/kg, dan 2,59 mg/kg. Konsentrasi logam berat kadmium di air sebesar 6,35 mg/l dan sedimen 7,54 mg/l. Konsentrasi logam berat Kadmium pada A. marina , air dan sedimen pada Perairan Percut Sei Tuan belum melampaui baku mutu pada tumbuhan, air maupun sedimen
Kata Kunci: Avicennia marina, Logam Berat, Kadmium (Cd), AAS, Percut Sei Tuan
PENDAHULUAN
Sungai Percut merupakan sungai yang mengalir di Kabupaten Deli Serdang yang bermuara ke Selat Malaka. Air sungai Percut digunakan untuk memenuhi kebutuhan irigasi pertanian (bendungan), bahan baku air
instalasi pengolahan air (WTP Mini) PDAM Tirtanadi, keperluan mandi cuci kakus (MCK) serta sebagai tempat pendaratan kapal nelayan Percut Sei Tuan. Adapun limbah yang masuk ke sungai Percut seperti limbah industri,
limbah domestik, limbah pertanian, serta limbah perikanan dapat menambah jumlah limbah yang masuk ke dalam badan perairan tersebut (Situmorang dkk., 2015).
Organisme perairan merupakan kelompok organisme yang pertama kali mengalami dampak secara langsung dari pengaruh limbah atau pencemaran logam berat di perairan. Satu diantara beberapa jenis organisme perairan yang menerima dampak langsung pencemaran logam berat adalah tanaman mangrove. Mangrove banyak dijumpai di wilayah pesisir yang terlindung dari ombak dan daerah yang landai. Mangrove tumbuh optimal di wilayah pesisir yang memiliki muara sungai besar dan delta yang aliran airnya banyak mengandung lumpur. Sedangkan di wilayah pesisir yang tidak bermuara sungai, pertumbuhan vegetasi mangrove tidak optimal. Mangrove sulit tumbuh di wilayah pesisir yang terjal dan berombak besar dengan arus pasang surut kuat, karena kondisi ini tidak memungkinkan terjadinya pengendapan lumpur yang diperlukan sebagai substrat bagi pertumbuhannya (Dahuri, 2003).
Spesies mangrove yang memiliki kemampuan dalam mengakumulasikan logam berat adalah Avicennia marina. Menurut Mukhtasar (2007), bahwa A. marina dapat digunakan sebagai indikator biologis lingkungan yang tercemar logam berat seperti Cu, Pb, Cd, Zn melalui monitoring berkala. Logam berat Cd dan Pb merupakan unsur logam berat yang tidak dapat terurai oleh proses alam serta dapat terakumulasi pada A. marina. Mekanisme yang terjadi pada A. marina untuk mengurangi toksisitas logam berat adalah menyimpan banyak air sehingga dapat mengencerkan konsentrasi logam berat dalam jaringan tubuhnya. A. marina dapat
dikembangkan sebagai pengendali pencemaran logam berat di wilayah pesisir.
Tujuan Penelitian
1. Mengetahui konsentrasi logam berat Kadmium (Cd) pada akar, kulit batang dan daun mangrove A. marina.
2. Mengetahui konsentrasi Kadmium (Cd) pada sedimen dan air.
3. Mengetahui bioakumulasi logam berat Kadmium (Cd) pada sedimen dan air.
Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan gambaran akumulasi logam berat (Cd) pada mangrove A. marina di kawasan perairan Percut Sei Tuan dan sebagai sumber informasi bagi pengelola yang membutuhkan informasi mengenai peranan A. marina dalam mengurangi pencemaran logam berat serta untuk kepentingan pengelolaan sumberdaya pesisir
METODE PENELITIAN Lokasi dan Waktu Penelitian
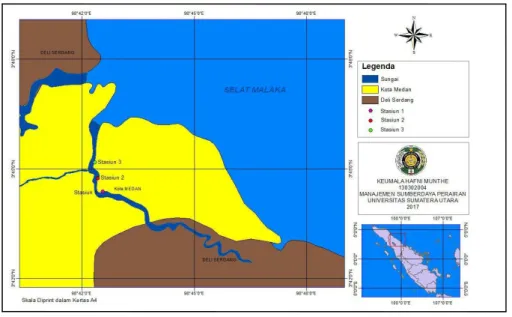
Penelitian ini dilakukan dari bulan Januari – Maret 2017 di Kawasan Mangrove Percut Sei Tuan Kabupaten Deli Serdang Sumatera Utara. Pengambilan sampel akar, kulit batang, daun, sedimen dan air dilakukan di tiga stasiun pengamatan. Pengambilan serta pengukuran parameter kualitas air dilakukan secara insitu. Analisis logam berat, sedimen dan air dilakukan di Balai Riset dan Standarisasi Industri Medan, Sumatera Utara.
Deskripsi Area
Stasiun 1: Lokasi ini berdekatan dengan kawasan Industri Medan (KIM) dan merupakan daerah pembuangan limbah KIM. Stasiun ini terletak pada
titik koordinat 3°44'33" LU dan 98°42'18,40"BT.
Stasiun 2: Lokasi ini merupakan kawasan mangrove. Stasiun ini terletak pada titik koordinat 03°44'51,09" LU dan 98°92'16,92"BT
Stasiun 3: Lokasi ini merupakan kawasan mangrove yang dekat dengan pemukiman penduduk. Mangrove disekitar kawasan ini sudah tidak terlalu rapat seperti sebelumnya. Stasiun ini terletak pada titik koordinat 03°45'05,88" LU dan 98°42'09,41"BT.
Alat dan Bahan
Alat yang digunakan adalah Global Positioning System (GPS), timbangan analitik, pH meter, thermometer, DO meter, kertas Whatman nomor 42, kertas saring Nucleopore, buku identifikasi mangrove (Noor dkk., 1999), labu erlenmeyer, alat pemotong, parang, alat tulis, kamera digital, botol aquades, pita ukur, mortal dan pastle, tanur (furmace), krus porselin, gelas ukur, hot plate, Spektrofotometri serapan atom, wadah sampel, labu takar, gelas beaker, oven, corong, pipet tetes, pengaduk kaca, bola hisap, pipet volume.
Bahan yang digunakan adalah akar, kulit batang, dan daun Avicennia marina, sampel sedimen dan sampel air laut, larutan standar Cd, larutan NHO3
Prosedur Penelitian Pengambilan Sampel
Pengambilan sampel dilakukan saat kondisi pasang atau surut dengan objek penelitian adalah tumbuhan mangrove (A. marina) dengan metode transek tegak lurus garis pantai yang dipilih secara acak (random). Pengambilan sampel mangrove dilakukan berdasarkan Ulqodry (2001), yaitu mangrove yang diambil untuk sampel adalah pohon. Jaringan mangrove yang digunakan adalah akar, kulit batang dan daun yang terkena pasang surut air laut (± 1,3 cm), dari jalur transek tersebut diambil 3 titik pengambilan sampel pada setiap lokasi dengan sistem acak (Random).
Pengukuran Parameter Fisika Kimia Perairan
Pengambilan sampel air dilakukan sebanyak dua kali yaitu pada saat pasang dan surut. Pengambilan sedimen dilakukan pada kedalaman ± 30 cm, serta pengukuran kualitas air yaitu suhu, pH, Oksigen Terlarut (DO) dan salinitas.
Preparasi Sampel Akar, Kulit Batang, Daun dan Sedimen
Sampel batang dan daun dihomogenkan dengan cara menggabungkan sampel yang diambil dari tiga titik pengambilan pada setiap stasiun pengamatan. Untuk preparasi kulit batang dan daun sampel dipotong kecil sebelum dihaluskan, sedangkan untuk sedimen, sampel dapat langsung dihaluskan. Setelah itu sampel dikeringkan dalam oven pada suhu 105ºC sampai kadar airnya konstan.
Setelah sampel mangrove dan sedimen di homogenkan, kemudian dilakukan pengarangan diatas hot plate sampai menjadi arang. Sampel yang telah menjadi arang kemudian dimasukkan kedalam tanur pada suhu 550ºC sampai menjadi abu. Setelah selesai proses pengabuan sampel kulit batang dan daun dilarutkan dengan 5 ml larutan HNO3 pekat serta ditambahkan akuades panas.
Hasil pencampuran larutan tersebut digerus didalam wadah krus porselin kemudian dimasukkan ke dalam labu ukur dan disaring menggunakan kertas saring Whatman ukuran 42. Larutan yang diperoleh siap untuk dianalis dengan menggunakan alat AAS.
Preparasi Sampel Air
Sampel air laut disaring menggunakan kertas saring kemudian diukur 100 ml. Setelah itu sampel air laut ditambahkan 5 ml larutan HNO3
pekat. Sampel dipanaskan dalam beaker glass di atas hot plate sampai volumenya berkurang menjadi 10-15 ml. Masukkan ke labu ukur yang berukuran 100 ml, kemudian ditambahkan aquades lalu dihomogenkan. Larutan yang telah homogen kemudian disaring fasa airnya dengan kertas saring Whatman ukuran 42. Larutan yang diperoleh siap untuk dianalisis dengan menggunakan alat Atomic Absorption Spectroscopy (AAS).
Pembuatan Larutan Standar Cd Larutan induk Pb yang memiliki konsentrasi 1000 ppm diambil sebanyak 10 ml lalu dimasukkan kedalam labu ukur 100 ml. Kemudian ditambahkan aquabides asam, sehingga larutan yang diperoleh adalah sebanyak 100 ppm. Dari larutan 100 ppm diambil sebanyak 10 ml lalu dimasukkan kedalam labu ukur 100 ml dengan menambahkan akuades sampai diperoleh larutan dengan konsentrasi 10 ppm.
Untuk mendapatkan konsentrasi larutan standar diambil sebanyak 2 ml, 4 ml, 6 ml, 8 ml, dan 10 ml dari larutan 10 ppm lalu masing-masing dimasukkan kedalam labu ukur 100 ml dan ditambahkan akuades
Prinsip Kerja AAS
Alat AAS diatur terlebih dahulu sesuai dengan instruksi pada alat tersebut, kemudian dikalibrasikan dengan kurva standar dari logam Pb dengan konsentrasi 0; 0,2; 0,4; 0,6; 0,8 dan 1 ppm. Lalu kemudian diukur absorbansi dan konsentrasi masing-masing sampel (air, sedimen dan A. marina)
Analisis Data Kadar Sebenarnya
Untuk mendapatkan konsentrasi logam berat yang sebenarnya, berdasarkan APHA (1995), maka digunakan rumus:
Kadar sebenarnya Mangrove:
Kadar sebenarnya (Air):
Faktor Biokonsentrasi (BCF) Faktor Biokonsentrasi dapat dilihat sebagai suatu proses kesetimbangan yang melibatkan pengambilan suatu senyawa antara biota dengan lingkungan disekitarnya. Faktor biokonsentrasi adalah angka banding antara konsentrasi mahluk hidup atau biota (Cd) dengan
konsentrasi lingkungan (Cm) (Connel dan Miller, 1995).
Untuk melihat perbandingan tingkat faktor biokonsentrasi logam berat pada akar, kulit batang dan daun pohon A. marina dengan air, digunakan rumus
HASIL DAN PEMBAHASAN Hasil
Parameter Fisika Kimia Perairan Parameter fisika-kimia perairan yang diamati pada penelitian ini adalah parameter suhu, derajat keasaman (pH), oksigen terlarut (DO) dan salinitas, perairan. Hasil pengamatan kondisi fisika dan kimia perairan yang dilakukan selama penelitian memberikan gambaran mengenai kondisi kualitas air di perairan percut sei tuan seperti yang terlihat pada Tabel 1.
Konsentrasi Logam Berat Kadmium di Air dan Sedimen
Hasil analisis konsentrasi logam berat Kadmium di air dan sedimen Perairan Percut Sei Tuan menunjukkan nilai yang bervariasi antara stasiun I dengan stasiun II dan III. Hasil analisis stasiun I konsentrasi
Kadmium pada air di Perairan Percut Sei Tuan berkisar 6,35 ppm sedangkan Stasiun II dan III memiliki konsentrasi sama yaitu < 0,003. Kedua stasiun ini mengalami konsentrasi yang rendah dibandingkan stasiun I. Konsentrasi konsentrasi Kadmium pada sedimen Perairan Percut Sei Tuan juga memiliki
Stasiun Parameter Suhu ºC Derajat Keasaman (pH) Oksigen Terlarut (DO) mg/l Salinitas (‰) I 28-31˚C 6,5-7 2,0 – 2,5 5-11 ppt II 27-31˚C 6,5-7 3,0 - 3,2 7-11 ppt III 28-30˚C 6,8-7 4,8 – 5,0 6-10 ppt Baku Mutu 28-31 ˚C 7,0- 8,5 >5 33-34 ppt Tabel 1. Parameter Kualitas Fisika dan Kimia di Perairan Percut Sei Tuan.
nilai yang berbeda. Pada stasiun I konsentrasi Kadmium bernilai 6,35 sedangkan untuk stasiun II dan III.
Memiliki nilai yang sama yaitu bernilai < 0,003 (Tabel 2).
Tabel 2. Nilai Konsetrasi Kadmium pada Air dan Sedimen
Konsentrasi Logam Berat Kadmium pada Akar, Kulit Batang dan Daun A. marina
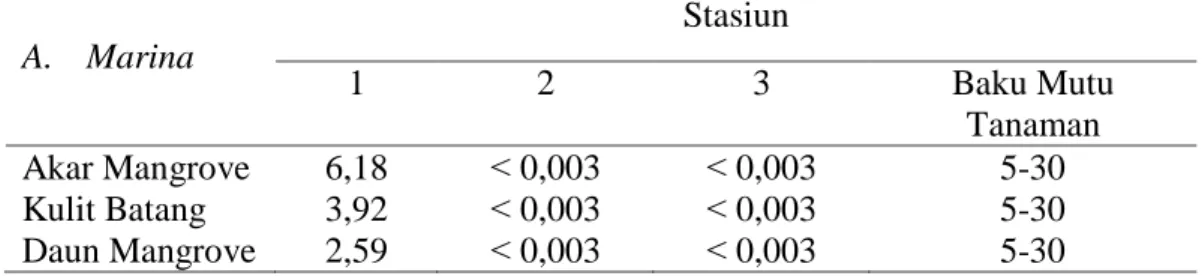
Berdasarkan hasil pengukuran rata-rata konsentrasi logam berat Kadmium pada akar, kulit batang, dan daun pohon A. marina diperoleh hasil bahwa akumulasi logam Kadmium
Faktor Biokonsentrasi (BCF)
Hasil perhitungan nilai faktor biokonsentrasi (BCF) diketahui nilai BCF tertinggi pada logam berat
akumulasi logam Kadmium lebih tinggi pada akar dibandingkan kulit batang dan daun. Kandungan logam berat Kadmium lebih tinggi pada stasiun I dibandingkan stasiun II dan III. Rata-rata kandungan logam berat Kadmium pada akar, kulit batang dan daun dapat dilihat pada Tabel 3
Kadmium pada stasiun I yaitu 10,507 ppm dan nilai BCF terendah yaitu < 0,003 ppm. Nilai faktor biokonsentrasi (BCF) Kadmium pada setiap stasiun pengamatan dapat dilihat pada Tabel 4 Parameter
Stasiun
I II III Baku Mutu
Air 6,35 ˂ 0,003 ˂ 0,003 0,001 Sedimen 7,54 ˂ 0,003 ˂ 0,003 30 A. Marina Stasiun 1 2 3 Baku Mutu Tanaman Akar Mangrove 6,18 ˂ 0,003 ˂ 0,003 5-30 Kulit Batang 3,92 ˂ 0,003 ˂ 0,003 5-30 Daun Mangrove 2,59 ˂ 0,003 ˂ 0,003 5-30 Konsentrasi Kadmium (Kadmium) ppm
Stasiun Tumbuhan Air BCF Kadmium
I 12,69 6,35 10,507
II < 0,003 < 0,003 < 0,003 III < 0,003 < 0,003 < 0,003
Tabel 3. Nilai Konsetrasi Kadmium pada Akar, Kulit Batang dan Daun A.marina
Tabel 4. Nilai Faktor Biokonsentrasi (BCF) Daun
Pembahasan
Parameter Fisika Kimia Perairan Suhu
Hasil pengukuran suhu pada stasiun I memiliki kisaran antara 28-31˚C, stasiun II 27-31˚C dan stasiun III 28-30˚C (Tabel 1). Kisaran suhu tersebut belum melebihi ambang batas dan masih dapat di toleransi oleh biota laut. Hal ini sesuai dengan Rahman (2006) kisaran suhu yang mampu ditoleransi suatu biota laut yaitu berkisar 20 - 35 ˚C sedangkan berdasarkan baku mutu Kepmen LH No 51 tahun 2004 untuk biota laut berkisar 28-30 ˚C.
Adanya variasi suhu (Tabel 1) pada perairan ini dipengaruhi oleh berbagai faktor yaitu kondisi arus (pasang surut) dan angin. Hal ini sesuai dengan pernyataan Menurut Qu dkk (2005) suhu permukaan laut bervarias secara spasial maupun temporal dan faktor yang mempengaruhi sangat kompleks, namun pada perairan Kepulauan Indonesia, faktor-faktor yang dominan berpengaruh adalah angin muson lokal dan percampuran massa air akibat pasang surut.
Hasil pengukuran suhu sebesar 27-31˚C (Tabel 1) berbeda dengan hasil penelitian Husainy dkk., (2014) yang berkisar antara 23-27 ˚C di perairan yang sama. Perbedaan ini dipengaruhi oleh beberapa faktor seperti curah hujan, arus perairan, dan kedalaman air. Hal ini sesuai dengan Patty dkk., (2013) distribusi suhu air laut di suatu perairan dipengaruhi oleh banyak faktor diantaranya ialah radiasi sinar matahari, kedalaman, letak geografis, angin dan musim
Derajat Keasaman (pH)
Derajat keasaman (pH) di perairan ini berkisar antara 6,5-7 (Tabel 1). Variasi nilai ini masih belum melebihi ambang batas. Kepmen LH
No 51 tahun 2004 menetapkan nilai pH untuk biota laut berkisar antara 7-8,5. Menurut Salm (1984) pH di suatu perairan yang normal berkisar antara 8,0-8,3. Dengan demikian pH air laut di perairan ini tergolong normal
Penelitian ini sama dengan hasil Husainy (2014) di perairan yang sama dengan kisaran pH 6,4 – 7 . Persamaan nilai ini terjadi karena perubahan pH pada perairan tidak terjadi secara cepat namun secara perlahan dan berlangsung lebih lama karena dapat mempengaruhi kehidupan biota laut. Hal ini sesuai dengan pernyataan Rukminasari dkk (2014) tidak semua makhluk bisa bertahan terhadap perubahan nilai pH, untuk itu alam telah menyediakan mekanisme yang unik agar perubahan tidak terjadi atau terjadi tetapi dengan cara perlahan
Oksigen Terlarut (DO)
Hasil pengukuran DO mendapatkan kisaran nilai 2,0 – 5,0 mg/l. konsentrasi DO tertinggi terdapat pada stasiun III yaitu 4,8-5,0 dan nilai DO terendah terdapat pada stasiun I yaitu 2,0 – 2,5 (Tabel 1) . Rendahnya konsentrasi DO pada stasiun I diduga lebih banyak menerima limbah yang berasal dari KIM II (Kawasan Industri Medan II) seperti limbah berbagai industri. Hal ini sesuai dengan pernyataan Susana (2009) perubahan konsentrasi oksigen yang berperan sebagai indikator kualitas perairan dapat terjadi sebagai akibat berlimpahnya senyawa-senyawa kimia baik yang bersifat polutan maupun bukan polutan. Limbah yang mengalir ke dalam perairan laut pada umumnya kaya akan bahan organik, berasal dari bermacam sumber seperti limbah rumah tangga, pengolahan makanan dan bermacam industri kimia lainnya.
Penelitian ini berbeda dengan hasil penelitian Safitri (2014) yang jauh
lebih tinggi dengan kisaran antara 3,2 – 7 di perairan yang sama. Perbedaan ini disebabkan oleh beberapa faktor seperti suhu, gerakan air dan salinitas. Hal ini sesuai dengan Simanjuntak (2007) oksigen terlarut di perairan ini sangat dipengaruhi oleh meningkatnya bahan-bahan organik yang masuk ke perairan disamping faktor-faktor lainnya diantaranya kenaikan suhu, salinitas, respirasi, adanya lapisan di atas permukaan air, senyawa yang mudah teroksidasi dan tekanan atmosfir.
Salinitas
Nilai kisaran salinitas stasiun 5 - 11 o/oo , stasiun II 7-11o/oo dan stasiun III 6 - 11 o/oo (Tabel 4) memiliki nilai yang bervariasi dan tergolong rendah hal ini dapat terjadi pada lokasi penelitian merupakan daerah yang dipengaruhi oleh aliran sungai. Hal ini sesuai dengan Riyadi dkk (2005) sebaran salinitas di laut dipengaruhi oleh berbagai faktor seperti pola sirkusi air, penguapan, curah hujan dan aliran sungai. Perairan dengan tingkat curah hujan tinggi dan dipengaruhi oleh aliran sungai memliki salinitas yang rendah sedangkan perairan yang memiliki penguapan yang tinggi salinitas perairannya tinggi.
Konsentrasi Logam Kadmium Berat di Air dan Sedimen
Hasil analisis konsentrasi logam berat Kadmium di air dan sedimen Perairan Percut Sei Tuan menunjukkan nilai yang bervariasi pada setiap stasiun pengamatan. Hasil konsentrasi Kadmium pada air lebih rendah dibandingkan dengan sedimen. Konsentrasi Kadmium di air yaitu 6,35 mg/kg sedangkan konsentrasi Kadmium pada sedimen menunjukkan hasil yang lebih tinggi yaitu 7,54 mg/kg (Tabel 2). Hal ini sesuai dengan
Leiwakabessy (2005) logam berat mempunyai sifat yang mudah mengikat bahan organik dan mengendap di dasar perairan dan bersatu dengan sedimen sehingga kadar logam berat dalam sedimen lebih tinggi dibanding dalam air
Hasil penelitian ini berbeda dengan hasil penelitian Safitri (2014) dengan nilai yang jauh lebih rendah yaitu 0,00065 mg/k pada air. Konsentrasi Kadmium saat ini lebih tinggi dengan nilai 6,35 mg/k pada air (Tabel 5). Hal ini diduga disebabkan waktu dalam pengambilan sampel. Apabila pengambilan sampel air pada saat surut maka konsentrasi logam berat akan tinggi dan sebaliknya apabila saat pasang maka konsentrasi kadmium akan berkurang hal ini sesuai dengan Windom (1992) bahan pencemar logam berat biasanya berasal dari darat.. Hal ini juga di dukung oleh Hutagalung (1984) pada saat memasuki laut, kadar logam berat sangat dipengaruhi oleh pasang surut air laut. Karena berasal dari darat maka kadar logam berat pada air laut surut lebih tinggi dibandingkan pada saat air laut pasang.
Konsentrasi Logam Berat Kadmium pada Akar A. marina
Hasil penelitian kandungan logam berat kadmium pada akar memiliki konsentrasi sebesar 6,18 mg/kg (Tabel 3). Nilai ini jauh lebih tinggi dibandingkan kadmium pada kulit batang dan daun. Tingginya konsentrasi di akar disebabkan akar merupakan organ yang langsung menyerap nutrien dari tanah/sedimen dan kemudian diteruskan ke organ tumbuhan lainnya (kulit batang dan daun). Hal ini sesuai dengan pernyataan Hardiani (2009) secara umum tumbuhan melakukan penyerapan oleh akar, baik yang berasal dari sedimen maupun air, kemudian terjadi
translokasi ke bagian tumbuhan yang lain dan lokalisasi atau penimbunan logam pada jaringan tertentu. Hal ini juga sesuai dengan Setiawan (2013) Besarnya kandungan logam berat di jaringan akar diduga karena jaringan akar mempunyai interaksi langsung dengan sedimen dan air yang telah terkontaminasi oleh logam berat yang mengendap.
Konsentrasi Logam Berat Kadmium pada Kulit Batang A. marina
Hasil penelitian kandungan logam berat Kadmium di kulit batang pada setiap stasiun memiliki nilai yang bervariasi Pada stasiun I kandungan logam berat Kadmium adalah sebesar 3,92 mg/kg, stasiun II dan III <0,003 mg/kg (Tabel 3). Perbedaaan kandungan logam berat Kadmium pada setiap stasiun disebabkan oleh besarnya batang pohon mangrove yang bervariasi. Pohon yang besar dinilai lebih lama terpapar sehingga lebih banyak mengakumulasikan logam berat dibandingkan ukuran yang kecil dan masih muda. Hal ini sesuai dengan Lase dkk., (2016) perbedaan diameter batang pohon menentukan banyaknya logam berat dan zat-zat lain yang terakumulasi di dalam pohon tersebut. Semakin besar diameter batang pohon, maka usia pohon juga semakin tua sehingga akumulasi zat-zat yang terdapat di dalam pohon tersebut semakin besar. Senyawa logam berat yang terdapat di dalam pembuluh pengangkut dan kulit batang tanaman dapat terlokalisasi dengan baik.
Konsentrasi Logam Berat Kadmium pada Daun A. marina
Hasil penelitian kandungan logam berat Kadmium di daun pada stasiun I adalah 2,59 mg/kg, stasiun II dan III sebesar <0,003 mg/kg (Tabel 3). Tingginya akumulasi kadmium di daun
pada stasiun I disebabkan jaringan daun sebagai tempat penimbunan logam berat sebelum dilepas ke lingkungan. Hal ini sesuai dengan Chaney dkk (1998) logam berat akan didistribusi ke seluruh jaringan tanaman sampai daun, melalui proses uptake pada akar, ditahan pada jaringan, dan dilepas ke lingkungan melalui pelepasan daun.
Pada stasiun II dan III konsentrasi logam pada daun cenderung sangat kecil dibandingkan stasiun I (Tabel 3). Penelitian hampir sama dengan penelitian Samil (2013) di perairan yang berbeda dengan spesies mangrove yanag sama yaitu A.marina dengan nilai <0.005. Hal ini dapat terjadi bahwa sifat logam kadmium pada alam sedikit namun pada waktu tertentu dapat meningkat dengan jumlah yang banyak. Hal ini sesuai dengan Darmono (1999) logam Cadmium cenderung memiliki jumlah yang kecil di alam, tetapi dapat meningkat jumlahnya dalam keadaan tertentu. Selain itu faktor penyebab lainnya adalah sumber pencemar yang masih sedikit di stasiun II dan III. Hal ini Sesuai dengan Samil (2013) logam Cd nilainya relatif sangat kecil sehingga tidak dapat terdeteksi. Hal ini disebabkan sumber pencemar yang sedikit pada lokasi penelitian
Faktor Biokonsentrasi (BCF)
Hasil perhitungan faktor biokonsentrasi bahwa A. Marina mampu mengakumulasikan logam berat Kadmium. Hasil faktor biokonsentrasi yang diperoleh adalah BCF = 10,507 (Tabel 4). Menurut Connel dan Miller (1995) kisaran faktor biokonsentrasi (BCF < 1000) termasuk dalam kemampuan tinggi (1000 > BCF > 250) kemampuan sedang dan (BCF > 250) kemampuan rendah. Berdasarkan kategori tersebut hasil ini termasuk kategori rendah dengan (BCF > 250).
Menurut Hutagalung (1991) besar kecilnya BCF tergantung pada jenis logam berat, organisme, lama pemaparan serta kondisi lingkungan perairan
Faktor biokonsentrasi tersebut membuktikan bahwa pohon A. Marina mempunyai kemampuan untuk mengakumulasikan logam berat kadmium yang terdapat disekitar habitatnya. Akar merupakan organ yang paling tinggi dalam mengakumulasikan logam berat karena akar merupakan jaringan yang pertama dalam menyerap unsur hara di air maupun yang terendap di sedimen. Hal ini sesuai dengan Tam dan Wong (1996) Tumbuhan mangrove mengakumulasi logam berat paling tinggi terdapat di bagian akarnya. Namun demikian faktor lain seperti mobilitas dan kelarutan logam juga berpengaruh terhadap akumulasi logam berat dalam tumbuhan .
Mac Farlane dkk (2003) mengatakan, bahwa akar A. marina dapat digunakan sebagai indikator biologis paparan lingkungan Cd, Pb dan Zn. Ini menunjukkan potensi Avicennia marina sebagai spesies fitoremediasi untuk ekosistem mangrove. Pertumbuhan A. marina tersebut subur dibandingkan dengan spesies mangrove lainnya, hal ini menunjukkan terhadap kemampuan adaptasinya bahkan dalam kondisi yang tercemar (Kumar dkk, 2011).
Mac Farlane dkk (2007) Logam cenderung terakumulasi dalam akar sama dengan konsentrasi yang ada pada sedimen yang berdekatan, sementara konsentrasi logam dalam daun adalah setengah dari akar atau lebih rendah. Kandungan logam dalam daun berada sepersepuluh atau kurang dari konsentrasi yang ada pada sedimen
KESIMPULAN DAN SARAN Kesimpulan
1. Konsentrasi logam berat Kadmium tertinggi pada akar A. marina terdapat pada stasiun I yaitu sebesar 6,18 mg/kg, Konsentrasi Logam berat Kadmium pada kulit batang tertinggi pada stasiun I dengan nilai 3,92 mg/kg. Kemudian konsentrasi logam Kadmium pada daun mangrove tertinggi pada stasiun I dengan nilai 2,59 mg/kg.
2. Konsentrasi logam berat Kadmium pada air tertinggi pada stasiun I dengan nilai 6,35 mg/kg. Sedangkan konsentrasi logam Kadmium pada sedimen paling tinggi terdapat di stasiun I dengan nilai sebesar 7,54 mg/kg.
3. Sedimen lebih mudah menyerap logam Kadmium dibandingkan dengan air sehingga konsentrasi konsentrasi logam berat Kadmium pada sedimen lebih tinggi (7,5 mg/kg) dibandingkan dengan air (6,35 mg/kg). Dimana air merupakan terbaik pelarut di perairan sehingga dapat mengurangi konsentrasi logam berat Kadmium di dalam air. Saran
Dari hasil penelitian yang sudah dilakukan pohon mangrove A. marina mampu mengakumulasi logam berat di perairan. Namun untuk saat ini Perairan Percut Sei Tuan belum melebihi baku mutu. Diperlukan penelitian lanjutan tentang keberadaan logam Kadmium dan disarankan untuk tetap melindungi vegetasi mangrove khususnya A.marina karena bermanfaat sebagai bioindikator pencemaran logam berat.
DAFTAR PUSTAKA
APHA. 1995. Standar Methods For The Examination Of Water And Wastewater. (19th ed). American Water Works Association, Water Pollution Control Federation. Washington D.C..
Connel, D. W., dan G. J. Miller. 1995. Kimia dan Ekotoksikologi Pencemaran.Universitas
Indonesia Press. Jakarta.
Chaney R.L, J.S. Angle dan S. L. Brown. 1998. Soil-Root Interface: Food Chain Contamination and Ecosystem Health. (3): 9-11.
Dahuri, R. 2003. Keanekaragaman Hayati Laut. Aset Pembangunan Berkelanjutan Indonesia. PT. Gramedia Pustaka Utama. Jakarta
Hardiani H. 2009. Potensi Tanaman Dalam Mengakumulasi Logam Cu Pada Media Tanah Terkontaminasi Limbah Padat
Industri Kertas. 44 (1) : 27 – 40.
Hutagalung, H.P. 1984. Pencemaran Logam Berat dan Analisa Logam Berat. Kerjasama antara UNESCO/UNDP, P3OLIPI dan Universitas Riau. Puslit UNRI. Pekanbaru.
Keputusan Menteri Lingkungan Hidup No.51/Men KLH/I/2004 Tentang Baku Mutu Air Laut Kumar. N. J. I. P. R. Sajish. R. N.
Kumar. Basil George and ShailendraViyol. 2011. Bioaccumulation of Lead, Zinc and Cadmium in Avicennia
marina Mangrove Ecosystem near Narmada Estuary in Vamleshwar. West Coast of Gujarat. India. 6 (1): 008-013 Lase, V. A., Yunasfi., dan Desrita.
2016. Daya Serap Mangrove Avicennia Marina Terhadap Logam Berat Kadmium (Cd) dan Timbal (Pb) di Kampung Nelayan Kecamatan Medan Belawan Sumatera. Universitas Sumatera Utara. Medan.
Leiwakabessy, F. 2005. Logam Berat Di Perairan Pantai Pulau Ambon Dan Korelasinya Dengan Kerusakan Cangkang, Rasio Seks, Ukuran Cangkang, Kepada Individu Dan Indeks Keragaman Jenis Siput Nerita (Neritidae: Gastropoda). Universitas Airlangga. Surabaya Mac Farlane, G. R. A. Pulkownik and M.D. Burchett. 2003. Accumulation and distribution of heavy metals in the grey mangrove Avicennia marina (Forsk.)123 : 139–151.
Mac Farlane, G.R. Claudia E. Kollerdan Simon P. Blomberg. 2007. Accumulation and partitioning of heavy metals in mangroves. (69) : 1454 –1464 Noor, Y., R. M. Khazali., dan I. N. N.
Suryadiputra. 1999. Panduan Pengenalan Mangrove di Indonesia. PKA/WI-IF. Bogor. Patty, W., Tarumingkeng dan Adrie.
2007. Variasi Temporal dari Penyebaran Suhu di Muara Sungai Sario. J. I. Kelautan. 12 (2):73-78.
Qu T., Y. Du, J. Strachan, G. Meyers, dan J. Slingo. 2005. Sea surface Temperature and Its variability In the Indonesian Region. Oceanography, 18 (4): 50-61 Rahman, A. 2006. Konsentrasi Logam
Berat Timbal (Pb) dan Kadmium (Cd) Pada Beberapa Jenis Krustasea di Pantai Batakan dan Takisung Kabupaten Tanah Laut Kalimantan Selatan. Bioscientiae 3 (2).
Riyadi.A. L. Widodo dan K. Wibowo. 2005. Kajian Kualitas Perairan Laut Kota semarang dan kelayakannya untuk budidaya laut. 6 (3) : 497-501
Rukminasari. N, Nadiarti dan K. Awaluddin. 2014. Pengaruh Derajat Keasaman (Ph) Air Laut Terhadap Konsentrasi Kalsium Dan Laju Pertumbuhan Halimeda Sp. 24 (1): 28-34 Setiawan. H. 2013. Akumulasi dan
Distribusi Logam Berat Pada Vegetasi Mangrove Di Perairan Pesisir Sulawesi Selatan. (3) 1 : 19-20.
Simanjuntak. M. 2007. Oksigen Terlarutdan Apparent Oxygen Utilization di Perairan Teluk Klabat. Pulau Bangka.12 (2) : 59 – 66.
Susana. T. 2009. Tingkat Keasaman (Ph) Dan Oksigen Terlarut Sebagai Indikator Kualitas Perairan Sekitar Muara Sungai Cisadane. 5 (2): 33-36.
Tam N.F. Y and Wong, YS. 1996. Retention and distribution of heavy metals in mangrove soils
receiving wastewater. (94): 283-291
Ulqodry, T. Z. 2001. Konsentrasi Logam Berat dalam Jaringan Mangrove Sonneratia Alba dan Avicennia marina di Pulau Ajkwa dan Pulau
Kamora, Kabupaten Timika,
Papua. [Skripsi]. Program Studi
Ilmu Kelautan Universitas
Diponegoro. Semarang
Windom, H.L. 1992. Contamination of Marine Environment from Land-Based Sources. Mar. Pollut. Bull. (25) :32 – 36