ANTARAKSI BAWANG PUTIH (Allium sativum L.) DAN ASETOSAL
DITINJAU DARI EFEK ANTITROMBOTIK PADA TIKUS PUTIH BETINA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh :
Johan Andreas Santoso NIM : 008114130
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2007
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
vi
How can I say thanks for the things that You have done for me? Things so undeserved yet You give to prove Your love for me The voices of a million angels could not express my gratitude All that I am and ever hope to be I owe it all to You
To God be the glory To God be the glory
To God be the glory for the things He has done With His blood He has saved me
With His power He has raised me
To God be the glory for the things He has done
Just let me live my life let it be pleasing Lord, to Thee Should I gain any praise let it go to Calvary
With His blood He has saved me With His power He has raised me
To God be the glory for the things He has done
Kupersembahkan kepada:
Papa, Mama dan adek, sebagai ungkapan terima kasih, hormat dan cintaku Almamaterku
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
INTISARI
Penelitian ini dilakukan dengan maksud untuk mengetahui dampak dari antaraksi antara bawang putih dan asetosal, dengan melakukan pengujian untuk melihat pengaruh praperlakuan perasan bawang putih terhadap efek antitrombotik asetosal dan seberapa besar pengaruhnya dengan hewan uji tikus putih betina.
Penelitian ini dilakukan dengan metode waktu perdarahan ekor tikus. Waktu perdarahan adalah waktu sejak terjadinya luka pada pembuluh darah hingga terbentuknya sumbat primer yang belum stabil, ditandai dengan berhentinya perdarahan. Dosis asetosal yang digunakan sebesar 325 mg dikonversikan kepada dosis untuk tikus sebesar 29,25 mg/kg BB dan dosis perasan bawang putih terdiri dari 3 peringkat dosis. Digunakan 56 ekor hewan uji yang dibagi sama banyak dalam 8 kelompok uji, yaitu: kelompok kontrol negatif CMC 1%, kelompok perlakuan suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB, kelompok perlakuan bawang putih dosis 32,81 mg/kg BB, kelompok perlakuan bawang putih dosis 46,87 mg/kg BB, kelompok perlakuan bawang putih dosis 60,94 mg/kg BB, kelompok antaraksi praperlakuan bawang putih dosis 32,81 mg/kg BB diberi suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB, kelompok antaraksi praperlakuan bawang putih dosis 46,87 mg/kg BB diberi suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB, kelompok antaraksi praperlakuan bawang putih dosis 60,94 mg/kg BB diberi suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB. Pemberian bahan uji dilakukan dengan cara per oral. Data dianalisis secara statistik menggunakan metode ANOVA satu arah dengan taraf kepercayaan 95% diikuti dengan uji Scheffe. Data disajikan dalam nilai rata-rata ± standar error (X ± SE).
Hasil dari penelitian ini menunjukkan bahwa asetosal dosis 325 mg tidak menunjukkan efek antitrombotik ketika diberikan tersendiri. Efek antitrombotik nampak setelah pemberian praperlakuan perasan bawang putih dengan peringkat dosis 32,81 mg/kg BB, 46,87 mg/kg BB dan 60,94 mg/kg BB dan memberikan peningkatan waktu perdarahan sebesar masing-masing 80,5%, 163,5% dan 264,5% seiring dengan peningkatan peringkat dosis praperlakuan perasan bawang putih.
Kata kunci: Antaraksi, Bawang Putih (Allium sativum L.), Asetosal, Antitrombotik
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
ABSTRACT
The aim of this research was to find out the effect of garlic (Allium sativum L.) and acetosal interaction, by observing what was the effect of garlic juice pretreatment to antithrombotic effect of acetosal and how far was the effect using female rats as the studied animal
This research was carried out with rat’s tail bleeding time method. Bleeding time was period needed for bleeding caused of vascular injury to stop. Dosage of acetosal used for this research was 325 mg, converted into dosage for rats as 29,25 mg/kg weight. Dosage of garlic juice comprised three different levels. Fifty-six female rats classified equally in eight study groups, those were: negative control group treated with 1% CMC, group treated with suspension of 1% acetosal in 1% CMC dosage 29,25 mg/kg weight, group treated with garlic dosage 32,81 mg/kg weight, group treated with garlic dosage 46,87 mg/kg weight, group treated with garlic dosage 60,94 mg/kg weight, group pretreated with garlic dosage 32,81 mg/kg weight given suspension of 1% acetosal in 1% CMC dosage 29,25 mg/kg weight, group pretreated with garlic dosage 46,87 mg/kg weight given suspension of 1% acetosal in 1% CMC dosage 29,25 mg/kg weight, and group pretreated with garlic dosage 60,94 mg/kg weight given suspension of 1% acetosal in 1% CMC dosage 29,25 mg/kg weight. All the tested material given to the animal object orally. The data were analyzed using one way ANOVA method with the level of degree 95% followed with post-hoc test Scheffe. The data served in mean value ± standard error (X ± SE).
The result of the research indicated that acetosal dosage 325 mg given individually, had not shown antithrombotic effect. The antithrombotics effect occurred after garlic juice pretreatment dosage 32,81 mg/kg weight, 46,87 mg/kg weight and 60,94 mg/kg weight were given. The increasement of bleeding time were 80,5%, 163,5% and 264,5% following the increasement of garlic juice dosage level.
vii
PRAKATA
Puji syukur penulis panjatkan kepada Tuhan Yang Maha Kuasa karena
berkat pertolongan-Nya penelitian ini dapat diselesaikan. Tentunya ada banyak pihak
yang terlibat dalam mewujudkan syukur ini, karenanya penulis hendak berterima
kasih kepada:
1. Rektor Universitas Sanata Dharma Yogyakarta
2. Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta
3. Kaprodi Farmasi Universitas Sanata Dharma, sekaligus Ketua Panitia Skripsi
Fakultas Farmasi Universitas Sanata Dharma, Ibu Christine Patramurti.
Terima kasih karena telah memberi saya kesempatan menyelesaikan ujian
skripsi ini.
4. Seluruh staf pengajar dan staf admin Fakultas Farmasi Universitas Sanata
Dharma Yogyakarta. Terima kasih untuk setiap ajaran, didikan, bimbingan,
pertemanan dan pertolongan selama ini.
5. Bapak Drs. Mulyono, Apt. sebagai dosen pembimbing skripsi ini. Terima
kasih karena telah memberi saya kesempatan untuk tetap bisa ujian skripsi..
Terima kasih juga untuk kesabaran membimbing saya selama ini.
6. Bapak Ipang Djunarko, M.Si., Apt. dan Ibu dr. Luciana Kuswibawati, M.Kes.
sebagai dosen penguji.
7. Ibu Phebe Hendra, M.Si., Apt. yang sempat menjadi pembimbing
pendamping. Terima kasih untuk kesabaran membimbing saya.
8. Papa dan Mama. Terima kasih telah melahirkan, memelihara, membimbing,
membiayai, mendisiplin, dan terutama mencintaiku selama ini.
9. Adekku Fani. Terima kasih telah menjadi saudara terdekatku dan sahabatku
yang begitu mencintaiku.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
pemberi semangat dan sahabat dalam segala situasi yang juga mengasihi
dengan tulus.
11.Keluarga besar Perkantas DIY. Mas Didik yang menemani dan membimbing
selama ini, teman-teman staf, teman-teman pengurus BPC, teman-teman
pengurus pelayanan siswa, mahasiswa, alumni dan medis yang telah
mendoakan dengan setia.
12.Teman-teman yang setia mendoakan. Nandar, Bernard, Hardo, Pipin, Pundi,
Iwan, Idus.
13.Adik-adik yang membanggakan. Pras, Ardi, Christian dan Thomas.
14.Teman-teman angkatan 2000 yang terus mendukung. Vica, Andhika, Indra,
Tossy, Priya, Tono dan Vitus juga teman-teman yang sekarang sudah tersebar
di Indonesia ini.
Tentunya masih ada banyak pihak yang membantu penyelesaian penelitian
ini hingga penyusunan laporan penelitian ini, yang tidak dapat penulis sebutkan satu
persatu.
Penulis menyadari bahwa laporan hasil penelitian ini masih jauh dari
sempurna. Karenanya penulis akan dengan senang hati menerima masukan yang
berguna untuk meningkatkan kemampuan dan mutu penulis.
DAFTAR ISI
Halaman
HALAMAN JUDUL...iii
HALAMAN PERSETUJUAN PEMBIMBING...iv
HALAMAN PENGESAHAN...v
HALAMAN PERSEMBAHAN...vi
PRAKATA...vii
PERNYATAAN KEASLIAN KARYA...ix
DAFTAR ISI...x
DAFTAR GAMBAR...xiv
DAFTAR TABEL...xv
DAFTAR LAMPIRAN...xvi
INTISARI...xvii
ABSTRACT......xviii
BAB I PENGANTAR...1
A. Latar belakang...1
1. Perumusan masalah...2
2. Keaslian penelitian...2
3. Manfaat penelitian...3
B. Tujuan penelitian...3
1. Tujuan umum...3
2. Tujuan khusus...3
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
BAB II PENELAAHAN PUSTAKA...4
A. Antaraksi obat……….4
1. Pendahuluan………...4
2. Jenis………5
a. Antaraksi farmakokinetika….………..6
b. Antaraksi farmakodinamika……….7
3. Sifat………8
B. Bawang putih………8
1. Deskripsi………8
2. Sinonim………10
3. Sistematika………...10
4. Kandungan kimia……….11
5. Kegunaan………..12
6. Efek antitrombotik………...………12
7. Toksisitas………..14
C. Darah………..14
D. Trombosit………...15
E. Pembekuan Darah………...16
1. Hemostasis………...16
2. Mekanisme koagulasi darah……..………...17
3. Mekanisme antikoagulasi darah………...…………19
F. Antitrombotik………..21
1. Rumus bangun………21
2. Pemerian……….21
3. Kinetika………..22
4. Kegunaan………22
5. Efek samping………..22
6. Efek antitrombotik…...………..23
H. Metode uji efek antitrombotik………23
I. Landasan Teori………...25
J. Hipotesis……….26
BAB III METODOLOGI PENELITIAN...27
A. Jenis dan rancangan penelitian...27
B. Variabel dan definisi operasional...27
C. Bahan atau materi penelitian...28
D. Alat penelitian...29
E. Tata cara penelitian...30
F. Tata cara analisis hasil...33
BAB IV HASIL DAN PEMBAHASAN...34
A. Uji pendahuluan...34
1. Perancangan metode penelitian...34
2. Penentuan dosis asetosal...36
3. Penyarian bawang putih...36
4. Penentuan dosis bawang putih...37
5. Penentuan selang waktu pemberian asetosal...38
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
B. Pengujian efek antitrombotik...38
BAB V KESIMPULAN DAN SARAN...54
A. Kesimpulan...54
B. Saran...54
DAFTAR PUSTAKA ...55
LAMPIRAN...58
xiv
DAFTAR GAMBAR
Gambar 1 : Bawang putih...9
Gambar 2 : Struktur kimia Z – Ajoene...11
Gambar 3 : Struktur kimia E – Ajoene...11
Gambar 4 : Mekanisme sintesis tromboksan A2 dan leukotrien...13
Gambar 5 : Skema pembekuan darah...17
Gambar 6 : Mekanisme koagulasi darah...20
Gambar 7 : Rumus bangun asetosal...21
Gambar 8 : Foto metode waktu perdarahan ekor...35
Gambar 9 : Umbi bawang putih...37
Gambar 10 : Hasil perasan bawang putih...37
Gambar 11 : Diagram waktu perdarahan...40
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
DAFTAR TABEL
Tabel I : Rata-rata waktu perdarahan...39
Tabel II : Hasil analisis ANOVA satu arah...41
xvi
DAFTAR LAMPIRAN
Lampiran : Output olah data dengan program
SPSS 12.0 for Windows...58
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
BAB I. PENGANTAR A. Latar Belakang
Sejak zaman dahulu bawang putih sudah dikenal sebagai bahan alam
yang dapat digunakan dalam masakan maupun dalam pengobatan tradisional.
Dalam masakan bawang putih digunakan sebagai salah satu bumbu yang
memberikan rasa dan bau yang khas. Dalam bidang kesehatan dan pengobatan
tradisional bawang putih sangat terkenal sebagai bahan alam yang memiliki
banyak khasiat, antara lain: penambah tenaga, antibakteri, mengobati sakit perut,
mengeluarkan gas dari dalam perut, sebagai analgesik, menurunkan tekanan darah
tinggi dan pencegahan penyakit jantung (Roser, 1991; Rukmana, 1995). Saat ini
banyak sediaan bawang putih yang diperdagangkan secara bebas. Beberapa ahli
menduga bawang putih mempunyai kemungkinan berantaraksi dengan obat-obat
diabetes atau obat-obat pengencer darah yang menimbulkan efek yang tidak
diharapkan (Graedon dan Graedon, 1997).
Seiring meningkatnya jumlah kejadian penyakit jantung dan angka
kematian yang diakibatkan olehnya banyak penelitian dilakukan untuk mencari
obat-obat baru dengan aktivitas yang dapat mencegah dan mengobati segala
keluhan dan penyebab penyakit jantung. Obat-obat yang disebut sebagai obat-obat
antitrombotik mulai banyak digunakan di masyarakat sebagai bagian dari
pencegahan dan penanganan penyakit jantung. Asetosal (aspirin) merupakan salah
satu obat yang memiliki efek antitrombotik dan banyak digunakan dalam
2
Dalam upaya pengobatan, sering kali beberapa obat digunakan
bersama-sama, baik itu atas anjuran tenaga medis maupun inisiatif pengguna obat.
Penggunaan dua obat atau lebih secara bersamaan mungkin menyebabkan
terjadinya peristiwa antaraksi obat. Antaraksi obat terjadi karena suatu obat
mempengaruhi obat lainnya. Pengaruh yang ditimbulkan ini dapat menyebabkan
kenaikan maupun penurunan efek atau toksisitas suatu obat sehingga antaraksi
obat menjadi suatu hal yang harus terus diwaspadai dan diperhatikan dalam
penggunaan obat-obat secara bersamaan. Selain itu beberapa obat dapat
berantaraksi dengan makanan, bahan alam maupun bahan kimia yang berasal dari
lingkungan sekitar (Setiawati, 1995; Stockley, 1994).
1. Perumusan masalah
Dari uraian di atas, permasalahan yang timbul adalah apa pengaruhnya
jika bawang putih diberikan bersama-sama asetosal terhadap efek antitrombotik
asetosal dan seberapa besar pengaruh antaraksi tersebut terhadap efek
antitrombotik asetosal?
2. Keaslian penelitian
Penelitian mengenai manfaat farmakologis bawang putih telah banyak
dilakukan, antara lain: pengaruh campuran ekstrak bawang putih dan minyak atsiri
daun sirih terhadap kadar kolesterol (Istyorini, 1989), daya antibakteri bawang
putih terhadap Staphylococcus aureus dan Escherichia coli secara in vitro
(Adriani, 1992), pengaruh praperlakuan bawang putih terhadap efek analgesik
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
asetosal (Karmila, 2001). Sejauh penelusuran peneliti, penelitian mengenai
pengaruh praperlakuan bawang putih terhadap efek antitrombotik asetosal belum
pernah dilakukan.
3. Manfaat penelitian
Manfaat teoritis dari penelitian ini adalah membuktikan adanya antaraksi
antara bawang putih dengan asetosal. Manfaat praktis dari penelitian ini adalah
memberikan informasi adanya dan seberapa besarnya pengaruh praperlakuan
bawang putih terhadap efek antitrombotik asetosal.
B. Tujuan Penelitian 1. Tujuan umum
Secara umum penelitian ini bermaksud untuk mengetahui dampak
antaraksi antara bawang putih dengan asetosal.
2. Tujuan khusus
Secara khusus penelitian ini bertujuan untuk mengetahui apakah
praperlakuan bawang putih berpengaruh terhadap efek antitrombotik asetosal dan
seberapa besar pengaruh praperlakuan bawang putih tersebut terhadap efek
BAB II.
PENELAAHAN PUSTAKA A. Antaraksi Obat 1. Pendahuluan
Obat hingga menghasilkan suatu efek melewati berbagai proses yang
kompleks dan rumit. Umumnya didasari suatu rangkaian reaksi, yang dibagi
dalam tiga fase, yaitu: fase farmasetika, fase farmakokinetika dan fase
farmakodinamika. Fase farmasetika meliputi hancurnya bentuk sediaan obat dan
melarutnya bahan obat di tempat absorpsi tertentu untuk diabsorpsi ke peredaran
sistemik. Fase farmakokinetika meliputi proses-proses pengambilan suatu bahan
obat, yaitu absorpsi dan distribusi, dan proses-proses yang menyebabkan
penurunan konsentrasi obat dalam tubuh, yaitu biotransformasi dan ekskresi. Fase
farmakodinamika merupakan interaksi obat-reseptor dan juga proses-proses yang
terlibat di mana akhir dari efek farmakologi terjadi (Mutschler, 1986). Rangkaian
reaksi dari fase-fase tersebut menghasilkan derajat farmakologi suatu obat yang
berupa mula kerja (onset), masa kerja (durasi) dan kekuatan (intensitas) efek.
Artinya jika terdapat faktor yang mempengaruhi rangkaian reaksi dari ketiga fase
di atas derajat farmakologi suatu obat juga akan terpengaruh.
Di antara berbagai faktor yang mempengaruhi respon tubuh terhadap
pengobatan terdapat faktor antaraksi obat (Setiawati, 1995). Berdasar akibat
(luaran), antaraksi ditakrifkan sebagai peristiwa manakala efek obat tertentu
(obat-obyek) diubah oleh obat lain (antaraktan) yang diberikan sebelum atau
bersama-PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
sama dengannya (Hartshorn, 1976; Hussar, 1980; Shinn dan Shrewsbury, 1985 cit
Donatus, 1995).
Suatu antaraksi dikatakan terjadi jika efek suatu obat diubah oleh
kehadiran obat lain, makanan, minuman atau oleh adanya bahan kimia dari
lingkungan. Antaraksi obat dianggap penting secara klinik bila berakibat
meningkatkan toksisitas dan/atau mengurangi efektivitas obat yang berantaraksi,
terutama bila menyangkut obat dengan batas keamanan yang sempit, misalnya
glikosida jantung, antikoagulan, dan obat-obat sitostatik. Demikian juga antaraksi
yang menyangkut obat-obat yang biasa digunakan atau yang sering diberikan
bersama tentu lebih penting daripada obat yang jarang dipakai (Stockley, 1994;
Setiawati, 1995).
2. Jenis
Beberapa istilah yang dapat digunakan untuk menjelaskan efek obat,
yakni: homoergi (sepasang obat menimbulkan efek yang benar-benar sama),
heteroergi (sepasang obat hanya salah satu yang menimbulkan efek tertentu),
homodinami (sepasang obat homoergi dengan mekanisme kerja yang sama), dan
heterodinami (sepasang obat homoergi dengan mekanisme kerja yang berbeda)
(Fingl dan Woodburry, 1970; Martin, 1971 cit Donatus, 1995). Berdasar sifat efek
pasangan obat tersebut antaraksi obat dapat digolongkan menjadi:
homoergi-homodinami yang luaran efeknya berupa penambahan (infra, sederhana atau
supra); homoergi-heterodinami dan heteroergi yang luaran efeknya berupa
6
Berdasarkan mekanisme kerjanya antaraksi obat digolongkan menjadi
dua, yaitu antaraksi farmakokinetika dan antaraksi farmakodinamika (Mutschler,
1986).
a. Antaraksi farmakokinetika.
Suatu peristiwa antaraksi dikatakan merupakan antaraksi
farmakokinetika bila terjadi perubahan farmakokinetika suatu obat (absorpsi,
distribusi, metabolisme atau ekskresi) disebabkan obat lain yang berantaraksi
dengannya (Katzung dan Trevor, 1998).
Dalam proses absorpsi antaraksi obat bisa mengakibatkan perubahan
jumlah obat yang diabsorpsi, baik itu kenaikan maupun penurunan, yang
diakibatkan perubahan harga pH saluran cerna dan pembentukan kompleks atau
khelat, pengubahan waktu pengosongan lambung, kompetisi untuk mekanisme
absorpsi aktif dan perubahan flora usus. Dalam proses distribusi antaraksi bisa
mengakibatkan perubahan kadar obat dalam plasma dengan cara kompetisi pada
ikatan obat-plasma. Dalam proses metabolisme atau biotransformasi antaraksi
dapat mengakibatkan perubahan kecepatan biotransformasi atau metabolisme
yang diakibatkan adanya kompetisi pada reaksi obat-enzim, adanya induksi atau
inhibisi enzim dan perubahan aliran darah hepar (berpengaruh khusus untuk
obat-obat yang dimetabolisme oleh hepar). Dalam proses ekskresi antaraksi dapat
mengakibatkan perubahan jumlah obat yang diekskresikan akibat dari adanya
perubahan pH urin dan persaingan terhadap tempat ikatan carrier.
Dalam lingkup farmakokinetika terdapat beberapa parameter yang dapat
digunakan untuk mengukur atau mengindikasikan adanya perubahan fisiologis
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
dan menerangkan peristiwa antaraksi farmakokinetika. Parameter-parameter
tersebut antara lain: tetapan laju absorpsi (Ka), volume distribusi (Vd), tetapan
laju eliminasi (Ke), waktu paruh dalam plasma atau waktu paruh eliminasi (t1/2),
bersihan atau klirens renal (Clr), bersihan atau klirens hati (Clh), bersihan atau
klirens total (Clt), luas area di bawah kurva kadar dalam plasma (AUC = Area
Under Curve) dan ketersediaan hayati (F) dan kadar obat dalam kondisi tunak
(Css). Parameter-parameter farmakokinetika tersebut diperoleh dari perubahan
konsentrasi bahan obat dan metabolitnya dalam cairan darah dan dalam urin
terhadap waktu (Mutschler, 1986; Setiawati, 1995).
b. Antaraksi farmakodinamika.
Suatu peristiwa antaraksi dikatakan sebagai antaraksi farmakodinamika
bila terjadi perubahan farmakodinamika suatu obat akibat suatu obat lain yang
berantaraksi dengannya (Katzung dan Trevor, 1998). Lebih lanjut dikatakan
antaraksi farmakodinamika terjadi jika dua obat atau lebih bekerja pada reseptor,
tempat kerja atau sistem fisiologik yang sama saling mempengaruhi sehingga
terjadi efek aditif, sinergis atau antagonis (Setiawati, 1995; Harkness, 1984).
Antaraksi farmakodinamika dikatakan bersifat aditif bila efek keseluruhan obat
yang diberikan bersama-sama sebanding dengan penjumlahan kekuatan kerja
masing-masing obat saat diberikan terpisah dengan dosis yang sama. Antaraksi
dikatakan bersifat sinergis bila pada pemakaian bersamaan dua obat atau lebih
efeknya lebih besar dari penjumlahan kekuatan kerja masing-masing obat saat
8
bila pada pemakaian bersamaan dua obat atau lebih efeknya lebih rendah dari
penjumlahan kekuatan kerja masing-masing obat saat diberikan terpisah dengan
dosis yang sama. Selanjutnya, antaraksi dikatakan potensiasi bila kemampuan
suatu obat yang tidak mempunyai efek pada fungsi tertentu dapat meningkatkan
efek obat lain pada fungsi tersebut (Katzung dan Trevor, 1998).
3. Sifat
Antaraksi obat dapat memiliki sifat merugikan atau menguntungkan.
Suatu peristiwa antaraksi obat dikatakan merugikan apabila efek yang ditimbulkan
menyebabkan peningkatan efek yang berlebihan atau peningkatan toksisitas dari
suatu obat. Penurunan efek suatu obat karena peristiwa antaraksi juga tergolong
antaraksi yang merugikan. Sedangkan suatu antaraksi dikatakan menguntungkan
bila efek suatu obat ditingkatkan oleh obat lain (dalam batas aman), atau toksisitas
suatu obat diturunkan karena pemberian bersama-sama dengan suatu obat lain
(Stockley, 1994).
B. Bawang Putih 1. Deskripsi
Bawang putih termasuk familia Liliaceae, merupakan tanaman yang
berasal dari daerah sub-tropis, umumnya ditanam di dataran tinggi yang berhawa
sejuk. Di daerah yang suhu udaranya di atas 250 C pertumbuhan bawang putih
akan terhambat, namun pada daerah dengan suhu udara kurang dari 15o C
pertumbuhan bawang putih akan merana atau umbinya kecil-kecil. Pada
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
perkembangannya beberapa varietas telah beradaptasi dengan tempat tumbuhnya
sehingga dapat hidup di tempat tropis seperti di Indonesia (Anonim, 1986;
Rukmana, 1995).
Struktur morfologi bawang putih terdiri atas: akar, batang utama, batang
semu, tangkai bunga yang pendek atau sama sekali tidak keluar, dan daun
(Rukmana, 1995). Batang semu bawang putih bisa mencapai panjang 30 cm.
Batang semu juga dapat mengalami perubahan bentuk dan fungsi menjadi tempat
penyimpanan cadangan makanan yang disebut “umbi”. Umbi ini terdiri atas
bagian-bagian yang disebut “siung”. Daunnya berbentuk pipih, rata, dengan arah
membujur, lebar daun antara 0,5 hingga 1,5 cm (Leung dan Foster, 1996).
Gambar 1. Bawang Putih (Anonim, 2007)
Di Indonesia dikenal tiga kelompok varietas bawang putih, yaitu:
Kelompok varietas Lumbu Hijau, kelompok varietas Lumbu Kuning, kelompok
10
lokal yang memiliki harapan baik untuk dikembangkan, yaitu: Suren, Jatibarang,
Sanur, Layur, Bagor, Sumbawa, Obleg, Wonosari, No. 2672 dan No. 2850
(Rukmana, 1995).
2. Sinonim
Inggris : Garlic (Inggris); vitlok (Swedia); thoam (Arab); ajo (Spanyol);
commun (Perancis); aglio (Italia); bawang bodas, bawang, bawang putih, bhabang
pote (Jawa); lasuna kebo, lasuna pute (Sulawesi); bawang handak, bawang putieh,
lasum, bawang mental, lasuna, palasuna, bawang hong (Sumatera); kasuna (Bali),
langsuna (Sasak), ncuna (Bima), kalfeofolen (Timor), bawang pulak (Tarakan),
kosai boti (Buru), bawa bodudo (Ternate), bawa fiufer (Irian Jaya) (Anonim,
1986; Anonim, 1995b; Rukmana, 1995).
3. Sistematika
Kerajaan : Plantae
Sub Kerajaan : Tracheobionta
Divisi : Magnoliophyta
Kelas : Liliopsida
Sub Kelas : Liliidae
Bangsa : Liliales
Keluarga : Liliaceae
Marga : Allium L.
Jenis : Allium sativum L. (Anonim, 2002)
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
4. Kandungan kimia
Bawang putih mengandung 0,1 – 0,36 % minyak atsiri, alliin
(S-alil-L-sistein sulfoksida), S-metil-L-(S-alil-L-sistein sulfoksida, enzim-enzim (seperti alliinase,
peroksidase dan mirosinase), ajoene (E,Z-ajoene, E,Z-metilajoene dan
dimetilajoene), protein, mineral-mineral, vitamin-vitamin (tiamin, riboflavin,
niasin), lipid dan asam-asam amino. Minyak atsiri mengandung allisin
(dialilsulfida-S-oksida; dialil tiosulfinat), alilpropil disulfida, dialil disulfida dan
dialil trisulfida sebagai komponen-komponen yang dominan. Beberapa senyawa
yang juga terdapat dalam minyak atsiri namun dalam jumlah yang lebih sedikit
adalah dimetil sulfida, dimetil disulfida, dimetil trisulfida, alilmetil sulfida dan
2,3,4-trithiapentan, tioglikosida dan hormon kelamin (Leung dan Foster, 1996;
Soedibyo, 1998).
S S
S
O
Gambar 2. Struktur kimia Z – Ajoene (Bruneton, 1999)
S
S
S
O
12
5. Kegunaan
Dalam bidang pengobatan bawang putih berguna untuk menurunkan
kadar lipid atau kolesterol dalam darah (untuk pencegahan dan pengobatan
atherosklerosis), hipoglikemik (untuk pencegahan dan pengobatan diabetes),
antibakteri dan antifungi, antitumor, antihepatotoksik (pada tikus), antimikotik
dan antiviral (in vitro dan in vivo), menurunkan viskositas darah, ekspektoran,
diuretic, antitrombotik, analgesik, tonikum, aprodisiaka (perangsang seksual),
mengobati cacingan, mengatasi gigitan binatang atau serangga, tuberkulosis,
rematik, batuk dan pilek, asma, demam, jerawat. (Banerjee dan Maulik, 2002;
Bisset, 1994; Leung dan Foster, 1996; Roser, 1991; Soedibyo, 1998).
6. Efek antitrombotik
Bawang putih memiliki efek antitrombotik dengan mekanisme
penghambatan terhadap enzim siklooksigenase dan enzim lipoksigenase.
(Banerjee dan Maulik, 2002) Penghambatan enzim siklooksigenase menghambat
pengubahan asam arakidonat menjadi tromboksan A2. Tromboksan A2 berfungsi
untuk menstimulasi agregasi trombosit dan terjadinya vasokonstriksi.
Penghambatan pembentukan tromboksan A2 menghambat terjadinya agregasi
trombosit dan vasokonstriksi dalam mekanisme hemostasis. Sedangkan
penghambatan enzim lipoksigenase menghambat pengubahan asam arakidonat
menjadi leukotrien. Leukotrien berperan dalam terjadinya vasokonstriksi.
(Mutschler, 1986) Dengan penghambatan pembentukan leukotrien terjadi
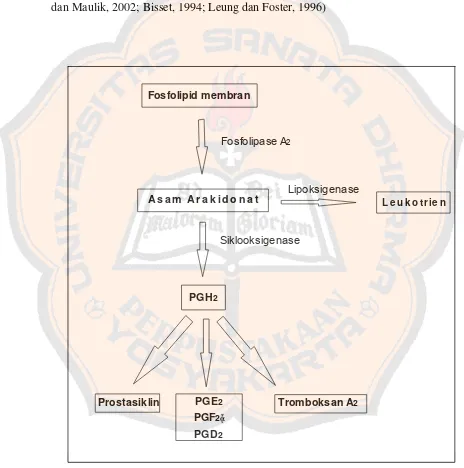
penghambatan vasokonstriksi. Mekanisme ini dapat dilihat secara ringkas dalam
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
gambar 4. Banyak penelitian membuktikan bahwa ajoene adalah senyawa kimia
dalam bawang putih yang memiliki efek antitrombotik. Dialil sulfida dan alilmetil
sulfida juga diduga memiliki aktivitas antitrombotik meski berdasar sebagian
penelitian ditemukan tidak aktif dalam menghambat agregasi trombosit. (Banerjee
dan Maulik, 2002; Bisset, 1994; Leung dan Foster, 1996)
Fosfolipid membran
A s a m A r a k i d o n a t Lipoksigenase L e u k o t r ie n
Siklooksigenase Fosfolipase A2
PGH2
Prostasiklin PGE2 PGF2a
PGD2
Tromboksan A2
Gambar 4. Mekanisme sintesis tromboksan A2 dan leukotrien
14
7. Toksisitas
Penggunaan bawang putih dalam pengobatan perlu diwaspadai terutama
dalam penggunaan bersama-sama dengan obat-obat pengencer darah seperti
warfarin atau heparin karena dapat meningkatkan waktu perdarahan yang
mengakibatkan terjadinya perdarahan pasca operasi. (Fugh-Berman, 2000) Pada
penggunaan bersama-sama dengan aspirin dapat menyebabkan terjadinya tukak
lambung karena penghambatan pada sintesis prostaglandin. Selain itu penggunaan
bersama-sama dengan obat-obat diabetes juga dapat menyebabkan efek yang tidak
diharapkan karena terjadinya peningkatan efek dari obat-obat diabetes oleh
bawang putih. (Graedon dan Graedon, 1997)
C. Darah
Darah tersusun dari unsur seluler darah, yaitu sel darah putih, sel darah
merah dan trombosit, yang tersuspensi di dalam plasma darah. Masing-masing
dari unsur seluler darah ini memegang peranan yang berbeda secara fisiologis. Sel
darah putih terutama berperan dalam mekanisme kekebalan tubuh. Sel darah
merah terutama berperan dalam transpor oksigen di dalam sirkulasi karena
mengandung hemoglobin, suatu protein yang berperan untuk mengikat oksigen,
dan membawanya ke jaringan melalui sistem sirkulasi. Trombosit terutama
berperan dalam penghentian perdarahan dan pembekuan darah. (Ganong, 1998;
Mutschler, 1986)
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
D. Trombosit
Sel ini terbentuk dalam sumsum tulang dan diturunkan dari megakariosit.
Bentuknya lempeng pipih atau cembung dengan panjang 1,5 hingga 4 µm dan
tebal 0,5 hingga 2 µm. Jumlah trombosit di dalam darah secara normal berkisar
antara 150.000 hingga 400.000/ μL darah.
Trombosit memiliki cincin mikrotubulus di sekeliling tepinya dan pada
bagian dalam mengandung organela-organela sitoplasma termasuk di dalamnya
adalah mikrofilamen kontraktil dan beberapa jenis granul yang mengandung
berbagai enzim, fosfolipid, Adenosin difosfat, Adenosin trifosfat, serotonin,
kalsium dan substansi tromboplastik. Lama waktu hidup trombosit dalam darah
adalah 8-10 hari (Candrasoma dan Taylor, 1995; Ganong, 1998; Mutschler, 1986).
Fungsi utama dari trombosit adalah pada proses hemostasis. Pada tahap
awal hemostasis setelah terjadi luka pada pembuluh darah trombosit menyumbat
dan menutup daerah luka pada dinding pembuluh darah. Proses pembentukan
sumbatan trombosit menyangkut 2 mekanisme,yaitu adhesi dan agregasi. Pada
saat terjadi luka pada dinding pembuluh darah trombosit akan melekat pada
kolagen. Peristiwa adhesi ini membutuhkan keberadaan faktor von Willebrand
yang disekresikan oleh sel-sel endothelial ke dalam serum. Selanjutnya terjadi
penggumpalan dan pelepasan granula-granula sitoplasmik. Peristiwa ini disebut
aktivasi trombosit. Degranulasi adalah suatu fenomena aktif yang berkaitan
dengan kontraksi mikroskeleton trombosit yang tergantung pada keberadaan
prostaglandin dan dihambat oleh keberadaan aspirin. Pelepasan granul-granul
16
dan agregasi sejumlah besar trombosit untuk membentuk sumbatan hemostatik
dalam rangka menghentikan perdarahan pada daerah luka. Proses agregasi ini juga
dirangsang oleh faktor pengaktif trombosit (Trombosit Activating Factor), yaitu
suatu sitokin yang disekresikan oleh netrofil, monosit dan trombosit (Candrasoma
dan Taylor, 1995; Ganong, 1998).
E. Pembekuan Darah 1. Hemostasis
Pembuluh darah memiliki suatu sistem yang mampu memelihara
keseimbangan antara mekanisme pembekuan dan peluruhan pembekuan-yang
merupakan reaksi pembatas yang mengimbangi pembekuan darah bila terjadi luka
pada pembuluh darah-yang disebut mekanisme hemostasis. Mekanisme ini
menjadi penting karena dengan demikian lumen pembuluh darah akan tetap bebas
dari pembekuan darah yang terbentuk sebagai respon fisiologis terhadap luka
pembuluh darah. Dalam mekanisme hemostasis ini terlibat beberapa faktor, yaitu
vasokonstriksi lokal, trombosit atau trombosit, koagulasi darah dan fibrinolisis
(Candrasoma dan Taylor, 1995). Vasokonstriksi lokal merupakan suatu metode
yang efektif untuk menutup luka pada pembuluh darah yang kecil namun tidak
pada pembuluh darah yang besar. Trombosit membentuk sumbatan hemostatik
yang menutup tempat luka pada pembuluh darah. Saat terjadi luka pada pembuluh
darah trombosit akan berikatan dengan kolagen dan membentuk agregat yang
membentuk bekuan di pembuluh darah. Pada saat yang sama trombosit
berkontraksi dan melepaskan faktor-faktor yang menstimulasi agregasi trombosit.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Pembekuan darah meliputi pembentukan fibrin dari prekursor plasma. Fibrin dan
trombosit menimbulkan sumbatan hemostatik yang permanen. Fibrinolisis
merupakan mekanisme produksi faktor-faktor seperti plasmin dari prekursor
plasma yang melisiskan dan menyingkirkan fibrin dan fibrinogen dari lumen
pembuluh darah. Skema pembekuan darah dapat dilihat pada Gambar 5.
Luka pada pembuluh darah
↓
Kolagen dari jaringan subendothelial terpapar oleh darah
↓
Adhesi trombosit pada kolagen
↓
Sekresi ADP
↓
Agregasi trombosit
↓
Terbentuk sumbatan trombosit
↓
Kontraksi Trombosit → Pembekuan darah ← Fibrin
Gambar 5. Skema pembekuan darah (Van De Graaff dan Fox, 1995)
Gangguan pada salah satu faktor dalam mekanisme hemostasis tersebut
dapat menyebabkan perdarahan yang abnormal atau trombosis (pembentukan
bekuan di dalam pembuluh darah) yang abnormal. Gangguan tersebut dapat
berasal dari penyakit maupun obat (Candrasoma dan Taylor, 1995; Ganong,
1998).
2. Mekanisme koagulasi darah
Proses koagulasi darah terdiri dari sistem intrinsik dan ekstrinsik. Pada
18
dikatalisis oleh kininogen berberat molekul tinggi menjadi faktor XII aktif (faktor
XIIa). Kininogen berberat molekul tinggi ini juga mengaktivasi prekallikrein
menjadi kallikrein yang juga terlibat dalam proses aktivasi faktor XII menjadi
faktor XIIa. Faktor XIIa mengaktifkan faktor XI (Anteseden tromboplastin
plasma, faktor antihemofilia C) kemudian faktor XI aktif mengaktifkan faktor IX
(faktor Christmas, faktor antihemofilia B). Reaksi yang terakhir ini bergantung
pada keberadaan kalsium. Faktor IX aktif ini kemudian mengaktifkan faktor X
(faktor Stuart-Prower) dengan adanya faktor VIII (faktor antihemofilia A) aktif
yang telah terpisah dari faktor von Willebrand, fosfolipid, dan kalsium. Selain itu
faktor IX aktif ini dapat secara langsung mengaktifkan faktor X. Sistem ekstrinsik
diawali oleh pelepasan tromboplastin jaringan. Tromboplastin merupakan suatu
campuran protein-fosfolipid yang mengaktifkan faktor VII (prokonvertin, faktor
stabil) menjadi faktor VIIa. Tromboplastin jaringan bersama faktor VIIa
mengaktifkan faktor IX dan X. Protrombin (faktor II) dikonversi menjadi trombin
oleh faktor X yang telah diaktifkan dengan adanya faktor V (proakselerin, faktor
labil) sebagai kofaktor, fosfolipid dan kalsium.
Trombin (suatu serin protease) yang terbentuk ini akan mengkatalisis
perubahan fibrinogen menjadi fibrin. Fibrinogen yang merupakan protein plasma
yang larut membebaskan dua pasang polipeptida dari masing-masing molekul
fibrinogen. Hasilnya adalah monomer fibrin yang kemudian akan mengalami
polimerisasi membentuk fibrin. Fibrin mulanya berupa gumpalan longgar
benang-benang yang saling menjalin. Gumpalan longgar ini diubah menjadi agregat yang
padat dan kencang melalui pembentukan ikatan silang kovalen yang dikatalisis
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
oleh faktor XIII (faktor penstabil fibrin) yang telah diaktifkan dan adanya kalsium
(Ganong, 1998; Newland, 1995). Skema mekanisme koagulasi dapat dilihat pada
Gambar 6.
3. Mekanisme antikoagulasi darah
Mekanisme antikoagulasi darah merupakan reaksi-reaksi pembatas yang
mengimbangi terbentuknya koagulasi darah secara in vivo. Reaksi- reaksi ini
cenderung menghambat pembekuan di dalam pembuluh darah dan melisiskan
bekuan yang terbentuk. Reaksi-reaksi ini meliputi antara lain antaraksi antara efek
agregasi trombosit yang dimiliki oleh Tromboksan A2 dan efek antiagregasi
prostasiklin, yang akan mengakibatkan pembentukan bekuan saat pembuluh darah
20
Keterangan: a = bentuk aktif faktor pembekuan HMW = berat molekul tinggi
PL = fosfolipid trombosit
TPL = tromboplastin jaringan
Gambar 6. Mekanisme koagulasi darah (Ganong, 1998)
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
F. Antitrombotik
Antitrombotik adalah senyawa atau obat yang dapat menghambat
agregasi trombosit untuk mencegah terjadinya trombus yang sering ditemukan
pada arteri (Mutschler, 1986).
Inhibitor agregasi trombosit menurunkan pembentukan sinyal-sinyal
kimiawi yang menyebabkan terjadinya agregasi trombosit. Obat-obat yang
menghambat fungsi trombosit diberikan dengan maksud sebagai profilaksi
terhadap terjadinya trombosis di arteri dan pencegahan terhadap serangan jantung.
Obat-obat antiinflamasi non-steroid (AINS), termasuk aspirin, menghambat
agregasi trombosit dan memperpanjang waktu perdarahan (Stringer, 2001).
G. Asetosal 1. Rumus bangun
Asetosal atau asam asetilsalisilat (C9H8O4) atau memiliki bobot molekul
180,16 dengan rumus bangun seperti pada gambar 7.
COOH
OCOCH3
Gambar 7. Rumus bangun asetosal (Anonim, 1995a). 2. Pemerian
Asetosal berupa hablur putih, umumnya seperti jarum atau lempengan
22
pada udara kering dan terhidrolisis secara bertahap pada udara lembab menjadi
asam salisilat dan asam asetat. Asetosal sukar larut dalam air, mudah larut dalam
etanol, kloroform dan eter, namun agak sukar larut dalam eter mutlak (Anonim,
1995a).
3. Kinetika
Asetosal diabsorpsi dengan cepat dalam saluran cerna terutama pada usus
halus dan lambung dan segera terhidrolisis menjadi asam salisilat yang aktif.
Kadar plasma tertinggi asetosal dicapai dalam waktu 14 menit sedangkan kadar
tertinggi asam salisilat dicapai dalam waktu 0,5-1 jam. Waktu paro asetosal
sekitar 17 menit sedangkan waktu paro asam salisilat sekitar 3,15 jam (Purwanto
dan Susilowati, 2000).
4. Kegunaan
Asetosal bermanfaat untuk mencegah kambuhnya infark miokard yang
fatal maupun non fatal, mencegah stroke karena penyumbatan, mencegah
kematian akibat gangguan pembuluh darah dan menurunkan jumlah iskemik
serebral transitorik yang signifikan secara statistik (Mutschler, 1986; Rosmiati dan
Gan, 1995).
5. Efek samping
Efek samping asetosal di antaranya adalah rasa tidak enak pada perut,
rasa mual dan perdarahan saluran cerna. Selain itu asetosal dapat mengganggu
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
hemostasis pada tindakan operasi dan dapat meningkatkan resiko perdarahan bila
diberikan bersama-sama dengan heparin atau antikoagulan oral (Mutschler, 1986)
6. Efek Antitrombotik
Asetosal menghambat agregasi trombosit secara ireversible. Mekanisme
kerjanya diduga dengan asetilasi protein membran trombosit dan protein plasma
serta menghambat enzim siklooksigenase. Akibat adanya penghambatan pada
enzim siklooksigenase sintesis tromboksan A2 dan prostasiklin di dalam
pembuluh darah menjadi tertekan, terutama pada dosis asetosal yang tinggi, yaitu
1-3 gram per hari (Mutschler dan Derendorf, 1995; Mutschler, 1986). Dosis yang
dianjurkan dalam terapi antitrombotik adalah sebesar 325 mg per hari (O’Neill,
2007; Rambe, 2004; Rosmiati dan Gan, 1995). Sebagian tenaga medis
menggunakan rentang antara 75-325 mg per hari (Belder, 2003). Meski demikian
belum jelas dengan dosis yang mana hasil terbaik akan dicapai dengan efek
samping yang kecil (Mutschler, 1986). Beberapa merek sediaan asetosal yang
banyak digunakan dalam pengobatan dan pencegahan trombosis adalah Aspirin®
Regimen Low Dose 81mg, Aspirin® Regimen Regular Dose 325mg,
Aspirin®Protect 100 dan 300mg, Aspirin Cardio®100mg, Ecotrin® Low Strength
81mg dan Ecotrin® Regular Strength 325mg.
H. Metode Uji Efek Antitrombotik
Metode-metode pengujian aktivitas antitrombotik dilakukan dengan
24
darah yang terluka. Pengujian ini bukan untuk pengujian koagulasi darah
melainkan lebih kepada pengujian kemampuan pembuluh darah untuk melakukan
vasokonstriksi dan trombosit untuk membentuk sumbatan hemostatik.
Pada manusia pengujian ini dapat dilakukan dengan cara menghitung
waktu perdarahan pada kulit yang dilukai. Beberapa uji lain yang biasa dilakukan
untuk mengetahui adanya kelainan pada proses hemostasis adalah pengamatan
waktu protrombin (prothrombin time), activated Partial Prothrombin Time
(aPTT), Thrombin Clotting Time (TCT) dan hitung trombosit (Platelets Count).
(Candrasoma dan Taylor, 1995; Yeganeh dan Rad, 2007) Pada hewan percobaan
(tikus) metode yang digunakan untuk mengukur aktivitas antitrombotik adalah
metode Subaqueous Tail Bleeding Time in Rodents (waktu perdarahan ekor pada
hewan pengerat)(Vogel, 2002).
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
I. Landasan Teori
Bawang putih merupakan salah satu bahan yang sangat dikenal oleh
masyarakat baik untuk digunakan dalam masakan sebagai bumbu dan sayuran
maupun dalam pengobatan tradisional. Khasiat bawang putih telah banyak diuji
secara eksperimental dan diakui sebagai bahan multikhasiat sehingga banyak
sediaan bawang putih yang dikembangkan. Salah satu khasiat yang membuat
bawang putih sangat terkenal adalah efeknya pada sistem kardiovaskular, antara
lain mencegah terbentuknya atherosklerosis, menurunkan kadar lipid dalam darah
dan efek antitrombotiknya yang diakui mampu mencegah terjadinya stroke dan
infark miokard. Mekanisme antitrombotik senyawa aktif di dalam bawang putih
menyerupai mekanisme antitrombotik asetosal. (Banerjee dan Maulik, 2002;
Mutschler, 1986)
Asetosal merupakan obat yang digunakan sangat luas di dalam
masyarakat. Penggunaannya terutama adalah sebagai obat analgesik non-narkotik
dan anti-inflamasi. Efek penghambatan agregasi trombosit atau trombosit melalui
penghambatan sintesis tromboksan A2 dan prostasiklin menjadikannya salah satu
obat yang digunakan sebagai obat antitrombotik. (Mutschler, 1986; Rosmiati dan
Gan, 1995)
Pemberian asetosal yang didahului dengan praperlakuan bawang putih
diduga dapat menyebabkan antaraksi karena mekanisme kerjanya yang mirip.
26
J. Hipotesis
Pemberian praperlakuan bawang putih akan memberi pengaruh terhadap
efek antitrombotik asetosal, yaitu peningkatan efek antitrombotik asetosal.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
BAB III.
METODOLOGI PENELITIAN A. Jenis dan Rancangan Penelitian
Penelitian tentang pengaruh praperlakuan bawang putih (Allium sativum
L.) terhadap efek antitrombotik asetosal pada tikus putih betina termasuk jenis
penelitian eksperimental murni dengan rancangan penelitian acak lengkap pola
satu arah.
B. Variabel dan Definisi Operasional
Dalam penelitian ini terdapat variabel utama, yang dijelaskan dengan
definisi operasional; variabel pengacau terkendali dan variabel pengacau tak
terkendali yang mungkin mempengaruhi hasil penelitian, yaitu
1. variabel utama
a. variabel bebas : peringkat dosis praperlakuan bawang putih.
Peringkat dosis adalah tingkatan dosis
perlakuan bawang putih yaitu 32,81 mg/kg
BB; 46,87 mg/kg BB dan 60,94 mg/kg BB
sebelum pemberian asetosal dosis 29,25
mg/kg BB pada tikus putih betina.
b. variabel tergantung : Waktu perdarahan
Waktu perdarahan adalah waktu sejak
28
terbentuknya sumbat primer yang belum stabil,
ditandai dengan berhentinya perdarahan.
2. variabel pengacau terkendali
a. tikus putih sebagai subyek uji adalah galur SD.
b. berat badan dari subyek uji antara 150 sampai dengan 200 gram.
c. jenis kelamin hewan uji, yaitu betina.
d. umur hewan uji, yaitu antara 2-3 bulan.
e. waktu pengamatan, yaitu antara pukul 08.00 – 14.00 WIB.
f. cara pemberian bahan uji, yaitu per oral.
3. variabel pengacau tak terkendali
a. kemampuan absorpsi bawang putih oleh tikus putih.
b. faktor-faktor internal tikus putih yang dapat mempengaruhi waktu
perdarahan.
C. Bahan atau Materi Penelitian
1. bahan utama
a. hewan uji : tikus putih betina galur SD dengan berat badan antara 130
hingga 200 gram umur 2 – 3 bulan, diperoleh dari Laboratorium
Farmakologi Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
b. umbi bawang putih diperoleh dari pasar Beringharjo Yogyakarta pada
tanggal 13 Mei 2004.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
2. bahan kimia
Kecuali dinyatakan lain semua bahan kimia yang digunakan berderajat
pro analisis (produksi Merck), meliputi:
a. asetosal
b. Carboxy Methyl Cellulose (CMC)
c. aquadest yang diperoleh dari Laboratorium Farmakologi Fakultas Farmasi
Universitas Sanata Dharma Yogyakarta
d. larutan NaCl 0,9% (larutan saline) yang diperoleh dari Apotek Sanata
Dharma
D. Alat Penelitian
Peralatan yang digunakan dalam mengerjakan penelitian ini meliputi:
1. alat penyari
a. blender merek Braun
b. kain penyaring
c. neraca analitik merek Mettler Toledo
d. alat-alat gelas (gelas ukur, beaker glass, pipet tetes) merek Pyrex.
2. alat uji efek antitrombotik
a. holder untuk tempat hewan uji
b. stopwatch
c. spuit oral dengan ujung bulat
d. seperangkat alat gelas berupa Beaker glass, pengaduk, pipet tetes,
30
e. gunting
E. Tata Cara Penelitian
1. Penyarian bawang putih
Bawang putih dilumat dengan blender kemudian diperas. Hasil perasan
yang sudah terpisah dari ampaslah yang digunakan untuk perlakuan bawang putih
selama penelitian.
2. Pembuatan kontrol negatif CMC 1%
Bahan berupa serbuk CMC ditimbang seksama seberat 500 mg kemudian
dilarutkan dalam aquadest panas hingga volume 50,0 ml diukur dengan labu ukur
50 ml.
3. Pembuatan suspensi asetosal 1% dalam CMC 1%
Timbang seksama serbuk asetosal seberat 100 mg, gerus. Suspensikan
dalam larutan CMC 1% sebanyak 10,0 ml diukur dengan labu ukur 10 ml.
4. Penentuan dosis asetosal
Dosis asetosal digunakan dosis tertinggi dari rentang dosis yang
direkomendasikan untuk penggunaan asetosal pada manusia sebagai obat
antitrombotik yaitu 325 mg per hari yang kemudian dikonversi ke dosis untuk
tikus didapat hasil sebesar 29,25 mg/kg BB. Dosis diberikan sebagai dosis
tunggal.
5. Penentuan dosis bawang putih
Dosis bawang putih menggunakan acuan dari hasil penelitian Banerjee
dan Maulik tahun 2002 tentang efek antitrombotik bawang putih pada hewan uji
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
kelinci. Hasil penelitian tersebut menyatakan bahwa penghambatan platelet
maksimum terjadi pada dosis 25 dan 100 mg/kg BB. Pada penelitian ini
digunakan dosis 25 mg/kg BB yang dikonversikan ke dosis untuk tikus dan
didapat hasil sebesar 46,87 mg/kg BB. Kemudian untuk mendapatkan peringkat
dosis bawang putih dilakukan penurunan dan peningkatan dosis masing-masing
sebesar 30%. Hasilnya adalah peringkat dosis 32,81 mg/kg BB, 46,87 mg/kg BB
dan 60,94 mg/kg BB.
6. Penentuan waktu pemberian Asetosal
Pada kelompok antaraksi praperlakuan bawang putih asetosal diberikan
15 menit setelah pemberian bawang putih untuk memberi kesempatan bawang
putih terabsorpsi dalam pencernaan hewan uji.
7. Penentuan waktu pemotongan ekor hewan uji
Pada kelompok kontrol negatif dengan CMC 1% dan kelompok
perlakuan suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kgBB
pemotongan ekor hewan uji dilakukan 15 menit setelah pemberian bahan uji
secara per oral. Pada kelompok perlakuan bawang putih pada ketiga peringkat
dosis dan pada kelompok antaraksi praperlakuan bawang putih pada ketiga
peringkat dosis diberi suspensi asetosal dosis 29,25 mg/kgBB pemotongan ekor
hewan uji dilakukan 30 menit setelah pemberian bawang putih secara per oral.
8. Pemilihan hewan uji
Hewan uji yang digunakan dalam penelitian ini adalah tikus putih betina
galur SD yang berumur 2 – 3 bulan dengan berat badan antara 130 hingga 200
32
9. Praperlakuan hewan uji
Semua tikus putih tersebut dipelihara dengan kondisi yang sama
meliputi: pakan, minum, kandang dan alasnya. Sebelum diperlakukan tikus putih
tersebut diadaptasikan pada tempat dan kondisi yang sama sekurang-kurangnya
dua minggu.
10. Perlakuan hewan uji
Lima puluh enam ekor tikus dibagi menjadi delapan kelompok sama
banyak secara acak. Kelompok I adalah kelompok kontrol negatif CMC 1%,
kelompok II adalah kelompok perlakuan suspensi 1% asetosal dalam CMC 1%
dosis 29,25 mg/kg BB. Kelompok III adalah kelompok perlakuan bawang putih
dosis 32,81 mg/kg BB. Kelompok IV adalah kelompok perlakuan bawang putih
dosis 46,87 mg/kg BB. Kelompok V adalah kelompok perlakuan bawang putih
dosis 60,94 mg/kg BB. Kelompok VI adalah kelompok antaraksi praperlakuan
bawang putih dosis 32,81 mg/kg BB diberi suspensi asetosal dosis 29,25 mg/kg
BB. Kelompok VII adalah kelompok antaraksi praperlakuan bawang putih dosis
46,87 mg/kg BB diberi suspensi asetosal dosis 29,25 mg/kg BB. Kelompok VIII
adalah kelompok antaraksi praperlakuan bawang putih dosis 60,94 mg/kg BB
diberi suspensi asetosal dosis 29,25 mg/kg BB. Pemberian bahan uji dilakukan
dengan cara per oral setelah sebelumnya hewan uji dipuasakan. Yang dimaksud
dengan dipuasakan adalah hewan uji tidak diberi makan selama 20-24 jam, namun
tetap diberi minum. Setelah waktu tertentu yang ditetapkan tercapai dilakukan
pemotongan ekor hewan uji untuk mengukur waktu perdarahan.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
11. Penentuan efek antitrombotik
Dikatakan terjadi peningkatan efek antitrombotik jika perbedaan rata-rata
waktu perdarahan kelompok antaraksi bermakna dibanding dengan kelompok
kontrol dan perlakuan.
F. Tata Cara Analisis Hasil
Data yang diperoleh dari perlakuan hewan uji, yaitu waktu perdarahan,
dianalisis secara statistik menggunakan metode ANOVA satu arah dengan taraf
kepercayaan 95% untuk membandingkan rata-rata tiap kelompok uji yang diikuti
dengan uji Scheffe untuk melihat signifikansi perbedaan rata-rata antar kelompok.
Data nilai perubahan rata-rata waktu perdarahan disajikan dalam nilai rata-rata ±
BAB IV.
HASIL DAN PEMBAHASAN A. Uji Pendahuluan
1. Perancangan metode penelitian
Pada awalnya penelitian ini direncanakan menggunakan metode
Subaqueous Tail Bleeding Time Methods in Rodents (waktu perdarahan ekor pada
hewan pengerat). Metode ini secara lengkap adalah sebagai berikut. Obat atau
senyawa uji diberikan kepada hewan uji tikus yang telah dianestesi dan diletakkan
pada pelat dengan suhu terkontrol (37oC) dengan posisi terlentang. Setelah waktu
laten tertentu yang ditetapkan dilakukan pemotongan ekor tikus kira-kira 4
milimeter dari ujung ekor. Segera setelah pemotongan, ekor dicelupkan ke dalam
wadah berisi larutan NaCl 0,9 % (larutan saline) dan diamati perdarahannya serta
dihitung berapa lama waktu yang dibutuhkan hingga perdarahan berhenti. (Vogel,
2002).
Pada saat dilakukan uji pendahuluan terhadap metode ini ditemukan
beberapa kesulitan, yaitu: alat berupa pelat dengan pengontrol suhu dan
pembiusan (anestesi) hewan uji sebelum diberi perlakuan senyawa uji. Kesulitan
alat berupa pelat dengan pengontrol suhu dapat diatasi dengan menggunakan alat
untuk pengujian analgesik metode pelat panas yang terus dikontrol suhunya
dengan termometer. Kesulitan berupa pembiusan (anestesi) hewan uji sebelum
diberi perlakuan senyawa uji sulit untuk diatasi. Pembiusan melalui jalur
intravaskular tidak dilakukan mengingat kemungkinan antaraksi yang terjadi
antara senyawa yang digunakan untuk anastesi dengan senyawa uji. Pembiusan
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
melalui jalur ekstravaskular dilakukan dengan menggunakan uap kloroform
sebagai zat anestesi. Hal ini pun mengalami kesulitan karena kesulitan
penghitungan dosis yang perlu diberikan kepada hewan uji, akibatnya mungkin
terjadi kematian hewan uji atau hewan uji kembali tersadar ketika pengamatan
waktu perdarahan masih berlangsung.
Sebagai upaya pemecahan masalah ini dilakukan pengkajian terhadap
metode ini. Pelat dengan pengontrol suhu yang diatur pada suhu 37o C dan larutan
saline diduga dimaksudkan untuk menjaga kondisi tubuh hewan uji tetap seperti
dalam keadaan sadar dan normal. Pembiusan hewan uji diduga dimaksudkan
untuk mempermudah perlakuan dan pengamatan peneliti terhadap hewan uji.
Untuk memperoleh kondisi tubuh hewan dalam keadaan sadar dan
normal tidak dilakukan anestesi terhadap hewan uji. Sedangkan untuk
mempermudah perlakuan dan pengamatan hewan uji diletakkan di dalam holder.
Penggunaan saline tetap dilakukan untuk menjaga sel-sel yang mengalami luka
pada saat dilakukan pemotongan ekor hewan uji tetap hidup dan mengeliminasi
kemungkinan pengaruh udara dan suhu lingkungan terhadap waktu perdarahan.
36
2. Penentuan dosis asetosal
Dosis asetosal sebesar 325 mg per hari adalah dosis tertinggi yang
direkomendasikan untuk terapi antitrombotik pada manusia. Dosis ini kemudian
dikonversikan ke dosis untuk tikus berat 200 gram dengan bilangan konversi
0,018. Perhitungan konversi tersebut adalah sebagai berikut:
Konversi dosis manusia 70 kg ke tikus 200 g = 0,018
Dosis antitrombotik asetosal tikus (200 g) = 0,018 X 325 mg
= 5,85 mg/ 200 g BB
= 29,25 mg/kg BB.
3. Penyarian bawang putih
Siung bawang putih dilumat dengan blender kemudian diperas. Hasil
perasan yang sudah terpisah dari ampaslah yang digunakan untuk perlakuan
perasan bawang putih selama penelitian. Dari hasil perasan tersebut dihitung
konsentrasi bawang putih yang didapat untuk menentukan volume pemberian
bawang putih kepada hewan uji. Pembuatan bawang putih dilakukan dalam 3
kelompok. Masing-masing kelompok menggunakan siung bawang putih sebanyak
100 gram. Hasil sari bawang putih dari masing-masing kelompok adalah 21, 27
dan 30 ml. Rata-rata hasil sari bawang putih dari ketiga kelompok adalah
3 30 27 21+ +
= 26 ml. Jadi 100 gram siung bawang putih setara dengan 26 ml sari
bawang putih dan 1 ml bawang putih setara dengan 3,846 gram siung bawang
putih. Gambar 9 dan gambar 10 menunjukkan umbi bawang putih yang digunakan
dan hasil perasan bawang putih yang digunakan untuk penelitian.
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
Gambar 9. Umbi Bawang Putih
Gambar 10. Hasil Perasan Bawang Putih
4. Penentuan dosis bawang putih
Dosis bawang putih menggunakan acuan dari hasil penelitian Banerjee
dan Maulik tahun 2002 tentang efek antitrombotik bawang putih pada hewan uji
kelinci. Hasil penelitian tersebut menyatakan bahwa penghambatan platelet
maksimum terjadi pada dosis 25 dan 100 mg/kg BB. Kedua dosis tersebut
dikonversikan ke dosis tikus dengan bilangan konversi 0,25 kemudian dicobakan.
38
Pada uji pendahuluan dengan dosis 187,5 mg/kg BB terjadi perdarahan berlebihan
pada ekor tikus. Uji pendahuluan dosis 46,87 mg/ kg BB memberikan hasil
rata-rata waktu perdarahan 112 detik. Berdasar hasil uji pendahuluan tersebut dipilih
dosis 46,87 mg/ kg BB untuk diujikan pada hewan uji tikus pada penelitian ini.
Kemudian untuk mendapatkan peringkat dosis bawang putih dilakukan penurunan
dan peningkatan dosis masing-masing sebesar 30%. Hasilnya adalah peringkat
dosis 32,81 mg/kg BB, 46,87 mg/kg BB dan 60,94 mg/kg BB.
5. Penentuan selang waktu pemberian asetosal
Bawang putih memberikan hambatan maksimal trombosit pada 0,5
hingga 6 jam (Banerjee dan Maulik, 2002). Kadar plasma tertinggi asetosal
dicapai dalam 14 menit (Purwanto dan Susilowati, 2000). Oleh karena itu dipilih
selang waktu pemberian asetosal adalah 15 menit setelah pemberian bawang
putih.
B. Pengujian Efek Antitrombotik
Bahan uji, yaitu suspensi asetosal dan perasan bawang putih dikatakan
memiliki efek antitrombotik jika memberikan perbedaan rata-rata waktu
perdarahan kelompok uji yang bermakna secara statistik dibandingkan dengan
rata-rata waktu perdarahan kelompok kontrol negatif, yaitu larutan CMC 1%.
Dikatakan terjadi peningkatan efek antitrombotik jika rata-rata waktu
perdarahan kelompok antaraksi praperlakuan asetosal yang diberi perasan bawang
putih berbeda bermakna secara statistik dibanding rata-rata waktu perdarahan
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
kelompok kontrol negatif, kelompok perlakuan suspensi 1% asetosal dalam CMC
1% dan kelompok perlakuan perasan bawang putih.
Pemberian bahan uji kepada hewan uji tikus putih betina galur SD
dilakukan melalui jalur oral menggunakan jarum suntik oral yang berujung bulat.
Pengujian efek antitrombotik yang dilakukan pada kelompok kontrol
negatif CMC 1%, perlakuan suspensi 1% asetosal dalam CMC 1% dosis 29,25
mg/kg BB, perlakuan perasan bawang putih dosis 32,81 mg/kg BB, 46,87 mg/kg
BB dan 60,94 mg/kg BB dan antaraksi praperlakuan perasan bawang putih dosis
32,81 mg/kg BB, 46,87 mg/kg BB dan 60,94 mg/kg BB diberi asetosal dosis
29,25 mg/kg BB memberikan hasil rata-rata waktu perdarahan sebagai berikut:
Tabel I. Rata-rata waktu perdarahan
Kelompok N Rata-rata Waktu Perdarahan (X ± SE) (Detik)
1 7 78,14 ± 3,39
Kelompok 1 : kelompok kontrol negatif CMC 1%
Kelompok 2 : kelompok perlakuan suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB Kelompok 3 : kelompok perlakuan perasan bawang putih dosis 32,81 mg/kg BB
Kelompok 4 : kelompok perlakuan perasan bawang putih dosis 46,87 mg/kg BB Kelompok 5 : kelompok perlakuan perasan bawang putih dosis 60,94 mg/kg BB
Kelompok 6 : kelompok antaraksi praperlakuan perasan bawang putih dosis 32,81 mg/kg BB diberi suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB
Kelompok 7 : kelompok antaraksi praperlakuan perasan bawang putih dosis 46,87 mg/kg BB diberi suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB
Kelompok 8 : kelompok antaraksi praperlakuan perasan bawang putih dosis 60,94 mg/kg BB diberi suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB
40
Kontrol Negatif CMC 1%
Perlakuan Suspensi 1% Asetosal dalam CMC 1% dosis 29,25 m g/ kg BB
Perlakuan Baw ang Putih dosis 32,81 m g/kg BB
Perlakuan Baw ang Putih dosis 46,87 m g/kg BB
Perlakuan Baw ang Putih dosis 60,94 m g/kg BB
Antaraksi Praperlakuan Baw ang Putih dosis 32,81 m g/kg BB diberi asetosal dosis 29,25 m g/kg BB
Antaraksi Praperlakuan Baw ang Putih dosis 46,87 m g/kg BB diberi asetosal dosis 29,25 m g/kg BB
Antaraksi Praperlakuan Baw ang Putih dosis 60,94 m g/kg BB diberi Asetosal dosis 29,25 m g/kg BB
Gambar 11. Diagram Waktu Perdarahan
Data waktu perdarahan tersebut kemudian dianalisis secara statistik
menggunakan metode uji Kolmogorov-Smirnov untuk melihat apakah distribusi
data tersebut normal. Hasil uji Kolmogorov-Smirnov menunjukkan bahwa data
yang diperoleh selama pengujian efek antitrombotik terdistribusi secara normal,
artinya pengujian selanjutnya, yaitu pengujian dengan metode ANOVA satu arah
dapat dilakukan.
Pengujian ANOVA satu arah dengan taraf kepercayaan 95% dilakukan
untuk membandingkan rata-rata waktu perdarahan tiap kelompok uji kemudian
dilanjutkan dengan uji post hoc Scheffe untuk melihat makna perbedaan rata-rata
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
waktu perdarahan antar kelompok uji. Seluruh analisis tersebut dilakukan dengan
menggunakan program statistik SPSS 12.0 for Windows. Dari analisis statistik
menggunakan metode ANOVA satu arah dengan taraf kepercayaan 95% didapat
hasil sebagai berikut:
Tabel II. Hasil Analisis ANOVA satu arah
ANOVA
Waktu Perdarahan
Jumlah
Kuadrat df
Kuadrat
Rata-rata F Sig. Antar Kelompok 1798186,6
96 7 256883,814 66,577 ,000 Dalam Kelompok 185204,85
7 48 3858,435
Total 1983391,5
54 55
Nilai F hasil analisis dibandingkan dengan nilai F tabel pada derajat bebas dan
taraf kepercayaan yang sesuai untuk menentukan apakah ada minimal dua
kelompok uji yang memiliki rata-rata waktu perdarahan berbeda bermakna. F
tabel menunjukkan nilai 2,69, nilai F hasil analisis lebih besar daripada nilai F
tabel, artinya berdasar uji ANOVA satu arah terdapat minimal dua kelompok uji
yang memiliki rata-rata waktu perdarahan berbeda bermakna.
Analisis statistik dilanjutkan dengan uji post hoc, yaitu uji Scheffe. Uji
ini dilakukan untuk mengetahui kelompok uji mana sajakah yang memiliki
42
Tabel III. Hasil Uji Scheffe
B =Berbeda Bermakna TB=Berbeda Tidak Bermakna
Keterangan:
Kelompok 1 : kelompok kontrol negatif CMC 1%
Kelompok 2 : kelompok perlakuan suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB Kelompok 3 : kelompok perlakuan perasan bawang putih dosis 32,81 mg/kg BB
Kelompok 4 : kelompok perlakuan perasan bawang putih dosis 46,87 mg/kg BB Kelompok 5 : kelompok perlakuan perasan bawang putih dosis 60,94 mg/kg BB
Kelompok 6 : kelompok antaraksi praperlakuan perasan bawang putih dosis 32,81 mg/kg BB diberi suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB
Kelompok 7 : kelompok antaraksi praperlakuan perasan bawang putih dosis 46,87 mg/kg BB diberi suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB
Kelompok 8 : kelompok antaraksi praperlakuan perasan bawang putih dosis 60,94 mg/kg BB diberi suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB
Hasil uji Scheffe menunjukkan bahwa rata-rata waktu perdarahan
kelompok kontrol negatif CMC 1% (78,14 ± 3,39 detik) berbeda bermakna
dengan rata-rata waktu perdarahan kelompok perlakuan perasan bawang putih
dosis 46,87 mg/kg BB (320,57 ± 7,62 detik), kelompok perlakuan perasan bawang
putih dosis 60,94 mg/ kg BB (322,14 ± 14,49 detik), kelompok antaraksi
praperlakuan perasan bawang putih pada setiap peringkat dosis, yaitu 32,81 mg/kg
BB, 46,87 mg/kg BB dan 60,94 mg/kg BB diberi suspensi 1% asetosal dalam
CMC 1% dosis 29,25 mg/kg BB (322,14 ± 14,49 detik, 469,85 ± 27,11 detik,
651,00 ± 52,79 detik), tetapi berbeda tidak bermakna dengan rata-rata waktu
perdarahan kelompok perlakuan suspensi 1% asetosal dalam CMC 1% dosis
29,25 mg/kg BB (178,71 ± 16,73 detik) dan kelompok perlakuan perasan bawang
putih dosis 32,81 mg/kg BB (119,57 ± 11,74 detik). Artinya pemberian asetosal
dosis 29,25 mg/kg BB dan perlakuan perasan bawang putih dosis 32,81 mg/kg BB
PLAGIAT MERUPAKAN TINDAKAN TIDAK TERPUJI
tidak memberikan peningkatan rata-rata waktu perdarahan yang bermakna secara
statistik dari asumsi rata-rata waktu perdarahan normal hewan uji yang diwakili
oleh rata-rata waktu perdarahan kelompok kontrol negatif CMC 1%.
Rata-rata waktu perdarahan kelompok perlakuan suspensi asetosal 1%
dalam CMC 1% dosis 29,25 mg/kg BB (178,71 ± 16,73 detik) memiliki
perbedaan yang bermakna dengan rata-rata waktu perdarahan kelompok perlakuan
perasan bawang putih dosis 46,87 mg/kg BB (320,57 ± 7,62 detik), kelompok
perlakuan perasan bawang putih dosis 60,94 mg/ kg BB (322,14 ± 14,49 detik)
dan kelompok antaraksi praperlakuan perasan bawang putih pada setiap peringkat
dosis, yaitu 32,81 mg/kg BB, 46,87 mg/kg BB dan 60,94 mg/kg BB diberi
suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB (322,14 ± 14,49
detik, 469,85 ± 27,11 detik, 651,00 ± 52,79 detik), tetapi berbeda tidak bermakna
dengan rata-rata waktu perdarahan kelompok kontrol negatif larutan CMC 1%
(78,14 ± 3,39 detik) dan kelompok perlakuan perasan bawang putih dosis 32,81
mg/kg BB (119,57 ± 11,74 detik). Dapat dinyatakan bahwa perlakuan dengan
bawang putih dosis 32,81 mg/kg BB tidak memberikan efek antitrombotik yang
lebih besar daripada efek antitrombotik asetosal dosis 29,25 mg/kg BB.
Rata-rata waktu perdarahan pada ketiga kelompok perlakuan perasan
bawang putih, yaitu kelompok perlakuan perasan bawang putih dosis 32,81 mg/kg
BB, dosis 46,87 mg/kg BB dan dosis 60,94 mg/kg BB menunjukkan peningkatan
seiring peningkatan dosis bawang putih. Rata-rata waktu perdarahan kelompok
perlakuan perasan bawang putih dosis 32,81 mg/kg BB adalah 119,57 ± 11,74
44
dosis 46,87 mg/kg BB adalah 320,57 ± 7,62 detik. Rata-rata waktu perdarahan
kelompok perlakuan perasan bawang putih dosis 60,94 mg/kg BB adalah 322,14 ±
14,49 detik. Meskipun demikian, rata-rata waktu perdarahan kelompok perlakuan
perasan bawang putih dosis 46,87 mg/kg BB dan rata-rata waktu perdarahan
kelompok perlakuan perasan bawang putih dosis 60,94 mg/kg BB dinyatakan
berbeda tidak bermakna secara statistik.
Rata-rata waktu perdarahan kelompok perlakuan perasan bawang putih
dosis 32,81 mg/kg BB (119,57 ± 11,74 detik) berbeda tidak bermakna secara
statistik dibandingkan dengan rata-rata waktu perdarahan kelompok kontrol
negatif CMC 1% (78,14 ± 3,39 detik) meskipun menunjukkan perbedaan rata-rata
waktu perdarahan sebesar 41,42 ± 33,20 detik. Dibandingkan dengan kelompok
perlakuan suspensi 1% asetosal dalam CMC 1% dosis 29,25 mg/kg BB (178,71 ±
16,73 detik) juga tidak terdapat perbedaan yang bermakna secara statistik
meskipun terdapat perbedaan rata-rata waktu perdarahan sebesar 59,14 ± 33,20
detik. Dibandingkan dengan rata-rata waktu perdarahan kelompok antaraksi
praperlakuan perasan bawang putih dosis 32,81 mg/kg BB diberi suspensi 1%
asetosal dalam CMC 1% dosis 29,25 mg/kg BB, yaitu 322,14 ± 14,49 detik,
tampak adanya perbedaan bermakna. Artinya pemberian bersama-sama perasan
bawang putih dosis 32,81 mg/kg BB dan asetosal dosis 29,25 mg/kg BB
meningkatkan rata-rata waktu perdarahan yang bermakna secara statistik.
Peningkatan rata-rata waktu perdarahan akibat praperlakuan perasan bawang putih
dosis 32,81 mg/kg BB tersebut sebesar 202,57 ± 33,20 detik atau sebesar kurang
lebih 170%.