51
KINETIKA ENZIMATIS POLIFENOL OKSIDASE YANG TERKANDUNG
DALAM BUAH APEL (MALUS DOMESTICA)
Anceu Murniati*, Buchari, Panji Febriadi Hussein
*Email : [email protected]
ABSTRAK
olifenol oksidase atau polyphenol oxidase(PPO) adalah enzim yang bertanggung jawab atas reaksi pencoklatan pada tanaman akibat adanya kerusakan sel pada tanaman tersebut. PPO telah diisolasi dari buah apel (Malus domestica) dalam bentuk crude-PPO diperoleh dengan cara isolasi dengan hasil yang cukup akurat.Aktivitas PPO dalam crude-PPO apel malang sebesar 47,2892unit/ml terhadap substrat fenol 0,25 mM dalam pelarut bufer fosfat 50 mM pada kondisi optimum pH 7 dan suhu ruang 25°C.
Kata kunci : Buah apel, PPO, fenol, aktivitas PPO. ABSTRACT
Polyphenol oxidase (PPO) is an enzyme which is responsible for the browning reactions in plants due to cell damage in the plant. PPO has been isolated from apple (Malus domestica) in the form of PPO obtained by isolation with a accurate results. PPO activity in crude-PPO apples is 47,2892 unit /mL with 0.25 mM phenol as a substrate, in 50 mM phosphate buffer at optimum pH is 7 and the temperature of 25 ° C.
Keywords: Apple, PPO, phenol, PPO activity. PENDAHULUAN
Reaksi pencoklatan pada kuinon sebagai produk dari oksidasi senyawa fenolik pada tanaman yang dikatalisis PPO ketika tanaman mengalami kerusakan struktur sel (Ho dkk., 1992; Mallick, 2011). PPO mampu mengkatalisis perubahan berbagai senyawa aromatik yang memiliki dua kelompoksenyawa fenolik.Oksidasi kelompok senyawa fenolikmenghasilkan sejumlah produk kuinon. Kuinon tersebut sangat reaktif sehingga dapat bereaksi satu sama lainnya. Hal inilah yang menyebabkan pencoklatansebagai kuinon yang lama kelamaan berwarna bintik-bintik gelap (pigmen coklat tua) sebagai senyawa melanin (Cheng dkk., 2005; Ekinci dkk., 2007;Ho dkk., 1992)yang terjadipada kulit buah, yang sering
membuat buah atau sayuran tidak termakan. Dalam sistem pangan, pencoklatan tersebut menyebabkan kerusakan buah dan sayuran yang mengakibatkan kerugian ekonomi yang besar (Ho dkk., 1992).
Dalam suatu limbah cair indusri tercemar fenol yang toksik, PPO dapat dimanfaatkan sebagai biokatalis proses oksidasi senyawa fenol menjadi kuinon berwarna coklat. Kuinon inilah yang akan berubah menjadi melanin berwarna coklat gelap yang lebih ramah lingkungan. PPO murni tersedia sangat terbatas dan diperoleh dengan biaya relatif mahal. Crude-PPO dapat disintesis dari beberapa bahan pangan seperti buah apel (Malus domestica) (Whitaker, 1994). Aktivitas PPO dapat ditentukan berdasarkan
__________________________________________________________________________________
berkurangnya konsentrasi fenol atau katekol dengan bertambahnya waktu reaksi yang membentuk produk kuinon. Struktur kristal PPO telah dipelajari Klabunde dkk. (1998) dan Kreb dkk.(2004) yang memlikiki sisi aktif katalitik dua atom tembaga dalam proses oksidasi fenol menjadi katekol dan kuinon. Sementara itu mekanisme siklus monofenolase, dan difenolase dipelajari oleh Siegbahn (2004). Dengan demikian, sejumlah aktivitas PPO dapat mendeteksi fenol, katekol dan kuinon dalam suatu sampel larutan yang tercemar fenol. Berdasarkan peneliti sebelumnya telah diperoleh aktivitasPPO dalam crude-PPO apel sebesar 10,14 unit/mL (Murniati dkk., 2014) dengan substrat katekol. Data hasil penelitian ini tentang aktivitas PPO dari crude-PPO apel akan berkontribusi pada pengembangan penelitian, yaitu kinerja PPO lebih efektif dalam oksidasu fenol apabila crude-PPO apel diamobilisasi dalam suatu bahan polimer (Murniati dkk., 2012; Murniati dkk., 2013b).
METODE
Prosedur penelitian sintesis crude PPO-apel dilakukan melalui tiga tahap yaitu preparasi, uji kualitatif dan uji aktivitas PPO (Murniati dkk., 2014). Preparasi sampel yaitu isolasi PPO dari 100 gram buah apel dengan penambahan sejumlah senyawa pengkhelat dalam pelarut bufer fosfat 50 mM pada pH 6 sampai dengan 7 dilakukan homogenasi dan sentrifugasi pada kecepatan 12.000 rpm. Uji kualitatif untuk menandakan terdapat sejumlah PPO dalam crude-apel Malang, dengan penambahan sejumlah substrat fenol dan mengamati waktu reaksi dan perubahan warna. Sementara itu, uji aktivitas PPO dalam crude-PPO apel berdasarkan teknik spektrofotometri (Murniati, 2013a) dengan mengamati laju berkurangnya konsentrasi fenol terhadap
perubahan waktu pada λmax-PPO dan
kurva kalibrasi fenol pada λmax-fenol.
HASIL DAN PEMBAHASAN
Sampel bahan pangan yang digunakan dalam penelitian ini dikenal dengan apel malang yang diperoleh dari pasar tradisional. Apel tersebut telah dikarakterisasi dengan nama apel (Malus domestica). Crude-PPO apel sebelum penambahan substrat fenol Crude-PPO apel setelah penambahan substrat fenol
Gambar 1. Wujud Crude-PPO apel dan reaksi pencoklatan sebagai kuinon setelah penambahan substrat fenol pada crude-PPO apel.
Apel dibuat menjadi crude-PPO apel seperti diperlihatkan pada Gambar 1 yang diperoleh melalui proses homogenasi dengan penambahan sejumlah senyawa pengkhelat (Murniati dkk., 2014) dalam 100 mL pelarut bufer fosfat 50 mM pada rentang pH 6, 6,5 dan 7, lalu disentrifugasi pada kecepatan 12.000 rpm selama 20 menit, sehingga diperoleh filtrat sebagai crude-PPO yang diduga mengandung sejumlah PPO. Hal ini telah diamati melalui perubahan warna menjadi coklat dalam crude-PPO apel dalam waktu reaksi tertentu ketika ditambahkan sejumlah larutan fenol sebagai substrat yang dirangkum dalam Tabel 1. Selama proses uji kualitatif digunakan variasi volume crude-PPO yaitu 2 sampai 5 ml yang dilarutkan dalam bufer fosfat hingga 10 ml. Perubahan warna tersebut terjadi
53
dengan waktu reaksi yang berbeda yaitu 5 ml crude-PPO dengan waktu reaksi pembentukan kuinon paling cepat mencapai 300 detik. Hasil yang diperoleh menunjukan semakin banyak crude-PPO maka semakin cepat perubahan warna terjadi. Hal ini terjadi karena diduga sejumlah unit PPO dalam crude-PPO dengan konsentrasi PPO tinggi. Semakin banyak jumlah unit PPO dalam mengkatalisis substrat fenol dalam proses oksidasi yang menghasilkan pencoklatan berlangsung lebih cepat.
Tabel 1. Peran PPO untuk reaksi pencoklatan sebagai kuinon setelah penambahan substrat fenol 0,25 mL pada crude-PPO apel dalam waktu tertentu volume crude-PPO (ml) volume bufer fosfat (ml) waktu reaksi (detik) 2 8 720 3 7 600 4 6 420 5 5 300
Penentuan laju reaksi PPO sangat efektif diambil dari laju awal karena tahap awal enzim dianggap stabil dan konstan. Pengukuran tergantung pada konsentrasi substrat, jenis enzim, pH, suhu, media, dan ada tidaknya kofaktor serta ion logam. Laju reaksi enzimatis dinyatakan berdasarkan kemiringan kurva dengan berkurangnya konsentrasi substrat terhadap waktu dan bertambahnya konsentrasi substrat terhadap waktu (Maranggoni, 2003).
Pengukuran aktivitas dilakukan variasi pengenceran crude-PPO apel berturut-turut 75 %, 50%, dan 25 % dalam pelarut bufer fosfat. Sementara itu, variasi konsentrasi substrat fenol 0,2; 0,25 dan
0,30 mM pada rentang pH 6,5 s.d. 7,0. Data tersebut diperlihatkan dalam Tabel 2.
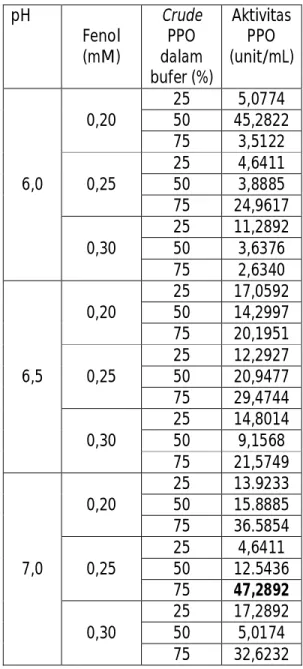
Tabel 2. Aktivitas PPO terhadap substrat fenol 0,2; 0,25 dan 0,3 mM pada rentang pH 6,0; 6,5 sampai 7,0 pH Fenol (mM) Crude PPO dalam bufer (%) Aktivitas PPO (unit/mL) 6,0 0,20 25 5,0774 50 45,2822 75 3,5122 0,25 25 4,6411 50 3,8885 75 24,9617 0,30 25 11,2892 50 3,6376 75 2,6340 6,5 0,20 25 17,0592 50 14,2997 75 20,1951 0,25 25 12,2927 50 20,9477 75 29,4744 0,30 25 14,8014 50 9,1568 75 21,5749 7,0 0,20 25 13.9233 50 15.8885 75 36.5854 0,25 25 4,6411 50 12.5436 75 47,2892 0,30 25 17,2892 50 5,0174 75 32,6232 Semakin encer crude-PPO apel yang terlarut dalam bufer fosfat diduga semakin sedikit sejumlah PPO yang terlibat dalam reaksi katalisis oksidasi fenol. Namun demikian, besarnya aktivitas PPO yang bervariasi dengan perubahan konsentrasi fenol. Hal tersebut mengalami perubahan nilai aktivitas PPO yang
__________________________________________________________________________________
fluktuatif ketika penambahan subsrat fenol dengan konsentrasi berbeda, sedemikian rupa sehingga diperoleh suatu kondisi yang paling optimum dari kombinasi antara crude-PPO dengan konsentrasi fenol. Kondisi optimum peran PPO dalam crude-PPO apel 75% mampu mengkatalisis proses oksidasi fenol 0,25 mM menjadi kuinon dalam bufer fosfat dicapai pada pH 7 dan suhu 25oC dengan aktivitas 47,2892 unit/mL. Hal ini diperlihatkan pula pada Gambar 2.
Gambar 2. Aktivitas PPO sebesar 47,2892 unit/mL terhadap substrat fenol 0,25 mM stabil pada bufer fosfat pH 7 dan suhu 250 C.
KESIMPULAN
Peran PPO dalam crude-PPO apel malang untuk mengkatalisis fenol menjadi kuinon dicapai pada aktivitas 47,2892 unit/ml dengan substrat fenol 0,25 mM yang stabil dalam pelarut bufer fosfat pH 7 dan suhu 250 C.
UCAPAN TERIMAKASIH
Terima kasih kepada Kemenristekdikti atas dukungan danaHibah Penelitian Kompetititf Nasional MasterPlan Percepatan Pembangunan Ekonomi Indonesia (Penprinas-MP3EI) 2014-2015. Terimakasih pula kepada Ketua kelompok Keahlian Laboratorium Kimia Analitik dan Instrumentasi ITB dan Kepala
Laboratorium Farmasi Unjani atas dukungan fasilitas penelitian.
DAFTAR PUSTAKA
Cheng GW, Crisosto CG. (2005): Browning potential, phenolic composition, and polyphenoloxidase activity of buffer extracts of peach and nectarine skin tissue. J. Amer. Soc. Horts. Sct. 120 (5):835-838
Ekinci,O., Boyukbayram., A.E., Kiralp,S., Toppare,L., Yagci, Y. (2007) : Characterization and potential applications of immobilized glucose oxidase and polyphenol oxidase, Journal of Macromolecular Science, Part A: Pure and Applied Chemistry, 44, 801-808.
Ho,C., Lee, C.Y., Huang, M.T. (1992) : Phenolic Compound in Food and Their Effects on Health I : Analysis, Occurence, and Chemistry, ACS Symposium Series, American Chemical Society Washington, DC.
Klabunde,T., Eicken,C., Sacchettini,J.C., Krebs,B. (1998) : Crystal structure of a plant catechol oxidase containing a dicopper center, Nature Structural Biology, 5, 1084 - 1090.
Kreb,B., Merkel,M., Rompel,A. (2004): Catechol oxidase and biometric approaches, The Journal of the Argentine Chemical Society, 92, 1-15. Mallick, M., Mukherjee, K., Udayakumar,
N, A. (2011) : Homology modelling of Polyphenol Oxidase from Stuolanum melongena : Sequence analysis and structural validation studies – in silico. International Journal of Pharma and Bio Sciences, 2,320.
Maranggoni, A.G (2003 ): Enzyme Kinetics: A Modern Approach, John Willey and sons Inc, ISBN: 0-471-15985-9.
Murniati, A., Buchari., Gandasasmita,S., Nurachman, Z., Adimurti, Widayanti, M. (2014): Aktivitas polifenol oksidase
pH 6 pH 7 47.2892 pH optimum
55
dalam buah apel Ceri Malang (Malus domestica) yang Berpotensi untuk Deteksi Fenol, Prosiding SNIJA Unjani-2014, ISBN:978-602-70361-0-9, 93-97. Murniati, A. (2013a). Amobilisasi Polifenol
Oksidase pada film Polipirol secara elektopolimerisasi. Disertasi, ITB, Bandung.
Murniati, A., Buchari., Gandasasmita, S., Nurachman, Z. (2013b) : Kasa baja terlapis polipirol polifenol oksidase, Paten P00201304730.
Murniati, A., Buchari, Gandasasmita, S., Nurachman, Z. (2012): Synthesis and Characterization of Polypyrrole Polyphenol Oxidase (PPy/PPO) on Platinum Elektrode, Research Journal of Pharmaceutical, Biological and Chemical Sciences, 3, 855-859.
Siegbahn,P.E.M (2004) : The catalytic cycle of catechol oxidase, Journal of
Biological Inorganic Chemistry, 12, 1251-1264.
Whitaker, J.R. (1994): Principles of Enzymology for the Food Sciences, Second Edition, Marcell Decker Inc, ISBN: 0-8247-9148-7.
Biodata singkat penulis :
Anceu Murniati adalah dosen tetap pada program studi Kimia FMIPA Unjani dan aktif dalam Kelompok Bidang Keahlian Kimia Fisik dan Anorganik FMIPA Unjani.
Buchari adalah profesor ITB yang mengepalai Kelompok Keahlian Kimia Analitik pada Program Studi Kimia FMIPA ITB.
Panji Febriadi Hussein adalah asisten peneliti yang tergabung dalam Kelompok Bidang Keahlian Kimia Fisik dan Anorganik FMIPA Unjani.