39 BAB IV
HASIL DAN PEMBAHASAN
A. Kemampuan Corynebacterium glutamicum FHCC-0062 dalam mereduksi Perak Nitrat menjadi Nanopartikel Perak
Pembuatan nanopartikel perak dalam penelitian ini menggunakan metode green chemistry dengan cara sintesis menggunakan bakteri. Larutan AgNO3 direduksi Corynebacterium glutamicum FHCC-0062 (Gambar 16). Setelah diamati selama 5 hari, awalnya warna larutan putih susu berubah menjadi kuning kecoklatan yang ditunjukkan oleh Gambar 17.
Gambar 16. Corynebacterium glutamicum FHCC-0062 pada Pengamatan Mikroskopik Perbesaran 1000x
40
Koloid nanopartikel perak hasil reduksi dari larutan AgNO3 berwarna kuning kecoklatan menunjukkan telah terbentuknya nanopartikel perak. Hal tersebut merujuk pada Zielinska et al. (2009: 1566) menyatakan bahwa koloid nanopartikel perak mempunyai warna kuning transparan, krem, hitam, abu-abu, dan ragam warna lainnya. Koloid nanopartikel perak menunjukkan warna berbeda karena penyerapan cahaya dan hamburan di daerah tampak berdasarkan resonansi plasmon. Frekuensi elektron berosilasi dalam menanggapi medan listrik dan terjadi radiasi elektromagnetik, namun hanya elektron bebas seperti Ag yang memiliki resonansi plasmon yang menimbulkan warna intens (Zielinska et al., 2009: 1560). Warna yang muncul tergantung pada bentuk dan ukuran nanopartikel serta konstanta dielektrik dari media (Sneha et al., 2010: 993).
Karakterisasi larutan AgNO3 dan nanopartikel perak dilakukan dengan menggunakan spektrofotometer UV-vis. Menurut Sileikaite et al. (2006: 289) menyatakan bahwa koloid nanopartikel perak memiliki panjang gelombang dengan rentang 350-550 nm pada analisis spektrofotometer UV- Vis. Analisis larutan AgNO3 dan nanopartikel perak pada penelitian ini dilakukan pada panjang gelombang 200-800 nm.
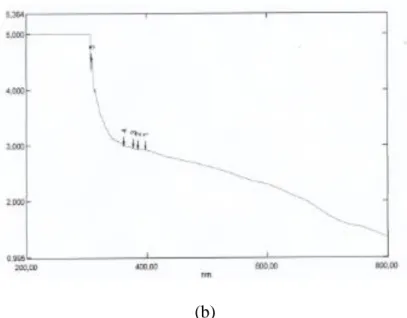
Hasil spektrum UV-Vis pada Gambar 18 (a) menunjukkan ada dua puncak yaitu, absorbansi larutan perak nitrat 0,006 M sebesar 0,016 pada panjang gelombang 305,50 nm, dan 2,743 pada panjang gelombang 224 nm. Hasil spektrum UV-Vis pada Gambar 18 (b) menunjukkan adanya 5 puncak, yaitu absorbansi koloid nanopartikel perak yang sudah direduksi dari larutan AgNO3
41
0,006 M oleh C. glutamicum FHCC-0062 sebesar 2,919 pada panjang gelombang 397,50 nm, 2,937 pada panjang gelombang 385 nm, 2,957 pada panjang gelombang 378 nm, dan 2,999 pada panjang gelombang 362 nm. Solomon et al. (2007: 322) menyatakan bahwa koloid nanopartikel perak dengan panjang gelombang 397,50 nm mempunyai ukuran partikel sebesar 10 sampai 14 nm dan Zielinska et al. (2009: 1565) menyatakan bahwa koloid nanopartikel perak berwarna kuning mempunyai ukuran partikel sebesar 12 nm.
42 (b)
Gambar 18. Spektrum UV-Vis (a) Larutan AgNO3 0,006 M, dan (b) Nanopartikel Perak Hasil Preparasi
C. glutamicum FHCC-0062 mereduksi Ag+ menjadi Ag0 secara ekstraseluler (Li et al., 2011: 4). Sneha mengungkapkan bahwa proses reduksi Ion Ag+ menjadi Ag0 melalui proses biosorbsi dan selanjutnya terjadi bioreduksi. Ion Ag+ tereduksi menjadi ion Ag0 karena, dinding sel C. glutamicum FHCC-0062 terdiri atas senyawa kimia dengan gugus fungsi
karboksilat, hidroksil, amida dan kelompok fosfat dalam berbagai polimer dinding selnya menjadi bersifat anion (Sneha et al., 2010: 991). Anion adalah ion negatif yang terbentuk ketika atom nonlogam memperoleh satu atau lebih elektron. Anion tertarik ke arah anoda (bidang positif) dalam medan listrik, anion bermuatan negatif karena jumlah proton dalam nukleoinya kurang dibandingkan jumlah elektron. Ketika logam kehilangan elektron, ada energi yang diperlukan untuk menghilangkan elektron itu. Elektron dapat menambah kulit terluar pada unsur yang baru (Kharisma Syaefuloh, 2015: 4), sehingga
43
pada proses tersebut terjadi penyerapan ion Ag+ oleh C. glutamicum FHCC-0062.
B. Kemampuan Antibakteri Bahan Tekstil yang dilapisi Nanopartikel Perak terhadap Staphylococcus aureus ATCC 25924 dan Escherichia coli ATCC 35218
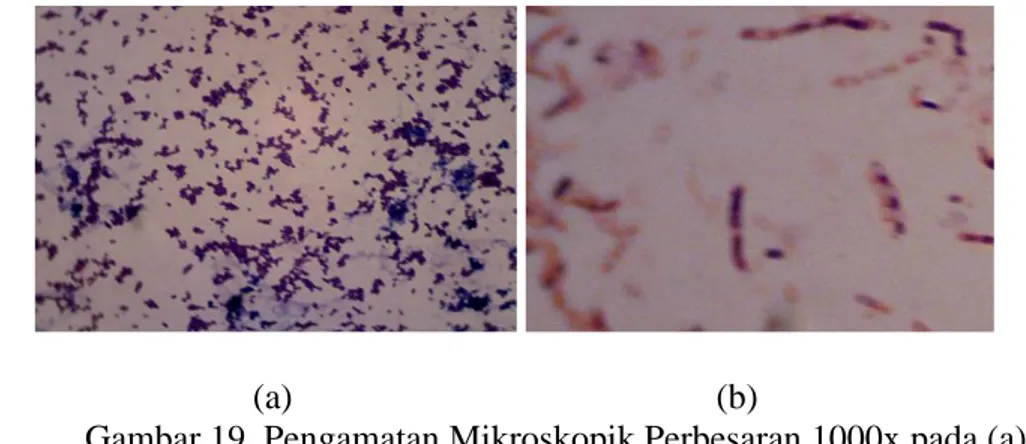
Bahan tekstil katun, nilon, poliester, dan spandek dilapisi dengan nanopartikel perak guna diuji sifat antibakteri pada Staphylococcus aureus ATCC 25924 (Gambar 19 (a)) dan Escherichia coli ATCC 35218 (Gambar 19 (b)). Warna kuning kecoklatan pada sampel bahan tekstil dilapisi nanopartikel perak berasal dari warna koloid nanopartikel perak. Hal tersebut menandakan nanopartikel perak berhasil menempel pada bahan tekstil. Kemampuan antibakteri bahan tekstil dilapisi nanopartikel perak ditunjukkan dengan terbentuknya zona jernih atau zona hambat pada media Nutrient Agar (NA) yang telah diberi suspensi Staphylococcus aureus ATCC 25924 dan Escherichia coli ATCC 35218 seperti yang terlihat pada Gambar 20.
(a) (b)
Gambar 19. Pengamatan Mikroskopik Perbesaran 1000x pada (a) Staphylococcus aureus ATCC 25924 dan (b) Escherichia coli ATCC 35218
44
(a) (b)
(c) (d)
(e) (f)
Gambar 20. Uji zona hambat, (a) kain katun S2, (b) kain nilon S2, (c) kain poliester S2, (d) kain spandek S2, (e) semua kain S1, (f) semua kain S3
45
Tabel 8. Data Zona Hambat Semua Perlakuan pada Bahan Tekstil terhadap S. aureus ATCC 25924 dan E. coli ATCC 35218
Keterangan: S1: bahan tekstil yang tidak dilapisi apapun (kontrol negatif) S2: bahan tekstil yang dilapisi nanopartikel perak
S3: bahan tekstil yang dilapisi kloramfenikol (kontrol positif). U1: ulangan 1
U2: ulangan 2 U3: ulangan 3 Jenis
kain
Perlakuan E. coli ATCC 35218 S. aureus ATCC 25924 Rerata Zona Hambat
Bahan Tekstil
Rerata Zona Hambat Bahan Tekstil U1 U2 U3 Rata2 U1 U2 U3 Rata2 Katun S1 0 0 0 0 0 0 0 0 S2 8,5 8,9 8,1 8,5 7,8 9,5 9,1 8,8 S3 2,2 6,4 6,5 5 6,7 7,4 6,8 6,9 Nilon S1 0 0 0 0 0 0 0 0 S2 9,9 10 7,3 9 8,9 11 7,7 9,2 S3 4,3 6,4 4,4 5 7,3 6,8 6,7 6,9 Poliester S1 0 0 0 0 0 0 0 0 S2 8,8 7,2 9,9 8,6 8,3 9,5 9,7 9,3 S3 6,6 6,7 2,4 5,2 7 7,2 6,7 6,9 Spandek S1 0 0 0 0 0 0 0 0 S2 7,1 6,8 7,4 7,1 7,9 8,8 8,2 8,3 S3 2,3 6,7 2,2 3,7 6,4 6,4 6,9 6,5
46
Gambar 21. Grafik Zona Hambat Semua Perlakuan pada Bahan Tekstil terhadap S. aureus ATCC 25924 berdasarkan Jam Pengamatan
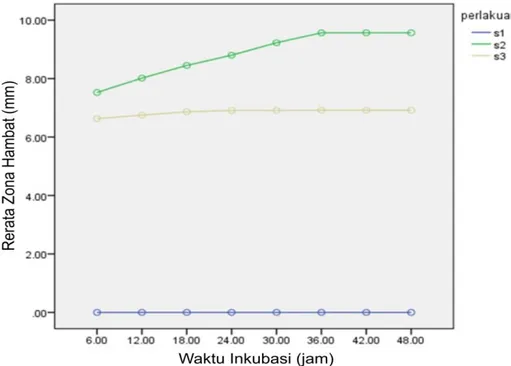
Gambar 22. Grafik Zona Hambat Semua Perlakuan pada Bahan Tekstil terhadap E. coli ATCC 35218 berdasarkan Jam Pengamatan
47
Berdasarkan data pada Tabel 8 diketahui bahwa bahan tekstil dilapisi nanopartikel perak mempunyai aktivitas antibakteri. Rerata diameter zona hambat keempat bahan tekstil antibakteri terhadap S. aureus ATCC 25924 dan E. coli ATCC 35218 menggunakan metode Kirby Bauer pada ketiga bahan uji (S1, S2, S3) memperlihatkan bahan tekstil dilapisi nanopartikel perak mempunyai rata-rata zona hambat paling besar jika dibandingkan pada kontrol negatif maupun kontrol positif seperti terlihat pada Gambar 21 dan Gambar 22. Bahan tekstil tidak dilapisi apapun sebagai kontrol negatif tidak mempunyai aktivitas antibakteri, yang ditunjukkan dengan tidak adanya zona hambat pada semua sampel kain terhadap S. aureus ATCC 25924 dan E. coli ATCC 35218. Bahan tekstil dilapisi kloramfenikol sebagai kontrol positif menunjukkan adanya zona hambat, tetapi rerata zona hambatnya masih di bawah rerata zona hambat bahan tekstil dilapisi nanopartikel perak.
Berdasarkan Gambar 21 diketahui bahwa zona hambat bahan tekstil katun, nilon, poliester, spandek dilapisi nanopartikel perak terhadap Staphylococcus aureus ATCC 25924 dari pengamatan jam ke-6 hingga jam ke-36 terus mengalami peningkatan dan jam ke-36 hingga jam ke-48 mempunyai rerata zona hambat sama. Berdasarkan Gambar 22 diketahui bahwa zona hambat bahan tekstil katun, nilon, poliester, spandek dilapisi nanopartikel perak terhadap Escherichia coli ATCC 35218 dari pengamatan jam ke-6 hingga jam ke-42 mengalami peningkatan dan jam ke-48 mempunyai nilai sama dengan jam ke-42. Peningkatan diameter zona hambat merupakan aktivitas eksponensial bakteri, sedangkan zona hambat mengalami stagnasi karena
48
koloni bakteri sudah dalam posisi death cell program (Kane dan Kandel, 2006: 385).
Tabel 9. Analisis ANOVA Bahan Tekstil dilapisi Nanopartikel Perak terhadap S. aureus ATCC 25924 dan E. coli ATCC 35218
Df mean square F Sig. Di antara grup 7 11,866 9,433 ,000 Di dalam grup 184 1,258
Selanjutnya, dikarenakan penelitian ini menggunakan disain rancangan acak lengkap, maka untuk melihat pengaruh variasi bahan tekstil yang dilapisi nanopartikel perak terhadap zona hambat pada bakteri uji S. aureus ATCC 25924 dan E. coli ATCC 35218, maka perlu dilakukan analisis ANOVA menggunakan program SPSS. Hasil uji one way ANOVA dengan taraf 5% dapat dilihat pada Tabel 9. Uji one way ANOVA menunjukkan nilai F hitung sebesar 9,433 dengan Sig. = 0,000. Oleh karena nilai sig. < 0,05 maka Ho (ρ = 0) ditolak (I Putu Sampurna dan Tjokorda Sari Nindhia, 2013: 40), yang artinya variasi bahan tekstil dilapisi nanopartikel perak secara simultan memiliki pengaruh yang signifikan terhadap zona hambat pada bakteri uji S. aureus ATCC 25924 dan E. coli ATCC 35218.
Tabel 10. Hasil uji lanjut LSD Semua Perlakuan pada Bahan Tekstil terhadap S. aureus ATCC 25924 dan E. coli ATCC 35218
Perlakuan Perbedaan Rerata Zona Hambat S1 terhadap S2 dan S3 Signifikan
S2 terhadap S1 dan S3 Signifikan S3 terhadap S1 dan S2 Signifikan
Berdasarkan uji lanjut LSD (Least Significance Different) dengan taraf 5%, yang digunakan untuk menguji beda nyata antar beberapa rerata zona
49
hambat pada semua perlakuan pada bahan tekstil terhadap S. aureus ATCC 25924 dan E. coli ATCC 35218 dapat dilihat pada Tabel 10. Bahan tekstil yang tidak dilapisi mempunyai perbedaan zona hambat yang signifikan terhadap bahan tekstil dilapisi nanopartikel perak dan bahan tekstil dilapisi kloramfenikol. Bahan tekstil yang dilapisi nanopartikel perak mempunyai perbedaan zona hambat yang signifikan terhadap bahan tekstil tidak dilapisi dan bahan tekstil dilapisi kloramfenikol. Bahan tekstil yang dilapisi kloramfenikol mempunyai perbedaan zona hambat yang signifikan terhadap bahan tekstil dilapisi nanopartikel perak dan bahan tekstil tidak dilapisi. Hal tersebut dapat bermakna bahwa bahan tekstil dilapisi nanopartikel perak mempunyai pengaruh antibakteri yang nyata terhadap kedua bakteri uji tersebut.
Menurut Song et al. (2006: 58), mekanisme antibakteri dapat dijelaskan melalui interaksi nanopartikel perak mendekat pada membran sel bakteri uji selama proses difusi sel berjalan dan masuk ke dalam sel bakteri. Nanopartikel perak berinteraksi dengan membran sel bakteri yang mengandung protein dengan gugus fungsi sulfhidril sebagai komponen utamanya, kemudian senyawa perak menyerang rantai metabolisme bakteri, dan juga berinteraksi dengan molekul DNA hingga pada akhirnya sel bakteri mengalami kerusakan dan mengalami kematian.
Feng et al. (2000: 668), melaporkan bahwa mekanisme penghambatan nanopartikel perak terhadap pertumbuhan Staphylococcus aureus dan Escherichia coli dapat terjadi karena ion perak berpengaruh terhadap
50
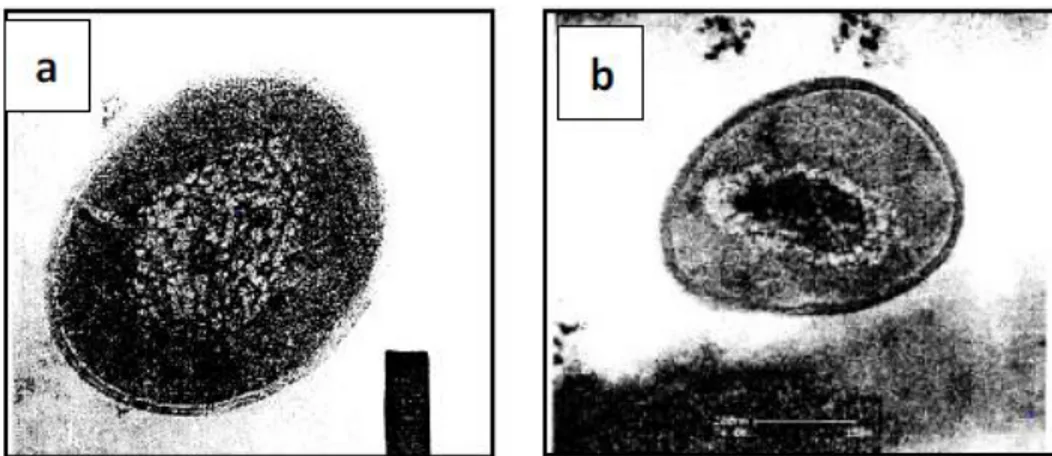
denaturasi protein dan menyebabkan molekul DNA bakteri menjadi kental dan bakteri kehilangan kemampuan untuk melakukan replikasi. Pengamatan langsung menunjukkan adanya perubahan morfologi dan struktur baik pada bakteri Staphylococcus aureus maupun bakteri Escherichia coli setelah perlakuan dengan nanopartikel perak dapat dilihat pada Gambar 23 dan 24. Bakteri Staphylococcus aureus dan Escherichia coli sehat memiliki molekul DNA tersebar acak pada hampir seluruh bagian sel. Sel bakteri Staphylococcus aureus dan Escherichia coli diberi perlakuan dengan nanopartikel perak memiliki DNA menggumpal pada bagian tepi sel. Gumpalan DNA tersebut terbentuk akibat adanya interaksi yang terjadi antara ion Ag0 dengan molekul DNA. Hal tersebut yang mungkin menyebabkan nanopartikel perak dapat menghambat pertumbuhan bakteri S. aureus ATCC 25924 dan E. coli ATCC 35218.
Gambar 23. Bakteri staphylococcus aureus pada Pengamatan SEM (a) Bakteri Sehat dan (b) Bakteri yang diberi Nanopartikel Perak (Feng
51
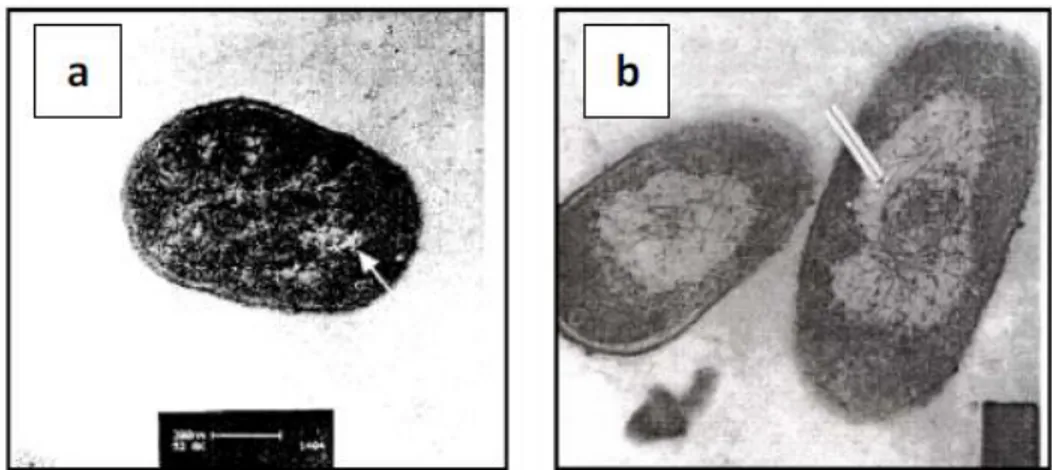
Gambar 24. Bakteri Escherichia coli pada Pengamatan SEM (a) Bakteri Sehat, dan (b) Bakteri yang diberi Nanopartikel Perak (Feng
et al., 2000: 664).
Aktivitas antibakteri bahan tekstil dilapisi nanopartikel perak terhadap Staphylococcus aureus ATCC 25924 menunjukkan rerata zona hambat lebih besar dibandingkan dengan Escherichia coli ATCC 35218 dapat dilihat pada Tabel 8. Hal tersebut tidak sesuai dengan pernyataan Cappuccino dan Sherman (2001: 385) bahwa bakteri gram negatif memiliki viabilitas lebih rendah dibandingkan dengan bakteri gram positif.
Perbedaan pernyataan Cappuccino dan Sherman (2001: 385) dengan hasil penelitian ini karena sel E. coli cepat dan mudah tumbuh, memiliki kemampuan tinggi dalam menyesuaikan diri terhadap lingkungan, serta menunjukakkan resistensi dan kekebalan terhadap beberapa zat antibakteri (M. H. Anshari, 2011: 27). Selain itu, M. H. Anshari (2011: 46) menyatakan bahwa S. aureus hanya mempunyai membran plasma tunggal yang dikelilingi dinding sel tebal berupa petidoglikan. Sekitar 90% dari dinding sel tersebut tersusun atas peptidoglikan, sedangkan sisanya berupa molekul lain berupa asam teikhoat. Di sisi lain E. coli memiliki sistem membran ganda, dimana membran
52
plasmanya diselimuti oleh membran luar permeabel. E. coli mempunyai dinding sel tebal berupa peptidoglikan, yang terletak di antara membran luar dan membran dalam, sehingga partikel nanopartikel perak lebih mudah melakukan difusi pada S. aureus, karena mempunyai hambatan lebih kecil dimana sel bakteri tersebut sebagian besar tersusun oleh plasma tunggal dibandingkan dengan E. coli.
Berdasarkan deskripsi tersebut dapat disimpulkan bahwa aktivitas antibakteri pada bahan tekstil dilapisi nanopartikel perak termasuk dalam aktivitas bakteriosidal berspektrum luas. Aktivitas bakteriosidal adalah aktivitas antibakteri yang membunuh bakteri patogen dalam kisaran luas (Michael et al., 2009: 786) dan antibakteri berspektrum luas yaitu antibakteri dapat menghambat atau membunuh bakteri dari golongan gram positif maupun gram negatif (Sylvia T. Pratiwi, 2008: 154). Hal tersebut dibuktikan dengan bahan tekstil dilapisi nanopartikel perak dalam membentuk zona hambat pada bakteri uji Staphylococcus aureus ATCC 25924 dan Escherichia coli ATCC 35218. Aktivitas bakteriosidal berspektrum luas pada bahan tekstil dilapisi nanopartikel perak dipengaruhi oleh ukuran partikel nano, dalam penelitian ini nano yang digunakan dimungkinkan berukuran 12 nm. Menurut Agus Haryono dan Sri Budi Harmami (2010: 4), aktivitas antibakteri pada nanopartikel perak didukung oleh luas permukaan partikel besar, sehingga memungkinkan terjadinya kontak sangat baik dengan mikroorganisme. Antimikroba partikel perak dipengaruhi oleh ukuran partikel, semakin kecil ukuran partikel semakin besar efek antimikroba (Cheng, Karim, dan Seow, 2003: 666).
53
C. Perbedaan Aktivitas Antibakteri di antara Kain Katun, Nilon, Poliester, dan Spandek yang dilapisi Nanopartikel Perak terhadap Staphylococcus aureus ATCC 25924
Mekanisme bakteriosidal bahan tekstil dilapisi nanopartikel perak terhadap pertumbuhan S. aureus ATCC 25924 adalah ion Ag0 berpengaruh terhadap molekul DNA bakteri, sehingga bakteri kehilangan kemampuan replikasi. Ion Ag0 juga berinteraksi dengan tiol dari protein, yang dapat menyebabkan inaktivasi protein bakteri. Selain itu, terdapat gugus –COOH dan gugus –NH2 pada protein yang dapat bereaksi dengan ion logam dan membentuk senyawa antiprotein, sehingga protein mengalami denaturasi (Feng et al., 2000: 669).
Gambar 25. Grafik Zona Hambat Bahan Tekstil dilapisi Nanopartikel Perak terhadap S. aureus ATCC 25924 berdasarkan Jenis Bahan Tekstil Berdasarkan grafik pada Gambar 25 diketahui bahwa bahan tekstil mempunyai daya hambat paling besar terhadap S. aureus ATCC 25924 adalah
54
kain nilon, kemudian poliester, katun, dan yang terkecil adalah kain spandek. Perbedaan zona hambat pada bahan tekstil katun, nilon, poliester, dan spandek terhadap S. aureus ATCC 25924 disebabkan oleh perbedaan banyak sedikitnya celah pada serat kait. Semakin banyak celah maka nanopartikel perak yang tertempel semakin banyak. Selain itu, disebabkan ada tidaknya pasangan elektron bebas pada gugus fungsi polimer bahan tekstil katun, nilon, poliester, dan spandek. Pasangan elektron bebas tersebut akan berikatan kovalen kordinasi dengan nanopartikel perak. Ikatan kovalen kordinasi terjadi dengan cara pemakaian bersama pasangan elektron yang berasal dari salah satu atom pasangan elektron bebas pada kain, sedangkan nanopartikel perak (Ag0) hanya menyediakan orbital kosong yang menerima pasangan elektron yang dan digunakan bersama (Wulan Yunianingsih dan Suyono, 2013: 4).
Bahan tekstil nilon mempunyai struktur kimia berupa rantai senyawa panjang poliamida sintetik dengan gugus berulang -CONH sebagai suatu bagian terpadu dari rantai polimernya. Gugus –CONH dalam nilon mempunyai pasangan elektron bebas pada atom O dan N, sehingga kemungkinan mengikat nanopartikel perak lebih banyak. Selain itu, serat poliamida mempunyai penampang melintang paling umum adalah bentuk trilobal dan bulat dapat dilihat pada Gambar 4. Bentuk trilobal dan bulat menyebabkan banyaknya celah antar serat pada kain nilon (Noerati dkk., 2013: 19), sehingga nanopartikel perak banyak menempel pada celah antar kain nilon. Berdasarkan Gambar 25 diketahui bahwa zona hambat kain nilon lebih besar dari pada poliester, katun, dan spandek. Hal tersebut karena nilon mempunyai pasangan
55
elektron bebas pada atom O dan N, sedangkan poliester dan katun hanya mempunyai pasangan elektron bebas pada atom O serta spandek tidak mempunyai pasangan elektron bebas.
Poliester merupakan serat buatan manusia tersusun atas gugus fungsi bersifat elektronegativitas berupa –COO. Gugus –COO mempunyai pasangan elektron bebas pada atom O yang berinteraksi dengan nanopartikel perak membentuk ikatan –OAg. Secara umum serat poliester berbentuk silinder lurus untuk penampang membujur dan bulat untuk penampang melintangnya dapat dilihat pada Gambar 6. Serat berbentuk silinder lurus untuk penampang membujur dan bulat untuk penampang melintangnya menyebabkan banyaknya celah antar serat pada kain poliester (Noerati dkk., 2013: 17), sehingga nanopartikel perak banyak yang menempel pada celah antar kain poliester. Berdasarkan Gambar 25 diketahui bahwa zona hambat poliester lebih kecil dari pada nilon, akan tetapi perbedaan itu tidak signifikan. Perbedaan yang tidak signifikan dimungkinkan karena kain nilon dan poliester sama-sama mempunyai celah antar serat yang banyak.
Kain katun bersumber dari serat kapas dengan kandungan utama adalah selulosa. Katun memiliki gugus bersifat elektronegativitas berupa –OH, artinya katun mempunyai pasangan elektron bebas pada atom O yang dapat berinteraksi dengan nanopartikel perak membentuk membentuk ikatan –OAg. Morfologi serat kapas jika dilihat di bawah mikroskop mempunyai penampang membujur seperti pita terpilin dan penampang melintang seperti ginjal dengan lubang ditengah disebut lumen seperti yang terlihat pada Gambar 2.
56
Penampang membujur seperti pita terpilin dan penampang melintang seperti ginjal menyebabkan banyaknya celah antar serat pada kain katun (Noerati dkk., 2013: 7). Berdasarkan Gambar 25 diketahui bahwa katun mempunyai rerata zona hambat lebih rendah dari nilon dan poliester. Hal tersebut karena permukaan katun besar dan kemampuannya menjaga kelembaban, serta bersifat hidrofilik menjadikan kain katun sebagai media yang baik untuk pertumbuhan mikroorganisme (Agus Haryono dan Sri Budi Harmami, 2010: 5).
Spandek merupakan serat buatan berpolimer yang mempunyai ciri khas adanya gugus fungsi uretan (NHCOO) dalam rantai utama polimer. Gugus -NHCOO pada spandek tidak mempunyai pasangan elektron bebas. Hal tersebut terjadi karena kemungkinan adanya interaksi di antara rantai polimer pada spandek. Spandek mempunyai penampang membujur silinder lurus dan penampang melintang berbentuk tulang anjing, ketika dibuat benang permukaan antar serat cenderung menempel satu sama lain, seperti yang terlihat pada Gambar 8. Permukaan antar serat cenderung menempel satu sama lain menyebabkan jumlah celah antar serat sedikit (Noerati, dkk., 2013: 23). Berdasarkan Gambar 25 diketahui bahwa spandek mempunyai rerata zona hambat paling rendah di antara nilon, poliester, dan katun. Hal tersebut karena permukaan antar serat spandek cenderung menempel satu sama lain menyebabkan sedikitnya celah antar serat dan tidak adanya pasangan elektron bebas pada gugus fungsi uretan, sehingga nanopartikel perak yang menempel pada serat kain spandek lebih sedikit dari nilon, poliester, dan katun.
57
Tabel 11. Hasil uji lanjut LSD Zona Hambat Bahan Tekstil dilapisi Nanopartikel Perak terhadap S. aureus ATCC 25924
Bahan Tekstil Perbedaan Rerata Zona Hambat Katun terhadap Nilon Tidak signifikan
Katun terhadap Poliester Tidak signifikan Katun terhadap Spandek Signifikan Nilon terhadap Katun Tidak signifikan Nilon terhadap Poliester Tidak signifikan Nilon terhadap Spandek Signifikan Poliester terhadap Katun Tidak signifikan Poliester terhadap Nilon Tidak signifikan Poliester terhadap Spandek Signifikan Spandek terhadap Katun Signifikan Spandek terhadap Nilon Signifikan Spandek terhadap Poliester Signifikan
Kain katun, kain nilon, dan kain poliester dilapisi nanopartikel perak mempunyai perbedaan rerata zona hambat yang signifikan terhadap kain spandek dilapisi nanopartikel perak begitupun sebaliknya, sedangkan di antara kain katun, kain nilon, dan kain poliester dilapisi nanopartikel perak perbedaan zona hambatnya tidak signifikan seperti terlihat pada Tabel 11. Katun, nilon, poliester menunjukkan hasil uji perbedaan zona hambat tidak signifikan dikarenakan jenis kain tersebut mempunyai gugus fungsi bersifat elektronegativitas yang terdapat pasangan elektron bebas dan sama-sama mempunyai banyak celah antar seratnya. Spandek menunjukkan perbedaan rerata zona hambat signifikan di antara katun, nilon, poliester karena spandek tidak mempunyai pasangan elektron bebas dalam gugus fungsinya dan mempunyai sedikit celah antar seratnya.
D. Perbedaan Aktivitas Antibakteri di antara Kain Katun, Nilon, Poliester, dan Spandek yang dilapisi Nanopartikel Perak terhadap Escherichia coli ATCC 35218
58
Mekanisme bakteriosidal nanopartikel perak terhadap pertumbuhan Escherichia coli adalah ion Ag0 berpengaruh terhadap molekul DNA bakteri, sehingga DNAnya menggumpal pada bagian tepi sel. Gumpalan DNA tersebut terbentuk akibat adanya interaksi yang terjadi antara ion Ag0 dengan molekul DNA. Hal tersebut menyebabkan nanopartikel perak dapat menghambat pertumbuhan E. coli ATCC 35218 perak (Feng et al., 2000: 664).
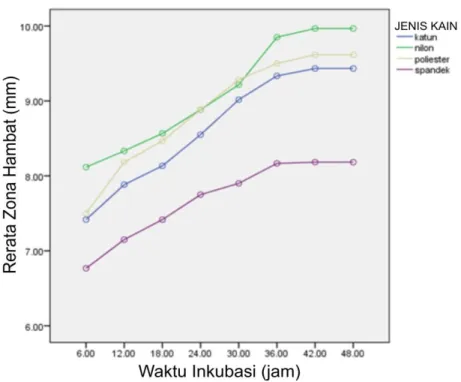
Gambar 26. Grafik Zona Hambat Bahan Tekstil dilapisi Nanopartikel Perak terhadap E. coli ATCC 35218 berdasarkan Jenis Bahan Tekstil Berdasarkan grafik pada Gambar 26 diketahui bahwa bahan tekstil mempunyai daya hambat paling besar terhadap E. coli ATCC 35218 adalah kain nilon, kemudian poliester, katun, dan yang terkecil adalah kain spandek. Perbedaan zona hambat pada bahan tekstil katun, nilon, poliester, dan spandek terhadap E. coli ATCC 35218 disebabkan oleh perbedaan banyak sedikitnya celah pada serat kait. Semakin banyak celah maka nanopartikel perak yang
59
tertempel semakin banyak. Selain itu, disebabkan ada tidaknya pasangan elektron bebas pada gugus fungsi polimer bahan tekstil katun, nilon, poliester, dan spandek. Pasangan elektron bebas tersebut akan berikatan kovalen kordinasi dengan nanopartikel perak. Ikatan kovalen kordinasi terjadi dengan cara pemakaian bersama pasangan elektron yang berasal dari salah satu atom pasangan elektron bebas pada kain, sedangkan nanopartikel perak (Ag0) hanya menyediakan orbital kosong yang menerima pasangan elektron yang dan digunakan bersama (Wulan Yunianingsih dan Suyono, 2013: 4).
Kain nilon mempunyai daya hambat paling besar terhadap E. coli ATCC 35218 karena bentuk serat nilon trilobal dan bulat dapat dilihat pada Gambar 4. Bentuk trilobal dan bulat menyebabkan banyaknya celah antar serat pada kain nilon, sehingga nanopartikel perak banyak menempel pada celah antar kain nilon. Selain itu, gugus –CONH dalam nilon mempunyai pasangan elektron bebas pada atom O dan N, sehingga kemungkinan mengikat nanopartikel perak lebih banyak (Noerati dkk., 2013: 19). Berdasarkan Gambar 26 diketahui bahwa zona hambat kain nilon lebih besar dari pada poliester, katun, dan spandek. Hal tersebut karena nilon mempunyai pasangan elektron bebas pada atom O dan N, sedangkan poliester dan katun hanya mempunyai pasangan elektron bebas pada atom O serta spandek tidak mempunyai pasangan elektron bebas.
Poliester mempunyai daya hambat terbesar ke dua terhadap E. coli ATCC 35218 karena serat poliester berbentuk silinder lurus dan bulat dapat dilihat pada Gambar 6. Serat berbentuk silinder lurus untuk penampang membujur dan
60
bulat untuk penampang melintangnya menyebabkan banyaknya celah antar serat pada kain poliester, sehingga nanopartikel perak banyak yang menempel pada celah antar kain poliester. Selain itu, gugus
–COO dalam poliester mempunyai pasangan elektron bebas pada atom O yang berinteraksi dengan nanopartikel perak membentuk ikatan –OAg (Noerati dkk., 2013: 17).
Katun mempunyai daya hambat terbesar ke tiga terhadap E. coli ATCC 35218 karena serat katun berbentuk seperti pita terpilin dan seperti ginjal dengan lubang ditengah disebut lumen seperti yang terlihat pada Gambar 2. Penampang membujur seperti pita terpilin dan penampang melintang seperti ginjal menyebabkan banyaknya celah antar serat pada kain katun. Selain itu, katun memiliki gugus –OH yang mempunyai pasangan elektron bebas pada atom O. Atom O dapat berinteraksi dengan nanopartikel perak membentuk ikatan –OAg (Noerati dkk., 2013: 7). Berdasarkan Gambar 26 diketahui bahwa katun mempunyai rerata zona hambat lebih rendah dari nilon dan poliester. Hal tersebut karena permukaan katun besar dan kemampuannya menjaga kelembaban, serta bersifat hidrofilik menjadikan kain katun sebagai media yang baik untuk pertumbuhan mikroorganisme (Agus Haryono dan Sri Budi Harmami, 2010: 5).
Spandek mempunyai daya hambat terkecil terhadap E. coli ATCC 35218 karena serat spandek berbentuk silinder lurus, ketika dibuat benang, permukaan antar serat cenderung menempel satu sama lain, seperti yang
61
terlihat pada Gambar 8. Permukaan antar serat cenderung menempel satu sama lain menyebabkan jumlah celah antar serat sedikit. Selain itu, gugus
-NHCOO pada spandek tidak mempunyai pasangan elektron bebas. Hal tersebut terjadi karena kemungkinan adanya interaksi di antara rantai polimer pada spandek (Noerati, dkk., 2013: 23).
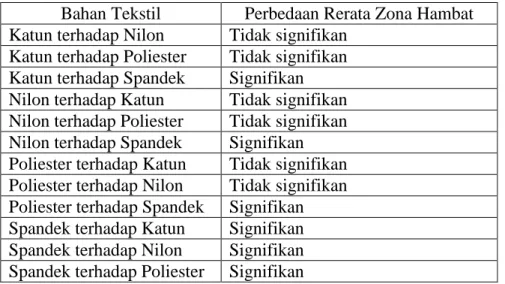
Tabel 12. Hasil uji lanjut LSD Zona Hambat Bahan Tekstil dilapisi Nanopartikel Perak terhadap E.coli ATCC 35218
Bahan Tekstil Perbedaan Rerata Zona Hambat Katun terhadap Nilon Tidak signifikan
Katun terhadap Poliester Tidak signifikan Katun terhadap Spandek Signifikan Nilon terhadap Katun Tidak signifikan Nilon terhadap Poliester Tidak signifikan Nilon terhadap Spandek Signifikan Poliester terhadap Katun Tidak signifikan Poliester terhadap Nilon Tidak signifikan Poliester terhadap Spandek Signifikan Spandek terhadap Katun Signifikan Spandek terhadap Nilon Signifikan Spandek terhadap Poliester Signifikan
Kain katun, kain nilon, dan kain poliester dilapisi nanopartikel perak mempunyai perbedaan rerata zona hambat yang signifikan terhadap kain spandek dilapisi nanopartikel perak begitupun sebaliknya, sedangkan di antara kain katun, kain nilon, dan kain poliester dilapisi nanopartikel perak perbedaan zona hambatnya tidak signifikan seperti terlihat pada Tabel 12. Katun, nilon, poliester menunjukkan hasil uji perbedaan zona hambat tidak signifikan dikarenakan jenis kain tersebut mempunyai gugus fungsi yang terdapat pasangan elektron bebas dan sama-sama mempunyai banyak celah antar seratnya. Spandek menunjukkan perbedaan rerata zona hambat signifikan di
62
antara katun, nilon, poliester karena spandek tidak mempunyai pasangan elektron bebas dalam gugus fungsinya dan mempunyai sedikit celah antar seratnya.