KEEFEKTIFAN CENDAWAN Metarhizium brunneum PETCH
TERHADAP HAMA UBI JALAR Cylas formicarius FABRICIUS
(COLEOPTERA: BRENTIDAE)
AHMAD FAISHOL
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
2011
ABSTRAK
AHMAD FAISHOL. Keefektifan Cendawan Metarhizium brunneum Petch terhadap Hama Ubi Jalar Cylas formicarius Fabricius (Coleoptera: Brentidae).
Dibimbing oleh TEGUH SANTOSO.
Cylas formicarius Fabr. merupakan hama utama pada ubi jalar (Ipomoea batatas) dan tersebar di seluruh dunia. Salah satu musuh alami penting hama tersebut adalah cendawan genus Metarhizium. Imago C. formicarius diberi perlakuan suspensi konidia M. brunneum pada kerapatan 0, 106, 107, 108, dan 109 konidia/ml. Sebagai pembanding digunakan cendawan Beauveria bassiana pada kerapatan yang sama. Aplikasi dilakukan dengan metode semprot terhadap serangga. Dengan kerapatan konidia 109/ml cendawan M. brunneum mampu mengakibatkan kematian C. formicarius hingga 95% pada hari ke-10 setelah perlakuan. Pada hari ke-10 diperoleh LC50 sebesar 4.2x106 konidia/ml dan LC95
sebesar 5.7x109 konidia/ml pada M. brunneum, sedangkan nilai LC50 dan LC95B. bassiana berturut-turut sebesar 2.0x108 konidia/ml dan 4.3x1010 konidia/ml. Dengan menggunakan kerapatan konidia 109/ml, diperoleh LT50 3.73 hari dan
LT95 7.82 hari (M. brunneum) dan LT50 6.00 hari dan LT95 23.16 hari (B. bassiana). Dari hasil yang diperoleh dapat disimpulkan bahwa M. brunneum
efektif untuk mengendalikan C. formicarius.
KEEFEKTIFAN CENDAWAN Metarhizium brunneum PETCH
TERHADAP HAMA UBI JALAR Cylas formicarius FABRICIUS
(COLEOPTERA: BRENTIDAE)
AHMAD FAISHOL
Skripsi
sebagai salah satu syarat untuk memperoleh
gelar sarjana pertanian
pada
Departemen Proteksi Tanaman
DEPARTEMEN PROTEKSI TANAMAN
FAKULTAS PERTANIAN
INSTITUT PERTANIAN BOGOR
2011
LEMBAR PENGESAHAN
Judul : Keefektifan Cendawan Metarhizium brunneum Petch
terhadap Hama Ubi Jalar Cylas formicarius Fabricius (Coleoptera: Brentidae)
Nama Mahasiswa : Ahmad Faishol
Nrp : A34061671
Disetujui, Dosen Pembimbing
Dr. Ir. Teguh Santoso, DEA NIP. 19570907 198003 1 006
Diketahui,
Ketua Departemen Proteksi Tanaman
Dr. Ir. Dadang, M. Sc NIP. 19640204 199002 1 002
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 22 Desember 1988, merupakan anak ketiga dari tiga bersaudara dari pasangan bapak Machfud Suprayogi dan ibu Nuraida. Penulis menamatkan studi SD di SDN 05 Malaka Jaya Jakarta pada tahun 1993-1999, lalu melanjutkan ke SMPN 139 Jakarta pada tahun 1999-2002. Setelah itu penulis melanjutkan studi di SMAN 71 Jakarta pada tahun 2002-2005 dan diterima di Institut Pertanian Bogor pada tahun 2006. Penulis aktif dalam beberapa organisasi kemahasiswaan dalam kampus diantaranya adalah Organisasi Himpunan Mahasiswa Departemen Proteksi Tanaman (HIMASITA), Club Majalah Metamorfosa, dan Entomologi club. Pengalaman magang pernah dilakukan penulis di Balai Penelitian Tanaman Kacang-kacangan dan Umbi-umbian (BALITKABI) Malang selama 1 bulan.
PRAKATA
Saya panjatkan puji syukur kepada Allah SWT yang telah memberikan segala rahmat dan karunia-NYA sehingga saya dapat melakukan dan menyelesaikan penelitian skripsi sebagai salah satu syarat untuk memperoleh gelar sarjana dengan berjudul “Keefektifan Cendawan Metarhizium brunneum
Petch terhadap Hama Ubi Jalar Cylas formicarius Fabricius (Coleoptera: Brentidae)”.
Saya mengucapkan terima kasih kepada bapak Dr. Ir. Teguh Santoso, DEA sebagai pembimbing skripsi, saya juga berterima kasih kepada teman-teman laboratorium patologi serangga dan teman proteksi tanaman yang telah banyak membantu dalam pelaksanaan penelitian. Terima kasih juga saya sampaikan kepada keluarga saya yang memberikan dukungan baik materil maupun moril dalam pelaksanaan penelitian ini.
Penulis menyadari bahwa penulisan skripsi ini jauh dari sempurna dari berbagai hal, oleh karena itu saran dan kritik sangat diterima untuk perbaikan kearah yang lebih baik kedepannya. Semoga tulisan ini dapat memberikan manfaat bagi penulis dan pembaca.
Bogor, 30 maret 2011
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTARGAMBAR ... viii
PENDAHULUAN ... 1
Latar Belakang ... 1
Tujuan Penelitian ... 2
TINJAUANPUSTAKA ... 3
Biologi Hama Boleng (Cylas formicarius (Fabr.)) ... 3
Bioekologi Cendawan Beauveria bassiana ... 5
Bioekologi Cendawan Metarhiziumbrunneum ... 6
Patologi Cendawan Entomopatogen ... 7
BAHANDANMETODE ... 9
Tempat dan Waktu ... 9
Bahan dan Metode ... 9
Perbanyakan Serangga Uji ... 9
Perbanyakan Isolat dan Penyiapan Suspensi Cendawan ... 10
Perlakuan Serangga Uji ... 10
Analisis Data ... 11
HASILDANPEMBAHASAN ... 12
Mortalitas Imago oleh M. brunneum dan B. bassiana ... 12
Perbandingan Virulensi Antara Cendawan M. brunneum dan B. bassiana . 15 KESIMPULAN DAN SARAN ... 18
DAFTAR TABEL
Halaman
1. Mortalitas kumulatif C. formicarius pada hari ke-10 setelah perlakuan cendawan M. brunneum dan B. bassiana ... 12 2. Nilai lethal time (LT) M. brunneum dan B. bassiana terhadap
DAFTAR GAMBAR
Halaman
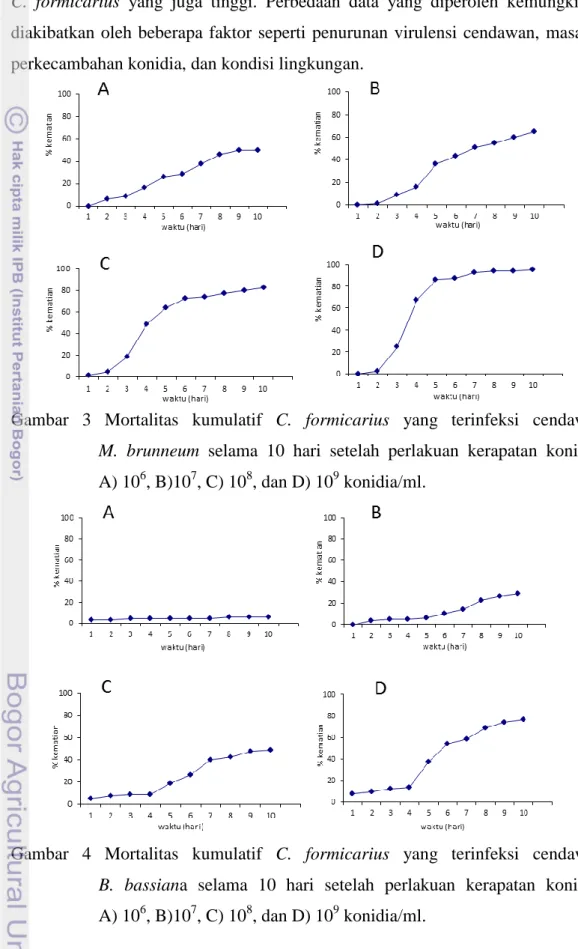
1. Wadah plastik sebagai tempat pemeliharaan serangga uji C. formicarius ... 9 2. Cawan Petri dengan alas kertas tisu yang berisi C. formicarius .... ... 11 3. Mortalitas kumulatif C. formicarius yang terinfeksi cendawan
M. brunneum selama 10 hari setelah perlakuan kerapatan konidia: A) 106, B)107, C) 108, dan D) 109 konidia/ml ... 13 4. Mortalitas kumulatif C. formicarius yang terinfeksi cendawan
B. bassiana selama 10 hari setelah perlakuan kerapatan konidia: A) 106, B)107, C) 108, dan D) 109 konidia/ml ... 13 5. Serangga terinfeksi cendawan dengan tubuh kaku dan diselimuti oleh hifa
cendawan (tanda panah), A) Serangga terinfeksi M. brunneum, B) Serangga terinfeksi B. bassiana . ... 14 6. Hubungan antara kerapatan konidia dengan mortalitas C. formicarius
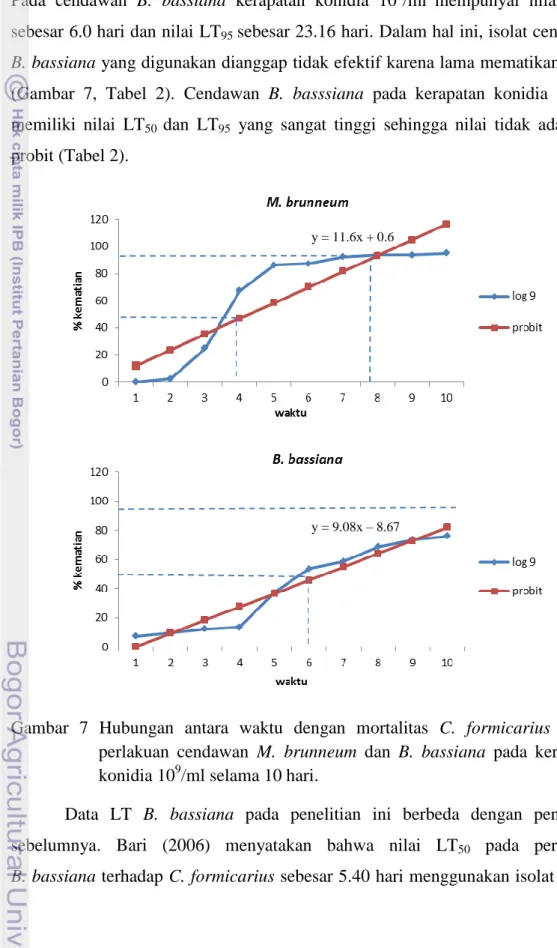
akibat perlakuan cendawan M. brunneum dan B. bassiana pada hari ke-10 setelah perlakuan . ... 15 7. Hubungan antara waktu dengan mortalitas C. formicarius akibat
perlakuan cendawan M. brunneum dan B. bassiana pada kerapatan konidia 109/ml selama 10 hari . ... 16
PENDAHULUAN
Latar Belakang
Ubi jalar (Ipomoea batatas L.) merupakan salah satu komoditas bahan makanan pokok penghasil karbohidrat urutan ke tujuh di dunia setelah gandum, padi, jagung, kentang, barley, dan ketela pohon (FAO 1990). Di Indonesia ubi jalar adalah komoditas pangan yang cukup penting sesudah beras dan jagung. Komoditas ubi jalar mampu tumbuh di daerah yang subur maupun kering sehingga dapat diusahakan masyarakat sepanjang tahun. Ubi jalar juga sangat banyak manfaatnya sehingga dapat digunakan sebagai berbagai macam produk olahan.
Kendala penanaman ubi jalar cukup tinggi di sektor hama dan penyakit.
Cylas formicarius Fabr. merupakan hama utama pada ubi jalar dan tersebar di seluruh dunia (Capinera 1998). CIP (1991) melaporkan bahwa C. formicarius
adalah hama utama dalam budidaya yang perlu mendapat perhatian. Kehilangan hasil akibat serangan hama ini berkisar antara 10-80%, bergantung pada lokasi, jenis lahan, dan musim (Widodo et al. 1994). Kerusakan kecil pun pada umbi menyebabkan umbi tidak layak dikonsumsi karena adanya senyawa terpenoid (Sato et al. 1982; Jansson et al. 1987). Dalam pengendalian hama C. formicarius
harus mempertimbangkan berbagai masalah lingkungan dan keamanan pangan. Ada empat masalah utama mutu dan keamanan pangan nasional yang berpengaruh terhadap perdagangan pangan baik domestik maupun global (Fardiaz 1996). Salah satunya mengenai produk pangan yang tidak memenuhi persyaratan mutu keamanan pangan dengan ditemukannya cemaran kimia berbahaya (pestisida, logam berat, obat-obat pertanian). Kendala tersebut dapat dikurangi dengan metode pengendalian hayati. Penggunaan agens hayati cendawan entomopatogen merupakan suatu upaya untuk mengurangi penggunaan pestisida sintetik yang selama ini banyak menyebabkan masalah lingkungan, dan diharapkan dapat menjadi suatu solusi di samping dapat menggali potensi sumber daya hayati lokal yang diperkirakan keberadaannya berlimpah di alam Indonesia
(Desyanti et al. 2005). Salah satu cendawan entomopatogen yang potensial digunakan sebagai agens hayati adalah Metarhizium anisopliae.
M. anisopliae telah lama digunakan sebagai agens hayati dan menginfeksi beberapa jenis serangga, antara lain dari ordo Coleoptera, Lepidoptera, Homoptera, Hemiptera, dan Isoptera (Strack 2003). Menurut Alexopoulos et al.
(1996) M. anisopliae ini bersifat parasit pada beberapa jenis serangga dan bersifat saprofit di dalam tanah dengan bertahan pada sisa-sisa tanaman. Dengan demikian cendawan ini cocok dikembangkan untuk pengendalian C. formicarius, mengingat hama ini melewatkan sebagian fase hidupnya di dalam umbi dalam tanah.
M. brunneum merupakan cendawan yang baru diujicobakan untuk pengendalian rayap Coptotermes gestroi (Desyanti et al. 2007). Hasil penelitian tersebut mendorong untuk pengujian lebih lanjut mengenai potensi M. brunneum, mengingat sifat cendawan tersebut mirip cendawan M. anisopliae.
Beauveria bassiana merupakan cendawan entomopatogen yang telah lama digunakan sebagai agens hayati. Studi laboratorium dan lapangan menunjukkan
B. bassiana efektif terhadap berbagai hama tanaman maupun hama dalam penyimpanan (Hansen dan Steenberg 2007). Keefektifan B. bassiana untuk pengendalian hama C. formicarius cukup tinggi. Bari (2006) menyatakan bahwa
B. bassiana efektif dalam mengendalikan hama C. formicarius dengan tingkat kematian hampir sebesar 100%. Dengan menggunakan B. bassiana sebagai pembanding, M. brunneum diteliti keefektifannya terhadap C. formicarius.
Tujuan Penelitian
Penelitian ini bertujuan untuk mempelajari tingkat keefektifan cendawan entomopatogen M. brunneum terhadap hama C. formicarius pada ubi jalar.
TINJAUAN PUSTAKA
Biologi Hama Boleng (Cylas formicarius (Fabr.))
C. formicarius merupakan kendala utama dalam peningkatan mutu ubi
jalar (CIP 1991) dan tersebar di seluruh dunia seperti Amerika, Kenya, dan Indonesia. Serangan C. formicarius tidak hanya di lapangan tetapi juga menimbulkan kerusakan yang nyata di penyimpanan. Umbi yang rusak menghasilkan senyawa terpenoid yang menyebabkan umbi pahit dan tidak enak dikonsumsi (Jansson et al. 1987). Dalam perkembangannya, hama ini melewati siklus sempurna atau holometabola, yaitu meliputi telur, larva, pupa, dan imago.
Telur. C. formicarius melakukan perkembangbiakan secara ovipar. Telur diletakkan di dalam suatu rongga kecil yang dibuat oleh kumbang betina dengan cara menggerek akar, batang, dan umbi. Telur diletakkan di bawah kulit atau epidermis, secara tunggal pada satu rongga dan ditutup kembali sehingga sulit dilihat (AVRDC 2004). Menurut Supriyatin (2001), telur C. formicarius sulit dilihat karena ditutup dengan bahan semacam gelatin yang berwarna cokelat.
Telur C. formicarius memiliki ciri-ciri yaitu berukuran kecil antara 0,46– 0,65 mm (Supriyatin 2001), mempunyai bentuk yang oval tak beraturan (AVRDC 2004) dan berwarna putih krem. Supriyatin (2001) mengungkapkan bahwa lama fase telur C. formicarius di Indonesia adalah 7 hari.
Larva. Larva yang baru keluar dari telurnya tidak memiliki tungkai, berwarna putih, dan lambat laun berubah menjadi kekuningan (AVRDC 2004). Larva tersebut langsung menggerek batang atau umbi. Larva menggerek batang menuju ke arah umbi. Perkembangan larva C. formicarius terdiri atas tiga instar dengan periode instar pertama 8-16 hari, instar kedua 2–21 hari, dan instar ketiga 35–56 hari (Capinera 1998). Supriyatin (2001) melaporkan bahwa perkembangan larva C. formicarius terdiri dari lima instar dalam waktu 25 hari. Suhu merupakan faktor utama yang mempengaruhi tingkat perkembangan larva. Larva instar akhir berukuran panjang 7,5-8 mm dan lebar 1,8-2 mm (CABI 2001), berwarna putih kekuningan. Caput besar berukuran sepertiga dari panjang badan dan seperdua
dari lebar badan. Kepala berwarna kuning hingga cokelat, mandibel kuning kehitaman dan abdomen agak besar. Larva menyerang akar, batang, dan umbi dengan cara membuat lubang gerekan, dan menumpuk sisa gerekan sehingga menimbulkan bau khas.
Pupa. Larva instar akhir membentuk pupa pada umbi atau batang, berbentuk oval, kepala dan elitra bengkok secara ventral. Panjang pupa berkisar antara 6-6,5 mm (Capinera 1998). Pupa berwarna putih dan kelamaan akan berubah menjadi abu-abu dengan kepala dan mata gelap. Periode pupa berkisar antara 7–10 hari, tetapi pada cuaca dingin dapat mencapai 28 hari (Capinera 1998).
Imago. Imago ini menyerupai semut, mempunyai abdomen, tungkai, dan caput yang panjang dan kurus (CABI 2001). Kepala berwarna hitam sedangkan antena, thoraks, dan tungkai berwarna oranye sampai coklat kemerahan; abdomen dan elitra biru metalik (Capinera 1998). Menurut Supriyatin (2001) C. formicarius
mempunyai kepala, abdomen, dan sayap depan berwarna biru metalik, sedangkan tungkai dan thoraks cokelat. Antena kumbang jantan berbentuk benang, ruas antena mempunyai jarak yang sempit yang tidak seragam, dan panjangnya lebih dari dua kali panjang flagellum. Antena kumbang betina berbentuk gada (CABI 2001).
Perkembangan dan lama hidup imago C. formicarius bergantung pada beberapa faktor antara lain suhu dan makanan. Suhu optimum untuk dapat hidup dengan baik adalah 15oC, sehingga serangga dapat hidup lebih dari 200 hari dengan makanan yang cukup. Namun, lama hidup kumbang menurun menjadi 3 bulan jika dipelihara pada suhu 30oC dengan makanan, dan 8 hari tanpa makanan (Capinera 1998). C. formicarius betina mampu bertelur sebanyak 90-340 ekor telur semasa hidupnya. C. formicarius dapat terbang tetapi jarang terjadi dan jarak terbangnya relatif dekat.
Bioekologi Cendawan Beauveria bassiana
Konidia cendawan bersel satu, berbentuk oval agak bulat sampai dengan bulat telur, hialin dengan diameter 2-3 μm. Konidiofor berbentuk zigzag merupakan ciri khas genus Beauveria (Barnett 1972).
B. bassiana dapat diisolasi secara alami dari pertanaman maupun dari tanah. Epizootiknya di alam sangat dipengaruhi oleh kondisi iklim, terutama membutuhkan lingkungan yang lembab dan hangat (Sutopo danIndriyani 2007). Variasi virulensi cendawan entomopatogen disebabkan oleh beberapa faktor baik faktor dalam yaitu asal isolat maupun faktor luar seperti medium perbanyakan cendawan, teknik perbanyakan dan faktor lingkungan yang mendukung (Sudarmadji 1997). Pada medium perbanyakan B. bassiana dapat tumbuh pada senyawa yang dapat dimanfaatkan cendawan untuk membuat materi sel baru berkisar dari molekul sederhana seperti gula sederhana dan asam organik, hingga kepada senyawa kompleks seperti karbohidrat, protein, lipid, dan asam nukleat. Media tersebut dapat berupa potato dextrose agar (PDA), media jagung maupun beras.
Suhu berpengaruh terhadap perkembangan koloni dan konidia yang berkecambah. Pada suhu yang tinggi perkembangan koloni lebih lambat dan konidia yang berkecambah menurun (Inglish et al. 1996). Suhu yang efektif untuk pertumbuhan cendawan ini berkisar antara 20-30oC dengan kelembaban relatif di atas 90% (Junianto dan Sukamto 1995). Perkecambahan tidak terjadi di bawah 10oC atau di atas 35oC. Titik temperatur kematian konidia diketahui berkisar 50oC selama 10 menit di air. pH optimal untuk pertumbuhannya adalah antara 5,7-5,9 dan untuk pembentukan konidia dibutuhkan pH 7-8 (Domsch et al. 1993)
Di beberapa negara, cendawan ini telah digunakan sebagai agensi hayati pengendalian sejumlah serangga hama mulai dari tanaman pangan, hias, buah-buahan, sayuran, kacang-kacangan, hortikultura, perkebunan, kehutanan hingga tanaman gurun pasir (Sutopo dan Indriyani 2007). B. bassiana mampu menginfeksi serangga pada berbagai umur dan stadia perkembangan. B. bassiana
telah digunakan untuk pengendalian penggerek batang kakao, ulat kantong kelapa sawit, penghisap buah/pucuk kakao, hama bubuk buah kopi, dan belalang.
Bioekologi Cendawan Metarhizium brunneum
Koloni awal cendawan bewarna putih, kemudian berubah menjadi hijau gelap dengan bertambahnya umur koloni. Menurut Ginting (2008) M. brunneum
menghasilkan warna koloni kuning sampai coklat, miselium bersekat, konidiofor tersusun tegak, berlapis, dan bercabang yang dipenuhi dengan konidia. Konidia
bersel satu berwarna hialin, berbentuk bulat silinder dengan ukuran 9,94 x 3,96 mµ.
M. brunneum dapat tumbuh di berbagai lokasi seperti tanah gambut di USA dan Oregon (CABI 1998), sedangkan Desyanti (2007) mengisolasi M. brunneum dari tanah berpasir. Pertumbuhan cendawan ini memerlukan temperatur optimum sebesar 22-27oC (Roddam dan Rath 1997). Keasaman yang dibutuhkan cendawan untuk tumbuh berkisar antara pH 3,3-8,5, sedangkan pertumbuhan optimal terjadi pada pH 6,5 (Domsch dan Gams 1980). Konidia akan membentuk kecambah pada kelembaban diatas 90%. Dalam pengembangannya M. brunneum
dapat tumbuh dengan baik pada media PDA, jagung, dan beras (Ginting 2008). Penggunaan cendawan ini di areal pertanaman belum pernah dilakukan. Percobaan penggunaan M. brunneum baru dilakukan Desyanti (2007) dalam studi pengendalian rayap tanah Captotermes spp. Perlakuan M. brunneum terhadap rayap menunjukan hasil yang efektif sebagai agens hayati yang potensial.
M. brunneum memiliki patogenisitas lebih tinggi yang dapat membunuh rayap dengan LC50 terendah dibandingkan spesies M. anisopliae, B. bassiana, Fusarium oxysporum dan Aspergillus flavus (Desyanti 2007). Keefektifan dalam penggunaan cendawan tersebut didukung oleh daya kecambah dan konidia yang dihasilkannya. M. brunneum memiliki daya kecambah mencapai 97,20% dalam waktu 12-24 jam setelah inkubasi, sedangkan M. anisopliae memiliki daya kecambah antara 85-90%. Jumlah konidia yang dihasilkan M. brunneum lebih tinggi daripada M. anisopliae yaitu sebesar 223.66 x 107/cawan Petri sedangkan
M. anisopliae 6.18 x 107/cawan Petri (Desyanti 2007). Hasil penelitian tersebut mendorong penelitian untuk pengujian lebih lanjut mengenai cendawan tersebut. Terhadap rayap Schedorhinotermes javanicus dan Captotermes curvignathus,
tingkat patogenisitas, sporulasi maupun viabilitas M. brunneum lebih tinggi daripada M. anisopliae, B. bassiana, dan Metarhizium roridum (Ginting 2008).
Patologi Cendawan Entomopatogen
Proses infeksi cendawan menurut St. Leger (1993) dibagi menjadi tiga tahap yaitu kejadian sebelum proses penetrasi meliputi penempelan serta pertumbuhan prapenetrasi, penetrasi ketubuh inang, dan pemapanan patogen dalam tubuh inang. Cendawan entomopatogen menginfeksi serangga dengan menempel dan melakukan penetrasi ke dalam tubuh melalui kontak diantara ruas-ruas tubuh serangga. Penetrasi dilakukan dengan menempelnya konidia pada kutikula atau mulut serangga. Konidia ini selanjutnya berkecambah dengan membentuk tabung kecambah. Apresorium yang awal dibentuk dengan menembus epitikula, selanjutnya menembus jaringan yang lebih dalam (Situmorang 1990).
Boucias & Pendland (1998) mengemukakan, cendawan entomopatogen dicirikan oleh kemampuannya untuk menempel dan menembus kultikula inang dan dapat tumbuh ke bagian internal inang (hemocoel) dan mengkonsumsinya sehinga nutrisi di hemolimph habis oleh pertumbuhan cendawan yang cepat sehingga inang akan mati. Cendawan juga dapat menghancurkan jaringan lainnya atau dengan melepaskan zat beracun yang mengganggu perkembangan inang secara normal. Zat beracun yang dihasilkan cendawan seperti beauvericin pada
B. bassiana dan destruxins pada M. anisopliae.
Pertumbuhan cendawan diikuti dengan produksi pigmen atau toksin yang dapat melindungi serangga dari mikroorganisme lain terutama bakteri. Ciri-ciri yang menyolok pada serangga yang terinfeksi cendawan adalah adanya miselia pada serangga yang mati setelah terinfeksi. Miselia cendawan mulai menembus kultikula luar dari tubuh serangga pada bagian yang mudah terserang yaitu ruas-ruas tubuh dan alat mulut dan akhirnya menutupi seluruh tubuh serangga. Miselia mulai tumbuh keluar tubuh satu hari setelah serangga mati (Neves dan Alves 2004). Pada kondisi optimal, kematian serangga akibat infeksi cendawan umumnya terjadi antara 3-5 hari setelah aplikasi (Inglish et al. 2001) sedangkan
dari penelitian (Neves dan Alves 2004) kematian serangga berkisar antara 2-3 hari. Cendawan tidak selalu keluar dari tubuh serangga, apabila kondisi tidak mendukung maka akan tetap berada di dalam tubuh serangga tanpa keluar menembus integumen (Santoso 1993).
Salah satu faktor yang berperan penting dalam keberhasilan penggunaan cendawan entomopatogen adalah stadia penggunaan serangga. Tidak semua stadia dalam perkembangan serangga rentan terhadap infeksi cendawan (Inglis et al. 2001). Selain itu keberhasilan pengendalian hama dengan cendawan entomopatogen juga ditentukan oleh kerapatan konidia yang digunakan setiap ml air. Jumlah konidia berkaitan dengan banyaknya biakan yang dibutuhkan tiap hektar (Wikardi 1993 dalam Prayogo 2006).
BAHAN DAN METODE
Tempat dan Waktu
Penelitian dilaksanakan di Laboratorium Patologi Serangga Departemen Proteksi Tanaman, Fakultas Pertanian Institut Pertanian Bogor dari bulan September 2010 hingga Februari 2011.
Bahan dan Metode
Perbanyakan Serangga Uji
Serangga uji C. formicarius diperoleh dari umbi yang memiliki gejala terserang hama tersebut. Umbi ini kemudian dimasukan ke dalam wadah plastik dengan garis tengah 13 cm, dan tinggi 20 cm. Tutup wadah plastik dibuang sebagian dan diganti dengan kain kasa (Gambar 1). Wadah plastik ditempatkan dalam laboratorium (suhu kamar) dan kemunculan serangga diamati setiap hari.
Gambar 1 Wadah plastik sebagai tempat pemeliharaan serangga uji C. formicarius
Umbi yang sudah memiliki gejala serangan yang cukup banyak dipisahkan ke dalam wadah lain untuk memisahkan imago yang baru muncul. Pengamatan
imago yang baru keluar dilakukan setiap hari untuk mendapatkan imago yang berumur homogen. Imago yang digunakan sebagai serangga uji berumur 2-10 hari.
Perbanyakan Isolat dan Penyiapan Suspensi Cendawan
Isolat Beauveria bassiana dan Metarizhium brunneum yang digunakan berasal dari biakan murni koleksi Laboratorium Patologi Serangga Departemen Proteksi Tanaman IPB. Isolat diperbanyak dengan menggunakan media PDA pada cawan petri berukuran 100 mm x 20 mm. Komposisi media PDA adalah kentang, agar, dextrose, dan chloramphenicol. Setelah inokulasi, cendawan ditumbuhkan dalam inkubator (suhu 25o).
Isolat B. bassiana dan M. brunneum yang telah berumur 21 HSI (hari setelah inokulasi) diambil konidianya dengan cara mengambil area pertumbuhan cendawan pada agar dengan menggunakan spatula steril. Cendawan (dengan media) digerus dengan menggunakan mortar. Gerusan dicampur dengan air aquades steril yang telah ditambahkan Tween20 sebanyak 0,025 ml per 50 ml air lalu disaring untuk mendapatkan suspensi konidia yang jernih. Kerapatan konidia dihitung dengan menggunakan hemasitometer Neubauer improved. Kerapatan yang digunakan adalah 106, 107, 108, dan 109 konidia/ml.
Perlakuan Serangga Uji
Imago C. formicarius yang berumur 2-18 hari dipisahkan sebanyak 20 ekor ke dalam masing-masing cawan yang berukuran 150 mm x 25 mm (Gambar 2). Di dasar cawan ditaruh kertas tisu yang dibasahi agar ruangan cawan memiliki kelembaban untuk pertumbuhan cendawan. Suspensi konidia yang telah dibuat disemprotkan terhadap serangga yang berada dalam cawan sebanyak 1 ml volume semprot. Masing-masing perlakuan diulang empat kali. Perlakuan kontrol dilakukan dengan menyemprotkan air steril yang telah ditambahkan Tween20. Setelah disemprot, serangga dimasukkan ke dalam cawan petri dan diberi makan potongan umbi segar.
Gambar 2 Cawan Petri dengan alas kertas tisu yang berisi C. formicarius. Pengamatan dilakukan setiap hari selama 10 hari dengan mencatat jumlah imago yang mati pada masing-masing kosentrasi. Untuk menjaga kelembaban dalam cawan, secara periodik tiap hari diteteskan air steril di kertas tisu. Imago yang terinfeksi pada umumnya akan memperlihatkan miselia putih yang tumbuh keluar tubuh imago.
Analisis data
Penelitian ini menggunakan Rancangan Acak Lengkap (RAL). Data diolah dengan menggunakan progam Statistic Analysis System (SAS) versi 9.1 dan Analisis Probit. Bila terdapat perbedaan di antara perlakuan yang diuji maka dilakukkan dengan uji selang ganda Duncan = 0,05.
HASIL DAN PEMBAHASAN
Mortalitas imago C. formicarius oleh M. brunneum dan B. bassiana
Secara umum data yang diperoleh menunjukan bahwa semakin banyak atau rapat konidia yang digunakan, maka semakin cepat cendawan tersebut menginfeksi dan mematikan C. formicarius (Tabel 1).
Tabel 1 Mortalitas kumulatif C. formicarius pada hari ke-10 setelah perlakuan cendawan M. brunneum dan B. bassiana.
Kerapatan konidia/ml Mortalitas (%)
1 M. brunneum B. bassiana 0 3.12e 3.12e 106 50.00c 6.25e 107 65.00bc 28.75d 108 82.50ba 48.75c 109 95.00a 76.25ba 1
Angka yang diikuti huruf yang sama pada kolom dan baris yang sama tidak berbeda nyata pada
uji Duncan =0,05
Perbedaan kerapatan konidia masing-masing cendawan M. brunneum dan
B. bassiana berpengaruh terhadap tingkat mortalitas C. formicarius. Mortalitas tertinggi didapat oleh M. brunneum dengan kerapatan konidia 109/ml sebesar 95.00%. Nilai mortalitas C. formicarius setelah perlakuan B. bassiana pada kerapatan konidia 109/ml sebesar 76.25% berbeda nyata dengan kerapatan konidia
M. brunneum 109/ml namun memiliki nilai tak berbeda nyata dengan
M. brunneum pada kerapatan konidia108/ml sebesar 82.50%. Mortalitas juga tak berbeda nyata antara perlakuan M. brunneum kerapatan konidia 106/ml yaitu sebesar 50.00% dengan mortalitas perlakuan B. bassiana pada kerapatan konidia 108/ml sebesar 48.75%. Nilai mortalitas pada kontrol sebesar 3.12%, nilai ini tidak berbeda nyata dengan perlakuan B. bassiana pada kerapatan konidia 106/ml sebesar 6.25%.
Bari (2006) melaporkan tingkat kematian C. fomicarius yang disebabkan oleh B. bassiana pada kerapatan konida 108/ml pada hari ke-6 sampai ke-10
mencapai hampir 100%. Capinera (1998) menyatakan bahwa B. bassiana mampu menyebabkan kematian yang besar pada kondisi kelembaban tinggi dan kepadatan
C. formicarius yang juga tinggi. Perbedaan data yang diperoleh kemungkinan diakibatkan oleh beberapa faktor seperti penurunan virulensi cendawan, masalah perkecambahan konidia, dan kondisi lingkungan.
Gambar 3 Mortalitas kumulatif C. formicarius yang terinfeksi cendawan
M. brunneum selama 10 hari setelah perlakuan kerapatan konidia: A) 106, B)107, C) 108, dan D) 109 konidia/ml.
Gambar 4 Mortalitas kumulatif C. formicarius yang terinfeksi cendawan
B. bassiana selama 10 hari setelah perlakuan kerapatan konidia: A) 106, B)107, C) 108, dan D) 109 konidia/ml.
Pada awal perlakuan serangga menunjukan keadaan yang mulai menunjukan ciri-ciri terinfeksi dengan 1-6% tingkat kematian (Gambar 3 dan 4). Kematian oleh cendawan M. brunneum mulai meningkat pada hari ke-4 dan mengalami penurunan pada hari ke-6, sedangkan kematian oleh cendawan
B. bassiana mengalami peningkatan pada hari ke-4 dan turun pada hari ke-7 dan ke-8 (Gambar 3 dan 4). C. formicarius yang terinfeksi cendawan M. brunneum
mengalami mortalitas lebih cepat dan peningkatan yang lebih stabil pada setiap kerapatan konidianya dibandingkan dengan B. bassiana yang perlahan dan memiliki perbedaan yang nyata pada setiap kerapatan konidia yang digunakan. Pengaruh jumlah konidia mempengaruhi kecepatan dalam menginfeksi dan membunuh serangga. Menurut Riyatno dan Santoso (1991) gerakan serangga yang terinfeksi lamban, nafsu makan berkurang bahkan berhenti, lama kelamaan diam dan mati dengan tubuh terselimuti oleh hifa cendawan (Gambar 5).
C. formicarius yang terinfeksi cendawan masih dapat melakukan kopulasi. Selama pengamatan ditemukan imago C. formicarius yang menunjukkan gejala terinfeksi pada waktu sedang kopulasi. Pada prosesnya, cendawan tidak selalu tumbuh keluar menembus integumen serangga, apabila keadaan kurang mendukung, perkembangan cendawan hanya berlangsung di dalam tubuh serangga (Santoso 1993). Agar hifa tumbuh dan keluar dari tubuh serangga dibutuhkan kelembaban yang tinggi.
Gambar 5 Serangga terinfeksi cendawan dengan tubuh kaku dan diselimuti oleh hifa cendawan (tanda panah), A) Serangga terinfeksi M. brunneum, B) Serangga terinfeksi B. bassiana.
0 20 40 60 80 100 6 7 8 9 10 % ke m at ia n
log kerapatan (konidia/ml)
B. bassiana
Perbandingan virulensi antara cendawan M. brunneum dan B. bassiana
Konsentrasi cendawan entomopatogen harus ditentukan secara tepat untuk mendapatkan hasil pengendalian yang optimal (Prayogo 2006). Keberhasilan pengendalian hama dengan cendawan entomopatogen juga ditentukan oleh konsentrasi cendawan yang diaplikasikan yaitu kerapatan konidia dalam setiap mililiter air (Hall 1980).
Lethal concentration (LC) adalah nilai yang menunjukkan jumlah racun per satuan berat yang dapat mematikan populasi hewan yang digunakan dalam
percobaan (Prijono 1985). Dalam pengujian menggunakan cendawan
M. brunneum diperoleh hasil LC50 sebesar 4.2x106 konidia/ml dan LC95 sebesar
5.7x109 konidia/ml sedangkan pengujian menggunakan B. bassiana diperoleh LC50 sebesar 2.0x108 konidia/ml dan LC95 sebesar 4.3x1010 konidia/ml (Gambar
6). Hal ini menunjukkan bahwa M. brunneum memiliki nilai LC yang rendah. Nilai LC yang rendah mempunyai arti cendawan M. brunneum memiliki daya virulensi yang lebih tinggi dibandingkan dengan B. bassiana.
Gambar 6 Hubungan antara kerapatan konidia dengan mortalitas C. formicarius
akibat perlakuan cendawan M. brunneum dan B. bassiana pada hari ke-10 setelah perlakuan.
Lethal Time (LT) adalah waktu yang diperlukan untuk mematikan populasi hewan uji pada dosis atau kosentrasi tertentu (Prijono 1985). Cendawan
M. brunneum pada kerapatan konidia 109/mlmempunyai nilai LT50 sebesar 3.73
hari dan LT95 sebesar 7.82 hari, yang berarti bahwa untuk mendapatkan kematian
sebesar 50% dibutuhkan waktu selama 3.73 hari dan kematian sebesar 95% dibutuhkan waktu 7.82 hari (Tabel 2). Hal ini membuktikan bahwa kerapatan ini memberikan hasil yang efektif dan cepat dalam mengendalikan C. formicarius. Pada cendawan B. bassiana kerapatan konidia 109/ml mempunyai nilai LT50
sebesar 6.0 hari dan nilai LT95 sebesar 23.16 hari. Dalam hal ini, isolat cendawan B. bassiana yang digunakan dianggap tidak efektif karena lama mematikan hama (Gambar 7, Tabel 2). Cendawan B. basssiana pada kerapatan konidia 106/ml memiliki nilai LT50 dan LT95 yang sangat tinggi sehingga nilai tidak ada pada
probit (Tabel 2).
Gambar 7 Hubungan antara waktu dengan mortalitas C. formicarius akibat perlakuan cendawan M. brunneum dan B. bassiana pada kerapatan konidia 109/ml selama 10 hari.
Data LT B. bassiana pada penelitian ini berbeda dengan pengujian
sebelumnya. Bari (2006) menyatakan bahwa nilai LT50 pada perlakuan B. bassiana terhadap C. formicarius sebesar 5.40 hari menggunakan isolat Bb-Cf
y = 11.6x + 0.6
dalam membunuh C. formicarius pada kerapatan konidia 108 konidia/ml. Perbedaan nilai LT50 pada B. bassiana dalam menginfeksi C. formicarius diduga
karena cendawan B. bassiana yang digunakan, telah mengalami penurunan tingkat virulensinya akibat terlalu lama dibiakkan dalam media. Soenartiningsih et al. (1999) mengungkapkan bahwa cendawan B. bassiana yang disimpan pada suhu kamar selama 3 bulan menyebabkan penurunan virulensi akibat terjadinya penurunan daya kecambah. Penggunaan cendawan yang telah lama seharusnya dilakukan proses reinfeksi atau infeksi ulang terhadap serangga uji kemudian di isolasi kembali.
Selain itu, ketidakefektifan dalam menginfeksi C. formicarius disebabkan masalah perkecambahan konidia yang tergantung pada kelembaban, suhu, cahaya, dan nutrisi (Tanada dan Kaya 1993). Menurut Junianto dan Sukamto (1995) perkecambahan konidia memerlukan kelembaban relatif diatas 90% dan suhu optimum antara 20-30oC sedangkan kelembaban pada cawan berubah-ubah selama pengamatan.
Tabel 2 Nilai lethal time (LT) M. brunneum dan B. bassiana terhadap
C. formicarius selama 10 hari. Kerapatan
konidia/ml
M. brunneum B. bassiana
LT50 (hari) LT95 (hari) LT50 (hari) LT95 (hari)
106 9.31 40.36 - -
107 7.19 21.48 19.24 106.80
108 4.65 13.73 10.84 65.25
109 3.73 7.82 6.00 23.16
Dalam percobaan ini B. bassiana memiliki nilai keefektifan lebih rendah dibandingkan dengan M. brunneum. Perbandingan keefektifan antara kedua
cendawan terlihat jelas daya virulensinya terhadap tingkat mortalitas
C. formicarius. Perlakuan yang memiliki kefektifan yang baik untuk pengendalian adalah M. brunneum dengan kerapatan konidia 109 konidia/ml sedangkan pada
kerapatan 108 konidia/ml, keefektifannya sebanding dengan cendawan
KESIMPULAN DAN SARAN
Kesimpulan
1. Semakin tinggi kerapatan konidia cendawan M. brunneum yang digunakan semakin tinggi pula tingkat kematian imago Cylas formicarius.
2. Cendawan M. brunneum efektif mengendalikan C. formicarius dengan kematian hingga 95% pada kerapatan 109 konidia/ml.
3. Pada hari ke-10 setelah perlakuan, nilai LC50 cendawan M. brunneum
sebesar 4.2x106 konidia/ml dan LC95 sebesar 5.7x109 konidia/ml
.
4. Nilai LT50 cendawan M. brunneum dengan kerapatan konidia 109/ml
sebesar 3.73 hari.
Saran
Perlu dikaji viabilitas cendawan entomopatogen yang digunakan agar memiliki pengaruh yang lebih efektif terhadap serangga uji. Perlu diadakan penelitian lanjut dilapang sehingga diketahui tingkat keefektifan sebenarnya dalam pengendalian hama.
DAFTAR PUSTAKA
Alexopoulos CJ, CW Mims, M Blackwell. 1996. Introductory Mycology. 4th ed. New York (USA): John Wiley and Sons Inc.
AVRDC 2004. Integrated Pest Management of Sweet Potato Weevil. http://www.AVRDC. org/LC/Sweet Potato/Weevil.
Bari D. 2006. Keefektifan beberapa isolat cendawan entomopatogen Beauveria bassiana (BALSAMO) Vuillemin Terhadap Hama Boleng Cylas formicarius (Fabr.) (COLEOPTERA: Curculionidae) di Laboratorium [skripsi] .Bogor (ID): Fakultas Pertanian, Insitut Pertanian Bogor.
Barnett HL, Hunter BB. 1972. Ilustrated Genera of Imperfect Fungi. 4th ed. Minnesota: APS Press.
Boucias DG, Pendland JC. 1998. Principles of Insect Pathology. London: Kluwer Academic Publishers.
CABI. 2001. Crop Protection Compendium. (CD-ROM), CABI, Rome.
Capinera JL. 1998. Sweet Potato Weevil, Cylas formicarius (Fabricius). Institute of Food and Agricultural Sciences.University of Florida.
CIP. 1991. Annual Report. Worldwide Potato and Sweet Potato Improvement. CIP, Peru. hlm 130-132.
Desyanti 2007. Kajian Pengendalian Rayap Tanah Captotermes Spp. (Isoptera: Rhinotermitidae) dengan menggunakan Cendawan Entomopatogen Isolat Lokal [disertasi]. Bogor (ID): Fakultas Kehutanan, Insitut Pertanian Bogor.
Desyanti, Hadi YS, Yusuf S, Santoso T. 2007. Keefektifan Beberapa Spesies
Cendawan Entomopatogen untuk Mengendalikan Rayap Tanah
Coptotermes gestroi WASMANN (Isoptera: Rhinotermitidae) dengan Metode Kontak dan Umpan. J. Ilmu & Teknologi Kayu Tropis 5(2):68-77. Domsch KH, W Gams, TH Anderson. 1993. Compendium of Soil Fungi, vol 1,
IHW-Verlag, Eching.
FAO. 1990. FAO Yearbook Production. Vol 42, 1989. Food and agricultural Organization of the United nations. Rome.
Fardiaz S. 1996. Food Control Policy, WHO national Consultant Report. Directorate General of Drug and Food Control, Ministry of Health. Jakarta.
Ginting S. 2008. Patogenisitas Beberapa Isolat Cendawan Entomopatogen Terhadap Rayap Tanah Captotermes curviganatus Holmgren dan
Schedorhinotermes javanicus Kemmer (Isoptera: Rhinotermitidae) [Thesis]. Bogor (ID). Fakultas Pertanian, Institut Pertanian Bogor.
Hall RA. 1980. Control of aphids by the fungus Verticillium lecanii: Effect of spore concentration. Entomology Experimental Application. (27): 1−5. Hansen LS, T Steenberg. 2007. Combining larval parasitoids and an
entomopathogenic fungus for biological control of Sitophilus granarius
(Coleoptera: Curculionidae) in stored grain. Biological Control. 40: 237-242.
Inglis GD, Goettel MS, Butt TM, Strasser H. 2001. Use of Hypomyceteous Fungi for Managing Insect Pests. Di dalam: Butt TM, Jackson CW, Magan N, editor. Fungi as biocontrol Agents: progress, problems, and potential. London: CABI publishing.
Inglis GD, Goettel MS, Johnson DL. 1993. Persistence of the entomopathogenic fungus, Beauveria bassiana, on phylloplanes of crested wheatgrass and alfalfa. BiologicalControl 3: 258-270.
Jansson R.K, HH Bryan, KA Sorensen. 1987. Within-vine distribution and damage of sweet potato weevil, Cylas formicarius elegentulus
(Coleoptera: Curculionidae), on four cultivars of sweet potato in Southern Florida. Florida Entomologist. 70(4): 523-526.
Junianto YD, S Sukamto. 1995. Pengaruh suhu dan kelembaban relatif terhadap perkecambahan, pertumbuhan, dan sporulasi beberapa isolat B. Bassiana. Pelita Perkebunan 11(2): 64-75.
Kaku K, M Yonena, H Yoshimura, N Ho. 1999. Movement behavior of adults of
Cylasformicarius on host plant. Research Bulletin of the Plant Protection Service, Japan. 35: 81.
Lacey LA, MS Goettel. 1995. Current developments in microbial control of insect pests and prospects for the early 21st century. Entomophaga (40): 3−27. Neves PMOJ, Alves SB. 2004. External events related to the infection process of
Cornitermes cumulans (Kollar) (Isoptera: Termitidae) by the entomopathogenic fungi Beauveria bassiana and Metarhiziumanisopliae. Neutropical Entomopogy 33(1): 51-56.
Prayogo Y. 2006. Upaya Mempertahankan Keefektifan Cendawan
Entomopatogen Untuk Mengendalikan Hama Tanaman Pangan. J Litbang Pertanian. [internet]. [diunduh 2011 feb 19]; 25(2): 47−54. Tersedia pada:
http://www.pustaka.litbang.deptan.go.id /publikasi/p3252062.pdf.
Prijono D. 1985. Penuntun Praktikum Pestisida dan Alat Aplikasi Bagian Insektisida. Bogor: IPB.
Riyatno, Santoso T. 1991. Cendawan Beauveria bassiana dan cara pengembangannya guna mengendalikan hama bubuk buah kopi. Direktorat Bina Perlindungan Tanaman Perkebunan. Ditjen Perkebunan. Jakarta. Roddam LF, AD Rath. 1997. Isolation and characterisation of Metarhizium
anisopliae and Beauveria bassiana from subantarctic Macquarie Island. J. Invertebrata Pathology. (69): 285-288.
Santoso T. 1993. Dasar-dasar patologi serangga. Di dalam: E. Martono, E. Mahrub, N.S. Putra, dan Y. Trisetyawati, editor. Simposium Patologi
Serangga I; 1993 Oktober 12-13;Yogyakarta. Universitas Gadjah Mada, Yogyakarta. hlm 1-15.
Sato K, I Uritani, T Saito. 1982. Properties of terpene-inducing factor extracted from adults of the sweet potato weevil, Cylas formicarius Fabricius (Coleoptera: Brethidae). Appl. Entomol. Zool. 17(3): 368−374.
Situmorang J. 1990. Petunjuk Praktikum Patologi Serangga PAV Bioteknologi. Yogyakarta. Universitas Gadjah Mada.
Soenartiningsih, D Baco, M Yasin. 1999. Pengendalian penggerek batang jagung dan penggerek tongkol dengan cendawan entomopatogenik B. bassiana.
hlm 25.Makalah disampaikan pada Temu Teknologi Hasil Pengendalian Hama Terpadu. Program Nasional PHT, Departemen Pertanian Jakarta. Cisarua, 30 Juni 1999.
St. Leger R. 1993. Biology and mechanisms of insect cuticle invasions by Deuteromycete fungal pathogens. Di dalam : Beckage NE, Thompson SN dan Federici BA, Editor. Parasites and Phatogens of insects Vol 2:
Pathogens. San Diego: Academic Press, Inc. hlm 211-229.
Strack BH. 2003. Biological control of termites by the fungal entomopathogen
Metarhizium anisopliae. www.utoronto.ca/forest/termite/metani_1.htm [24 Febuari 2011].
Sudarmadji D. 1997. Optimasi pemanfaatan Beauveria bassiana Bals.(vuill) untuk Pengendalian Hama. Pertemuan Teknis Perlindungan Tanaman. Direktorat Bina Perlindungan Tanaman, Ditjen Perkebunan. Cipayung, 16-18 Juni 1997.
Supriyatin 2001. Hama boleng pada ubi jalar dan cara pengendaliannya. Palawija 2: 22−29.
Sutopo D, Indriyani IGAA. 2007. Status, Teknologi, dan Prospek B. Bassiana
Untuk Pengendalian Serangga Hama. Balai Penelitian Tanaman Tembakau dan Serat. Malang.
Tanada Y, Kaya HK. 1993. Insect Pathology. San Diago: Academic Press, INC. Harcourt Brace Jovanovich, Publisher.
Widodo Y, Supriyatin, AR Braun. 1994. Rapid assessment of IPM needs for sweet potato in some commercial production areas of Indonesia. International Potato Center, Bogor, Indonesia and Malang Research Institute for Food Crops. Malang.