Jurnal Kesehatan Khatulistiwa. Volume 5. Nomor 2A. Juli 2019
Studi Docking Senyawa Apigenin terhadap Reseptor p66 dan p51 Reverse Transkriptase Human Immunodeficiency Virus
Hafrizal Riza1, Arif Wicaksono2, Muhammad Andre Reynaldi3
1, Program Studi Farmasi, FK UNTAN
2 Departemen Antomi Medik, Program Studi Kedokteran, FK UNTAN
3 Program Studi Kedokteran, FK UNTAN
Abstrak
Latar Belakang. Acquired Immunodeficiency Disease (AIDS) masih menjadi kendala dalam tantangan kesehatan sementara pengobatan retroviral ditemukan resistensi, efek yang tidak diinginkan, kegagalan terapi dan masalah kepatuhan pasien sehingga dibutuhkan penemuan obat baru.
Studi ini menganalisis peluang mekanisme aksi molekuler nukleosida reverse transcriptase inhibitor (NRTI) dan non nukleosida reverse transcriptase inhibitor (NNRTI) senyawa apigenin. Metode.
Analisis afinitas yaitu energi interaksi apigenin dan enzim reverse transcriptase HIV dilakukan menggunakan Program Autodock Vina 1.1.2 version dengan Autodock Tools dan analisis residu asam amino reseptor yang terikat dengan apigenin menggunakan Discovery Studio 4.5. Hasil. Hasil analisis menunjukkan afinitas yaitu energi interaksi reseptor substrat enzim reverse transcriptase HIV-1 dengan apigenin dan nevirapin untuk mekanisme NRTI berturut turut -8,5 dan -7,5. Sedangkan energi interaksi reseptor enzim reverse transcriptase HIV-1 dengan apigenin dan zidovudin untuk mekanisme NNRTI berturut turut -8,3 dan -6,4. Asam amino reseptor yang terikat dengan apigenin dan nevirapin ada pada bagian jari dan telapak tangan domain Polimerase dari enzim reverse transcriptase HIV-1.
Sedangkan asam amino reseptor yang terikat dengan apigenin dan zidovudin ada pada RNA substrat dari enzim reverse transcriptase HIV-1. Kesimpulan. Apigenin memiliki mekanisme obat NRTI dan NNRTI.
Kata kunci : Doking, Apigenin, Reverse Transcriptase, HIV-1.
Background. Acquired Immunodeficiency Disease (AIDS) has been still becoming a problem. There are resistencies, adverse effects and patient adherence problems found in the antiretroviral therapy.
Therefore, we need a new agent. This study analysis drug mechanisms of apigenin as NRTI and NNRTI. Method. The affinity for the interaction energies between the ligand and the receptor were analyzed using Autodock Vina 1.1.2 version with Autodock Tools. The amino acids residues of the receptor bound to ligands were analyzed using Discovery Studio 4.5. Result. The analysis result shows that the interaction energies of the receptor of reverse transcriptase HIV-1 substrat with apigenin and nevirapin as NRTI are substituvely 18,5 and -7,5. The interaction energies of the receptor of reverse transcriptase HIV-1 with apigenin and zidovudin as NNRTI are substituvely -8,3 and -6,4. The amino acids of the receptor bound to apigenin and nevirapin are located in the palm and the finger of Polimerase domain of reverse transcriptase HIV-1, and the amino acids of the receptor bound to apigenin and zidovudin are located in RNA, substrat of reverse transcriptase HIV- 1. Conclusion. Based on the analysis datas, could be concluded that apigenin has NRTI and NNRTI mechanism.
Keyword : Docking, Apigenin, Reverse Transcriptase, HIV-1
Jurnal Kesehatan Khatulistiwa. Volume 5. Nomor 2A. Juli 2019 PENDAHULUAN
Acquired Immunodeficiency Disease (AIDS) masih menjadi kendala dalam tantangan kesehatan nasional masa mendatang di Indonesia. Menurut Kementerian Kesehatan Indonesia prevalensi penyakit ini masih cukup berarti., disebabkan penyebaran yang cepat dan kompleks disertai prevalensiyang cenderung meningkat dari 2011 sampai 2016.1
Disisi penyakit, beberapa penyebab menentukan prevalensi dan penyebaran penyakit ini. Human Immunodeficiency Virus (HIV) yang merupakan virus penyebab AIDS menyerang sel CD4 yang merupakan pusat sel daya tahan tubuh.
Berbagai koordinasi sistem pertahanan tubuh manusia dikendalikan oleh sel ini. 2 Di sisi pengobatan, sampai saat ini belum ada obat yang dapat menyembuhkan penyakit AIDS. Kemampuan penggunaan obat antiretroviral hanya dapat menurunkan status penyakit dari penyakit mematikan menjadi penyakit kronis. Hal
ini membuat penderita penyakit harus mengkonsumsi obat selama hidupnya untuk menekan angka virus di dalam darah. Efek samping obat yang besar dapat mempengaruhi kepatuhan penderita dalam minum obat. Resistensi obat dapat memberikan kontribusi pada kegagalan terapi karena itu dibutuhkan inovasi penemuan obat baru. 3,4
Kemampuan penyebaran penyakit AIDS sangat ditentukan oleh kemampuan replikasi virus. Enzim reverse transcriptase HIV tipe 1 (HIV-1 RT) memainkan peran penting dalam duplikasi virus HIV-1. Virus yang masuk ke dalam sel host, enzim HIV-1 RT mentranskripsi untai tunggal gen Ribosa Nukleatid Acid (RNA) virus menjadi untai ganda Deoxyribosa Nukleatid Acid (DNA) yang selanjutnya bergabung ke dalam gen sel host dengan bantuan enzim integrase.5
Non Nucleoside Inhibitor Binding Pocket (NNIBP) merupakan tempat ikatan obat pada subunit p66 dengan 560 asam amino dan subunit p51 dengan 440 asam
Jurnal Kesehatan Khatulistiwa. Volume 5. Nomor 2A. Juli 2019 amino dari enzim reverse transcriptase.
Subunit p66 memiliki 2 domain yaitu polimerase dan ribonuklease H. Domain polimerase mencakup empat subdomain yang berfungsi menambah dan merangkai kopi basa.6 Sedangkan subunit p51 diketahui memiliki peran pada struktur.
7Domain Polimerase pada p66 tersusun dari 4 subdomain yaitu finger (residu 1–85 dan 118–155), palm (residu 86–117 dan 156–236), thumb (237–318), dan connection (319–426). Asam nukleat yang terikat cleft dibentuk terutama oleh jari p66, telapak tangan/palm, ibu jari dan koneksi, dan subdomain RNase H dari p66. Tempat aktif polimerase ini tersusun oleh tiga karboksilat katalitik pada subdomain telapak tangan/palm dari p66 (D110, D185, and D186) yang terikat dengan dua ion divalent, oleh karena itu NNIBP menjadi tempat berikatan reseptor dan obat NNRTI pada residu asam amino yang berbeda pada reseptor. 8,9
Beberapa obat yang digunakan sebagai terapi HIV AIDS memiliki
mekanisme kerja yang berbeda pada enzim reverse transkriptase. Analog nukleosida merupakan mekanisme obat dengan bergabung pada DNA sebagai analog basa pada saat sintesis dan berlaku sebagai stop kodon. Obat ini menghentikan pemanjangan untai karena menghalangi melekatnya basa selanjutnya yang disebut nucleoside reverse transcriptase inhibitor (NRTI). Sedangkan inhibitor non nukleosida reverse transkriptase (NNRTI) memiliki mekanisme ikatan hidrofobik pada subarea p66 dari enzim reverse transkriptase sehingga menghalangi kemampuan domain polimerase atau ribonuklease dalam beraktivitas merangkai pemanjangan untai. 10
Kandidat obat dari bahan alam yang memiliki aktivitas terhadap enzim RT HIV-1 dapat memiliki mekanisme kerja baik sebagai analog nucleoside maupun non nucleoside reverse transcriptase (NNRTI). Apigenin merupakan senyawa flavonoid yang memiliki potensi penghambatan aktivitas
Jurnal Kesehatan Khatulistiwa. Volume 5. Nomor 2A. Juli 2019 enzim HIV-1 RT. Berdasarkan penelitian
yang dilakukan oleh Bhakti Yuliangkara bahwa ekstrak etanol 70% daun tanaman ini menunjukkan aktivitas antiHIV pada tikus coba. Ekstrak ini terbukti dapat menghambat aktivitas enzim reverse transkriptase virus secara in vitro. Ekstrak terbukti memiliki aktivitas penghambatan sebagai analog nukleosida pada enzim HIV-1 RT in vitro. Penelitian lain menemukan bahwa sebagian besar kandungan senyawa dalam ekstrak etanol 70% tanaman ini adalah suatu glikosida apigenin yang dinamakan Gendarusin A.
11,12
Penelitian yang dilakukan di Thailand bahwa isolate apigenin memiliki aktivitas terhadap enzim reverse transcriptase HIV-1 secara in vitro, oleh karena itu perlu dilakukan pembuktian lebih lanjut mengenai mekanisme obat dalam penghambatan aktivitas enzim HIV- 1 RT.13
Pendekatan modern untuk menemukan generasi baru target terapi
atau mekanisme aksi obat diantaranya berdasarkan informasi 3 dimensi mengenai ikatan obat (ligan) dengan reseptor. Suatu cara efektif untuk memprediksi struktur ikatan suatu substrat dalam reseptor dapat dijelaskan dengan simulasi docking, yang berhasil digunakan pada beberapa aplikasi.
Perhitungan ini didasarkan pada perhitungan yang konsisten dari interaksi antara atom-atom dari senyawa, oleh karena itu akan dilakukan penilaian potensi mekanisme kerja senyawa apigenin, Gendarussin A, melalui studi docking melalui informasi ikatan dengan reseptor pada enzim RT HIV-1.
METODE
Bahan dan Alat
Program ChemDraw 15.0 untuk membuat struktur 2-Dimensi dan penentuan sifat kimia-fisika, Program Chem 3D 15.0 untuk membuat struktur 3- Dimensi, Program Autodock Vina 1.1.2 version dengan Autodock Tools untuk docking dan analisis asam amino,
Jurnal Kesehatan Khatulistiwa. Volume 5. Nomor 2A. Juli 2019 Discovery Studio 4.5 dan reseptor 3HVT
(Protein Data Bank). Laptop yang digunakan adalah Asus X455L Series dengan Intel Core i3-inside TM, 2,1 Ghz.
Penyiapan reseptor dan ligand
Struktur tiga dimensi reseptor target enzim reverse transkriptase HIV (PDBID: 3HVT) untuk mekanisme non nucleoside reverse transkriptase dan substrat untuk mekanisme nucleoside reverse transcriptase diperoleh dari RSCB
data bank protein
(http://www.rcsb.org/pdb/home/home.do).
Struktur 2 dan 3 dimensi senyawa apigenin dan kontrol nevirapin dan zidovudin diperoleh dengan menggunakan program komputer ChemDraw 15.0. Struktur ligand diatur ke dalam bentuk yang paling stabil dengan cara meminimalkan energi dengan tool MMF sehingga dapat diperoleh bentuk geometri yang paling terbaik dalam berikatan dengan stereokimia reseptor.
Perlu diperhatikan pembuatan faktor stereokimia yaitu adanya atom C asimetris (khiral), karena dapat mempengaruhi
proses interaksi obat-reseptor dan berdampak pada aktivitas biologis senyawa.
Analisis potensial interaksi reseptor dan ligand
Deteksi tempat aktif, docking dan analisis asam amino reseptor serta jenis interaksi yang terikat dilakukan dengan menggunakan program komputer Autodock Vina dengan Autodock Tools.
Docking dilakukan pada semua tempat aktif potensial dengan mengatur Grid Box pada reseptor enzim reverse transcriptase.
Grid box untuk reseptor substrat enzim reverse transcriptase digunakan dimensi dengan pusat_x, y dan z berturut-turut adalah 126.985, -3.069 dan 70.794 dengan ukuran x, y dan z berturut-turut adalah 126, 96 dan 94. Sedangkan grid box untuk reseptor enzim reverse transcriptase digunakan dimensi dengan pusat_x, y dan z berturut-turut adalah -3.361, -36.073 dan 19.039 dengan ukuran x, y dan z berturut- turut adalah 126, 126 dan 94.
Jurnal Kesehatan Khatulistiwa. Volume 5. Nomor 2A. Juli 2019 Analisis Data
Afinitas inetraksi anatar reseptor dan ligand ditunjukkan melalui energi yang terlibat yaitu Affinity Score, dan HBond, serta nilai RMSD (Root Mean Square Deviation). Pengamatan kemungkinan terjadinya potensial jenis ikatan serta asam amino dari reseptor dilakukan menggunakan aplikasi Discovery Studio senyawa.
HASIL
Penyiapan Reseptor dan Ligand
Reseptor dalam format protein data bank (pdb) diperoleh dari RSCB data bank protein
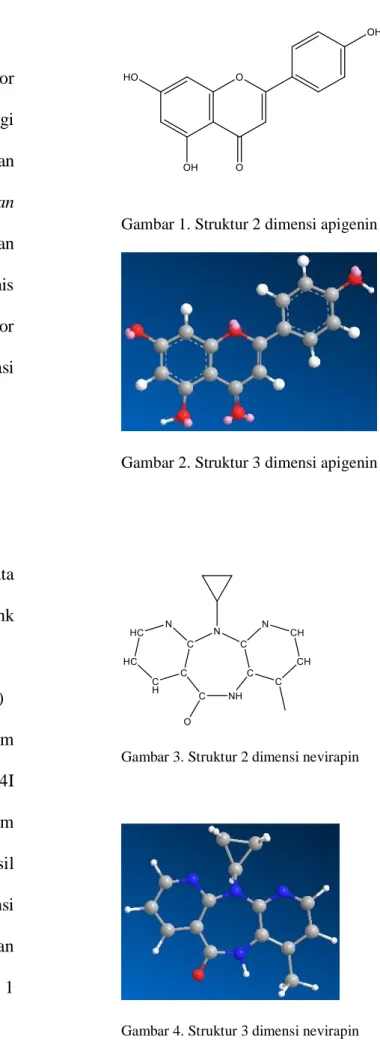
(http://www.rcsb.org/pdb/home/home.do) dengan kode 3HVT untuk reseptor enzim reverse transcriptase HIV-1 dan kode 3V4I untuk reseptor berupa substrat enzim reverse transcriptase HIV-1. Hasil pembuatan struktur 2 dan 3 dimensi senyawa apigenin, nevirapin dan zidovudin dapat dilihat pada gambar 1 berikut.
Gambar 1. Struktur 2 dimensi apigenin
Gambar 2. Struktur 3 dimensi apigenin
Gambar 3. Struktur 2 dimensi nevirapin
Gambar 4. Struktur 3 dimensi nevirapin
Jurnal Kesehatan Khatulistiwa. Volume 5. Nomor 2A. Juli 2019
Gambar 5. Struktur 2 dimensi zidovudin
Gambar 6. Struktur 3 dimensi zidovudin
Gambar menunjukkan adanya perbedaan struktur kimia antara apigenin dengan kontrol positif nevirapin dan zidovudin. Apigenin memiliki struktur cincin heterosiklik benzen namun nevirapin dan zidovuidn terdiri dari cincin hetero siklik tunggal. Selain itu senyawa
nevirapin dan zidovudin mengandung tidak hanya atom oksigen namun juga atom nitrogen. Perbedaan jenis dan susunan atom serta struktur cincin ketiga senyawa ini akan menyebabkan perbedaan bangun geometri ketiga senyawa sehingga mempengaruhi interaksi dengan reseptor.
15,16
Analisis potensial interaksi reseptor dan ligand
Hasil doking apigenin dengan reseptor untuk mekanisme NNRTI dan NRTI menunjukkan potensial interaksi yang baik. Terdapat interaksi yang baik antara apigenin dengan reseptor baik substrat enzim reverse transcriptase HIV-1 dan reseptor enzim reverse transcriptase.
PEMBAHASAN
Interaksi dilihat berdasarkan afinitas antara ligand dan reseptor. Afinitas interaksi antara Apigenin dengan reseptor enzim reverse transcriptase HIV ada pada energi minus atau di bawah nol. Hal ini menunjukkan terjadinya pelepasan energi
Jurnal Kesehatan Khatulistiwa. Volume 5. Nomor 2A. Juli 2019 saat interaksi ligan reseptor terjadi. Energi
komplek interaksi jauh lebih rendah dibandingkan dengan saat ligand dan reseptor belum berinteraksi. Semakin rendah energi semakin mudah interaksi yang terjadi antara reseptor dan ligand. Hal ini disebabkan interaksi menyebabkan komplek reseptor dan ligand semakin stabil dari segi energi. 15
Kontrol positif memperlihatkan efek yang serupa, obat yang sudah dibuktikan mekanisme aktivitasnya terhadap reseptor dan penggunaannya secara in vivo dan klinis terhadap penurunan jumlah virus dalam darah manusia, juga menunjukkan afinitas yang baik dengan energi minus atau di bawah nol. Afinitas yang ditunjukkan oleh kontrol positif ini menunjukkan validitas metode yang digunakan karena metode dapat memberikan hasil yang sesuai dengan aktivitas obat secara in vivo dan klinis. RMSD dari hasil doking antara ligand dan reseptor menunjukkan pengulangan uji yang konsisten untuk
melihat interaksi antara reseptor dan ligan.16
Adapun residu asam-amino dari reseptor yang berinteraksi dengan ligan menunjukkan potensial interaksi antara reseptor dan ligand mungkin berkontribusi pada aktivitas penghambatan reseptor.
Apigenin berinteraksi pada residu asam amino yang berperan pada aktivitas reseptor enzim reverse transcriptase HIV RT-1 dan reseptor substrat enzim reverse transcriptase HIV RT-1. Apigenin berinteraksi dengan 4 jenis interaksi dengan asam amino residu Lisin22, Glisin 23, Asetonin57 Treonin131, Peolin133, Serin134, Asetonin137, Treonin139, Prolin140 yang masuk pada domain finger, Glutanin89, Glisin91, Leusin92 dan Glisin161 yang masuk domain palm.
Interaksi pada daerah ini dapat merubah konformasi bentuk sehingga menghalangi fungsi jari dan telapak tangan domain Polimerase enzim Reverse Transcriptase.
Nevirapin berinteraksi dengan 6 jenis interaksi dengan asam amino residu
Jurnal Kesehatan Khatulistiwa. Volume 5. Nomor 2A. Juli 2019 Lisin11, Lisin13, Prolin14, Glutanin53,
Asetonin54, Prolin55, Tirosin56, Treonin84 yang masuk domain finger, dan Fenilalanin87 yang masuk domain palm.
Interaksi pada daerah ini dapat merubah konformasi bentuk domain jari sehingga menghalangi fungsi jari enzim reverse Transcriptase HIV-1. Jika dibandingkan apigenin memiliki residu asam amino reseptor yang lebih banyak terikat dibanding kontrol positif nevirapin.
Nevirapin berinteraksi banyak pada finger, namun hanya satu residu asam amino domain palm yang terikat.
Hal ini sesuai dengan energi afinitas apigenin sedikit lebih besar dibanding nevirapin. Banyaknya asam amino yang terikat semakin mudah dan stabil berinteraksi dengan reseptor ditunjukkan dengan semakin rendahnya energi afinitas sehingga semakin memicu terjadinya perubahan konformasi domain jari dan telapak tangan reseptor (Janja, 2008).
Apigenin dan kontrol positif zidovudin dapat berinteraksi pada sebagai basa yang dapat ikut dalam sintesis DNA virus HIV-1. Karena kedua ligan tidak memiliki gugus fosfat maka tidak dapat berikatan dengan basa berikutnya. Hal ini membuat kedua ligan berlaku sebagai stop kodon sehingga menyebabkan terjadinya terminasi transkripsi balik RNA menjadi DNA. Sehingga apigenin memiliki peluang untuk merubah konformasi domain enzim RT HIV-1 pada jari dan telapak tangan sehingga menghambat fungsi enzim dalam aktivitasnya mentranskripsi balik RNA virus HIV-1 menjadi DNA, dan juga memiliki peluang untuk berkompetisi dengan substrat enzim RT HIV-1 dalam transkripsi balik RNA virus HIV-1 menjadi DNA.18
Hasil penelitian ini sesuai dengan penelitian studi doking yang dilakukan oleh Riza yang menguji interaksi hesperidin yang memiliki kemiripan struktur sebagai flavonoid dengan apigenin dan juga uji in vitronya sebagai analog
Jurnal Kesehatan Khatulistiwa. Volume 5. Nomor 2A. Juli 2019 substrat menggunakan metode Elisa dalam
penghambatan aktivitas enzim RT HIV- 1.19
Penelitian ini sejalan dengan penelitian yang dilakukan oleh Prayogo, dkk bahwa ekstrak etanol 70 % Justicia gendarussa Burm.f memiliki aktivitas in vitro sebagai analog substrat enzim reverse transcriptase HIV-1, yang kandungan utama dalam ekstrak tersebut adalah apigenin.11
Penelitian ini memiliki keterbatasan belum dapat melihat dampak interaksi ligand dan reseptor terhadap perubahan konformasi domain reseptor yang dapat menghambat fungsi reseptor pada aktivitasnya. Oleh karena itu, perlu dilakukan pemastian pengaruh senyawa pada aktivitas enzim Reverse Transcriptase secara in vitro. Selain itu, pengaruh membran dalam tubuh dapat mempengaruhi kemampuan penetrasi senyawa ke dalam tubuh, oleh karena itu perlu dipastikan pengaruh senyawa secara in vivo.
KESIMPULAN
Berdasarkan afinitas energi interaksi ligand dan reseptor serta lokasi domain residu asam amino reseptor yang terikat disimpulkan apigenin dapat menghambat aktivitas enzim reverse transcriptase HIV- 1 baik sebagai analog substrat enzim dan menghambat struktur enzim yang berperan dalam metranskripsi balik RNA menjadi DNA HIV-1.
DAFTAR PUSTAKA
1. Kementerian Kesehatan Republik Indonesia, 2014, Estimasi dan Proyeksi HIV/AIDS di Indonesia Tahun 2011- 2016,).Indonesia, Jakarta
2. Vidya Vijayan KK, Karthigeyan KP, Tripathi SP and Hanna LE, 2017, Pathophysiology of CD4+ T-Cell Depletion in Hiv-1 and Hiv-2 infections, Front Immunol, Vol. 8, p. 580.
3. Li H, Marley G, Ma W, Wei C, Lackey M, Ma Q, Renaud F, et al, 2017, The Role of ARV Associated Adverse Drug Reactions in Influencing Adherence Among HIV- Infected Individuals: A Systematic Review and Qualitative Meta-Synthesis, AIDS Behav. Vol. 21, Issue 2, p. 341–351.
4. Brooks K, Diero L, DeLong A, Balamane M, Reitsma M, Kemboi E, Et al, 2016, Treatment failure and drug resistance in HIV-positive patients on tenofovir-based first-line antiretroviral therapy in western Kenya, Journal of the International AIDS Society, Vol. 19, p. 20798.
5. Hu W S and Hughes S H, 2012, HIV-1 Reverse Transcription, Cold Spring Harb Perspect Med, Vol. 2, p. a006882.
6. Béthune M. P, 2009, Non-nucleoside Reverse Transcriptase Inhibitors (NNRTIs), their Discovery, Development, and use in the Treatment of HIV-1 Infection: A Review of the Last 20 Years (1989-2009), Antiviral Research, Vol. 85, Issue 1, p. 75–90.
Jurnal Kesehatan Khatulistiwa. Volume 5. Nomor 2A. Juli 2019
7. Prajapati D.G, Ramajayam R., Yadav M.R., Giridhar R., 2009, The Search for Potent, Small Molecule NNRTIs: A Review, Bioorganic & Medicinal Chemistry, Vol. 17, Issue 16, p. 5744–
5762.
8. Sarafianos SG, Marchand B, Das K, Himmel DM, Parniak MA, Hughes SH, Arnold E, 2009, Structure and Function of HIV-1 Reverse Transcriptase; Molecular Mechanisms of Polymerization and Inhibition, National Center for Biotechnology Information, Vol. 385, Issue 3, p. 693-713.
9. Das K, Lewi P.J, Hughes S.H, Arnold E, 2005, Crystallography and the Design of Anti-AIDS Drugs: Conformational Flexibility and Positional adaptability are important in the Design of Non-nucleoside HIV-1 Reverse Transcriptase Inhibitors, Progress in Biophysics & Molecular Biology, Vol. 88, Issue 1, p. 209–231.
10. Maga G, Radi M, Gerard M A, Botta M, and Ennifar E, 2010, HIV-1 RT Inhibitors with a Novel Mechanism of Action:
NNRTIs that Compete with the Nucleotide Substrate, Viruses, Vol. 2, Issue 4, p. 880–
899.
11. Prajogo B, Widiyanti P, Riza H, 2014, Effect of ethanolic extract of Justicia gendarussa Burm f against the activity of reverse transcriptase HIV enzyme in vitro.
J Bahan Alam Indonesia, Vol. 8, p. 384-8.
12. Prajogo E W B, Nasronudin, Cholies N and Neny P, 2010, Development of Justicia gendarussa Burm.f as ANTI-HIV, Universitas Airlangga
13. Yeon-Ju K, Hyun-Jeong O, Hyo-Min A, Ho-Jung Kang, Jung-Hyun K, and Young- Hwan K, 2009Flavonoids as Potential Inhibitors of Retroviral Enzymes, Journal of the Korean Society for Applied Biological Chemistry, Vol. 52, pp. 321–
326.
14. Leroy D, Kajava A V, Frei C and Gasser S M, 2001, Analysis of Etoposide Binding to Subdomain of Human DNA Topoisomerase II α in the Absence of DNA, Biochemistry, Vol. 40, p. 1624–
1634.
15. Jensen F. Introduction to computational chemistry. 2nd Ed. Hoboken: United States: John Wiley and Sons Ltd; 2006. p.
69-416.
16. Irwin D. Kuntz, Jeffrey M. Blaney, Stuart J. Oatley, Robert Langridge, Thomas E.
Ferrin, A geometric approach to macromolecule-ligand interactions, Journal of Molecular Biology, Vol. 161, Issue 2, p. 269-288.
17. Alberto C, Mattia S, Ivana M, Antonella C and Stefano M, 2015, Dock bench: an integrated informatic platform bridging the gap between the robust validation of docking protocols and virtual screening simulations, Molecules, Vol. 20, p. 9977- 93.
18. Janja M, 2008, Pharmacogenetics of Drug Receptors, access on 17th of July 2019, https://www.ncbi.nlm.nih.gov/pmc/articles /PMC4975341/pdf/ejifcc-19-048.pdf.
19. Riza H, Fahrurroji A, Wicaksono A, Nugroho AK, Martono S, 2018, Docking Study Of Methyl Hesperidin As Nucleoside Reverse Transcriptase Inhibitor, Int J Pharm Pharm Sci, Vol 10, Issue 3, 85-89.