i
PENGARUH PROSES PENCAMPURAN DAN PERLAKUAN
KALSINASI DALAM SINTESIS SOL-GEL CdS
MENGGUNAKAN AMILUM SEBAGAI
AGEN PENGOMPLEKS
SKRIPSI
Diajukan kepadaFakultas Matematika dan Ilmu Pengetahuan Alam Universitas Negeri Yogyakarta Untuk Memenuhi Sebagian
Persyaratan Guna Memperolah Gelar Sarjana Sains Kimia
Oleh : Syaiful Anwar
12307141013
PROGRAM STUDI KIMIA JURUSAN PENDIDIKAN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS NEGERI YOGYAKARTA
v MOTTO
Barang siapa menginginkan kebahagiaan didunia maka dapat diraih dengan ilmu, Barang siapa yang menginginkan kebahagiaan di akhirat maka dapat diraih dengan ilmu, dan barang siapa ingin kebahagiaan dua-duanya maka dapat diraih dengan ilmu
(Nabi Muhammad SAW)
Jembaring ilmumu gumantung soko prihatining awakmu
vi
HALAMAN PERSEMBAHAN
Skripsi ini kupersembahkan kepada:
1. Allah SWT
2. Nabi Muhammad SAW
3. Kepada Ayahku
4. Kepada Ibuku
5. Kepada Adik-Adikku
6. Tesia Aisyah Rahmania
7. Teman – teman seperjuangan skripsi, Mamay, Eti, Fia, Yuza, Nana dan Hari
8. Teman – teman Kimia B 2012
9. Almamaterku tercinta Prodi Kimia, FMIPA Universitas Negeri Yogyakarta
vii
PENGARUH PROSES PENCAMPURAN DAN PERLAKUAN KALSINASI DALAM SINTESIS SOL-GEL MENGGUNAKAN AMILUM
SEBAGAI AGEN PENGOMPLEKS Oleh:
Syaiful Anwar NIM: 12307141013
Pembimbing: Dr. Cahyorini Kusumawardani, M. Si.
ABSTRAK
Penelitian ini bertujuan untuk mengetahui pengaruh proses pencampuran
dan perlakuan kalsinasi dalam karakter CdS hasil sintesis dengan metode sol-gel
menggunakan amilum sebagai agen pengompleks.
Sintesis dilakukan dengan mencampurkan prekursor Cd dari senyawa Cd(NO3)2 dan surfaktan (amilum) dengan variasi 0,2; 0,5; 1,0; 2,0 dan 3,0.
Selanjutnya ditambahkan senyawa (NH4)2S sebagai precursor S dengan rasio mol
Cd : S = 1:1. Proses sintesis sol-gel dilakukan dengan pengadukan selama 2 x 24
jam untuk menghasilkan padatan kuning CdS. Setelah proses penyaringan, padatan
yang diperoleh dipanaskan pada temperature 100oC selama 4 jam untuk
menghasilkan nanopartikel CdS. Senyawa hasil sintesis dikarakterisasi
menggunakan X-Ray Diffraction (XRD), UV-Vis, IR dan SEM EDX.
Hasil XRD menunjukkan bahwa sintesis CdS semua variasi amilum berbentuk kubik. Hasil analisa dengan spektra IR setelah dikalsinasi menunjukkan masih adanya amilum. Hasil karakterisasi dengan UV-Vis menghasilkan nilai energi celah pita pada amilum 3 gram yang telah dikalsinasi sebesar 1,72 eV. Hasil analisis dengan menggunakan SEM-EDX menunjukkan ukuran partikel sebesar
0,683 – 1,897 µm dan perbandingan atom sebesar 0,40:0,28.
viii
THE EFFECT OF MIXING PROCESS AND CALCINATION TREATMENT CdS SYNTHESIZED BY SOL-GEL USING
STARCH AS COMPLEXING AGENT
By: Syaiful Anwar NIM: 12307141013
Supervisor : Dr. Cahyorini Kusumawardani, M. Si.
ABSTRACT
This research aimed to know the effect of mixing process and calcination treatment from character of CdS produced with sol-gel method using starch as the complexing agent.
Synthesis was done by mixing precursors Cd of Cd(NO3)2 and surfactan
(starch) with variations of 0.2; 0.5; 1.0; 2.0 and 3.0 gram. And then, added (NH4)S
as precursor S compound in the mole ratio Cd and S of 1:1. Sol-gel synthesis process was done by stirring for 2 x 24 hours to result yellow solid of CdS. After filtering
process, solid were heated at 100oC for 4 hours to produce CdS nanoparticles. The
result of synthesis was characterized by using X-Ray Diffraction(XRD), UV-Vis,
IR and SEM-EDX.
The X-Ray Diffraction showed that synthesis of CdS for all starch variation has a cubic structure. Result of the analysis spectra IR showed that the crystal still containing a starch. Characterization of CdS with UV-Vis showed that the 3 gram starch obtained band gap energy 1.72 eV. Result of the analysis SEM-EDX showed
that particles-size are 0,683 – 1,897 µm with atomic comparison 0.40:0.28.
ix
KATA PENGANTAR
Segala puji bagi Allah Yang Maha Pengasih lagi Maha Penyayang yang telah
melimpahkan rahmat dan hidayah-Nya sehingga atas kehendak-Nya penulis dapat
menyelesaikan skripsi dengan judul Pengaruh Metode Pencampuran Dalam
Sintesis Sol Gel CdS Menggunakan Amilum Sebagai Agen Pengompleks.
Penulis menyadari dalam menyelesaikan skripsi ini tidak terlepas dari
bimbingan, arahan, motivasi dan bantuan dari berbagai pihak. Oleh karena itu,
melalui kesempatan ini penulis mengucapkan terima kasih kepada:
1. Bapak Dr. Hartono selaku Dekan FMIPA Universitas Negeri Yogyakarta yang
telah memberikan ijin penelitian.
2. Bapak Jaslin Ikhsan, Ph. D selaku Ketua Jurusan Pendidikan Kimia dan
Koordinator Program Studi Kimia serta Koordinator Tugas Akhir Skripsi
Kimia FMIPA Universitas Negeri Yogyakarta yang telah memberikan ijin
penelitian dan memberikan nasihat serta saran-saran.
3. Bapak Dr. P. Yatiman selaku Dosen Penasehat Akademik yang telah
membimbing akademik selama 4 tahun.
4. Ibu Dr. Cahyorini Kusumawardani, M.Si selaku pembimbing skripsi, yang telah
memberikan bimbingan, ilmu, pertanyaan, saran, dan masukannya.
5. Ibu Rr Lis Permana Sari, M.Si selaku sekretaris penguji, yang telah memberikan
x
6. Bapak Prof K H Sugiyarto, Ph.D dan Dr Hari Sutrisno berturut-turut selaku
penguji utama dan penguji pendamping yang telah memberikan pertanyaan,
kritik, dan saran.
7. Seluruh Dosen, Staf, dan Laboran Jurusan Pendidikan Kimia FMIPA UNY
yang telah banyak membantu selama perkuliahan dan penelitian.
8. Semua pihak yang telah membantu dalam penyelesaian skripsi ini.
Dalam penyusunan skripsi ini, penulis menyadari adanya keterbatasan
kemampuan, pengetahuan, dan pengalaman sehingga masih terdapat kekurangan.
Oleh karena itu, saran dan kritik yang bersifat membangun sangat penulis harapkan.
Akhirnya besar harapan penulis semoga skripsi ini dapat bermanfaat bagi
pembaca sekalian.
Yogyakarta, Juni 2016
xi DAFTAR ISI
JUDUL ... i
PERSETUJUAN ... ii
PENGESAHAN ... iii
MOTTO ... v
HALAMAN PERSEMBAHAN ... vi
ABSTRAK ... vii
ABSTRACT ... viii
KATA PENGANTAR ... ix
DAFTAR ISI ... xi
DAFTAR TABEL ... xiv
DAFTAR GAMBAR ... xv
DAFTAR LAMPIRAN ... xvi
BAB I PENDAHULUAN ... 1
A. Latar Belakang Masalah ... 1
B. Identifikasi Masalah ... 3
C. Pembatasan Masalah ... 4
xii
E. Tujuan Penelitian ... 5
F. Manfaat Penelitian ... 5
BAB IIKAJIAN PUSTAKA ... 6
A. Deskripsi Teori ... 6
1. Semikonduktor CdS ... 6
2. Sintesis CdS ... 7
3. Amilum ... 9
5. Analisis X-Ray Diffraction (XRD) ... 10
6. Analisis Spektrometer IR ... 12
7. Analisis Spektrofotometer UV-Vis ... 13
8. Analisis SEM-EDX ... 15
B. Penelitian yang Relevan... 16
C. Kerangka Berfikir ... 18
BAB IIIMETODE PENELITIAN ... 19
A. Alat dan Bahan ... 19
1. Alat yang digunakan ... 19
2. Bahan yang digunakan ... 19
B. Waktu dan Tempat Penelitian ... 20
C. Prosedur Penelitian ... 20
xiii
D. Analisis Data ... 21
BAB IVHASIL DAN PEMBAHASAN ... 24
A. Sintesis Senyawa CdS ... 24
B. X-Ray Diffraction (XRD) ... 25
1. Senyawa CdS tanpa amilum ... 26
2. Senyawa CdS dengan variasi amilum ... 28
C. Analisis Spektrometer IR ... 31
D. Analisis UV-Vis ... 35
E. Analisis SEM-EDX ... 41
BAB VKESIMPULAN DAN SARAN ... 43
A. Kesimpulan ... 43
B. Saran ... 43
DAFTAR PUSTAKA ... 44
xiv
DAFTAR TABEL
Tabel 1. Perbandingan Data JCPDS Struktur Kubik dan Sampel... 27
Tabel 2. Perhitungan Ukuran Partikel... 27
Tabel 3. Perhitungan Ukuran Kristal Rata-rata dengan Variasi Amilum... 28
Tabel 4. Parameter Kisi Senyawa CdS Hasil Kalsinasi………... 30
Tabel 5. Perhitungan Ukuran Kristal Rata-rata dengan Variasi Kalsinasi…... 31
Tabel 6. Perbandingan serapan amilum, kalsinasi 200oC dan 300oC……….. 34
Tabel 7. Absorbansi Senyawa CdS variasi amilum……….. 36
Tabel 8. Nilai energi celah pita variasi amilum……….. 38
xv
DAFTAR GAMBAR
Gambar 1. Struktur Kubik Material CdS... 7
Gambar 2. Tahapan Pembuatan Sol dan Gel... 8
Gambar 3. Struktur Amilosa dan Amilopektin... 9
Gambar 4. Difraksi Sinar X... 11
Gambar 5. Energi Celah Pita... 14
Gambar 6. Difraktogram Senyawa CdS Tanpa Amilum... 26
Gambar 7. Difraktogram Senyawa CdS dengan Penambahan Amilum... 29
Gambar 8. Difraktogram Senyawa CdS Setelah di Kalsinasi……….. 30
Gambar 9. Spektrum IR dari Amilum………. 32
Gambar 10. Spektrum IR Hasil Kalsinasi pada Suhu β00˚C………. 33
Gambar 11. Spektrum IR Hasil Kalsinasi pada Suhu γ00˚C………. 33
Gambar 12. Spektrum UV-Vis Senyawa CdS Variasi Amilum……… 35
Gambar 13. Grafik Energi Celah Pita Senyawa CdS tanpa amilum………… 36
Gambar 14. Grafik Energi Celah Pita Senyawa CdS amilum 0,5 gram……. 37
Gambar 15. Grafik Energi Celah Pita Senyawa CdS amilum 1,0 gram…….. 37
Gambar 16. Grafik Energi Celah Pita Senyawa CdS amilum β,0 gram…….. 38
Gambar 17. Spektrum UV-Vis Senyawa CdS setelah kalsinasi……….. 39
Gambar 18. Grafik Energi Celah Pita Senyawa CdS……….. 40
Gambar 19 Hasil SEM Senyawa CdS……… 41
xvi
DAFTAR LAMPIRAN
Lampiran 1. Skema Kerja……….. 49
Lampiran 2. Perhitungan Massa Timbang dalam Preparasi Bahan Untuk
Sintesis Senyawa CdS tanpa Amilum……… 50
Lampiran 3. Perhitungan Massa Timbang dalam Preparasi Bahan Untuk
Sintesis Senyawa CdS dengan Variasi Amilum……… 51
Lampiran 4. Difraktogram XRD Senyawa CdS Tanpa Amilum………... 52
Lampiran 5. Difraktogram XRD Senyawa CdS dengan Variasi Amilum. 53
Lampiran 6. Difraktogram XRD Senyawa CdS dengan Variasi Amilum
Setelah Kalsinasi……….. 58
Lampiran 7. Perhitungan Ukuran Kristal Senyawa CdS tanpa Amilum
dan Senyawa CdS dengan Variasi Amilum………. 61
Lampiran 8. Parameter Kisi Senyawa CdS Tanpa Amilum dan Senyawa
CdS Variasi Amilum………. 71
Lampiran 9. Perhitungan Ukuran Kristal Senyawa CdS tanpa Amilum
dan Senyawa CdS dengan Variasi Amilum Setelah
Kalsinasi……… 77
Lampiran 10. Parameter Kisi Senyawa CdS Tanpa Amilum dan Senyawa
CdS Variasi Amilum Setelah Kalsinasi……… 83
Lampiran 11. Data JCPDS Standar CdS dengan Struktur Kubik………... 85
Lampiran 12. Spektrum IR Senyawa Amilum dan CdS Menggunakan
xvii
Lampiran 13. Hasil UV-Vis Senyawa CdS Sebelum Kalsinasi…………... 89
Lampiran 14. Hasil UV-Vis Senyawa CdS Setelah Kalsinasi….………... 90
Lampiran 15. Hasil SEM-EDX... 92
1 BAB I PENDAHULUAN
A. Latar Belakang Masalah
Cadangan sumber daya energi di Indonesia saat ini sudah semakin terbatas.
Sebagai gambaran, Indonesia saat ini hanya memiliki 4.300 juta ton cadangan
minyak atau hanya sekitar 0,36% dari total cadangan minyak dunia tahun 2006
yaitu sebesar 1.208.200 juta ton. Dengan produksi sebesar 390 juta ton per tahun,
minyak bumi di Indonesia diperkirakan hanya dapat bertahan untuk 11 tahun ke
depan. Sementara itu, gas alam yang juga merupakan salah satu sumber energi
utama di Indonesia hanya memiliki cadangan yang ekuivalen dengan massa
produksi selama 35,54 tahun ke depan (Jauhari, 2007).
Pemanfaatan pembangkit energi primer yang bersifat terbarukan akhirnya
memiliki posisi yang sangat penting dalam mengatasi permasalahan kekurangan
energi, karena energi terbarukan keberadaannya sangat besar sekali atau tidak
terbatas. Pengembangan energi terbarukan, seperti fotovoltaik atau sel surya
menghasilkan teknologi pembangkit listrik yang ramah lingkungan dan tidak
menimbulkan polusi udara dan suara seperti pada pembangkit listrik konvensional
(Hasyim Asy’ari, β014).
Perkembangan sel surya sendiri sampai saat ini sudah mencapai generasi
ketiga, yakni sel surya berbasis nanostruktur semikonduktor dengan gabungan
material organik-anorganik. Penelitian terus dilakukan untuk mencapai efisiensi
2
masyarakat. Sel surya ini antara lain sel surya tersensitisasi zat warna atau
Dye-Sensitized Solar Cell (DSCC) (Gratzel, 2003). Sel surya generasi ini untuk
produksinya tidak memerlukan biaya yang mahal, karena material yang
dibutuhkan tidak memerlukan tingkat kemurnian yang tinggi. Perkembangan
DSSC untuk aplikasi yang lebih luas mengalami masalah pada degradasi zat
warna sehingga dikembangkan sensitiser semikonduktor seperti CdS, CdSe, PbSe,
ZnS dan seterusnya (Jun et al., 2013). Penggunaan semikonduktor ini
menggantikan fungsi zat warna (dye) untuk meningkatkan respon TiO2 pada
sistem sel surya tersensitisasi Quantum Dots Sensitized Solar Cell (QDSSC) (Jun
et al., 2013). CdS merupakan salah satu bahan semikonduktor tipe n pada p-n junction (Al-Tamemee et al., 2012) dan di alam dapat ditemukan dalam bentuk
padatan berwarna kuning sebagai mineral Greenockite (Djamas, 2010). Sintesis
CdS juga dapat dilakukan dengan metode seperti CVD (Chemical Vapor
Deposition) (Nur et al., 2007), spin coating (Al-Juaid et al.,2012), teknik DVT
(Kadash et al., 2014) dan sol-gel (Bansal et al., 2012).
Metode sol-gel yang melibatkan agen pengompleks merupakan metode yang
paling mudah untuk mengontrol sifat dan karakter CdS. Agen pengompleks
merupakan bahan yang digunakan untuk menghambat pertumbuhan partikel,
sehingga diperoleh struktur yang seragam. Amilum dapat digunakan sebagai agen
pengompleks pada sintesis CdS melalui metode presipitasi air pada tingkat pH
yang berbeda untuk mempelajari kondisi optimum menghasilkan distribusi
nanopartikel yang seragam (Rozi et al., 2011). Penelitian tersebut menggunakan
3
temperatur rendah jika dibandingkan dengan metode presipitasi air, CVD
maupun spin coating (Nugroho et al, 2014). Selain itu, metode sol gel lebih
mudah mengontrol komposisi bahan, jenis pelarut, prekursor, temperatur reaksi,
konsentrasi dan parameter lainnya (Zeng et al, 1999).
Penambahan agen pengompleks pada proses sintesis mempengaruhi
karakter hasil sintesis. Oleh karena itu, pada penelitian ini akan dilakukan variasi
proses pencampuran pada sintesis sol gel CdS menggunakan amilum sebagai agen
pengompleks.
B. Identifikasi Masalah
Berdasarkan latar belakang, dapat diidentifikasi masalah sebagai berikut.
1. Metode yang digunakan untuk mensintesis senyawa CdS.
2. Proses sintesis CdS
3. Sumber Cd yang digunakan.
4. Sumber S yang digunakan.
5. Agen pengompleks yang digunakan.
6. Variasi agen pengompleksyang digunakan.
7. Suhu sintesis CdS.
4 C. Pembatasan Masalah
Berdasarkan identifikasi masalah yang telah diuraikan, dapat ditentukan
pembatasan masalah sebagai berikut.
1. Metode yang digunakan untuk mensintesis senyawa CdS adalah metode
sol-gel.
2. Proses pencampuran yaitu ada 2 proses.
3. Sumber Cd yang digunakan adalah Cd(NO3)2.4H2O
4. Sumber S yang digunakan adalah (NH4)2S.9H2O
5. Agen pengompleks yang digunakan adalah amilum.
6. Variasi agen pengompleks yang digunakan adalah 0,2; 0,5; 1,0; 2,0 dan 3,0
gram dengan perbandingan Cd(NO3)2.4H2O 3 gram.
7. Suhu yang digunakan saat sintesis adalah suhu kamar.
8. Suhu kalsinasi yang digunakan adalah 200◦C, 250◦C, 300◦C dan 400◦C.
D. Rumusan Masalah
Berdasarkan batasan masalah yang diuraikan, diambil perumusan masalah
sebagai berikut.
1. Bagaimana pengaruh metode pencampuran dalam proses sintesis terhadap
struktur CdS hasil sintesis?
5 E. Tujuan Penelitian
Berdasarkan perumusan masalah di atas, tujuan dari penelitian ini adalah
sebagai berikut.
1. Mempelajari pengaruh metode pencampuran dalam proses sintesis terhadap
struktur CdS hasil sintesis.
2. Mempelajari pengaruh variasi suhu kalsinasi terhadap struktur CdS hasil
sintesis.
F. Manfaat Penelitian
Manfaat penelitian yang diharapkan adalah sebagai berikut.
1. Memberikan informasi tentang metode sintesis CdS menggunakan amilum
dengan metode pencampuran yang berbeda.
6 BAB II
KAJIAN PUSTAKA
A. Deskripsi Teori 1. Semikonduktor CdS
Kadmium merupakan bahan alami yang terdapat dalam kerak bumi.
Kadmium murni berupa logam berwarna putih perak dan lunak, namun bentuk ini
tak lazim ditemukan di lingkungan (Widowati et al., 2008). Umumnya kadmium
terdapat dalam kombinasi dengan elemen lain seperti Oxigen (Cadmium Oxide),
klorin (Cadmium Chloride) atau belerang (Cadmium Sulfide). Hanya terdapat satu
jenis mineral kadmium di alam yaitu greennockite (CdS) yang selalu ditemukan
bersamaan dengan mineral spalerite (ZnS) (Jayaratnam dan David Koh, 2010).
Kadmium Sulfida merupakan semikonduktor dengan rumus kimia CdS dan di alam
ditemukan sebagai senyawa berwarna kuning. Menurut Lee at al (2003) CdS
sebagai bahan semikonduktor mempunyai energi celah pita pada suhu kamar
sebesar 2,42 eV.
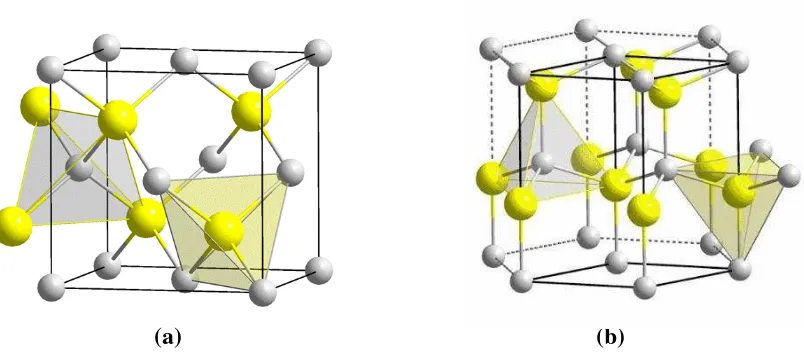
CdS membentuk kristal dengan struktur kubik, heksagonal dan bahkan
campuran fase keduanya. Kristal dengan struktur kubik memiliki harga parameter
7
(a) (b)
Gambar 1. (a) Struktur Kubik
Material CdS (b) Struktur Heksagonal Material CdS
2. Sintesis sol-gel CdS
Metode-metode yang dapat digunakan untuk sintesis CdSantara lain metode
sol-gel (Thambidurai et al., 2010), chemical bath deposition (Liu et al., 2010) metal organic chemical vapor deposition (MOCVD) (Hsu et al., 2004), electrodeposition
dan photochemical deposition (PCD) (Ichimura et al.,2001). Metode sol–gel
merupakan salah satu metode yang paling sukses dalam mempreparasi material
oksida logam berukuran nano. Dalam metode ini terjadi perubahan dari suspensi
koloid (sol) menjadi fase cair (gel). Sol merupakan sistem koloid padatan dengan
ukuran 0,1–1 m yang terdispersi dalam cairan (Ismunandar, β004). Gel adalah
emulsi dalam medium pendispersi zat padat yang dapat dianggap sebagai hasil
pembentukan dari penggumpalan sebagian zat cair.
Metode sol-gel adalah metode penumbuhan lapisan yang dilakukan pada
suhu kamar (Iriani, 2009). Metode ini merupakan salah satu metode yang tidak
membutuhkan biaya yang besar karena tidak membutuhkan banyak peralatan dan
8
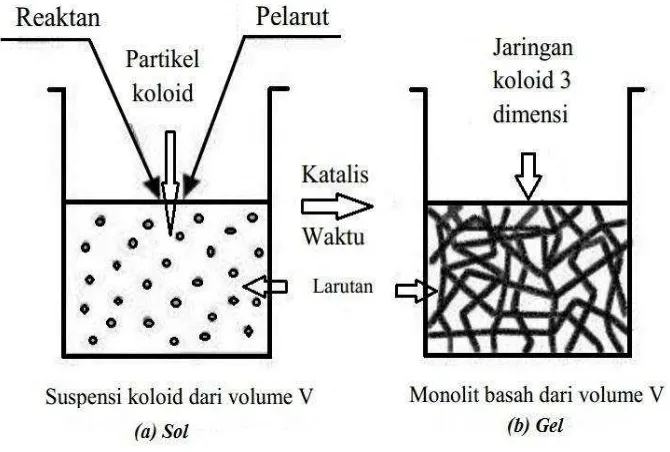
menggunakan metode ini dalam skala laboratorium (Adem, 2003). Proses
tahapan pembentukan sol dan gel ditampilkan pada Gambar 2.
Gambar 2. (a) Tahap Pembuatan Sol, (b) Tahap Pembuatan Gel
Beberapa keuntungan menggunakan metode sol-gel antara lain sebagai
berikut.
1. Tingkat stabilitas termal yang baik
2. Luas permukaan BET yang tinggi
3. Fase pemisahan cepat dan kristalisasi cepat.
4. Daya tahan pelarut yang baik
5. Modifikasi permukaan dapat dilakukan dengan berbagai kemungkinan
Pada proses pembuatan nanomaterial (pemecahan struktur material menjadi
ukuran yang lebih kecil) dipengaruhi oleh beberapa faktor yaitu: temperatur,
kecepatan pengadukan, zat penstabil (agen pengompleks), pH larutan dan
9
digunakan agen pengompleks yang berfungsi untuk membantu mencegah
pertumbuhan nanopartikel secara berlebih dan terjadinya agregasi serta untuk
mengontrol struktur nanopartikel (Zhiqiang and Yadong, 2014). Pertumbuhan dari
nanopartikel bergantung pada kondisi saat sintesis, suhu sintesis dan waktu sintesis
untuk penyelesaian reaksi.
3. Amilum
Amilum merupakan polisakarida hasil sintesis dari tanaman hijau melalui
proses fotosintesis. Amilum memiliki bentuk kristal bergranula yang tidak larut
dalam air pada temperatur kamar memiliki ukuran dan bentuk tergantung pada
jenis tanamannya. Pada umumya amilum tersusun dari 25% amilosa dan 75%
amilopektin. Amilosa merupakan polimer berbentuk panjang dan lurus dan sedikit
cabang (kurang dari 1%) dengan berat molekul 500.000 g/mol (Nwokocha, 2008).
Unit-unit glukosa terhubung oleh ikatan α-1,4 pada molekul amilosa. Molekul
amilosa berbentuk helix dan bersifat hidrofobik. Amilopektin memiliki bentuk
yang bercabang dan memiliki berat molukul 107-109 g/mol bergantung pada jenis
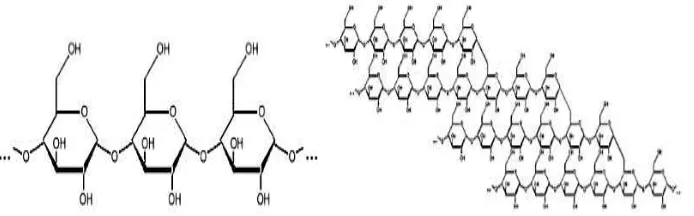
tanamannya. Amilum terbentuk dari monomer-monomer glukosa. Gambar 3
menunjukkan struktur amilosa dan amilopektin
10
Amilum tersusun dari monomer monosakarida enam karbon D-glukosa.
Struktur monosakarida D-glukosa dapat digambarkan dalam struktur rantai
terbuka atau dalam cincin. Rumus molekul amilum adalah (C6H10O5)n, dimana
n terdiri atas 40-3000 unit D-glukosa (Anna, 1994). Pada dasarnya, amilum
merupakan salah satu surfaktan yang biasa digunakan dalam sintesis nanopartikel.
Amilum merupakan jenis surfaktan netral. Surfaktan netral mengandung suatu
gugus non-ion seperti suatu karbohidrat yang dapat membentuk ikatan hidrogen
dengan air. Surfaktan digunakan sebagai agen peningkat dalam sintesis
nanomaterial yang berfungsi untuk mengontrol mekanisme dan kinetika reaksi.
Amilum mampu memengaruhi morfologi dan ukuran partikel dari produk akhir.
Distribusi ukuran nanopartikel dapat dikontrol dengan menambahkan surfaktan.
Surfaktan lain selain amilum yang juga biasa digunakan dalam sintesis
nanopartikel adalah natrium dodesil sulfat (SDS), polivinil pirolidon (PVP),
gliserol, bis (2-ethylhexyl) sulfosuccinate (AOT), cetyltrimethyl amonium bromida
(CTAB), dan dietil sulfosuccinate (DES) (Yadav et al, 2012).
5. Analisis X-Ray Diffraction (XRD)
Difraksi sinar-X merupakan teknik yang digunakan untuk mengidentifikasi
adanya fasa kristalin di dalam material-material benda dan serbuk, untuk
menganalisis sifat-sifat struktur sperti stress, ukuran butir, cacat kristal, dan fasa
komposisi oriental kristal dari tiap fasa. Metode ini menggunakan suatu berkas
sinar-X yang terdifraksi seperti sinar yang direfleksikan dari setiap bidang,
berturut-turut dibentuk oleh atom-atom kristal dari material sampel. Selanjutnya
11
yang dikenal sebagai data JCPDS (Joint Commite on Powder Diffraction
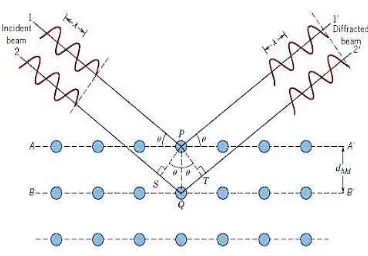
Standars). Gambar 4 menjelaskan bahwa seberkas sinar-X dipantulkan dari
sehimpunan bidang kristal yang berjarak antara d.
Gambar 4. Difraksi Sinar X
Prinsip difraksi untuk sampel berbentuk serbuk adalah cahaya monokromatik
sinar X dikenakan pada kristal, satu pantulan atau difraksi dari variasi sudut sinar
X akan menunjukkan sinar mula-mula, jika seberkas sinar X menumbuk partikel
berukuran atom maka sinar tersebut akan dipantulkan oleh partikel atomik yang
ditumbuknya (Bird, 1987: 34-36). Sinar X yang terdifraksi oleh bidang permukaan
sampel memiliki sudut refleksi yang sama dengan sudut sinar datang (West, 1989
12
Dalam penelitian ini, sampel dianalisis untuk memperoleh informasi tentang
struktur kristal, ukuran kristal dan parameter kisi. Untuk mengetahui struktur
kristal dari senyawa yang dianalisis perlu dibandingkan dengan data standar
JCPDS CdS no. 75-1546 untuk struktur kubik dan JCPDS CdS no. 41-1049 untuk
struktur heksagonal. Data standar JCPDS CdS untuk struktur kubik memiliki nilai
βθ yaitu 26,505o; 43,969o; dan 52,076 o dengan hkl (111), (220) dan (311). Untuk
data standar JCPDS CdS dengan struktur heksagonal memiliki nilai βθ yaitu
26,507o; 47,839o; dan 52,795o dengan hkl (002), (103) dan (201).
6. Analisis Spektrometer IR
Spektrometer inframerah merupakan instrumen yang digunakan untuk
mengukur radiasi pada berbagai panjang gelombang. Spektrofotometer IR
memberikan analisis secara kualitatif dengan mengidentifikasi macam gugus
fungsi yang terdapat dalam suatu senyawa. Suatu senyawa akan memancarkan
energi yang kemudian akan diserap oleh alat dengan spektra. Radiasi inframerah
terjadi pada panjang gelombang 4000-670 cm-1 sehingga energi yang dihasilkan
rendah. Energi dalam radiasi inframerah ini tidak mampu memecahkan suatu
molekul menjadi komponen-komponennya, namun hanya dapat memberikan efek
vibrasi (getaran) pada gugus-gugus yang terkena pancaran inframerah ini. Efek
vibrasi yang ditimbulkan menghasilkan hasil yang spesifik untuk masing-masing
gugus, atau dengan kata lain efek vibrasi pada masing-masing gugus terjadi pada
panjang gelombang yang berbeda-beda. Data inilah yang menjadi acuan dalam
spektrometer inframerah untuk menyimpulkan gugus fungsional yang terkandung
13
Setiap gugus fungsional suatu senyawa memiliki daerah penyerapan radiasi
yang berbeda-beda sehingga dalam aplikasinya apabila berbeda gugus fungsional
maka akan bebeda pula data radiasi panjang gelombang yang ditunjukkan. Namun
tidak semua ikatan dalam molekul dapat menyerap energi inframerah, hanya ikatan
yang memiliki momen dipol yang dapat menyerap radiasi inframerah
(Sastrohamidjojo, 1992). Pada penelitian ini fungsi dari FTIR adalah untuk
mengetahui gugus fungsi yang terdapat di dalam sintesis senyawa CdS yang telah
dikalsinasi. FTIR juga difungsikan untuk mengetahui apakah masih terdapat
amilum di dalam sintesis senyawa CdS.
7. Analisis Spektrofotometer UV-Vis
Spektrofotometer UV-Vis adalah pengukuran panjang gelombang dan
intensitas sinar ultraviolet dan cahaya tampak yang diabsorbsi oleh sampel. Sinar
ultraviolet dan cahaya tampak memiliki energi yang cukup untuk mempromosikan
elektron pada kulit terluar ke tingkat energi yang lebih tinggi. Panjang gelombang
terhadap transmisi spektrum absorbansi yang diukur dengan alat UV-Vis dapat juga
digunakan sebagai pengukuran awal untuk menentukan besaran celah pita. Sinar
Ultraviolet mempunyai panjang gelombang antara 200-400 nm, sementara sinar
tampak mempunyai panjang gelombang 400-800 nm (Dachriyanus, 2004).
Prinsip dari spektrofotometer UV-Vis adalah jika material disinari dengan
gelombang elektromgnetik maka cahaya akan diserap oleh elektron dalam
material. Setelah menyerap cahaya, elektron akan berusaha meloncat ke tingkat
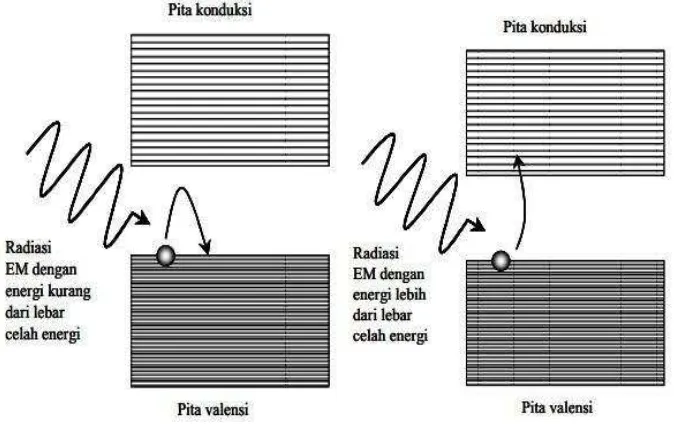
energi yang lebih tinggi. Jika energi cahaya yang diberikan kurang dari lebar
14
baru akan meloncat ke pita konduksi apabila energi cahaya yang diberikan
lebih besar daripada lebar celah pita energi, seperti yang ditunjukan pada Gambar
[image:31.596.129.466.174.386.2]5.
Gambar 5. Energi Celah Pita
Penentuan energi celah pita (band-gap) dengan Diffuse ReflectanceUV
Metode spektrofotometri UV-Vis Diffuse Reflectance digunakan untuk
mengetahui besarnya energi celah pita dari material CdS. Energi celah pita
diperoleh dengan mengubah besaran %R ke dalam faktor Kubelka-Munk
(F(R)), sesuai dengan rumus sebagai berikut.
Dimana, F(R) adalah faktor Kubelka-Munk, K adalah koefisien absorbansi, S
adalah koefisien scattering, dan R adalah nilai reflektansi. Selanjutnya besaran
15
dimana, Eg adalah energi celah pita (band gap), h adalah konstanta Planck
(6,626 x 10-34 Joule), c adalah kecepatan cahaya di udara (2,998 x 108 m/s), dan
adalah panjang gelombang (nm).
8. Analisis SEM-EDX
SEM-EDX (Scanning Electron Microscopy – Electron Dispersive X-Ray
Analyser). SEM adalah sebuah mikroskop electron yang didesain untuk menyelidiki
permukaan dari objek solid secara langsung. SEM memiliki perbesaran 10 –
3.000.000x, deph of field 4 – 0,4 mm dan resolusi sebesar 1 – 10 nm. Kombinasi
dari perbesaran yang tinggi, depth of field yang besar, resolusi yang baik,
kemampuan untuk mengetahui komposisi dan informasi kristalografi membuat
SEM banyak digunakan untuk keperluan penelitian dan industri.
Perlu diperhatikan, saat mengoperasikan SEM, electron optical coloumn
dan sample chamber harus dalam kondisi vakum agar elektron yang ditembakkan
dan dipantulkan tidak berhamburan karena dapat merusak kualitas gambar yang
dihasilkan (Jaya., 2005:19(2): 417-422).
EDX menggunakan emisi spektrum sinar-X dari sampel yang ditembak
dengan elektron yang terfokus untuk analisis kandungan kimianya. Analisis
16
kuantitatif membandingkan setiap unsur pada sampel dengan unsur yang sama pada
standar kalibrasi yang telah diketahui komposisinya (Goldstein, 2003).
Pada dasarnya SEM-EDX merupakan pengembangan SEM. Kombinasi
SEM dengan EDX (Energy Dispersive X-Ray Spectroscopy) merupakan dua
perangkat analisis yang digabungkan menjadi satu panel analitis sehingga
mempermudah analisis dan lebih efisien. Analisa SEM-EDX dilakukan untuk
memperoleh gambaran permukaan atau fitur material dengan resolusi sangat tinggi
hingga memperoleh suatu tampilan dari permukaan sampel yang kemudian
dikomputasikan dengan software untuk menganalisis komponen materialnya baik
dari kuantitatif maupun kualitatifnya. Karakterisasi sampel pada penelitian ini
menggunakan alat SEM JEOL JED-2300.
B. Penelitian yang Relevan
Penelitian yang dilakukan oleh Bansal, Jaggi dan Rohilla (2012) telah
berhasil mensintesis kadmium sulfida melalui metode sol gel dengan glukosa
sebagai agen pengompleks. Kadmium sulfida disintesis dengan mencampur
Cd(NO3)2 dengan Na2S kemudian ditambahkan glukosa kemudian dipanaskan
pada suhu 100°C. Variasi glukosa yang digunakan yaitu 0,001 M; 0,1 M dan 0,5
M. Dari hasil penelitiannya dilaporkan bahwa hasil analisis XRD menunjukan
kadmium sulfida memiliki ukuran nanopartikel dan berstruktur kubik.
Qinglian et al. berhasil mensintesis nanopartikel CdS menggunakan
amilum sebagai agen pengompleks Nanopartikel dikarakterisasi dengan
17
fotoluminesen. Analisis Difraksi Sinar-X (XRD) menunjukan bahwa nanopartikel
CdS dengan struktur kubik. AFM memberikan ukuran partikel rata-rata sekitar 10
nm (Qinglian et al., 2004).
Rodriguez et al. (2008) berhasil mensintesis nanopartikel CdS melalui teknik
presipitasi kimia dan menyatakan banwa polimer amilum dapat digunakan sebagai
agen pengompleks yang efektif. Difraksi sinar-X dari sintesis nanopartikel CdS
menunjukkan bahwa kristal berukuran kecil. Pola XRD menunjukkan tiga
puncak pada 26,5o; 43,9 o; dan 52,1 o, yang sesuai dengan hkl (111), (220) dan
(311) pada fase kubik CdS (Rodriguez et al., 2008)
Djamas, (2010) berhasil membuat lima sampel CdS menggunakan metode
Thermal Evaporation dengan temperatur 200°C - 250°C. Semikonduktor CdS
memiliki struktur heksagonal (Wurzite) dengan orientasi bidang 002 dan parameter
kisi a= (4,108 – 4,141) Å dan c= (6,72 – 6,797) Å.
Ria, (2015) berhasil mensintesis nanopartikel CdS menggunakan amilum
sebagai agen pengompleks. Nanopartikel yang dihasilkan menggunakan metode
sintesis sol-gel. Pada penelitian yang dilakukan, Cd(NO3)2.4H2O dihomogenkan
dengan (NH4)2S selama 24 jam yang kemudian dilakukan penambahan amilum.
Nanopartikel dikarakterisasi menggunakan X-Ray Diffraction (XRD) dan
absorbansi UV-Vis. Pada analisis sinar-X diketahui berstruktur heksagonal dengan
ukuran kristal rata-rata 17 nm dan energi celah pita dari analisis UV-Vis rata-rata
sebesar 2,3 eV.
18 C. Kerangka Berfikir
Penelitian ini dilakukan untuk mendapatkan senyawa semikonduktor CdS
yang berukuran nanopartikel dan efektif digunakan sebagai energi alternatif.
Bahan bahan yang digunakan untuk penelitian ini adalah Cd(NO3)2.4H2O 98%
dari Aldrich, amilum dari Alchemix sebagai agen pengompleks dan variasi
konsentrasi dari amilum masing-masing 0,2; 0,5; 1,0; 2,0; dan 3,0 gram serta
(NH4)2S 98% dari Merck.
Amilum sebagai agen pengompleks digunakan untuk mencegah atau
menghambat pertumbuhan partikel dan untuk menstabilkan nanopartikel CdS saat
proses sintesis sehingga ukuran partikel yang didapatkan bias sesuai dengan yang
diinginkan. Agar didapatkan ukuran nanopartikel yang sesuai dengan yang
diinginkan, kondisi sintesis seperti suhu maupun waktu penyelesaian sangat
berpengaruh. Maka dari itu dibutuhkan agen pengompleks untuk menghambat
ukuran partikel.
Proses pencampuran pada penelitian ini dilakukan untuk mengetahui
karakter hasil sintesis, serta untuk membandingkan hasil sintesis pada penelitian
yang telah dilakukan oleh Ria (2015). Hasil sintesis kemudian dianalisis dan
dikarakterisasi menggunakan X-Ray Diffraction untuk mengetahui struktur kristal
maupun ukuran kristal. Setelah diketahui ukuran kristal terkecil, kemudian
dikalsinasi pada suhu 250°C. Kemudian dilakukan analisa menggunakan FTIR,
19 BAB III
METODE PENELITIAN
A. Alat dan Bahan 1. Alat yang digunakan
a. Alat-alat gelas
b. Stirer
c. Oven
d. Penyaring Kering
e. MufleFurnance
f. XRD (X-Ray Diffraction) Rigaku Multiflex dengan radiasi
CuK(=1,5405981 Å)
g. FTIR merek Shimadzu
h. UV-Visible 1700 Pharmaspec Spectrophotometer Specular
Reflectance Attchment
i. SEM-EDX (Scanning Electron Microscopy-Electron Dispersive
X-Ray Analyzer)
2. Bahan yang digunakan
1. Cd(NO3)2.9H2O 98% dari Aldrich
2. (NH4)2S 98% dari Merck
3. Amilum dari Alchemix.
4. Akuades dari General
20
6. Kertas saring no.42 dari Whatmann
7. Kaca gelas
B. Waktu dan Tempat Penelitian
Penelitian ini dilakukan di Laboratorium penelitian III dan
Laboratorium Kimia Analisis Universitas Negeri Yogyakarta untuk
sintesis nanopartikel CdS dan lapis tipis CdS. Penelitian ini dilaksanakan
pada bulan Juni 2015 sampai April 2016. Uji karakterisasi yang dilakukan
adalah uji karakteristik menggunakan alat XRD (X-Ray Diffraction) merek
Rigaku Multiflex dengan radiasi Cu K (=1,54056 Å) yang dilakukan di
Laboratorium Analisis Instrumen FMIPA Universitas Negeri Yogyakarta,
Uji FTIR merek Shimadzu yang dilakukan di Laboratorium Kimia Organik
FMIPA Universitas Gajah Mada, Uji UV-Visible 1700 Pharmaspec
Spectrophotometer Specular Reflectance Attchment yang dilakukan di
Laboratorium kimia FMIPA Universitas Gajah Mada dan uji SEM-EDX
JEOL JED2300 yang dilakukan di LPPT Universitas Gajah Mada
C. Prosedur Penelitian 1. Sintesis Nanopartikel CdS
Langkah kerja yang dilakukan untuk menghasilkan nanopartikel CdS
adalah larutan Cd(NO3)2 0,1 M diaduk dan kemudian ditambahkan amilum
dengan variasi konsentrasi 0,2; 0,5; 1,0; 2,0; dan 3,0 gram dan dilakukan
pengadukan selama 24 jam sehingga diperoleh larutan homogen. Kemudian,
ditambahkan tetes demi tetes larutan (NH4)2S ke dalam campuran Cd(NO3)2
21
kuning. Endapan lalu disaring dan dikeringkan dengan suhu 100 C selama 4
jam dan kemudian setelah kering digerus untuk mendapatkan serbuk CdS.
2. Variasi Kalsinasi CdS
Hasil sintesis yang didapatkan berupa serbuk CdS kemudian di analisis
menggunakan X-Ray Diffractometer untuk mengetahui ukuran kristal dan
parameter kisi. Setelah didapatkan ukuran kristal yang terkecil kemudian
diambil untuk dikalsinasi dengan variasi suhu 200oC, 250 oC, 300oC dan 400oC.
Kalsinasi dilakukan selama 6 jam. Dari hasil kalsinasi ini, selanjutnya
dilakukan analisis menggunakan X-Ray Diffraction untuk mengetahui ukuran
kristal terkecil dan diidentifikasi menggunakan spektrometer IR, UV-Vis dan
SEM.
D. Analisis Data
Senyawa CdS yang telah divariasi konsentrasi amilumnya dan telah
disintesis kemudian di analisis menggunakan XRD dengan panjang
gelombang ( ) 1,5406 A pada range β0 sampai 900 dengan laju sebesar 0,02.
Hasil analisis Sinar-X digunakan untuk mengetahui informasi berupa
struktur kristal, ukuran kristal dan parameter kisi. Data yang diperoleh
berupa hubungan antara intensitas dengan sudut difraksi βθ, hasil tersebut
kemudian dibandingkan atau dicocokkan dengan data JCPDS dan akan
diketahui bidang-bidang hkl dari sampel. Hasil dari pencocokan
menggunakan data JCPDS adalah dapat diketahui struktur senyawa tersebut.
Sedangkan untuk mengetahui ukuran kristal dan parameter kisi yang
22
Kristal dapat diketahui dengan menggunakan metode Debye Scherrer
(Morales et al.,2007) yaitu menggunakan persamaan:
� =
�. �
����
D adalah ukuran kristal (nm), k merupakan konstanta material yang
nilainya 0,λ, merupakan panjang gelombang yang digunakan pada waktu pengukuran (nm), merupakan Full Widht Half Maximum (FWHM) puncak yang dipilih (γ puncak utama) dan θ merupakan sudut difraksi dari data
grafik βθ pada difraktogram. Sedangkan untuk mengetahui nilai parameter
kisi ditentukan dengan menggunakan persamaan:
=
�
√�
Berdasarkan persamaan tersebut dapat diketahui nilai parameter kisi
dengan struktur kubik. Untuk parameter kisi dengan struktur kubik adalah
a=b=cdan (α= = ).
Selain itu juga dilakukan analisis dengan menggunakan spektronik infra
red (FTIR). Sepktra IR digunakan untuk mengetahui kandungan senyawa
apasaja yang berada di dalam hasil sintesis tersebut. Pembacaan spectra IR
dengan cara membandingkan antara hasil spectra IR dari amilum dengan hasil
spectra IR senyawa CdS. Dari hasil tersebut maka dapat diketahui perbedaan
antara amilum dengan senyawa CdS yang telah disintesis sebelumnya.
Analisis data dilakukan dengan menggunakan XRD, spektrometer IR,
spektrofotometer UV-Vis dan SEM. Spektrofotometer UV-Vis digunakan
23
maksimum ( maks) dan data reflektasi untuk mengetahui energi celah pita
atau nilai band gap. Dari data spektrofotometer nantinya akan didapatkan
grafik hubungan antara %R dengan panjang gelombang ( ).
Energi celah pita didapatkan dengan mengubah %R yang ada kedalam
persamaan Kubelka-Munk (F(R)) dan mengubah panjang gelombang ( )
menjadi besaran eV. Kemudian akan diperoleh grafik hubungan antara
F(R’∞ x hv)1/2 dengan eV.
Senyawa hasil sintesis juga dianalisis dengan menggunakan
SEM-EDX. Analisis SEM digunakan untuk menentukan morfologi partikel
(permukaan) dan ukuran partikel sedangkan hasil analisis EDX digunakan
untuk menentukan komposisi senyawa dari suatu sampel. Scanning
Electrone Microscope (SEM) adalah sebuah mikroskop electron yang
didesain untuk menyelidiki permukaan dari objek solid secara langsung.
SEM memiliki perbesaran 10 – 3.000.000x, depth of field 4 – 0,4 mm dan
24 BAB IV
HASIL DAN PEMBAHASAN
A. Sintesis Senyawa CdS
Nanopartikel CdS disintesis melalui metode sol-gel dengan menggunakan
amilum sebagai agen pengompleks. Agen pengompleks digunakan untuk
menghambat pertumbuhan partikel. Penelitian ini bertujuan untuk mengetahui
pengaruh metode pencampuran pada sintesis CdS sol-gel dengan menggunakan
amilum sebagai agen pengompleks. Proses pencampuran yang dipelajari pada
penelitian ini adalah penambahan agen pengompleks amilum yang dilakukan
sebelum dicampur dengan precursor S, [(NH4)2S]. Variasi agen pengompleks dan
suhu kalsinasi digunakan untuk mengetahui pengaruh terhadap CdS hasil sintesis.
Pada penelitian sebelumnya, penambahan amilum dilakukan kedalam campuran
prekursor.
Beberapa bahan yang digunakan untuk sintesis senyawa nanopartikel CdS
adalah Cd(NO3)2, (NH4)2S dan amilum. Proses pertama yang dilakukan adalah
mengencerkan senyawa Cd(NO3)2 dan (NH4)2S. Selanjutnya mengaduk terlebih
dahulu 0,1 M Cd(NO3)2 yang kemudian ditambahkan amilum dengan variasi 0,2;
0,5; 1; 2 dan 3 gram dan diaduk selama 24 jam di dalam suhu kamar. Pengadukan
ini dilakukan agar campuran larutan bersifat homogen. Setelah itu, ditambahkan
secara tetes demi tetes 0,1 M (NH4)2S dan diaduk selama 24 jam pada
suhu kamar. Proses pengadukan ini dilakukan agar larutan Cd(NO3)2 yang telah
25
sehingga semua bahan-bahan yang digunakan menjadi homogen. Reaksi yang
terjadi pada sintesis tersebut adalah sebagai berikut:
Cd(NO3)2(aq) + Amilum(s) Cd-Amilum(s) + NO3- (aq)
Cd-Amilum + NO3- + (NH4)2S CdS + NH4NO3 + Amilum
Larutan hasil pengadukan kemudian disaring untuk memisahkan filtrat dan
endapan menggunakan kertas saring kemudian dicuci menggunakan aquades dan
etanol. Endapan yang sudah disaring kemudian dipanaskan pada suhu 100°C
selama 4 jam untuk menghilangkan air dan etanol yang bersisa. Senyawa yang
dihasilkan tersebut berupa padatan berwarna kuning yang kemudian digerus untuk
dijadikan serbuk. Dari hasil dapat diketahui bahwa semakin banyak agen
pengompleks atau amilum yang digunakan maka warna dari padatan yang
dihasilkan akan semakin kuning cerah.
Berdasarkan hasil penelitian sebelumnya, yang dilakukan oleh Ria (2015)
proses sintesis yang dilakukan adalah mencampurkan Cd(NO3)2 dengan (NH4)2S
terlebih dahulu yang kemudian setelah homogen ditambahkan agen pengompleks
yaitu amilum. Hasil sintesis tersebut didapatkan padatan berwarna kuning.
B. X-Ray Diffraction (XRD)
Karakterisasi dengan X-Ray Diffraction (XRD) menggunakan sumber radiasi
CuKα, pada rentang βθ yaitu 2o sampai 90o dengan interval 0,02 dan laju 2. Senyawa
CdS yang telah dikarakterisasi dengan menggunakan X-Ray Diffraction (XRD)
26
intensitas (I) puncak spektrum kristal dan sudut difraksi (βθ). Dari data yang
dianalisis dapat diperoleh informasi berupa struktur kristal senyawa CdS.
1. Senyawa CdS tanpa amilum
Pada penelitian ini dilakukan sintesis senyawa CdS tanpa penambahan
amilum sebagai agen pengompleks. Hal ini bertujuan untuk mengetahui struktur
dan ukuran kristal dari senyawa CdS tanpa penambahan amilum. Dari karakterisasi
menggunakan X-Ray Diffraction (XRD) pada senyawa CdS tanpa menggunakan
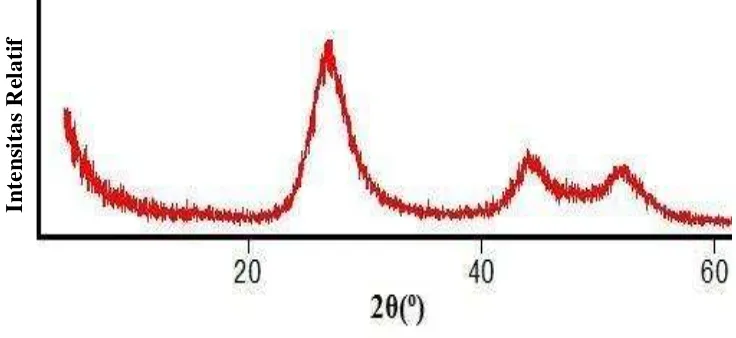
[image:43.596.118.486.338.507.2]amilum didapatkan data dan puncak sebagaimana Gambar 6.
Gambar 6. Difraktogram senyawa CdS tanpa Amilum
Berdasarkan data yang diperoleh dan grafik yang didapatkan, maka
dapat diketahui struktur dari senyawa CdS, ukuran kristal dan parameter
kisinya. Struktur kristal diketahui dengan cara membandingkan data XRD
berupa βθ atau d(A) dari hasil sintesis dengan data JCPDS yang telah
didapatkan sebelumnya. Data JCPDS standar untuk senyawa CdS adalah no.
75-1546 yang dapat dilihat pada Tabel.1
In
te
n
sitas Re
27
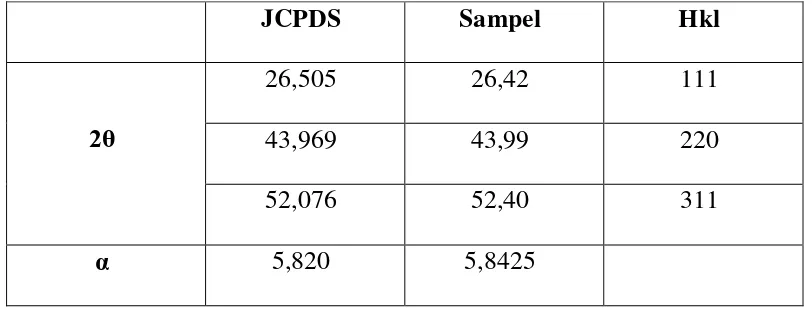
Tabel 1. Perbandingan Data JCPDS Struktur Kubik dan Data Sampel
JCPDS Sampel Hkl
2θ
26,505 26,42 111
43,969 43,99 220
52,076 52,40 311
α 5,820 5,8425
Dari data di atas dan perbandingan yang telah dilakukan maka dapat diketahui
bahwa struktur dari senyawa CdS tanpa tambahan amilum adalah kubik. Hal yang
sama telah dilaporkan oleh Barman et al. (2008) dimana pembentukan struktur CdS
yang dilakukan pada suhu kamar membentuk struktur kubik. Data tersebut
menunjukkan bahwa γ puncak yang muncul secara jelas pada βθ yaitu β6,4βo;
43,99o; dan 52;40o secara berurutan menunjukkan bidang kristal (111), (220) dan
(311) sehingga menunjukkan bahwa senyawa tersebut berbentuk kubik.
Berdasarkan data difraktogram sinar-X, dapat dihitung ukuran kristal dari
senyawa CdS menggunakan persamaan Scherer. Hasil perhitungan disajikan pada
Tabel 2.
Tabel 2. Perhitungan Ukuran Kristal
2θ B (FWHM) Cos θ λ(nm) d(nm)
26,42 0,0678 0,9735 1,5406 2,1007
43,99 0,0661 0,9272 1,5406 2,2623
52,40 0,0762 0,8972 1,5406 2,0280
Berdasarkan perhitungan dan data pada Tabel 2 diatas dapat diketahui bahwa
[image:44.596.110.516.112.267.2]28
tersebut adalah sebesar 2,1303 nm yang berarti berukuran quantum dots. Quantum
dots sendiri merupakan senyawa yang berukuran antara 2 nm- 10 nm.
2. Senyawa CdS dengan variasi amilum
Hasil dari sintesis senyawa CdS dengan variasi amilum kemudian dianalisis
menggunakan X-Ray Diffraction. Dari data yang diperoleh dan grafik yang
didapatkan, maka dapat diketahui struktur dari senyawa CdS dengan variasi
amilum, ukuran kristal dan parameter kisinya. Berdasarkan perhitungan dengan
menggunakan rumus Scherer diketahui ukuran kristalnya. Struktur dari senyawa
CdS dengan variasi amilum juga sama dengan hasil sintesis CdS tanpa amilum,
yaitu berstruktur kubik. Hasil perhitungan ukuran kristal untuk masing-masing
[image:45.596.118.506.419.529.2]variasi amilum dapat dilihat pada Tabel 3.
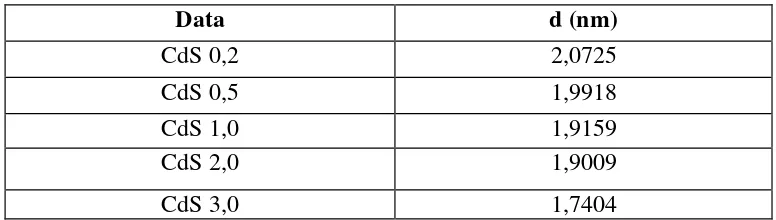
Tabel 3. Perhitungan ukuran kristal rata-rata dengan variasi amilum.
Data d (nm)
CdS 0,2 2,0725
CdS 0,5 1,9918
CdS 1,0 1,9159
CdS 2,0 1,9009
CdS 3,0 1,7404
Berdasarkan Tabel 3 diketahui semakin besar konsentrasi amilum, maka
semakin kecil ukuran kristalnya. Hal tersebut karena semakin banyak agen
pengompleks yang ditambahkan, maka pertumbuhan partikelnya semakin
terhambat. Perhitungan ukuran partikel ini didapatkan dari hasil difraktogram
29
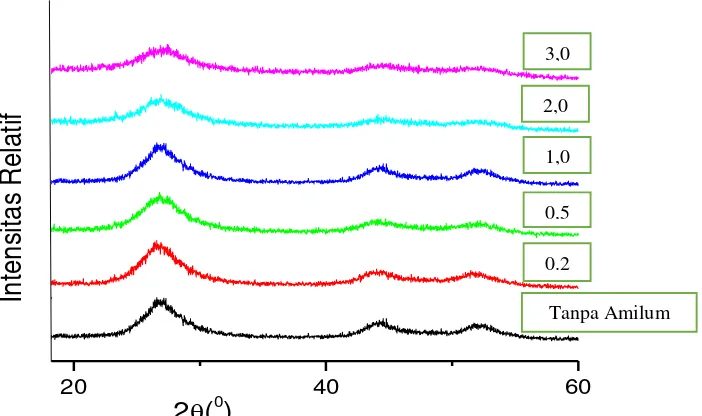
[image:46.596.144.495.85.293.2]
Gambar 7. Difraktogram XRD Senyawa dengan Penambahan Amilum
Gambar 7 menunjukkan struktur CdS yang sama dan tidak menunjukkan
perbedaan pola puncak yang signifikan. Proses pencampuran dengan penambahan
amilum terhadap campuran precursor Cd dan S menghasilkan struktur yang
berbentuk heksagonal (Ria, 2015). Penelitian Ria diketahui bahwa perbedaan
metode percampuran dapat mempengaruhi struktur senyawa CdS.
Pada Tabel 3 diketahui bahwa ukuran terkecil dari senyawa CdS dengan
penambahan amilum sebanyak 3 gram. Setelah diketahui senyawa dengan ukuran
terkecil kemudian dilakukan kalsinasi dengan variasi suhu 200°C, 250°C dan
300°C. Kalsinasi dilakukan untuk mengetahui karakter hasil sintesis CdS yang
optimum. Hasil kalsinasi dari masing-masing senyawa kemudian dilakukan
analisais menggunakan XRD untuk mengetahui ukuran kristal yang paling sesuai,
yaitu yang paling kecil. Dari hasil analisis menggunakan XRD maka didapatkan
difraktogram seperti pada Gambar 8.
20 40 60
amilum
2(0)
30
0 20 40 60 80 100
2-theta
[image:47.596.94.481.88.347.2]200 C 250 C 300 C
Gambar 8. Difraktogram Senyawa CdS Setelah Kalsinasi
Gambar 8 menunjukkan bahwa senyawa CdS hasil variasi kalsinasi
[image:47.596.111.519.461.546.2]memiliki struktur yang sama, yaitu kubik.
Tabel 4. Parameter kisi senyawa CdS hasil kalsinasi
Suhu α
200°C 5,8563
250°C 5,8897
300°C 5,8675
Dari hasil analisis ini kemudian dilakukan perhitungan untuk mendapatkan
ukuran kristal. Ukuran kristal didapatkan dengan menggunakan rumus Scherer.
In
ten
sitas
R
elati
31
Tabel 5. Perhitungan ukuran kristal rata-rata dengan variasi kalsinasi
Data d (nm)
200°C 2,3169
250°C 3,7824
300°C 14,740
Tabel 6 menunjukkan bahwa semakin besar suhu kalsinasi maka ukuran
kristalnya semakin besar. Ukuran kristal pada senyawa CdS dengan suhu kalsinasi
200°C adalah sebesar 2,31 nm. Selanjutnya untuk senyawa CdS dengan suhu
kalsinasi 250°C diketahui ukuran kristalnya adalah 3,78 nm dengan warna
senyawa yang telah dikalsinasi berwarna kuning pekat mendekati keabu-abuan..
Kalsinasi terakhir adalah variasi kalsinasi dengan suhu 300°C. Hasil kalsinasi ini
kemudian dilakukan analisa XRD dan diketahui bahwa ukurannya adalah 14,79
nm. Hal ini menunjukkan bahwa semakin besar suhu kalsinasi maka ukuran
kristalnya semakin besar. Ketiga variasi suhu kalsinasi maka dipilih senyawa yang
memiliki kondisi optimum, yaitu ditandai dengan warna senyawa yang masih
berwarna kekuningan dan ukuran kristal yang relatif kecil. Ketiga suhu kalsinasi
didapatkan kondisi optimum yaitu pada suhu 250°C. Difraktogrm pada suhu 250oC
diketahui masih mengandung CdS murni dan semakin kristalin. Sedangkan pada
difraktogram suhu 300oC diketahui sudah terjadi perubahan fasa. Diketahui pada
suhu 300oC ditemukan CdO pada βθ γγ,41 dan 70, λγ. Dengan bidang hkl (111
32 C. Analisis Spektrofotometer IR
Karakterisasi hasil sintesis menggunakan spektrometer IR bertujuan untuk
mengidentifikasi keberadaan senyawa amilum sebagai agen pengompleks yang
terdapat pada hasil sintesis CdS. Hasil spektrum IR dari senyawa amilum dapat
[image:49.596.111.511.231.571.2]dilihat pada Gambar 9.
Gambar 9. Spektrum IR dari Amilum
Spektrum IR Gambar 9 menunjukkan bahwa di dalam senyawa amilum
tersebut terdapat gugus -OH pada daerah serapan 3448,72 cm-1, kemudian pada
daerah 2981,80 cm-1 serapan untuk gugus alkana, gugus alkena terdapat pada
daerah serapan 1651,07 cm-1 dan yang teakhir terdapat serapan untuk gugus
33
CdS menggunakan amilum sebagai agen pengompleks dapat dilihat pada Gambar
[image:50.596.115.521.115.395.2]10.
[image:50.596.111.523.139.639.2]Gambar 10. Spektrum IR Hasil Kalsinasi pada Suhu 200°C
34
Gambar 10 dan 11 menunjukkan senyawa CdS hasil kalsinasi. Gambar 10
menunjukkan hasil kalsinasi pada suhu 200oC, sedangkan Gambar 11 menunjukkan
hasil kalsinasi pada suhu 300oC. Interpretasi senyawa IR dari hasil kalsinasi pada
[image:51.596.113.515.207.348.2]suhu 200oC dan 300oC senyawa CdS dapat dilihat pada Tabel 6.
Tabel 6. Perbandingan serapan amilum, kalsinasi 200oC dan 300oC
Bilangan Gelombang (cm-1)
Gugus Fungsi Amilum Kalsinasi 200oC Kalsinasi 300oC
3448,72 3448,72 3456,44 -OH
2981,80 - - C-C
1651,07 - - C=C
1157,29 1111,00 1111,00 C-O-C
Senyawa CdS yang telah dikalsinasi kemudian dianalisis dengan
menggunakan spektrofotometer IR. Analisis ini dilakukan untuk mengetahui
kandungan amilum dalam senyawa CdS setelah proses kalsinasi. Hasil analisis
senyawa yang telah dikalsinasi pada suhu 200°C dan 300°C menunjukkan bahwa
senyawa hasil kalsinasi masih mengandung amilum. Hal ini diketahui dari spektrum
IR yaitu masih ada puncak-puncak yang menunjukkan gugus fungsi dari amilum.
Akan tetapi jumlah atau intensitas dari amilum cenderung berkurang. Pada
kalsinasi 200°C dan 300°C masih terdapat serapan gugus –OH pada daerah serapan
34478,42 cm-1 dan 3456,44 cm-1. Sedangkan pada daerah serapan 1110 cm-1 pada
kalsinasi 200°C dan 300°C masih menunjukkan adanya serapan gugus C-O-C.
Kedua puncak spektrum IR hasil kalsinasi hampir mirip, yang menyatakan bahwa
35 D. Analisis UV-Vis
Senyawa CdS yang telah dikalsinasi pada suhu 250°C dilakukan
karakterisasi menggunakan spektroskopi UV-Vis untuk mengetahui absorbansi
atau kemampuan material untuk menyerap cahaya dan energi celah pita. Serbuk
hasil kalsinasi sebelum dianalisis perlu dilakukan preparasi sampel pada kaca
preparat dengan cara menempelkan serbuk CdS yang telah dilarutkan dengan
sedikit etanol pada kaca preparat. Kaca preparat yang telah terlapis sampel
dipanaskan selama 30 menit dengan suhu 80oC untuk menguapkan etanol yang
digunakan sebagai pelarut.
Pada penelitian ini pengukuran dilakukan pada panjang gelombang 200 –
800 nm. Kisaran radiasi untuk UV adalah 180 – 380 nm sedangkan untuk visibel
[image:52.596.151.454.422.706.2]adalah 380 – 780 nm (Fessenden & Fessenden, 1997). Hasil absorbansi variasi amilum sebelum dilakukan kalsinasi ditunjukkan Gambar 12.
36 0 0.0002 0.0004 0.0006 0.0008 0.001
1.5 1.6 1.7 1.8 1.9 2 2.1 2.2 2.3
FR’∞ x h v 1/2 eV
[image:53.596.100.525.233.398.2]Gambar 12 menunjukkan hasil absorbansi UV-Visibel senyawa CdS variasi amilum. Berdasarkan Gambar 12 dapat diketahui nilai energi celah pita. Data absorbansi dari spektra senyawa CdS digunakan untuk mengetahui perubahan transisi elektronik pada daerah UV maupun sinar tampak. Berikut merupakan Tabel 7 data absorbansi yang diperoleh.
Tabel 7. Absorbansi Senyawa CdS Variasi Amilum.
Sampel λ (nm) Ket
CdS
273
UV 306
510 Visibel
CdS 0,5 312 UV
397 Visibel
CdS 1,0
312
UV 341
411 Visibel
CdS 2,0 361 415 Visibel UV
Berdasarkan data absorbansi, maka dapat diketahui energi celah pita dari
[image:53.596.125.474.481.697.2]setiap variasi amilum. Nilai energi celah pita setiap variasi amilum ditunjukkan
Gambar 13-16.
37 0 0.0002 0.0004 0.0006 0.0008 0.001
1.5 1.6 1.7 1.8 1.9 2 2.1 2.2 2.3
F R’∞ x h v 1/2 eV 0 0.0002 0.0004 0.0006 0.0008 0.001
1.5 1.6 1.7 1.8 1.9 2 2.1 2.2 2.3
[image:54.596.135.492.81.339.2]FR ’∞ x h v 1/2 eV
Gambar 14. Grafik Energi Celah Pita Senyawa CdS amilum 0,5 gram
[image:54.596.135.488.366.592.2]38 0 0.0002 0.0004 0.0006 0.0008 0.001
1.5 1.6 1.7 1.8 1.9 2 2.1 2.2 2.3
[image:55.596.138.488.83.298.2]FR ’∞ x h v 1/2 eV
Gambar 16. Grafik Energi Celah Pita Senyawa CdS amilum 2,0 gram
Berdasarkan keempat grafik diatas terlihat perbedaan yang tidak terlalu
signifikan. Gambar 13 dan 14 menunjukkan nilai energi celah pita yang hampir
sama sebesar 1,98 eV dan 1,96 eV. Sedangkan pada Gambar 15 dan Gambar 16
menunjukkan nilai energi celah pita sebesar 2,14 eV.
Untuk energi celah pita masing-masing dari sampel senyawa CdS dapat
dilihat pada Tabel 8.
Tabel 8. Nilai energi celah pita variasi amilum
Sampel Nilai energy celah pita (eV)
CdS tanpa amilum 1,98
CdS 0,5 1,96
CdS 1,0 2,14
CdS 2,0 2,14
Nilai energi celah pita dari Tabel 8 menunjukkan bahwa variasi amilum
[image:55.596.111.514.518.662.2]39
200 300 400 500 600 700 800 0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 Abs nm CdS
dilakukan pengukuran UV-Visibel. Gambar 17 merupakan absorbansi senyawa
[image:56.596.184.452.127.358.2]CdS hasil kalsinasi.
Gambar 17. Spektrum UV-Vis Senyawa CdS Setelah Kalsinasi
Data absorbansi dan spektra senyawa CdS digunakan juga untuk
mengetahui perubahan transisi elektronik pada daerah UV. Tabel 9 merupakan data
absorbansi senyawa CdS setelah dilakukan kalsinasi yang diperoleh.
Tabel 9. Absorbansi Senyawa CdS Variasi Amilum.
Sampel λ (nm)
Visibel UV
CdS 341
267 410
Berdasarkan data diatas maka dapat ditentukan perubahan transisi
elektronik pada daerah UV. Pada umumnya, tipe transisi n→π* terjadi pada daerah
maks 401 nm – 700 nm. Pada senyawa CdS yang telah dikalsinasi pada suhu 250
[image:56.596.112.512.497.571.2]40 0 0.0002 0.0004 0.0006 0.0008 0.001
1.5 1.6 1.7 1.8 1.9 2
F R’∞ x h v 1/2 eV
→π* terjadi pada daerah 200 nm – 400 nm. Senyawa CdS pada kalsinasi 250 oC
memberikan nilai maks sebesar 267 nm dan 341 nm.
Energi celah pita merupakan besarnya energi yang digunakan untuk
melepaskan elektron dari pita valensi ke pita konduksi. Energi celah pita
memengaruhi kemampuan fotokatalitik suatu katalis, sehingga sangat penting
dilakukan pengukuran. Untuk mengetahui besar energi celah pita yang terdapat
pada sampel senyawa CdS digunakan data reflektansi yang diperoleh. Metode yang
digunakan dalam menentukan energi celah pita adalah metode spektrofotometri
UV-Vis Diffuse Reflektansi.
Nilai energi celah pita diperoleh dengan mengubah besaran %R ke dalam
faktor Kubelka-Munk (F(R’∞ x hv)1/2) dan besaran panjang gelombang diubah
menjadi besaran eV. Selanjutnya, diperoleh kurva persamaan garis lurus. Besarnya
energi celah pita merupakan perpotongan sumbu x dari persamaan garis yang
[image:57.596.133.464.456.659.2]diperoleh seperti Gambar 18.
41
Gambar 18 menunjukan nilai energi celah pita yang dihasilkan oleh sampel
pada kalsinasi 250°C yaitu sebesar 1,72 eV. Penelitian yang dilakukan oleh Ria
(2015) menunjukkan energi celah pita pada berbagai konsentrasi senyawa CdS
sebesar 2,1 – 2,3 eV. Hal ini menunjukkan perbedaan energi celah pita antara
senyawa CdS sebelum dikalsinasi dengan sesudah dikalsinasi. Perbedaan energi
celah pita ini menunjukkan bahwa metode pencampuran dan variasi suhu
kalsinasi berpengaruh terhadap nilai energi celah pita.
E. Analisis SEM-EDX
Scanning Electron Microscopy – Electron Dispersive X-Ray Analyser
(SEM-EDX) digunakan untuk menganalisis morfologi permukaan dan komposisi
senyawa dari suatu sampel. Sampel yang dianalisa adalah senyawa CdS yang telah
dikalsinasi pada suhu 250°C. Pada analisis SEM kali ini, dilakukan perbesaran
mulai dari 500 X hingga 20000 X. Hasil SEM senyawa CdS menunjukkan bahwa
Kristal senyawa ini memiliki morfologi yang tidak homogen. Perbesaran elektron
[image:58.596.114.512.498.651.2]micrograph senyawa CdS berturut-turut ditunjukkan pada Gambar 19.
Gambar 19. Hasil SEM senyawa CdS perbesaran (a) 3000x ,(b) 10000x
42
Dari Gambar 19 maka dapat diketahui bahwa pada senyawa CdS yang telah
dikalsinasi memiliki ukuran partikel sebesar 0,683 - 1, 897 µm. Karakterisasi
dengan EDX dapat digunakan untuk mengetahui prosentase unsur Cd dan S yang
ada di dalam senyawa CdS. Spektra EDX dari senyawa CdS yang telah dikalsinasi
[image:59.596.119.415.213.431.2]dapat dilihat pada Gambar 20.
Gambar 20. Spektra EDX senyawa CdS
Dalam penelitian ini, hasil karakterisasi EDX menunjukkan bahwa senyawa
CdS mengandung unsur S sebesar 16,94% dan unsur Cd sebesar 83,06%. Serta
menunjukkan persentase atom untuk S sebesar 41,68% dan Cd sebesar 58,32%.
Sehingga hasil karakterisasi EDX menunjukkan perbandingan atom Cd dan S yaitu
sebesar 0,40 : 0,28. Hal ini tidak sesuai dengan perhitungan awal, yaitu 1:1.
Kemungkinan yang terjadi adalah S menguap dan bereaksi dengan oksigen,
43 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Berdasarkan hasil penelitian yang diperoleh, maka dapat ditarik kesimpulan
sebagai berikut.
1. Metode pencampuran dalam proses sintesis berpengaruh terhadap struktur CdS
hasil sintesis. Pengaruh tersebut terjadi dengan adanya perubahan struktur
senyawa dan ukuran kristal. Diketahui bahwa semakin banyak penambahan
amilum maka ukuran kristal semakin kecil.
2. Variasi suhu kalsinasi berpengaruh terhadap struktur CdS hasil sintesis.
Pengaruh tersebut terjadi pada ukuran kristal, energi celah pita dan komposisi
atom. Semakin tinggi suhu kalsinasi maka ukuran kristalnya semakin besar.
Setelah dikalsinasi energi celah pita juga semakin kecil.
B. Saran
Penelitian ini masih memerlukan pengembangan yang lebih luas dan masih
berada dalam lingkup yang sederhana. Saran untuk penelitian lebih lanjut
sebagai berikut.
1. Perlu dilakukan penelitian lebih lanjut untuk mempelajari sintesis senyawa
CdS dengan metode yang berbeda.
2. Perlu dilakukan penelitian lebih lanjut bahwa senyawa CdS setelah
dikalsinasi menghasilkan ukuran kristal yang besar tetapi memiliki energi celah
44
DAFTAR PUSTAKA
Adem. U. (2003). Preparation of BaxSr1-xTiO3 Thin Films By Chemical Solution
Deposition and Their Electrical Charaterization. Thesis. The Departement of
Metallurgical & Materials Engineering. The Middle East Technical University.
Al-Juaid, F., Merazga, A., Abdel-Wahab, F. & Al-Amoudi, N. (2012). ZnO Spin-
Coating of TiO2 Photo-Electrodes to Enhance The Efficiency of Dye-
Sensitized Solar Cells. World Journal of Condensed Matterial Physics
(2). 192-196.
Al-Tememee, Nathera A., N. M. Saeed, S. M. A. Al-Dujayli, B. T. Chiad. (2012).
The Effect of Zn Concentration on the Optical Properties Of Cd10xZnxS Films
for Solar Cells Application. Advances in Material Physics and Chemistry 2,
69-74.
Anna P., Titin S. (1994). Dasar-dasar Biokimia. Jakarta: UI Press.
Azmi, Ardita N. (2014). Preparasi Senyawa Nanokomposit N-TiO2/CdS Dengan
Metode Chemical Bath Deposition. Skripsi. Yogyakarta: FMIPA
Universitas Negeri Yogyakarta.
Bansal. P., Jaggi N. & Rohilla S. K. (2012). “Green” Synthesis of CdS
Nanoparticles and Effect of Capping Agent Concentration on Crystallite
Size. Research Journal of Chemical Scienes 2(8). 69-71.
Bird, T. (1987). Kimia Fisikia Untuk Universitas. Jakarta : PT Gramedia.
Barman, J., Sarma, K. C., Sarma, M., & Sarma, K. (2008). Structural and Optical
Studies of Chemically Prepared CdS Nanocrystalline Thin Films. Indian
Journal of Pure and Applied Physics (46). 339-343.
Dachriyanus, Dr. (2004). Analisis Struktur Senyawa Organik Secara Spektroskopi.
Padang: Andalas University Press. 8-9.
.Djamas, Djusmaini. (2010). Penentuan Microstructure Lapisan Tipis CdS
Menggunakan X-Ray Diffractrometer. EKSAKTA. (1), 9-19.
Fessenden, R. J., & J. S. Fessenden. (1997). Kimia Organik Edisi Ketiga.
45
Goldstein, Joseph. (2003). Scanning Electron Microscopy and X-Ray
Microanalysis. The Journal of Scanning Microscopies 27(4): 215-216.
Hasyim Asy’ari, Jatmiko, Angga. (β01β). Intensitas Cahaya Matahari Terhadap
Daya Keluaran Panel Sel Surya. Simposium Nasional. Universitas
Muhammadiyah Surakarta.
Hsu Yung-Jung, Shih-Yuan Lu. (2004). Additive Effects on Chemical Vapor
Deposition of CdS. Hsu et al., Aerosol and Air Quality Research 4(1). 17-26.
Ichimura,. M, Kazuki,. T, Eisuke,. A. (2001). Photochemical Deposition of Se and
CdSe Films From Aqueos Solution. Journal Thin Solid Films 384(2):
157-159.
Iriani, Y. (2009). Penumbuhan Lapisan Tipis Barium Stronrium Titanat (Ba
1-xSrxTiO3) dengan Berbagai Doping Untuk Aplikasi Memori. Disertasi.
Program Studi Ilmu Material Universitas Indonesia.
Ismunandar. (2004). Padatan oksida logam: struktur, sintesis dan sifat-sifatnya.
Bandung : Departemen Kimia FMIPA ITB.
Jauhari, Muhammad. (2007). Potensi Industri Pengolahan Batubara Cair.
Economic Review. No. 208.
Jaya, D.M.N. (2005). A Study on the Growth and Structure of Titania Nanotubes.
Journal of Material Research 19(2): 417-422.
Jararatnam, J., David Koh. (2010). Buku Ajar Praktik Kedokteran Kerja. Buku
Kedokteran EGC: Jakarta.
Jun, H. K., Careem, M. A. & Arof, A. K. (2013). Quantum Dot-Sensitized Solar Cells-Perspective and Recent Developments: A Review of Cd
Chalcogenide Quantum Dots as Sensitizers. Renewable and Sustainable
Energy Reviews (22). 148-167.
Kadash, E. A., AL Hattami, A. A., Rathod, J. R., Patel, K. D. & Pathak, V. M. (2014). Synthesis and Caracterization of Cadmium Sulfide Crystals Grown
By DVT Technique. International Journal of Pure Applied Sciences and
Technology 22(1). 18-26.
Lee, J. Hyeong, Woo-Chang Song, Jun-Sin Yi, Kea-Joon Yang, Wun-Dong Han,
Joon Hwang. (2003). Growth and Properties of the Cd1-xZnxS Thin Films for
Solar Cell Application. Elsevier. Thin Solid Films 431-432, 349-353.
Liu Fangyang, Yanqing Lai, Yexiang Liu. (2010) Characterization of Chemical Bath Deposited CdS Thin Films at Different Deposition Temperature.
46
Nakatani, K., Kento, H., Yuki, K., Yuuki, N., Haruho, A., Takashi, O., Masahiko, M. & Kurodo-Sona, T. (2015). Synthesis, Crystal Structure, and Electroconducting Properties of a ID Mixed-Valence Cu(I)-Cu(II) Coordination Polymer With a Dicyclohexyl Dithiocarbamate Ligand.
Crystals 5(2). 215-225.
Nwokocha, L. M., (2009). A comparative study of some properties of cassava
(Manihot esculenta, Crantz) Carbohydrate Polymers