12 BAB II
TINJAUAN PUSTAKA
2.1 Ulkus Peptikum
Ulkus peptikum adalah ulkus yang terjadi meluas sampai dibawah epitel pada mukosa bagian saluran pencernaan misalnya, lambung atau usus (duodenum atau jejunum). Kerusakan mukosa yang tidak meluas sampai kebawah epitel disebut sebagai erosi, walaupun sering dianggap juga sebagai “ulkus”. Sekitar 2 hingga 3% dari semua ulkus lambung mengalami perforasi dan menyebabkan sekitar 65% kematian akibat penyakit ulkus peptikum (Price dan Wilson, 2006).
Lambung dilindungi terhadap faktor iritan oleh lapisan mukus, epitel, tetapi beberapa faktor iritan seperti makanan, minuman dan obat antiinflamasi non steroid (OAINS), alkohol dan empedu yang dapat menimbulkan defek lapisan mukus dan terjadi difusi balik ion H+, sehingga timbul tukak lambung (ulkus lambung). Asam lambung (HCl) adalah salah satu faktor terutama yang menginduksi penyakit ulkus lambung. Telah dilaporkan bahwa kira-kira 50% pasien yang menderita ulkus lambung merupakan hipersekresi asam dan pepsin. Disamping itu faktor lain seperti kuman Helicobacter pylori dan Sindroma Zollinger-Ellison juga merupakan penyebab terjadinya ulkus lambung. Sindroma Zollinger-Ellison adalah suatu sindroma yang disebabkan oleh tumor pankreas mengeluarkan gastrin dalam jumlah yang banyak. Gastrin yang berlebihan ini merangsang lambung untuk menyekresi sejumlah besar HCl dan pepsin, yang memicu terjadinya ulkus (Tarigan, 2006 ; Amandeep, et al., 2012).
13
atau rekurensi tukak, dan mencegah komplikasi. Obat-obat yang digunakan untuk terapi ulkus lambung yaitu obat golongan antasida yang mengandung aluminium dan magnesium, obat penangkal kerusakan mukus misalnya sukralfat, obat golongan antagonis reseptor H2 seperti ranitidin, dan obat golongan proton pump inhibitor (PPI) seperti omeprazol (Tarigan, 2006).
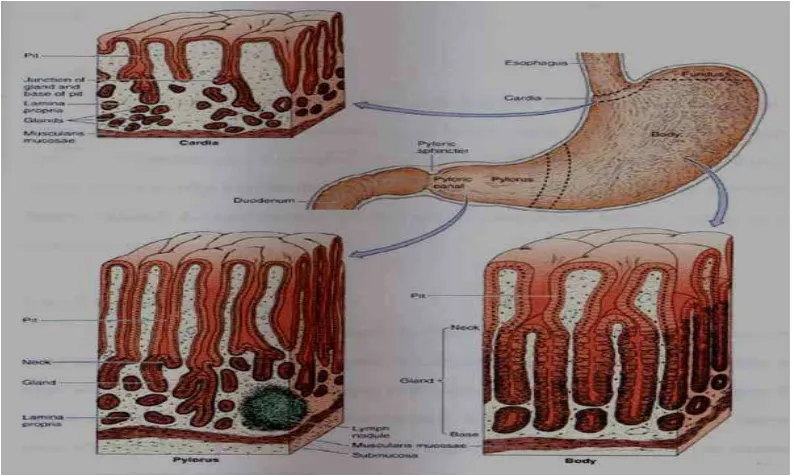
2.2 Lambung
Lambung secara anatomi dibagi atas 4 bagian, yakni: kardia, fundus, korpus dan
pilorus. Fundus dan korpus memiliki struktur histologis yang identik (Gambar 2.1).
Berdasarkan histologi, dinding saluran pencernaan terdiri dari empat lapisan yaitu sebelah
dalam sekali lapisan mukosa, lalu berturut – turut ke arah luar lapisan submukosa, lapisan
muskularis (otot) dan lapisan yang paling luar sekali adalah lapisan serosa atau
adventisia. Setiap lapisan terdiri atas beberapa komponen yang mempunyai struktur yang
berbeda–beda (Junqueira dan Carneiro, 2005)
14 2.2.1 Mukosa
Mukosa lambung terdiri dari epitel permukaan yang mengalami invaginasi dengan berbagai kedalaman di dalam lamina propria, membentuk gastric pits. Lamina propria dari lambung terdiri dari jaringan penghubung yang jarang yang diselilingi dengan sel-sel otot polos dan limfoid. Lapisan otot yang memisahkan mukosa dari submukosa adalah mukosa muskularis. Stres dan faktor-faktor psikosomatik lain; konsumsi substansi seperti aspirin, etanol, makanan yang hiperosmolar, dan beberapa mikroorganisme misalkan Helicobacter pylori dapat mengganggu permukaan epitel ini dan menyebabkan ulkus (Junqueira dan Carneiro, 2005).
Membran mukosa terdiri dari suatu lapisan epitel yang ditutupi oleh mukus. Mukus terutama berfungsi sebagai suatu pelicin untuk mengurangi gaya gesekan dan sebagai suatu lapisan pelindung terhadap bahan-bahan yang berbahaya. Di lapisan mukosa terdapat 3 jenis sel yaitu sel goblet, parietal dan sel chief. Sel-sel goblet yang terletak dalam epithelium merupakan kelenjar yang mengeluarkan mukus atau lendir untuk menjaga lapisan terluar sel agar tidak rusak karena enzim pepsin dan asam lambung. Sel parietal untuk memproduksi
asam lambung yang berguna dalam pengaktifan enzim pepsin. Sel chief
memproduksi enzim pepsin dalam bentuk tidak aktif agar enzim tersebut tidak
mencerna protein yang dimiliki oleh sel tersebut yang dapat menyebabkan
kematian pada sel tersebut. Mukus terutama terdiri dari air (95%), garam-garam
15
Mucin adalah suatu glikoprotein yang terdiri dari rantai oligosakarida yang terikat pada suatu inti protein. Seperempat dari inti protein adalah glikosilat yang memberikan karakteristik seperti gel. Sisanya yang nonglikosilat berpautan silang (cross linking) melalui ikatan disulfida diantara molekul mucin. Mukus adalah bermuatan negatif karena adanya sialic acid (pka=2,6) dan ester sulfat pada ujung dari rantai samping oligosakarida. Densitas muatan yang tinggi disebabkan muatan negatif yang menghasilkan bioadhesi. Rantai samping oligosakarida terdiri dari residu 8-10 monosakarida dari lima jenis yang berbeda yaitu L-fukosa, D-galaktosa, N-asetil-D-glukosamin, N-asetil-D-galaktosamin, dan sialic acid. Asam amino yang terutama dalam blok protein yang bercabang adalah proline, serine dan threonine (Deghan dan Khan, 2009; Swetha, et al., 2012).
2.2.2 Kardia
Kardia merupakan pita sirkuler sempit pada peralihan antara esophagus dan lambung. Lamina proprianya mengandung kelenjar-kelenjar kardia tubular simpleks bercabang. Bagian terminal kelenjar-kelenjar ini seringkali bergelung dan sering mempunyai lumen yang besar. Sel-sel sekresi mereka menghasilkan mucus dan lisozim (enzim yang berfungsi menyerang dinding bakteri). Kelenjar-kelenjar ini strukturnya sama seperti Kelenjar-kelenjar kardia bagian terminal esophagus. 2.2.3 Korpus dan Fundus
16
parietal (oksintik). Bagian basis kelenjar terdiri dari sel parietal, sel zimogen dan sel enteroendokrin.
2.2.4 Cairan Lambung (Gastric Juice)
Cairan lambung adalah campuran heterogen dari cairan jernih, flocculent, dan mukus jernih. Konstituen utama dari cairan lambung adalah asam hidroklorida, protease lambung (pepsin dan gastricsin), faktor hematopoietik, hormon lambung, dan mucosubstance (aminopolysaccharida, mukopoliuronida, mukoid, dan mukoprotein). Protease lambung yang utama adalah pepsin dan gastricsin, pepsinogen adalah precursor yang diubah menjadi pepsin aktif oleh HCl bebas dan oleh proses autokatalitik (Perigard, 2000).
2.2.5 Fisiologi Sekresi Lambung
Asam klorida dan pepsin produk yang paling utama dapat menimbulkan kerusakan mukosa lambung. Asam lambung disekresi oleh sel-sel parietal dalam lambung. Ada dua jenis sekresi asam yaitu basal dan akibat perangsangan. Sekresi asam basal dalam pola sirkadia, terjadi terus menerus dan tertinggi terjadi pada malam hari (kira-kira jam 10 malam sampai tengah malam) dan terendah pada pagi hari ( jam 4 sampai 8 pagi). Pola sekresi asam ini bertanggung jawab bagi salah satu karakteristik dari penyakit ulkus lambung dan duodenum, yang mana rasa sakit terjadi pada malam hari ketika sekresi asam tinggi dan tanpa dinetralkan oleh makanan. Sekresi basal sebagian besar dikontrol oleh nervus fagus dan neurotransmitter asetil kolin (Gregory, 2000; Tolman, 2000)
17
perangsangan nervus fagus. Fase gastrik terjadi ketika makanan masuk kedalam lambung, komponen sekresi adalah kandungan makanan yang terdapat di dalamnya (asam amino dan amino bentuk lain) yang secara langsung merangsang sel G untuk melepaskan gastrin yang selanjutnya mengaktifasi sel-sel parietal melalui mekanisme langsung maupun meknisme tidak langsung. Peregangan dinding lambung memicu pelepasan gastrin dan produksi asam.
Fase terakhir (fase intestinal) sekresi asam lambung dimulai pada saat makanan masuk kedalam usus dan diperantarai oleh adanya peregangan usus dan pencampuran kandungan makanan yang ada (Tarigan, 2006).
Gambar 2.2 Mekanisme sekresi asam lambung dan faktor-faktor yang mempengaruhi (Tarigan, 2006)
(sel-18
sel parietal) maupun tidak langsung (menurunkan pelepasan histamin dari sel-sel seperti enterokromafin (ECL) dan menimbulkan pelepasan gastrin melalui sel-sel G. Faktor rangsang tambahan yang dapat mengimbangi sekresi asam, antara lain neural (sentral dan perifer) dan hormonal (sekretin dan kolesistokinin). Dalam keadaan fisiologi fase-fase tersebut berlangsung secara bersamaan (Gambar 2.2) (Tarigan, 2006).
Dalam keadaan puasa, pH cairan lambung sangat asam (1 dan 2) sehingga setiap mukosa lambung yang tidak terproteksi akan cepat mengalami auto-digesti.
Pertahanan mukosa terhadap serangan asam terdiri :
a. Barrier mukus merupakan pertahanan yang penting. Sel yang melapis epitel permukaan lambung mensekresi cairan kental glikoprotein netral yang membentuk satu lapis mukus tidak bergerak pada permukaan. b. Permukaan epitel merupakan pertahanan kedua; untuk fungsinya yang
tepat memerlukan integritas kedua aspeks membran plasma sebagai barrier terhadap transfer ion, dan fungsi metabolik seluler termasuk produksi bikarbonat. Ulserasi dapat timbul akibat destruksi atau hilangnya barier mukosa, atau hilangnya integritas epitel permukaan (Underwood, 1994)
2.3 Sistem Pelepasan Obat Sustained Release
19
jumlah obat dalam trayek terapeutik untuk waktu yang lama dalam darah dan dengan demikian lama kerja obat menjadi singkat. Sistem pelepasan extended-release disebut juga sustained extended-release dan slow-extended-release. Keuntungan sistem pelepasan lambat (sustained release) yaitu akan meningkatkan keutungan terapeutik, mengurangi efek samping obat dan biaya pengobatan, dan pengelolaan penyakit kronis akan menjadi lebih baik (Rajabi-Siahboom, et al., 2013).
Sustained release (SR) menguraikan suatu pelepasan yang lambat dari bahan obat dari suatu sediaan untuk mempertahankan respon terapeutik dalam waktu yang panjang yaitu 8-12 jam dan kriteria sediaan SR yaitu jumlah obat yang terdisolusi selama 3 jam adalah 20-50% untuk 6 jam adalah 45-75% dan 12
jam ≥ 75% (Murthy dan Sellasie, 1993).
Formulasi sustained release menggabungkan satu atau lebih dari pendekatan teknologi yang umum berikut ini (Rajabi-Siahboomi, et al., 2013):
1. Sistem matriks. Matriks dapat digambarkan sebagai zat pembawa padat inert yang didalamnya obat disampur secara merata. Obat dimasukkan sebagai partikel-partikel terdispersi atau terlarut dalam matriks. Suatu matriks dapat dibentuk secara sederhana dengan mengempa atau menyatukan obat dengan bahan matriks bersama-sama. Sistem ini terdiri dari satu atau lebih bahan yang mengontrol pelepasan dengan obat terdispersi dalam matriks. Berdasarkan sifat dari bahan yang mengontrol kecepatan pelepasan obat dapat dibagi 2 yaitu:
20
metil sellulosa, hidroksietil selulosa, hidroksipropil metilselulosa, natrium karboksimetilselulosa, natrium alginat, xanthan gum dan karbopol.
b. Sistem matriks yang tidak larut: obat terdispersi dalam suatu polimer yang tidak larut dalam air atau lilin; pelepasan obat terjadi misalnya cairan lambung permeasi ke matriks dan melarutkan obat.
2. Sistem reservoir: Suatu unit yang mengandung obat (inti) ditutupi oleh suatu penyalut sawar polimerik. Sistem ini terdiri dari:
a. Sistem diffusi sederhana, suatu inti yang mengandung obat dikelilingi oleh suatu penyalut polimer yang tidak larut dalam air. Pelepasan obat tercapai oleh difusi obat melalui penyalutan.
b. Sistem osmotik mengandung bahan osmotik dalam inti obat yang disalut. Pelepasan obat terjadi melalui suatu lubang dalam lapisan penyalutan disebabkan suatu gradient tekanan osmosa yang dihasilkan oleh masuknya cairan lambung kedalam inti.
Bahan-bahan yang digunakan untuk matriks sistem pelepasan lambat (sustained release) yaitu (Rajabi-Siahboomi, et al., 2013):
a. Matriks lilin meliputi lilin karnauba, fatty alcohol, gliserol palmitostearat, stearil alkohol, aluminium monostearat, dan gliserol monostearat. Bahan ini dapat digunakan sendiri atau kombinasi dengan polimer hidrofilik.
21
c. Polimer yang larut dalam air yang membentuk matriks yang inert meliputi etil selulosa, metilakrilat, metilmetakrilat, dan polivinil asetat. d. Polimer yang digunakan dalam formulasi matriks hidrofilik meliputi
hidroksipropilmetilselulosa, natrium karboksimetilselulosa, natrium alginat, kitosan, karbomer, dan karagenan.
2.3.1 Pelepasan Obat dari Matriks
Kinetika pelepasan obat dapat dipengaruhi oleh banyak faktor seperti pengembangan polimer, erosi polimer, kelarutan obat atau karakteristik difusi, distribusi obat dalam matriks, perbandingan obat dan polimer dan sistem geometri dari matriks (silinder maupun bulat). Selama mengalami sentuhan dengan cairan (air atau media fisiologis), polimer matriks mengembang dan pelarutan obat dapat terjadi. Seketika setelah konsentrasi pelarut di sekitarnya melebihi ambang batas, ikatan polimerik terlepas sehingga terjadi perubahan polimer dari bentuk seperti kaca ke bentuk seperti karet menghasilkan peningkatan yang besar terhadap mobilitas rantai-rantai polimer sehingga lubang-lubang jaring polimer bertambah besar dan obat tersebut dapat larut dan berdifusi melalui lapisan gel. Secara singkat pelepasan obat dari sistem matriks dapat diamati dari tiga bidang utama yang muncul selama proses penglepasan yaitu bidang yang terkikis, bidang yang mengembang dan bidang yang mengalami difusi.
22
rendah disebabkan relaksasi dari rantai polimer sehingga obat dapat keluar dari polimer yang seperti karet (Grassi dan Grassi, 2005).
2.3.2 Pengamatan Kinetika Pelepasan Obat yang Lambat (Sustained Release)
Metode dari pengamatan kinetika pelepasan obat dari suatu formulasi dapat berdasarkan persamaan matematika. Model matematika yang berbeda dapat diaplikasikan untuk mendeksripsikan kinetika proses pelepasan obat. Kinetika pelepasan obat dapat ditentukan dengan menemukan hasil yang sesuai dari data pelepasan obat secara berturut-turut ke dalam plot persamaan model orde nol, orde satu, Higuchi dan Korsmeyer-Peppas (Dash,et al., 2010):
a. Orde nol
Disolusi obat dari bentuk sediaan lepas lambat idealnya mengikuti kinetika orde nol yaitu pelepasan obatnya konstan dari awal sampai akhir (Dash, dkk.2010). Orde nol menjelaskan sistem yang mana kecepatan pelepasan obat tidak tergantung kepada konsentrasi. Pelepasan obat yang mengikuti kinetika orde nol terjadi melalui mekanisme erosi.
Qt = Q0+K0t Keterangan:
Ot = jumlah obat yang terlarut dalam waktu t
Q0 = jumlah obat mula-mula dalam larutan biasanya (Q0=0) K0 = konstanta pelepasan orde nol
Dalam model ini plot persen obat yang terlepas versus waktu adalah linear. b. Orde satu
23 dC/dt = -Kc
Keterangan : K adalah konstanta kecepatan orde ke satu (menit-1) Persamaan dapat dibuat menjadi :
Log C = Log Co-Kt/2,303
Persamaan orde satu diperoleh dari plot log persen kumulatif obat terdisolusi versus waktu yang akan memberikan garis lurus dengan slope – K/2,303.
Persamaan orde satu diperoleh dari plot log persen kumulatif terdisolusi versus waktu. Ini dapat digunakan untuk menguraikan disolusi obat dari beberapa sediaan yang dimodifikasi pelepasannya seperti sistem transdermal, tablet matriks dengan obat yang lambat larut dalam bentuk disalut, dan lain-lain.
c. Model Higuchi
Higuchi menguraikan sistem pelepasan obat dari matriks yang tidak larut dalam air sebagai proses yang tergantung kepada akar waktu berdasarkan persamaan difusi Fickian
Qt = KH.t .½ Keterangan :
Qt = jumlah obat yang terlepas pada waktu t (mg) KH = konstanta kecepatan Higuchi (menit-½)
Data disolusi in vitro di plot sebagai akar waktu versus persen kumulatif obat. Beberapa kondisi percobaan yang mekanisme pelepasan obatnya menyimpang dari persamaan Fickian berarti mengikuti pelepasan non-Fickian.
24
Gambar 2.3 Matriks dengan pori-pori (Sinko, 2011).
d. Model Korsmeyer-Peppas (Power Law)
Model Korsmeyer-Peppas dapat ditunjukkan melalui persamaan : Mt/M∞ = Ktn
Keterangan :
Mt/M∞ = jumlah obat yang dilepaskan pada waktu t K = konstanta laju pelepasan
n = eksponen pelepasan
Data disolusi in vitro di plot sebagai log % kumulatif obat versus log waktu untuk membuat grafik Korsmeyer-Peppas (Paulo dan Jose, 2001).
Persamaan dapat juga ditulis dalam logaritma yaitu: Log Mt/M∞ = n log t + log k
Nilai n digunakan untuk mengkarakterisasi mekanisme pelepasan yang berbeda seperti yang ditunjukkan dalam Tabel 2.1.
Matriks Polimer
Bagian yang berkelok (tortuous path), tempat obat dikeluarkan dari matriks
25
Tabel 2.1. Eksponen difusi (n) dan mekanisme teoritis pelepasan obat dari sistem penyampaian terkontrol polimerik bentuk sferis
Eksponen difusi (n) Mekanisme pelepasan obat 0,43 < n < 0,5 Difusi Fickian
0,5 < n <0 ,89 Difusi Anomalous (non-Fickian) 0,89 < n <1 ,00 Case- II Transport
n > 1,00 Super Case- II transport
Sumber : Allen, 2013; Siepmann dan Peppas, 2001
Nilai n dapat diperoleh dari slope grafik pelepasan Korsmeyer-Peppas < 60% obat yang mula-mula (Costa dan Lobo, 2001 ; Dash, et al., 2010)
2.4 Gastroretentif
Banyak obat-obat yang dikategorikan pemakaian yang sekali sehari dari sediaan konvensional telah menunjukkan absorbsi yang suboptimal disebabkan tergantung kepada waktu transit dari sediaan tersebut dan hal ini yang membuat pelepasan obat yang diperpanjang perlu dikembangkan. Salah satu bentuk sediaan lepas terkendali oral yang memungkinkan obat untuk tinggal lebih lama di saluran gastrointestinal bagian atas adalah sediaan dengan sistim penghantaran obat tertahan di lambung. Sistem gastroretentif merupakan sebuah sistem yang dirancang agar sediaan dapat tertahan di lambung dalam waktu yang lama dan melepaskan zat aktifnya (Deghan dan Khan, 2009).
Jenis sistem penghantaran obat tertahan di lambung terdiri dari (Dehghan dan Khan, 2009; Ami, et al., 2012; Swetha, et al., 2012):
a. Sistem mengembang dan membesar (swelling and expandable system) b. Sistem bioadhesif (bioadhesive systems)
26
d. Sistem berdensitas tinggi (high-density systems)
Gambaran dari sistem penghantaran obat tertahan di lambung ditunjukkan pada Gambar 2.4.
Kandidat obat yang sesuai untuk sediaan yang tertahan di lambung atau gastroretentif (Pratima, et al., 2012):
a. Obat-obat yang mempunyai segmen absorpsi sempit (narrow absorption window di dalam saluran pencernaan misalnya: riboflavin dan levodopa b. Obat-obat yang diabsorbsi terutama di lambung dan bagian atas (bagian
proksimal) usus halus misalnya: klordiazepoksida dan cinnarazin
c. Obat-obat yang bekerja lokal di lambung misalnya: antasida dan misoprostol d. Obat-obat yang terurai dalam kolon misalnya: ranitidin HCl, metronidazol
dan metformin HCl
e. Obat-obat yang mengganggu bakteri kolon normal misalnya: amoksilin trihidrat
Gambar 2.4 Sistem penghantaran obat tertahan di lambung (gastroretentif Sediaan floating
Isi lambung
Sediaan mukoadhesif
Sediaan densitas tinggi
27
Keuntungan dari sistem penghantaran Obat Gastroretentif (Swetha, et al., 2012; Nayak, et al., 2012):
a. Bioavailabilitas dari obat dapat ditingkatkan terutama untuk obat-obat yang di metabolis dalam saluran pencernaan sebelah atas
b. Obat-obat yang mempunyai waktu paruh singkat, pelepasan lambat mengurangi frekwensi pemberian yang akan meningkatkan kepatuhan pasien
c. Digunakan untuk penghantaran obat dengan segmen absorbsi yang sempit
d. Digunakan untuk obat-obat yang tidak stabil dalam cairan usus
e. Sistem penghantaran ini dapat memperlama pelepasan obat untuk terapi lokal misalnya dalam pengobatan penyakit yang berhubungan dengan lambung dan usus halus.
f. Penghantaran obat ke bagian spesifik (site-spesific drug delivery) mengurangi efek samping dari obat.
2.4.1 Sistem mengembang
28
(Deghan dan Khan, 2009; Swetha, et al., 2012). Pelepasan obat terkontrol dapat dicapai melalui pemilihan dari polimer berat molekul sesuai dan pengembangan dari polimer menahan pelepasan obat. Pada waktu kontak dengan cairan lambung, polimer mengembang. Keseimbangan antara besar dan lamanya pengembangan dipertahankan oleh derajat tautan silang antara rantai-rantai polimer. Derajat tautan silang yang tinggi menahan kemampuan pengembangan dari sistem yang mempertahankan keutuhan fisik untuk waktu yang lama (Ami, et al., 2012).
2.4.2 Sistem mengapung (floating)
29 2.4.3 Sistem bioadhesif
Definisi bioadhesi adalah pengikatan suatu makromolekul alam atau sintetik pada jaringan biologi dalam waktu yang lama. Apabila pengikatan tersebut pada jaringan biologi yang merupakan membran mukosa maka fenomena ini disebut mukoadhesi (Peppas et al., 1985).
Sediaan yang dibuat dengan polimer adhesif akan tinggal dalam waktu yang lebih lama sampai proses adhesi berakhir selama beberapa jam (lebih dari 7-8 jam) berada pada segmen saluran cerna. Sediaan akan terikat pada permukaan sel epitel lambung atau mucin. Pembentukan ikatan elektrostatik dan hydrogen pada antarmuka polimer mukus cendrung ke bioadhesi (Deghan dan Khan, 2009; Swetha, et al,. 2012).
2.4.3.1 Mekanisme yang terlibat dalam mukoadhesi
Mekanisme dari mukoadhesi belum jelas sekali. Tiga tingkatan yang terlibat terjadinya mukoadhesi adalah (Das, et al., 2011) :
Tingkat 1: Penyebaran, pembasahan dan pengembangan dari sediaan pada permukaan mukosa, memulai kontak yang rapat antara polimer
dan lapisan mukus
Tingkat 2: Interdifusi dan interpenetrasi terjadi antara rantai dari polimer mukoadhesif dan jaringan gel mukus yang menghasilkan suatu area kontak yang lebih besar
30
Ada tiga jenis utama dari interaksi antara suatu polimer dan lapisan mukosa, ikatan fisik atau mekanik, ikatan kimia sekunder dan ikatan kimia kovalen. Ikatan fisik melibatkan belitan dari glikoprotein mucin dengan rantai polimer dan interpenetrasi dari rantai mucin dalam matrik polimer. Interpenetrasi dari makromolekular ini akan tergantung kepada fleksibilitas rantai masing-masing dan koefisien diffusi. Interaksi kimia sekunder meliputi ikatan ionik, interaksi Van der Waals dan ikatan hidrogen. Ikatan hidrogen mungkin merupakan interaksi kimia sekunder yang paling penting dalam mukoadhesi. Beberapa gugus fungsi yang membentuk ikatan hidrogen adalah hidroksil, karboksil, sulfat dan amin. Ikatan kovalen dilibatkan melalui reaksi kimia dari polimer dan substrat. Ikatan ini adalah permanen.
Suatu polimer mukoadhesif yang ideal mempunyai karakteristik berikut : a. Polimer dan produk degradasi harus tidak toksik dan tidak diabsorbsi
dari saluran pencernaan
b. Tidak mengiritasi pada membran mukosa
c. Membentuk suatu ikatan non kovalen yang kuat dengan mucin d. Tidak menghalangi pelepasan obat
e. Tidak terurai pada penyimpanan atau selama shelf life sediaan f. Harganya tidak mahal
Sifat-sifat yang menunjukkan suatu mukoadhesif yang baik adalah sebagai berikut (Yadav, et al., 2010) :
31 b. Muatan anionik kuat
c. Fleksibilitas rantai polimer yang cukup untuk penetrasi jaringan mukus
d. Karakteristik tegangan permukaan yang sesuai yang akan menghasilkan penyebaran kedalam lapisan mukus
e. Berat molekul yang tinggi.
f. Polimer yang mempunyai sifat hidrofilik dapat membentuk ikatan adhesif yang kuat dengan membran mukosa karena lapisan mukosa mengandung jumlah air yang banyak
2.4.4 Bentuk sediaan-sediaan gastroretentif yang telah diteliti
32
33 Tabel 2.2 Sediaan-sediaan gastroretentif yang telah diteliti
Bentuk Sediaan (Bahan Aktif)
Polimer yang digunakan
Metode Pembuatan Hasil Penelitian Referensi
Tablet floating
Tablet diformulasi dengan berbagai konsentrasi polimer yang digunakan. Nabikarbonat dan asam sitrat digunakan sebagai bahan pembentuk gas agar tablet floating. Ranitidin HCl digunakan sebagai model obat.
Tablet dari semua formula menunjukkan sifat floating 11 sampai 18 jam dan pelepasan obat sampai 12 jam. Kinetika pelepasan adalah mengikuti difusi pelepasan terkontrol.
-HPMC Tablet diformulasi dengan berbagai konsentrasi HPMC. Natrium bikarbonat digunakan sebagai bahan pembentuk gas agar tablet floating dan psyllum husk sebagai bahan pengembang
Tablet yang dihasilkan mengembang lebih dari 12 jam dalam lambung karena penambahan suatu bshan pengembang psyllum husk.
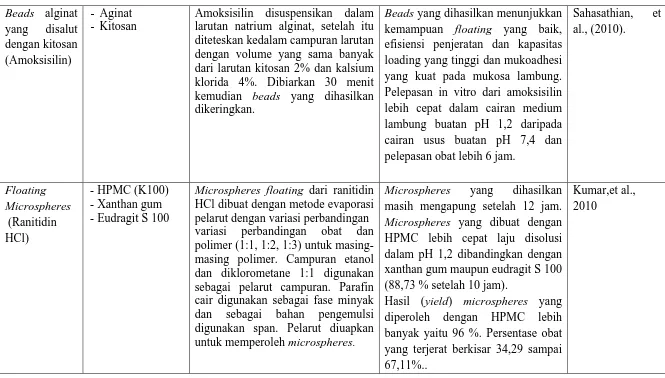
34 larutan natrium alginat, setelah itu diteteskan kedalam campuran larutan dengan volume yang sama banyak dari larutan kitosan 2% dan kalsium klorida 4%. Dibiarkan 30 menit kemudian beads yang dihasilkan dikeringkan.
Beads yang dihasilkan menunjukkan kemampuan floating yang baik, efisiensi penjeratan dan kapasitas loading yang tinggi dan mukoadhesi yang kuat pada mukosa lambung. Pelepasan in vitro dari amoksisilin lebih cepat dalam cairan medium lambung buatan pH 1,2 daripada cairan usus buatan pH 7,4 dan pelepasan obat lebih 6 jam.
Sahasathian, et
Microspheres floating dari ranitidin HCl dibuat dengan metode evaporasi pelarut dengan variasi perbandingan variasi perbandingan obat dan polimer (1:1, 1:2, 1:3) untuk masing-masing polimer. Campuran etanol dan diklorometane 1:1 digunakan sebagai pelarut campuran. Parafin cair digunakan sebagai fase minyak dan sebagai bahan pengemulsi digunakan span. Pelarut diuapkan untuk memperoleh microspheres.
Microspheres yang dihasilkan masih mengapung setelah 12 jam. Microspheres yang dibuat dengan HPMC lebih cepat laju disolusi dalam pH 1,2 dibandingkan dengan xanthan gum maupun eudragit S 100 (88,73 % setelah 10 jam).
Hasil (yield) microspheres yang diperoleh dengan HPMC lebih banyak yaitu 96 %. Persentase obat yang terjerat berkisar 34,29 sampai 67,11%..
35
Etil selulosa dengan jumlah yang bervariasi digunakan sebagai bahan matriks dan karbopol 934 sebagai polimer mukoadhesif. Aseton digunakan sebagai pelarut. Parafin cair digunakan sebagai fase minyak untuk membentuk mikroemulsi (micropheres) dan sebagai bahan pengemulsi digunakan span 80. Pelarut diuapkan sampai terbentuk mikrospheres.
Partikel yang dihasilkan berukuran 500-560 µm dan menunjukkan sifat mukoadhesif yang baik. Jumlah etil selulosa semakin meningkat maka pelepasan semakin lambat, Pelepasan obat setelah 6 jam adalah 82,15%.
(tidak memenuhi pelepasan sustained release).
Yellanki, bahan sukrosa sebagai pemanis, sedangkan sebagai bahan pengental digunakan sorbitol dan gliserin. Karbopol C934 atau Karbopol C940 digunakan sebagai polimer
mukoadhesif. Pembuatan suspensi menggunakan alat ultrasonic homogenizer.
Pelepasan obat lebih cepat dalam buffer pH 1,2 daripada buffer pH 7,2. Hal ini disebabkan karbopol mempunyai pka 6 sehingga pada pH 1,2 tidak terionisasi sehingga tidak mengembang sempurna, obat cepat dilepaskan sebelum mengembang sempurna.
Kinetika pelepasan obat dari polimer C940 dalam buffer fosfat adalah relaksasi polimer yang diikuti difusi dari obat, sedangkan dari polimer C934 dikontrol oleh pengembangan dan relaksasi dari polimer (super case II transport)
36
Microspheres gastroretentif dari ranitidin HCl dibuat dengan variasi perbandingan polimer kitosan dan natrium karboksimetil selulosa. Jumlah glutaraldehida digunakan sebagai bahan cross linking agent bervariasi. Parafin cair sebagai fase minyak dan span digunakan sebagai bahan pengemulsi untuk membuat mikroemulsi M/A. Microspheres yang dihasilkan dicuci dengan petroleum eter dan dikeringkan selama 24 jam.
Formulasi dengan perbandingan kitosan dan NaCMC 3 : 1 dan jumlah glutaraldehida 1,25 ml dipilih sebagai formulasi yang ideal berdasarkan hasil uji mukoadhesi 31 % setelah 8 jam dan pelepasan obat 84,77 % setelah 14 jam. Model pelepasan obat mengikuti Higuchi dan mekanisme pelepasan adalah non-Fickian. Namun demikian Efisiensi penjeratan obat yang di;peroleh kecil yaitu 66,22 %
Dua dan
Gelatin Metode one step desolvation menggunakan variasi jumlah gelatin sebagai polimer mukoadhesif. Pluronic F-68 digunakan sebagai
bahan pengstabil dispersi.
Glutaraldehyda sebagai bahan cross linking dari nanopartikel. Pembuatan nanopartikel dilakukan dengan pengadukan 1000 rpm menggunakan magnetic stirrer.
Formulasi nanopartikel dengan perbandingan gelatin dan pluronic F-89 dalam 1:2 menunjukkan hasil yang memuaskan yaitu ukuran partikel 207,7 nm, indeks polidispersitas 0,338, efisiensi penjeratan 54,21 %, loading efficiency 43,13 % , dan kekuatan mukoadhesif 6,012 g
37
2.5 Bahan-Bahan Polimer dan Bahan Obat yang Digunakan dalam Penelitian
2.5.1 Bahan-bahan polimer
2.5.1.1 Natrium alginat
Natrium alginat merupakan produk pemurnian karbohidrat yang diekstraksi dari alga coklat (Phaeophyceae) dengan menggunakan basa lemah (Grasdalen. et al.. 1979). Alginat ini diperoleh dari spesies Macrocystis pyrifera, Laminaria, Ascophyllum dan Sargassum. Alginat merupakan bahan yang non toksik, non alergi, biodegradabel dan biokompatibel (Rehm, 2009).
Asam alginat adalah kopolimer biner yang terdiri dari residu β
-D-mannuronat (M) dan α-L-asam guluronat (G) yang tersusun dalam blok-blok yang membentuk rantai linear Kedua unit tersebut berikatan pada atom C1 dan C4 dengan susunan homopolimer dari masing-masing residu (MM dan GG) dan suatu blok heteropolimer dari dua residu (MG) (Thom, et al., 1981). Struktur alginat dapat dilihat pada Gambar 2.5.
Gambar 2.5 Struktur kimia alginat (Thom, et al., 1981)
38
kalsium. Gel ini merupakan jaringan taut silang yang tersusun dari kalsium alginat yang membentuk konformasi kotak telur (egg box type of conformation) (Morris, et al,. 1978).
Pembentukan gel dan taut silang dari polimer-polimer adalah terutama dicapai melalui pertukaran ion natrium dari asam guluronat dengan ion kalsium dan membentuk struktur seperti yang ditunjukkan dalam Gambar 2.6.
Gambar 2.6 Bentuk konformasi “ kotak telur” kalsium alginat (Morris, et al,. 1978 ; Sacchan, et al., 2009)
Pengikatan kation dan sifat-sifat pembentukan gel tergantung kepada komposisi dan urutannya. Afinitas terhadap kasium meningkat dengan
peningkatan jumlah residu α-L asam guluronat dalam alginat. Sifat-sifat fisik dari
gel tergantung kepada rasio dari asam uronat dalam rantai polisakarida, alginat
yang kaya dalam α-L guluronat membentuk gel yang kaku tapi rapuh sedangkan
yang kaya dalam β-D asam mannuronat lebih lemah tetapi lebih fleksibel.
2.5.1.2Kitosan
Kitosan merupakan aminopolisakarida hasil deasetilasi dari kitin. Kitin terdapat dalam cangkang crustacea seperti udang, lobster dan kepiting. Kitosan menunjukkan sifat polimer biomedis seperti nontoksik, biokompatibel, dan biodegradabel (Felt, et al., 1998). Kitosan merupakan biopolimer yang linear,
39
tidak bercabang, polimer yang dibangun dari monomer-monomer glukosamin dan
N-asetilglukosamin yang terikat pada pola β-(1-4). Struktur kimia dari kitosan
ditunjukkan seperti pada Gambar 2.7.
Gambar 2.7 Struktur kimia kitosan (Felt, et al., 1998).
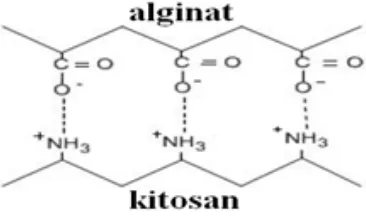
2.5.2 Interaksi Antara Alginat dengan Kitosan
Alginat yang merupakan polianionik dan kitosan berupa polikationik dapat berinteraksi melalui gugus asam karboksilat dari alginat dan gugus amino dari kitosan untuk membentuk kompleks polielektrolit dari muatan yang berlawanan seperti yang ditunjukkan pada Gambar 2.8.
Gambar 2.8 Kompleks polielektrolit alginat dan kitosan (Takahashi, et al.,1990
40 2.5.3 Bahan obat ranitidin hidroklorida
2.5.3.1Spesifikasi ranitidin hidroklorida
Menurut DitJen POM. (1995), struktur kimia dan spesifikasi ranitidin hidroklorida adalah seperti ditunjukkan pada Gambar 2.9.
Gambar 2.9 Rumus bangun ranitidin hidroklorida (DitJen POM, 1995)
Rumus Molekul : C13H22 N4O3S. HCl. Berat Molekul : 350,87.
Nama Kimia : N-[2-[[[5-[(dimetilamino)metil]-2-furanil]metil]tio]etil]-N’- metil-2-nitro-1,1-etenadiamina hidroklorida.
Pemerian : Serbuk hablur putih sampai kuning pucat, praktis tidak berbau, peka terhadap cahaya dan kelembaban. Melebur pada suhu lebih kurang 140°C disertai peruraian.
Kelarutan : Sangat mudah larut dalam air, cukup larut dalam etanol dan sukar larut dalam kloroform.
pH : Larutan 1% dalam air adalah 4,5-6,0.
2.5.3.2 Uraian ranitidin hidroklorida
41
dibandingkan dengan penghambat reseptor H2 yang lain seperti simetidin. famotidin dan nizatidin (Ramachandran, et al., 2011).
Ranitidin mampu memberikan pengurangan lebih dari 90% terhadap sekresi asam lambung basal dan sekresi asam lambung yang distimulasi oleh makanan setelah pemberian dosis tunggal. Ranitidin dapat diberikan pada dosis 150 mg dua kali sehari atau 300 mg saat jam tidur. Ranitidin efektif untuk mencegah ulkus akibat stress pada pasien yang sakit kritis (Grant, et al., 1989; Katzung, 2004).