BAB II
TINJAUAN PUSTAKA 2.1 SEPSIS
2.1.1 Definisi
Definisi Sepsis pertama sekali diperkenalkan oleh American college OfChest
Physicians (ACCP) dan The Society Of Critical Care Medicine (SCCM) Consensus
Conference pada tahun 1991, dimana sepsis diartikan sebagai suatu respons inflamasi sisemik
(systemic inflammatory response) terhadap infeksi (Dellinger et al.,2013). Meskipun SIRS, sepsis dan syok septik biasanya berhubungan dengan infeksi bakteri, namun tidak harus
terdapat bakterimia. Hal ini terjadi karena di dalam darah kemungkinan terdapat endo
maupun eksotoksemia sedangkan bakterinya berada dalam jaringan. Bakterimia adalah
keberadaan bakteri hidup dalam komponen cairan tubuh, biasanya dijumpai setelah jejas pada
permukaan mukosa, primer (jika fokus infeksi tidak teridentifikasi) ataupun sekunder
terhadap fokus infeksi intravaskuler atau ekstravaskuler, sehingga biakan darah tidak harus
positif. (Cohen, 2002;Nasronudin,2007;Guntur,2014).
Sepsis berat adalah sepsis yang berhubungan dengan adanya disfungsiorgan (satu atau
lebih) hipoperfusi jaringan atau hipotensi. Hipoperfusi termasuk asidosis laktat, oligouria dan
perubahan status (Nasronudin,2007;Guntur,2014;Dellinger et al.,2013;Morrell et al.,2009;O’Brien dan Ali,2009). Sedangkan syok sepsis adalah sepsis yang disertai hipotensi (TDS< 90mmHg atau penurunan ≥ 40 mmHg dari tekanan darah sebelumnya) tanpa ada
penyebab hipotensi lainnya, yang menetap walaupun telah dilakukan resusitasi cairan yang
adekuat. (Cohen,2002)
2.1.2 Epidemiologi
Sepsis dalam 20 tahun terakhir meningkat di Amerika Serikat,diperkirakan jumlah
kasus sepsis 400.000–500.000 setiap tahunnya. Data di Amerika Serikat menunjukkan pada
tahun 1979 tercatat 164.000 kasus sepsis (87,2/100.000 populasi), sedangkan pada tahun
2000 tercatat 600.000 kasus (240,4/100.000 populasi) sehingga terjadi peningkatan insiden
pertahun 8,7%.Sepsis merupakan penyebab terbanyak kematian di ruang rawat intensif pada
seluruh dunia dengan angka mortalitas 28.6% untuk sepsis, 32.2% sepsis berat dan 54%%
syok sepsis. Di Amerika Serikat, sepsis merupakan penyebab kematian utama pada pasien
jantung yang dirawat di Intensive Care Unit (ICU) (Artetoet al.,2012;Kausset al.,2010;Pittet
Suatu analisa retrospektif dari database internasional melaporkan bahwa secara global
insidensi sepsis yaitu 437 per 100.000 orang per tahun antara tahun 1995-2015,walaupun data
ini tidak merefleksikan kontribusi dari negara yang berpendapatan rendah dan
menegah.Insidensi sepsis bervariasi diantara ras dan etnik,namun tampaknya lebih tinggi
pada lelaki keturunan aftika-amerika.Insidensi juga paling tinggi selama musim dingin
mungkin berhubungan dengan meningkatnya prevalensi infeksi pernafasan. Pasien yang lebih
tua >65 tahun sebagai mayoritas penderita sepsis (60-85%) (Arteroet al.,2012)
Di RSUP Persahabatan tahun 2001 sepsis merupakan penyebab kematian , 48 %
diantaranya penderita rawat inap adalah kasus infeksi berat dan 14,6 % diantaranya kasus non
tuberkulosis.Di RSUD Dr. Soetomo Surabaya di peroleh data sekitar 180 pneumonia
komuniti dengan angka kematian berkisar antara 20% - 35 %. (Wahyudi,2006)
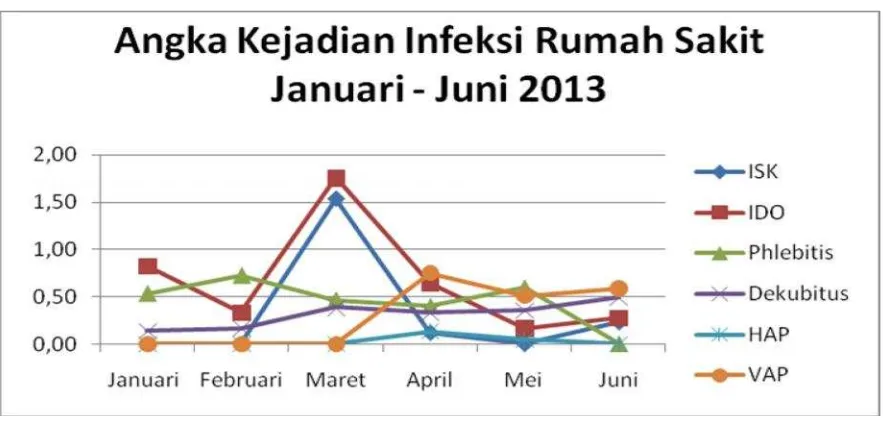
Data Pengendalian Pencegahan Infeksi RSUP H. Adam Malik Medan bahwasanya
periode Januari-Juni tahun 2013 di RSUP H. Adam Malik Medan, angka kejadian infeksi
yang ditemukan sebesar 13,41% dari beberapa etiologi terhadap kasus infeksi, dimana infeksi
pada daerah operasi mendapat peringkat tertinggi, diikuti oleh infeksi saluran kemih, infeksi
dari entilator aquired pneumoniae,phlebitis, dan dekubitus.(Gambar.1) (Josia,2013).
Gambar 2.1. Angka Kejadian Infeksi Rumah Sakit di RSUP H Adam Malik,
2.1.3 Etiologi
Infeksi pada sepsis dapat disebabkan oleh bakteri Gram-negatif atau Gram-positif,
namun penyebab sepsis terbesar adalah bakteri gram negatif dengan persentase 60-70% yang
menghasilkan berbagai produk yang menstimulasi sistem imun. Produk yang berperan
penting terhadap sepsis adalah lipopolosakarida (LPS). LPS atau endotoksin glikoprotein
kompleks merupakan komponen utama terluar dari bakteri gram negatif. Selama periode
1979–2000 di Amerika Serikat angka sepsis terus meningkat sampai 13,7% per tahun. Dari
hasil biakan kuman yang tumbuh, 52,1% diantaranya adalah gram positif, 37,5% gram
negatif, 4,7% polimikrobial, 4,6% jamur, dan 1% bakteri anaerob. Infeksi bakteri gram positif
terus meningkat disebabkan oleh peningkatan infeksi nosokomial dari berbagai sumber
seperti kateterisasi atau terapi imunosupresif. Hal ini ditunjukkan dari meningkatnya kasus
MRSA (Methicillin-Resistant Staphylococcus Aureus) dari 29% menjadi 45%. Infeksi
terutama terjadi pada saluran nafas (40-44%), diikuti oleh infeksi saluran genitourinarius
(9-18%) dan infeksi intra abdominal (9-14%) (Guntur ,2014; Arteroet al.,2012).
2.1.4 Patogenesis Dan Patofisiologi
Sepsis merupakan puncak dari interaksi yang kompleks antara organisme penyebab
infeksi dan host imun. Kedua hal yakni respon host dan karakteristik dari organisme
penyebab infeksi mempengaruhi outcome sepsis. Pada sepsis diawali dengan aktifasi sistem
imun bawaan, sebagai respons terhadap infeksi, melalui pengenalan terhadap benda asing
yakni lipopolisakarida bakteri (endotoksin atau LPS). Mekanisme ini antara lain pelepasan
sitokin, aktifasi neutrofil, monosit, makrofag dan sel endotel serta aktifasi komplemen,
koagulasi, fibrinolitik, dan sistem kontak(Nevire,2009;O’Reilly,1999;Balk,2000).
Toll-like receptors (TLR) mengatur mekanisme pertahanan tubuh dan berperan penting dalam aktifasi imun bawaan. TLR adalah reseptor pada permukaan sel yang
mengenali komponen molekuler dari mikroorganisme. Pada fase awal dari infeksi, TLR
mengaktifasi sistem imun bawaan dan menghancurkan patogen dari makrofag, natural killer cellsdan sistem komplemen. Pada fase kedua, TLR mengaktifasi sistem imun didapat dengan mengaktifasi limfosit T dan B. Disini produksi sitokin berperan penting, makrofag dan
monosit yang teraktifasi adalah sel yang utama yang menghasilkan sitokin, tapi fibroblast,
neutrofil dan sel endotel juga dapat menghasilkan sitokin. (O’Brien dan Ali,2007;
Nevire,2009; Balk,2000).
TLR-4 mengenali LPS bakteri gram negatif, TLR-2 mengenali peptidoglikan bakteri
intracellular signal transduction pathway yang mengaktifkan cytosolic nuclear factor kB (NF-kB). NF-kB meningkatkan transkripsi sitokin. Sitokin akan mengaktifkan sel endotel
dengan meningkatkan ekspresi molekul permukaan dan memperkuat adhesi neutrofil dan
endotel di tempat infeksi. Sitokin juga menyebabkan injuri sel endotel melalui induksi
neutrofil, monosit, makrofag dan trombosit yang melekat pada sel endotel.
(Nevire,2009;O’Reillyet al.,1999;Balk,2000;Ertelet al.,1995;Hotchkiss dan Karl,2003).
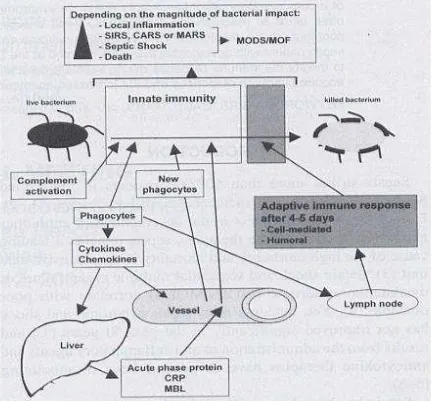
Gambar 2.2 Respon Imun terhadap Infeksi Organisme
Sitokin melepaskan mediator seperti protease, oksidan, prostaglandin, dan leukotrine.
Protease, oksidan, prostaglandin, dan leukotrien, akan merusak sel endotel, menimbulkan
peningkatan pemeabilitas, vasodilatasi dan perubahan keseimbangan prokoagulan dan
koagulan. Sitokin juga mengaktifasi kaskade koagulasi. Selain itu endotel yang teraktifasi
akan melepaskan nitric oxide (NO), suatu bahan vasodilator poten yang berperan pada syok
sepsis. Sitokin dibedakan menjadi proinflamsi dan anti inflamasi, tergantung fungsinya.
TNF-α, IL-1ß, IL-6, Il-8, Il-12 adalah sitokin proinflamasi utama yang berperan dalam aktifasi
awal dari respons inflamasi sistemik pada sepsis. TNF-α terutama diproduksi oleh monosit
dan makrofag, dan bekerja merangsang produksi molekul adhesi pada sel endotel serta sistem
koagulasi dan komplemen. IL-1 terutama dihasilkan oleh monosit dan makrofag. IL-1ß dan
TNF-α mempunyai efek sinergik. IL-1ß merangsang produksi IL-6, IL-8 dan TNF-α dan
dapat menyebabkan perubahan hemodinamik sama seperti shock sepsis. Pada banyak
penelitian didapat bahwa kadar IL-1ß tidak berhubungan dengan beratnya penyakit,
sedangkan TNF-α berhubungan dengan beratnya penyakit pada beberapa studi
(Nasronudin,2007;Guntur,2014;Nevire,2009;O’Reillyet al.,1999;Balk,2000).
Sepsis juga mengaktifkan produksi dan pelepasan sitokin anti inflamasi. IL-1 receptor
antagonist (IL-1ra) menghambat IL-1, yang berikatan secara kompetitif dengan reseptor IL-1
dan menghambat kerja IL-1. IL-1ra dihasilkan terutama oleh makrofag, beberapa studi gagal
membuktikan bahwa pemberian IL-1ra pada sepsis dapat memperbaiki mortalitas pada
sepsis.24,25IL-10 adalah sitokin anti inflamasi utama. Sitokin ini menghambat produksi
TNF-α, IL-1ß, IL-6, IL-8. Sitokin ini juga menekan pelepasan radikal bebas dan aktifitas NO serta
produksi prostaglandin. Beberapa sel yang dapat memproduksi IL-10 adalah CD-4, CD-8,
makrofag, monosit, limfosit B, sel dendrite dan sel epitel. Pada syok sepsis, monosit
merupakan sumber utama dari sitokin ini. IL-10 tidak hanya membatasi beratnya respons
imflamasi, tapi juga mengatur proliferasi sel T, sel B, natural killer cells, antigen precenting
cells, cel mast dan granulosit. Sitokin ini berperan dalam imun supresi, sebagai stimulator
imunitas bawaan dan imunitas TH-2. Beberapa studi mendapatkan bahwa pada keadaan
sepsis kadar sitokin IL-10 meningkat dan lebih meningkat lagi pada syok sepsis. (Ertel et al.,1995;Hotchkiss dan Karl, 2003;Sharma dan Kumar, 2003;Jilmaet al.,1999).
IL-6 merupakan sitokin yang paling banyak diteliti pada sepsis dan paling sering
ditemukan meningkat. Kadarnya meningkat lebih lama dibandingkan TNF-α dan iIL-1ß.
Sitokin ini terutama diproduksi oleh monosit dan makrofag dan sel indotel dan berhubungan
dengan derajat beratnya sepsis sehingga peningkatan yang persisten berhubungan dengan
diferensiasi dari sel limfosit B dan T. Sitokin ini adalah pirogen endogen dan demam pada
pasien sepsis disebabkan oleh sitokin ini. Sitokin ini juga bersifat anti inflamasi yang
menghambat produksi sitokin pro-inflamasi lainnya dan respons yang adekuat dapat
mengaktivasi HPA pada penyakit kritis. (Cohen,2002;Nasronudin,2007;Guntur,2014).
IL-8 berfungsi mengaktifasi dan sebagai kemotaksis netrofil ke tempat inflamasi.
Konsentrasi tinggi dari sitokin ini dapat merangsang infiltrasi netrofil, merusak endotel,
kebocoran plasma dan injuri jaringan lokal. Sebaliknya sitokin ini juga menghambat migrasi
netrofil apabila berada dalam sirkulasi, sehingga sitokin ini bersifat pro dan anti inflamasi.
(Nasronudin, 2007)
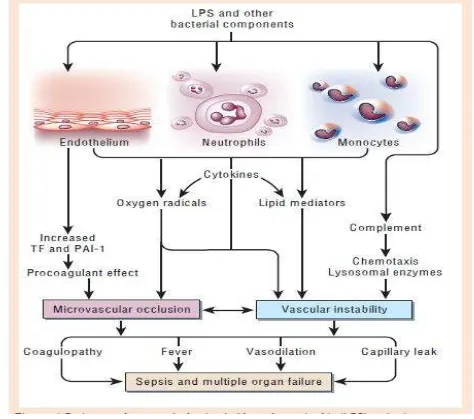
Gambar 2.3. Patogenesis Terjadinya Multiple Organ Failure dan Syok pada Sepsis
2.1.5 Diagnosis
Gejala klinis sepsis biasanya tidak spesifik seperti demam, menggigil dan gejala
konstitusional seperti lelah, malaise, gelisah, kebingungan sampai penurunan kesadaran.
Manifestasi klinis sepsis akan lebih berat bila terjadi pada penderita usia lanjut, diabetes
mellitus, keganasan, HIV atau komorbid dengan penyakit immunokompromise lainnya.
Manifestasi SIRS dapat berupa dua atau lebih dari gejala berikut: 1) Suhu > 38 C atau
<36 C; 2) Takikardia (HR > 90 kali/menit; 3) Takipneu (RR > 20 kali/menit) atau PaCO2 <
32 mmHg; 4) Lekosit darah > 12.000/µL, <4.000/µL atau neutrofil batang > 10%
(Nasronudin,2007;Guntur,2014).
Tabel 2.1 Kriteria Diagnostik Sepsis
Dikutip dari: Dellinger PR,Crit Care Med. (2013); 41:580–63
.
Infection.documented or suspected, and some of the following:
General Variable
- Fever (>38,3oC)
- Hypothermia (core temperature <36oC)
- Heart rate >90/min or more than two sd above than normal value for age
- Tachypnea
- Altered mental status
- Significant edema or positive fluid chalange (>20ml/kg over 24 hr)
- Hyperglicemia (plasma glucose >140mg/dl or 7,7 mmol/L) in the absence of
diabetes
Inflamatory variables
- Leukocytosis (WBC count >12.000µL)
- Leukopenia (WBC count <4.000µL)
- Normal WBC count with greater than 10% immature forms
- Plasma C-reactive protein more than two sd above the normal value
Hemodynamic variables
- Arterial hypotension (SBP <90mmHg,MAP<70mmHg or an SBP decrease
>40mmHg in adults or less than two sd below the normal for age)
Organ dysfunction variables
- Arterial hypoxemia (PaO2/FiO2 <300)
- Acute oliguria (urine output <0,5ml/kg/hr for at least 2 hrs despite adequate fluid
resucitation)
- Creatinine increase >0,5mg/dl or 44,2µmol/L
- Coagulation abnormalities (INR>1,5 or aPTT >60s)
- Ileus (absent bowel sound)
- Thrombocytopenia (platelet count <100.000µL)
- Hyperbilirubinemia (plasma total bilirubin > 4mg/dl or 70 µmol/L)
Tissue perfusion variables
- Hyperlactatnemia (>1 mmol/L)
Tabel 2.2. Kriteria sepsis berat
Dikutip dari: Dellinger PR,Crit Care Med. (2013)
Severe sepsis definition = sepsis-induced tissue hypoperfusion or organ
dysfunction (any of the following thought to be due to the infection
Sepsis-induced hypotension
Lactate above upper limits laboratory normal
Urine output <0,5ml/kg/hr for more than 2 hrs despite adequate fluid resucitation
Acute lung injury with PaO2/FiO2 <250 in the absence of pneumonia in infection
source
Acute lung injury with PaO2/FiO2 <200 in the presence of pneumonia in infection
source
Low-density lipoprotein berasal dari VLDL dan IDL didalam plasma dan
mengandung sejumlah besar kolesterol dan kolesteryl ester. Hampir dua pertiga kolesterol
dan esternya yang ditemukan dalam plasma dikaitkan dengan LDL. Mekanisme pengolahan
dan pengangkutan kolesterol di dalam sel adalah rumit. Terdapat beberapa bentuk lipoprotein
pembawa kolesterol termasuk low density lipoprotein (LDL) dan high density lipoprotein
(HDL). LDL adalah pembawa plasma utama kolesterol, LDL diperlukan untuk mengangkut
kolesterol dari hati (melalui sintesis hepatik dari VLDL) ke jaringan perifer, terutama adrenal,
gonad, dan jaringan adiposa, dan HDL terlibat dalam transportasi terbalik kolesterol dari
jaringan kembali ke hati. Kedua proses ini bekerja sama untuk mengatur kadar kolesterol dan
Ada tiga jalur utama yang saling berhubungan utama yang terlibat dalam metabolisme
lipoprotein : (1) pengangkutan makanan atau lemak eksogen; (2) pengangkutan hati atau
endogen lemak; dan (3) transportasi kolesterol terbalik (reverse kolesterol transport). Jalur ini
saling tergantung dan gangguan dalam salah satu jalur mempengaruhi fungsi yang lain.
Sebagai contoh, mutasi seperti satu di protein ABC1 bisa mengganggu transportasi normal
dan pengolahan kolesterol. High-density lipoprotein kolesterol (HDL-C) memiliki sifat
kardioprotektif karena keterlibatannya dalam proses tertentu sepert revers transportasi
kolesterol dan penghambatan low-density lipoprotein kolesterol (LDL-C) oksidasi. agen
tertentu, seperti niacin, meningkatkan HDL-C, menurunkan lipoprotein (a), dan target enzim
atau reseptor tertentu, mungkin sangat bermanfaat bagi pasien dengan resiko penyakit
kardiovaskular (Peter Oet al, 2000)
Pengambilan kolesterol dari IDLs ( Intermediate Density Lipoprotein) dan LDL terjadi
menyusul interaksi partikel lipoprotein dengan reseptor LDL (juga disebut reseptor apoB-100
/ apoE). IDLs dimiliki kedua apoB-100 dan apoE, di mana kehadiran apoE meningkatkan
pengikatan IDLs ke reseptor LDL. Di sisi lain, satu-satunya apoprotein yg dijumpai dalam
LDL adalah apoB-100, yang diperlukan untuk interaksi dengan reseptor LDL, tetapi
kurangnya apoE mengurangi afinitas keseluruhan LDL untuk reseptor LDL (Neda Asem et al, 2009;Henk Jet al, 2003)
Tingkat kolesterol intraseluler diatur melalui penekanan kolesterol yang disebabkan
sintesis reseptor LDL dan penghambatan kolesterol oleh sintesis kolesterol. Peningkatan level
kolesterol intraseluler yang dihasilkan dari penyerapan LDL memiliki efek tambahan
mengaktifkan SOAT2, sehingga memungkinkan penyimpanan kelebihan kolesterol dalam
sel. Namun, efek penekanan kolesterol oleh sintesis reseptor LDL adalah penurunan tingkat
di mana LDL dan IDLs dikeluarkan dari serum. Hal ini dapat menyebabkan tingkat sirkulasi
kelebihan kolesterol dan kolesterol ester ketika asupan makanan lemak dan kolesterol
melebihi kebutuhan tubuh. Kelebihan kolesterol cenderung disimpan di kulit, tendon, dan
dalam arteri, yang menyebabkan aterosklerosis (Neda Asem et al, 2009;Riaz A Memon, 2000).
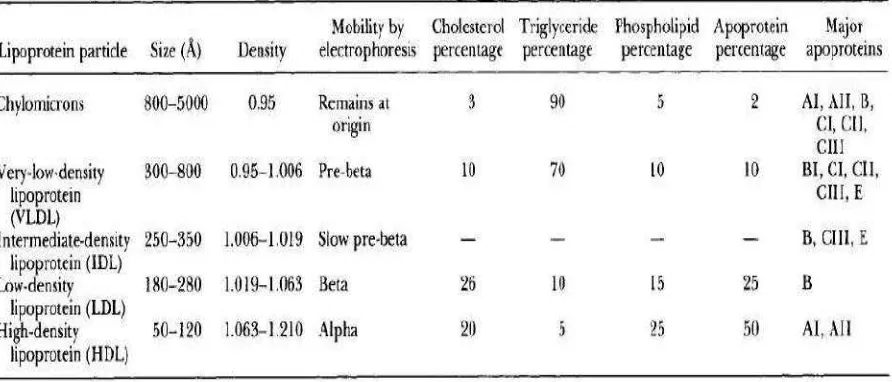
Partikel plasma lipoprotein terdiri dari berbagai proporsi pada 4 element utama yakni :
Tabel 2.3. Karakteristik dan persentase lipoprotein berdasarkan berat partikel
Dikutip dari: (Khovidhunkit, 2004)
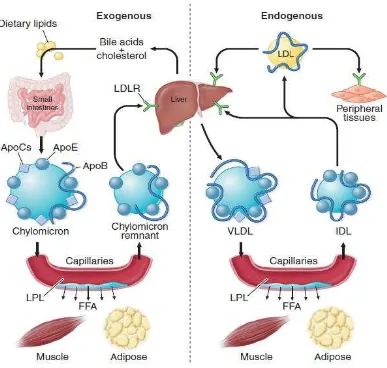
Sistem transportasi lipid pada plasma terbagi atas dua jalur :
1. Exogen pathway
2. Endogen pathway
2.2.1 Exogen pathway
Diawali penyerapan trigliserida dan kolesterol di intestinal. Trigliserida masuk ke
jaringan adipose dan jaringan otot. Kolesterol masuk ke dalam hati. Setelah terjadi
penyerapan , trigliserida dan kolesterol dire esterifikasi di intestinal dan akan terikat dalam
berbagai apoprotein, fosfolipid dan chylomicron. Chylomicron akan disekresi ke kelenjar
lymph intestinal masuk ke aliran darah melalui duktus thoracicus dan kapiler- kapiler
dijaringan adipose serta jaringan otot skelet.Chylomicron berinteraksi dengan enzim
lipoprotein lipase yang menyebabkan hidrolisis trigliserida dan pembebasan asam lemak
bebas . Asam lemak bebas akan dideposit atau dioksidasi pada jaringan adipose ataupun disel
otot skelet . Pada kondisi fisiologis , Chylomicron dijumpai pada plasma selama 1 – 5 jam
setelah konsumsi daging dan susu. Chylomicron akan hilang disirkulasi setelah 12 jam
2.2.2 Endogen pathway
Liver membentuk trigliserda dari asam lemak bebas dan karbohidrat. Trigliserida
endogen ini akan disekresi ke sirkulasi dalam bentuk VLDL. Pembentukan dan sekresi
VLDL pada tingkat sel mirip seperti chylomicron , kecuali B apoprotein, C apoprotein dan E
apoprotein. VLDL akan berinteraksi dengan lipoprotein lipase dijaringan kapiler dan terjadi
hidrolisa trigliserida dan akan memproduksi sisa sisa VLDL yang kaya akan kolesterol
disebut Intermediate Density Lipoprotein ( IDL ) yang akan mengalami hidrolisis dan
berubah menjadi LDL dan pembebasan asam lemak bebas. Sebagian sisa sisa partikel akan
hilang disirkulasi 2 -6 jam setelah diikat disel hati (Emancipator K et al,1992;Murch O et
al,2007;Wendel Met al, 2007)
Gambar 2.4. Pathway Metabolisme Lipid
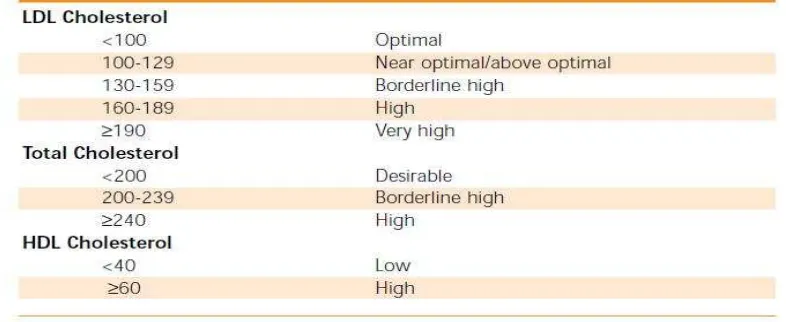
Tabel 2.4. Klasifikasi LDL, Total Kolesterol, dan HDL berdasrkan NCEP ATP III
(Dikutip dari : Scott M. Grundy et al,National Institutes of Health NIH Publication No. 01-36701;40:3)
2.2.3 LDL Receptor-Related Proteins (LRPs)
LDL Receptor-Related Proteins (LRPs) merupakan kelompok protein transmembran
struktural terkait yang terlibat dalam berbagai kegiatan biologis termasuk metabolisme lipid,
transportasi nutrisi, perlindungan terhadap aterosklerosis, serta berbagai proses
perkembangan. LDL reseptor (LDLR) merupakan pembentuk protein. LRPs termasuk LRP1,
LRP1B, LRP2 (juga disebut megalin), LRP4 (juga disebut MEGF7 untuk beberapa faktor
pertumbuhan epidermal-seperti domain protein 7), LRP5, LRP6, LRP8 (juga disebut apoE
reseptor 2), reseptor VLDL (VLDLR) , dan SORL1 (menyortir reseptor terkait protein yang
mengandung LDLR kelas A) (JHM Levels;Maja Gruber,2009)
Proprotein konvertase Subtilisin / Kexin Jenis-9 (PCSK9) merupakan kandidat yg
menarik untuk pengobatan karena sasaran strategi anti-PCSK9 adalah organisme , bukan
respon inang. Manfaat mengenai pendekatan ini muncul dari pemahaman tentang jalur
pembersihan normal sepsis-inisiasi molekul patogen. Sistem kekebalan tubuh bawaan
memberikan respon awal ketika terinfeksi kuman patogen ketika pathogen associated
mollecular patterns (PAMPs) mengikat dan mengaktifkan reseptor imun bawaan, seperti
Toll-Like reseptor. Kunci PAMPs dari bakteri adalah molekul lipid yang berasal dari dinding
sel bakteri, seperti lipopolisakarida (LPS) bakteri Gram-negatif, atau asam lipotechoic dari
bakteri Gram-positif. Untuk membersihkan patogen lipid ini dari sirkulasi darah pasien
(LBP) dan bakterisidal/ permeability-inducing protein (BPI). Transfer Protein ini sangat
homolog terhadap lipid lainnya dalam membawa protein, seperti phospolipid transfer protein
(PLTP) dan cholesterol ester transfer protein (CETP), molekul yang
lebih familiar dengan kardiologis. Seperti PLTP dan CETP, transfer lipid patogen yang
dilakukan dalam menyeimbangkan antara high-density lipoprotein (HDL), low-density
lipoprotein (LDL), very low density lipoprotein (VLDL). Kemudian, lipid patogen yang
dibersihkan oleh hati melalui LDL reseptor diekspresikan pada hepatosit (Joseph P
Gaut,2001;JHM Levels;Maja Gruber,2009)
LDL reseptor merupakan langkah kunci dalam clearance patogen lipid dari sirkulasi
di sepsis, sepsis berat dan shock septik. Partikel LDL berikatan dengan reseptor LDL dan,
dengan reseptor LDL, diinternalisasikan dalam hepatosit. Ketika dibersihkan dari LDL,
reseptor ini kemudian diedarkan kembali ke permukaan sel hepatosit. Jumlah LDL reseptor
yang diekspresikan pada hepatosit diatur oleh PCSK9. PCSK9 dalam sirkulasi mengikat
reseptor LDL pada hepatosit. Ketika reseptor LDL diinternalisasi, terikat PCSK9
menargetkan reseptor LDL untuk degradasi lisosom. Hal ini menyebabkan penurunan
densitas reseptor LDL pada hepatosit yang, pada gilirannya, mengurangi LDL receptor
mediated dan juga mengurangi clearance patogen lipid. Sebaliknya, obat-obatan atau variasi
genetik yang mengurangi fungsi PCSK9, meningkatkan ekspresi reseptor LDL pada
hepatosit, dan dengan demikian meningkatkan clearance LDL dari darah (Joseph P
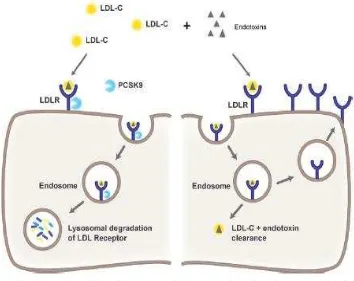
Gambar 2.5. Bersihan Lipid Patogen dari Sirkulasi
(Dikutip dari: James A Russel et al,2015)
Gambar diatas menunjukkan Patogen lipid dalam sirkulasi. Lipid patogen, seperti
endotoksin dari bakteri Gram-negatif dan lipotechoic acid dari bakteri Gram-positif, dibawa
oleh partikel HDL, LDL, dan VLD dalam darah. Lipid patogen yang terkandung dalam
kolesterol LDL (LDL-C) kemudian dibersihkan melalui reseptor LDL (LDLR) pada
hepatosit. Panel sebelah kiri menggambarkan peranan proprotein konvertase Subtilisin /
Kexin type 9 (PCSK9) dalam pengaturan klirens. PCSK9 mengikat LDLR dan ketika LDLR
terinternalisasi, sebagai bagian dari serapan hepatosit LDL-C, pengikatan PCSK9 dengan
LDLR membuat degradasi lisosom. Akibatnya, kepadatan LDLR pada permukaan sel
kepadatan LDLR meningkat, sehingga clearance LDL-C meningkat. Dalam pengaturan
sepsis, ketika LDL-C membawa lipid patogen, peningkatan kepadatan LDLR juga
menghasilkan peningkatan clearance lipid patogen, yang mengarah ke pengurangan respon
inflamasi dan hasil sepsis meningkat (Joseph P Gaut,2001;JHM Levels;Maja Gruber,2009;
James A Russel et al,2015).
Aterosklerosis dan komplikasinya menyebabkan kematian setengah dari orang
dewasa di Amerika Serikat. Lesi, atau ateroma, adalah penanda inflamasi di mana berbagai
sel, produk sel, dan interaksi lipoprotein yg menyebabkan cedera dan penyakit. Konsekuensi
penting dari interaksi ini adalah oksidasi seluler LDL, yang mengubah lipoprotein menjadi
bentuk yang sangat aterogenik. Berbagai sel jenis hadir dalam lesi aterosklerotik, termasuk
monosit/makrofag, sel-sel otot polos, dan sel-sel endotel, dapat mengoksidasi LDL . Pada
gilirannya, LDL teroksidasi menimbulkan cedera sel, proliferasi sel otot polos, pembentukan
sel busa, kemotaksis leukosit, sekresi seluler mediator inflamasi, dan hal lain yang
memodulasi ateroma biologi. LDL teroksidasi telah terdeteksi pada atherom kelinci dan
manusia, dan terapi antioksidan dapat menurunkan peristiwa kardiovaskular dan kematian,
mungkin dengan menghambat oksidasi lipoprotein. Oleh karena itu, oksidasi LDL, sebuah
mekanisme biologis dari modifikasi LDL, mungkin menjelaskan
mengapa kadar plasma tinggi LDL asli merupakan faktor risiko utama terhadap penyakit
arteri koroner. Peranan aterosklerosis sebagai penyakit inflamasi mengembangkan peran agen
infeksi yg mungkin menimbulkan pengembangan ateroma. LDL oksidasi diukur oleh agarose
gel elektroforese untuk mendeteksi kenaikan LDL oksidasi terhadap LDL sebenarnya.
(Joseph P Gaut,2001; JHM Levels;Maja Gruber,2009; James A Russel et al,2015).
2.3 PROCALCITONIN
2.3.1. Induksi dan Properti Biokimia Procalcitonin
Procalcitonin (PCT) digambarkan sebagai suatu marker sepsis pada 1993. PCT
merupakan suatu protein soluble yang dilepaskan ke sirkulasi dari pasien sebagai respon terhadap inflamasi sistemik,terkhususnya infeksi bakteri. Secara biokimia, PCT merupakan
pro-hormon dari calcitonin, tetapi fungsi biologis dan induksinya berbeda dari calcitonin.
Induksi dari sirkulasi PCT terkait dengan aktivasi dan adherensi dari sel monositik,yang
terjadi selama sepsis,demikian juga kondisi lainnya seperti setelah suatu trauma jaringan tisu
Kadar plasma PCT pada orang sehat adalah rendah (<0,1ng/ml) (Wiedermann et al.,2002). Untuk mengekslusi sepsis dan inflamasi sistemik , digunakan rentang referensi ≤
0,2ng/ml) Sebagai cut-off untuk diagnosis sepsis, nilai≥0,5ng/ml dianggap sebagai abnormal
dan mengarah kepada sepsis (Meisner, 2014)
Setelah mencapai puncaknya, PCT yang bersirkulasi akan menurun dengan 50% plasma-diappearance rate dalam 1-1,5 hari. Pada pasien dengan disfungsi ginjal yang berat, rerata eliminasi mungkin lebih lama , tetapi tidak ada akumulasi dari PCT. Berbagai fungsi biologis
dari PCT telah diketahui. Termasuk modulasi dari fungsi imunologis dan vasomotilitas.
Beberapa efek bersifattime dependent. Sebagai tambahan, PCT mempengaruhi ekspresi dari sitokin (Meisner, 2014).
Sitokin dan beberapa marker sepsis lainnya tidak menujukkan adanya keuntungan yang
signifikan dibandingkan dengan PCT, kecuali untuk beberapa fitur tertentu. Marker-marker
ini tidak mengindikasi beratnya inflamasi sistemik, atau spesifisitas relatif untuk bakteri yang
menginduksi sepsis masih rendah (Meisner,2014).
2.3.2 Diagnosis Sepsis,Sepsis Berat dan Syok Sepsis
Nilai PCT yang tinggi memiliki nilai prediksi yang tinggi untuk mendiagnosis
sepsis,sepsis berat dan syok sepsis (PCT >0,5 hingga >2ng/ml). Kontras dengan itu,PCT yang
normal atau rendah memiliki nilai presiksi negatif yang tinggi untuk menyingkirkan
inflamasi sistemik dan sepsis (PCT <0,25 hingga <0,5ng/ml).
Infeksi bakteri merupakan suatu stimulus yang kuat untuk produksi PCT, dimana bila
inflamasi sistemik disebabkan oleh virus, induksi PCT adalah rendah. Pada pasie dengan
PCT yang rendah, antibiotik sebaiknya dihentikan,jika tidak ditemukan adanya
infeksi.Antibiotik sebaiknya ditunda pada pasien neutropenia dengan demam dan nilai PCT
yang normal, dan pada pasien pankreatitis akut dengan nilai PCT yang normal masih
didiskusikan (Meisner,2014)
Beberapa guideline telah mengubah dan menambahkan PCT sebagai panduan terapi. Sebagai
contoh, guideline pneumonia terbaru dan guideline sepsis di Jerman merekomendasikan
pengobatan yang bersifat individual menggunakan PCT sebagai alat diagnosis dan
pengobatan (Hoffken et al.,2009;Reinhart et al.,2010). Sebagai tambahan, the Surviving sepsis campaign 2012 mengindikasikan PCT dapat digunakan sebagai diagnosis sepsis dan
menghentikan antibiotik pada pasien yang awalnya sepsis,tetapi tidak ada bukti infeksi
2.4 KERANGKA TEORI
INFEKSI
Pelepasan Mediator Inflamasi
Peningkatan PCT Penurunan LDL
Keparahan Sepsis
Pelepasan Sitokin anti inflamasi :(IL-1ra), IL-10
Menghambat Produksi TNF-α, IL-1ß, IL-6, IL-8