I. PENDAHULUAN
1.1 Latar Belakang Masalah
Proses penuaan dan penyakit degeneratif seperti kanker, asteroklerosis, stroke, tekanan darah tinggi, katarak serta terganggunya sistem imun tubuh, merupakan beberapa penyakit yang berkaitan dengan aktivitas radikal bebas. Banyak sekali sumber radikal bebas yang dapat masuk dan terbentuk di dalam tubuh, diantaranya melalui pernafasan, lingkungan yang tidak sehat dan banyaknya mengkonsumsi makanan yang berlemak ataupun yang tidak sehat. Menurut Qauliyah (2006), radikal bebas tersebut sebenarnya dapat dihambat dengan antioksidan.
Di dalam tubuh manusia, sudah diproduksi beberapa antioksidan seperti superoksid dismutase (SOD) (Maestro, 1991) dan gluthation peroksidase (Sies, 1991). Akan tetapi, antioksidan ini diproduksi hanya dalam jumlah tertentu. Jadi, jika tubuh dalam keadaan dan aktivitas normal, asupan makanan yang seimbang membuat kita tak perlu tambahan segala macam suplemen. Dalam keadaan tertentu, seperti meningkatnya usia, sakit, stres, bekerja terlalu keras, ibu hamil dan menyusui yang mengalami gangguan selera makan, orang yang hidup dalam lingkungan yang tidak sehat dan tercemar oleh berbagai polusi, berolahraga berat, perokok berat atau pada peminum alkohol, serta yang makanannya banyak mengandung lemak, maka mungkin sekali perlu tambahan suplemen antioksidan.
Sementara itu, dalam bunga rosella ungu mengandung antosianin sebesar 1.48 g/100 g kelopak kering (Anonymous, 2008). Antosianin merupakan salah satu jenis pigmen yang juga berfungsi sebagai antioksidan yang dapat menghambat oksidasi radikal bebas dalam tubuh (Best, 2004). Pemanfaatan kelopak bunga rosella merah sudah banyak dikenal antara lain sebagai minuman seduhan, manisan, jeli, sirup, permen dan pewarna makanan. Sedangkan pemanfaatan kelopak bunga rosella ungu belum banyak dikenal. Hal ini dikarenakan keberadaan tanaman rosella ungu saat ini masih langka. Dengan adanya pengolahan kelopak bunga rosella ungu lebih lanjut, yakni menjadi tablet effervescent sebagai suplemen antioksidan, maka akan memberikan nilai tambah dari kelopak rosella ungu itu sendiri.
Oleh karena itu, perlu dilakukan proses pembuatan produk tablet effervescent rosella ungu serta pengujian aktivitas antioksidannya secara in vivo. Harapannya dengan adanya penelitian ini akan memberikan diversifikasi produk tablet effervescent, sehingga menjadi suplemen antioksidan dan sebagai alternatif pengolahan kelopak bunga rosella ungu untuk menghindari kebusukan pasca-panen.
1.2 Perumusan Masalah
Dari uraian yang dipaparkan diatas maka dapat dirumuskan masalah yang diteliti yaitu :
1. Formulasi proporsi antara jumlah filtrat rosella ungu dengan maltodekstrin untuk mendapatkan tablet effervescent dengan sifat fisik, kimia dan organoleptik yang terbaik.
2. Aktivitas antioksidan produk tablet effervescent rosella ungu perlakuan terbaik secara in vivo.
1.3 Tujuan Program
1. Menentukan formulasi proporsi antara jumlah filtrate rosella ungu dengan maltodekstrin untuk mendapatkan tablet effervescent dengan sifat fisik, kimia dan organoleptik yang terbaik.
2. Mengetahui aktivitas antioksidan produk tablet effervescent rosella ungu perlakuan terbaik secara in vivo
1.4 Luaran yang Diharapkan
Luaran yang diharapkan dari program ini adalah diperolehnya proporsi yang tepat pada produk tablet effervescent rosella ungu sebagai suplemen antioksidan
1.5 Kegunaan Program
1. Mengangkat potensi rosella ungu untuk menambah keanekaragaman produk pangan yang memiliki sifat fungsional.
2. Memberikan masukan kepada instansi pangan dan farmasi untuk mengoptimalkan pemanfaatan tablet effervescent rosella ungu sebagai suplemen antioksidan.
3. Meningkatkan pengetahuan dan wawasan dalam dunia penelitian tentang potensi bunga rosella ungu dan produk olahannya, yaitu tablet effervescent. II. TINJAUAN PUSTAKA
Tablet Effervescent
Tablet adalah sediaan obat padat takaran tunggal yang dikempa atau dicetak dari serbuk kering, kristal, atau granulat. Umumnya dengan penambahan bahan pembantu menggunakan tekanan tinggi (Voigt, 1995). Sedangkan tablet effervescent merupakan tablet berbuih yang dibuat dengan cara kompresi granul yang mengandung garam effervescent atau bahan-bahan lain yang mampu melepaskan gas ketika bercampur dengan air (Ansel, 1989). Dasar formula pada minuman serbuk dan tablet effervescent adalah reaksi antara asidulan dengan karbonat atau bikarbonat menghasilkan karbondioksida (Hui, 1992).
Rosella Ungu
Rosella berasal dari wilayah India sampai Malaysia, dimana tanaman ini dibudidayakan dan mulai dibudidayakan pula di Afrika. Tanaman ini telah menyebar secara luas di wilayah subtropis dan di berbagai wilayah India Barat dan Amerika Tengah (Morton,1999). Terdapat dua macam warna, yakni merah dan ungu, dimana semakin tinggi intensitas warnanya, maka semakin tinggi kadar antioksidannya. Hal ini berarti bahwa kandungan antioksidan pada rosella ungu lebih besar daripada rosella merah.
Bagian rosella yang dapat diproses untuk makanan adalah kelopak bunga yang disebut kaliks (Som, 2003). Kaliks mengandung vitamin C,D,B1,dan B2. Kaliks juga mengandung 13% campuran asam malat dan asam sitratserta antosinin dan 0,004-0,0055 asam askorbat. Antosianin dipercaya sebagai salah satu pencegah munculnya penyakit diusia lanjut seperti kanker dan serangan jantung.
Antosianin
Antosianin telah dikonsumsi secara luas, suatu studi di Italia menyebutkan konsumsi per hari dari antosianin berkisar antara 25 – 215 mg tiap orang bergantung jenis kelamin dan usia, dimana dosis yang tinggi dapat mengurangi efek farmakologis. Antosianin dari Hibiscus sabdariffa (Malvaceae)
telah digunakan secara efektif pada obat kedokteran untuk melawan hipertensi, dan gangguan hati. Dianjurkan untuk mengkonsumsi minuman ringan, yang mengandung pigmen Hibiscus dimana pada dosis rendah (50 mg/kg) menunjukkan aktifitas antioksidan pada sebuah studi (Vargas and Lopez, 2003). Stabilitas Antosianin
Faktor yang penting dalam kestabilan antosianin adalah harus diproses dan diolah pada temperature rendah dengan sedikit kehadiran oksigen serta cahaya (Vargaz and Lopez, 2003). Efek suhu terhadap stabilitas antosianin pada produk makanan telah diselidiki oleh banyak peneliti dan kesimpulan secara umum bahwa antosianin akan rusak dengan pemanasan dan penyimpanan. Markakis (1982), menunjukkan bahwa pengolahan strawberry pada 100ºC dalam 1 hari menghasilkan 50% kerusakan antosianin dan bila disimpan pada suhu 38ºC dapat bertahan hingga 10 hari.
Antioksidan
Antioksidan merupakan inhibitor yang bekerja menghambat oksidasi dengan cara bereaksi dengan radikal bebas reaktif membentuk radikal bebas tak reaktif yang relatif stabil. Sistem ini dinamakan dengan sistem prtoteksi non enzimatik (Widodo, 1997).
Antioksidan dapat menetralisir radikal bebas dengan menerima atau mendonorkan sebuah elektron untuk menghasilkan molekul yang lebih stabil (berpasangan). Ini berarti molekul antioksidan menjadi radikal bebas dalam proses menetralkan molekul radikal bebas menjadi molekul yang non-radikal bebas (Best, 2004)
Radikal Bebas
Dalam dunia kedokteran, pengertian oksidan dan radikal bebas sering dibaurkan. Hal ini disebabkan karena keduanya memiliki sifat yang mirip. Aktifitas kedua senyawa ini sering menghasilkan akibat yang sama walaupun prosesnya berbeda (Tjokroprawiro, 1993). Namun, dipandang dari sudut ilmu kimia, keduanya haruslah dibedakan (Suryohudoyo, 1997). Dalam ilmu kimia, oksidan berarti senyawa penerima elektron (electron acceptor) atau senyawa yang dapat menarik elektron (Tjokroprawiro, 1993).
Bahan Pengisi
Menurut Dewi (2000), bahan pengisi merupakan bahan yang ditambahkan pada proses pengolahan pangan untuk melapisi komponen-komponen flavor, meningkatkan jumlah total padatan, memperbesar volume, mempercepat proses pengeringan dan mencegah kerusakan bahan akibat panas. Bahan tersebut berupa padatan dengan berat molekul tinggi yang mudah terdispersi (Hartomo dan Widiatmoko, 1994).
Sukrosa
Sukrosa mempunyai sifat sedikit higroskopis dan mudah larut dalam air. Semakin tinggi suhu, kelarutannya semakin besar. Kristal sukrosa bersifat stabil di udara terbuka dan dalam keadaan yang langsung berhubungan dengan udara dapat menyerap air sebanyak 1% dari total berat dan akan dilepaskan kembali apabila dipanaskan pada suhu 90ºC (Sudarmaji, 1982)
Bahan Tambahan - Natrium Bikarbonat
Senyawa karbonat yang banyak digunakan dalam formulasi effervescent adalah garam karbonat kering karena kemampuannya menghasilkan
karbondioksida. Natrium bikarbonat (NaHCO3) dipilih sebagai penghasil karbondioksida dalam pembuatan effervescent karena harganya murah dan bersifat larut sempurna dalam air (Dewi, 2000).
- Asam Sitrat
Asam sitrat adalah asidulan yang sering digunakan untuk makanan dan minuman karena dapat memberikan kombinasi sifat yang diinginkan selain karena tersedia dalam jumlah yang besar dengan harga murah. Asidulan dapat berfungsi sebagai pemberi rasa asam, penguat rasa dan mengontrol pH (Hui,1992).
Pengujian In Vivo
Pengujian secara biologis biasanya menggunakan hewan coba untuk membantu menjalankan penelitian yang tidak bisa secara langsung dilakukan dalam tubuh manusia dengan asumsi semua jaringan, sel-sel penyusun tubuh serta enzim-enzim yang ada dalam tubuh hewan coba memiliki kesamaan dengan manusia (Arrington, 1972). Hewan percobaan yang banyak digunakan dalam uji ini adalah tikus, mencit, hamster, marmot, kucing, anjing, babi, primate, kambing. Pada tahun 1996 penelitian menggunakan hewan coba menunjukkan bahwa 85 % dari 2,72 juta prosedur menggunakan rodentia. Rodentia merupakan kelompok hewan mamalia yang habitatnya mudah ditemukan dengan sifat yang hampir sama.
III. METODE PENDEKATAN 3.1 Rancangan Penelitian
Rancangan penelitian yang digunakan adalah Rancangan Acak Lengkap (RAL) yang tersusun atas 2 faktor, dimana faktor pertama terdiri dari 3 level dan faktor kedua terdiri dari 3 level, dengan 3 kali ulangan. Faktor tersebut adalah: Faktor I : % penambahan bahan pengisi terhadap filtrat
F1 = 40% dekstrin (b/v filtrat rosela) F2 = 50% dekstrin (b/v filtrat rosela) F3 = 60% dekstrin (b/v filtrat rosela) Faktor II : Metode pengeringan
P1 = oven kabinet P2 = oven kering P3 = oven vakum
Dari kedua faktor tersebut diperoleh kombinasi perlakuan sebagai berikut : F1P1 = 40% dekstrin (b/v) dengan metode pengeringan oven kabinet F1P2 = 40% dekstrin (b/v) dengan metode pengeringan oven kering F1P3 = 40% dekstrin (b/v) dengan metode pengeringan oven vakum F2P1 = 50% dekstrin (b/v) dengan metode pengeringan oven kabinet F2P2 = 50% dekstrin (b/v) dengan metode pengeringan oven kering F2P3 = 50% dekstrin (b/v) dengan metode pengeringan oven vakum F3P1 = 60% dekstrin (b/v) dengan metode pengeringan oven kabinet F3P2 = 60% dekstrin (b/v) dengan metode pengeringan oven kering F3P3 = 60% dekstrin (b/v) dengan metode pengeringan oven vakum 3.2 Analisa Data
Data yang diperoleh dianalisa dengan Analisis Varian (ANOVA) dilanjutkan dengan uji beda nyata yaitu BNT (Beda Nyata Terkecil) menggunakan selang kepercayaan 1% dan 5% serta DMRT (Duncan Multiple Range Test) dengan selang kepercayaan 1% dan 5% (Yitnosumarto,1991).
IV. PELAKSANAAN PROGRAM 4.1 Waktu dan Tempat Pelaksanaan
Penelitian ini akan dilaksanakan selama 4 bulan dan dilakukan di beberapa tempat, yaitu:
1. Laboratorium Pengolahan Pangan, THP-UB, tempat pembuatan tablet effervescent.
2. Laboratorium Biokimia dan Nutrisi, THP-UB, tempat analisa kimia.
3. Laboratorium Farmasetika, Fakultas Farmasi UNAIR, tempat pentabletan. 4. Laboratorium Farmakologi, FK-UB, tempat pemeliharaan tikus, pengujian
nilai MDA dan SOD. 4.2 Jadwal Pelaksanaan
Jenis kegiatan
Waktu Kegiatan (Minggu ke-) Bulan 1 Bulan 2 Bulan 3 Bulan 4 1. Penyiapan alat dan bahan
2. Pembuatan filtrat rosella ungu 3.Pembuatan tablet effervescent rosella
ungu
4. Tahap pengujian
5. Pemeliharaan tikus
6. Tahap in vivo
7. Tahap pengujian akhir
8. Pengumpulan data
9. Analisa data
10. Penyusunan laporan akhir 4.3 Instrumen pelaksanaan
Alat
Alat yang digunakan dalam membuat ekstrak rosella ungu adalah blender kering, spatula, beaker glass 500ml, baskom, kain saring, gelas ukur 50ml, dan timbangan analitik (Denver instrument M-310). Oven kabinet, oven kering, oven vakum dan alat pencetak tablet.
Alat-alat yang digunakan untuk analisa antara lain timbangan analitik (Mettler AE 160 kapasitas maksimal 150 g), pH meter, gelas ukur 50, erlenmeyer, beaker glass, sentrifuse, tabung reaksi, pemanas, spektrofotometer, dan pipet. Bahan
Bahan yang digunakan dalam penelitian ini adalah kelopak bunga rosella ungu yang diperoleh dari Kecamatan Semen Kabupaten Kediri. Bahan pengisi yaitu dekstrin, asam sitrat, natrium bikarbonat dan sukrosa.
Bahan untuk analisa yaitu kertas saring, indikator PP, akuades, etanol p.a, methanol, HCl, NaOH, Nelson arsenomolibdat, larutan DPPH 0,2 M, folin ciocalteu, asam galat, EDTA, bu
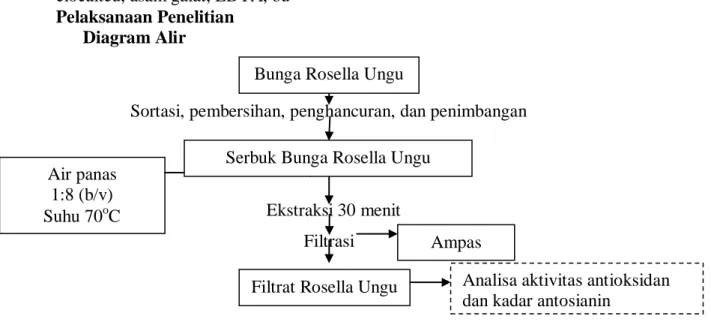
Pelaksanaan Penelitian Diagram Alir
.
Gambar 1. Diagram Alir Proses Pembuatan Filtrat Rosella Ungu
Analisa aktivitas antioksidan dan kadar antosianin
Air panas 1:8 (b/v)
Suhu 70oC Ekstraksi 30 menit
Filtrasi Ampas Filtrat Rosella Ungu
Sortasi, pembersihan, penghancuran, dan penimbangan Bunga Rosella Ungu
Serbuk Bunga Rosella Ungu
Pencampuran Ekstrak Rosella Ungu Basah Perlakuan Faktor II (metode pengeringan)
Diblender 1 menit Filtrat Rosella Ungu
40% (b/v) 50% (b/v) 60% (b/v)
Oven kabinet Oven kering Oven vakum
Serbuk Ekstrak Rosella Ungu - Asam sitrat 16 % (b/b)
- Gula pasir 75% (b/b) - Na-bikarbonat 16% (b/b)
Perlakuan Faktor I (% penambahan dekstrin) Dekstrin
Diblender 2 menit
Gambar 2. Diagram Alir Proses Pembuatan Tablet Effervescent Rosella Ungu Pengamatan Penelitian
Pengamatan penelitian tablet effervescent rosella ungu meliputi analisa terhadap pH (Apriyantono, 1989), derajat kecerahan (Yuwono dan Susanto), derajat kemerahan (Yuwono dan Susanto), aktivitas antioksidan, kadar antosianin (Giusti and Wrolstad, 2000), kecepatan larut, dan organoleptik meliputi uji kesukaan.
4.4 Rancangan dan Realisasi Biaya 1. Bahan baku
Jenis Bahan Kebutuhan Jumlah
1. Bahan Baku Penelitian - Kelopak bunga rosella ungu - Maltodekstrin - Dekstrin - Asam sitrat - Na-bikarbonat - Sukrosa Rp. 90.000/kg Rp. 25.000/kg Rp. 19.600/kg Rp. 20.000/kg Rp. 12.000/kg Rp. 17.300/kg 4,5 kg 1 kg 2,5 kg 1 kg 1 kg 1,5 kg Rp. 405.000 Rp. 25.000 Rp. 49.000 Rp. 20.000 Rp. 12.000 Rp. 25.950 2. Bahan Kimia untuk analisa
- DPPH 0,2 mM - Etanol p.a
- KCl, Na-asetat, HCl - Aquadest
- Methanol
- bahan kimia lain
Rp. 2.150/ml - - Rp. 1000/liter - - 100 mL 1 liter - 50 liter 2,5 liter - Rp. 215.000 Rp. 190.000 Rp. 147.500 Rp. 50.000 Rp. 301.000 Rp. 100.000
3. Tikus wistar - 35 ekor Rp. 1.100.000
Total Rp. 2.640.450
2. Peralatan penunjang
Jenis Biaya satuan Kebutuhan Jumlah
1. Kain saring Rp. 10.000/meter 3 Rp. 30.000
2. Peralatan Tambahan - - Rp. 263.865 3. Loyang Rp. 11.000/loyang 4 Rp. 44.000 4. Pentabletan - 40 tablet Rp. 90.000 5. Pemakaian lab. - - Rp. 20.000 Total Rp. 447.865 Homogenisasi Pengayakan 60 mesh Pentabletan Analisa: 1. pH 2. Derajat kemerahan 3. Aktivitas antioksidan 4. Kadar antosianin 5. Kecepatan larut 6. Organoleptik Serbuk Effervescent Rosella Ungu
3. Lain-lain
Jenis Biaya satuan Kebutuhan Jumlah
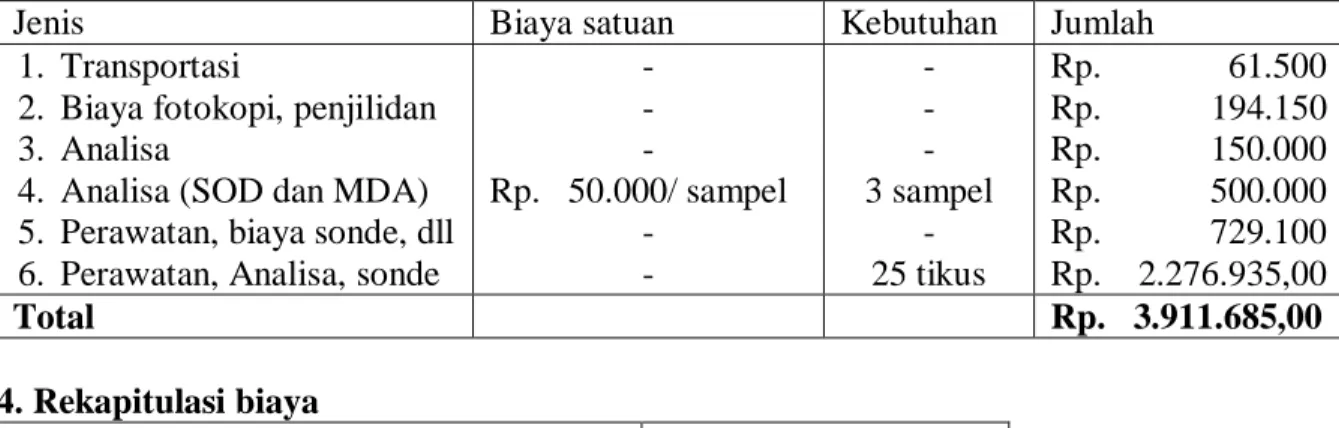
1. Transportasi
2. Biaya fotokopi, penjilidan 3. Analisa
4. Analisa (SOD dan MDA) 5. Perawatan, biaya sonde, dll 6. Perawatan, Analisa, sonde
- - - Rp. 50.000/ sampel - - - - - 3 sampel - 25 tikus Rp. 61.500 Rp. 194.150 Rp. 150.000 Rp. 500.000 Rp. 729.100 Rp. 2.276.935,00 Total Rp. 3.911.685,00 4. Rekapitulasi biaya Jenis Jumlah 1. Bahan baku Rp. 2.640.450 2. Peralatan penunjang Rp 447.865 3. Lain-lain Rp. 3.911.685 Total Rp. 7.000.000
V. HASIL DAN PEMBAHASAN
Penelitian yang sudah dilakukan meliputi pemisahan pembuatan filtrat rosella ungu, pembuatan tablet effervescent rosella ungu, analisa pH, derajat kecerahan, derajat kemerahan, aktivitas antioksidan, kadar antosianin, kecepatan larut dan organoleptik serta pengujian SOD dan MDA.
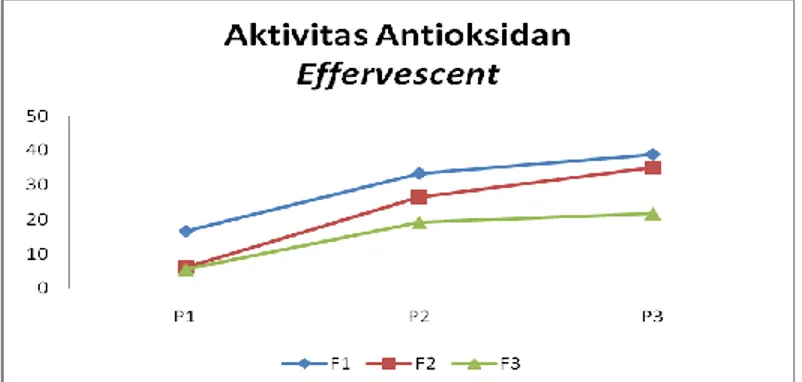
1. Analisa aktivitas antioksidan
Pada perlakuan oven vakum, aktivitas antioksidan paling tinggi dikarenakan antioksidan tidak bisa keluar dari lingkungan vakum saat proses pemanasan. Selain itu, semakin sedikit konsentrasi bahan pengisi maka aktivitas antioksaidan juga akan semakin tinggi. Hal ini dikarenakan konsentrasi filtrat yang ada pada bahan jumlahnya besar. 2. Analisa MDA
Gambar 3. Grafik pengaruh pemberian effervescent rosella ungu terhadap nilai MDA pada tikus wistar perlakuan normal, jelantah dan jelantah + dosis I
Nilai MDA paling tinggi ada pada perlakuan jelanntah lalu diikuti oleh jelantah + dosis 1. Hal ini dikarenakan antioksidan yang ada di dalam hewan coba tidak mencukupi untuk menangkal radikal bebas (berupa pemberian minyak jelantah yang mempunyai bilangan peroksida 118 mek/kg) yang diperlakukan terhadap hewan coba.
3. Analisa SOD
Gambar 4. Grafik pengaruh pemberian effervescent rosella ungu terhadap nilai MDA pada tikus wistar perlakuan normal, jelantah dan jelantah + dosis II
Nilai SOD paling tinggi ada pada perlakuan normal lalu diikuti oleh minyak jelantah dosis II. Nilai SOD tinggi, hal ini dikarenakan SOD bereaksi dengan antioksidan. Dapat disimpulkan bahwa semakin tinggi antioksidan, maka nilai SOD juga semakin tinggi.
VI. KESIMPULAN DAN SARAN Kesimpulan
1. Didapatkan formulasi proporsi antara jumlah filtrat rosella ungu dengan dekstrin 50% perlakuan oven vakum dalam bentuk tablet effervescent rosella ungu.
2. Aktivitas antioksidan terbaik ada pada perlakuan dosis 3 (2700mg/ 12ml) seduhan effervescent rosella ungu terhadap tikus wistar.
Saran
1. Menggunakan pemanis buatan yang kemanisan tinggi supaya didapatkan sifat organoleptik yang baik.
2. Perlu adanya analisa kuantitatif terhadap jenis pigmen yang ada pada rosella ungu.
VII. DAFTAR PUSTAKA
Anonymous. 2008. Roselle. http://www.wikipedia.org/wiki/Roselle/. [8 Februari 2008]
Ansel, H., 1989. Pengantar Bentuk Sediaan Farmasi. Edisi ke – 4. UI Press. Jakarta
Best, Ben. 2004. General Antioxidants Actions. Journal Chemistry and Biochemistry Free Radical
Dewi, A.K. 2000. Pengaruh Jenis dan Konsentrasi Bahan Pengisi Terhadap Sifat Fisik, Kimia dan Organoleptik Serbuk Effervescent Temulawak (Curcuma Xanthoririza Roxb.). Skripsi. Fakultas Teknologi Pertanian. Universitas Brawijaya. Malang
Hui, Y.H., 1992. Encyclopedia of Food Science and Technology. Jhon Wiley and Sons Inc. New York
Kim, O.S. 2005. Radical Scavenging Capacity and Antioxidants Activity of The E Vitamin Fraction in Rice Bran. J. Food Science Vol. 70 No. 3.208-213 Maestro, R.D. 1991. Free Radical as Mediators of Tissue Injury. Di dalam
Dreosti I.E., edition. Trace Elements, Micronutrients, and Free Radicals. Humana Press. New Jersey
Markakis, O. 1982. Anthocyanins as Food Additive. Dalam Stabilitas Antosianin Garcina Mangostana dalam Minuman Berkarbonat. Skripsi. Budiarto, H. 1991. FTP. IPB. Bogor
Morton, J. F. 1999. Roselle Hibiscus sabdariffa L. http://www.transgenica.com/ database/h/hibiscus.htm. [1 Oktober 2009
Qauliyah, Asta. 2006. Mekanisme Kerja Beberapa Antioksidan.
http://astaqauliyah.com/2006/04/17/mekanisme-kerja-beberapa-antioksidan/. [30 September 2009]
Sies, H. 1991. Oxidative Stress. From Basic Research to Clinical Aplication. The American Journal Medicine 91: Suppl 3c. Cahners Publishing Company Som. Fandah Mohd. 2003. Roselle Bunga yang Enak Dimakan. Pusat Teknologi
Makanan. Mardi Serdang
Sudarmadji, Slamet, Haryono, Bambang, dan Suhardi. 1997. Prosedur Analisa untuk Bahan Makanan dan Pertanian. Liberty. Yogyakarta
Suryohudoyo, P. 1997. Oksidan dan Antioksidan pada Diabetes Melitus. Di dalam Tjokroprawiro, A. et al. Proceedings of The Third Surabaya Diabetes Up Date. Surabaya.
Tjokroprawiro, A. 1997. Diabetes Up Date 1997A. In Tjokroprawiro, A. et al. Proceedings of The Third Surabaya Diabetes Up Date. Surabaya.
Vargaz, F. D. and Lopez, O.P., 2003. Natural Colorants for Food and Nutraceutial Uses. CRC Press. USA.
Voight, R. 1995. Buku Pelajaran Teknologi Farmasi. Edisi Kedua. Penerjemah Soendari. Gajah Mada University Pers. Yogyakarta
LAMPIRAN
Dokumentasi Kegiatan Penelitian
Gambar 5. Rosella Ungu kering Gambar 6. Rosella Merah vs Ungu
Gambar 7. Proses penyeduhan Gambar 8. Filtrasi
Gambar 11. Perlakuan oven listrik Gambar 12. Perlakuan oven vakum
Gambar 13. Serbuk effervescent Gambar 14. Sampel siap disentrifuge
Gambar 15. Pengukuran aktivitas antioksidan
Gambar 17. Uji organoleptik Gambar 18. Penyondean jelantah oleh panelis
Gambar 16. Pengukuran bilangan peroksida minyak jelantah
Analisa nilai pH
Gambar 19. Grafik Pengaruh Perlakuan % Penambahan Dekstrin dengan Metode Pengeringan Terhadap Nilai pH Tablet Effervescent Rosella Ungu Analisa derajat kemerahan (*a)
Gambar 20. Grafik Pengaruh Perlakuan % Penambahan Dekstrin dengan Jenis Metode Pengeringan Terhadap Derajat Kemerahan (a*) Sesudah Pelarutan Tablet Effervescent Rosella Ungu
Analisa aktivitas antioksidan
Gambar 21. Grafik Pengaruh Perlakuan % Penambahan Dekstrin dengan Metode Pengeringan Terhadap Aktivitas Antioksidan Tablet Effervescent Rosella Ungu
Analisa kadar antosianin
Gambar 22. Grafik Pengaruh Perlakuan % Penambahan Dekstrin dengan Metode Pengeringan Terhadap Kadar Antosianin Tablet Effervescent Rosella Ungu
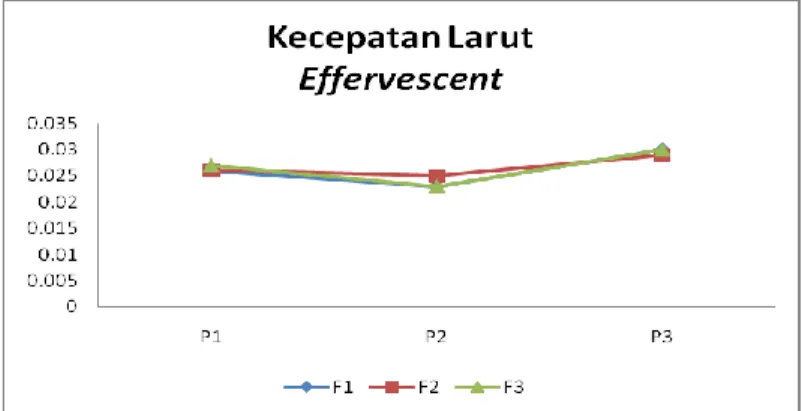
Analisa kecepatan larut
Gambar 23. Grafik Pengaruh Perlakuan % Penambahan Dekstrin dengan Metode Pengeringan Terhadap Kecepatan Larut Tablet Effervescent Rosella Ungu
METODE ANALISA SOD DAN MDA Pemeriksaan SOD
Panjang gelombang maksimal formazan (sebagai penentu aktivitas SOD) yaitu 580 nm.
Penentuan xanthine-xanthine oxidase untuk 1 unit SOD dan kurva baku SOD :
Konsentrasi per 3 cc = jadi absorbansi untuk 3 unit/ 3 cc (1 unit) SOD sama dengan 50% absorbansi jika tanpa diberikan SOD (0 unit). Kondisi ini yang dipakai untuk pengukuran sampel berikut.
Evaluasi SOD dari sampel serum
Prinsip pemeriksaan SOD : mengukur formazan, hasil reduksi NBT (nitro blue tetrazolium) oleh radikal superoksid. Radikal superoksid terbentuk dari reaksi xanthine dan xanthine oxidase. Satu unit aktivitas SOD menunjukkan sejumlah enzim yang dibutuhkan untuk menghambat reduksi NBT menjadi 50% dalam kondisi tertentu (Rukmin et al., 2004).
Serum diambil dari 250µL dimasukkan ke dalam tabung, ditambahkan berturut-turut EDTA 200µL, NBT 100µL, xanthine 100µL, xanthine oxidase 100µL dan buffer fosfat 1cc. Inkubasi pada temperature 37ºC selama 30 menit. Kemudian sentrifus dan ambil supernatant. Tambahkan buffer fosfat hingga 3.3cc. Siap diukur dengan spektrofotometer pada panjang gelombang 580nm
Pemeriksaan Malonaldehid (MDA)
Prinsip pengukuran : MDA yang merupakan produk sekunder dari lipid peroksidasi akan bereaksi dengan thiobarbituric acid (TBA) pada suasana asam (pH 2-3) dan temperature 97-100ºC memberikan warna pink (Rukmini et al., 2004)
Penentuan panjang gelombang maksimal : didapatkan 531,6 nm Penentuan kadar MDA sampel (serum)
200µL serum + TCA 40%, kocok + 0.25ml HCl 0.1 N
+ air/ bides 0.5ml + Sodium Barbiturat Acid 10%
Panaskan 105ºC selama 25 menit (Flower, 1973)
Sentrifuge dan ambil supernatannya, bila masih keruh lalu disaring dengan kertas saring biasa
Kemudian jadikan 3 ml, baca pada spektrofotometer dengan panjang gelombang 531,6nm (532nm)