EVALUASI STABILITAS SEDIAAN SALEP
EKSTRAK KULIT BUAH PINANG (Areca
catechu L.) di JAYAPURA
SKRIPSI
Oleh :
MUHAMMAD ZAENAL BASRI RAHIM NIM 0110540102
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS CENDERAWASIH
JAYAPURA 2015
EVALUASI STABILITAS SEDIAAN SALEP
EKSTRAK KULIT BUAH PINANG (Areca
catechu L) di JAYAPURA
SKRIPSI
Diajukan Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Farmasi Program Studi Farmasi
Oleh :
MUHAMMAD ZAENAL BASRI RAHIM NIM 0110540102
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS CENDERAWASIH
JAYAPURA 2015
ABSTRAK
Rahim, M. Zaenal Basri. 2015. Evaluasi Stabilitas Sediaan Salep Ekstrak Kulit
Buah Pinang (Areca catechu L) di Jayapura
.
Skripsi Program Studi Farmasi, Jurusan Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Cenderawasih Jayapura.Kulit buah pinang (Areca catechu L.) merupakan salah satu tanaman asal Papua yang memiliki potensi secara tradisional dalam mengobati berbagai macam penyakit seperti bisul, sebagai obat sakit kulit, pendarahan, gangguan pencernaan, sembelit. Pinang (Areca catechu L.) merupakan famili dari Arecaceae. Metode skrining fitokimia kulit buah pinang menggunakan metode Farnsworth. Hasil dari ekstrak etanol kulit buah pinang mengandung golongan senyawa alkaloid, flavonoid, tanin, saponin, dan kuinon. Pada penelitian ini ekstrak kulit buah pinang diformulasi menjadi salep dengan berbagai konsentrasi ekstrak kulit buah pinang 0,2%, 0,4%, 0,6%. Penelitian ini bertujuan untuk mengetahui kestabilan sediaan yakni organoleptik, uji homogenitas, daya sebar, daya lekat, uji pH serta dilakukan uji keamanan (uji iritasi). Dari hasil penelitian stabilitas ketiga formulasi sediaan salep memiliki nilai pH=5, terdapat peningkatan daya sebar pada ketiga formulasi salep dan adanya penurunan waktu daya lekat ketiga formulasi salep kulit buah pinang, pada uji iritasi ketiga formulasi tidak mengiritasi kulit.
ABSTRACT
Rahim, M. Zaenal Basri. 2015. Stability evaluation of ointment formulation of
Bettle Nut Skin extract (Areca catechu L.) Thesis Program Study of Pharmacy,
Biology Department, Faculty Of Mathematics and Natural Sciences, Cendrawasih University.
Bettle nut skin (Areca catechu L.) is one original plants of Papua which has potential traditional in treatment various disease in treating a wide range of as it boils, as pain medication skin, bleeding, indigestion, constipation. Bettle nut
(Areca catechu L.) is the family of Arecaceae. The phytochemical screening
Bettle nut skin was done by using Farnswort method. The result showed that ethanolic extract of skin Areca catechu Linn countain flavonoid, alkaloids, tannins, saponins, and quinone. In this study, formulated extract Bettle nut skin in the ointment base with concentration extract 0,2%, 0,4%, 0,6%. This study aims to determine stability the ointment formulation is organoleptic test, homogenity, dispersive power, adhesion power, pH, and irritation test. Result of evaluation stability ointment from Bettle nut skin has a pH=5, here is an increase in the third dispersive power ointment formulations and a decrease in the stickiness of a third formulation of Bettle nut skin ointment, the third irritation test formulation does not irritate the skin.
LEMBAR PERSETUJUAN
Skripsi dengan judul: EVALUASI STABILITAS SEDIAAN SALEP
EKSTRAK KULIT BUAH PINANG (Areca catechu L) DI JAYAPURA oleh
Muhammad Zaenal Basri Rahim telah siap diujikan
Jayapura, 9 Oktober 2015
LEMBAR PENGESAHAN
Skripsi dengan judul: Evaluasi Stabilitas Sediaan Salep Ekstrak Kulit Buah
Pinang (Areca catechu L) Di Jayapura oleh Muhammad Zaenal Basri Rahim telah dipertahankan di depan Dewan Penguji pada hari Senin tanggal 12 Oktober 2015.
Dewan Penguji
Nama Jabatan Tanda
Tangan
1 Dr. Frans A. Asmuruf, M.Si Ketua (...) NIP. 19750428 200112 1 003
2 Elsye Gunawan, S.Farm, M.Sc, Apt Sekertaris (...) NIP. 19821118 2012 12 2001
3 Dr. Linus Yhani Chrystomo, M.Si Anggota (...) NIP. 19590201 198803 1 002
4 Septriyanto Dirgantara, S.Farm., M.Si., Apt Anggota (...) NIP. 19860903 201212 1 002
5 Rani Dewi Pratiwi, S.Farm., M.Si., Apt Anggota (...) NIP. 19870929 201404 2 001
Mengesahkan
Dekan Fakultas MIPA Ketua Prodi Farmasi
Drs. Daniel Napitupulu, M.Si Dr. Linus Yhani Chrystomo, M.Si NIP. 19610517 199203 1 001 NIP. 19590201 198803 1 002
PERSEMBAHAN
Skripsi ini saya persembahkan kepada Ayahanda dan Ibunda tercinta : Abdul Rahim Barata dan Apriati Saudara terkasih : Nurwahida Puspati Muhammad Rahmat Muhammad Syaeful Siti F. Nurhartina
PEDOMAN PENGGUNAAN SKRIPSI
Skripsi S1 FMIPA Uncen yang tidak dipublikasikan, terdaftar dan tersedia di Perpustakaan Universitas Cenderawasih dan terbuka untuk umum dengan ketentuan bahwa hak cipta ada pada penulis.
Referensi kepustakaan diperkenankan dicatat, tetapi pengutipan atau peringkasan hanya dapat dilakukan seizin penulis, dan harus disertai dengan kebiasaan ilmiah untuk menyebutkan sumbernya.
Memperbanyak atau menerbitkan sebagian atau seluruh skripsi haruslah seizin Rektor Universitas Cenderawasih.
Perpustakaan yang meminjam skripsi ini untuk keperluan anggotanya harus mengisi nama dan tanda tangan peminjam dan tanggal pinjam.
UCAPAN TERIMAKASIH
Puji syukur penulis panjatkan kehadirat Allah SWT yang telah melimpahkan rahmat dan karunia-Nya sehingga penulis dapat menyelesaikan tugas akhir dalam bentuk skripsi dengan judul : “Evaluasi Stabilitas Sediaan
Salep Ekstrak Kulit Buah Pinang (Areca catechu L) Di Jayapura”.
Dalam kesempatan ini penulis ingin mengucapkan terima kasih kepada semua pihak yang telah bersedia memberikan bantuan baik moril maupun material selama masa perkuliahan hingga skripsi ini selesai, yakni kepada :
Penulis mengucapkan terima kasih kepada :
1 Rektor Universitas Cenderawasih, Bapak Dr. Onesimus Sahuleka, S.H., M.Hum, yang telah memberikan izin kepada penulis, untuk mengikuti program Pendidikan S1 di Universitas Cenderawasih.
2 Dekan FMIPA, Bapak Drs. Daniel Napitupulu, M.Si, beserta karyawan yang telah memberikan fasilitas dan pelayanan selama menjalankan pendidikan S1 Farmasi.
3 Ketua Jurusan Biologi, Bapak Dr. Dirk Runtuboi, M.Kes.
4 Ketua Program Studi Farmasi, Bapak Dr. Linus Y. Chrystomo, M.Si
5 Bapak Dr. Frans A. Asmuruf, M.Si selaku pembimbing I, atas segala bantuan dan bimbingan selama penelitian berjalan hingga penulisan skripsi
6 Ibu Elsye Gunawan, S.Farm, M.Sc, Apt Selaku Pembimbing II, atas segala bantuan dan bimbingan selama penelitian berjalan hingga penulisan skripsi 7 Bapak Frans Deminggus dan Bapak Frans Kafiar yang telah memberikan izin,
serta membantu dalam pelaksanakan penelitian di Laboratorium Kimia.
8 Dosen-dosen Farmasi yang selama 4 tahun ini telah membantu, membina, dan memberikan motivasi bagi penulis.
9 Kepada kedua orang tua, Bapak Abdul Rahim Barata dan Ibu Apriati serta kakak Nurwahida Puspati, kakak Muh. Rahmat, kakak Muh. Syaeful dan adik Siti F. Nurhartina yang tak pernah berhenti memberikan perhatian, kasih sayang, cinta dan do’a yang tulus untuk keberhasilan penulis dalam menggapai mimpi dan cita-cita.
10 Para sahabat, Dina, Vivi, Indah, Betty, Ani, Vani, Ambar, Trya, Ity, Lina, dan Sepe atas semangatnya selama ini.
11 Teman-teman farmasi angkatan 2011, terimakasih untuk kebersamaan selama 4 tahun ini.
12 Semua pihak baik langsung maupun tidak langsung yang telah membantu penulis selama penelitian dan penulisan skripsi ini.
Penulis menyadari bahwa skripsi ini masih jauh dari kesempurnaan. Untuk itu penulis mengharapkan kritik dan saran yang membangun demi kesempurnaan skripsi ini. Akhir kata penulis berharap semoga skripsi ini dapat bermanfaat bagi ilmu pengetahuan khususnya di bidang Farmasi.
Jayapura, September 2015
DAFTAR ISI
Halaman ABSTRAK...iii ABSTRACT...iv LEMBAR PERSETUJUAN...v LEMBAR PENGESAHAN...vi PERSEMBAHAN...viiPEDOMAN PENGGUNAAN SKRIPSI...viii
UCAPAN TERIMAKASIH...ix DAFTAR ISI...xi DAFTAR LAMPIRAN...xiv DAFTAR GAMBAR...xv DAFTAR TABEL...xvi DAFTAR SINGKATAN...xvii BAB I PENDAHULUAN...1 1.1 Latar Belakang...1 1.2 Rumusan Masalah...3 1.3 Tujuan Penelitian...3 1.4. Manfaat Penelitian...3
BAB II TINJAUAN PUSTAKA...4
2.1 Tumbuhan Pinang...4 2.1.1 Klasifikasi...4 2.1.2 Morfologi...4 2.1.3 Kandungan...6 2.2 Simplisia...6 2.3 Ekstrak...7 2.3.1 Metode Ekstraksi...7
2.4 Tinjauan Sediaan Salep...9
2.4.2 Persyaratan salep...9 2.4.3 Penggolongan salep...10 2.4.4 Monografi Bahan...11 2.5. Uji Stabilitas...11 2.5.1. Uji Organoleptik...12 2.5.2. Uji Homogenitas...12 2.5.3. Uji pH...12
2.5.4. Uji Daya Sebar...12
2.5.5. Uji Daya Lekat...12
2.5.6. Uji Keamanan (Patch Test)...13
2.5.7. Uji Stabilitas/Penyimpanan...13
BAB III METODE PENELITIAN...14
3.1 Waktu Penelitian...14
3.2. Alat dan Bahan...14
3.2.1. Alat...14 3.2.2. Bahan...14 3.3. Metode...14 3.4. Prosedur Kerja...15 3.4.1. Pengumpulan Sampel...15 3.4.2. Pembuatan Simplisia...15 3.4.3. Ekstraksi...15 3.4.4. Skrining Fitokimia...15
3.4.5. Pembuatan Formulasi Sediaan Salep Ekstrak Kulit Buah Pinang...17
3.5 Analisis Stabilitas...18
3.5.1. Uji Organoleptik...18
3.5.2. Uji pH...18
3.5.4. Uji Daya Sebar...18
3.5.5. Uji Daya Lekat...19
3.5.6. Uji Stabilitas Sediaan Salep...19
3.5.7. Pengujian Keamanan Sediaan Salep...19
BAB IV HASIL DAN PEMBAHASAN...20
4.1 Pembuatan Simplisia Kulit Buah Pinang...20
4.2 Pemeriksaan Organoleptik...21
4.3 Ekstraksi Kulit Buah Pinang...21
4.4 Skrining Fitokimia Simplisia...22
4.5 Hasil Pengamatan Formulasi dan Pemeriksaan Stabilitas Sediaan Salep...24
4.5.1. Hasil Uji Organoleptik Salep Kulit buah pinang...24
4.5.2. Uji pH Salep Ekstrak Kulit Buah Pinang...26
4.5.3. Uji Homogenitas...26
4.5.4. Uji Daya Sebar Salep Ekstrak Kulit Buah Pinang...27
4.5.5. Uji Daya Lekat Sediaan Salep Ekstrak Kulit buah pinang...29
4.5.6 Pengujian Keamanan Sediaan Salep Ekstrak Kulit Buah Pinang 30 BAB V PENUTUP...31 5.1 Kesimpulan...31 5.2 Saran...31 DAFTAR PUSTAKA...32 LAMPIRAN...35
DAFTAR LAMPIRAN
Halaman Lampiran 1. Proses pembuatan simplisia kulit buah pinang (Areca
catechu L.)...35
Lampiran 2. Proses pembuatan ekstrak etanol kulit buah pinang (Areca catechu L.)...36 Lampiran 3. Hasil uji skrining fitokimia pada simplisia kulit buah
pinang (Areca catechu L.)...37 Lampiran 4. Hasil uji skrining fitokimia pada ekstrak etanol kulit
buah pinang (Areca catechu L.)...37 Lampiran 5. Pembuatan Formulasi Sediaan Salep dari Ekstrak
Kulit buah pinang (Areca catechu L.)...38 Lampiran 6. Hasil Evaluasi Stabilitas Formulasi Sediaan Salep
Dari Ekstrak Kulit buah pinang (Areca catechu L.)...39 Lampiran 7. Hasil Uji Daya Lekat Salep Ekstrak Kulit Buah Pinang
Hari 1 dan Hari 21...41 Lampiran 8. Hasil Uji Keamanan Salep Ekstrak Kulit Buah Pinang
DAFTAR GAMBAR
Halaman Gambar 2.1. Gambar Pinang (Arecha catechu L.)...5
DAFTAR TABEL
Halaman Tabel 4.1. Hasil Uji Organoleptik Simplisia Kulit buah pinang...21 Tabel 4.2. Rendemen Ekstrak Etanol Kulit Buah Pinang (Areca
catechu L.)...22
Tabel 4.3. Hasil Skrining Fitokimia Simplisia dan Ekstrak Etanol Kulit Buah Pinang...23 Tabel 4.4. Hasil Uji organoleptik sediaan Salep Ekstrak Kulit Buah
Pinang Hari ke 1...24 Tabel 4.5. Hasil Uji Organoleptik Sediaan Salep Ekstrak Kulit Buah
Pinang Hari ke 21...25 Tabel 4.6. Hasil Uji pH Sediaan Salep Ekstrak Kulit Buah Pinang26 Tabel 4.7. Hasil Uji Homogenitas Salep Ekstrak Kulit Buah Pinang
...27 Tabel 4.8. Hasil Uji Daya Sebar Salep Ekstrak Kulit Buah Pinang 28 Tabel 4.9. Hasil Uji Daya Lekat Salep Ekstrak Kulit buah pinang
hari ke 1 dan hari ke 21...29 Tabel 4.10. Hasil Uji Keamanan Salep Salep Ekstrak Kulit Buah
DAFTAR SINGKATAN
Singkatan Nama singkatan
Pemakaian pertama kali pada halaman IC50 Inhibitory Concentration 2 µg Mikro Gram 2 mL Mili liter 2 pH Power of Hydrogen 3 cm Centi meter 4 M Meter 4 Mm Mili meter 5
PEG Polietilen Glikol 9 PD Pereaksi Dragendrof 15 PS Pereaksi Steasny 15 PM Pereaksi Mayer 15 P-LB pereaksi Liebermann-Burchard 15 0C Derajat Celcius 15 G Gram 16
BAB I
PENDAHULUAN
1.1 Latar BelakangIndonesia merupakan negara yang sangat kaya akan sumber daya alam. Baik yang berasal dari nabati maupun hewani. Sumber daya alam hayati yang melimpah tersebar luas dari berbagai pulau, mulai dari pulau Sumatera hingga pulau Irian jaya Banyak tumbuhan telah dikenal sejak lama oleh nenek moyang dan digunakan secara tradisional, khususnya masyarakat yang berada di daerah pedalaman. Khasiat tanaman sebagai obat telah banyak dibuktikan melalui berbagai penelitian (Paputungan dkk, 2014).
Wilayah yang memiliki keanekaragaman hayati yang sangat tinggi salah satunya adalah di Papua. Keanekaragaman tumbuhan baik liar maupun budidaya merupakan salah satu sumber daya biologi, dimana manusia mendapatkan keperluan untuk kebutuhan sehari-harinya seperti pangan, obat, tradisi dan sebagainya (Rahayu dan Sulistriani, 2008). Salah satu tanaman yang banyak tumbuh di Papua khususnya di daerah pesisir dan menjadi salah satu bahan makanan favorit masyarakat Papua adalah pinang (Areca catechu L).
Tanaman pinang yang termasuk ke dalam family (Arecaceae) merupakan tumbuhan obat potensial asal Papua yang terbukti secara empiris berkhasiat untuk menyembuhkan berbagai macam penyakit. Secara etnofarmakologi tanaman pinang telah digunakan sebagai obat oleh masyarakat Papua sebagai obat bisul, sebagai obat sakit kulit, pendarahan dan masyarakat Papua juga menggunakan pinang sebagai teman makan sirih. Tanaman ini dikatakan sebagai tanaman serbaguna karena mulai dari daun, batang, serabut, dan biji dapat dimanfaatkan. Daun tanaman tersebut banyak mengandung minyak atsiri, biji buahnya banyak mengandung tannin dan alkaloid sebagai obat dan penyamak pada industri kulit. Serabut buahnya digunakan sebagai obat gangguan pencernaan, sembelit dan beri- beri (Sulastri, 2009). Batang pohonnya digunakan sebagai bahan bangunan, jembatan, pagar dan tempat duduk. Buah dan biji dimanfaatkan sebagai obat, bahan pewarna dan menyirih, sedangkan akar tumbuhan ini dapat bermanfaat sebagai obat (Lutony dkk,1992).
Biji buah pinang mengandung alkaloid, seperti Arekolin (C8H13NO2), arekolidine,
arekain, guvakolin, guvasine dan isoguvasine. Ekstrak etanolik biji buah pinang mengandung tanin terkondensasi, tannin terhidrolisis, flavan, dan senyawa fenolik, asam galat, getah, lignin, minyak menguap dan tidak menguap, serta garam (Wang and Lee, 1996). Ekstrak etanolik buah pinang tersebut memperlihatkan aktivitas antioksidan dengan IC50 sebesar 45,4 μg/ml (Lee and
Choi, 1999).
Biji dan kulit biji bagian dalam dapat juga digunakan bersama-sama dengan sirih untuk menguatkan gigi goyah. Air rendaman biji pinang muda digunakan untuk obat sakit mata oleh suku Dayak Kendayan di Kecamatan Air Besar, Kalimantan Barat (Kristina dan Syahid, 2007).
Pinang muda digunakan bersama dengan buah sirih untuk menguatkan gigi, hal ini sering dilakukan oleh masyarakat Papua. Selain sebagai obat penguat gigi, masyarakat pesisir pantai desa Assai dan Yoon-noni, yang didiami oleh suku Menyah, Arfak, Biak dan Serui (Papua) menggunakan biji pinang muda sebagai obat untuk mengecilkan rahim setelah melahirkan untuk kaum wanita dengan cara memasak buah pinang muda tersebut dan airnya diminum selama satu minggu (Kristina dan Syahid, 2007).
Tanaman pinang oleh masyarakat Papua khususnya di wilayah Jayapura secara empiris diyakini memiliki khasiat untuk membersihkan dan memperkuat gigi. biasanya masyarakat hanya menkonsumsi buah biji pinang sedangkan kulitnya biasanya digosokkan di gusi untuk membersihkan gigi atau tidak di gunakan sama sekali (dibuang) yang sebagian besar menjadi sampah atau limbah di sekitar.
Kulit buah pinang berwarna hijau jika masih muda, dan akan berubah menjadi orange kekuningan jika sudah tua. Kulit buah pinang diduga mengandung alkaloid, saponin, flavonoid, dan fenol karena kulit buah pinang masih satu bagian dengan biji buah pinang yang telah banyak diteliti kandungan dan manfaatnya. Sebagai contoh (Yulineri T, 2006) yang menggunakan akar dan ekstrak biji pinang sebagai antiseptik obat kumur, (Widayanti dkk, 2013) yang membuat sediaan tablet hisap ekstrak kental biji pinang.
Berdasarkan hal tersebut dilakukan penelitian ini yang bertujuan untuk mengetahui kandungan dari kulit buah pinang serta dapat membuat formulasi salep dari ekstrak kulit buah pinang.
1.2 Rumusan Masalah
Rumusan yang dapat diambil dari latar belakang di atas yakni:
1 Apakah ekstrak etanol kulit buah pinang dapat dibuat sediaan salep? 2 Bagaimanakah stabilitas sediaan salep ekstrak etanol kulit buah pinang?
1.3 Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1 Untuk membuat sediaan salep dari ekstrak etanol kulit buah pinang
2 Untuk mengetahui stabilitas sediaan salep ekstrak etanol kulit buah pinang.
1.4. Manfaat Penelitian
Melalui penelitian ini diharapkan dapat memberikan manfaat kepada masyarakat tentang pemanfaatan ekstrak kulit buah pinang dalam bentuk sediaan salep.
BAB II
TINJAUAN PUSTAKA
2.1 Tumbuhan Pinang 2.1.1 Klasifikasi
Tanaman pinang diklasifikasikan sebagai berikut: Divisi : Spermatophyte (Tumbuhan berbiji) Sub divisi : Angiospermae (Berbiji terbuka) Kelas : Monocotyledonae (Berkeping satu) Bangsa : Arecales
Suku : Arecaceae/palmae (Pinang-pinangan) Marga : Areca
Jenis : Areca catechu L. (Syamsuhidayat dan Hutapea,1991).
2.1.2 Morfologi
Pinang (Areca catechu L.) merupakan tanaman famili Arecaceae yang dapat mencapai tinggi 15-20 m dengan batang tegak lurus bergaris tengah 15 cm. Buahnya berkecambah setelah 1,5 bulan dan 4 bulan kemudian mempunyai jambul daun-daun kecil yang belum terbuka. Pembentukan batang baru terjadi setelah 2 tahun dan berbuah pada umur 5-8 tahun tergantung keadaan tanah (Dirjen POM, 1989).
Bagian-bagian dari tanaman pinang antara lain: (a). Akar: berakar serabut, putih kotor. (b). Batang: tegak lurus dengan tinggi 10-30 meter, bergaris tengah 15 cm, tidak bercabang dengan bekas daun yang lepas. (c). Daun: majemuk menyirip tumbuh berkumpul di ujung batang membentuk roset batang dan panjang helaian daun 1-1,8 m. Pelepah daun berbentuk tabung, panjang sekitar 80 cm, dan tangkai daun pendek. Helai anak daun mempunyai panjang 85 cm, lebar 5 cm, dengan ujung sobek dan bergigi. (d).
Bunga: tongkol bunga dengan seludang panjang yang mudah rontok, keluar dari bawah roset daun, panjang sekitar 75 cm, dengan tangkai pendek bercabang rangkap. Ada satu bunga betina pada pangkal, di atasnya banyak bunga jantan tersusun dalam dua baris yang tertancap dalam alur. Bunga jantan panjang 4 mm, berwarna putih kuning, dan benang sari 6. Bunga betina panjang sekitar 1,5 cm, hijau, bakal buah beruang satu. Buah bentuk buni, bulat telur sunsang memanjang, panjang 3,5-7 cm, dinding buah bersabut, warna merah jingga jika masak. (f). Biji: biji satu, bentuknya seperti kerucut pendek dengan ujung membulat, pangkal agak datar dengan suatu lekukan dangkal, panjang 15-30 mm, permukaan luar berwarna kecoklatan sampe coklat kemerahan, agak berlekuk-lekuk menyerupai jala dengan warna yang lebih muda. Pada bidang irisan biji tampak perisperm berwarna coklat tua dengan lipatan tidak beraturan. Pinang memiliki nama daerah seperti pineng, pineung (Aceh), pinang (Gayo), batang mayang (Karo), pining (Toba), batang pinang (Minangkabau), dan jambe (Sunda, Jawa) (Dirjen POM, 1989).
Tanaman ini berbunga pada awal dan akhir musim hujan dan memiliki masa hidup 25-30 tahun. Biji buah berwarna kecoklatan sampai coklat kemerahan, agak berlekuk-lekuk dengan warna yang lebih muda. Pada bidang irisan biji tampak perisperm berwarna coklat tua dengan lipatan tidak beraturan menembus endosperm yang berwarna agak keputihan (Dirjen POM, 1989).
Gambar 2.1. Gambar Buah Pinang (Areca catechu L.)
2.1.3 Kandungan
Biji pinang mengandung alkaloida (seperti: arekolin (C8H13NO2), arekolidine,
arekain, guvakolin, guvasine dan isoguvasine), saponin, dan flavonoid (Syamsuhidayat dan Hutapea, 1991). Ekstrak etanolik biji buah pinang juga mengandung tanin terkondensasi, tannin terhidrolisis, flavan, dan senyawa fenolik, asam galat, getah, lignin, minyak menguap dan tidak menguap, serta garam (Wang and Lee, 1996)
2.2 Simplisia
Simplisia adalah bahan alamiah yang dipergunakan sebagai obat yang belum mengalami pengolahan apapun juga dan kecuali dinyatakan lain, berupa bahan yang telah dikeringkan. Simplisia dibedakan menjadi simplisia nabati, simplisia hewani dan simplisia pelikan (mineral). Simplisia nabati adalah simplisia yang berupa tumbuhan utuh, bagian tumbuhan atau eksudat tumbuhan. Eksudat tumbuhan ialah isi sel yang secara spontan keluar dari selnya, atau senyawa nabati lainnya yang dengan cara tertentu dikeluarkan dari selnya, atau senyawa nabati lainnya dengan cara tertentu dipisahkan dari tumbuhannya dan belum berupa senyawa kimia murni. Simplisia hewani adalah simplisia berupa hewan utuh, bagian hewan atau zat yang dihasilkan hewan yang masih belum berupa zat kimia murni. Simplisia mineral adalah simplisia berasal dari bumi, baik telah diolah atau belum, tidak berupa zat kimia murni. Benda organik asing disingkat benda asing adalah satu atau keseluruhan dari apa yang disebutkan di bawah ini:
1 Fragmen bagian atau bagian tanaman asal simplisia selain bagian tanaman yang disebutkan dalam paparan Makroskopik atau bagian sedemikian yang nilai batasnya disebutkan monografi.
2 Hewan atau hewan asing berikut fragmennya, zat yang dikeluarkan hewan, kotoran hewan, batu, tanah atau zat pengkotor lainnya (DepKes RI,1979).
2.3 Ekstrak
Ekstrak adalah sediaan kering, kental atau cair dibuat dengan menyari simplisia nabati atau hewani menurut cara yang cocok, di luar pengaruh cahaya matahari langsung (DepKes RI,1979).
Ekstrak adalah sediaan kental yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai,
kemudian semua atau hampir semua pelarut diuapkan dan massa atau serbuk yang tersisa diperlakukan sedemikian rupa hingga memenuhi baku yang telah ditetapkan.
Sebagian besar ekstrak dibuat dengan mengekstraksi bahan baku obat secara perkolasi. Seluruh perkolat biasanya dipekatkan secara destilasi dengan pengurangan tekanan, agar bahan sesedikit mungkin terkena panas (DepKes RI,1995)
2.3.1 Metode Ekstraksi
Beberapa metode ekstraksi dengan menggunakan pelarut yaitu (BPOM, 2000):
2.3.1.1. Cara dingin
1. Maserasi
Maserasi adalah proses penyarian simplisia menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur kamar. Maserasi yang dilakukan pengadukan secara terus-menerus disebut maserasi kinetik, sedangkan maserasi yang dilakukan dengan pengulangan penambahan pelarut setelah dilakukan penyaringan terhadap maserat pertama dan seterusnya disebut remaserasi.
2. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai terjadi penyarian sempurna yang umumnya dilakukan pada temperatur kamar. Proses perkolasi terdiri dari tahap pengembangan bahan, tahap perendaman antara, tahap perkolasi sebenarnya (penetesan/penampungan ekstrak) terus-menerus sampai diperoleh ekstrak (perkolat).
2.3.1.2. Cara panas
1. Refluks
Refluks adalah ekstraksi pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarut terbatas yang relatif konstan dengan adanya pendingin balik. Umumnya dilakukan pengulangan proses pada residu pertama sampai 3-5 kali sehingga dapat termasuk proses ekstraksi sempurna.
2. Digesti
Digesti adalah maserasi dengan pengadukan terus-menerus pada temperatur lebih tinggi dari temperatur ruangan, secara umum dilakukan pada temperatur 40-50oC.
3. Sokletasi
Sokletasi adalah ekstraksi menggunakan pelarut yang selalu baru, umumnya dilakukan menggunakan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah pelarut relatif konstan dengan adanya pendingin balik.
4. Infundasi
Infundasi adalah ekstraksi dengan pelarut air pada temperatur 90o C selama waktu
15 menit. 5. Dekoktasi
Dekoktasi adalah ekstraksi dengan pelarut air pada temperatur sampai titik didih air selama 30 menit atau lebih (BPOM,2000).
2.4 Tinjauan Sediaan Salep 2.4.1 Salep
Salep (unguents) adalah preparat setengah padat untuk pemakaian luar. Salep dapat mengandung obat atau tidak mengandung obat (Ansel ,2005). Salep adalah sediaan setengah padat yang mudah dioleskan dan digunakan sebagai obat luar. Bahan obat harus larut atau terdispersi homogen ke dalam dasar salep yang cocok (DepKes RI,1979).
2.4.2 Persyaratan salep
Pemerian salep tidak boleh berbau tengik. Kadar salep kecuali dinyatakan lain dan untuk salep yang mengandung obat keras atau narkotik, kadar bahan obat adalah 10% (DepKes RI,1979).
Dasar salep kecuali dinyatakan lain, sebagai bahan dasar salep (basis salep) digunakan vaselin putih (vaselin album). Tergantung dari sifat bahan obat dan tujuan pemakaian salep, dapat dipilih beberapa bahan dasar salep sebagai berikut :
1 Dasar salep Senyawa hidrokarbon : vaselin putih, vaselin kuning (vaselin flavum), malam putih (cera album), malam kuning (cera flavum), atau campurannya.
2 Dasar salep Serap : lemak bulu domba (adeps lanae), campuran 3 bagian kolesterol, 3 bagian stearil-alkohol, 8 bagian mala putih dan 86 bagian vaselin putih, campuran 30 bagian malam kuning dan 70 bagian minyak wijen.
3 Dasar salep yang dapat dicuci dengan air atau dasar salep, emulsi, misalnya emulsi minyak dalam air (M/A).
4 Dasar salep yang dapat larut dalam air, misalnya PEG atau campurannya.
Homogenitas salep jika dioleskan pada sekeping kaca atau bahan transparan lain yang cocok, harus menunjukkan susunan yang homogen. Penandaan pada etiket harus tertera “obat luar” (DepKes RI,1979).
2.4.3 Penggolongan salep
1. Menurut konsistensinya salep dapat dibagi :
a Unguenta : salep yang mempunyai konsistensi seperti mentega, tidak mencair pada suhu biasa, tetapi mudah dioleskan tanpa memakai tenaga.
b Cream (krim) : salep yang banyak mengandung air, mudah diserap kulit, suatu tipe yang dapat dicuci dengan air.
c Pasta : salep yang mengandung lebih dari 50% zat padat (serbuk), suatu salep tebal, karena merupakan penutup atau pelindung bagian kulit yang diolesi.
d Cerata : salep berlemak yang mengandung persentase lilin (wax) yang tinggi sehingga konsistensinya lebih keras (ceratum labiale)
e Gelones/spumae/jelly : salep yang lebih halus, umumnya cair dan sedikit mengandung atau tanpa mukosa, sebagai pelicin atau basisnya terdiri atas campuran sederhana dari minyak dan lemak dengan titik lebur rendah. Contoh: starch jellies (10% amilum dengan air mendidih).
2. Menurut farmakologi / teraupetik dan penetrasinya, salep dapat dibagi
a Salep epidermis (epidermic ointment ; salep penutup) guna melindungi kulit dan menghasilkan efek lokal, tidak diabsorpsi, kadang-kadang ditambahkan antiseptik, astringensia untuk meredakan rangsangan atau anestesi lokal. Dasar salep yang baik adalah dasar salep senyawa hidrokarbon.
b Salep endodermis : salep bahan obatnya menembus kedalam kulit, tetapi tidak melalui kulit, terabsorpsi sebagaian, digunakan untuk melunakkan kulit atau selaput lendir. Dasar salep yang terbaik adalah minyak lemak.
c Salep diadermis : salep yang bahan obatnya menembus kedalam tubuh melalui kulit dan mencapai efek yang diinginkan, misalnya salep yang mengandung senyawa merkuri iodida.
3. Menurut dasar salepnya, salep dapat dibagi :
a Salep hidrofobik yaitu salep yang tidak suka air atau salep dengan dasar salep berlemak (greasy bases) tidak dapat dicuci dengan air, misalnya : campuran lemak-lemak minyak lemak, malam.
b Salep hidrofilik yaitu salep yang suka air atau kuat menarik air, biasanya dasar salep tipe M/A (Syamsuni, 2006).
2.4.4 Monografi Bahan 2.4.4.1 Polietilen glikol 400
Polietilen glikol 400 adalah polimer dari etilen oksida dan air, dinyatakan dengan rumus H(O-CH2-CH2)nOH. Pemerian cairan kenta jernih, tidak berwarna atau praktis
tidak berwarna,bau khas lemak dan adak higroskopis. Kelarutan larut dalam air, dalam etanol, dalam aseton dalam glikol lain dan dalam hidrokarbon aromatik, praktis tidak larut dalam eter dan dalam hidrokarbon alifatik (Depkes RI,1995).
2.4.4.2 Polietilen glikol 4000
Polietilen glikol 4000 adalah polietilenglikol, H(O-CH2-CH2)nOH. Harga n
antara 68 dan 84. Pemerian serbuk licin putih atau potongan putih kuning gading, praktis tidak berbau dan berasa. Kelarutan mudah larut dalam air, dalam etanol, dan dalam kloroform, praktis tidak larut dalam eter (DepKes RI,1979).
2.5. Uji Stabilitas
Pengujian stabilitas sangat penting dalam sediaan obat, kosmetik dan olahan makanan, stabilitas didefinisikan sebagai kemampuan suatu produk untuk bertahan kualitasnya sesuai spesifikasi kualitas yang ditetapkan sepanjang periode waktu penyimpanan. Uji stabilitas dilakukan untuk menjamin identitas, kekuatan, kualitas dan kemurnian produk. Berdasarkan
hasil uji stabilitas dapat diketahui pengaruh faktor lingkungan seperti suhu dan kelembaban terhadap parameter-parameter stabilitas seperti kadar zat aktif, pH, berat jenis, bau, warna dan lainnya sehingga dapat ditetapkan tanggal kadaluarsanya. Untuk sediaan obat dan kosmetika stabilitas lebih ditujukan pada kemampuan produk tersebut untuk mempertahankan sifat dan karateristik agar sama dengan yang dimiliki pada saat dibuat hingga batasan yang ditetapkan sepanjang periode penyimpanan (Rismana dkk, 2013).
2.5.1. Uji Organoleptik
Organoleptik, merupakan pengujian sediaan dengan menggunakan panca indra untuk mendiskripsikan bentuk atau konsistensi (misalnya padat, serbuk, kental, cair), warna (misalnya kuning, coklat) dan bau (misalnya aromatik, tidak berbau) (Juwita dkk, 2013).
2.5.2. Uji Homogenitas
Pengujian homogenitas dilakukan untuk melihat dan mengetahui tercampurnya bahan-bahan sediaan salep (Juwita dkk,2013).
3 Uji pH
Pengujian pH sediaan salep bertujuan untuk mengetahui keamanan sediaan salep saat digunakan agar tidak mengiritasi kulit. pH yang diinginkan untuk pH kulit adalah 4,5-6,5 (Anief, 2007).
4 Uji Daya Sebar
Tujuan melakukan uji ini untuk mengetahui daya sebar yang baik, menyebabkan kontak antara obat dengan kulit menjadi luas, sehingga absorpsi obat ke kulit berlangsung cepat. Caranya yakni salep dengan volume tertentu dibawa ke pusat antara dua lempeng gelas, lempeng sebelah atas dalam interval waktu tertentu dibebani oleh peletakan dari anak timbang. Permukaan penyebaran yang dihasilkan dengan menaiknya pembebanan menggambarkan suatu karakteristik untuk daya hambur (Voigt, 1984).
5 Uji Daya Lekat
Daya lekat merupakan kemampuan salep untuk melapisi permukaan kulit secara kedap dan tidak menyumbat pori – pori serta tidak menyumbat fungsi fisiologis kulit. Uji daya lekat ditunjukkan dengan waktu yang diperlukan untuk melepaskan dua gelas objek
dengan luas permukaan tertentu yang telah diolesi salep dan telah diberi beban tertentu. Uji daya melekat menggambarkan kemampuan salep untuk melekat pada kulit, semakin lama waktu salep untuk melekat pada kulit berarti semakin baik ikatan antara salep dengan kulit sehingga ikatan antara obat dengan sel-sel penyerap pada kulit akan semakin baik, sehingga memperbaiki adsorbs pada kulit (Aisha, 2010).
6 Uji Keamanan (Patch Test)
Uji Keamanan dilakukan untuk mengetahui apakah timbul kemerahan dan gatal-gatal pada kulit, untuk mengetahuinya dilakukan dengan cara pengolesan pada kulit manusia, uji ini dilakukan dengan cara sediaan salep diambil 1 gram, kemudian dioleskan pada kulit dan diamati gejala yang timbul seperti kemerahan dan gatal-gatal pada kulit (Lukman dkk, 2012).
7 Uji Stabilitas/Penyimpanan
Uji stabilitas dilakukan untuk mengetahui apakah terjadi perubahan pada sediaan salep selama penyimpanan tiap formulasi disimpan dan diukur parameter kestabilannya yaitu organoleptik, daya sebar, pH, dan daya lekat selama 21 hari (Setiawan, 2010).
BAB III
METODE PENELITIAN
3.1 Waktu PenelitianPenelitian ini dilakukan di Laboratorium Farmasi Jurusan Biologi Universitas Cenderawasih Jayapura. Waktu penelitian berlangsung dari bulan Februari 2015 sampai dengan bulan Agustus 2015.
3.2. Alat dan Bahan 3.2.1. Alat
Alat yang digunakan pada penelitian ini adalah satu set alat maserasi, satu set alat destilasi neraca analitik,batang pengaduk hot plate, oven, mortar dan stemper, wadah untuk sediaan salep,gelas beker, cawan porselen, ayakan, pH universal.
3.2.2. Bahan
Bahan yang digunakan dalam penelitian ini adalah Etanol 96%, simplisia kulit buah pinang, PEG 400, PEG 4000, ammonia, kloroform, pereaksi dragendrof (PD), pereaksi mayer (PM), amil alcohol, asam klorida, natrium hidroksida, besi (III) klorida, gelatin, pereaksi steasny (PS), serbuk magnesium, pereaksi Liebermann-Burchard (PL-B), asam stearate, cetil alcohol, kertas saring, aquades.
3.3. Metode
Metode penelitian yang akan digunakan dalam penelitian ini menggunakan metode eksperimen dan jenis uji pada penelitian ini meliputi pembuatan simplisia kulit buah pinang, pembuatan ekstrak etanol kulit buah pinang, pembuatan formulasi serta uji stabilitas sediaan (meliputi Uji pH, uji homogenitas, uji organoleptis, uji daya sebar, uji daya lekat, uji penyimpanan serta uji keamanan sediaan salep)
3.4. Prosedur Kerja
3.4.1. Pengumpulan Sampel
Bahan yang digunakan pada penelitian diperoleh dari Kabupaten Jayapura, Provinsi Papua.
3.4.2. Pembuatan Simplisia
Kulit buah pinang dicuci dan dibersihkan kotoran-kotorannya kemudian dipotong-potong menjadi bagian lebih kecil, potongan kulit buah pinang diangin-anginkan kemudian dikeringkan menggunakan oven pada suhu 40-60oC, kulit
buah pinang yang sudah kering dibelender hingga menjadi simplisa halus kulit buah pinang.
3.4.3. Ekstraksi
Ekstraksi dilakukan menggunakan metode maserasi dengan menggunakan pelarut etanol 96% selama 3x24 jam.
3.4.4. Skrining Fitokimia
Penapisan fitokimia dilakukan terhadap simplisia, ekstrak dan fraksi aktif meliputi pemeriksaan terhadap golongan alkaloid, flavonoid, saponin, kuinon, tanin dan triterpenoid/steroid (Farnsworth, 1966).
3.4.4.1. Pemeriksaan Alkaloid
Sebanyak 2 gram serbuk ditambahkan dengan 5 mL ammonia 25% digerus dalam mortir, kemudian ditambahkan 20 mL kloroform, digerus kuat dan saring. Ke dalam filtrat ditambahkan asam klorida (1:10 v/v), kemudian dibagi 2, masing-masing ditambahkan Pereaksi Dragendrof dan Pereaksi Mayer. Reaksi positif alkaloid pada penambahan Pereaksi Dragendrof terbentuk endapan merah bata dan pada Pereaksi Mayer terbentuk endapan putih.
3.4.4.2. Pemeriksaan Flavonoid
Sebanyak 1 gram serbuk simplisia dalam 10 mL air panas dididihkan selama 5 menit, kemudian disaring. Filtrat yang diperoleh
digunakan juga untuk penapisan senyawa golongan saponin, kuinon dan tanin, yang disebut dengan larutan C. Ke dalam 5 mL larutan C ditambahkan serbuk magnesium dan 2 mL asam klorida-etanol (1:1), kemudian dikocok dengan 10 mL amil alkohol. Reaksi positif ditunjukkan dengan terbentuknya warna jingga, kuning atau merah yang tertarik pada lapisan amil alkohol.
3.4.4.3. Pemeriksaan Saponin
Sebanyak 10 mL larutan C dalam tabung reaksi dikocok selama 10 detik secara vertikal. Terbentuknya busa yang mantap selama tidak kurang dari 10 menit, setinggi 1 cm yang tidak hilang dengan penambahan asam klorida, menunjukkan adanya saponin.
3.4.4.4. Pemeriksaan Kuinon
Ke dalam larutan C sebanyak 5 mL ditambahkan beberapa tetes NaOH 1 N. Jika terbentuk warna merah menunjukkan adanya kuinon.
3.4.4.5. Pemeriksaan Tanin
Sebanyak 5 mL larutan C direaksikan dengan larutan besi (III) klorida 1%. Jika terbentuk warna biru kehitaman menunjukkan adanya tanin dan polifenol. Kemudian 5 mL larutan C ditambahkan larutan gelatin, jika terbentuk endapan berwarna putih menunjukkan adanya tanin. Selanjutnya 5 mL larutan C ditambahkan Pereaksi Steasny (formaldehid-asam klorida pekat = 1:2), jika terbentuk endapan merah muda menunjukkan adanya tanin katekat. Endapan disaring lalu filtrat dijenuhkan dengan natrium asetat dan ditambahkan besi (III) klorida. Jika terbentuk warna biru-hitam menunjukkan adanya tanin galat.
3.4.5. Pembuatan Formulasi Sediaan Salep Ekstrak Kulit Buah Pinang
Sediaan salep yang akan dibuat dalam penelitian ini memiliki konsentrasi ekstrak Kulit buah pinang yang berbeda-beda, yaitu 0,2% ; 0,4%; dan 0,6% sebanyak 40 gram
Bahan Formula 1(%) Formula 2 (%) Formula 3 (%)
Ekstrak Kulit buah pinang 0,2 0,4 0,6 PEG 400 59,88 59,76 59,64 PEG 4000 39,92 39,84 39,76 Keterangan :
Formula I : Salep dengan ekstrak etanol kulit buah pinang dengan konsentrasi 0,2 % Formula II : Salep dengan ekstrak etanol kulit buah pinang dengan konsentrasi 0,4% Formula III : Salep dengan ekstrak etanol kulit buah pinang dengan konsentrasi 0,6% (Windriyati dkk, 2008)
3.4.5.1. Pembuatan Salep
Pembuatan salep ekstrak kulit buah pinang dengan konsentrasi 0,2%, 0,4% dan 0,6% di lakukan dengan cara:
1 Mensterilkan peralatan yang akan digunakan.
2 Basis salep ditimbang dalam cawan porselen dengan menggunakan neraca analitik.
3 Setelah itu basis salep dituang dalam mortar yang telah disterilkan kemudian dipanaskan .
4 Setelah dipanaskan kemudian diaduk sampai homogen,
5 Setelah basis salep agak dingin lalu ekstrak kulit buah pinang dituang kedalam basis kemudian diaduk lagi sampai benar-benar homogen dan dingin.
6 Salep yang sudah jadi kemudian ditempatkan pada pot salep yang disterilkan
3.5 Analisis Stabilitas 3.5.1. Uji Organoleptik
Pengujian Organoleptik dilakukan dengan mengamati sediaan dari bentuk, bau dan warna sediaan.
3.5.2. Uji pH
Sebanyak 0,5 g sediaan salep ekstrak kulit buah pinang diencerkan dengan 5 mL aquadest, kemudian dengan menggunakan pH universal maka didapat nilai pH.
3.5.3. Uji Homogenitas
Uji Homogenitas sediaan dilakukan dengan cara mengamati hasil pengolesan salep pada plat kaca. Salep yang homogen ditandai dengan tidak terdapatnya gumpalan pada hasil pengolesan, struktur yang rata dan memiliki warna yang seragam dari titik awal pengolesan sampai titik akhir pengolesan. Salep yang diuji diambil dari tiga tempat yaitu bagian atas, tengah dan bawah dari wadah salep. Salep ekstrak kulit buah pinang diambil secukupnya pada bagian atas, tengah dan bawah kemudian dioleskan pada gelas objek atau kepingan kaca untuk diuji homogenitas sediaan salep. Sediaan salep yang homogen ialah sediaan salep dimana dasar salep, bahan aktif dan bahan tambahan lainnya tercampur merata dengan baik.
3.5.4. Uji Daya Sebar
Sebanyak 0,5 g sediaan salep diletakkan di atas kaca bulat yang berdiameter 15 cm, kaca lainnya diletakkan diatasnya dan dibiarkan selama 1 menit. Diameter sebar diukur kemudian ditambahkan beban 50, 100 g, dan 150 gram didiamkan selama 1 menit lalu diukur diameter konstannya.
3.5.5. Uji Daya Lekat
Sediaan salep dengan berat 0,25 gram diletakkan pada gelas obyek dan ditekan dengan beban 1 kg selama 5 menit. Setelah itu gelas obyek dipasang pada alat tes yang diberi beban 80 gram dan kemudian dicatat waktu pelepasan salep dari gelas obyek.
3.5.6. Uji Stabilitas Sediaan Salep
Formula yang telah dibuat kemudian dituang ke dalam wadah sebanyak 10 ml, di simpan selama 21 hari kemudian diamati dan dievaluasi kembali.
3.5.7. Pengujian Keamanan Sediaan Salep
Pengujian keamanan sediaan salep yang dibuat dilakukan terhadap Sembilan orang sukarelawan dengan uji tempel terbuka (Patch Test), yakni Sejumlah sediaan uji dioleskan pada punggung tangan kanan sukarelawan dan dibiarkan terbuka selama lima menit. Punggung tangan kiri diolesi sediaan basis salep tanpa ekstrak sebagai pembanding. Selanjutnya perubahan warna yang terjadi pada punggung tangan kanan masing-masng sukarelawan diamati. Jika tidak terjadi reaksi (tidak merah dan tidak
bengkak) diberi tanda (-), jika terjadi reaksi (kulit memerah) diberi tanda (+), selanjutnya jika terjadi pembengkakan diberi tanda (++)
BAB IV
HASIL DAN PEMBAHASAN
4.1 Pembuatan Simplisia Kulit Buah Pinang
Penelitian ini menggunakan bahan tanaman yaitu kulit buah pinang (Areca catechu L.). Dalam penelitian ini bagian kulit buah pinang dipotong-potong kecil-kecil untuk memudahkan proses pengeringan dan pembuatan simplisia halus. Kulit buah pinang yang digunakan dalam penelitian ini adalah dalam bentuk simplisia kering karena kadar air yang lebih sedikit memudahkan pelarut masuk ke dalam sel dan menarik zat aktif yang terkandung secara sempurna. Proses pengeringan dilakukan dengan cara diangin-anginkan terlebih dahulu, kemudian dengan oven pengering pada suhu 40-600C bertujuan untuk mendapatkan pengeringan
yang merata dan suhu yang tidak terlalu tinggi karena penggunaan suhu yang terlalu tinggi dan tidak stabil dapat menurunkan mutu karena merusak komponen senyawa yang terdapat didalamnya. Pengeringan juga bertujuan untuk menghentikan proses enzimatik dan juga mencegah timbulnya mikroba yang dapat merusak kandungan kimia.
Hasil pengeringan kulit buah pinang setelah diangin-anginkan dan dioven didapatkan berat simplisia kering sebesar 447 g dari berat basah yaitu sebanyak 512 gram. Bahan yang sudah kering kemudian dihaluskan dengan menggunakan blender. Pembuatan simplisia halus bertujuan untuk memperluas permukaan partikel yang berinteraksi dengan pelarut sehingga proses penyarian dapat berlangsung efektif. Untuk mempermudah proses penyarian ekstrak, simplisia dibuat menjadi bentuk halus. Setelah dihaluskan dengan cara diblender simplisia yang didapatkan tidak berbentuk serbuk halus tetapi kulit buah pinang berbentuk serabut. Pembuatan simplisia halus ini agar dapat mempermudah pada saat proses ekstraksi. Selanjutnya simplisia serbuk disimpan dalam wadah tertutup rapat.
4.2 Pemeriksaan Organoleptik
Pemeriksaan organoleptik Hasil Pemeriksaan Organoleptik
Bentuk Padatan
Warna Krem
Rasa Khas
Bau Khas
Hasil pemeriksaan organoleptik didasarkan pada proses penginderaan. Penginderaan diartikan sebagai suatu proses fisio-psikologis, yaitu kesadaran atau pengenalan alat indra akan sifat-sifat benda karena adanya rangsangan yang diterima alat indra yang berasal dari benda tersebut. Pengindraan dapat juga berarti reaksi mental (sensation) jika alat indra mendapat rangsangan (stimulus). Untuk hasil pemeriksaan organoleptik menunjukkan bahwa simplisia kulit buah pinang (Areca catechu L.) berwarna krem, bau khas, dan rasa khas.
4.3 Ekstraksi Kulit Buah Pinang
Ekstraksi dilakukan dengan cara maserasi selama 3 x 24 jam dengan memasukkan 150 gram simplisia serbuk kulit buah pinang (Areca catechu L.) ke dalam 5 liter etanol 96% pada bejana maserasi hingga terjadi perubahan warna kuning. Adanya perubahan warna dapat dianggap bahwa semua senyawa sampai yang berbobot molekul rendah telah terekstraksi.
Simplisia serbuk kulit buah pinang (Areca catechu L.) dimaserasi dengan pelarut etanol teknis 96% untuk mengekstraksi komponen senyawa kimia baik yang polar maupun nonpolar. Pelarut etanol 96% dipilih sebagai pelarut karena senyawa yang akan diekstrak adalah senyawa polar, selain itu etanol 96% dapat bertahan lama karena dapat mencegah pertumbuhan mikroba pada ekstrak yang digunakan dibandingkan dengan air serta mempermudah dalam proses penguapan. Selain itu, penggunaan pelarut etanol lebih baik jika dibandingkan dengan pelarut lain seperti metanol karena etanol lebih aman untuk digunakan dan tidak terlalu toksik seperti metanol.
Metode maserasi (ekstraksi cara dingin) dipilih karena senyawa yang akan diuji belum diketahui apakah merupakan senyawa termostabil (tahan terhadap panas) atau termolabil (tidak tahan terhadap panas). Hal ini dilakukan untuk menghindari senyawa yang bersifat termolabil menjadi rusak karena pemanasan. Hasil ekstraksi dari simplisia 150 g diperoleh ekstrak 5,8745 g. Seperti yang di perlihatkan di tabel 4.2.
Tabel 4.2. Rendemen Ekstrak Etanol Kulit Buah Pinang (Areca catechu L.) Sampel Berat simplisia (g) Volume pelarut (ml) Berat Ekstrak (g) Rendemen (%) Areca catechu L. 150 5000 5.8745 3,916
Hasil maserasi kemudian disaring dan dpekatkan dengan metode distilasi pada suhu 73ºC hingga pelarut terlihat sedikit dan ekstrak mulai mengental dengan tujuan untuk menghilangkan pelarut sehingga yang digunakan ialah ekstrak kental, kemudian dipindahkan dan diuapkan dengan hotplate hingga ekstrak yang didapatkan benar-benar telah kental.
Warna dari ekstrak kulit buah pinang (Areca catechu L.) adalah kekuningan. Ekstrak kental ditimbang beratnya yaitu 5,8745 g dengan rendemen 3,916 % (Tabel 1.). Nilai rendemen ini dihitung dengan tujuan untuk menilai seberapa efisien dan efektif metode ekstraksi yang digunakan, semakin besar nilai rendemen, berarti semakin banyak pula senyawa kimia yang tersari.
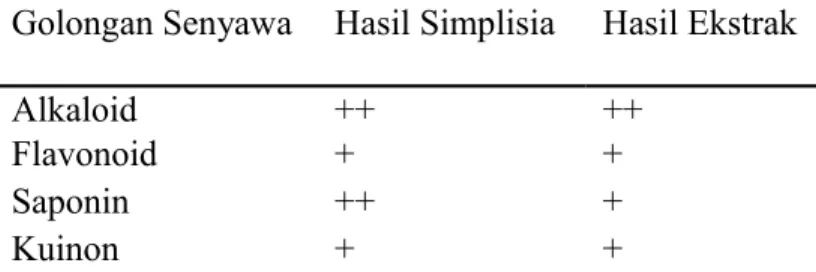
4.4 Skrining Fitokimia Simplisia
Skrining fitokimia simplisia kulit buah pinang (Areca catechu L.) dilakukan untuk mengetahui kandungan secara kualitatif senyawa metabolit sekunder yang terkandung dalam kulit buah pinang (Areca catechu L.). Data ini dijadikan acuan studi awal untuk mencari dan menemukan lead compound (senyawa penuntun/senyawa aktif) yang akan dipakai sebagai bahan obat. Hasil skrining fitokimia simplisia kulit buah pinang (Areca catechu L.) dapat dilihat pada tabel berikut:
Tabel 4.3. Hasil Skrining Fitokimia Simplisia dan Ekstrak Etanol Kulit Buah Pinang
Golongan Senyawa Hasil Simplisia Hasil Ekstrak Alkaloid ++ ++
Flavonoid + +
Saponin ++ +
Tanin ++ ++
Keterangan: (-) Tidak ada; (+) Sedikit; (++) Sedang; (+++) Banyak
Berdasarkan hasil uji fitokimia awal dapat diketahui bahwa kulit buah pinang (Areca
catechu L.) mengandung berbagai golongan metabolit sekunder. Pada pengujian fitokimia yang
menggunakan simplisia, kulit buah pinang (Areca catechu L.) mengandung senyawa golongan alkaloid, flavonoid, saponin, kuinon, dan tanin sedangkan untuk uji fitokimia pada ekstrak, kulit buah pinang (Areca catechu L.) mengandung alkaloid, flavonoid, saponin, kuinon, dan tanin.
Untuk alkaloid terdapat sama banyak pada simplisia dan ekstrak kulit buah pinang (Areca
catechu L.). Alkaloid merupakan suatu golongan senyawa yang memiliki fungsi dalam
pengobatan, salah satunya adalah sebagai antikanker karena bersifat sitotoksik, contohnya ialah vinkristin dan vinblastin. Alkaloid diduga memiliki kemampuan sebagai antibakteri dengan mekanisme mengganggu komponen penyusun peptidoglikan pada sel bakteri, sehingga lapisan dinding sel tidak terbentuk secara utuh dan menyebabkan kematian sel tersebut (Robinson, 1995).
Untuk golongan senyawa flavonoid cukup terlihat pada simplisia dan ekstrak kulit buah pinang (Areca catechu L.). Flavonoid bersifat anti inflamasi karena kemampuannya mencegah oksidasi dan menghambat zat yang bersifat yang bisa timbul pada luka. Flavonoid juga dapat menyebabkan rusaknya susunan dan perubahan mekanisme permeabilitas dari dinding sel bakteri (Harbone, 1996).
Golongan senyawa saponin yang terdapat pada simplisia (Areca catechu L.). Lebih banyak jika dibandingkan pada ekstrak (Areca catechu L.), hal ini terlihat dengan pembentukan busa yang lebih banyak di simplisia sedangkan pada ekstrak sangat sedikit bahkan hampir tidak terlihat. Hal ini disebabkan karena saponin merupakan senyawa ampifilik yang gugus gula (heksosa) pada saponin dapat larut dalam air tetapi tidak larut dalam alkohol absolut, kloroform, eter dan pelarut organik non polar lainnya sedangkan pelarut yang digunakan untuk mengekstrak (Areca catechu L.) adalah etanol. Hal inilah yang menyebabkan saponin terlihat cukup banyak pada simplisia dan sedikit terlihat pada ekstrak (Areca catechu L.). Saponin mempunyai kemampuan sebagai pembersih dan antiseptik yang berfungsi membunuh atau mencegah pertumbuhan dari mikroorganisme yang timbul pada luka sehingga luka tidak mengalami infeksi yang berat (Robinson, 1995).
Golongan senyawa kuinon cukup terlihat pada simplisia dan ekstrak etanol kulit buah pinang (Areca catechu L.). Kuinon dalam bidang farmasi digunakan sebagai antibiotik dan penghilang rasa sakit.
Untuk senyawa tanin terdapat di simplisia dan ekstrak terlihat sama banyak, hal ini disebabkan karena kandungan tanin yang tinggi pada kulit buah pinang (Areca catechu L.), dan juga tanin merupakan senyawa yang larut dalam etanol (Sulastri, 2009) sehingga saat pengujian pada ekstrak, komposisi tanin ikut tersari oleh pelarut etanol yang digunakan. Dalam bidang farmasi, tanin bermanfaat sebagai antikanker (Septina dan Yosefine, 2005).
5 Hasil Pengamatan Formulasi dan Pemeriksaan Stabilitas
Sediaan Salep
4.5.1. Hasil Uji Organoleptik Salep Kulit Buah pinang
Uji organoleptik bertujuan untuk melihat tampilan fisik sediaan. Pengujian organoleptik dilakukan dengan cara melakukan pengamatan terhadap bentuk, warna dan bau salep tersebut. Hasil pengamatan terhadap salep ekstrak kulit buah pinang dapat dilihat pada tabel berikut:
Tabel 4.4. Hasil Uji organoleptik sediaan Salep Ekstrak Kulit Buah Pinang Hari ke 1
Formulasi Warna Bau Bentuk
F I Krem Khas ekstrak Semipadat F II Krem Khas ekstrak Semipadat F III Krem Khas ekstrak Semipadat
Tabel 4.5. Hasil Uji Organoleptik Sediaan Salep Ekstrak Kulit Buah Pinang Hari ke 21
Formulasi Warna Bau Bentuk
F I Krem Khas ekstrak Semipadat F II Krem Khas ekstrak Semipadat F III Krem Khas ekstrak Semipadat Keterangan:
Formula I : Salep dengan konsentrasi 0,2 % Formula II : Salep dengan konsentrasi 0,4% Formula III : Salep dengan konsentrasi 0,6%
Pada pengujian organoleptik, diamati bentuk, warna, bau dari basis salep dan salep ekstrak kulit yang dibuat dengan variasi konsentrasi menunjukkan bentuk dari basis salep dan salep ekstrak kulit buah pinang memiliki bentuk fisik yang sama yakni setengah padat .
Hasil pemeriksaan warna pada setiap formula sediaan salep menunjukkan tidak adanya perubahan selama waktu penyimpanan pada suhu kamar, yakni sediaan salep dengan formula basis salep masing-masing menunjukkan warna krem.
Pengamatan terhadap bau dari salep ekstrak kulit buah pinang dengan variasi konsentrasi 0,2%, 0,4%, 0,6% memiliki bau khas yang sama yakni bau khas dari ekstrak kulit buah pinang. Hal ini dikarenakan ekstrak yang terkandung didalam masing-masing salep menutupi bau dari basis salep tersebut. Semakin tinggi ekstrak yang digunakan dalam sediaan salep, semakin mudah mengetahui bau khas ekstrak yang digunakan pada salep tersebut.
Pada pengamatan organoleptik sediaan salep kulit buah pinang pada hari ke 1 hingga ke 21 tidak terjadi perubahan bau, warna, dan bentuk. Hal ini menunjukkan bahwa sediaan salep dari kulit buah pinang stabil selama penyimpanan.
4.5.2. Uji pH Salep Ekstrak Kulit Buah Pinang
Pemeriksaan pH adalah salah satu bagian dari kriteria pemeriksaan fisika-kimia dalam memprediksi kestabilan sediaan salep. Dimana profil pH menentukan stabilitas bahan aktif dalam suasana asam atau basa.
Tabel 4.6. Hasil Uji pH Sediaan Salep Ekstrak Kulit Buah Pinang Formulas i Uji pH Hari ke 1 Hari ke 21 F I 5 5 F II 5 5 F III 5 5
Keterangan:
Formula I : Salep dengan konsentrasi 0,2 % Formula II : Salep dengan konsentrasi 0,4% Formula III : Salep dengan konsentrasi 0,6%
Pada pemeriksaan pH salep ekstrak kulit buah pinang pada tabel 4.7 menunjukkan bahwa ketiga formulasi tersebut pada hari ke 1 hingga ke 21 tidak mengalami perubahan yaitu memiliki nilai pH 5. pH tersebut memenuhi persyaratan pH sediaan topikal yaitu antara 4,5 – 6,5. Kulit yang normal memiliki pH antara 4,5 - 6,5 sehingga sediaan topikal harus memiliki pH yang sama dengan pH normal kulit tersebut. Kesesuaian pH kulit dengan pH sediaan topikal mempengaruhi penerimaan kulit terhadap sediaan. Sediaan topikal yang ideal adalah tidak mengiritasi kulit. Kemungkinan iritasi kulit akan sangat besar apabila sediaan terlalu asam atau terlalu basa.
4.5.3. Uji Homogenitas
Salep ekstrak kulit buah pinang diambil secukupnya pada bagian atas, tengah dan bawah kemudian dioleskan pada gelas objek atau kepingan kaca untuk diuji homogenitas sediaan salep. Sediaan salep yang tidak homogen akan diketahui dengan melihat terbentuknya gumpalan pada sediaan. Sediaan salep yang homogen ialah sediaan salep dimana dasar salep, bahan aktif dan bahan tambahan lainnya tercampur merata dengan baik. Hasil pengamatan dapa dilihat pada tabel berikut ini :
Tabel 4.7. Hasil Uji Homogenitas Salep Ekstrak Kulit Buah Pinang
Formulas i
Uji Homogenitas
Hari Ke 1 Hari ke 21 Atas Tengah Bawah Ata
s
Tengah Bawah
F I + + + + + +
F II + + + + + +
F III + + + + + +
Keterangan: (+) Homogen; (-) Tidak Homogen Formula I : Salep dengan konsentrasi 0,2 % Formula II : Salep dengan konsentrasi 0,4%
Formula III : Salep dengan konsentrasi 0,6%
Dari hasil uji homogenitas dilakukan untuk melihat bahan-bahan dari sediaan salep tercampur dan tersebar menjadi homogen. Dari tabel 4.8, menunjukkan bahwa ketiga formulasi salep ekstrak kulit buah pinang yang dihasilkan dalam penelitian ini merupakan salep yang homogen pada lempeng kaca hari ke 1 hingga hari ke 21. Pada bagian atas, tengah, dan bawah sediaan juga memiliki sifat fisik dan tekstur yang sama. Hasil uji homogenitas yang dilakukan pada setiap salep terbukti homogen apabila tidak terdapat partikel-partikel yang menggumpal serta memiliki warna yang merata pada seluruh bagian salep. Hal ini menunjukkan bahwa ekstrak kulit buah pinang yang terkandung dalam sediaan salep ekstrak kulit buah pinang tetap homogen.
4.5.4. Uji Daya Sebar Salep Ekstrak Kulit Buah Pinang
Pengujian daya sebar untuk tiap sediaan dilakukan untuk melihat kemampuan sediaan menyebar pada kulit, dimana suatu basis salep sebaiknya memiliki daya sebar yang baik untuk menjamin pemberian bahan obat yang memuaskan. Perbedaan daya sebar sangat berpengaruh pada kecepatan difusi zat aktif dalam melewati membran. Jika semakin besar daya sebar maka semakin luas zat aktif akan terdistribusi dengan baik. Hasil daya sebar dari salep ekstrak kulit buah pinang dapat dilihat pada tabel berikut
Tabel 4.8. Hasil Uji Daya Sebar Salep Ekstrak Kulit Buah Pinang Beban
(gram )
Uji daya Sebar (cm) Uji daya Sebar (cm)
Hari ke 1 Hari ke 21 F I F II F III F I F II F III 0 2,3 2,4 2,5 2,4 2,4 2,5 50 2,5 2,5 2,6 2,5 2,8 2,7 100 2,6 2,7 2,8 2,7 3 3 150 2,9 2,9 3 3 3,2 3,2 Keterangan:
Formula I : Salep dengan konsentrasi 0,2 % Formula II : Salep dengan konsentrasi 0,4% Formula III : Salep dengan konsentrasi 0,6%
Pengujian daya sebar bertujuan untuk mengetahui kelunakan massa salep sehingga dapat dilihat kemudahan pengolesan sediaan salep ke kulit. Sediaan salep yang bagus dapat menyebar dengan mudah di tempat aksi tanpa menggunakan tekanan (Hernani dkk, 2012).
Daya sebar yang baik menyebabkan kontak antara obat dengan kulit menjadi luas, sehingga absorpsi obat ke kulit berlangsung cepat. Viskositas suatu sediaan berpengaruh pada luas penyebarannya. Semakin rendah viskositas suatu sediaan maka penyebarannya akan semakin besar sehingga kontak antara obat dengan kulit semakin luas dan absorbsi obat ke kulit akan semakin cepat.
Hasil uji daya sebar menunjukkan bahwa terdapat perbedaan daya sebar terhadap ketiga formulasi dari hari pertama hingga hari ke 21, nilai daya sebar pada formula III lebih besar dibanding dengan F II dan F I, hal ini menunjukkan bahwa semakin besar konsentrasi ekstrak kulit buah pinang yang ditambahkan maka akan semakin besar pula nilai daya sebarnya seiring penambahan beban. Pada penyimpanan selama 21 hari terjadi peningkatan daya sebar terhadap ketiga formulasi, hal ini berhubungan dengan kekentalan sediaan salep yang menurun sehingga menyebabkan daya sebar meningkat.
4.5.5. Uji Daya Lekat Sediaan Salep Ekstrak Kulit buah pinang
Pengujian daya lekat bertujuan untuk mengetahui waktu yang dibutuhkan oleh salep untuk melekat di kulit, mampu menjamin waktu kontak yang efektif dengan kulit sehingga tujuan penggunaannya tercapai. Hasil daya lekat dari salep ekstrak kulit buah pinang dapat dilihat pada tabel berikut.
Tabel 4.9. Hasil Uji Daya Lekat Salep Ekstrak Kulit buah pinang hari ke 1 dan hari ke 21
Uji Daya Lekat ( Detik) Hari ke 1 dan Hari ke 21
Formulasi Rata-rata
Hari 1 Hari 21
F II 00:09:37 00:08:09 F III 00:06:04 00:05:54 Keterangan:
Formula I : Salep dengan konsentrasi 0,2 % Formula II : Salep dengan konsentrasi 0,4% Formula III : Salep dengan konsentrasi 0,6%
Hasil uji daya waktu lekat menunjukkan bahwa terdapat perbedaan daya lekat terhadap ketiga formulasi dari hari ke 1 hingga hari ke 21. Pada tabel 4.9 dapat dilihat bahwa kemampuan melekat dari sediaan salep cenderung menurun dengan semakin besarnya konsentrasi ekstrak.
4.5.6 Pengujian Keamanan Sediaan Salep Ekstrak Kulit Buah Pinang
Uji keamanan dilakukan untuk mengetahui keamanan dari sediaan salep ekstrak kulit buah pinang, uji ini dilakukan untuk melihat apakah adanya reaksi iritasi pada kulit yang dapat menyebabkan kulit kemerahan dan terasa perih. Hasil uji keamanan salep dapat dilihat pada tabel 4.10
Tabel 4.10. Hasil Uji Keamanan Salep Salep Ekstrak Kulit Buah Pinang Uji Iritasi (Keamanan Sediaan salep)
Formulasi Hasil Uji iritasi
F I
-F II
-F III
-Keterangan:
Formula I : Salep dengan konsentrasi 0,2 % Formula II : Salep dengan konsentrasi 0,4% Formula III : Salep dengan konsentrasi 0,6% (-) : Tidak terjadi iritasi
Dari data hasil pengamatan, dapat diketahui bahwa setiap formula sediaan salep yang mengandung variasi ekstrak kulit buah pinang tidak memberikan reaksi iritasi baik reaksi kemerahan maupun pembengkakan pada kulit sukarelawan. Sehingga dapat disimpulkan bahwa sediaan salep tersebut aman untuk digunakan.
BAB V
PENUTUP
5.1 Kesimpulan
Berdasarkan hasil dari penelitian yang telah dilakukan, maka dapat disimpulkan bahwa: 1 Ekstrak etanol kulit buah pinang (Areca catechu L.) dapat dibuat menjadi sediaan salep. 2 Sediaan salep kulit buah pinang (Areca catechu L.) memiliki stabilitas yang baik.
5.2 Saran
Berdasarkan penelitian yang telah dilakukan maka disarankan agar:
1 Perlu dilakukan pengembangan bentuk sediaan agar sediaan yang diperoleh memiliki kriteria yang lebih baik.
2 Disarankan untuk melanjutkan penelitian lebih lanjut tentang pengujian efektivitas antioksidan dan antibakteri dari sediaan salep ekstrak kulit buah pinang (Areca catechu L.).
DAFTAR PUSTAKA
Aisah Nur. 2010. Formulasi Salep Minyak Atsiri Rimpang Temu Glenyeh (Curcuma soloensis Vall) Dengan Basis Larut Air dan Basis Lemak: Sifat Fisik dan Aktivitas Antijamur
Candida Albicans Secara In Vitro. Skripsi. Fakultas farmasi Universitas Muhammadiyah
Surakarta, Surakarta 2010.
Anief, M. 2007. Farmasetika. Gadjah Mada University Press, Yogyakarta.
Ansel H. C. 2005. Pengantar Bentuk Sediaan Farmasi Edisi Keempat. Universitas Indonesia-Press: Jakarta.
BPOM, 2000, Parameter Standar Umum Ekstrak Tumbuhan Obat, Departemen Kesehatan RI
Direktorat Jenderal Pengawasan Obat Dan Makanan Direktorat Pengawasan Obat Tradisional,Halaman 10-12
Departemen Kesehatan Republik Indonesia, 1979, Farmakope Indonesia, Edisi III, Jakarta: Departemen Kesehatan RI, Halaman 9, 33, 502
Departemen Kesehatan Republik Indonesia, 1995, Farmakope Indonesia, Edisi IV, Jakarta: Departemen Kesehatan RI, Halaman 7, 511
Direktorat Jendral POM, 1989, Materia Medika Indonesia, Jilid IV, Cetakan Pertama. Jakarta: Direktorat Jenderal Pengawasan Obat Dan Makanan.
Farnsworth NR. 1966. Biological and Phytochemical Screening of Plant. J. pharm. Sci. 55(3) : 225-265.
Harbone, J. B. 1996. Metode Fitokimia : Penuntun Cara Modern Menganalisis Tumbuhan. diterjemahkan oleh Padmawinata K., dan Sudiro I. terbitan kedua. ITB : Bandung. Hernani M. Y, Mufrod, Sugiyono, 2012, Formulasi Salep Ekstrak Air Tokek (Gekko gecko L.)
Untuk Penyembuhan Luka, Majalah Farmaseutik, 8, 120
Juwita A. P., Paulina V.Y Yamlean, Hosea Jaya Edy 2013. Formulasi Krim Ekstrak Etanol Daun Lamun (Syringodium isoetifolium). jurnal Ilmiah Farmasi-UNSRAT, 2(2), 8-12.
Kristina, N.N. dan S.F.Syahid, 2007. Penggunaan Tanaman Kelapa, Pinang, dan Aren Sebagai Tanaman Obat. Warta Puslitbangbun.13
Lee, K.K., and Choi, J.D., 1999, The Effects of Areca Catechu L Extract on Anti-Inflammation and Anti-Melanogenesis, International Journal of Cosmetic Science21, 275–284.
Lukman Anita, Emma S, Roli O. 2012. Formulasi gel Minyak Kulit Kayu Manis( Cinnamomum burmanni BI) Sebagai Sediaan Antinyamuk. Jurnal Penelitian Farmasi Indonesia 1(1), 24-29
Lutony, Tony luqman,1992, Pinang sirih: komoditi Ekspor dan Serbaguna. Penerbit Kanisius, 43.
Paputungan F, Yamlean V. Y. P, Gayatri C., 2014, Uji Efektifitas Salep Ekstrak Etanol Daun Bakau Hitam (Rhizophora mucronata Lamk) Dan Pengujian Terhadap Proses Penyembuhan Luka Punggung Kelinci Yang Diinfeksi Bakteri Staphylococcus aureu,
PHARMACON Jurnal Ilmiah Farmasi – UNSRAT, 3(1), 15-26
Rahayu M, Sulistiarini D ,2008, Etnobotani ‘ Hoinu’ Abelmosch esculentus (L.) Moench. : Pemanfaatan, Prospek Dan Pengembangannya Di Sulawesi Tenggara. J. Tek. Ling
Vol.9,79-84
Rismana Eriawan, Susi Kusumaningrum, Idah Rosidah, Nizar dan Erna Yulianti. 2013.Pengujian Stabilitas Sediaan Antiacne Berbahan Baku Aktif Nanopartikel Kitosan/Ekstrak Manggis – Pegagan. Bul. Penelit. Kesehat, 41(4), 207 – 216.
Robinson, T. 1995. Kandungan Organik Tumbuhan Tinggi. Penerjemah: Padmawinata, K. Penerbit ITB. Bandung.
Septina A., dan Yosefine. 2005. Identifikasi Dan Uji Toksisitas Asam Tanat Dalam Ekstrak Daun Ketapang (Terminalia catappa L.). In: Seminar Tugas Akhir S1 Jurusan Kimia
FMIPA UNDIP , Jurusan Kimia UNDIP.
Setiawan Tri. 2010. Uji Stabilitas Fisik dan penentuan nilai spf krim tabir surya yang mengandung ekstrak oktil metoksinomat dan titanium dioksida. Skripsi, Fakultas MIPA Universitas Indonesia
Sulastri.I., 2009. Analisa kadar Tanin Ekstrak air dan Ekstrak Etanol pada Biji Pinang Sirih
(Areca Catechu L.). Jurnal Chemica,10(1), 59-63.
Syamsuhidayat SS, Hutapea JR. 1991. Inventaris Tanaman Obat Indonesia . Volume I. Departemen Kesehatan Republik Indonesia, Badan Penelitian dan Pengembangan Kesehatan. Jakarta. Halaman 64-65.
Voigt, 1984, Buku Pelajaran Teknologi Farmasi , diterjemahkan oleh Soendani, N.S., dan Widianto, M.B., Edisi V, 351, Gadjah Mada University Press, Jogjakarta.
Wang, C.K., and Lee, W.H., 1996, Separation, Characteristics, and Biological Activities of Phenolics in Areca Fruit, J. Agric. Food Chem., 44, 2014 -2019
Widayanti A, Rahmah Elfiyani, Ferra Tania, 2013. Optimasi Kombinasi Sukrosa-Manitol Sebagai Pengisi Dalam Sediaan Tablet Hisap Ekstrak Kental Biji Pinang (Areca catechu L.) SECARA GRANULASI BASAH. Media Farmasi, Vol 10 No.2 September
2013 : 9-17
Windriyati Yulias Ninik, Oktaria Esti, 2008, Pengaruh Perbedaan Konsentrasi Ekstrak Eter Rebusan Daun Sirih (Piper betl E Linn) Dalam Sediaan Salep Terhadap Sifat Fisik Dan Daya Antibakterinya, Jurnal Ilmu Farmasi dan Farmasi Klinik, 5(2), 1-5
Yulineri T, 2006, Selenium dari Ekstrak Biji dan Akar Pinang (Areca catechu L.) yang Difermentasi dengan Konsorsium Acetobacter–Saccharomyces sebagai Antiseptik Obat Kumur, BIODIVERSITAS, 7(1),18-20
LAMPIRAN
Lampiran 1. Proses pembuatan simplisia kulit buah pinang (Areca catechu L.)
a Simplisia Utuh Kulit buah pinang
b Pengeringan Simplisia
c Simplisia Halus Kulit buah pinang
Lampiran 3. Hasil uji skrining fitokimia pada simplisia kulit buah pinang (Areca catechu L.)
a Perendaman Ekstrak (Maserasi)
b. Penyaringan Ekstrak
c. Ekstrak Cair d. Penguapan Pelarut (Destilasi)
e. Ekstrak Kental
Lampiran 4. Hasil uji skrining fitokimia pada ekstrak etanol kulit buah pinang (Areca
catechu L.)
Tanin Alkaloid Saponin Kuinon Flavonoid
Lampiran 5. Pembuatan Formulasi Sediaan Salep dari Ekstrak Kulit buah pinang (Areca catechu L.) Kuino n Sapon in Alkaloid Flavonoi d
Alkaloid Saponin Kuinon Flavonoid
Lampiran 6. Hasil Evaluasi Stabilitas Formulasi Sediaan Salep Dari Ekstrak Kulit buah pinang (Areca catechu L.)
a Uji Homogenitas
b Uji pH
c Uji Daya sebar
Lampiran 7. Hasil Uji Daya Lekat Salep Ekstrak Kulit Buah Pinang Hari 1 dan Hari 21
Uji Daya Lekat ( Detik) Hari ke 1 Formulas i Replikasi Rata-rata 1 2 3 F I 03:09:09 03:12:00 03:06:00 3:09:03 F II 00:08:55 00:08:31 00:10:18 0:09:37 F III 00:06:53 00:07:17 00:04:01 0:06:04
Uji Daya Lekat ( Detik) Hari ke 21 Formulas i Replikasi Rata-rata 1 2 3 F I 03:03:58 03:12:00 03:05:02 3:07:00 F II 00:06:51 00:05:22 00:12:13 0:08:09 F III 00:04:38 00:06:50 00:06:13 0:05:54 Keterangan:
Formula I : Salep dengan ekstrak etanol kulit buah pinang konsentrasi 0,2 % Formula II : Salep dengan ekstrak etanol kulit buah pinang konsentrasi 0,4% Formula III : Salep dengan ekstrak etanol kulit buah pinang konsentrasi 0,6%
Uji Iritasi (Keamanan Sediaan salep) Formula si P 1 P 2 P 3 P 4 P 5 P 6 P 7 P 8 P 9 P 10 F I - - - -F II - - - -F III - - - -Keterangan:
Formula I : Salep dengan ekstrak etanol kulit buah pinang konsentrasi 0,2 % Formula II : Salep dengan ekstrak etanol kulit buah pinang konsentrasi 0,4% Formula III : Salep dengan ekstrak etanol kulit buah pinang konsentrasi 0,6% (-) : Tidak terjadi iritasi
(+) : Terjadi iritasi (P) : Panelis