SEMINAR NASIONAL PENELITIAN DAN PENDIDIKAN KIMIA
“Kontribusi Penelitian Kimia Terhadap Pengembangan Pendidikan Kimia”
KARAKTERISASI DAN KAJIAN KINERJA BENTONIT SEBAGAI ADSORBEN ZAT WARNA
Oleh:
Asep Supriatna, Hayat Solihin dan Cepi Kurniawan
ABSTRAK
Penelitian tentang kinerja bentonit sebagai adsorben zat warna telah dilakukan. Bentonit yang digunakan adalah bentonit alami, bentonit teraktivasi asam dan bentonit teraktivasi pemanasan yang berasal dari daerah Tasikmalaya. Pengukuran konsentrasi zat warna dilakukan dengan menggunakan spektrofotometer spektronik 20, sedangkan karakterisasi terhadap bentonit alami dan benton it teraktivasi dan bentonit -zat warna dilakukan dengan menggunakan SEM, Spektroskopi IR dan XRD. Pengukuran terhadap ion logam yang dipertukarkan dari bentonit dilakukan dengan menggunakan AAS. Pengukuran dengan XRD terhadap bentonit alami dan bentonit ter aktivasi menunjukkan adanya perubahan difraktogram bentonit teraktivasi pemanasan pada 2θ = 5,515 dan 9,000. Hasil SEM menunjukkan bahwa zat warna terserap pada permukaan bentonit. Sedangkan pengukuran dengan IR terhadap bentonit alami, bentonit teraktivas i dan bentonit-zat warna menunjukkan adanya perubahan pada pita serapan vibrasi –NH dan deformasi –NH3+. Hasil pengukuran dengan AAS menunjukkan adanya pelepasan ion Ca2+ dan Mg2+ dari bentonit yang mungkin dipertukarkan dengan zat warna.
Hasil pengukuran terhadap persen penurunan intensitas warna larutan menunjukkan bahwa urutan penurunan intensitas warna larutan menggunakan bentonit teraktivasi asam > bentonit alami > bentonit teraktivasi pemanasan. Penurunan intensitas warna larutan mencapai 98% dengan adanya penambahan PAC (Polyaluminiumchloride) terhadap bentonit alami dan proses pengendapan (settling) berlangsung lebih cepat. Kata Kunci : Bentonit, aktivasi bentonit, adsorben, zat warna, PAC, Spektronik 20+, SEM, XRD, IR, AAS.
I. PENDAHULUAN
Zat warna sintetis biasa digunakan pada industri pewarnaan tekstil (dyeing,
printing) dan pewarnaan dalam bidang fotografi bahkan sebagai zat aditif pada produk
minyak bumi. Hampir 10 – 15% zat warna yang digunakan untuk keperluan industri tersebut dibuang bersama limbah lainnya (Young, L. Jian, 1999; Danies et al., 1998) pada sistem perairan.
Kontaminasi tanah dan air tanah oleh senyawa organik terklorinasi atau senyawa organik sintesis lainnya telah menarik perhatian banyak kalangan sejak beberapa tahun kebelaka ng. Hal ini diakibatkan oleh buangan limbah yang mengandung zat warna dalam konsentrasi yang cukup tinggi dapat menyebabkan keracunan pada komunitas perairan (Lee et al., 1999). Untuk itu berbagai kebijakan untuk penanganan limbah sebelum dibuang perlu diperhatikan. Pada umumnya untuk menurunkan kadar zat warna ini banyak digunakan karbon aktif. Akan tetapi Walker dan Weatherly (1998), menyatakan bahwa karbon aktif merupakan material yang terlalu mahal karena
Melimpahnya mineral alami memberikan alternatif pemilihan material yang dapat digunakan sebagai adsorben. Dalam penelitian ini dikaji kinerja bentonit alam dan bentonit teraktivasi dalam menyerap zat pewarna. Diharapkan melalui penelitian ini diperoleh alternatif bahan pengadsorpsi dalam pengolahan limbah cair.
II. BENTONIT
Bentonit adalah tanah liat yang dihasilkan dari proses vulkanis. Bentonit merupakan kelompok mineral lempung (mineral clay) yang didominasi oleh mineral montmorillonit (85%). Bentonit memiliki kemampuan mengadsorpsi karena ukuran partikel koloidnya sangat kecil dan mempunyai kapasitas penukar ion yang tinggi. Pengembangan pada bentonit terjadi karena adanya penggantian isomorphus dalam lapisan oktahedral (Mg oleh Al) melengkapi suatu kelebihan muatan di ujung kisi. Dengan adanya pengembangan, jarak antara unit makin melebar dan kepingannya menjadi serpihan pada pengocokan dalam air serta mempunyai permukaan yang luas dalam zat pensuspensi.
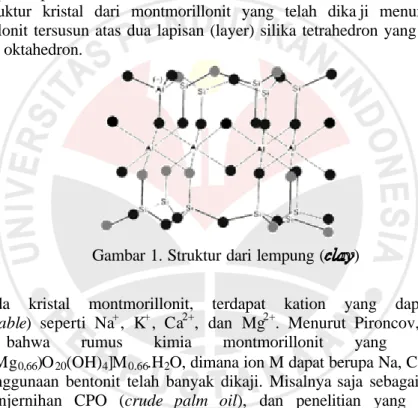
Struktur kristal dari montmorillonit yang telah dika ji menunjukkan bahwa montmorillonit tersusun atas dua lapisan (layer) silika tetrahedron yang disisipi lapisan aluminium oktahedron.
Gambar 1. Struktur dari lempung ( )
Pada kristal montmorillonit, terdapat kation yang dapat tergantikan (exchangeable) seperti Na+, K+, Ca2+, dan Mg2+. Menurut Pironcov, Soev “et al.” (1991), bahwa rumus kimia montmorillonit yang ideal adalah [Si8(Al3,34Mg0,66)O20(OH)4]M0.66.H2O, dimana ion M dapat berupa Na, Ca, dan Mg.
Penggunaan bentonit telah banyak dikaji. Misalnya saja sebagai adsorben pada proses penjernihan CPO (crude palm oil), dan penelitian yang dilakukan oleh Ramakrishna et al., (1997) menemukan bahwa bentonit dapat menyerap zat warna tekstil. Namun kajian Ramakrishna hanya terbatas pada pemanfaatan bentonit alami saja. Untuk itu dalam penelitian ini dikaji efektivitas bentonit alami dan bentonit yang diaktivasi dalam menyerap zat warna.
III. EKSPERIMEN 3.1 Alat dan Bahan
Kontak antara adsorben dengan larutan dilakukan dalam keadaan statis dengan menggunakan shaking machine. Pengukuran konsentrasi zat warna dilakukan dengan menggunakan spektrofotometer spectronic 20 pada panjang gelombang 615 nm.
Bentonit yang digunakan berukuran 200 mesh. Zat warna yang digunakan adalah pewarna biru yang merupakan zat warna dari kelompok disperse (blue disperse).
3.2 Cara Kerja
Preparasi Bentonit Teraktivasi. Penurunan kadar air dilakukan dengan cara
pemanasan pada suhu 1050C selama 1 jam. Untuk memperoleh bentonit teraktivasi asam dilakukan aktivasi dengan H2SO4 2N dengan cara direfluks. Sementara Bentonit
teraktivasi pemanasan diperoleh dengan pemanasan pada suhu 350 0C selama 3 jam.
Karakterisasi Bentonit. Dilakukan dengan menggunakan Scanning Electron
Microscope (SEM), difraktometer XRD powder diffraction (PW 3710) yang dilengkapi
dengan radiasi Kα Cu, serta menggunakan spektrofotometer FTIR.
Karakterisasi Zat Warna. Panjang gelombang maksimum ditentukan dengan
menggunakan spectronik 20+. Zat warna di karakterisasi menggunakan FTIR
(Shimadzu FTIR 8400). Sementara kadar logam dalam larutan uji diukur menggunakan
spektrofotometer AAS.
Studi Kesetimbangan Adsorpsi. Untuk mengkaji waktu kesetimbangan
adsorpsi zat warna dilakukan variasi waktu kontak antara adsorben dengan larutan uji: selama 0 - 6 jam dengan kecepatan shaking machine 150 menit-1. Jumlah zat warna yang terserap diperoleh dengan mengukur perbedaan serapan awal dan serapan akhir supernatan pada panjang gelombang 615 nm.
Pengaruh jumlah adsorben terhadap adsorpsi zat warna. Dilakukan dengan
menempatkan bentonit di dalam 50 mL larutan Uji dengan variasi massa 1 – 20 gram. Percobaan ini dilakukan selama 1 jam dalam shaking machine. Untuk mengetahui kinerja bentonit dengan PAC (Polyaluminiumchloride) dilakukan juga pengujian sinergisitas dengan menambahkan bentonit pada larutan uji yang telah dikoagulasi dengan 1000 ppm (part per million) PAC.
IV. HASIL DAN DISKUSI
Analisis Scanning Electron Microscope (SEM). Bentonit merupakan senyawa
amorf, hal ini seperti teramati pada bentonit yang belum mengalami perlakuan terhadap larutan uji terlihat adanya lapisan-lapisan khas lempung. Setelah dikontakkan dengan larutan uji, tampak adanya perubahan pada permukaan bentonit, sebagian permukaan tertutupi oleh material lain. Dari gambar 2 teramati adanya senyawa lain yang menempel pada permukaan bentonit, senyawa yang diasumsikan sebagai adsorbat dari zat warna tampak sebagai benda bulat dan kasar, serta teramati pula absorbat lain yang berbentuk kristal. Dari analisis permukaan bentonit menggunakan SEM ini diperoleh juga informasi bahwa bentonit yang telah mengalami perlakuan dengan larutan uji zat warna tekstil memiliki konduktivitas lebih besar dibandingkan bentonit awal.
Gambar 2. Foto SEM Bentonit
Sesudah perlakuan dengan larutan zat warna
Pengaruh Perlakuan Aktivasi terhadap Karakteristik Bentonit. Pada
gambar 3 berikut, tampak bahwa bentonit yang diaktivasi dengan H2SO4 2N dan
pemanasan (350 0C) mengalami perubahan intensitas. Seperti teramati pada daerah-daerah khas untuk puncak silika (900 – 1200; 794,5 dan 525 cm-1) terjadi perubahan akibat adanya pertukaran ion. Manea dan Badulescu, mengungkapkan bahwa dalam larutan dengan pH rendah pertukaran ion pada lepung – terutama lapisan oktahedral– teramati sebagai pita serapan dengan bilangan gelombang 610 dan 770 cm-1.
Gambar 3. Spektra infra merah (IR) bentonit setelah aktivasi
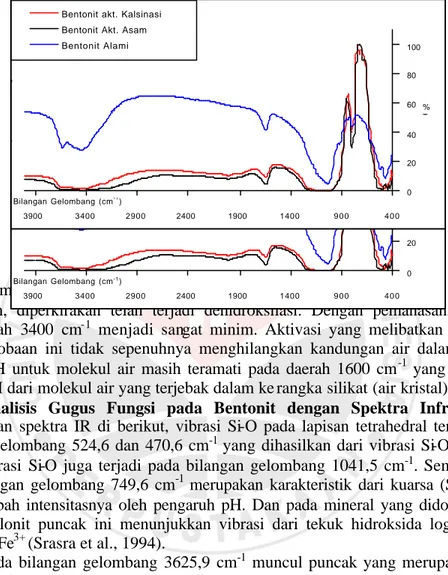
Gambar di atas menunjukkan adanya pelebaran pita uluran dari OH akibat pemanasan, diperkirakan telah terjadi dehidroksilasi. Dengan pemanasan, intensitas pada daerah 3400 cm-1 menjadi sangat minim. Aktivasi yang melibatkan pemanasan pada percobaan ini tidak sepenuhnya menghilangkan kandungan air dalam bentonit. Uluran OH untuk molekul air masih teramati pada daerah 1600 cm-1 yang merupakan vibrasi OH dari molekul air yang terjebak dalam ke rangka silikat (air kristal).
Analisis Gugus Fungsi pada Bentonit dengan Spektra Infrared (IR).
Berdasarkan spektra IR di berikut, vibrasi Si-O pada lapisan tetrahedral teramati pada bilangan gelombang 524,6 dan 470,6 cm-1 yang dihasilkan dari vibrasi O-Al dan Si-O-Si. Vibrasi Si-O juga terjadi pada bilangan gelombang 1041,5 cm-1. Sementara pita pada bilangan gelombang 749,6 cm-1 merupakan karakteristik dari kuarsa (SiO2), yang
akan berubah intensitasnya oleh pengaruh pH. Dan pada mineral yang didominasi oleh montmorillonit puncak ini menunjukkan vibrasi dari tekuk hidroksida logam seperti Mg2+ dan Fe3+ (Srasra et al., 1994).
Pada bilangan gelombang 3625,9 cm-1 muncul puncak yang merupakan uluran dari gugus OH yang terletak pada lapisan oktahedral, yait u gugus OH yang terikat pada Al (Srasra et al., 1994). Berikut adalah spektra IR dari bentonit yang telah dikontakkan dengan larutan uji zat warna tekstil yang bersifat basa:
0 20 40 60 80 100 4 0 0 9 0 0 1400 1900 2400 2900 3400 3900 Bilangan Gelombang (cm-1) % T
Bentonit akt. Kalsinasi Bentonit Akt. Asam Bentonit Alami 0 20 40 60 80 100 4 0 0 9 0 0 1400 1900 2400 2900 3400 3900 Bilangan Gelombang (cm-1) % T
Bentonit akt. Kalsinasi Bentonit Akt. Asam Bentonit Alami
Gambar 4. Spektra Infra merah (IR) bentonit
setelah perlakuan dengan larutan uji
Teramati bahwa ada pergeseran dan pelebaran pada pita ν(Si-O) dimana intensitasnya tidak setajam bentonit awal diperkirakan terdapat vibrasi Si-O-R (R=senyawa alifatik). Juga ditunjukkan dengan adanya gugus lain yang terdeteksi pada bilangan gelombang 3386 cm-1 yang merupakan pita vibrasi dari gugus amina, yang dipertegas dengan adanya pita uluran dari C-N yang diperkirakan berasal dari senyawa organik sintetis dalam larutan uji yang digunakan sebagai zat warna. Pita pada bilangan gelombang 1458,1 cm-1 juga menunjukkan uluran dari gugus NH. Deformasi senyawa -NH3+ juga ditunjukkan dengan adanya pita pada bilangan gelombang 1519,8 cm-1.
Sementara pada bilangan gelombang 749,6 dan 825,5 cm-1 terdapat perubahan intensitas pada bentonit setelah terjadi pertukaran ion dalam larutan yang sangat asam/basa.
Tabel. 1 Perubahan Kadar Logam dalam larutan Uji Akhir (ppm)
Logam Awal
(ppm) Bentonit Alami Bentonit Teraktivasi Asam
Bentonit Teraktivasi Pemanasan
Mg 1,3 227 25 1,4
Ca 22,3 557 46 18
Analisis X-Ray Diffraction (XRD). Berdasarkan diffraktogram XRD berikut,
mineral dasar yang terdapat dalam bentonit adalah Ca-Montmorillonit, cristobalite dan albite. Meskipun bentonit dikelompokkan pada mineral amorf, tetapi mineral dasarnya berbentuk kristalin. Intensitas Ca-montrorillonit pada 5,515 dan 21,995 (2θ) muncul dengan puncak yang sangat kuat, artinya bentonit dari Karangnunggal ini sangat didominasi oleh Ca-Montmorillonit meskipun demikian kuantitas masing-masing mineral kristalin ini belum diketahui dengan pasti.
0 2 0 4 0 6 0 8 0 100 400 900 1400 1900 2400 2900 3400 3900 Bilangan Gelombang (cm-1) %T Bentonit+Zat Warna Bentonit Alami Zat Warna
Gambar 5 . XRD bentonit Alami dan teraktivasi [bentonit alami (A), bentonit
teraktivasi asam (B) dan bentonit teraktivasi kalsinasi (C)]
Gambar di atas adalah hasil analisis XRD dari bentonit alami setelah perlakuan aktivasi dengan asam dan pemanasan. Dari gambar 5 diperoleh bahwa beberapa mineral dasar tidak berubah komposisinya, meskipun terjadi fluktuasi intensitas. Intensitas montmorillonit (2θ = 5,515) pada bentonit teraktivasi pemanasan (350 0C) menjadi sangat kecil, sebaliknya pada Bentonit teraktivasi asam (H2SO4 2N), terjadi peningkatan
intensitas puncak montmorillonit (2θ = 5,515).
Kajian Kinerja Adsorpsi. Dengan memperhatikan alur kurva massa bentonit
terhadap penurunan warna seperti terlihat pada gambar 6a, menunjukkan bahwa bentonit teraktivasi asam mampu menurunkan warna lebih baik dibandingkan bentonit alami dan bentonit teraktivasi pemanasan.
Gambar 6. Kurva variasi massa bentonit (a)
dan waktu kesetimbangan adsorpsi (b)
Demikian pula dengan waktu kesetimbangan adsorpsi bentonit teraktivasi asam jauh lebih cepat dibandingkan dengan bentonit lainnya (gambar 6b).
Ketika dilakukan pengujian lebih lanjut pada titik yang sama (massa bentonit = 5 gram), dengan waktu kontak dilakukan pada masing-masing waktu kesetimbanga nnya, bentonit teraktivasi asam mampu menurunkan intensitas warna sampai 95% sementara bentonit
B C A 2θ 0 20 40 60 80 100 120 0 1 2 3 4 5 6 7 Waktu (Jam)
% Penurunan Intensitas Warna
Akt. Asam Akt. Kalsinasi Alami Optimasi Dosis 0 20 40 60 80 100 120 0 5 10 15 20 massa Bentonit/50 mL
% penurunan intensitas warna
Alami Akt. Asam Akt. Kalsinasi
alami dan bentonit teraktivasi pemanasan masing-masing menurunkan intensitas warna sampai 88% dan 86%.
Kecepatan Pengendapan. Penurunan warna dalam larutan uji juga dilakukan
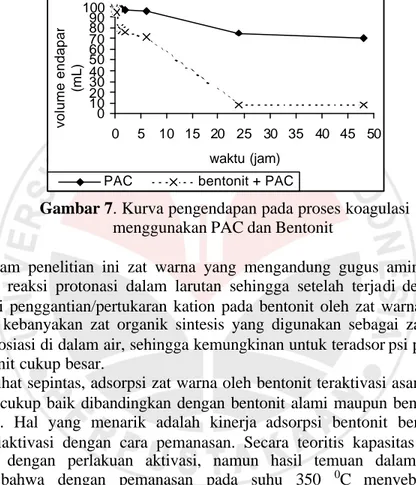
dengan proses koagulasi menggunakan PAC (polyaluminiumchloride), meskipun penurunan intensitas warna mencapai 90%, namun pengendapan (settling) agregat berlangsung sangat lambat. Dalam penelitian uji dikaji kinerja bentonit sebagai alat bantu koagulasi (coagulan aid ) dan menunjukkan hasil yang sangat baik pula penurunan warna meningkat menjadi 98% dan waktu pengendapan (settling) berlangsung lebih cepat seperti terlihat pada gambar 7. Berikut hasil percobaan penambahan bentonit terhadap kecepatan penurunan endapan menggunakan PAC:
Gambar 7. Kurva pengendapan pada proses koagulasi
menggunakan PAC dan Bentonit
Dalam penelitian ini zat warna yang mengandung gugus amina diperkirakan mengalami reaksi protonasi dalam larutan sehingga setelah terjadi deformasi –NH3+ baru terjadi penggantian/pertukaran kation pada bentonit oleh zat warna dalam larutan uji. Untuk kebanyakan zat organik sintesis yang digunakan sebagai zat warna tekstil akan terdisosiasi di dalam air, sehingga kemungkinan untuk teradsor psi pada permukaan aktif bentonit cukup besar.
Dilihat sepintas, adsorpsi zat warna oleh bentonit teraktivasi asam menunjukkan hasil yang cukup baik dibandingkan dengan bentonit alami maupun bentonit teraktivasi pemanasan. Hal yang menarik adalah kinerja adsorpsi bentonit berkurang setelah bentonit diaktivasi dengan cara pemanasan. Secara teoritis kapasitas adsorpsi akan meningkat dengan perlakuan aktivasi, namun hasil temuan dalam penelitian ini diperoleh bahwa dengan pemanasan pada suhu 350 0C menyebabkan struktur montmorillonit pada bentonit berubah. Diperkirakan dengan kondisi ini kapasitas serapan bentonit pun menjadi berkurang.
Selain itu, kadar logam Ca dalam larutan uji setelah dikontakkan dengan bentonit teraktivasi pemanasan mengalami penurunan. Kemungkinan karena
exchangeable ion yang terdapat pada pori-pori dalam tertutupi oleh lelehan kristal.
Sehingga logam-logam dalam larutan uji terserap pada permukaan bentonit.
KESIMPULAN
Kajian karakteristik dan pemanfaatan bentonit sebagai adsorben zat warna menunjukkan hasil yang sangat baik. Zat pewarna yang mengandung gugus -NH diperkirakan terserap pada permukaan bentonit, hal ini dibuktikan dengan adanya vibrasi NH pada bentonit (ν=1458,1 cm-1) serta pita deformasi -NH3+ (ν = 1519,8 cm-1).
Bentonit cukup efektif digunakan sebagai adsorben alternatif dalam penanganan 0 10 20 30 40 50 60 70 80 90 100 0 5 10 15 20 25 30 35 40 45 50 waktu (jam) volume endapan (mL)
88%. Perlakuan aktivasi bentonit dengan asam mineral (H2SO4) dapat meningkatkan
kemampuan adsorpsi warna sampai 95%, sementara bentonit yang mengalami perlakuan aktivasi pemanasan (3500C) menurun menjadi 86%. Perlakuan pemanasan ini menyebabkan perubahan pada mineral dasar montmorillonit yang mungkin paling berperan dalam proses adsorpsi.
Pada proses koagulasi dengan menggunakan PAC warna berkurang sampai 90% namun penurunan endapan berlangsung lambat. Penambahan bentonit menyebabkan agregasi molekul dengan bobot yang lebih tinggi akibatnya endapan dapat lebih cepat turun, selain itu penurunan warna menjadi 98% .
DAFTAR PUSTAKA
1. Benefield, Larry D., (1982). “Proces Chemistry For Water and Wastewater Treatment”. Rainbow-Bridge Book Co.
2. Diaz, et al., (2001), “Studies on the Acid Activation of Brazilian Smectite Clays”, Quim. Nova, 24, (3), 345 – 353.
3. Filipovic – Petrovic, et. Al., (2002), “The Effects of the Fine Grinding on the Phsycochemical Properties and Thermal Behavior of Bentonite Clay”, J. Serbian Chemistry Soc., 67, (11), 753 – 760.
4. Grim, (1962), "Applied Clay Mineralogy", McGraw -Hill Book Company. Inc. New York, 335 - 351.
5. Haffad, D., et al., (1998), “Characterization of Acid-Treated Bentonite. Reactivity, FTIR study and 27Al MAS NMR”, Catalysis Letters 54, 227 – 233.
6. Johnston, C. T., et al., (2001), “Polarized ATR-FTIR Study of Smectite in Aquaous Suspension”, American Shemical Society.
7. Little, L. H., (1966) "Infrared Spectra of Adsorbed Species", Academic Press. New York.
8. Manea, F., dan Roxana Badulescu, (tanpa tahun), “Ionic Exchange Equilibrium of the Bentonites in Aqueous Solutions at Various Values of pH”. [online] : www.sud-hemie.com/scmcms/web/binary.jsp? nodeId=5156&binaryId= 4714%lang=enpal (29 Mei 2004)
9. Michail, R. S., dan Erich Robens, (1983), “Microstructure and Thermal Analysis of Solid Surface”. John willey & sons : New York.
10. Silverstein, R., (1963), "Spectrometric Indentification of Organic Compounds", John Willey & Son, Inc. New York.
11. Vaudrias, E., et al., (2002), “Sorption – Desorption Isotherms of Dyes from Aqueous Solutions and Wastewaters with Different Sorbent Materials”, [online] : www.gnest.org/Journal/Vol4_No1/vourdias.pdf (05 Mei 2004) 12. Zulkarnain, Ir., (1998), “Pengkajian Optimasi Aktivasi Bentonit Asal
Karangnunggal Kabupaten Tasikmalaya Jawa Barat dengan Asam Sulfat”, Bidang Litbang Teknologi Pengolahan Mineral PPTM Bandung.


![Gambar 5 . XRD bentonit Alami dan teraktivasi [bentonit alami (A), bentonit teraktivasi asam (B) dan bentonit teraktivasi kalsinasi (C)]](https://thumb-ap.123doks.com/thumbv2/123dok/4305793.3156684/6.918.211.758.114.933/bentonit-teraktivasi-bentonit-bentonit-teraktivasi-bentonit-teraktivasi-kalsinasi.webp)