EFFECT OF VARIATION AND CONCENTRATION OF AUXIN TOWARD STEM CUTTINGS OF NONI (Morinda citrifolia L.)
Sisilia Purnama Sari
Department of Biology, Faculty of Mathematics and Natural Sciences, Sebelas Maret University
Surakarta
ABSTRACT
Noni (Morinda citrifolia L.) is a plant from family Rubiaceae which until now has been widely used as an antibacterial and analgesic. Noni plant has begun intensively cultivated by farmers in Indonesia vegetatively, that is by cuttings. However, propagation by cuttings is not done optimally. The purpose of this study was to determine the effect of variations in the type and concentration of auxin on stem cuttings noni.This research used a Completely Randomized Design (CRD) with nine of treatments. This study used three types of auxin which were IAA, NAA, and IBA, each with three levels of concentration; 25 ppm, 50 ppm and 75 ppm. There were three replications for each treatment, so there were 30 experimental units. The variables measured were the number of roots, root length, root fresh weight, root dry weight, while emerging shoots, shoot number, leaf number, and leaf length. The data were analyzed with statistical test Analysis of Variance (ANOVA) and Duncan Multiple Range Test (DMRT) was conducted with significance level of 5%. The results showed that variations in the type and concentration of auxin were not induce the formation and growth of roots on stem cuttings of noni. Application of variations and concentration of auxin give no significant effect on the time to appear shoots, but significantly affected the growth and development of shoots on the number of shoots and number of leaves parameters. The application of IAA has significant effect due to the leaf length of stem cuttings of noni.
EFEK PEMBERIAN VARIASI JENIS DAN KONSENTRASI AUKSIN TERHADAP STEK BATANG MENGKUDU (Morinda citrifolia L.)
Sisilia Purnama Sari
Program Studi Biologi, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Sebelas Maret
Surakarta
ABSTRAK
Tanaman mengkudu (Morinda citrifolia L.) merupakan tanaman dari familia Rubiaceae yang sampai sekarang ini telah banyak digunakan sebagai zat antibakteri dan analgetik. Tanaman mengkudu sudah mulai dibudidayakan secara intensif oleh petani di Indonesia secara vegetatif, yaitu dengan cara stek. Perbanyakan dengan cara stek belum dilakukan secara maksimal. Tujuan penelitian ini adalah untuk mengetahui pengaruh pemberian variasi jenis dan konsentrasi auksin terhadap stek batang mengkudu. Penelitian ini menggunakan variasi jenis auksin yaitu IAA, NAA, dan IBA, masing-masing jenis auksin dengan tiga konsentrasi 25 ppm, 50 ppm, dan 75 ppm. Penelitian menggunakan Rancangan Acak Lengkap (RAL) dengan 9 macam perlakuan dan tanpa perlakuan (0 ppm) sebagai kontrol. Terdapat 3 ulangan untuk setiap perlakuan, sehingga terdapat 30 unit percobaan. Variabel penelitian yang diamati adalah waktu muncul akar, jumlah akar, panjang akar, waktu muncul tunas, jumlah tunas, jumlah daun, dan panjang daun. Data yang diperoleh dianalisis dengan
Analysis of Variance (ANOVA). Bila menunjukkan beda nyata diantara
kelompok perlakuan, dilanjutkan dengan uji Duncan Multiple Range Test
(DMRT) dengan tingkat signifikansi 5%. Hasil penelitian menunjukkan pemberian variasi jenis dan konsentrasi auksin tidak mendorong adanya pembentukan dan pertumbuhan akar. Pemberian variasi jenis dan konsentrasi auksin memberikan pengaruh yang tidak nyata terhadap waktu muncul tunas, tetapi berpengaruh nyata terhadap pertumbuhan dan perkembangan tunas yaitu untuk parameter jumlah tunas dan jumlah daun. Pemberian auksin jenis IAA berpengaruh nyata terhadap panjang daun stek batang mengkudu.
PENDAHULUAN
Mengkudu (Morinda citrifolia L.) merupakan tanaman dari familia
Rubiaceae yang sampai sekarang ini telah banyak digunakan sebagai zat
antibakteri dan analgesik (Rahmayani, 2013). Kemampuan tanaman mengkudu
sebagai antibakteri dilihat pada kemampuannya dalam menekan pertumbuhan
Blood Disease Bacterium (BDB) pada buah pisang (Baroroh, 2014). Kegunaan
lain tanaman mengkudu sebagai antibakteri selain terhadap buah pisang, tanaman
ini juga mampu melawan bakteri menular seperti Pseudomonas aeruginosa,
Proteus morgaii, Staphylococcus aureus, Bacillus subtilis, Escherichia coli,
Salmonella sp. dan Shigella sp. (Mohtar et al., 1998; Jayasinghe et al., 2002).
Zat-zat antibakteri yang terkandung dalam buah mengkudu berperan dalam
pengobatan infeksi kulit, pilek, demam, dan masalah kesehatan lain yang
disebabkan oleh bakteri (Atkinson, 1956). Younos et al. (1990) menguji efek
analgesik dan obat penenang dari ekstrak buah mengkudu terhadap tikus. Ekstrak
buah mengkudu memiliki khasiat sebagai analgesik 70% lebih baik daripada
morfin.
Tanaman mengkudu sudah mulai dibudidayakan secara intensif oleh
petani di Indonesia sejak awal perkembangan industri obat tradisional di
Indonesia pada tahun 1999, terutama disekitar Jawa Tengah, pembudidayaan ini
kemudian menyebar ke beberapa daerah di Indonesia seperti Jawa Barat, Jawa
Timur, dan Banten. Pembudidayaan dilakukan untuk memenuhi kebutuhan buah
mengkudu yang semakin meningkat, selain itu dengan membudidayakan
mengkudu dianggap dapat memberikan hasil yang menguntungkan (Djauhariya et
al., 2006). Menurut Djauhariya et al. (2006), teknologi pembudidayaan yang
selama ini dilakukan oleh para petani umumnya masih sangat sederhana dan
belum memenuhi standar Good Agricultural Practice (GAP). Cara perbanyakan
mengkudu yang umum dilakukan petani adalah dengan menggunakan biji dari
buah mengkudu. Cara ini tidak dapat mempertahankan sifat genetis yang dimiliki
oleh induknya. Petani kemudian melakukan perbanyakan mengkudu secara
vegetatif untuk tetap mempertahankan sifat genetis mengkudu agar sama dengan
mampu meningkatkan pembentukan akar. Auksin merupakan hormon yang
berperan dalam pembentukan dan pertumbuhan akar. Indole-3-Acetic Acid (IAA),
α–Naphthalene Acetic Acid (NAA), Indole Butyric Acid (IBA) merupakan golongan auksin yang saat ini sudah banyak digunakan dalam pembentukan dan
perkembangan akar. IBA dipercaya memiliki kemampuan lebih dalam
pembentukan akar pada stek dibandingkan IAA maupun zat pengatur tumbuh
lainnya (Wudianto, 1993). Kemampuan IBA dalam pembentukan akar dibuktikan
oleh Djauhariya dan Rahardjo (2004) pada stek batang mengkudu. IBA dengan
konsentrasi 59 ppm mampu meningkatkan panjang akar pada stek batang
mengkudu. Penelitian ini bertujuan untuk mengetahui pengaruh pemberian variasi
jenis dan konsentrasi auksin terhadap stek batang mengkudu.
METODE PENELITIAN
A. Alat
Beker gelas, mistar, kertas label, gelas pengaduk, gelas ukur, pisau,
gunting, timbangan elektrik, alumunium foil, botol gelap.
B.Bahan
Stek batang tanaman mengkudu (Morinda citrifolia L.) yang diambil
di Ngoresan, Surakarta dengan diameter cabang 2-3 cm, larutan hidroponik
yang dicampur dengan aquades, Indole Butyric Acid (IBA), Indole-3-Acetic
Acid (IAA), α–Naphthalene Acetic Acid (NAA), etanol absolut, aquades.
C. Cara kerja
a. Persiapan stek batang mengkudu
Persiapan stek batang mengkudu diambil dari batang yang berwarna
coklat dengan menggunakan pisau yang tajam dan bersih. Batang diambil
dari indukan yang dipotong miring dengan panjang 20 cm dengan 2-3 mata
tunas aksiler dan diameter 2-3 cm dengan meninggalkan 2-3 helai daun.
b. Pembuatan media dasar
Pembuatan media dasar dilakukan dengan membuat larutan nutrisi
Pembuatan media air dibuat dengan perbandingan 90 % air, 5 % pekatan A,
dan 5 % pekatan B. Setiap 1 l media dibuat dengan mencampurkan 900 ml
air dengan 50 ml pekatan A dan 50 ml pekatan B.
c. Pembuatan stok ZPT
Pembuatan lautan stok IAA, IBA, NAA dengan masing-masing
taraf konsentrasi 25 ppm, 50 ppm, 75 ppm. Untuk membuat larutan zat
pengatur tumbuh dengan konsentrasi 75 ppm, yaitu dengan menimbang 75
mg IAA yang dilarutkan dalam etanol absolut tetes demi tetes sampai zat
pengatur tumbuh larut sempurna kemudian ditambahkan 1.000 ml aquades.
Pembuatan larutan dilakukan cara yang sama pada IBA dan NAA. Stok zat
pengatur tumbuh disimpan dalam elenmeyer 1.000 ml dan ditutup dengan
alumunium foil serta diberi label. Semua larutan stok yang sudah dibuat
disimpan dalam lemari pendingin (Trisna et al., 2013; Waziri et al., 2015).
Penghitungan volume larutan stok menggunakan rumus :
Vstok.Mstok = Vmedia.Media
(Hendaryono dan Wijayani, 1994)
Keterangan :
Vstok = volume larutan stok yang dicari
Mstok = konsentrasi larutan stok yang tersedia
Vmedia = volume larutan stok yang akan dibuat
Mmedia = konsentrasi larutan stok yang akan dibuat
d. Pembuatan media perlakuan
Media perlakuan adalah media dasar yang ditambahan dengan zat
pengatur tumbuh. Pembuatan media perlakuan dengan cara melarutkan
media dasar dengan penambahan zat pengatur tumbuh dari larutan stok
IAA, NAA, IBA sesuai dengan taraf konsentrasi sesuai rancangan
penelitian. Media perlakuan dimasukkan ke dalam botol gelap
masing-masing 150 ml kemudian ditutup dengan plastik (Muhamad, 2014).
e. Tahap penanaman stek batang
Batang mengkudu yang sudah dipotong direndam dalam media
pengatur tumbuh dalam botol gelap kemudian stek yang sudah ditanam
ditutup kembali dengan plastik untuk mengurangi penguapan. Selanjutnya
pemeliharaan dilakukan selama 23 hari. Selama pemeliharaan, stek batang
disimpan dalam green house dengan suhu ruangan 26-27 oC (Hasanah dan
Setiari, 2007; Trisna et al., 2013; Waziri et al., 2015).
f. Pengamatan
Pengamatan dilakukan pada stek batang mengkudu berumur 23 hari
setelah tanam (HST). Variabel yang diamati pada penelitian ini adalah
waktu muncul akar, jumlah akar adventif, panjang akar adventif, waktu
muncul tunas, jumlah tunas, jumlah daun, panjang daun.
D. Analisis Data
Data yang diperoleh dianalisis dengan uji statistik Analysis of Variance
(ANOVA). Apabila menunjukkan beda nyata diantara kelompok perlakuan,
kemudian dilanjutkan dengan uji Duncan Multiple Range Test (DMRT)
dengan tingkat signifikansi 5% (Gehlot et al., 2014).
HASIL DAN PEMBAHASAN
A. Pembentukan dan pertumbuhan akar
Hasil pengamatan selama 23 hari pada stek batang mengkudu
menunjukkan bahwa pemberian variasi jenis dan konsentrasi auksin terhadap stek
batang mengkudu tidak menunjukkan adanya pembentukan dan pertumbuhan
akar, akan tetapi berpengaruh pada pembentukan dan pertumbuhan pertunasan
saja. Hingga akhir pengamatan tidak ada satupun akar yang muncul pada stek
batang mengkudu. Stek yang direndam dalam larutan auksin mengalami
pembusukan dan akhirnya mati. Pembusukan pangkal batang pada stek batang
mengkudu terjadi sebelum stek membentuk akar akan tetapi terbentuk tunas.
Pembusukan pangkal batang diduga disebabkan karena faktor fisologis tanaman
yang digunakan. Faktor fisiologis ini berperan dalam keberhasilan stek. Faktor
fisiologis yang mempengaruhi penyetekan adalah umur bahan stek, jenis tanaman
yang digunakan, ada tidaknya tunas dan daun muda pada bahan stek, persediaan
bahan stek yang digunakan dalam penelitian ini masih tergolong sangat muda.
Umur bahan yang digunakan berhubungan dengan kadar karbohidrat dan nitosgen
pada tanaman. Karbohidrat merupakan salah satu hasil proses fotosintesis yang
berlangsung di daun dan dialirkan ke seluruh bagian tanaman. Cadangan makanan
tersebut akan digunakan pada saat tanaman mengalami kondisi tidak
menguntungkan atau untuk pembentukan sel atau organ baru. Stek batang
yang memiliki kandungan karbohidrat yang tinggi dan rendahnya kandungan
nitogen tidak mampu menghasilkan akar akan tetapi akan terbentuk tunas. Stek
dengan kandungan nitrogen tinggi akan menghasilkan akar yang banyak dan kuat.
Stek yang masih terlalu muda menandakan kandungan karbohidrat rendah dan
nitrogen yang tinggi, hal ini menyebabkan stek mengalami pembusukan
(Hartmann dan Kester, 1983)
Hal ini diduga karena konsentrasi zat pengatur tumbuh yang digunakan
tidak sesuai dengan konsentrasi optimal yang dapat menginduksi perakaran pada
stek batang mengkudu. Konsentrasi masing-masing auksin yang digunakan masih
bertaraf rendah yaitu 25 ppm, 50 ppm, dan 75 ppm. Ternyata pada konsentrasi
tersebut belum mampu menghasikan akar pada stek batang mengkudu.
Kebanyakan pada konsentrasi auksin yang tinggi mampu menghasilkan akar pada
stek batang. Sevik dan Guney (2013) menjelaskan IAA pada konsentrasi 1.000
ppm mampu menghasilkan persentase stek berakar pada stek batang lemon balm
(Melissa officinalis L.) lebih banyak. Akar merupakan pusat penyerapan nustrisi
yang dibutuhkan tanaman. Peranan akar adventif pada stek batang sangat
diperlukan untuk penyerapan nustrisi dari media tanam. Terbentuknya tunas pada
stek batang mengkudu diduga karena adanya hormon sitokinin yang terdapat pada
stek batang mengkudu. Perbandingan kombinasi sitokinin dan auksin pada stek
batang menyebabkan terjadinya pembelahan sel yang menstimulasi pembentukan
tunas pada stek. Sitokinin yang lebih tinggi bila dibandingkan konsentrasi auksin
akan mendorong pembentukan tunas, hal ini mengakibatkan tidak terjadinya
B. Pembentukan dan pertumbuhan tunas
Pemberian variasi jenis dan konsentrasi auksin tidak berpengaruh nyata
terhadap waktu muncul tunas, akan tetapi pemberian variasi jenis dan konsentrasi
auksin berpengaruh nyata terhadap pembentukan dan pertumbuhan tunas pada
variabel jumlah tunas, jumlah daun, dan panjang daun. Variasi jenis dan
konsentrasi auksin yang diberikan pada stek batang mengkudu dapat memberikan
respon yang berbeda terhadap tunas yang diamati..
1. Waktu muncul tunas
Kemunculan tunas pada stek batang mengkudu ditandai dengan pecahnya
nodus yang ditandai dengan munculnya tonjolan pada nodus batang. Rata-rata
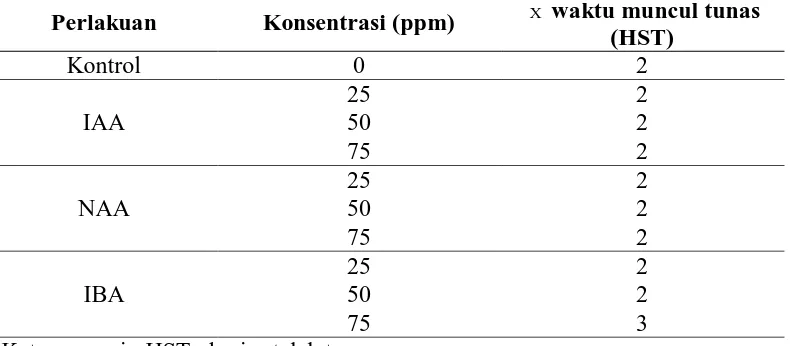
[image:8.595.113.508.373.546.2]waktu muncul tunas pada stek batang mengkudu disajikan pada Tabel 3:
Tabel 3. Rata-rata waktu kemunculan tunas pada stek batang mengkudu setelah 23 HST dengan pemberian variasi jenis dan konsentrasi auksin
Perlakuan Konsentrasi (ppm) X waktu muncul tunas (HST)
Kontrol 0 2
IAA
25 2
50 2
75 2
NAA
25 2
50 2
75 2
IBA
25 2
50 2
75 3
Keteranganri : HST : hari setelah tanam
X : rata-rata
Waktu muncul tunas pada penelitian menunjukkan sebagian besar pada
hari ke-2 pada setiap perlakuan kecuali pada perlakuan IBA dengan taraf
konsentrasi 75 ppm waktu munculnya tunas pada hari ke-3 setelah tanam.
Kemunculan tunas terjadi pada setiap perlakuan. Hal ini menunjukkan pemberian
variasi jenis dan konsentrasi auksin terhadap stek batang mengkudu tidak
berpengaruh besar dalam kemunculan tunas. Danu dan Tampubolon (1993)
menunjukkan bahwa pemberian IBA pada stek batang sungkai (Peronema
canescens Jack) tidak memberikan pengaruh nyata terhadap pertumbuhan tunas.
IBA dengan konsentrasi yang semakin tinggi pada stek damar (Agathis
loranthifolia Salisb.) justru mengakibatkan pertumbuhan dan perkembangan
tunas. Akan tetapi pernyataan ini tidak sesuai dengan hasil penelitian Apriliani et
al. (2015) terhadap stek pucuk bayur (Pterospermum javanicum Jungh.) dengan
pemberian IBA 100 ppm dan 200 ppm memberikan nilai rata-rata kemunculan
tunas lebih cepat dibandingkan pemberian IAA dan NAA pada taraf konsentrasi
yang sama. IBA dengan konsentrasi rendah tidak akan mempengaruhi
pertumbuhan tunas akan tetapi pemberian IBA dengan konsentrasi yang tinggi
akan mempengaruhi pertumbuhan dan perkembangan tunas. Leopold dan
Kriedemann (1975) menjelaskan bahwa IBA berperan dalam pembelahan sel,
sehingga mengakibatkan terjadinya perpanjangan sel pada organ-organ vegetatif
sehingga mampu membentuk tunas.
Tumbuhnya tunas lateral pada stek batang terjadi karena adanya
pematahan dominansi apikal akibat adanya pemangkasan pucuk. Pemangkasan
pucuk mengakibatkan suplai auksin yang berasal dari tunas apikal terhenti,
sehingga kadar auksin yang berada di bawah pemangkasan berkurang. Dengan
adanya pemangkasan pucuk, tanaman akan mempercepat pertumbuhan tunas
lateral. Kondisi ini dinamakan pematahan dominansi apikal. Dominansi apikal
adalah pertumbuhan ujung pucuk tumbuhan yang menyebabkan pertumbuhan
tunas lateral terhambat. Dominansi apikal pada stek batang mengkudu terjadi
karena adanya zat pengatur tumbuh yang berada pada tunas apikal. Menurut
Heddy (1989) auksin berperan dalam peristiwa dominansi apical yaitu dalam
penghambatan tunas lateral.
Kemunculan tunas pada setiap perlakuan diduga disebabkan karena
adanya hormon endogen yang terkandung pada tanaman itu sendiri. Tanaman
mampu menghasilkan zat pengatur tumbuh secara endogen dalam jumlah yang
sedikit. Zat pengatur tumbuh yang dihasilkan ini mampu mempengaruhi sel yang
mampu mengekspresikan suatu gen untuk memunculkan tunas. Astuti (2014)
menyatakan pada penelitiannya terhadap bambu kuning (Bambusa vulgaris)
secara in vitro bahwa tanaman secara alami menghasilkan hormon sitokinin yang
2. Jumlah muncul tunas
Pemberian variasi jenis dan konsentrasi auksin memberikan hasil yang
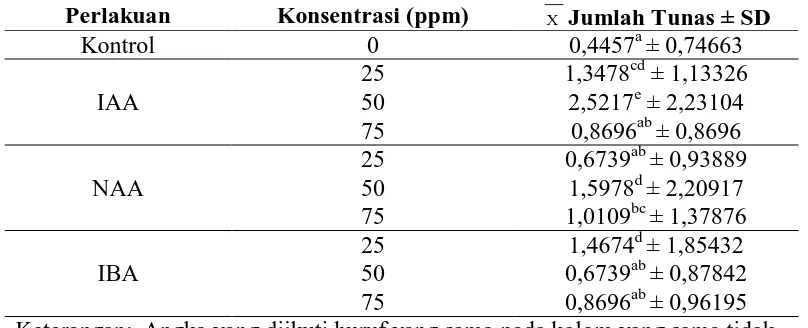
beragam terhadap jumlah tunas pada stek batang mengkudu (Tabel 4).
Tabel 4. Rata-rata jumlah tunas pada stek batang mengkudu setelah 23 HST dengan pemberian variasi jenis dan konsentrasi auksin
Perlakuan Konsentrasi (ppm) X Jumlah Tunas ± SD
Kontrol 0 0,4457a ± 0,74663
IAA
25 1,3478cd ± 1,13326
50 2,5217e ± 2,23104
75 0,8696ab ± 0,8696
NAA
25 0,6739ab ± 0,93889
50 1,5978d ± 2,20917
75 1,0109bc ± 1,37876
IBA
25 1,4674d ± 1,85432
50 0,6739ab ± 0,87842
75 0,8696ab ± 0,96195
Keterangan: Angka yang diikuti huruf yang sama pada kolom yang sama tidak menunjukkan beda nyata pada uji lanjut DMRT taraf 5%.
SD : Standar Deviasi
HST : hari setelah tanam
X : rata-rata
Pemberian variasi jenis dan konsentrasi auksin pada stek batang
mengkudu memberikan pengaruh nyata terhadap rata-rata jumlah tunas pada stek
batang mengkudu setelah diuji dengan ANOVA (Lampiran 2a). Pemberian variasi
jenis auksin yang diberikan pada stek batang mengkudu memberikan hasil optimal
yang berbeda pada setiap konsentrasinya. Pemberian auksin IAA memberikan
hasil optimal terhadap jumlah tunas pada stek batang mengkudu pada konsentrasi
50 ppm, NAA yang optimal terhadap jumlah tunas pada konsentrasi 50 ppm,
sedangkan IBA yang optimal terhadap pembentukan jumlah tunas pada taraf
konsentrasi 25 ppm. Pemberian variasi jenis dan konsentrasi auksin yang optimal
terhadap pembentukan dan pertumbuhan jumlah tunas terdapat pada IAA pada
konsentrasi 50 ppm karena memiliki nilai yang lebih tinggi yaitu sebesar 2,5217.
Jumlah munculnya tunas dipengaruhi oleh beberapa faktor yaitu zat
pengatur tumbuh yang digunakan, konsentrasi yang digunakan, interval waktu,
cara pemberian, serta faktor dari dalam tanaman itu sendiri (Adinugraha et al.,
[image:10.595.106.510.204.368.2]pertumbuhan tunas, sedangkan konsentrasi yang rendah tidak efektif dalam
memacu pertumuhan tunas. Dari hasil pengamatan IAA menunjukkan jumlah
tunas yang lebih baik bila dibandingkan dengan auksin yang lain. Adinugraha et
al. (2006) juga menjelaskan bahwa IAA mampu meningkatkan jumlah tunas,
panjang tunas dan berat kering tunas pada tanaman sukun yang dipangkas pada
pucuknya.
3. Jumlah daun
Pemberian variasi jenis dan konsentrasi auksin memberikan hasil yang
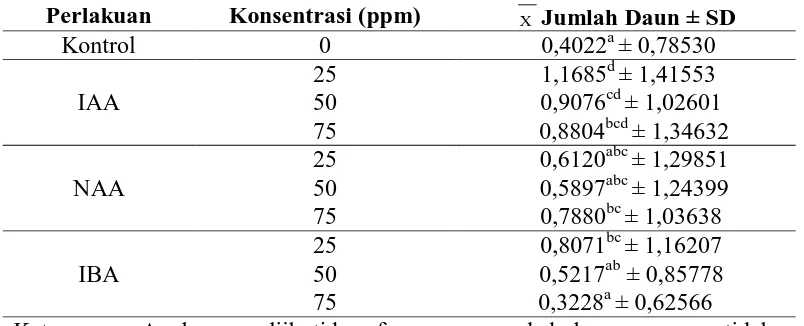
[image:11.595.107.509.328.491.2]beragam terhadap jumlah daun pada stek batang mengkudu (Tabel 5).
Tabel 5. Rata- rata jumlah daun pada stek batang mengkudu setelah 23 HST dengan pemberian variasi jenis dan konsentrasi auksin
Perlakuan Konsentrasi (ppm) X Jumlah Daun ± SD
Kontrol 0 0,4022a ± 0,78530
IAA
25 1,1685d ± 1,41553
50 0,9076cd ± 1,02601
75 0,8804bcd ± 1,34632
NAA
25 0,6120abc ± 1,29851
50 0,5897abc ± 1,24399
75 0,7880bc ± 1,03638
IBA
25 0,8071bc ± 1,16207
50 0,5217ab ± 0,85778
75 0,3228a ± 0,62566
Keterangan: Angka yang diikuti huruf yang sama pada kolom yang sama tidak menunjukkan beda nyata pada uji lanjut DMRT taraf 5%.
SD : Standar Deviasi
HST : hari setelah tanam
X : rata-rata
Hasil uji ANOVA menunjukkan pemberian variasi jenis dan konsentrasi
auksin memberikan pengaruh nyata terhadap kontrol (Lampiran 2b) Pemberian
auksin IAA memberikan hasil optimal terhadap jumlah daun pada stek batang
mengkudu pada konsentrasi 25 ppm, hormon NAA yang optimal terhadap jumlah
daun pada konsentrasi 75 ppm, sedangkan IBA yang optimal terhadap
pembentukan jumlah daun pada taraf konsentrasi 25 ppm. Pemberian variasi jenis
dan konsentrasi auksin yang optimal terhadap pembentukan dan pertumbuhan
jumlah daun terdapat pada auksin IAA pada konsentrasi 25 ppm karena memiliki
Hasil yang diperoleh menunjukkan bahwa pemberian variasi jenis dan
konsentrasi auksin berpengaruh nyata terhadap jumlah daun pada stek mengkudu.
Panjang tunas dan jumlah daun berhubungan satu sama lain, apabila panjang tunas
meningkat maka jumlah daun juga meningkat. IAA menghasilkan jumlah daun
lebih banyak dibandingkan jenis auksin yang lain. Konsentrasi yang mampu
menghasilkan jumlah daun juga relatif rendah yaitu 25 ppm. Yeshiwas et al.
(2015) dalam penelitiannya terhadap stek batang mawar membutuhkan
konsentrasi yang tinggi untuk memperoleh jumlah daun yang lebih banyak yaitu
dengan penambahan IBA 2.500 ppm. Pertumbuhan daun pada stek mengkudu
disebabkan karena tersedianya zat pengatur tumbuh yang mampu mendorong
terbentuknya daun. Jumlah daun yang muncul pada setiap nodus pada stek batang
mengkudu menunjukkan pada stek mengalami pertumbuhan dan perkembangan
yang lebih baik. Daun yang tumbuh berperan dalam proses fotosintesis yang
kemudian menghasilkan fotosintat yang diperlukan tanaman sebagai sumber
energi dalam proses pertumbuhan dan perkembangannya.
4. Panjang daun
Pemberian variasi jenis dan konsentrasi auksin memberikan hasil yang
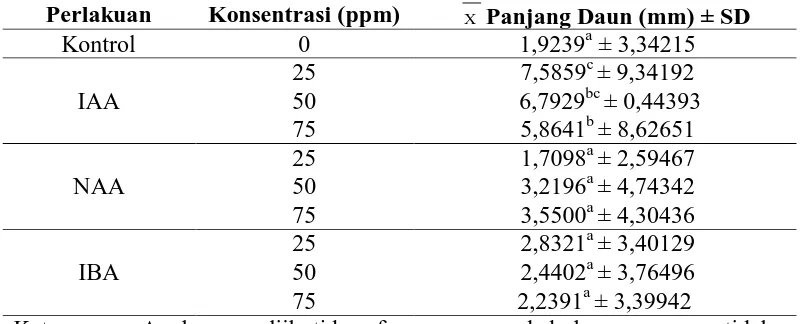
[image:12.595.107.510.515.677.2]beragam terhadap panjang daun pada stek batang mengkudu (Tabel 6).
Tabel 6. Rata-rata panjang daun pada stek batang mengkudu setelah 23 HST dengan pemberian variasi jenis dan konsentrasi auksin
Perlakuan Konsentrasi (ppm) X Panjang Daun (mm) ± SD
Kontrol 0 1,9239a ± 3,34215
IAA
25 7,5859c ± 9,34192
50 6,7929bc ± 0,44393
75 5,8641b ± 8,62651
NAA
25 1,7098a ± 2,59467
50 3,2196a ± 4,74342
75 3,5500a ± 4,30436
IBA
25 2,8321a ± 3,40129
50 2,4402a ± 3,76496
75 2,2391a ± 3,39942
Keterangan: Angka yang diikuti huruf yang sama pada kolom yang sama tidak menunjukkan beda nyata pada uji lanjut DMRT taraf 5%.
SD : Standar Deviasi
HST : hari setelah tanam
Hasil uji ANOVA menunjukkan pemberian variasi konsentrasi IAA
terhadap stek batang mengkudu memberikan pengaruh nyata terhadap kontrol dan
perlakuan lain (Lampiran 2c). Pemberian variasi jenis auksin ternyata
memberikan hasil yang berbeda terhadap panjang daun pada stek batang
mengkudu pada konsentrasi yang berbeda. Auksin IAA optimal pada konsentrasi
25 ppm, auksin NAA optimal terhadap panjang daun pada konsentrasi 75 ppm,
sedangkan auksin IBA yang optimal terhadap pembentukan panjang daun pada
taraf konsentrasi 25 ppm. Pemberian variasi jenis dan konsentrasi auksin yang
optimal terhadap pembentukan dan pertumbuhan panjang daun terdapat pada IAA
pada konsentrasi 25 ppm karena memiliki nilai yang lebih tinggi yaitu sebesar
7,5859 mm.
IAA pada konsentrasi rendah mampu menghasilkan panjang daun yang
lebih panjang bila dibandingkan dengan IAA konsentrasi yang tinggi. Pada stek
batang lemon balm (Melissa officinalis L.) yang dilakukan oleh Sevik dan Guney
(2013) memperlihatkan dengan konsentrasi IAA 1.000 ppm mampu menghasilkan
panjang daun yang lebih baik dibandingkan IAA 5.000 ppm. Menurut Gardner et
al. (1991), panjang tunas pada stek batang mengkudu merupakan hasil
pemanjangan tunas yang terjadi karena adanya proses pembelahan dan
pembesaran sel pada meristem ujung.
Keberhasilan stek dapat dipengaruhi oleh beberapa faktor, baik faktor dari
dalam tanaman maupun faktor dari luar tanaman itu sendiri (Hartmann dan
Kester, 1983). Faktor dalam yang mempengaruhi keberhasilan stek yaitu
kemampuan tumbuhan untuk mengubah zat pengatur tumbuh menjadi aktif atau
kurang aktif. Faktor luar yang mempengaruhi keberhasilan stek adalah faktor
lingkungan yaitu suhu dan kelembapan. Suhu udara yang optimal yaitu pada suhu
29oC, pada suhu ini dapat merangsang pembelahan sel perakaran. Suhu yang
KESIMPULAN
Variasi jenis dan konsentrasi auksin tidak mendorong pembentukan dan
pertumbuhan akar pada stek batang mengkudu (Morinda citrifolia L.). Pemberian
variasi jenis dan konsentrasi auksin memberikan pengaruh yang tidak nyata
terhadap waktu muncul tunas, tetapi berpengaruh nyata terhadap pertumbuhan dan
perkembangan tunas stek batang mengkudu (Morinda citrifolia L.) utamanya pada
parameter jumlah tunas dan jumlah daun. Pemberian auksin jenis IAA
berpengaruh nyata terhadap panjang daun stek batang mengkudu.
DAFTAR PUSTAKA
Adinugraha, H.A., D. Setiadi dan M.N. Ambari. 2006. Kemampuan Bertunas Tanaman Sukun di Kebun Pangkas dari Enam Populasi dengan Aplikasi Hormon IAA. Jurnal Penelitian Hutan Tanaman 3 (1) : 265 – 273.
Apriliani, A., Z.A. Noli dan Suwirmen. 2015. Pemberian Beberapa Jenis dan Konsentrasi Auksin untuk Menginduksi Perakaran pada Stek Pucuk Bayur (Pterospermum javanicum Jungh.) dalam Upaya Perbanyakan Tanaman Revegetasi. Jurnal Biologi Universitas Andalas 4 (3) : 178-187.
Atkinson, N. 1956. Antibacterial Substance from Flowering Plants. Antibacterial Activity of Dried Australian Plant by A Rapid Direct Plate Test.
Australian J. Exp. Biol. 34 : 17-26.
Baroroh, F.H., L.Q. Aini, dan A.L. Abadi. 2014. Uji Efektivitas Antibakteri
Ekstrak Daun dan Buah Mengkudu (Morinda citrifolia L.) terhadap Blood
Disease Bacterium. Jurnal Hama dan Penyakit Tumbuhan 2(2):87-97. Danu, D. 1993. Pengaruh Bahan Stek dan Zat Pengatur Tumbuh terhadap
Pertumbuhan Sungkai (Peronema canescens Jack). Laporan Penelitian. Balai Penelitian dan Pengembangan Kehutanan. Balai Teknologi Pembenihan. Departemen Kehutanan Bogor, Bogor.
Danu, D.,A. Subiato, dan K.P. Putri. 2011. Uji Stek Pucuk Damar (Agathis loranthifolia Salisb.) pada Berbagai Media dan Zat Pengatur Tumbuh.
Jurnal Penelitian Hutan dan Konservasi Alam 8(3):245-252.
Djauhariya, E. dan M. Rahardjo. 2004. Pengaruh Zat Pengatur Tumbuh terhadap Keberhasilan Perbanyakan Tanaman Mengkudu dengan Stek Batang.
Prosiding Seminar Nasional XXV Tumbuhan Obat Indonesia . Kelompok Kerja Nasional Tanaman Obat Indonesia, Tawangmangu 24-28 April 2004, hal. 79-86.Djauhariya, E., M. Rahardjo, dan Ma’mun. 2006. Karakterisasi Morfologi Dan Mutu Buah Mengkudu. Bul. Plasma Nutfah
12 (I) : 1-8.
Gehlot, A., R.K. Gupta, A. Tripathi, I.D. Arya, and S. Arya. 2014. Vegetative Propagation of Azadirachta indica: Effect of Auxin and Rooting Media on Adventitious Root Induction in Mini-cuttings. Advances in Forestry Science 1(1) : 1-9.
Hartmann H. T. and Kester D. E.. 1983. Plant Propagation : Principles and Practices. 4th Editions. Englewood Cliffs, New Jersey.
Hasanah, F.N. dan N. Setiari. 2007. Pembentukan Akar pada Stek Batang Nilam (Pogostemon cablin Benth.) Setelah Direndam IBA (Indol Butyric Acid) pada Konsentrasi Berbeda. Buletin Anatomi dan Fisiologi 15(2):1-6.
Heddy, S. 1989. Hormon Tumbuhan. CV. Rajawali, Jakarta.
Hendaryono, D.P.S., dan Wijayani, A. 1994. Teknik Kultur Jaringan. Penerbit Kanisius, Yogyakarta.
Jayasinghe, U.L.B., C.P. Jayasooriya, B.M.R. Bandara, S.P. Ekanayake, L. Merlini, and G. Assante. 2002. Antimicrobial Activity of Some Srilanka Rubiaceae and Meliaceae. Fitoterapia 73(5) : 424-427.
Kramer, D.J. dan T.T. Kozlowski. 1960. Physiology of Tress. Mc Graw Hill Book Co, New York
Leopold, A. C. dan P. E. Kriedmann. 1975. Plant Growth and Development.
McGraw– Hill, New York.
Mohtar, M., K. Shaari, N.A.M. Ali, and A.M. Ali. 1998. Antimicrobial Activity of Selected Malaysian Plants Against Micro-organisms Related to Skin Infection. Journal of Tropical Forest Products 4(2) : 199-206.
Muhamad, M. 2014. Membuat Pupuk Alternatif untuk Hidroponik.
http://www.academia.edu/8340509/Membuat_Pupuk_Alternatif_untuk_Hi droponik. Diakses pada tanggal 26 Februari 2015.
Rahmayani, I. P., A. M. Maskoen, dan B. S. Hernowo. 2013. Peran Ekstrak Etanol Daun Mengkudu (Morinda citrifolia L.) pada Penyembuhan Luka Ditinjau dari Imunoekspresi CD34 dan Kolagen pada Tikus Galur Wistar.
Bandung Medical Journal 45(4) : 226-233.
Sevik, H. and K. Guney. 2013. Effects of IAA, IBA, NAA, and GA3 on Rooting and Morphological Features of Melissa officinalis L. Stem Cuttings. The Scientific World Journal 2013 : 1 – 5.
Trisna, N., H. Umar, dan Irmasari. 2013. Pengaruh Berbagai Jenis Zat Pengatur Tumbuh terhadap Pertumbuhan Stump Jati (Tectona grandis L.f.). Warta Rimba 1(1) : 1-9.
Waziri, M.S., M. Ibrahim, M.A. Ibrahim, and M. Bulama. 2015. Effect of Various IBA Concentrations on The Rooting and Growth of Delonix regia Stem Cuttings in Maiduguri. Donnish Journal of Agricultural Research 2(1) : 10-15.