EFEK HEPATOPROTEKTIF JANGKA PENDEK INFUSA BIJI ATUNG (Parinarium glaberimum Hassk) PADA TIKUS JANTAN GALUR WISTAR TERINDUKSI
KARBON TETRAKLORIDA
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Gregorius Kevin Besari NIM : 138114050
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA
YOGYAKARTA
HALAMAN PERSEMBAHAN
Kupersembahkan karya ini untuk :
Tuhan Yang Maha Esa atas segala rahmat dan karunianya dalam hidupku
Papa, Mama dan Adik tercinta yang selalu memberikan doa dan kasih sayang
Teman-teman yang telah mendukung dan menyemangati
PRAKATA
Puji syukur kepada Tuhan Yang Maha Esa, atas berkat, rahmat, cinta kasih dan karunia-Nya penulis dapat menyelesaikan skripsi yang berjudul “EFEK HEPATOPROTEKTIF JANGKA PENDEK INFUSA BIJI ATUNG (Parinarium glaberimum Hassk) PADA TIKUS
JANTAN GALUR WISTAR TERINDUKSI KARBON TETRAKLORIDA”.
Skripsi ini disusun untuk memenuhi salah satu persyaratan untuk memperoleh gelar Sarjana Farmasi (S. Farm) program studi Farmasi Universitas Sanata Dharma Yogyakarta. Penulis menyadari bahwa dalam pelaksanaan dan penyusunan skrpsi ini tidak terlepas dari bantuan dan dukungan berbagai pihak. Oleh karena itu, pada kesempatan ini penulis mengucapkan terimakasih kepada :
1. Ibu Aris Widayati, M.Sc., Ph.D., Apt., selaku Dekan Fakultas Farmasi Universitas Sanata Dharma.
2. Ibu Yunita Linawati, S.Si., M.Sc., Apt., selaku Dosen Pembimbing Skripsi yang telah membimbing dan mendampingi dengan baik selama proses penyusunan skripsi ini.
3. Ibu Phebe Hendra, M.Si., Ph.D., Apt., selaku Dosen Penguji yang telah memberi kritik dan saran yang membangun dalam proses pelaksanaan dan penyusunan skripsi.
4. Ibu Dr. Yustina Sri Hartini Apt., selaku Dosen Penguji yang telah memberi kritik dan saran yang membangun dalam proses pelaksanaan dan penyusunan skripsi.
5. Ibu Dr. Dewi Setianingsih, M.Sc., Apt., selaku Kepala Laboratorium Fakultas Farmasi yang telah memberikan izin penggunaan fasilitas laboratorium untuk kepentingan skripsi. 6. Bapak Florentinus Dika Octa Riswanto, M.Sc., selaku Dosen Pembimbing Akademik atas
bimbinganya selama ini.
7. Bapak Heru, Bapak Kayat dan Bapak Parjiman, selaku Laboran Laboratorium Fakultas Farmasi atas bantuan dan dukungannya selama proses pengerjaan skripsi
8. Keluarga tercinta Bapak Rufinus Yusmintoro, Ibu Felicia Rosniyati, dan adik Gabriella Viagiani Besari atas segala doa, cinta, semangat dan dukungannya kepada penulis selama proses penyelesaian skripsi.
10. Rekan-rekan tim skripsi M.A.N : Meliana, Ajeng Dwi Kartika dan Masrial Zaluku atas kerjasama, dukungan, bantuan dan persahabatan yang terjalin selama ini
11. Teman-teman FSM B, FST 2013 serta seluruh anggota Fakultas Farmasi Universitas Sanata Dharma terkhusus angkatan 2013 atas kebersamaanya.
12. Semua pihak yang tidak dapat disebutkan satu per satu oleh penulis yang telah berperan dalam membantu penulis selama proses penyelesaian skripsi ini.
Penulis menyadari bahwa masih banyak kelemahan dan kekurangan dalam penulisan skripsi ini. Oleh karena itu, besar harapan penulis terhadap kritik dan saran yang membangun dan bermanfaat khususnya bagi pengembangan ilmu pengetahuan. Semoga tulisan ini dapat memberikan manfaat khususnya di bidang Farmasi, serta semua pihak baik di lingkungan akademis maupun masyarakat.
Yogyakarta, Mei 2017 Penulis
DAFTAR ISI
HALAMAN JUDUL. . . i
HALAMAN PERSETUJUAN PEMBIMBING . . . ii
HALAMAN PENGESAHAN . . . iii
HALAMAN PERSEMBAHAN. . . iv
PERNYATAAN KEASLIAN KARYA. . . v
PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH . . . vi
PRAKATA. . . vii
DAFTAR ISI. . . ix
DAFTAR TABEL. . . x
DAFTAR GAMBAR . . . xi
DAFTAR LAMPIRAN. . . xii
ABSTRAK . . . xiii
ABSTRACT. . . xiv
PENDAHULUAN . . . 1
METODOLOGI. . . 2
HASIL DAN PEMBAHASAN. . . 5
KESIMPULAN . . . 14
SARAN . . . 15
DAFTAR PUSTAKA. . . 15
LAMPIRAN . . . 17
DAFTAR TABEL
DAFTAR GAMBAR
Gambar I. Histogram Rata-rata Aktivitas ALT Setelah Pemejanan CCl4 Dosis 2 mL/kgBB pada Waktu 0, 24 & 48 jam . . . 7 Gambar II. Histogram Rata-rata Aktivitas AST Setelah Pemejanan CCl4 Dosis 2 mL/kgBB pada Waktu 0, 24 & 48 jam . . . 8 Gambar III. Histogram Rata-rata Aktivitas ALT pada Semua Kelompok
Perlakuan . . . . . 10 Gambar IV. Histogram Rata-rata Aktivitas AST pada Semua Kelompok
DAFTAR LAMPIRAN
Lampiran 1. Surat Ethical Clearance. .. . . . . . 18
Lampiran 2. Surat Determinasi Tanaman. . . 19
Lampiran 3. Bahan Uji dan Infusa Biji Parinarium glaberimum Hassk . . . 20
Lampiran 4. Penetapan Kadar Air Serbuk Biji Parinarium glaberimum Hassk . . . 21
Lampiran 5. Surat Legalitas Hewan Uji . . . 22
Lampiran 6. Surat Legalitas Penggunaan SPSS . . . 23
Lampiran 7. Analisis Statistik Aktivitas ALT dan AST pada Uji Pendahuluan Waktu Pencuplikan Darah Hewan Uji . . . 24
Lampiran 8. Analisis Statistik Aktivitas ALT dan AST pada Uji Pendahuluan Penetapan Dosis Infusa Biji Parinarium glaberimum Hassk . . . 29
Lampiran 9. Purata dan Hasil Uji Post-Hoc Data ALT & AST Uji Pendahuluan Penetapan Dosis Infusa Biji Parinarium glaberimum Hassk . . . 39
Lampiran 10. Analisis Statistik Data Perlakuan . . . 40
Lampiran 11. Perhitungan persen hepatoprotektif . . . 50
ABSTRAK
Hati merupakan organ terbesar di dalam tubuh manusia yang berperan penting dalam metabolisme tubuh. Hati memiliki potensi untuk mengalami kerusakan karena beberapa proses metabolismenya dapat menghasilkan metabolit yang bersifat toksik. Salah satu senyawa toksik yang dapat menyebabkan kerusakan hati adalah karbon tetraklorida (CCl4). CCl4 di dalam hati akan dimetabolisme oleh enzim sitokrom P450 menjadi senyawa radikal triklorometilperoksi yang dapat merusak hati. Salah satu tanaman herbal di Indonesia yaitu tanaman Atung (Parinarium glaberimum Hassk) diketahui memiliki kandungan senyawa polifenol terutama pada bagian biji yang dapat dimanfaatkan sebagai antioksidan sehingga dapat menangkap radikal bebas penyebab kerusakan hati akibat senyawa toksik CCl4. Tujuan dari penelitian ini adalah untuk mengetahui efek hepatoprotektif pemberian jangka pendek infusa biji Atung (Parinarium glaberimum Hassk) pada tikus jantan galur Wistar terinduksi karbon tetraklorida. Penelitian merupakan penelitian eksperimental murni dengan rancangan acak lengkap pola searah. Penelitian ini menggunakan 30 ekor tikus jantan galur Wistar berusia 2-3 bulan dengan berat badan ± 160-250 gram yang dibagi secara acak ke dalam enam kelompok dengan jumlah yang sama. Kelompok I (kontrol hepatotoksin) diberi karbon tetraklorida dengan dosis 2 mL/kg BB secara intraperitonial dan setelah jam ke-24 dilakukan pencuplikan darah. Kelompok II (kontrol negatif) diberi olive oil 2 mL/kg BB secara intraperitonial kemudian pada jam ke-24 dilakukan pencuplikan darah. Kelompok III (kontrol infusa) diberi perlakuan infusa biji Parinarium glaberimum Hassk dosis tertinggi yaitu 20 g/kgBB dan 6 jam kemudian dilakukan pencuplikan darah. Kelompok IV-VI (kelompok perlakuan) diberikan perlakuan infusa biji Parinarium glaberimum Hassk dengan variasi dosis yaitu 5, 10, 20 g/kgBB secara peroral. Jam ke-6 setelah pemberian infusa biji Parinarium glaberimum Hassk, kelompok IV-VI dipejani dengan karbon tetraklorida dosis 2 mL/kg BB secara intraperitonial, lalu pada jam ke-24 dilakukan pencuplikan darah melalui sinus orbitalis mata, kemudian dilakukan pengujian aktivitas serum ALT-AST. Data ALT dan AST dianalisis menggunakan uji Kolmogorov Smirnov dilanjutkan dengan uji One Way Anova dengan taraf kepercayaan 95% dan dilanjutkan dengan menggunakan uji Post-Hoc LSD.
Hasil penelitian menunjukkan bahwa infusa biji Parinarium glaberimum Hassk dosis 5, 10, 20 g/kgBB memiliki efek hepatoprotektif jangka pendek pada tikus jantan galur Wistar terinduksi karbon tetraklorida.
ABSTRACT
The liver is the largest organ in the human body that plays an important role in the metabolism of the body. The liver has the potential to damage due to some process of metabolism can produce toxic metabolites. One of the toxic compounds which can cause liver damage is carbon tetrachloride (CCl4). CCl4 in the liver will be metabolized by the enzyme cytochrome P450 into trichloromethyl peroxy radical compounds that can damage the liver. One of the herbal plant in Indonesia is the Atung plant (Parinarium glaberimum Hassk) known to contain polyphenol compounds, especially in the seeds can be used as an antioxidant that can capture free radicals that cause liver damage from toxic compounds CCl4. The aim of study were to know the hepatoprotective effect of short term period of Parinarium glaberimum Hassk seeds infusion in male Wistar rats induced by carbon tetrachloride
This purely experimental research with randomized complete direct sampling. This research used 30 male Wistar rats aged 2-3 months with body weight ± 160-250 grams divided randomly into 6 groups in the same amount. Group I (hepatotoxin control) was given carbon tetrachloride dose 2 mL/kgBW intraperitoneally and on 24 hours the blood drown. Group II (negative control) was given olive oil dose 2 mL/kgBW intraperitoneally and on 24 hours the blood drown. Group III (infusion control) was given Parinarium glaberimum Hassk seeds infusion at high dose 20 g/kgBW and on 6 hours the blood drown. Group IV-VI (treatment groups) were given pre-treatment with Parinarium glaberimum Hassk seeds infusion at dose 5, 10, and 20 g/kgBW orally. Then 6 hours after treatment given carbon tetrachloride at a dose of
2 mL/kgBW intraperitoneally. On 24 hours, the blood drawn through rat’s eyes sinus orbitalis
for measuring ALT and AST activities. The result of ALT and AST activity were analyzed with Kolmogorov Smirnov, One Way Anova, then Post-Hoc LSD.
The result of study shown that Parinarium glaberimum Hassk seeds infusion at dose 5, 10, and 20 g/kgBW have short-term hepatoprotective effect in male Wistar rats induced by carbon tetrachloride.
Keywords : Short Term Period, Parinarium glaberimum Hassk Seeds, Infusion, Hepatoprotective, ALT, AST, CCl4.
PENDAHULUAN
Hati merupakan organ terbesar di dalam tubuh manusia yang berkontribusi sebesar 2% dari bobot total tubuh atau sekitar 1,5 kilogram. Hati berperan penting dalam fungsi fisiologis tubuh diantaranya adalah berperan dalam proses filtrasi darah; metabolisme karbohidrat, protein, lemak, hormon dan senyawa asing; produksi empedu; serta menyimpan vitamin dan zat besi (Hall, 2016). Hati memiliki potensi untuk mengalami kerusakan karena beberapa proses metabolismenya dapat menghasilkan metabolit yang bersifat toksik (Sumardi, 2010).
Kerusakan pada organ hati dapat mengganggu kemampuan dalam menjalankan fungsinya. Meskipun hati memiliki kemampuan regenerasi yang cepat, hati dapat mempertahankan fungsinya hanya sampai batas tertentu bila terjadi gangugan ringan. Pada gangguan yang lebih berat, terjadi gangguan fungsi yang serius dan berakibat fatal. Penyebab kerusakan hati bervariasi, sebagian besar disebabkan oleh virus yang menular dan efek toksik dari obat-obatan, alkohol, racun, jamur dan lain-lain (Depkes RI, 2007) Kerusakan yang disebabkan oleh berbagai macam senyawa kimia (hepatotoksik) dapat melalui dua cara yaitu akumulasi lemak (steatosis) dan kematian sel hati (nekrosis) (WHO, 2005).
Karbon tetraklorida (CCl4) merupakan senyawa toksik yang menyebabkan kerusakan hati. Secara umum CCl4 dapat menyebabkan steatosis atau akumulasi lemak trigliserida pada sel hepatosit (Timbrell, 2009). Enzim sitokrom P450 pada hati akan memetabolisme CCl4 menjadi senyawa radikal bebas yang dapat menimbulkan gangguan pada hati. Paparan CCl4 dalam dosis tinggi dapat merusak retikulum endoplasmik, mengakumulasi lipid, mengurangi sintesis protein, mengacaukan proses oksidasi, menyebabkan pembengkakan hati dan pemberian jangka panjang akan menyebabkan nekrosis (Panjaitan et al., 2007). Pembentukan radikal bebas yang bersifat toksik menyebabkan tubuh perlu tambahan antioksidan dari luar tubuh untuk melindungi hati (hepatoprotektif) (Tappi et al., 2013).
Kemampuan obat tradisional sebagai agen hepatoprotektif dapat diketahui dengan berbagai mekanisme, diantaranya adalah dengan adanya kandungan senyawa yang memiliki potensi antiinflamasi, antioksidan, meningkatkan regenerasi sel-sel hati dengan meningkatkan sintesis protein, menjaga integritas membrane sel, dan sebagainya (Wahyudi, 2011). Beberapa tanaman alami diketahui memiliki potensi sebagai agen hepatoprotektif. Salah satu tanaman herbal di Indonesia yang memiliki potensi untuk dijadikan sebagai agen hepatoprotektif yaitu tanaman Atung (Parinarium glaberimum Hassk) yang tumbuh secara alami di daerah Maluku (Heyne, 1987). Berdasarkan penelitian Moniharapon (1998), diketahui bahwa biji tanaman atung mengandung senyawa polifenol. Polifenol dikenal sebagai golongan senyawa alami yang memiliki aktivitas sebagai antioksidan sehingga dapat mengatasi stress oksidatif yang disebabkan karena radikal bebas (Christensen, 2014).
Berdasarkan uraian tersebut maka dilakukan penelitian menggunakan sediaan berupa infusa biji Atung (Parinarium glaberimum Hassk) dengan pemberian jangka pendek sebagai agen hepatoprotektif pada tikus jantan galur Wistar yang terinduksi karbon tetraklorida terhadap aktivitas ALT-AST. Jangka pendek dipilih karena belum pernah dilakukan penelitian dalam membuktikan efek hepatoprotektif dari infusa biji Parinarium glaberimum Hassk secara jangka pendek. Pemberian jangka pendek dilakukan dalam rentang waktu selama 6 jam. Sediaan berupa infusa dipilih karena dapat menyari senyawa polifenol dan penggunaanya mudah diterapkan pada masyarakat.
METODOLOGI
Penelitian ini merupakan penelitian eksperimental murni dengan rancangan acak lengkap pola searah.
Alat dan Bahan
sentrifuge, vortex, pipa kapiler, tabung Eppendorf, blue tip, stopwatch, spuit injeksi dan spuit peroral.
Metode
Penelitian ini mengukur aktivitas ALT dan AST pada subjek uji tikus jantan galur Wistar yang terinduksi karbon tetraklorida. Subjek uji diperoleh dari peternakan hewan uji daerah Bantul, Yogyakarta. Tikus Wistar yang digunakan berusia 2-3 bulan dengan berat badan ± 160 – 250 gram. Tikus dibagi menjadi 6 kelompok yaitu kelompok I sebagai kontrol hepatotoksin (CCl4 dosis 2 mL/kgBB), kelompok II sebagai kontrol negatif (olive oil dosis 2 mL/kgBB), kelompok III sebagai kontrol perlakuan (infusa Parinarium glaberimum Hassk dosis tertinggi) dan kelompok IV,V dan VI sebagai kelompok perlakuan infusa biji Parinarium glaberrimum Hassk. Uji pendahuluan dilakukan untuk menetapkan dosis karbon tetraklorida,
waktu pencuplikan darah dan peringkat dosis infusa biji Parinarium glaberrimum Hassk. Pengumpulan, Pengeringan dan Pembuatan Infusa
Biji Parinarium glaberimum Hassk yang dikumpulkan berasal dari lingkungan Fakultas Perikanan Universitas Pattimura, Ambon. Biji yang dipilih adalah biji dengan umur panen 3 bulan dengan kulit luar berwarna cokelat merah bata tua. Biji Parinarium glaberimum Hassk dicuci dengan air mengalir dan diangin-anginkan hingga kering. Kemudian biji diiris tipis-tipis dan dimasukan kedalam oven pada suhu 50oC selama 1 minggu. Biji yang telah kering diserbuk dengan alat penyerbuk dan diayak menggunakan ayakan no. 40 untuk mendapatkan serbuk halus. Konsentrasi Infusa yang dibuat yaitu sebesar 10% (Badan Pengawas Obat dan Makanan, 2010) namun dilakukan sedikit modifikasi terhadap konsentrasi infusa yang dibuat menjadi 100% dengan cara serbuk halus biji Parinarium glaberrimum Hassk ditimbang sebanyak 100 g kemudian dimasukan ke dalam panci enamel dan ditambah 100 mL aquadest, panaskan di atas penangas air selama 15 menit dimulai saat suhu mencapai 90oC sambil sesekali diaduk. Hasilnya diserkai selagi panas melalui kain flannel, tambahkan air panas secukupnya melalui ampas hingga diperoleh volume yang dikehendaki
Penetapan Kadar Air
suhu 120oC dan dihitung hingga satu menit setelah suhu mencapai 120oC. Hasil kadar air akan tertera pada layar dan dilakukan tiga kali replikasi.
Pembuatan Larutan Karbon Tetraklorida Konsentrasi 50%
Larutan karbon tetraklorida dibuat dengan perbandingan volume karbon tetraklorida dan olive oil sebagai pelarut, yaitu 1:1. Larutan dibuat dengan melarutkan karbon tetraklorida ke dalam olive oil dengan volume yang sama.
Uji Pendahuluan
Dosis Karbon tetraklorida yang digunakan untuk menginduksi kerusakan hati tikus jantan galur Wistar adalah 2 mL/kgBB dengan perbandingan volume antara CCl4 dengan pelarut olive oil, yaitu 1:1 (Janakat dan Al-Merie, 2002).
Uji Penetapan waktu pencuplikan darah ditentukan melalui orientasi dengan tiga kelompok perlakuan waktu, yaitu pada jam ke-0, 24, dan 48 setelah diinduksi karbon tetraklorida. Setiap kelompok perlakuan terdiri dari 3 ekor tikus. Pencuplikan darah dilakukan melalui sinus orbitalis mata. Setelah pencuplikan darah kemudian diukur aktivitas ALT dan AST di Laboratorium Biokimia Universitas Sanata Dharma Yogyakarta.
Penetapan dosis infusa biji Parinarium glaberimum Hassk didasarkan pada konsentrasi tertinggi infusa yang dapat di spuit dan tidak menyebabkan kematian. Konsentrasi tertinggi yang didapat yaitu 100% sehingga didapatkan dosis tertinggi 20 g/kgBB berdasarkan volume maksimal pemberian dan bobot maksimum tikus (250 g). Kemudian volume pemberian pada tikus dihitung dengan rumus :
Volume
Pengelompokan dan Perlakuan Hewan Uji
Penelitian ini menggunakan tikus jantan galur Wistar sebanyak 30 ekor yang dibagi ke dalam 6 kelompok secara acak dan sama banyak. Kelompok I (kontrol hepatotoksin) diberi larutan karbon tetraklorida dalam olive oil 1:1 dengan dosis 2 mL/kgBB secara intraperitoneal kemudian pada jam ke-24 dilakukan pencuplikan darah. Kelompok II (kontrol negatif) diberi perlarut olive oil dosis 2 mL/KgBB secra intraperitoneal dan pada jam ke-24 dilakukan pencuplikan darah. Kelompok III (kontrol infusa) diberikan infusa biji Atung (Parinarium glaberimum Hassk) dosis 20 g/kgBB secara per oral, 6 jam kemudian dilakukan pencuplikan
larutan karbon tetraklorida dalam olive oil 1:1 dengan dosis 2 mL/kgBB secara intraperitoneal dan pada jam ke-24 dilakukan pencuplikan darah melalui sinus orbitalis lalu darah dimasukkan kedalam tabung Eppendorf dan disentrifuge dengan kecepatan 8000 rpm selama 15 menit. Kemudian dilakukan pengukuran aktivitas ALT dan AST menggunakan Microlab 200 dan reagen ALT Diasys® & AST Diasys®. Aktivitas ALT diukur dengan cara bagian yang jernih diambil (supernatan), dimasukkan kedalam tabung reaksi kecil, ditambah dengan 1000 L reagen I, divorteks dan ditunggu selama 5 menit kemudian ditambah 250 L reagen II, divorteks dan ditunggu 1 menit, setelah itu dlakukan pengukuran menggunakan Microlab 200. Cara yang sama dilakukan untuk mengukur aktivitas serum AST, namun digunakan reagen untuk pengukuran aktivitas AST. Hasil aktivitas ALT dan AST yang didapat kemudian dianalisis dengan menggunakan Kolmogorov Smirnov, dilanjutkan dengan uji One Way Anova dengan taraf kepercayaan 95% dan dilanjutkan dengan uji Post Hoc LSD. Selanjutnya dilakukan perhitungan persen hepatoprotektif dengan rumus seperti pada Lampiran 11.
HASIL DAN PEMBAHASAN
Penelitian ini bertujuan untuk mengetahui efek hepatoprotektif jangka pendek infusa biji atung (Parinarium glaberimum Hassk) pada tikus jantan galur Wistar terinduksi karbon tetraklorida.
Determinasi tanaman
Tujuan dari determinasi tanaman adalah untuk memastikan bahwa tanaman yang digunakan dalam penelitian merupakan buah Atung (Parinarium glaberimum Hassk). Determinasi tanaman dilakukan di Fakultas Biologi Universitas Gadjah Mada Yogyakarta. Hasil determinasi membuktikan bahwa tanaman yang digunakan adalah benar merupakan tanaman Atung (Parinarium glaberimum Hassk) (Lampiran 2).
Pembuatan Serbuk Kering
Penetapan Kadar Air
Penetapan kadar air bertujuan untuk memenuhi persyaratan serbuk yang baik yaitu kadar air kurang dari 10% (Badan Pengawas Obat dan Makanan, 2014). Dengan kadar air kurang dari 10% dapat dipastikan kualitas dan penyimpanan serbuk (terkait dengan pertumbuhan mikroba). Penetapan kadar air dengan menggunakan alat moisture balance. Hasil pengujian didapatkan bahwa kandungan air serbuk biji Parinarium glaberimum Hassk sebesar 6,52% sehingga memenuhi syarat sebagai serbuk yang baik (Lampiran 4).
Uji Pendahuluan
Uji pendahuluan dilakukan untuk menetapkan waktu pencuplikan darah hewan uji dan menentukan dosis infusa biji Parinarium glaberimum Hassk. Hasil aktivitas ALT dan AST pada waktu pencuplikan darah dapat dilihat pada Tabel I.
Tabel I. Aktivitas ALT dan AST Tikus Setelah Pemejanan CCl4 2mL/KgBB pada Waktu 0, 24 & 48 jam
Keterangan : SE = Standar Error, n = Jumlah Hewan Uji
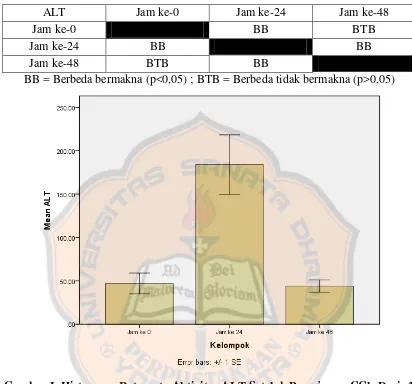
Tabel II. Hasil Uji LSD Kadar ALT Setelah Pemejanan CCl4 Dosis 2 mL/kgBB pada Waktu 0, 24 & 48 jam
ALT Jam ke-0 Jam ke-24 Jam ke-48
Jam ke-0 BB BTB
Jam ke-24 BB BB
Jam ke-48 BTB BB
BB = Berbeda bermakna (p<0,05) ; BTB = Berbeda tidak bermakna (p>0,05)
Gambar I. Histogram Rata-rata Aktivitas ALT Setelah Pemejanan CCl4 Dosis 2 mL/kgBB pada Waktu 0, 24 & 48 jam
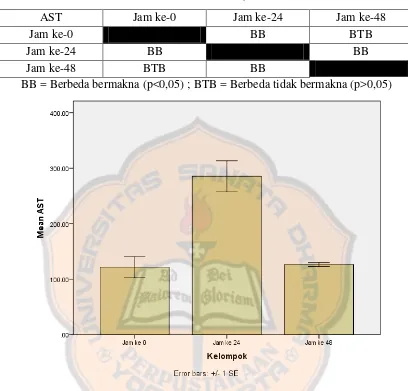
Tabel III. Hasil Uji LSD Kadar AST Setelah Pemejanan CCl4 Dosis 2 mL/kgBB pada Waktu 0, 24 & 48 jam
AST Jam ke-0 Jam ke-24 Jam ke-48
Jam ke-0 BB BTB
Jam ke-24 BB BB
Jam ke-48 BTB BB
BB = Berbeda bermakna (p<0,05) ; BTB = Berbeda tidak bermakna (p>0,05)
Gambar II. Histogram Rata-rata Aktivitas AST Setelah Pemejanan CCl4 Dosis 2 mL/kgBB pada Waktu 0, 24 & 48 jam
kadar normal. Berdasarkan hasil analisis aktivitas ALT dan AST maka jam ke-24 dipilih sebagai waktu pencuplikan darah.
Penetapan dosis infusa biji Parinarium glaberimum Hassk didasarkan pada hasil orientasi dalam menentukan dosis tertinggi, kemudian diturunkan sebanyak 2 dan 4 nilai dari dosis tertinggi. Penentuan dosis tertinggi berdasarkan pada bobot masksimum hewan uji yang digunakan (250 gram), konsentrasi maksimal infusa yang dapat dibuat (100%), dan volume maksimal peroral yang dapat diberikan pada tikus (5 mL). Dosis tertinggi yang didapatkan yaitu 20 g/kgBB. Kemudian diturunkan sebanyak 2 nilai dari dosis tertinggi sebagai dosis II dan 4 nilai dari dosis tertinggi sebagai dosis I, dengan demikian diperoleh peringkat dosis 5, 10, dan 20 g/kgBB (Lampiran 9).
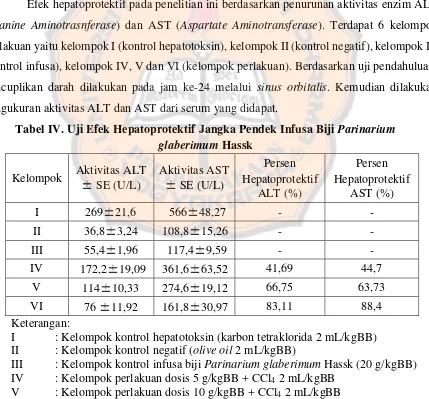
Hasil Uji Efek Hepatoprotektif
Efek hepatoprotektif pada penelitian ini berdasarkan penurunan aktivitas enzim ALT (Alanine Aminotrasnferase) dan AST (Aspartate Aminotransferase). Terdapat 6 kelompok perlakuan yaitu kelompok I (kontrol hepatotoksin), kelompok II (kontrol negatif), kelompok III (kontrol infusa), kelompok IV, V dan VI (kelompok perlakuan). Berdasarkan uji pendahuluan, pencuplikan darah dilakukan pada jam ke-24 melalui sinus orbitalis. Kemudian dilakukan pengukuran aktivitas ALT dan AST dari serum yang didapat.
Tabel IV. Uji Efek Hepatoprotektif Jangka Pendek Infusa Biji Parinarium glaberimum Hassk
I : Kelompok kontrol hepatotoksin (karbon tetraklorida 2 mL/kgBB) II : Kelompok kontrol negatif (olive oil 2 mL/kgBB)
III : Kelompok kontrol infusa biji Parinarium glaberimum Hassk (20 g/kgBB) IV : Kelompok perlakuan dosis 5 g/kgBB + CCl4 2 mL/kgBB
VI : Kelompok perlakuan dosis 20 g/kgBB + CCl4 2 mL/kgBB SE : Standar Error
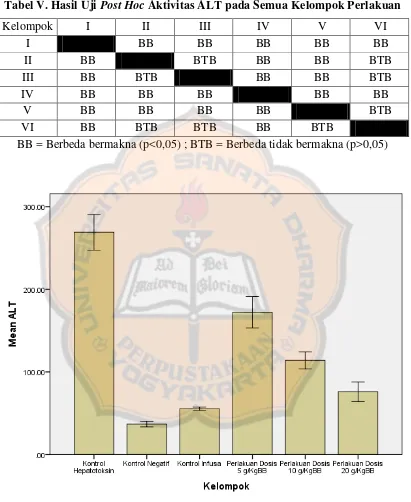
Tabel V. Hasil Uji Post Hoc Aktivitas ALT pada Semua Kelompok Perlakuan
Kelompok I II III IV V VI
I BB BB BB BB BB
II BB BTB BB BB BTB
III BB BTB BB BB BTB
IV BB BB BB BB BB
V BB BB BB BB BTB
VI BB BTB BTB BB BTB
BB = Berbeda bermakna (p<0,05) ; BTB = Berbeda tidak bermakna (p>0,05)
Tabel VI. Hasil Uji Post Hoc Aktivitas AST pada Semua Kelompok Perlakuan
Kelompok I II III IV V VI
I BB BB BB BB BB
II BB BTB BB BB BTB
III BB BTB BB BB BTB
IV BB BB BB BTB BB
V BB BB BB BTB BB
VI BB BTB BTB BB BB
BB = Berbeda bermakna (p<0,05) ; BTB = Berbeda tidak bermakna (p>0,05)
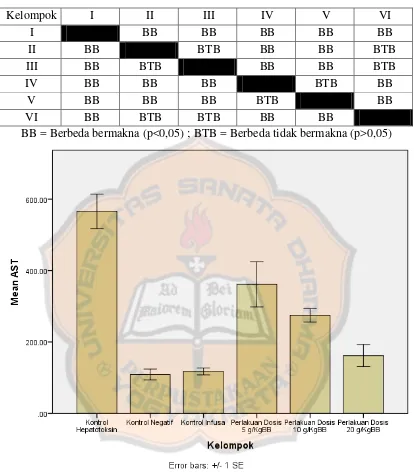
Gambar IV. Histogram Rata-rata Aktivitas AST pada Semua Kelompok Perlakuan a. Kontrol Hepatotoksin
bermakna (p<0,05) terhadap kontrol negatif, kontrol infusa dan kelompok perlakuan (dosis IV,V, dan VI) seperti pada Tabel V dan Tabel VI. Hal tersebut menjelaskan bahwa pemberian karbon tetraklorida dengan dosis 2 mL/kgBB memiliki efek hepatotoksin yang ditandai dengan adanya peningkatan aktivitas ALT dan AST.
b. Kontrol Negatif
Kontrol negatif dalam penelitian ini berupa olive oil yang merupakan pelarut dari karbon tetraklorida. Tujuan dari kontrol negatif (Kelompok II) adalah untuk mengetahui pengaruh pemberian olive oil sebagai pelarut karbon tetraklorida terhadap aktivitas ALT dan AST pada tikus dan memastikan bahwa peningkatan aktivitas serum ALT dan AST adalah akibat dari pemberian karbon tetraklorida bukan dari olive oil. Hasil aktivitas ALT dan AST olive oil pada Tabel IV lebih rendah dibandingkan dengan kontrol heptotoksin. Berdasarkan
Tabel V dan Tabel VI, baik aktivitas ALT maupun AST menunjukkan perbedaan bermakna (p<0,05) terhadap kontrol hepatotoksin. Selain itu berdasarkan penelitian yang dilakukan oleh Yuliani (2015), menunjukan data bahwa aktivitas ALT dan AST olive oil pada jam ke-24 jika dibandingkan dengan jam ke-0 menunjukkan perbedaan yang tidak bermakna. Hal tersebut menjelaskan bahwa olive oil dapat dijadikan patokan sebagai nilai normal dan dapat diketahui bawha olive oil tidak mempengaruhi aktivitas ALT dan AST.
c. Kontrol Infusa
Kontrol infusa (Kelompok III) bertujuan untuk mengetahui pengaruh pemberian infusa biji Parinarium Glaberimum Hassk dosis tertinggi 20 g/kgBB terhadap aktivitas ALT dan AST pada tikus. Aktivitas ALT dan AST menunjukkan hasil yang lebih rendah dibandingkan dengan kontrol hepatotoksin dan menunjukkan hasil yang hampir sama dengan kontrol olive oil (Tabel IV). Berdasarkan uji statistik (Tabel V dan Tabel VI) dapat dilihat bahwa kontrol infusa memiliki perbedaan tidak bermakna (p>0,05) dengan kontrol negatif olive oil dan memiliki perbedaan bermakna (p<0,05) dengan kontrol hepatotoksin baik pada aktivitas ALT maupun AST. Hal ini menjelaskan bahwa pemberian infusa dosis tinggi tidak mempengaruhi aktivitas ALT dan AST.
d. Kelompok Peringkat Dosis
terdapat perbedaan bermakna (p<0,05) pada aktivitas ALT dan AST terhadap kelompok kontrol hepatotoksin dan kelompok kontrol negative (Tabel V dan VI), artinya infusa biji Parinarium glaberimum dosis 5 g/kgBB memiliki kemampuan menurunkan aktivitas ALT
dan AST namun belum mendeikati nilai normal. Presentase efek hepatoprotektif infusa biji Parinarium glaberimum Hassk dosis 5 g/kgBB sebesar 41,69% untuk aktivitas ALT dan
44,7% untuk Aktivitas AST (Tabel IV). Semakin besar persen efek hepatoprotektif maka perlindungan terhadap kerusakan hati juga semakin besar. Dengan demikian dapat disimpulkan bahwa pemberian infusa biji Parinarium glaberimum Hassk dosis 5 g/kgBB mampu memberikan efek hepatoprotektif terhadap tikus jantan terinduksi karbon tetraklorida.
Kelompok pemberian infusa biji Parinarium glaberimum Hassk dosis 10 g/kgBB (kelompok V) menghasilkan aktivitas ALT dan AST secara berturut-turut sebesar 114± 10,33 U/L dan 274,6±19,12 U/L (Tabel IV). Analisis Post Hoc aktivitas ALT dan AST seperti pada Tabel V dan VI, menunjukkan perbedaan bermakna (p<0,05) terhadap kelompok kontrol hepatotoksin dan kelompok kontrol negatif. Berdasarkan hasil tersebut menunjukkan bahwa pemberian infusa biji Parinarium glaberimum Hassk dosis 10 g/kgBB dapat menurunkan aktivitas ALT dan AST namun belum mendekati nilai normal. Presentase efek hepatoprotektif yang didapat sebesar 66,75% untuk aktivitas ALT dan 63,73% untuk aktivitas ALT (tabel IV). Jadi dapat disimpulkan bahwa infusa biji Parinarium glaberimum Hassk dosis 10 g/kgBB memiliki efek hepatoprotektif.
glaberimum Hassk dosis 20 g/kgBB, dapat disimpulkan bahwa pemberian infusa biji Parinarium glaberimum Hassk dengan dosis 20 g/kgBB mampu memberikan perlindungan
optimal terhadap kerusakan hati tikus akibat pejanan karbon tetraklorida karena penurunan aktivitas ALT dan AST mendekati normal dan persen hepatoprotektif yang tinggi yaitu sebesar 83,11% untuk ALT dan 88,4% untuk AST.
Karbon tetraklorida merupakan penyebab kerusakan pada hati tikus yang ditandai dengan meningkatnya kadar enzim ALT dan AST. CCl4 kemudian dimetabolisme menjadi
senyawa radikal bebas •CCl3 yang merusak struktur dan fungsi retikulum endoplasmik
sehingga metabolisme lipid di hati terganggu dan menyebabkan akumulasi lemak pada hati.
Reaksi •CCl3 dengan oksigen akan menghasilkan senyawa radikal Cl3COO• yang juga
bersifat toksik dan semakin memperparah kerusakan pada hati (Timbrell, 2009). Efek hepatoprotektif infusa biji Parinarium glaberimum Hassk dipengaruhi oleh adanya kandungan senyawa polifenol. Berdasarkan penelitian Moniharapon (1998), biji Parinarium glaberimum Hassk mengandung senyawa polifenol. Senyawa polifenol memiliki
kemampuan sebagai antioksidan sehingga berperan dalam menangkap senyawa radikal/reactive oxygen species (ROS) (Widayati, 2012). Reaksi radikal karbon tetraklorida tersebut dapat dihentikan aktivitasnyaa oleh senyawa polifenol dengan cara mendonorkan elektron dari atom hidrogen kepada senyawa radikal •CCl3 dan Cl3COO• sehingga molekulnya memiliki atom yang stabil (tidak reaktif) dan menghambat terjadinya kerusakan hati (Fahrudin et al., 2015).
Parameter untuk mengukur kerusakan hati dalam penelitian ini adalah aktivitas enzim ALT dan AST. Parameter tersebut cukup membuktikan adanya kerusakan hati yang terjadi namun perlu data pendukung seperti data uji histopatologi untuk mengamati perubahan kondisi jaringan hati yang terjadi akibat perlakuan. Oleh karena itu dalam perkembangan penelitian selanjutnya perlu dilakuan uji histopatologi sebagai data pendukung.
KESIMPULAN
SARAN
1. Uji histopatologi hati hewan uji sebagai data pendukung.
2. Uji mengenai mekanisme antioksidan dari kandungan senyawa kimia yang ada pada biji Parinarium glaberimum Hassk.
DAFTAR PUSTAKA
Armansyah, T., Sutriana, A., Aliza, D., Vanda, H., dan Rahmi, E., 2010, Aktivitas Hepatoprotektif Ekstrak Etanol Daun Kucing-kucingan (Acalypha indica L.) pada Tikus Putih (Rattus Novergicus) yang Diinduksi Parasetamol, Jurnal Ilmiah Ilmu-Ilmu Peternakan, 8 (6), 293.
Badan Pengawas Obat dan Makanan RI, 2010, Acuan Sediaan Herbal, Badan POM RI, 5 (1), 3-4.
Badan Pengawas Obat dan Makanan RI, 2014, Persyaratan Mutu Obat Tradisional, Peraturan Kepala Badan POM RI.
Christensen, L.P., dan Christensen, K.B., 2014, Polyphenol in Human Health and Disease, In : The Role of Direct and Indirect Polyphenolic Antioxidants in Protection Against Oxidative Stress, Elsevier Inc., NewYork, 291-294.
Departemen Kesehatan RI, 2007, Pharmaceutical Care Untuk Penyakit Hati, Direktorat Bina Farmasi Komunitas dan Klinik dan Ditjen Bina Kefarmasian dan Alat Kesehatan, Jakarta, 2, 4-9.
Fahrudin, F., Solihin, D.D., Kusumorini, N., dan Ningsih, S., 2015, Efektifitas Esktrak Gambir (Uncaria gambir (Hunter)Roxb.) sebagai Hepatoprotektor pada Tikus (Rattus novergicus L.) yang Diinduksi CCl4, Jurnal Ilmu Kefarmasian Indonesia, 13 (2), 115-122.
Guyton dan Hall, 2016, Text Book of Medical Physiology, 13thEd., Elsevier, Inc., Philadelphia, 881.
Heyne, K., 1987, Tumbuhan Berguna Indonesia, Vol. 4, Koperasi Karyawan Departemen Kehutanan, Jakarta.
Ide, P., 2010, Health Secret of Pepino, PT Elex Media Komputindo, Jakarta, 14-19.
Janakat, S., Al-Merie, H., 2002, Optimization of The Dose and Route of Injection, and Characterization of The Time Course of Carbon Tetrachloride-induced Hepatotoxicity in The Rat, J. Pharm. Tox. Methods, 48, 41-44.
Marinda, F.D., 2014, Hepatoprotective Effect of Curcumin in Chronic Hepatitis, J MAJORITY, 3 (7), 53.
Moniharapon, T., 1998, Kajian Fraksi Bioaktif Dari Buah Atung (Parinarium glaberimum Hassk) Sebagai Bahan Pengawet Pangan, Disertasi, PPs IPB, Bogor.
Panjaitan, R.G.P., Handharyani, E., Chairul, Masriani, Zakiah, Z., dan Manalu, W., 2007, Pengaruh Pemberian Karbon Tetraklodira Terhadap Fungsi Hati dan Ginjal Tikus, Makara Kesehatan, 11 (1), 11-16.
Sumardi, M., dan Wijayahadi, N., 2010, Efek Meniran (Phyllanthus niruri Linn) Terhadap Kadar AST dan ALT Mencit Balb/C yang Diinduksi Asetaminofen, Laporan Akhir Hasil Penelitian Karya Tulis Ilmiah, Program Pendidikan Sarjana Kedokteran Universitas Diponegoro, Semarang, 4.
Tappi, E.S., Lintong, P., dan Loho, L.L., 2013, Gambaran Histopatologi Tikus Wistar yang Diberikan Jus Tomat (Solanum Lycopersum) Pasca Kerusakan Hati Wistar yang Diinduksi Karbon Tetraklorida (CCl4), Jurnal e-Biomedik (eBM), 1(3), 1127.
Timbrell, J.A., 2009, Principles of Biochemical Toxicology, 5th Ed., Informa Healthcare USA, Inc., New York, 309.
Vijayabhaskar, K., Venkateshwarlu, G., Bhaskar, J., Srisailam, K., dan Swapna, M., 2011, Antioxidant and Hepatoprotective Effects of The Methanol Extract of The Flowers of Tamarindus indica, Asian J.Pharm. Tech., 1 (3), 73-78.
Wahyudi, K.T., 2011, Hepatoprotektor Herbal untuk Gangguan Hati, Majalah Cermin Dunia Kedokteran, Edisi 182, 38 (1), 47.
Widayati, E., 2012, Oxidasi Biologi, Radikal Bebas, dan Antioxidant, Jurnal Majalah Ilmiah Sultan Agung, 50 (128), 26-32.
World Health Organization, 2005, Bahaya Bahan Kimia pada Kesehatan Manusia dan Lingkungan, Penerbit Buku Kedokteran EGC, Jakarta, 64-7.
Yuliani, V.S., 2015, Efek Hepatoprotektif Jangka Panjang Infusa Daun Tempuyung (Sonchus arvensis L.) Terhadap Aktivitas Alanin Aminotransferase dan Aspartate Transaminase Pada Tikus Jantan Terinduksi Karbon Tetraklorida, Skripsi, Program Sarjana Universitas Sanata Dharma, Yogyakarta, 43-44.
LAMPIRAN
Lampiran 3. Bahan Uji dan Infusa Biji Parinarium glaberimum Hassk
Pohon Parinarium glaberimum Hassk
Buah Parinarium glaberimum Hassk Simplisia Biji
Parinarium glaberimum Hassk
Serbuk Biji
Parinarium glaberimum Hassk
Infusa Biji
Lampiran 4. Penetapan Kadar Air Serbuk Biji Parinarium glaberimum Hassk
Hasil rata-rata replikasi = ,93 + ,9 + ,
3 = 6,52
Lampiran 7. Analisis Statistik Aktivitas ALT dan AST pada Uji Pendahuluan Waktu Pencuplikan Darah Hewan Uji
Descriptives
Kelompok Statistic Std. Error
ALT Jam ke 0 Mean 47.0000 12.01388
95% Confidence Interval
for Mean
Std. Deviation 20.80865
Minimum 34.00
Maximum 71.00
Range 37.00
Interquartile Range .
Skewness 1.714 1.225
Kurtosis . .
Jam ke 24 Mean 184.0000 34.35598
95% Confidence Interval
for Mean
Std. Deviation 59.50630
Minimum 125.00
Maximum 244.00
Range 119.00
Interquartile Range .
Skewness .076 1.225
Kurtosis . .
Jam ke 48 Mean 44.0000 7.02377
95% Confidence Interval
for Mean
Lower Bound 13.7792
Upper Bound 74.2208
5% Trimmed Mean .
Variance 148.000
Std. Deviation 12.16553
Minimum 36.00
Maximum 58.00
Range 22.00
Interquartile Range .
Skewness 1.680 1.225
Kurtosis . .
One-Sample Kolmogorov-Smirnov Test
ALT
N 9
Normal Parametersa,b Mean 91.6667
Std. Deviation 76.33970
Most Extreme Differences Absolute .273
Positive .273
Negative -.225
Test Statistic .273
Asymp. Sig. (2-tailed) .051c
a. Test distribution is Normal.
b. Calculated from data.
c. Lilliefors Significance Correction.
Test of Homogeneity of Variances
ALT
Within Groups 8244.000 6 1374.000
Multiple Comparisons
Dependent Variable: ALT
LSD
(I) Kelompok (J) Kelompok
Mean
Difference (I-J) Std. Error Sig.
95% Confidence Interval
Lower Bound Upper Bound
Jam ke 0 Jam ke 24 -137.00000* 30.26549 .004 -211.0570 -62.9430
*. The mean difference is significant at the 0.05 level.
Descriptives
Kelompok Statistic Std. Error
AST Jam ke 0 Mean 121.6667 18.98537
95% Confidence Interval
for Mean
95% Confidence Interval
Minimum 247.00
95% Confidence Interval
for Mean
Normal Parametersa,b Mean 177.7778
Std. Deviation 85.91097
Most Extreme Differences Absolute .254
Positive .254
Negative -.174
Test Statistic .254
Asymp. Sig. (2-tailed) .096c
a. Test distribution is Normal.
b. Calculated from data.
Test of Homogeneity of Variances
Within Groups 6956.000 6 1159.333
Total 59045.556 8
Multiple Comparisons
Dependent Variable: AST
LSD
(I) Kelompok (J) Kelompok
Mean
Difference (I-J) Std. Error Sig.
95% Confidence Interval
Lower Bound Upper Bound
Jam ke 0 Jam ke 24 -163.66667* 27.80088 .001 -231.6930 -95.6404
*. The mean difference is significant at the 0.05 level.
Lampiran 8. Analisis Statistik Aktivitas ALT dan AST pada Uji Pendahuluan Penetapan Dosis Infusa Biji Parinarium glaberimum Hassk
Descriptives
Kelompok Statistic Std. Error
ALT Kontrol Hepatotoksin Mean 207.6667 25.30042
95% Confidence Interval
for Mean
Kontrol Negatif Mean 41.6667 3.48010
95% Confidence Interval
for Mean
Kontrol Infusa Mean 57.0000 3.60555
95% Confidence Interval
for Mean
Lower Bound 41.4866
Upper Bound 72.5134
Median 55.0000
Perlakuan Dosis 5 g/kgBB Mean 181.6667 39.87202
95% Confidence Interval
for Mean
95% Confidence Interval
Perlakuan Dosis 20
g/kgBB
Mean 79.3333 12.33333
95% Confidence Interval
for Mean
Normal Parametersa,b Mean 118.2222
Std. Deviation 71.13579
Most Extreme Differences Absolute .166
Positive .166
Negative -.124
Test Statistic .166
Asymp. Sig. (2-tailed) .200c,d
a. Test distribution is Normal.
b. Calculated from data.
c. Lilliefors Significance Correction.
d. This is a lower bound of the true significance.
Test of Homogeneity of Variances
ALT
Levene Statistic df1 df2 Sig.
ANOVA
ALT
Sum of Squares df Mean Square F Sig.
Between Groups 71136.444 5 14227.289 11.467 .000
Within Groups 14888.667 12 1240.722
Total 86025.111 17
Multiple Comparisons
Dependent Variable: ALT
LSD
(I) Kelompok (J) Kelompok
Mean
Kontrol Negatif 166.00000* 28.76018 .000 103.3369 228.6631
Kontrol Infusa 150.66667* 28.76018 .000 88.0036 213.3297
Perlakuan Dosis 5
Kontrol Infusa -15.33333 28.76018 .604 -77.9964 47.3297
Perlakuan Dosis 5
Kontrol Negatif 15.33333 28.76018 .604 -47.3297 77.9964
Perlakuan Dosis 20
Hepatotoksin -26.00000 28.76018 .384 -88.6631 36.6631
Kontrol Negatif 140.00000* 28.76018 .000 77.3369 202.6631
Kontrol Infusa 124.66667* 28.76018 .001 62.0036 187.3297
Perlakuan Dosis 10
Kontrol Negatif 100.33333* 28.76018 .004 37.6703 162.9964
Kontrol Infusa 85.00000* 28.76018 .012 22.3369 147.6631
Perlakuan Dosis 5
Kontrol Negatif 37.66667 28.76018 .215 -24.9964 100.3297
Kontrol Infusa 22.33333 28.76018 .452 -40.3297 84.9964
Perlakuan Dosis 5
*. The mean difference is significant at the 0.05 level.
Descriptives
Kelompok Statistic Std. Error
AST Kontrol Hepatotoksin Mean 587.6667 61.17007
95% Confidence Interval
Std. Deviation 105.94967
Kontrol Negatif Mean 128.0000 17.78576
95% Confidence Interval
for Mean
Kontrol Infusa Mean 131.0000 5.03322
95% Confidence Interval
for Mean
Perlakuan Dosis 5 g/kgBB Mean 536.6667 65.68951
95% Confidence Interval
Mean 290.6667 33.82471
95% Confidence Interval
for Mean
Mean 202.0000 37.89899
95% Confidence Interval
Interquartile Range .
Skewness .341 1.225
Kurtosis . .
One-Sample Kolmogorov-Smirnov Test
AST
N 18
Normal Parametersa,b Mean 312.6667
Std. Deviation 200.40899
Most Extreme Differences Absolute .195
Positive .195
Negative -.144
Test Statistic .195
Asymp. Sig. (2-tailed) .068c
a. Test distribution is Normal.
b. Calculated from data.
c. Lilliefors Significance Correction.
Test of Homogeneity of Variances
AST
Levene Statistic df1 df2 Sig.
2.965 5 12 .057
ANOVA
AST
Sum of Squares df Mean Square F Sig.
Between Groups 616910.000 5 123382.000 22.476 .000
Within Groups 65874.000 12 5489.500
Multiple Comparisons
Dependent Variable: AST
LSD
(I) Kelompok (J) Kelompok
Mean
Kontrol Negatif 459.66667* 60.49518 .000 327.8590 591.4743
Kontrol Infusa 456.66667* 60.49518 .000 324.8590 588.4743
Perlakuan Dosis 5
Kontrol Infusa -3.00000 60.49518 .961 -134.8077 128.8077
Perlakuan Dosis 5
Kontrol Negatif 3.00000 60.49518 .961 -128.8077 134.8077
Perlakuan Dosis 5
Hepatotoksin -51.00000 60.49518 .416 -182.8077 80.8077
Kontrol Negatif 408.66667* 60.49518 .000 276.8590 540.4743
Perlakuan Dosis 10
Kontrol Negatif 162.66667* 60.49518 .020 30.8590 294.4743
Kontrol Infusa 159.66667* 60.49518 .022 27.8590 291.4743
Kontrol Negatif 74.00000 60.49518 .245 -57.8077 205.8077
Kontrol Infusa 71.00000 60.49518 .263 -60.8077 202.8077
Perlakuan Dosis 5
g/kgBB -334.66667
* 60.49518 .000 -466.4743 -202.8590
Perlakuan Dosis 10
g/kgBB -88.66667 60.49518 .168 -220.4743 43.1410
Lampiran 9. Purata dan Hasil Uji Post-Hoc Data ALT & AST Uji Pendahuluan Penetapan Dosis Infusa Biji Parinarium glaberimum Hassk
Kelompok Purata aktivitas ALT ±SE (U/L) Purata Aktivitas AST ±SE (U/L)
I : Kelompok kontrol hepatotoksin (karbon tetraklorida 2 mL/kgBB) II : Kelompok kontrol negatif (olive oil 2 mL/kgBB)
III : Kelompok kontrol infusa biji Parinarium glaberimum Hassk (20 g/kgBB) IV : Kelompok perlakuan dosis 5 g/kgBB + CCl4 2 mL/kgBB
V : Kelompok perlakuan dosis 10 g/kgBB + CCl4 2 mL/kgBB VI : Kelompok perlakuan dosis 20 g/kgBB + CCl4 2 mL/kgBB SE : Standar Eror
Hasil uji Post-Hoc aktivitas ALT pada semua kelompok perlakuan
Kelompok I II III IV V VI
BB = Berbeda bermakna (p<0,05) ; BTB = Berbeda tidak bermakna (p>0,05)
Hasil uji Post-Hoc aktivitas AST pada semua kelompok perlakuan
Kelompok I II III IV V VI
Lampiran 10. Analisis Statistik Data Perlakuan
Descriptives
Kelompok Statistic Std. Error
ALT Kontrol Hepatotoksin Mean 269.0000 21.60555
95% Confidence Interval for Mean
Lower Bound 209.0134
Upper Bound 328.9866
5% Trimmed Mean 268.7778
Median 244.0000
Kontrol Negatif Mean 36.8000 3.24654
95% Confidence Interval
for Mean
Lower Bound 27.7862
Upper Bound 45.8138
5% Trimmed Mean 36.7222
Median 38.0000
Kontrol Infusa Mean 55.4000 1.96469
95% Confidence Interval
for Mean
Lower Bound 49.9452
Upper Bound 60.8548
5% Trimmed Mean 55.1667
Median 54.0000
Std. Deviation 4.39318
Perlakuan Dosis 5 g/KgBB Mean 172.2000 19.09293
95% Confidence Interval
for Mean
Lower Bound 119.1895
Upper Bound 225.2105
5% Trimmed Mean 172.5000
Median 170.0000
Mean 114.0000 10.33925
95% Confidence Interval
for Mean
Lower Bound 85.2937
Upper Bound 142.7063
5% Trimmed Mean 113.3333
95% Confidence Interval
for Mean
Upper Bound
109.0968
5% Trimmed Mean 75.1667
Median 80.0000
Normal Parametersa,b Mean 120.5667
Std. Deviation 85.47058
Most Extreme Differences Absolute .155
Positive .155
Negative -.142
Test Statistic .155
Asymp. Sig. (2-tailed) .065c
a. Test distribution is Normal.
b. Calculated from data.
c. Lilliefors Significance Correction.
Test of Homogeneity of Variances
ALT
Levene Statistic df1 df2 Sig.
ANOVA
ALT
Sum of Squares df Mean Square F Sig.
Between Groups 189956.567 5 37991.313 41.644 .000
Within Groups 21894.800 24 912.283
Total 211851.367 29
Multiple Comparisons
Dependent Variable: ALT
LSD
(I) Kelompok (J) Kelompok
Mean
Kontrol Negatif 232.20000* 19.10270 .000 192.7740 271.6260
Kontrol Infusa 213.60000* 19.10270 .000 174.1740 253.0260
Perlakuan Dosis
Kontrol Infusa -18.60000 19.10270 .340 -58.0260 20.8260
Perlakuan Dosis
Kontrol Negatif 18.60000 19.10270 .340 -20.8260 58.0260
Perlakuan Dosis
5 g/KgBB -116.80000
Perlakuan Dosis
Kontrol Negatif 135.40000* 19.10270 .000 95.9740 174.8260
Kontrol Infusa 116.80000* 19.10270 .000 77.3740 156.2260
Perlakuan Dosis
Kontrol Negatif 77.20000* 19.10270 .000 37.7740 116.6260
Kontrol Infusa 58.60000* 19.10270 .005 19.1740 98.0260
Perlakuan Dosis
Kontrol Negatif 39.20000 19.10270 .051 -.2260 78.6260
Kontrol Infusa 20.60000 19.10270 .292 -18.8260 60.0260
Perlakuan Dosis
5 g/KgBB -96.20000
* 19.10270 .000 -135.6260 -56.7740
Perlakuan Dosis
10 g/KgBB -38.00000 19.10270 .058 -77.4260 1.4260
*. The mean difference is significant at the 0.05 level.
Descriptives
Mean 566.0000 48.27629
95% Confidence Interval for
Mean
Lower Bound 431.9635
Upper Bound 700.0365
Median 491.0000
Kontrol Negatif Mean 108.8000 15.26237
95% Confidence Interval for
Mean
Lower Bound 66.4249
Upper Bound 151.1751
5% Trimmed Mean 108.0556
Median 97.0000
Kontrol Infusa Mean 117.4000 9.59479
95% Confidence Interval for
Mean
Lower Bound 90.7606
Upper Bound 144.0394
5% Trimmed Mean 118.6667
Perlakuan Dosis 5
g/KgBB
Mean 361.6000 63.52527
95% Confidence Interval for
Mean
Lower Bound 185.2256
Upper Bound 537.9744
5% Trimmed Mean 362.0000
Median 411.0000
Mean 274.6000 19.12747
95% Confidence Interval for
Mean
Lower Bound 221.4936
Upper Bound 327.7064
5% Trimmed Mean 273.3889
Median 267.0000
Mean 161.8000 30.97644
95% Confidence Interval for
Mean
Lower Bound 75.7956
Upper Bound 247.8044
5% Trimmed Mean 159.1667
Median 139.0000
Variance 4797.700
Std. Deviation 69.26543
Minimum 101.00
Range 169.00
Normal Parametersa,b Mean 265.0333
Std. Deviation 180.48068
Most Extreme Differences Absolute .158
Positive .158
Negative -.140
Test Statistic .158
Asymp. Sig. (2-tailed) .056c
a. Test distribution is Normal.
b. Calculated from data.
c. Lilliefors Significance Correction.
Test of Homogeneity of Variances
AST
Between Groups 784295.767 5 156859.153 23.481 .000
Within Groups 160329.200 24 6680.383
Multiple Comparisons
Dependent Variable: AST
LSD
(I) Kelompok (J) Kelompok
Mean Difference
Kontrol Negatif 457.20000* 51.69288 .000 350.5111 563.8889
Kontrol Infusa 448.60000* 51.69288 .000 341.9111 555.2889
Perlakuan Dosis
Kontrol Infusa -8.60000 51.69288 .869 -115.2889 98.0889
Perlakuan Dosis
Kontrol Negatif 8.60000 51.69288 .869 -98.0889 115.2889
Perlakuan Dosis
Kontrol Negatif 252.80000* 51.69288 .000 146.1111 359.4889
Perlakuan Dosis
Kontrol Negatif 165.80000* 51.69288 .004 59.1111 272.4889
Kontrol Infusa 157.20000* 51.69288 .006 50.5111 263.8889
Perlakuan Dosis
Kontrol Negatif 53.00000 51.69288 .315 -53.6889 159.6889
Kontrol Infusa 44.40000 51.69288 .399 -62.2889 151.0889
Perlakuan Dosis
Lampiran 11. Perhitungan Persen Hepatoprotektif
Rumus yang digunakan untuk menghitung persen hepatoprotektif adalah sebagai berikut : }x 100%
}x 100%
(Vijayabhaskar et al., 2011)
1. ALT
}x 100% % hepatoprotektif kelompok IV = {1- } x 100% = 41,69% % hepatoprotektif kelompok V = {1- } x 100% = 66,75% % hepatoprotektif kelompok VI = {1- x 100% = 83,11%
2. AST
}x 100% % hepatoprotektif kelompok IV = {1- } x 100% = 44,7% % hepatoprotektif kelompok V = {1- } x 100% = 63,73% % hepatoprotektif kelompok VI = {1- } x 100% = 88,4%
Lampiran 12. Perhitungan Konversi Dosis Infusa Biji Parinarium glaberimum Hassk untuk Manusia
Nilai konversi tikus 200 g ke manusia 70 kg = 56
Dosis untuk manusia 70 kg = dosis tikus 200 g x nilai koversi Dosis infusa biji Parinarium glaberimum Hassk :
1. Infusa biji Parinarium glaberimum Hassk dosis 5 g/kgBB 5 g/kgBB = 5 g/1000gBB = 1 g/200gBB
1 g/200gBB x 56 = 56 g/70kgBB manusia
2. Infusa biji Parinarium glaberimum Hassk dosis 10 g/kgBB 10 g/kgBB = 10 g/1000gBB = 2 g/200gBB
2 g/200gBB x 56 = 102 g/70kgBB manusia
3. Infusa biji Parinarium glaberimum Hassk dosis 20 g/kgBB 20 g/kgBB = 20 g/1000gBB = 4 g/200gBB
4 g/200gBB x 56 = 204 g/70kgBB manusia
BIOGRAFI PENULIS