ABSTRAK
Tanaman Lada (Piper nigrum L.) termasuk dalam famili Piperaceae yang diketahui memiliki kandungang kimia yaitu Flavonoid yang termasuk dalam golongan senyawa polifenol. Polifenol merupakan senyawa utama yang paling banyak terdapat pada tanaman, yang memiliki potensi sebagai antioksidan. Tujuan dari penelitian ini adalah untuk mengetahui seberapa besar kandungan fenolik total dan aktivitas antioksidan yang terdapat dalam fraksi etil asetat ekstrak metanol daun lada (Piper nigrum L.). Penetapan kangungan fenolik total dilakukan dengan metode Folin-Ciocalteu, sedangkan untuk pengukuran aktivitas antioksidan dilakukan dengan metode Ferric Thiocyanate (FTC) dan Thiobarbituric Acid (TBA) dengan menggunakan BHT (butylated hydroxy toluene). Jumlah peroksida pada tahap awal peroksidasi lemak diukur dengan metode FTC, sedangkan jumlah peroksida pada tahap kedua diukur dengan metode TBA. Hasil penelitian menunjukan bahwa fraksi etil asetat ekstrak metanol daun lada mempunyai kandungan fenolik total sebesar 133,83 ± 5,4365 mg ekivalen asam galat. Aktivitas antioksidan fraksi etil asetat ekstrak metanol daun lada dengan metode FTC dan TBA secara berturut-turut sebesar (5,061 ± 0,598)%, dan (93,19 ± 2,245)%.
ABSTRACT
Pepper is a plant in piperaceae family which has been known to have phytochemical content such as flavonoid included in the polyphenol group. Polyphenol is the most numerous main compound in plant which have a potential as antioxdant. The aim of this research were to measure total phenolic content and antioxidant activity in ethyl acetate fraction of methanol exstract of pepper leaves (Piper nigrum L.) total phenolic content were measured by Folin-Ciocalteu method mean while antioxidant activity were measured by ferric thiocyanat (FTC) method and thiobarbituric acid (TBA) using BHT (butylated hydroxy toluene. Peroxide amount in the first stage of lipid peroxidation were measured by FTC method, meanwhile ferric-thiocyanate complex reaction and to measure peroxide amount in the secound stage of lipid peroxidation were measured by TBA metho. The result showed that ethyl acetate fraction of methanol exstract of pepper leaves has a total phenolic content of 133,83 ± 5,4365 mg gallic acid equivalents (GAE). Antioxidant activity of ethyl acetate fraction of methanol exstract of pepper leaves showed as percent inhibition value was (5,061 ± 0,598)%, and (93,19 ± 2,245)% for FTC and TBA method respectively.
PENETAPAN KANDUNGAN FENOLIK TOTAL DAN UJI AKTIVITAS ANTIOKSIDAN FRAKSI ETIL ASETAT EKSTRAK METANOL
DAUN LADA (Piper nigrum L.)
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Yuliana Rati Kamara Dewi NIM: 128114017
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
i
PENETAPAN KANDUNGAN FENOLIK TOTAL DAN UJI AKTIVITAS ANTIOKSIDAN FRAKSI ETIL ASETAT EKSTRAK METANOL
DAUN LADA (Piper nigrum L.)
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Farmasi
Oleh:
Yuliana Rati Kamara Dewi NIM: 128114017
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
vi
HALAMAN PERSEMBAHAN Dear God,
Thank you for creating such a magical piece Known as a “smile”. It’s indescribable, the feeling when someone smiles at you sincerely, and their eyes
sparkle as they do so. No matter how close, no matter how much of a stranger, a
sincere smile just melts the heart.
Dear God,
Thank you for creating another magical piece known as a “cry”. The feeling of seeing someone cry warms my heart, because it simply shows how
fragile and connected we all are. And, the feeling when i my self cry, it brings
relief and appreciation to life.
Dear God,
I enjoy talking to You
~Dian Rikasari~
Ku persembahkan karya ini untuk:
Tuhan Yesus Kristus, Bunda Maria
Papa Kolai, Mama Emma, dan Kakak ku tercinta Maria
Semua keluarga besar serta para sahabat yang selalu mendukung & medoakan ku
He has made everything beautiful in it’s time.
vii PRAKATA
Puji dan syukur kehadirat Tuhan Yang Maha Esa atas berkat dan rahmat-Nya serta segenap kasih-rahmat-Nya sehingga penulis dapat menyelesaikan skripsi
dengan baik yang berjudul “Penetapan Kandungan Fenolik Total dan Uji
Aktivitas Antioksidan Fraksi Etil Asetat Ekstrak Metanol Daun Lada (Piper nigrum L.)”. Skripsi ini disusun untuk memenuhi salah satu syarat untuk memperoleh gelar Sarjana Strata Satu (S1) Program Studi Farmasi (S.Farm) di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Dalam proses penyusunan skripsi ini penulis banyak mendapat bantuan dan bimbingan dari berbagai pihak, sehingga penulis ingin mengucapkan terima kasih kepada:
1. Dr. Yustina Sri Hartini, M.Si., Apt. sebagai Dosen Pembimbing yang telah memberikan bimbingan, pengarahan, serta ilmu dalam penelitian dan penyusunan skripsi ini.
2. Yohanes Dwiatmaka, M.Si. sebagai Dosen Penguji atas masukan, kritik, saran dan kesediaannya menguji skripsi ini.
3. Dr. Erna Tri Wulandari, M.Si., Apt. sebagai Dosen Penguji atas masukan, kritik, saran dan kesediaannya menguji skripsi ini.
4. Aris Widayati, M.Si., Ph.D., Apt. sebagai Dekan Fakultas Farmasi Universitas Sanata Dharma.
5. Agustina Setiawati, M.Sc., Apt. sebagai Kepala Penanggung Jawab Laboratorium Fakultas Farmasi Universitas Sanata Dharma atas izin penggunaan laboratorium yang diberikan kepada penulis.
6. Segenap laboran dan karyawan Fakultas Farmasi Universitas Sanata Dharma, khususnya Pak Wagiran, Mas Bimo, Pak Parlan, Mas Sigit, Mas Agung, dan Pak Ketul atas bantuan dan kerjasamanya selama ini.
viii
menyerah dan selalu menyertakan Tuhan Yesus Kristus dan Bunda Maria dalam menjalani segala sesuatu.
8. Sepupu-sepupuku tercinta Gita, Andri, Kori, Tuti,Yuyun, Titin, Sari, Fran dan segenap keluarga besar yang tidak bisa saya sebutkan satu per satu atas dukungan dan doanya.
9. Teman-teman skripsi payung piperaceae, Violeta Jesmile, Maria Indah Rosari, Agatha Herny Sekar Natalia, dan Clementia Nova, terimakasih atas suka, duka dan kerjasmanya yang telah dilewati bersama selama penelitian ini.
10.Sahabat penulis: Violeta, Hossianna Yosi Agustina, Elisabeth Sarci Fitriwati Enny, Fransisca Melani, Monika Meitasari Astuti, Dewi Anugrah Fitriani, Indah, Agtha yang selalu menjadi tempat berbagi suka dan duka, selalu memberikan dukungan dan semangat. Terima kasih atas kebersamannnya selama ini, senang bisa mengenal kalian.
11.Teman-teman KKN reguler kelompok 32: Agustinus Bambang Satria Utama, Lucia Ida Ayu Kristiana, Kurnia Novariany, terima kasih atas dinamika, tawa, canda dan persahabatannya selama KKN sampai KKN berakhir. Bisa bertemu dan mengenal kalian adalah salah satu anugerah terindah dalam hidupku. 12. Teman-teman kost Amakus: Kak Ita, Kak seruni, Kak Herta, Kak Nita, Kak
Intan, Kak Dewi, Kak Geka, Eni, Esthy, Friesca, Ratri, Indah, Herlina, Karina, Penina, Chyntia, Valent terima kasih atas kebersamaannya selama ini. 13.Teman-teman angkatan 2012 yang luar biasa, khususnya FSM A dan FKK A 2012 yang telah memberikan semangat dan dukungan bagi penulis, terima kasih atas kebersamaannya.
14.Semua pihak yang turut membantu dalam penyusunan skripsi ini yang tidak dapat disebutkan satu persatu.
ix
Yogyakarta, ……Juni 2016
x DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
PERNYATAAN KEASLIAN KARYA ... iv
PERSETUJUAN PUBLIKASI ... v
HALAMAN PERSEMBAHAN ... vi
PRAKATA ... vii
DAFTAR ISI ... x
DAFTAR TABEL ... xi
DAFTAR GAMBAR ... xii
DAFTAR LAMPIRAN ... xii
ABSTRAK ... xiv
ABSTRACT ... xv
PENDAHULUAN ... 1
METODE PENELITIAN ... 2
HASIL DAN PEMBAHASAN ... 6
KESEMPULAN DAN SARAN ... 13
DAFTAR PUSTAKA ... 14
xi Daftar Tabel
Halaman Tabel I. Hasil pengukuran absorbansi kurva baku asam
galat replikasi 3 ... ... 8 Tabel II. Hasil penetapan kandungan fenolik total fraksi etil asetat
daun Lada ... 9 Tabel III. Perhitungan persen inhibisi berdasarkan
absorbansi hari ke-6 ... 11 Tabel IV. Aktivitas antioksidan sampel (Fraksi Etil Asetat Ekstrak
xii
Daftar Gambar
Halaman
Gambar 1. Reaksi Reagen Folin-Ciocalteu Dengan ... Senyawa Fenol ... 8 Gambar 2. Reaksi Pembentukan Kompleks Fe3+-Tiosianat dari
Kompleks Fe2+ Tiosianat oleh Hiperoksida ... 9
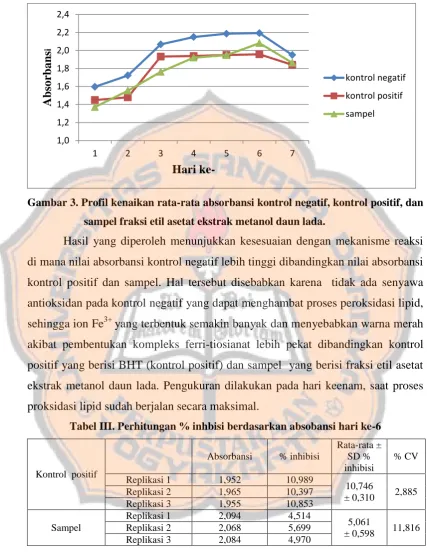
Gambar 3. Profil Kenaikan Rata-Rata Absorbansi Kontrol Negatif Kontrol Positif, dan Sampel Fraksi Etil Asetat Ekstrak
xiii
Daftar Lampiran
Halaman
Lampiran 1. Surat Determinasi Tanaman ... 17
Lampiran 2. Klasifikasi Tanaman Lada ... 18
Lampiran 3. Perhitungan Penetapan Kadar Air ... 18
Lampiran 4. Perhitungan Rendemen Ekstrak dan Fraksi ... 19
Lampiran 5. Data Penimbangan Untuk Kandungan Fenolik Total ... 19
Lampiran 6. Data Perhitungan Konsentrasi Asam GalatDan Fraksi Etil Asetat Untuk Penetapan Kandungan Fenolik Total ... 20
Lampiran 7. Hasil Optimasi Operating Time Untuk Penetapan Kandungan Fenolik Total ... 22
Lampiran 8. Optimasi Panjang Gelombang Maksimum Untuk Kandungan Fenolik Total ... 23
Lampiran 9. Hasil Pengukuran Kurva Baku Untuk Penetapan Kandungan Fenolik Total ... 26
Lampiran 10. Perhitungan Kandungan Fenolik Total Fraksi Etil Asetat ... 27
Lampiran 11. Data Penimbangan untuk Uji Aktivitas Antioksidan Metode FTC-TBA ... 28
Lampiran 12. Optimasi Metode Uji Aktivitas Antioksidan FTC-TBA ... 29
Lampiran 13. Perhitungan Persen Inhibisi Uji Aktivitas Antioksidan Metode FTC-TBA ... 33
Lampiran 14. Hasil Pengukuran Uji Aktivitas Antioksidan Dengan Metode TBA ... 35
xiv ABSTRAK
Tanaman Lada (Piper nigrum L.) termasuk dalam famili Piperaceae yang diketahui memiliki kandungang kimia yaitu Flavonoid yang termasuk dalam golongan senyawa polifenol. Polifenol merupakan senyawa utama yang paling banyak terdapat pada tanaman, yang memiliki potensi sebagai antioksidan. Tujuan dari penelitian ini adalah untuk mengetahui seberapa besar kandungan fenolik total dan aktivitas antioksidan yang terdapat dalam fraksi etil asetat ekstrak metanol daun lada (Piper nigrum L.). Penetapan kangungan fenolik total dilakukan dengan metode Folin-Ciocalteu, sedangkan untuk pengukuran aktivitas antioksidan dilakukan dengan metode Ferric Thiocyanate (FTC) dan Thiobarbituric Acid (TBA) dengan menggunakan BHT (butylated hydroxy toluene). Jumlah peroksida pada tahap awal peroksidasi lemak diukur dengan metode FTC, sedangkan jumlah peroksida pada tahap kedua diukur dengan metode TBA. Hasil penelitian menunjukan bahwa fraksi etil asetat ekstrak metanol daun lada mempunyai kandungan fenolik total sebesar 133,83 ± 5,4365 mg ekivalen asam galat. Aktivitas antioksidan fraksi etil asetat ekstrak metanol daun lada dengan metode FTC dan TBA secara berturut-turut sebesar (5,061 ± 0,598)%, dan (93,19 ± 2,245)%.
xv ABSTRACT
Pepper is a plant in piperaceae family which has been known to have phytochemical content such as flavonoid included in the polyphenol group. Polyphenol is the most numerous main compound in plant which have a potential as antioxdant. The aim of this research were to measure total phenolic content and antioxidant activity in ethyl acetate fraction of methanol exstract of pepper leaves (Piper nigrum L.) total phenolic content were measured by Folin-Ciocalteu method mean while antioxidant activity were measured by ferric thiocyanat (FTC) method and thiobarbituric acid (TBA) using BHT (butylated hydroxy toluene. Peroxide amount in the first stage of lipid peroxidation were measured by FTC method, meanwhile ferric-thiocyanate complex reaction and to measure peroxide amount in the secound stage of lipid peroxidation were measured by TBA metho. The result showed that ethyl acetate fraction of methanol exstract of pepper leaves has a total phenolic content of 133,83 ± 5,4365 mg gallic acid equivalents (GAE). Antioxidant activity of ethyl acetate fraction of methanol exstract of pepper leaves showed as percent inhibition value was (5,061 ± 0,598)%, and (93,19 ± 2,245)% for FTC and TBA method respectively.
1 1. Pendahuluan
Berbagai penyakit dalam tubuh disebabkan oleh adanya radikal bebas. Radikal bebas merupakan molekul berbasis oksigen atau nitrogen dengan elektron tidak berpasangan yang umumnya dihasilkan di dalam tubuh pada saat proses metabolisme. Radikal bebas yang berlebihan dapat mengakibatkan penyakit-penyakit degeneratif seperti diabetes, penyakit-penyakit jantung dan kanker (Winarsi, 2011).
Antioksidan merupakan suatu senyawa yang dapat melindungi kerusakan sel karena mampu menetralkan radikal bebas dengan mekanisme mendonorkan atom hidrogen ke atom yang tidak memiliki pasangan elektron (Muhtadi, 2014.)
Senyawa fenolik dari tanaman obat memiliki berbagai bioaktivitas yang memainkan peran penting dalam pencegahan kanker. Bioaktvitas dari senyawa fenolik memiliki efek misalnya, antioksidan, anti kanker, antimutagenik dan anti inflamasi (Huang dan Cai, 2010). Senyawa fenolik berfungsi sebagai antioksidan karena senyawa fenolik dapat bereaksi dengan reactive oxygen species (ROS) dan menghilangkan aktivitas radikalnya sehingga tidak berbahaya lagi terhadap sel tubuh manusia (Sochor et al., 2010).
Rempah-rempah dan tanaman herbal merupakan salah satu sumber antioksidan alami dan memiliki peran penting dalam pencegahan penyakit kanker dan penuaan dini. Salah satu famili tanaman yang telah diketahui menunjukkan potensi yang besar sebagai antioksidan adalah Piperaceae (Dodson, et al., 2000). Piper nigrum atau biasa disebut lada merupakan salah satu tanaman dalam famili
piperaceae. . Pada penelitian yang dilakukan oleh Nahak dan Sahu (2011) daun
lada diketahui memiliki kandungan kimia seperti: alkaloid, glikosida, terpenoid, steroid, flavonoid, tanin, gula pereduksi, dan antrakuinon. Flavonoid termasuk dalam golongan senyawa polifenol. Polifenol merupakan senyawa utama yang paling banyak terdapat pada tanaman, yang memiliki aktivitas antioksidan.
2
lada dapat terambil secara optimal (Andersen dan Markham, 2006). Sedangkan pemilihan ekstrak metanol didasarkan pada penelitian Cowan (1999) yang menyatakan bahwa metanol dapat menarik lebih banyak senyawa metabolit dibandingkan dengan air, etanol, klorofrom, diklorometanol, eter dan aseton.
Berdasarkan latar belakang tersebut, maka dalam penelitian ini ingin mengetahui seberapa besar aktivitas antioksidan dari daun lada (Piper nigrum L.) dengan menggunakan metode Ferric Thiocyanate (FTC) dan Thiobarbituric Acid (TBA). Untuk mendukung hasil aktivitas antioksidan yang didapat maka pada penelitian ini dilakukan penentuan jumlah fenolik total untuk mempresentasikan jumlah fenolik yang menyebabkan aktivitas antioksidan.
2. Metode penelitian A. Alat dan Bahan
Bahan yang digunakan dalam penelitian ini adalah: Daun lada segar yang diperoleh dari kebun obat “MERAPI FARMA” daerah KM 21,5, Kaliurang, Cangkringan, Sleman, Yogyakarta. Akuades, metanol teknis,metanol p.a 99,6%, etanol p.a 99,6 %, etanol 75%, etil asetat p.a, buffer fosfat 0,05m (pH7), asam galat p.a (sigma), reagen Folin-Ciocalteu, larutan Na2CO3 1 M, amonium tiosianat
30%, FeCl3 0,02 M, asam linoleat 2,5% (sigma), larutan asam trikloroasetat (TCA
10%), larutan tiobarbitarat 0,67%, dan BHT (butylated hydroxy toluene) p.a (Sigma).
3 B. Persiapan sampel
1. Pembuatan simplisa
Tanaman lada diperoleh dari kebun obat “MERAPI FARMA” daerah KM 21,5, Kaliurang, Cangkringan, Sleman, Yogyakarta. Pengumpulan dilakukan pada bulan maret 2016. Determinasi tanaman Lada dilakukan di Laboratorium Taksonomi Tumbuhan Fakultas Biologi Universitas Gadjah Mada Yogyakarta. Determinasi tanaman lada ini untuk memastikan bahwa tumbuhan yang digunakan untuk penelitian benar-benar tumbuhan lada. Daun lada dicuci dengan cara dialiri dengan air mengalir sambil dibersihkan kotoran yang melekat pada daun. Pencucian dilakukan sebanyak tiga kali, agar daun lada bersih dari pengotor. Daun lada dirajang dengan ukuran seragam kurang lebih 1 cm. Daun lada yang masih basah kemudian dikeringkan menggunakan oven dengan suhu 60o C. Daun lada yang telah kering ditunjukan dengan mudah hancurnya daun ketika diremas. Setelah itu, daun lada kering dipisahkan dari bahan-bahan pengotor yang ikut serta selama proses pengeringan. Daun lada dibuat menjadi serbuk dengan blender, kemudian dilakukan pengayakan dengan ayakan nomor mesh 50, kemudian dilakukan uji kadar air dan dilakukan perhitungan rendemen ekstrak. Serbuk daun lada yang telah diperoleh kemudian disimpan dengan cara membungkus serbuk menggunakan wadah kedap udara. Penyimpanan serbuk daun lada dilakukan pada suhu ruangan.
2. Pembutan ekstrak metanol daun lada (Piper nigrum L.)
Pembuatan ekstrak metanol lada mengacu pada jurnal penelitian Artini et al., (2013) sebanyak 31,509 g serbuk simplisia daun Lada ditimbang, kemudian
4
menggunakan vacuum rotary evaporator pada suhu 400C. Kemudian diuapkan kembali dengan menggunakan water bath ada suhu 40 0C untuk diperoleh ekstrak kental yang bebas dari penyari yang diketahui melalui selisih antar penimbangan ekstrak pertama dan penimbangan kedua sebesar 0,0005.
3. Pembuatan fraksi etil asetat ekstrak metanol Daun Lada
Ekstrak kental yang diperoleh difraksinasi menggunakan metode cair-cair. Ekstrak kental dilarutkan dalam akuades hangat, kemudian difraksinasi menggunakan etil asetat dengan perbandingan akuades : etil asetat 1:1 v/v didalam corong pisah. Terbentuk dua lapisan, yaitu lapisan air dan lapisan etil asetat. Lapisan etil asetat (bagian atas) kemudian diambil dan ditampung dalam wadah. Lapisan air (bagian bawah) difraksinasi kembali menggunakan etil asetat dengan perbandingan yang sama. Tahapan ini diulang hingga fraksi jernih. Fraksi etil asetat kemudian dipekatkan menggunakan vaccum rotary evaporator pada suhu 770C yang merupakan titik didih dari etil asetat. Fraksi etil asetat pekat kemudian dikeringkan menggunakan waterbath. Fraksi etil asetat yang diperoleh kemudian di simpan dalam desikator.
C. Penetapan kandungan fenolik total.
Larutan sampel dibuat dengan menimbang fraksi eti asetat ekstrak metanol daun lada sebanyak 10 mg kemudian dilarutkan dalam 10 mL metanol:air (1:1) sehingga didapatkan konsentrasi larutan stok 1 mg/mL. Kemudian dibuat larutan intermedietdengan konsentrasi 200 µg/mL. Sebanyak 0,5 mL larutan intermediet dengan konsentrasi 200 µg/mL. Sebanyak 0,5 mL larutan intermediet dicampur dengan 2 mL reagen Folin-Ciocalteu dan diinkubasi selama 5 menit. Selanjutnya ditambahkan 4 ml larutan Na2CO3 1 M kemudian didiamkan selama operating time yang telah ditentukan sebelumnya yaitu 30 menit dan dibaca pada panjang
5
D. Uji aktivitas antioksidan dengan metode FTC-TBA a. Pembuatan larutan A
Larutan A dibuat dengan menimbang fraksi etil asetat ekstrak metanol daun lada sebanyak 4 mg, dilarutkan dengan etanol pada tabung raksi bertutup, kemudian ditambahkan 4,1 mL asam linoleat 2,5 % , 8 mL buffer fosfat (pH 7) 0,05 m, 3,9 mL aquadest kemudian diinkubasi didalam oven dengan suhu 37-40oC selama 24 jam. Dibuat replikasi sebanyak 3 kali.
b. Pembuatan larutan B
Preparasi larutan B dibuat dengan cara menambahkan 9,7 mL etanol 75% dengan 0,1 mL ammonium thiocyanate 30% dalam tabung flakon, selanjutnya ditambahkan 100µL sampel larutan A yang sudah diinkubasi selama 24 jam, 100µL FeCl3 0,02 m ditunggu selama operating time yaitu 5 menit dan diukur ada
panjang gelombang 488,5 nm.
E. Penegasan aktivitas antioksidan dengan metode TBA
Larutan sampel dan larutan standar yang digunakan pada metode FTC pada hari terakhir diambil sebanyak 2 mL dan ditambahkan 1 mL larutan trikloroasetat 20%, 2 mL larutan asam tiobarbiturat 0,67%. Setelah didihkan selama 10 menit, sampel didinginkan, kemudian disentrifugasi dengan kecepatan 3.000 rpm selama 30 menit. Absorbansi supernatan dibaca pada panjang gelombang 532 dengan spektrofotometer visibel.
F. Analisis data
1. Penetapan kandungan fenolik total
Kandungan fenolik total dinyatakan dalam nilai mg ekivalen asam galat per gram fraksi etil asetat. Nilai tersebut didapatkan dari analisis regresi linier dengan data kurva baku asam galat, sehingga diperoleh kandungan fenolik total dengan perhitungan menggunakan rumus:
Kandungan fenolik total = X
X = kadar fenolik yang diperoleh dari persamaan kurva baku (mg/ml) v = volume akhir larutan dikali faktor pengenceran (ml)
6
Aktivitas antioksidan dengan metode FTC-TBA dinyatakan dalam persen inhibisi yang dapat dihitung dengan rumus:
Persentase inhibisi = 100 –[ ] A1 = absorbansi maksimum sampel
A0 = absorbansi maksimum kontrol negatif 3. Analisis statistik
Analisis statistik dilakukan dengan One Sampel T-Test menggunakan program PSPP untuk persen inhibisi antar kelompok kontrol positif dan sampel (fraksi etil asetat ekstrak metanol daun Lada) pada FTC dan TBA untuk melihat perbedaan keduanya.
3. Hasil dan Pembahasan
Senyawa fenolik termasuk fenol sederhana, asam fenolik, kumarin, flavonoid, stilbenes, hydrolysabl, tanin terkondensasi, lignan, dan lignin. Senyawa fenolik merupakan metabolit sekunder yang paling banyak terkandung dalam tanaman. Senyawa tersebut berfungsi sebagai pencegahan proses pigmentasi, antioksidan dan agen pelindung terhadap sinar UV (Kambojo et al., 2015).
Banyak metode yang digunakan untuk mengkuantifikasi senyawa fenolik. Salah satu metode yang sering digunakan adalah kuantifikasi dengan sektrofotometri, karena mudah dilakukan, cepat dan dapat diterapkan dilaboratorium secara rutin, dan murah. Reaksi kolorimetri banyak digunakan dalam metode spektrofotometri UV-VIS. Metode ini akan mengukur konsentrasi senyawa fenolik secara total dalam ekstrak tumbuhan (Blainski, et al., 2013). Prinsip metode kolorimetri Folin Ciocalteu adalah reaksi oksidasi yang cepat dengan menggunakan alkali (biasanya natrium karbonat), dimana nilai yang didapat signifikan dengan ion fenolat (Cicco dan Latanzio, 2011)
7
berwarna tersebut akan mengalami kerusakan sehingga menyebabkan intensitas warnanya menurun dan absorbansinya juga menurun (Gandjar dan Rohman, 2007).
Penentuan operating time pada metode Folin-Ciocalteu untuk penetapan kandungan fenolik total ini dilakukan selama 60 menit. Absorbansi larutan diukur setiap 5 menit pada panjang gelombang teoritis (750 nm). Absorbansi yang diperoleh selama 60 menit kemudian dilihat pada menit keberapa menghasilkan absorbansi yang cenderung stabil atau selisihnya kecil. Operating time yang didapat untuk penetapan kandungan fenolik total adalah 30 menit. Pada waktu tersebut diperoleh nilai absorbansi yang stabil.
Penentuan panjang gelombang maksimum bertujuan untuk mendapatkan nilai serapan maksimum dari hasil reaksi antara asam galat dengan reagen Folin-Ciocalteu. Pengukuran suatu analit harus pada panjang gelombang maksimum karena pada panjang gelombang maksimum kepekaannya tinggi, sehingga perubahan absorbansi untuk setiap satuan konsentrasi adalah paling besar (Gandjar dan Rohman, 2007). Pada panjang gelombang maksimum digunakan tiga tingkat konsentrasi yaitu rendah (40 µg/mL), sedang (60 µg/mL), tinggi (80 µg/mL). Tujuan dilakukan scanning pada tiga tingkat konsentrasi yang berbeda adalah untuk mempresentasikan panjang gelombang maksimum pada tiap konsentrasi. Pengukuran lambda maksimum dilakukan pada rentang panjang gelombang 600-800 nm.
Panjang gelombang maksimum yang digunakan adalah 735 nm. Hasil yang diperoleh dari scanning panjang gelombang maksimum menunjukan hasil yang berbeda dengan lambda maksimum teoritis. Hal ini dapat disebabkan oleh beberapa hal antara lain jenis pelarut, pH larutan, suhu, konsentrasi tinggi, dan zat-zat penganggu (Gandjar dan Rohman, 2007).
8
mendekati 1) akan digunakan untuk menentukan kandungan fenolik total. Tabel I berikut ini menunjukkan hasil pengukuran absorbansi kurva baku asam galat yang digunakan.
Tabel I. Hasil pengukuran absorbansi kurva baku asam galat replikasi 3
Konsentrasi Absorbansi Persamaan regresi
40,4 µg/Ml 0,369
Persamaan yang digunakan dalam menentukan kandungan fenolik total adalah persamaan regresi dari replikasi ketiga, yaitu y = 0,00624x + 0,0974 dengan linearitas sebesar 0,9924. Nilai linearitas menunjukan korelasi antara konsentrasi dan absorbansi yang dihasilkan. Semakin baik nilai linearitas (nilai R sama dengan 1 atau mendekati 1) maka korelasinya juga semakin baik.
Uji kandungan fenolik total bertujuan untuk mengetahui jumlah fenol yang terdapat pada sampel. Uji kandungan fenolik total dilakukan dengan menggunakan metode Folin-Ciocalteu. Kompleks biru yang terbentuk terjadi karena reaksi oksidasi reduksi dari fenolat senyawa uji dengan pereaksi fenol Folin-Ciocalteu. Dimana oksidasi dari senyawa fenol oleh reagen molibdotungstat akan membentuk kompleks berwarna biru di sekitar panjang gelombang 745-750 nm (Ronald, et al., 2005). Adapun reaksi yang terjadi sebagai berikut:
9
Tabel II. Hasil penetapan kandungan fenolik total fraksi etil asetat ekstrak metanol daun lada
Konsentrasi Absorbansi Kandungan
Fenolik total
Tabel II menunjukan hasil pengukuran sampel uji pada penetapan kandungan fenolik total. Absorbansi sampel yang diperoleh kemudian dimasukkan ke dalam persamaan regresi linier yang telah didapatkan. Hasil perhitungan menunjukan bahwa fraksi etil asetat ekstrak metanol daun lada memiliki nilai kandungan fenolik total sebesar 133,83 ± 5,4365 mg ekivalen asam galat. Radikal bebas dan peroksidasi lemak dalam tubuh dapat menyebabkan penyakit degeneratif seperti kanker, atherosklerosis dan inflamasi, dengan adanya senyawa antioksidan kecepatan peroksidasi lemak dapat dikurangi (Thitilertdecha, et al.,1999).
Salah satu metode penentuan aktivitas antioksidan adalah metode FTC (Ferri-tiosianat) yang mengukur jumlah peroksida pada tahap awal peroksidasi lemak (Aris, et al., 2009). Pada metode FTC, asam linoleat yang digunakan sebagai sumber peroksida. Peroksida yang terbentuk akan bereaksi dengan FeCl2
untuk membentuk ion Fe3+ yang kemudian bereaksi dengan ammonium tiosianat
(SCN) membentuk kompleks ferri-tiosianat (Fe(SCN)3) berwarna merah yang
dibaca absorbansinya dengan spektrofotometer pada panjang gelombang teoritis 500 nm. Adapun reaksi yang terjadi sebagai berikut
10
pada tahap kedua peroksidasi lipid dan mengukur radikal bebas yang ada setelah oksidasi peroksida (Aqil, et al., 2006; Rezaeizadeh, et al., 2011).
Penentuan operating time pada uji aktivitas antioksidan dengan metode FTC dilakukan dengan menggunakan antioksidan sintesis yaitu Butylated hydroxyrotoluene (BHT) sebagai kontrol positif yang diukur selama 10 menit,
dengan waktu pengukuran pada menit ke- 1,3, 5, 7, dan 10 secara triplo. Pengukuran dilakukan menggunakan spektrofotometri UV-Vis pada panjang gelombang teoritis yaitu 500 nm (Aris, et al., 2009). Dari pengukuran diperoleh operating time untuk metode FTC adalah 5 menit, yang ditunjukkan dengan nilai
absorbansi yang stabil.
Penentuan panjang gelombang maksimum dilakukan bertujuan untuk mendapatkan daerah serapan maksimum. Pada uji aktivitas antioksidan metode FTC dilakukan dengan menggunakan tiga kali pengukuran yang diukur pada rentang 400-600 nm. Lambda yang dipilih adalah pengukuran ketiga yang absorbansinya paling besar yaitu 488,5 nm dengan absorbansi sebesar 1,222.
11
Gambar 3. Profil kenaikan rata-rata absorbansi kontrol negatif, kontrol positif, dan sampel fraksi etil asetat ekstrak metanol daun lada.
Hasil yang diperoleh menunjukkan kesesuaian dengan mekanisme reaksi di mana nilai absorbansi kontrol negatif lebih tinggi dibandingkan nilai absorbansi kontrol positif dan sampel. Hal tersebut disebabkan karena tidak ada senyawa antioksidan pada kontrol negatif yang dapat menghambat proses peroksidasi lipid, sehingga ion Fe3+ yang terbentuk semakin banyak dan menyebabkan warna merah akibat pembentukan kompleks ferri-tiosianat lebih pekat dibandingkan kontrol positif yang berisi BHT (kontrol positif) dan sampel yang berisi fraksi etil asetat ekstrak metanol daun lada. Pengukuran dilakukan pada hari keenam, saat proses proksidasi lipid sudah berjalan secara maksimal.
Tabel III. Perhitungan % inhbisi berdasarkan absobansi hari ke-6
Kontrol positif
12
nilai persen inhibisi kedua sampel tersebut berbeda bermakna (P<0,05). Hal ini menunjukan bahwa fraksi etil asetat ekstrak metanol daun Lada kurang mampu menghambat peroksidasi yang terbentuk jika dibandingkan dengan kontrol positif (BHT). Meskipun demikian ekstrak metanol daun Lada tetap memiliki akivitas antioksidan yang ditunjukan dengan nilai absorbansi yang lebih kecil dibandingkan kontrol negatif.
Pada hari kedelapan setelah pengujian aktivitas antioksidan dengan metode FTC dilakukan penegasan dengan menggunakan metode TBA (Thiobarbituric Acid) untuk mengukur nilai MDA, yang merupakan produk oksidasi sekunder yang terbentuk setelah tahap pertama peroksidasi lipid. Pada tahap kedua peroksidasi lipid, asam linoleat yang sudah banyak terbentuk menjadi radikal terkomposis menjadi senyawa yang lebih sederhana dan relatif stabil, yaitu MDA (malondialdehida). Malondialdehida digunakan sebagai biomarker untuk mengetahui tahap akhir peroksida lipid. Prinsip metode ini adalah pengukuran serapan dengan spektrofotometer dari reaksi MDA dengan asam tiobarbiturat yang berwarna merah muda pada panjang gelombang 532 nm. Adapun reaksi yang terjadi sebagai berikut:
Gambar 4. Reaksi pembentukan kompleks MDA-TBA (Moon dan Shimbamoto, 2009)
13
Tabel IV. Aktivitas antioksidan sampel (fraksi etil asetat ekstrak metanol daun lada) dengan metode TBA
Absorbansi % Inhibisi
Kontro negatif 1,001 ± 0,004 0
Kontrol positif 0,168 ± 0,009 83,217 ± 0,888
Fraksi etil asetat ekstrak metanol
daun lada 0,069 ± 0,022 93,19 ± 2,245
Tabel IV menunjukan bahwa nilai absorbansi persen inhibisi fraksi etil asetat ekstrak metanol daun Lada terhadap MDA lebih besar dibandingkan kontrol positif (BHT). Nilai persen inhibisi fraksi etil asetat ekstrak metanol daun Lada sebesar (93,19 ± 2,245) %, sedangkan nilai persen inhibisi kontrol positif (BHT) sebesar (83,217 ± 0,888) %. Hal tersebut menunjukan bahwa pada tahap kedua peroksidasi lipid, aktivitas penghambatan radikal bebas oleh fraksi etil asetat ekstrak metanol daun lada lebih besar dibandingkan pada tahap pertama peroksidasi lipid.
4. Kesimpulan dan Saran
Kandungan fenolik total per gram sampel pada fraksi etil asetat ekstrak metanol daun Lada sebesar 133,83 ± 5,4365 mg ekivalen asam galat. Aktivitas antioksidan fraksi etil asetat ekstrak metanol daun lada yang dinyatakan dalam persen inhibisi untuk metode FTC dan metode TBA berturut-turut sebesar (5,061 ± 0,598)%, (93,19 ± 2,245)%.
14 Daftar Pustaka
Andersen, O.M., Markham, K.R., 2006, Flavonoids: Chemistry, Biochemistry, and
Application, Taylor & Francis Group, London, P.2.
Aris, S. R. S., Mustafa,S., Ahmat, N., Jaafar, F.Moh. & Ahmad, R, 2009, Phenolic Content and Antioxidant Activity of Fruit Ficus dettoidea var, Angustifolis sp., The
Malaysian Journal of Analytical Sciences, 13 (2), Pp. 146-150.
Artini, P. E. U. D., Astuti, K. W., Warditiani, N. K., 2013, Uji Fitokimia Ekstrak Etil Asetat Rimpang Bangle (Zingiber purpureum Roxb.) Jurnal Farmasi Udayana, Indonesia.
Blanski, A., Lopes,G.C., and De Mello, J. C. P., 2013, Application and Analysis of the Follin Ciocalteu Method for Determination of the Total Phenolic Content from
Limonium brasiliense L., Molecules,18, Pp. 6852-6865.
Cicco, N., and Lattanzio, V., 2011, The Influence of Initial Carbonate Concentration on the Folin-Ciocalteu Micro-Method for the Determination of Phenolic with Low Concentration in the Presence of Methanol: A Comparative Study of Real-Time Monitored Reactions, Am. J. Anal. Chem., Pp.840-845.
Cowan, M.M., 1999, Plant Products as Antimicrobial Agents, Clinical Microbiology
Review,Vol.12, No. 4, Pp.564-582.
Dodson, C. D., Dyer, L. A., Searcy, J., Wright, Z., and Letoumeau, D. K., 2000, Cenocladamide: A Diydropyridone Alkaloid from Piper Cenocladum,
Phytochemistry, Vo. 53, pp. 51-54.
Gandjar, I. G., Rohman, A., 2007, Kimia Farmasi Analisis, Pustaka Pelajar, Yogyakarta, Hal.220-265.
Huang, Y. W., Cai, Z. Y., 2010, Natural Phenolic Compounds From Medicina Herbs and Ditary Plants: Potenttial Use for Cancer Prevention, Nutrion and Cancer, Pp. 1-2.
Kamboj, A., Rana, A., Kaur, R., Jain, U., 2015, Application and Analysis of the Follin Ciocalteu Method for the Determination of the Total Phenolic Content from Leaves, Stems and Seeds of Cucumis sativus L., Journal of Pharmacy Research, Pp.323-329.
Moon, J.K., Shibamoto, T., 2009, Antioxidant Assays for Plant and Food Components, J.
Agric. Chem., Vol. 57, Pp.1655-1666.
Muhtadi, Hidayati, A.L., Suhendi, A., Sudjono, T.A., Haryanto., 2014, Pengujian Daya Antioksidan Dari Beberapa Ekstrak Kulit Buah Asli Indonesia dengan Metode FTC, Simposium Nasional RAPI XIII, Hal.1-9.
15
Prakash, A., 2001, Antioxidant Activity, Takes you into the Heart of a Giant Resource, Vol 19, No.2, Pp. 1-2.
Ronald, L., Piror, Wu, X., and Schaica, K., 2005, Standardized Methods for the Determination of Antioxidant Capacity and Phenolics in Food and Dietary Supplemnts, J. Agr. Food Chem., Pp. 4290-4302
Sochor, J., Zitaka, O., Skutkova, H., Pavlik, D., Babula, P., Krska, B., Homan, A., Adam, V., Provaznik, I., and Kizek, R., 2010, Content of phenolic Compounds and Antioxidant Capacity in Fruits of Apricot Genotypes, Molecule, pp.
6285-6305.
Thitilertdecha, N., Teerawutgulrag, A., and Rakariyatham, N., 2010, Identification of Major Phenolic Compound from Nephelium lappaceum L. and Their Antioxidant Activities, Molecules, 15, Pp. 1453-1465.
16
18
Lampiran 2. Klasifikasi Tanaman Lada (Piper nigrum L.)
Menurut United States Departement of Agriculture klasifikasi dari tanaman lada, yaitu:
Kerajaan : Plantae Sub kerajaan : Tracheobionta Super divisi : Spermatophyta Divisi : Magnoliophyta Kelas : Magnoliopsida Sub kelas : Magnoliidae Ordo : Piperales Suku : Piperaceae Genus : Piper L.
Spesies : Piper nigrum L.
Lampiran 3. Perhitungan Pentapan Kadar Air Daun Lada Kadar Air Simplisia =
Keterangan Berat Simplisia (g) Kadar Air (%) Rata-Rata
19 Replikasi 3
Kadar Air Simplisia =
= 7,573 %
Lampiran 4. Perhitungan rendemen ekstrak dan fraksi a. Ekstrak metanol daun lada
Bobot (gram) Bobot simplisia yang digunakan 31,509 Bobot cawan kosong 80,3737 Bobot cawan + ekstrak 81,5782
Bobot ekstrak 1,2247
% rendemen ekstrak =
% rendemen ekstrak =
x 100 = 3,886%
b. Fraksi etil asetat daun lada
Bobot (gram) Bobot simplisia yang digunakan 31,509 Bobot cawan kosong 22,3606 Bobot cawan + fraksi etil asetat 22,5707 Bobot fraksi etil asetat 0,2101
% rendemen fraksi =
% rendemen fraksi =
Lampiran 5. Data penimbangan untuk penetapan kandungan fenolik total a. Penimbangan asam galat
1. Asam galat untuk operating time Replikasi 1 Bobot bekker 63,7284 61,4635 62,1535 Bobot bekker + zat 63,7385 61,4735 62,1636
Bobot zat 0,0101 0,0100 0,0101
20
Bobot bekker 61,7794 61,5234 61,6027 Bobot bekker
+ zat
61,7894 61,5334 61,6127
Bobot fraksi 0,01 0,01 0,01
Lampiran 6. Data perhitungan konsentrasi asam galat dan fraksi etil asetat untuk penetapan kandungan fenolik total
a. Contoh perhitungan konsentrasi asam galat
Bobot asam galat replikasi 1 = 0,0101g = 10,1 mL
Konsentrasi larutan stok asam galat =
=
1010 µg/mL21 Seri 5 :
V1 . C1 = V2 . C2
0,8 mL . 1010 µg/mL = 10 mL . C2 C2 = 80,8 µg/mL
Replikasi 2 Replikasi 3
Seri 1 40 µg/mL 40,4 µg/mL
Seri 2 50 µg/mL 50,5 µg/mL
Seri 3 60 µg/mL 60,6 µg/mL
Seri 4 70 µg/mL 70,7 µg/mL
Seri 5 80 µg/mL 80,8 µg/mL
b. Contoh perhitungan konsentrasi fraksi etil asetat ekstrak metanol daun lada. Bobot fraksi etil asetat replikasi 1 = 0,0100 gram = 1000 µg/mL
Pengenceran fraksi etil asetat replikasi 1 V1 . C1 = V2 . C2
2 mL . 1000 µg/mL = 10mL . C2 C2 = 200 µg/mL
Replikasi 2 Replikasi 3
22
Lampiran 7. Hasil optimasi operating time untuk penetapan kandungan fenolik total
a. Replikasi 1
Pada replikasi 1, operating time yang didapat menit ke 30 b. Replikasi 2
Menit ke -
Absorbansi pada panjang gelombang 750 nm 40 µg/ml 60 µg/ml 80 µg/ml
Pada replikasi 2 operating time yang didapat menit ke 30
Menit ke- Absorbansi pada panjang gelombang 750 nm
23 c. Replikasi 3
Menit ke -
Absoorbansi pada panjang gelombang 750 nm 40 µg/mL 60 µg/mL 80 µg/mL
5 0.345 0.406 0.581
10 0.362 0.487 0.606
15 0.379 0.529 0.633
20 0.387 0.535 0.650
25 0.399 0.538 0.653
30 0.402 0.544 0.664
35 0.404 0.543 0.664
40 0.414 0.543 0.661
45 0.418 0.544 0.659
50 0.420 0.543 0.665
55 0.423 0.544 0.667
60 0.425 0.544 0.665
Pada replikasi 3 operating time yang didapat menit 30
Lampiran 8. Optimasi panjang gelombang maksimum untuk penetapan kandungan fenolik total
26
Lampiran 9. Hasil pengukuran kurva baku untuk penetapan kandungan fenolik total
a. Replikasi 1
b. Replikasi 2
Seri Konsentrasi Absorbansi Persamaan kurva baku 1 40,0 µg/mL 0,390 A = 0,1264
B = 0,00618 r = 0,9894
y = 0,00618x + 0,1264 2 50,0 µg/mL 0,419
3 60,0 µg/mL 0,484 4 70,0 µg/mL 0,569 5 80,0 µg/mL 0,624
Seri Konsentrasi Absorbansi Persamaan kurva baku 1 40,4 µg/mL 0,349 A = 0,07
B = 0,00711 r = 0,9831
y = 0,00711x + 0,07 2 50,5 µg/mL 0,430
27 b. Replikasi 3
Lampiran 10. Perhitungan kandungan fenolik total fraksi etil asetat Konsentrasi Absorbansi Kandungan
Fenolik total
Contoh perhitungan kandungan fenolik total: a. Replikasi 1 Bobot fraksi = 0,0100 gram
c. Replikasi 3
y = 0,00662x + 0,0974
0,285 = 0,00662x + 0,0974x x = 0, 285- 0,0974/0,00662
28 = 28,3384 µg/mL
= 0,0283384 mg/mL 0,0283 mg/mL Bobot fraksi = 0,0100 gram
Rumus perhitungan kandungan fenolik total
Kandungan fenolik total = x
a. Replikasi 1
Kandungan fenolik total = 0,0261 x 50/0,0100 = 130,5 mg/gram
Jadi, kandungan fenolik total dalam sampel replikasi 1 sebesar 130,5 mg asam galat ekuivalen per gram fraksi etil asetat.
b. Replikasi 2
Kandungan fenolik total = 0,0259 x 50/0,0100 = 129,5 mg/gram
Jadi, kandungan fenolik total dalam sampel replikasi 1 sebesar 129,5 mg asam galat ekuivalen per gram fraksi etil asetat.
c. Replikasi 3
Kandungan fenolik total = 0,0283 x 50/0,0100 = 141,5 mg/gram
Jadi, kandungan fenolik total dalam sampel replikasi 1 sebesar 141,5mg asam galat ekuivalen per gram fraksi etil asetat.
Lamiran 11. Data Penimbangan untuk Uji Aktivitas Antioksidan Metode FTC-TBA
a. Penimbangan BHT untuk Optimasi Metode
OT (gram) Lamda (gram)
Replikasi 1 Replikasi 2 Replikasi 3 Berat Cawan Kosong 63.0377 61.5081 61.7617 63.6569 Berat Cawan + sampel 63.0418 61.5122 61.7657 63.6609
29 Berat Cawan Kosong 62.4275 27,9617 27,2143 20,6965 Berat Cawan + sampel 62.4316 27,9657 27,2183 20,7005
Berat Sampel 0.0041 0,0040 0.0040 0.0040
Lampiran 12. Optimasi Metode Uji Aktivitas Antioksidan FTC-TBA a. Penentuan Operating Time (OT)
Hasil OT, CBHT = 4 mg
OT (Menit ke-)
Absorbansi (Triplo)
Pengukuran 1 Pengukuran 2 Pengukuran 3
1 0.985 0.959 0.948
3 0.918 0.907 0.899
5 0.875 0.875 0.874
7 0.864 0.862 0.860
30 b. Penentuan Lamda max
Replikasi 1
33
Lampiran 13. Perhitungan Persen Inhibisi Uji Aktivitas Antioksidan FTC-TBA
a. Nilai absorbansi kontrol negatif, kontrol positif dan sampel fraksi etil asetat ekstrak metanol daun lada
Hari
Berdasarkan hasil pengukuran absorbansi kontrol negatif dengan spektrofotometer UV/Vis maka dapat disimpulkan bahwa pada hari ke-6 reaksi peroksidasi lipid telah mencapai batas maksimum.
b. Profil absorbansi kontrol negatif, kontrol positif, dan sampel fraksi etil asetat ekstrak metanol daun lada
34
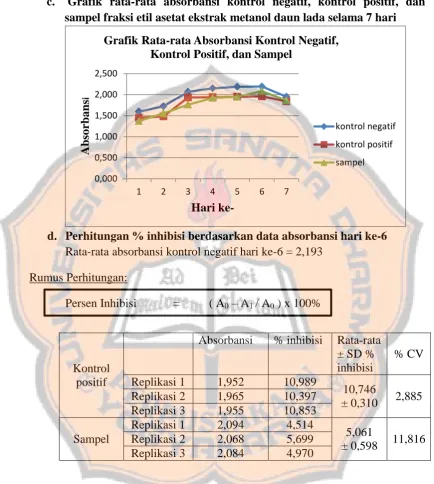
c. Grafik rata-rata absorbansi kontrol negatif, kontrol positif, dan sampel fraksi etil asetat ekstrak metanol daun lada selama 7 hari
d. Perhitungan % inhibisi berdasarkan data absorbansi hari ke-6
Rata-rata absorbansi kontrol negatif hari ke-6 = 2,193 Rumus Perhitungan:
Contoh perhitungan nilai % inhibisi sampel replikasi 1 hari ke-6 1. Kontrol positif
Grafik Rata-rata Absorbansi Kontrol Negatif, Kontrol Positif, dan Sampel
35 Persen inhibisi =
= 4,514 %
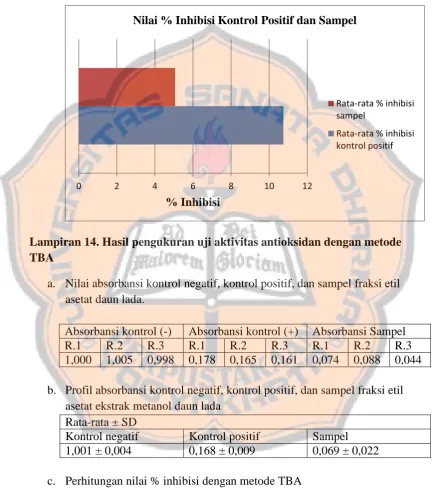
e. Grafik rata-rata nilai % inhibisi kontrol positif dan sampel fraksi etil asetat ekstrak metanol daun lada
Lampiran 14. Hasil pengukuran uji aktivitas antioksidan dengan metode TBA
a. Nilai absorbansi kontrol negatif, kontrol positif, dan sampel fraksi etil asetat daun lada.
Absorbansi kontrol (-) Absorbansi kontrol (+) Absorbansi Sampel R.1 R.2 R.3 R.1 R.2 R.3 R.1 R.2 R.3 1,000 1,005 0,998 0,178 0,165 0,161 0,074 0,088 0,044
b. Profil absorbansi kontrol negatif, kontrol positif, dan sampel fraksi etil asetat ekstrak metanol daun lada
Rata-rata ± SD
Kontrol negatif Kontrol positif Sampel 1,001 ± 0,004 0,168 ± 0,009 0,069 ± 0,022
c. Perhitungan nilai % inhibisi dengan metode TBA % inhibisi = (A0-A1/A0) x 100%
d. Contoh perhitungan nilai % inhibisi sampel replikasi 1:
Persen inhibisi =
= 83,217 %
0 2 4 6 8 10 12
% Inhibisi
Nilai % Inhibisi Kontrol Positif dan Sampel
Rata-rata % inhibisi sampel
36
37
Lampiran 15. Gambar-gambar Proses Penelitian Lampiran 1. Proses Pembuatan Simplisia Daun Lada a. Proses pencucian daun lada
38 c. Proses pengayakan daun Lada
39
Lampiran 2. Proses pembuatan fraksi etil-asetat ekstrak metanol daun Lada
1. Proses penguapan dengan menggunakan vacuum rotary evaporator
40
3. Pemisahan antara air dan etil asetat
4. Uji pendahuluan penetapan kandungan fenolik total dengan metode folin-ciocalteu.
Lapisan etil asetat
Lapisan air
A
B
41 Keterangan
A = kontrol negatif (metanol : air (1:1) + reagen Folin-Ciocalteau + Na2CO3)
B = Kontrol positif (asam galat + reagen Folin-Ciocalteau + Na2CO3)
C = Sampel (fraksi etil asetat ekstrak metanol daun Lada + reagen Folin-Ciocalteau + Na2CO3)
5. Asam galat
6. Hasil penetapan kandungan fenolik total replikasi
42
Lampiran 3. Uji Aktivitas Antioksidan Dengan Metode FTC-TBA 1. Pengukuran menggunakan metode FTC selama 7 hari
Replikasi 1
Replikasi 2
Replikasi 3
Replikasi 1
Replikasi 2
Replikasi 3
Relikasi 1
Replikasi 2
43
Replikasi 1
Replikasi 2
Replikasi 3
Replikasi 1
Replikasi 2
Replikasi 3
Replikasi 1
Replikasi 2
44 2. Pengukuran TBA pada hari ke delapan
Replikasi 1
Replikasi 2
Replikasi 3
Sampel replikasi 1
Sampel replikasi 2
Sampel replikasi 3
Replikasi 1
Replikasi 2
45
BIOGRAFI PENULIS
Penulis lahir di Tanjung Kerja pada tanggal 21 Juni 1994. Penulis memiliki seorang ayah bernama Kolenius Kolai dan seorang ibu bernama Emma, serta seorang kakak bernama Maria Magdalena. Penulis menyelesaikan pendidikan dasar di SDN. 09 Banua Tengah pada tahun 2006. Setelah itu, penulis melanjutkan pendidikan menengah di SMP Karya Budi Putussibau pada tahun 2006 hingga 2009, SMA Karya Budi Putussibau pada tahun 2009 hingga 2012. Penulis kemudian melanjutkan di Fakultas Farmasi Sanata Dharma Yogyakarta dari tahun 2012 hingga 2016.