Bab II Tinjauan Pustaka
II.1. Tinjauan Umum Tumbuhan Artocarpus
Artocarpus atau oleh masyarakat di Indonesia dikenal sebagai tumbuhan “nangka-nangkaan”, yang merupakan salah satu genus utama dalam famili Moraceae disamping Morus dan Ficus. Keberadaan tumbuhan ini sangat melimpah di wilayah Indonesia terutama di pulau Sumatera, Jawa dan Kalimantan. Selain di Indonesia, tumbuhan ini dilaporkan tersebar di wilayah Asia Selatan, Papua Nugini dan Pasifik Selatan (Lemmens, 1995).
sub genus Artocarpus sub genus Psedojaca
Gambar II.1. Skema hubungan genetik tumbuhan Artocarpus dan genus lain
pada famili Moraceae (Kanzaki dkk., 1997)
Berdasarkan skema tersebut, genus Artocarpus memiliki tingkatan evolusi yang lebih tinggi dibandingkan dengan genus lain (Morus dan Ficus) pada famili Moraceae. Selanjutnya, skema tersebut memperlihatkan pula bahwa A. heterophyllus, A. integer dan A. altilis berada pada percabangan yang sama, sedangkan A. rigidus berada pada percabangan yang lain. Hal ini menunjukkan bahwa A. heterophyllus, A. integer dan A. altilis memiliki hubungan genetik yang lebih dekat satu sama lain dibandingkan terhadap A. rigidus. Secara umum kajian berdasarkan cpDNA (Kanzaki dkk., 1997) tersebut ternyata sejalan dengan kajian morfologi yang disarankan oleh Jarret (1959; 1960).
Tumbuhan genus Artocarpus juga mempunyai nilai ekonomi yang tinggi dan telah dimanfaatkan oleh masyarakat antara lain buahnya (A. heterophylus, A. champeden dan A. altilis) dapat dikonsumsi dan kayunya (A. gomezianus) dipergunakan sebagai bahan pembuatan kursi dan meja. Selain itu, beberapa spesies Artocarpus digunakan sebagai obat tradisional, antara lain getah A. elasticus sebagai obat disentri dan pereda demam, serta seduhan kulit batangnya dimanfaatkan sebagai anti-fertilitas (Heyne, 1987).
penelusuran pustaka, umumnya tumbuhan genus ini mengandung senyawa turunan fenol terutama golongan flavonoid (Venkataraman, 1972; Nomura dkk., 1998; Hakim dkk., 2006) dan senyawa non fenolik, yaitu senyawa-senyawa turunan triterpen (Achmad dkk.,1996; Altman dkk., 1976). Senyawa-senyawa metabolit sekunder tersebut ternyata dilaporkan memiliki aktivitas biologis yang beragam, antara lain sebagai antioksidan (Fukai dkk., 2003), cancer chemopreventive anticarcinogen (Botta dkk., 2005), anti tumor (Nomura dkk., 1998; Pedro dkk., 2005) dan antimalaria (Widyawaruyanti dkk., 2007; Boonphong dkk., 2007).
II.2 Ilmu Kimia Tumbuhan Artocarpus
Kajian ilmu kimia Artocarpus diawali oleh Perkin dan Cope, yang berhasil mengisolasi senyawa pigmen warna kuning dari A. heteropyllus yaitu sianomaklurin (31) dan morin (34) pada tahun 1895 (Venkataraman, 1972). Walaupun demikian penentuan struktur kedua senyawa tersebut baru dapat ditetapkan pada tahun 1963 (Venkataraman, 1972). Selanjutnya, kajian fitokimia terhadap Artocarpus menunjukkan bahwa kandungan metabolit sekunder pada genus ini adalah senyawa fenolik dengan flavonoid sebagai komponen utamanya. Senyawa golongan flavonoid pada genus ini memiliki kerangka calkon, flavanon, flavan-3-ol, flavon, 3-prenilflavon dan turunan 3-prenilflavon (Venkataraman, 1972; Nomura dkk., 1998; Hakim dkk., 2006). Senyawa fenolik lainnya yaitu senyawa golongan adduct Diels-Alder, stilbenoid dan 2-aril benzofuran (Nomura dkk., 1998; Syah dkk., 2006).
II.2.1 Senyawa Flavonoid
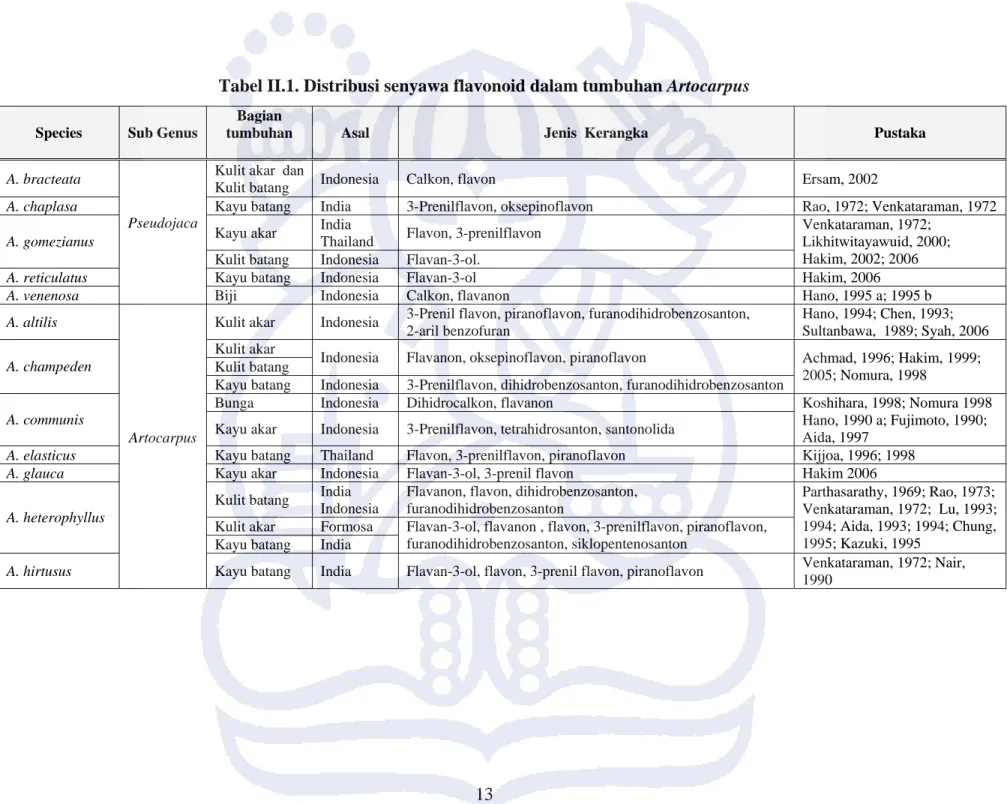
Tabel II.1. Distribusi senyawa flavonoid dalam tumbuhan Artocarpus
Species Sub Genus
Bagian
tumbuhan Asal Jenis Kerangka Pustaka
A. bracteata Kulit akar dan
Kulit batang Indonesia Calkon, flavon Ersam, 2002
A. chaplasa Kayu batang India 3-Prenilflavon, oksepinoflavon Rao, 1972; Venkataraman, 1972 Kayu akar India
Thailand Flavon, 3-prenilflavon A. gomezianus
Kulit batang Indonesia Flavan-3-ol.
Venkataraman, 1972; Likhitwitayawuid, 2000; Hakim, 2002; 2006
A. reticulatus Kayu batang Indonesia Flavan-3-ol Hakim, 2006
A. venenosa
Pseudojaca
Biji Indonesia Calkon, flavanon Hano, 1995 a; 1995 b A. altilis Kulit akar Indonesia 3-Prenil flavon, piranoflavon, furanodihidrobenzosanton,
2-aril benzofuran
Hano, 1994; Chen, 1993; Sultanbawa, 1989; Syah, 2006 Kulit akar
Kulit batang Indonesia Flavanon, oksepinoflavon, piranoflavon A. champeden
Kayu batang Indonesia 3-Prenilflavon, dihidrobenzosanton, furanodihidrobenzosanton
Achmad, 1996; Hakim, 1999; 2005; Nomura, 1998 Bunga Indonesia Dihidrocalkon, flavanon
A. communis
Kayu akar Indonesia 3-Prenilflavon, tetrahidrosanton, santonolida
Koshihara, 1998; Nomura 1998 Hano, 1990 a; Fujimoto, 1990; Aida, 1997
A. elasticus Kayu batang Thailand Flavon, 3-prenilflavon, piranoflavon Kijjoa, 1996; 1998 A. glauca Kayu akar Indonesia Flavan-3-ol, 3-prenil flavon Hakim 2006
Kulit batang India Indonesia
Flavanon, flavon, dihidrobenzosanton, furanodihidrobenzosanton
Kulit akar Formosa A. heterophyllus
Kayu batang India
Flavan-3-ol, flavanon , flavon, 3-prenilflavon, piranoflavon, furanodihidrobenzosanton, siklopentenosanton Parthasarathy, 1969; Rao, 1973; Venkataraman, 1972; Lu, 1993; 1994; Aida, 1993; 1994; Chung, 1995; Kazuki, 1995 A. hirtusus Artocarpus
Tabel II.1. Distribusi senyawa flavonoid dalam tumbuhan Artocarpus (lanjutan)
Species Sub Genus Bagian
tumbuhan Asal Jenis Kerangka Pustaka
Papua Nugini Flavanon
A. incisa Kayu batang
India Flavon Shimizu, 1998; Venkataraman, 1972
A. integer Kayu batang India 3-Prenilflavon, oksepinoflavon Pendse, 1972; 1976 A. kemando Kayu akar Indonesia 3-Prenilflavon, oksepinoflavon, piranoflavon,
furanodihidrobenzosanton, kuinodihidrosanton Seo, 2003; Hakim 2006 A. lanceifolius Kayu dan kulit
batang Indonesia
3-Prenilflavon, piranoflavon, dihidrobenzosanton, furanodihidrobenzosanton, santonolida,
Mujahidin, 1997; Hakim, 2002; 2006
A. maingayii Kulit batang Indonesia 3-Prenilflavon, oksepinoflavon, piranoflavon Eliza, 1998; Hakim 2006 A. nobilis Kulit batang India Dihidrobenzosanton, furanodihidrobenzosanton Hakim, 2002; 2006
A. rigida Kulit batang Indonesia Formosa
Flavon, 3-prenilflavon, dihidrobenzosanton, furanodihidrobenzosanton, kuinodihidrosanton
Hano, 1990 c; Hano, 1993; Lin, 1996; Chung, 2000; Ko, 2001; Likhitwitayawuid, 2001; Lu, 2002 A. rotunda Kulit akar Indonesia 3-Prenilflavon, furanodihidrobenzosanton,
kuinonodihidrosanton Sultanbawa, 1989; Seo, 2003 A. teysmanii
Artocarpus
Berdasarkan tabel di atas, terdapat suatu pola bahwa tumbuhan Artocarpus dari sub genus Pseudojaca cenderung untuk menghasilkan senyawa metabolit sekunder golongan flavonoid dengan kerangka calkon dan flavan-3ol seperti yang diperlihatkan pada spesies A. bracteata, A. reticulatus dan A. venenosa. Walaupun demikian, senyawa-senyawa dengan kerangka flavon dan 3-prenilflavon masih dapat ditemukan pada beberapa spesies dari subgenus ini seperti pada spesies A. chaplasa dan A. gomezianus. Sementara itu, sub genus Artocarpus memiliki kecenderungan untuk menghasilkan senyawa metabolit sekunder dengan kerangka flavon, 3-prenil flavon dan turunannya, yang ditunjukkan oleh sebagian besar spesies pada sub genus ini. Selain itu, umumnya penelitian dilakukan pada jaringan kulit dan kayu baik akar maupun batang. Menarik untuk dicatat, bahwa bagian kulit dan kayu dari spesies yang sama memiliki perbedaan kandungan metabolit sekunder, seperti ditunjukkan oleh metabolit sekunder yang berhasil diisolasi dari A. champeden (Hakim, 2005). Ditinjau dari asal sampel tumbuhannya, tampak bahwa sebagian bahan penelitian berasal dari Indonesia dan beberapa berasal dari luar Indonesia yaitu dari India, Thailand, dan Papua Nugini. Tabel II.1 juga menunjukkan bahwa keanekaragaman senyawa yang dihasilkan dari Artocarpus asal Indonesia berbeda dengan yang diperoleh dari Artocarpus yang berasal dari luar Indonesia.
Secara umum, keanekaragaman kerangka senyawa flavonoid pada Artocarpus mengikuti jalur biogenesis yang lazim pada pembentukan senyawa flavonoid pada tumbuhan. Pembentukan flavonoid diawali dari kombinasi antara jalur asetat-malonat dengan jalur shikimat, yaitu kombinasi antara unit C6-C3 (jalur shikimat)
dengan tiga unit C2 (jalur asetat-malonat) menghasilkan unit C6-C3-(C2+C2+C2).
Tiga unit C2 yang berasal dari jalur asetat-malonat ini selanjutnya membentuk
cincin A pada struktur senyawa flavonoid, sedangkan unit C6-C3 membentuk
O OH Asam sinamat OH HO SCoA O O OH OH HO O O O - H2O O OH OH OH HO OH O OH OH OH HO O calkon f lavanon 3
3 unit asetil ko-A
A
B (calkon sintase)
Gambar II.2 Pokok-pokok biosintesis flavonoid (Manitto, 1981)
Berdasarkan biosintesis ini, pembentukan flavonoid dimulai dengan memperpanjang unit C6-C3 yang berasal dari turunan sinamat.
Percobaan-percobaan sebelumnya juga menunjukkan bahwa calkon dan isomer flavanon yang sebanding juga berperan sebagai senyawa antara dalam biosintesis berbagai jenis flavonoid lainnya. Adapun hubungan biogenetik antara berbagai flavonoid tercantum pada Gambar II.3 (Manitto, 1981).
O OH OH OH HO OH O OH OH OH HO O calkon f lavanon O O OH OH OH HO O O H O OH OH OH HO O OH + OH - OH O OH OH OH HO O H H - H f lavon O OH OH OH HO O H
Gambar II.3 Hubungan biogenetik berbagai jenis flavon (Manitto, 1981)
memungkinkan terjadinya reaksi siklisasi antara gugus-gugus tersebut menghasilkan senyawa-senyawa turunan 3-prenil-flavon dengan kerangka piranoflavon, oksepinoflavon, dihidrobenzosanton, furanodihidrobenzosanton, kuinodihidrosanton, tetrahidrosanton, siklopentenosanton dan santonolida (Achmad, 1999). O 2' 5 7 4' A B O 3 8 8a 4a Kemungkinan oksigenasi di cincin B
unit isopren yang terikat pada C-3
5'
Gambar II.4 Kecenderungan pola oksigenasi dan isoprenilasi
senyawa flavonoid Artocarpus
Berikut adalah beberapa contoh senyawa golongan flavonoid yang diperoleh dari tumbuhan genus Artocarpus, yang berasal dari subgenus Artocarpus dan Pseudojaca.
a. Calkon dan dihidrocalkon
Tabel II.2. Distribusi senyawa calkon pada Artocarpus
Nama senyawa Spesies Bagian
Tumbuhan Asal tumbuhan Pustaka Paratokarpin D (9) A. venenosa Biji Indonesia Hano, 1995 a
Kanzonol (21) A. bracteata Kulit akar dan
kulit batang
Indonesia Ersam, 2002
Paratokarpin F (22) A. venenosa Biji Indonesia Hano, 1995 b
Paratokarpin E (23) Paratokarpin C (24) Paratokarpin B (25)
A. venenosa Biji Indonesia Hano, 1995 a
Paratokarpin G (26) A. venenosa Biji Indonesia Hano, 1995 b Paratokarpin A (27) A. venenosa Biji Indonesia Hano, 1995 a Artoindonesianin J (28) A. bracteata Kulit akar dan
kulit batang
Indonesia Ersam, 2002
Berdasarkan gugus isoprenil yang dimiliki, senyawa calkon Artocarpus dapat dibedakan menjadi dua jenis, yaitu senyawa calkon dengan substituen isoprenil bebas dan senyawa calkon dengan substituen isoprenil yang termodifikasi. Senyawa calkon dengan substituen isoprenil bebas pada kedua cincin aromatiknya diantaranya yaitu kanzonol (21) diperlihatkan pada Gambar II.5.
OH O OH HO kanzonol (21) α β 2 4 2' 4' A B
Gambar II.5 Struktur senyawa kelompok calkon Artocarpus
dengan substituen isoprenil bebas
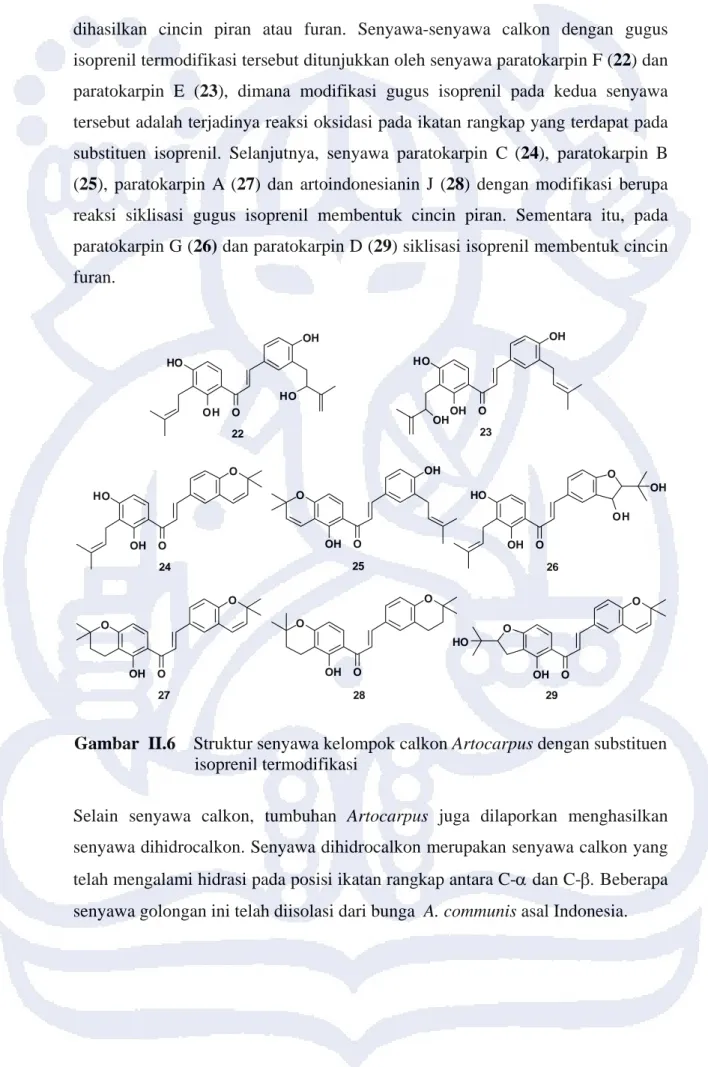
dihasilkan cincin piran atau furan. Senyawa-senyawa calkon dengan gugus isoprenil termodifikasi tersebut ditunjukkan oleh senyawa paratokarpin F (22) dan paratokarpin E (23), dimana modifikasi gugus isoprenil pada kedua senyawa tersebut adalah terjadinya reaksi oksidasi pada ikatan rangkap yang terdapat pada substituen isoprenil. Selanjutnya, senyawa paratokarpin C (24), paratokarpin B (25), paratokarpin A (27) dan artoindonesianin J (28) dengan modifikasi berupa reaksi siklisasi gugus isoprenil membentuk cincin piran. Sementara itu, pada paratokarpin G (26) dan paratokarpin D (29) siklisasi isoprenil membentuk cincin furan. OH OH O HO HO 22 OH OH O OH HO 23 HO OH O O 24 O OH O OH 25 OH O O OH OH HO 26 O OH O O 27 OH O O O 28 OH O O O HO 29
Gambar II.6 Struktur senyawa kelompok calkon Artocarpus dengan substituen
isoprenil termodifikasi
OH O HO OH 30 OH O HO OH OH 31 OH O HO O OH 32 α β A B 2 4 4' 2'
Gambar II.7 Struktur senyawa kelompok dihidrocalkon Artocarpus
Berdasarkan pola oksigenasi pada cincin B, maka senyawa dihidrocalkon Artocarpus dapat dibedakan menjadi dua jenis, yaitu senyawa dihidrocalkon dengan pola monooksigenasi pada posisi C-4 di cincin B, seperti ditunjukkan oleh senyawa AC-3-2 (30) (Nomura, 1998) dan senyawa dihidrocalkon dengan pola dioksigenasi pada posisi C-3 dan C-4 di cincin B, seperti ditunjukkan oleh senyawa AC-5-1 (31) (Koshihara dkk., 1998) dan AC-3-1 (32) (Nomura dkk., 1998).
Menarik untuk dicatat, bahwa senyawa dihidrocalkon Artocarpus yang diperoleh dari jaringan bunga ini memiliki kecenderungan untuk berkondensasi dengan unit geranil pada posisi C-5’ atau pada posisi C-5’ dan C-2. Substituen geranil tersebut dapat berada dalam keadaan bebas atau tersiklisasi dengan gugus hidroksil pada cincin B.
b. Flavanon
Senyawa flavanon Artocarpus umumnya memiliki pola dioksigenasi pada cincin A, yaitu pada posisi C-5 dan C-7, sedangkan pola oksigenasi pada cincin B cukup beragam, sehingga dapat dikelompokkan menjadi senyawa flavanon dengan pola monooksigenasi, dioksigenasi dan trioksigenasi di cincin B.
kelompok senyawa flavanon dengan pola monooksigenasi di cincin B ditunjukkan pada Tabel II.3 dan Gambar II.8
Tabel II. 3. Senyawa flavanon dengan pola monooksigenasi di cincin B
Nama senyawa Spesies Bagian Tumbuhan Asal tumbuhan Pustaka Paratokarpin J (33) Paratokarpin L (34) Paratokarpin H (35) Paratokarpin I (36) Paratokarpin K (37)
A. venenosa Biji Indonesia Hano, 1995 b
AC-3-3 (38) A. communis Bunga Indonesia Nomura, 1998
O OH O O OH 33 O OH O OH HO 34 O HO OH O O 36 35 O OH O O OH O OH O O O 37 O HO OH OH O 38 2 1' 4' 8 3' 4 6 4a 8a A B
Gambar II.8 Struktur senyawa kelompok flavanon dengan pola monooksigenasi
di cincin B
oleh senyawa 35 dan 37. Selain itu, senyawa AC-3-3 (38) yang berhasil diisolasi dari bagian bunga A. communis menunjukkan kecenderungan yang sama dengan kelompok senyawa senyawa flavonoid lain (kelompok senyawa dihidrocalkon) yang diperoleh dari jaringan bunga, yaitu kecenderungan untuk berkondensasi dengan unit geranil pada cincin A. Selanjutnya, kelompok senyawa flavanon yang kedua adalah kelompok senyawa flavanon dengan pola dioksigenasi di cincin B. Umumnya pola oksigenasi terjadi pada posisi C-2’dan C-4’, tetapi berbeda untuk senyawa A5-2 (39) dimana pola oksigenasinya terjadi pada posisi 3’ dan C-4’. Selengkapnya kelompok senyawa tersebut ditunjukkan pada Tabel II.4 dan Gambar II.9.
Tabel II. 4. Senyawa flavanon dengan pola dioksigenasi di cincin B
Nama senyawa Spesies Bagian Tumbuhan
Asal
tumbuhan Pustaka Nortokarpanon (7) A. incisus Kayu batang Papua Nugini Shimizu, 1998 Artokarpanon (8) A. champeden Kulit akar Indonesia Hakim, 2005;
Nomura, 1998 Dihidromorin (9) A. heterophyllus Kayu batang India Venkataraman,
1972
AC-5-2 (39) A. communis Bunga Indonesia Nomura, 1998
Artokarpanon A (40) A. champeden Kulit akar Indonesia Hakim, 2005; Nomura, 1998 O HO OH OH O OH 39 O OH O OH HO HO 7 6 8 3 3' 5' 6' 2 1' O HO OH OH HO OH O 8 O H3CO OH HO OH O 40 O H3CO OH HO OCH3 O 9
Gambar II.9 Struktur senyawa kelompok flavanon dengan pola dioksigenasi
Pola oksigenasi pada posisi C-3’ dan C-4’ dan adanya gugus geranil pada posisi C-2’ yang terdapat pada senyawa AC-5-2 (39), nampaknya menjadi kekhasan dari senyawa flavonoid (kelompok flavanon dan dihidrocalkon) yang diisolasi dari jaringan bunga, dan berbeda dengan senyawa flavanon yang diisolasi dari jaringan kulit dan batang yang teroksigenasi pada posisi C-2’ dan C-4’.
Kelompok yang terakhir adalah kelompok senyawa flavanon dengan pola trioksigenasi di cincin B. Yang menarik dari kelompok ini adalah posisi pola oksigenasi pada C-2’, C-4’ dan C-6’ yang tidak lazim pada senyawa flavonoid Artocarpus lainnya. Selain itu, semua gugus hidroksil pada cincin B tersebut telah mengalami metilasi menjadi gugus metoksi. Selengkapnya kelompok senyawa tersebut ditunjukkan pada Tabel II.5 dan Gambar II.10.
Tabel II. 5. Senyawa flavanon dengan pola trioksigenasi di cincin B
Nama senyawa Spesies Bagian Tumbuhan
Asal
tumbuhan Pustaka Artoindonesianin E (41) A. champeden Kulit akar Indonesia Hakim, 2005
A. heterophyllus Formosa Lu, 1993
Heteroflavanon A (42)
A. champeden Indonesia Hakim, 2005
Lu,1994 Heteroflavanon C (43) Heteroflavanon B (44) A. heterophyllus Kulit akar Formosa Lu, 1993 O HO OH OCH3 OCH3 H3CO O 41 O H3CO OH H3CO OCH3 O OCH3 42 O HO OH H3CO OCH3 O OCH3 43 O H3CO OH H3CO OCH3 O OCH3 44
Gambar II.10 Struktur senyawa kelompok flavanon dengan pola trioksigenasi
c. Flavan-3-ol
Sama halnya seperti senyawa calkon, senyawa flavan-3-ol merupakan kelompok senyawa yang jarang ditemukan pada genus Artocarpus. Walaupun demikian, beberapa senyawa kelompok ini dilaporkan telah berhasil diperoleh dari beberapa spesies Artocarpus, antara lain senyawa afzelecin (45) dan katecin (47) yang berhasil diisolasi dari A. glauca, A. gomezianus, dan A. reticulatus (Hakim, 2006). Selain itu, senyawa flavan-3-ol yang mengikat gugus gula (ramnosil), yaitu afzelecin ramnosida (46) juga berhasil diisolasi dari A. reticulatus (Hakim, 2006). Selanjutnya, dari kayu batang A. heterophyllus dan A. hirtusus berhasil diperoleh senyawa sianomaklurin (48) (Venkataraman, 1972).
O OH HO OH OH 45 O OH HO OH OH OH 47 O O HO OH OH 46 O O OH HO OH OH H H H 48 1 2 4 5 6 8 2' 4' O OH OH OH CH3 A B
Gambar II.11 Struktur senyawa kelompok flavan-3-ol Artocarpus
sianomaklurin (48) dan pola ortodihidroksi pada posisi C-3’ dan C-4’ seperti ditunjukkan oleh senyawa katecin (47).
d. Flavon dan flavon terprenilasi
Senyawa flavon pada tumbuhan Artocarpus umumnya mempunyai ciri utama, yaitu terisoprenilasi pada cincin aromatik dan pada posisi C-3. Walaupun demikian, flavon sederhana (tidak terisoprenilasi) masih ditemukan pada beberapa spesies genus ini, antara lain dari A. heterophyllus, A. hirtusus dan A. insica yaitu, norartokarpetin (10) dan morin (50) (Venkataraman, 1972). Selanjutnya senyawa flavon sederhana lainnya, yaitu artokarpetin (49) diperoleh dari A. heterophyllus (Venkataraman, 1972) dan A. champeden (Hakim dkk., 1999).
O HO OH OH OH O 10 O H3CO OH OH OH O 49 O HO OH OH OH O OH 50
Gambar II.12 Struktur senyawa kelompok flavon sederhana dari Artocarpus
Penelusuran literatur menunjukkan bahwa kelompok senyawa flavon sederhana dari Artocarpus tidak memiliki keanekaragaman seperti kelompok senyawa flavon terisoprenilasi. Apabila ditinjau dari pola oksigenasi pada cincin B, maka semua senyawa flavon sederhana dari Artocarpus memiliki pola dioksigenasi pada posisi C-2’ dan C-4’ seperti yang ditunjukkan pada Gambar II.12. Modifikasi yang terjadi pada senyawa kelompok ini adalah adanya reaksi metilasi pada gugus hidroksil pada posisi C-7 (ditunjukkan oleh senyawa 49) serta oksigenasi pada posisi C-3 (ditunjukkan oleh senyawa 50).
terisoprenilasi pada Artocarpus dapat dibedakan menjadi dua yaitu senyawa flavon terisoprenilasi tanpa gugus isoprenil pada posisi C-3 serta senyawa flavon terisoprenilasi dengan gugus isoprenil pada posisi C-3.
Senyawa kelompok flavon terprenilasi tanpa gugus isoprenil pada posisi C-3, dilaporkan telah berhasil diisolasi dari beberapa spesies Artocarpus, antara lain dari A. heterophyllus, A. hirsutus, dan A. gomezianus. Selengkapnya senyawa tersebut ditunjukkan pada Tabel II.6 dan Gambar II.13.
Tabel II.6 Senyawa flavon terisoprenilasi tanpa gugus isoprenil pada C-3
Nama senyawa Spesies Bagian Tumbuhan Asal tumbuhan Pustaka Artokarpesin (11) A. heterophyllus A. hirtusus A. gomezianus
Kayu batang India Randhakrishnan, 1965;
Parthasarathy, 1969;
Venkataraman, 1972
Sikloartokarpesin (12) Kayu batang India Parthasarathy,
1969
Artonin U (51) Kulit batang Indonesia Aida, 1994
Oksidihidroartokarpesin (52)
A. heterophyllus
Kayu batang India Parthasarathy, 1969
Gambar II.13 Struktur senyawa flavon terisoprenilasi
Kelompok senyawa ini umumnya memiliki pola dioksigenasi pada posisi C-2’ dan C-4’ di cincin B, kecuali senyawa oksidihidroartokarpesin (51) yang hanya memiliki pola monooksigenasi, yaitu pada posisi C-4’. Selain itu, penelusuran literatur juga memperlihatkan bahwa gugus isoprenil yang terikat pada cincin aromatik lazimnya terikat pada cincin A pada posisi C-6 atau C-8 berbeda dengan kelompok calkon yang memiliki kecenderungan untuk terisoprenilasi pada kedua cincin aromatiknya. Selanjutnya seperti lazimnya gugus isoprenil pada golongan flavonoid lainnya, gugus ini memiliki kemampuan untuk melakukan reaksi oksidasi (ditunjukkan oleh senyawa 52) atau siklisasi dengan gugus hidroksil menghasilkan cincin kromen, seperti ditunjukkan oleh senyawa 12. Senyawa 12 merupakan senyawa yang dihasilkan dari reaksi siklisasi antara isoprenil pada posisi C-6 dengan hidroksil pada posisi C-7 dari senyawa 11.
Secara biogenesis, adanya gugus isoprenil pada posisi C-3 dapat disarankan berasal dari kondensasi antara unit isoprenil dengan suatu flavon sederhana, sebagaimana ditunjukkan oleh Gambar II.14 (Hakim dkk., 2005).
artokarpetin (49) O OH OH OH H3CO O PPO O OH OH OH H3CO O H integrin (54) O OH OH OH H3CO O
Berdasarkan pola oksigenasi di cincin B, senyawa kelompok ini juga dapat dibedakan menjadi dua jenis, yaitu yang memiliki pola dioksigenasi dan trioksigenasi di cincin B. Kelompok senyawa 3-prenil flavon dengan pola dioksigenasi di cincin B antara lain, seperti ditunjukkan pada Tabel II.7 dan Gambar II.15.
Tabel II.7 Senyawa 3-prenil flavon dengan pola dioksigenasi di cincin B
Nama senyawa Spesies Bagian Tumbuhan Asal tumbuhan Pustaka Kudraflavon C (13) A. champeden A. glauca Kayu batang Kayu akar Indonesia Hakim, 2006 A. heterophyllus A. hirtusus A. gomezianus A. chaplasa A. insica
Kayu batang India Venkataraman, 1972 Artokarpin (14) A. maingayii A. champeden Kulit batang Kulit dan Kayu akar Indonesia Hakim, 2006 Hakim, 1999 A. heterophylus A. insica
Kayu batang India Venkataraman, 1972
Norartokarpin (54)
A. champeden Kulit dan Kayu akar
Indonesia Hakim, 1999
Artokarpetin A (55) Artokarpetin B (56)
A. rigida Kulit batang Formosa Lin, 1996
O O H3CO OH OH OH 53 O O OH HO OH OH 13 O O OH OH OH HO 54 O O OH OH OH H3CO 14 O O OH OH OH H3CO 55 O O OH OCH3 OH H3CO 56 57 O O OH HO OH OH O O OH OH O OH OH 58
Gambar II.15 Struktur senyawa 3-prenil flavon dengan pola dioksigenasi
di cincin B
Gambar II.15 menunjukkan bahwa pola dioksigenasi di cincin B umumnya pada posisi 2’ dan C4’, kecuali pada senyawa 58 yang teroksigenasi pada posisi C-3’ dan C-4’. Selanjutnya kelompok senyawa 3-prenil flavon dengan pola trioksigenasi di cincin B antara lain ditunjukkan pada Tabel II.8 dan Gambar II.16.
Tabel II.8 Senyawa 3-prenil flavon dengan pola trioksigenasi di cincin B
Nama senyawa Spesies Bagian Tumbuhan Asal tumbuhan Pustaka A. rigida A. communis Indonesia Hano, 1990 a; 1990 b; Artonin E (15)
A. lanceifolius Kulit batang Indonesia Singapura
O O OH HO OH 59 O O OCH3 OH HO OH HO 60 O O OH OH O 15 61 O O OH OH O HO OH HO OH HO OH
Gambar II.16 Struktur senyawa 3-prenil flavon dengan pola trioksigenasi
di cincin B
Penelusuran literatur lebih lanjut menunjukkan bahwa kelompok senyawa 3-prenil flavon dengan pola trioksigenasi di cincin B cenderung dihasilkan dari spesies Artocarpus yang memiliki tingkat evolusi tinggi (merujuk pada hasil penelitian Kanzaki dkk., 1997) seperti, A .altilis, A. rigidus dan A. laceifolius.
Selain itu hal menarik lain adalah adanya kemampuan dari senyawa kelompok ini untuk berkondensasi dengan gugus geranil pada posisi C-3, seperti ditunjukkan oleh senyawa artonin H (62) yang berhasil diisolasi dari kulit batang A. rigida (Hano dkk., 1990 b). 62 O O OH HO OH HO OH e. Oksepinoflavon
oksepin pada kelompok ini terbentuk melalui reaksi siklisasi oksidatif yang menghasilkan ikatan – C – O – C – antara gugus OH pada C-2’ dengan C-10 dari gugus isopren pada C-3. Reaksi ini diperlihatkan pada pembentukan senyawa morusin hidroperoksida yang berasal dari senyawa morusin, melalui iradiasi menggunakan lampu merkuri bertekanan tinggi (Hakim dkk., 2005).
O O OH OH OH O O O OH O OH O OOH Iradiasi morusin O O OH O OH O OO H O O OH O morusin hidroperoksida O OOH OH 2' 3 9 10
Gambar II.17 Reaksi pembentukan senyawa kelompok oksepinoflavon
(Hakim dkk., 2005)
Senyawa golongan oksepinoflavon yang pertama kali diisolasi adalah caplasin (66) yang berasal dari kayu batang A. chaplasha (Rao, 1972). Beberapa senyawa golongan oksepinoflavon yang berhasil diisolasi dari Artocapus diperlihatkan pada Tabel II.9 dan Gambar II.18.
Tabel II.9. Distribusi senyawa oksepinoflavon pada Artocarpus
Nama senyawa Spesies Bagian Tumbuhan
Asal
tumbuhan Pustaka Siklointegrin (63) A. integer Kayu batang India Pendse, 1976
Artonin S (64)
Isosikloheterofilin (65)
A. heterophyllus Kulit batang India Indonesia Aida, 1994 Rao, 1973 Caplasin (66) A. chaplasha A. maingayii A. champeden Kayu batang Kulit batang Kulit akar India Indonesia Indonesia Rao, 1972 Hakim, 2006 Hakim, 2005
O H3CO OH O O OH O H3CO OH O O OH HO O H3CO OH O O OH HO O H3CO OH O O OH HO O H3CO OH O O OH HOO O O OH O O OH HO 63 64 65 66 67 68
Gambar. II.18 Struktur senyawa kelompok oksepinoflavon dari Artocarpus
Senyawa-senyawa pada Gambar II.18 memperlihatkan, bahwa prekursor senyawa kelompok oksepinoflavon adalah senyawa kelompok 3-prenilflavon yang memiliki pola 2’,4’-dioksigenasi di cincin B, kecuali senyawa oksisiklointegrin (68) yang diperoleh dari A. integer (Pendse, 1976) disarankan berasal dari senyawa kelompok 3-prenilflavon dengan pola 2’, 4’, 5’-trioksigenasi di cincin B.
f. Piranoflavon
Seperti halnya senyawa kelompok oksepinoflavon, senyawa piranoflavon juga merupakan turunan dari senyawa 3-prenil flavon. Pembentukan senyawa kelompok ini secara biogenesis disarankan berasal dari hasil reaksi siklisasi oksidatif antara gugus OH pada C-2’ dengan C-9 dari gugus isopren pada C-3 seperti diperlihatkan pada Gambar II.19.
Gambar II.19 Saran biogenesis pembentukan senyawa kelompok piranoflavon
Berdasarkan ciri struktur senyawa piranoflavon yang diisolasi dari beberapa spesies Artocarpus, maka kelompok senyawa ini dapat dibedakan menjadi dua jenis, yaitu senyawa piranoflavon dengan pola 2’4’-dioksigenasi di cincin B serta senyawa piranoflavon dengan pola 2’,4’,5’-trioksigenasi di cincin B.
Jenis kelompok senyawa piranoflavon dengan pola 2’4’-dioksigenasi di cincin B ditunjukkan pada Tabel II.10 dan Gambar II.20.
Tabel II.10. Senyawa piranoflavon dengan pola dioksigenasi di cincin B
Nama senyawa Spesies Bagian Tumbuhan Asal tumbuhan Pustaka Sikloartokarpin (17) A. champeden A. maingayii A. kemando
Kulit batang Indonesia Hakim, 2006
Isosiklomorusin (18) A. altilis Kayu batang Formosa Chen, 1993 Siklokomunol (69) A communis Kulit akar Formosa Lin, 1992 Siklokomunin (70) A communis A. champeden Kulit akar Kulit batang Formosa Indonesia Lin, 1992 Syah, 2004 Sikoheterofilin (71) A. heterophyllus Kulit akar
O O OH OH O HO O O OH OH O HO 69 70 O O H3CO OH OH O 17 O O HO OH OCH3 O 71 O O OH OH O O 18 O O OH OH O HO 72 O O OH OH O O 73
Gambar II.20 Struktur senyawa piranoflavon dengan pola dioksigenasi
di cincin B
Berdasarkan gambar dan tabel tersebut terlihat bahwa senyawa piranoflavon dengan pola dioksigenasi di cincin B memiliki keanekaragaman struktur yang disebabkan oleh adanya gugus isoprenil sebagai subtituen pada cincin A. Gugus isoprenil pada cincin A tersebut dapat berada dalam keadaan bebas atau tersiklisasi dengan melibatkan gugus hidroksil pada C-7 untuk membentuk cincin kromen (2,2 dimetil piran) seperti diperlihatkan oleh senyawa 18 dan 73.
O O HO OH OH OH O 74 O O OH OCH3 O HO OH 75 O O OH OH OH O H3CO 76 O O OH OH O H3CO OCH3 77 O O OH OCH3 OH O O 78 O O OH OH O O OH 79
Gambar. II. 21 Struktur senyawa piranoflavon dengan pola trioksigenasi
di cincin B
Seperti halnya pada kelompok senyawa piranoflavon dengan pola dioksigenasi pada cincin B, senyawa piranoflavon dengan pola trioksigenasi pada cincin B juga memiliki substituen berupa gugus isoprenil pada cincin A yang terikat pada C-6 dan atau C-8 yang berada dalam keadaan bebas atau tersiklisasi.
g. Dihidrobenzosanton dan furanodihidrobenzosanton
Kelompok senyawa dihidrobenzosanton merupakan turunan senyawa 3-prenilflavon yang memiliki pola 2’,4’,5’-trioksigenasi di cincin B. Penelusuran literatur sejauh ini belum pernah melaporkan adanya senyawa kelompok dihidrobenzosanton atau furanodihidrobenzosanton yang berasal dari kelompok senyawa 3-prenil-2’4’-dioksigenasi di cincin B. Oleh karena itu, selain adanya gugus isoprenil pada posisi C-3, ternyata gugus hidroksil dengan orientasi orto pada cincin B, yaitu pada posisi C-4’ dan C- 5’ merupakan gugus yang penting pula pada pembentukan kerangka dihidrobenzosanton dan furano-dihidrobenzosanton.
3-prenilflavon dan dilanjutkan dengan reaksi siklisasi dari radikal yang dihasilkan, seperti diperlihatkan pada Gambar II.22. Pada gambar tersebut ditunjukkan reaksi siklisasi oksidatif yang terjadi pada senyawa artonin E (15) yang telah teroksidasi menghasilkan senyawa sikloartobilosanton (20) yang memiliki kerangka furanodihidrobenzosanton serta artobilosanton (19) yang memiliki kerangka dihidrobenzosanton. O O O HO OH OH OH Artonin E (15) O O HO OH OH - e O2 O2 - H+ O O HO OH O OOH O O HO OH O OOH H O O HO OH O OOH H O O HO OH OH OOH H H2O2 H2O2 O O O HO OH O OH Sikloartobilosanton (20) O O O HO OH OH OH Artobilosanton (19)
Gambar II.22 Saran biogenesis pembentukan kerangka dihidrobenzosanton (19)
dan furanodihidrobenzosanton (20) dari 3-prenilflavon (15)
(Nomura dkk., 1998)
O OH OH HO O OH O O OCH3 OH HO O OH O O OH HO O OH H3CO O O OH HO O OH OH O O OH HO O OH HO O O OH HO O OH O O 19 80 81 82 83 84
Gambar. II.23 Struktur senyawa kelompok dihidrobenzosanton dari Artocarpus
O H3CO O OH HO OH O O O OH HO OH O HO O OH HO OH O O O OH HO OH O O O OH HO OH O O OH HO OH O 86 20 89 90 91 92 O H3CO O OH HO OH 85 O O HO O O OH HO OH 87 O O H3CO O OH HO OH O 88 O O O O O
Gambar. II.24 Struktur senyawa kelompok furanodihidrobenzosanton
dari Artocarpus
h. Kuinodihidrosanton
O O HO OH O O O OCH3 O OH O O O OCH3 O O OH O O O OCH3 O O O OH O O O O O O OH O O O O OCH3 93 94 95 96 97
Gambar. II.25 Struktur senyawa kelompok kuinohidrosanton dari Artocarpus
Keanekaragaman senyawa kelompok ini terjadi karena adanya substituen yang terikat pada kerangka utama kelompok senyawa ini. Substituen yang lazim terikat pada kerangka utama kelompok senyawa ini adalah, gugus hidroksil, metoksil dan gugus isopren. Gugus isopren yang terikat pada kerangka utama kelompok ini dapat berada dalam keadaan bebas atau tersiklisasi membentuk cincin kromen.
i. Tetrahidrosanton
O OH O OH HO O OH O O O O OH O O O O OH HO H O O O O OH HO H O OH O O O Retro Diels-Alder 98 19 O O O O OH HO H O
Gambar II.26 Saran biogenesis pembentukan artonol A (98)
dari artobilosanton (19) (Nomura dkk., 1998)
Gambar II.26 menunjukkan bahwa oksidasi pada kelompok senyawa dihidrobenzosanton [artobilosanton (19)] menghasilkan kelompok senyawa kuinodihidrosanton. Selanjutnya terjadi reaksi retro Diels-Alder pada kelompok senyawa kuinodihidrosanton kelompok senyawa tetrahidrosanton [artonol A (98)].
j. Siklopentenosanton dan santonolida
Penelusuran literatur menunjukkan bahwa beberapa senyawa kelompok siklopentenosanton telah berhasil diisolasi dari kulit batang A. heterophyllus (Aida dkk., 1994) yaitu artonin Q (100) dan artonin R (101). Selain itu, artoindonesianin C (99) yaitu suatu senyawa yang berhasil diisolasi dari A. teysmanii (Makmur, 2000). O O COOCH3 OH O O OH O COOCH3 OH O O OH O O COOCH3 OH O O OH O OH 99 100 101 A 8 6
Gambar II.27 memperlihatkan bahwa kelompok senyawa ini memiliki keragaman berdasarkan gugus isopren yang terikat pada cincin A, dimana gugus isopren tersebut dapat terikat pada C-6 dan atau C-8.
Selanjutnya, penelusuran literatur memperlihatkan bahwa sejauh ini satu-satunya kelompok santonolida adalah senyawa artonol B (102) yang berhasil diisolasi dari A. communis (Aida, 1997) dan A. lanceifolius (Hakim, 2002).
O O O O O OH O 102
Secara biogenesis senyawa kelompok siklopentenosanton dan santonolida ini berasal dari hasil oksidasi senyawa kelompok dihidrobenzosanton, yang dilanjutkan dengan reaksi penataan ulang Favorskii, seperti diperlihatkan pada Gambar II.28. O OH O OH O OH HO O O O O O H O O O OH O OH O O OH O O H O H O O OH O OH O O CH3 O O O OH O O C CH3 O O H O O C CH3 O OH O OH O O CH3 O O O O O OH O H O 2H 2 -CO 2 [O ] + H 2O - H 2O artobilosanton (1 9) artonol B (1 02) Senyawa kelompok siklopen tenosanton
Gambar II.28 Saran biogenesis pembentukan kelompok senyawa
Dari beberapa jenis senyawa santon yang telah berhasil diisolasi dari Artocarpus, terlihat bahwa senyawa dengan kerangka dihidrobenzosanton, yaitu artobilosanton (19) merupakan senyawa prekursor untuk pembentukan senyawa-senyawa turunan santon.
II.2.2 Senyawa turunan fenol lainnya dari Artocarpus
a. Adduct Diels-Alder
Secara biogenesis senyawa kelompok ini merupakan hasil reaksi siklisasi intermolekul (reaksi Diels-Alder) antara senyawa calkon terprenilasi (dienofil) dengan senyawa turunan dihidroprenilfenol (diena) seperti ditunjukkan pada Gambar II.29. OH HO OH OH OH HO OH O O HO HO OH OH OOH OH OH HO O isobavacalkon (131) moracalkon A (6) kuwanon R (104) Reaksi Diels-Alder
Gambar II.29 Reaksi pembentukan senyawa kelompok Adduct Diels-Alder
(Nomura dkk., 1998)
HO HO OH OOH OH HO O OH O 105 HO HO OH OH OOH OH HO O HO HO OH OH OOH OH HO O 103 104
Gambar II.30 Struktur senyawa kelompok adduct Diels-Alder
dari Artocarpus
Senyawa adduct Diels-Alder yang diperoleh dari Artocarpus lazimnya berasal dari calkon terprenilasi. Senyawa calkon terprenilasi tersebut bertindak sebagai sumber diena maupun sumber dienofil pada proses pembentukan senyawa adduct pada Artocarpus.
b. Stilben
gugus metoksi pada C-5 dilaporkan berhasil diisolasi dari kulit kayu A. gomezianus (Hakim dkk., 2002). HO OH OH HO OH OH OH HO OH OH OH HO OH OH OH HO OH OCH3 HO OH OH O 106 107 108 109 110 111 3 5 4' 2'
Gambar II.31 Struktur senyawa kelompok stilbenoid dari Artocarpus
Berdasarkan pola oksigenasinya, maka senyawa stilben pada Artocarpus dapat dibedakan menjadi senyawa stilben dengan pola 3,5,4’-trihidroksistilben dan 3,5,2’,4’-tetrahisroksistilben. Selanjutnya Gambar II.31 memperlihatkan adanya kecenderungan posisi gugus isoprenil pada kerangka stilben Artocarpus. Umumnya gugus isoprenil pada kerangka stilben tersebut akan terikat pada C-4.
Selanjutnya, senyawa stilben pada Artocarpus dilaporkan juga dapat berupa dimer. Senyawa dimer stilben yang telah dilaporkan, yaitu artogomezianol (112) dan andalasin A (113) yang berhasil diisolasi dari A. gomezianus (Likhitwitayawuid dkk., 2001). HO OH OH OH OH HO OH OH OH OH OH 113 112 OH OH HO OH
Berdasarkan monomer pembentuknya, senyawa dimer stilben yang telah dilaporkan tersebut berasal dari jenis 3,5,2’,4’-tetrahidroksistilben.
c. Senyawa turunan fenol lainnya
Senyawa turunan fenol lain yang diperoleh dari Artocarpus, antara lain senyawa artokarpol A (115) (Chung dkk., 2000), artokarpol F (116) (Ko dkk., 2001) dan artokarpol G (114) (Lu dk., 2002) dari A. rigida. Secara biogenesis senyawa-senyawa tersebut berasal dari reaksi kondensasi antara senyawa-senyawa stilbenoid dengan gugus geranil yang termodifikasi.
O O HO OH O H O O HO OH O O HO OH O O H H H 114 115 116
Gambar II.33 Struktur senyawa kelompok polifenol terprenilasi
dari Artocarpus
O HO OH OH O OH OCH3 HO 117 118 2' 4' 3 5
Gambar II.34 Struktur senyawa kelompok 2-arilbenzofuran dari Artocarpus
Selanjutnya, senyawa heterofilol (119) dilaporkan telah berhasil diisolasi dari kayu akar A. heterophyllus (Lin dkk., 1995). Apabila dikaji strukturnya, maka senyawa ini berasal dari kelompok senyawa stilbenoid dengan pola oksigenasi dan prenilasi yang tidak lazim ditemukan pada genus Artocarpus. Oksigenasi pada senyawa ini terjadi pada posisi 2,4,2’,4’-tetraoksigenasi stilben dengan gugus isopren pada posisi C-5 dan isopren termodifikasi pada C-6. Selanjutnya reaksi siklisasi oksidatif terjadi antara gugus isoprenil termodifikasi di C-6 dengan olefin dari kerangka stilbenoid dan gugus hidroksil pada cincin B menghasilkan cincin C dan D. O H H H3CO OCH3 OH 119 2 4 5 2' 4' A B C D 6
Gambar II.35 Struktur senyawa heterofilol (119)
H OH OH O 120 H OH HO OH O 121
Gambar II.36 Struktur senyawa turunan benzaldehida dari Artocarpus
II.2.3 Senyawa non fenolik dari Artocarpus
Selain senyawa turunan fenol beberapa senyawa turunan non-fenol juga berhasil ditemukan pada Artocarpus, misalnya golongan triterpenoid. Senyawa triterpenoid tersebut terdiri atas senyawa triterpenoid tetrasiklik dengan kerangka sikloartan dan senyawa triterpenoid pentasiklik dengan kerangka glutan.
Senyawa triterpenoid dengan kerangka sikloartan yang berhasil diisolasi dari Artocarpus, yaitu sikloartenol (122) dari A. champeden (Achmad dkk., 1996) dan A. altilis (Altman dkk., 1976). Dari A. champeden juga telah berhasil diisolasi senyawa dengan kerangka yang sama, yaitu sikloeukalenol (123), 2,4-metilensikloartenon (124) dan sikloartenon (125) (Achmad dkk., 1996). Senyawa sikloartenon (125) ini juga diisolasi dari A. heterophyllus (Dayal dkk., 1974). Kemudian, selain sikloartenon (125) dari A. heterophyllus juga dilaporkan telah ditemukan senyawa (24R)-9,19-siklolanost-3-on-24,25-diol (126) dan (24S)-9,19-siklolanost-3-on-24,25-diol (127) (Barik dkk., 1997). HO H O OH OH HO H O H O H 122 123 124 125 126 127 24 (24R) (24S)
Selanjutnya, senyawa triterpen pentasiklik kerangka glutan yang dikenal sebagai glutinol (128) telah diisolasi dari A. champeden (Achmad dkk., 1996).
HO
H
128
II.3 Bioaktivitas Metabolit Sekunder dari Tumbuhan Artocarpus
Tinjauan etnobotani menunjukkan bahwa masyarakat Indonesia telah menggunakan tumbuhan genus Artocarpus sebagai bahan obat tradisional yang dikenal sebagai “jamu”. Genus ini antara lain dipergunakan untuk mengobati berbagai penyakit seperti inflamasi, malaria, demam dan antifertilitas (Takahashi dkk., 1988). Berdasarkan tinjauan tersebut maka kajian bioaktivitas metabolit sekunder dari Artocarpus banyak dilakukan.
Laporan-laporan penelitian mengenai aktivitas biologi dari beberapa metabolit sekunder yang berasal dari tumbuhan Artocarpus memperlihatkan hasil yang menarik terutama untuk senyawa-senyawa turunan flavonoid terprenilasi, antara lain senyawa artokarpin (14) yang menunjukkan sifat toksik tehadap benur udang Artemia salina. Selain itu, senyawa artokarpin (14) dan heteroflavanon A (42) dilaporkan memiliki aktivitas dalam menghambat transport asam amino leusin pada membran usus ulat sutera Bombyx mori (Hakim dkk., 1998). Aktivitas serupa juga diperlihatkan oleh senyawa siklocampedol (74) (Achmad dkk., 1996; Parenti dkk., 1997). Selain dilaporkan memiliki aktivitas toksik terhadap benur udang dan penghambat transport asam amino, senyawa artokarpin (14) juga dilaporkan memiliki aktivitas penghambatan terhadap enzim 5α-reduktase serta memiliki aktivitas sebagai pemutih kulit (Shimizu dkk., 2000).
dari metabolit sekunder. Beberapa senyawa diantaranya menunjukkan aktivitas yang signifikan, seperti ditunjukkan pada Tabel II.11 (Hakim dkk., 2006).
Tabel II.11 Aktivitas sitotoksik senyawa flavonoid dari Artocarpus
terhadap sel murine leukemia P-388 *
Nama Senyawa Kelompok Senyawa IC50 (μg/mL)
Artokarpanon (8) Flavanon 19,3 Artokarpin (14) 3-Prenilflavon-teroksigenasi -2’,4’ 1,9 Artonin E (15) 3-Prenilflavon-teroksigenasi -2’,4’,5’ 0,6 Caplasin (66) Oksepinoflavon 2,0 Sikloartokarpin (17) Piranoflavon 3,9 Artobilosanton (19) Dihidrobenzosanton 1,7 Sikloartobilosanton (20) Furanodihidrobenzosanton 3,2 Artonin O (91) Kuinodihidrobenzosanton 0,9 Artonol B (102) Santonolida > 100
* Senyawa dikategorikan sangat aktif apabila memiliki nilai IC50 0-2,0 μg⁄mL, aktif apabila nilai
IC50 2,1-4,0μg⁄mL, dan tidak aktif apabila nilai IC50 > 4,0 μg⁄mL (Alley, 1998)
Tabel II.10 menunjukkan bahwa kelompok senyawa 3-prenilflavon yang teroksigenasi pada posisi C-2’, C-4’ dan C-5’ yaitu artonin E (15), memiliki aktivitas sitotoksik paling tinggi terhadap sel murine leukemia P-388 dibandingkan kelompok senyawa lainnya. Tabel tersebut juga memperlihatkan bahwa modifikasi lebih lanjut dari gugus isoprenil pada posisi C-3 yang membentuk kelompok senyawa turunan santon tampaknya menurunkan aktivitas sitotoksik. Hal ini menunjukkan bahwa adanya gugus isoprenil bebas pada posisi C-3 memiliki peranan yang sangat signifikan terhadap aktivitas sitotoksik senyawa turunan flavonoid dari Artocarpus (Hakim, 2006).