PEMBUATAN PUPUK KALIUM SULFAT
DARI LIMBAH BIODIESEL MINYAK GORENG BEKAS
NANI SURYANI
PROGRAM STUDI KIMIA
FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH
JAKARTA
PEMBUATAN PUPUK KALIUM SULFAT
DARI LIMBAH BIODIESEL MINYAK GORENG BEKAS
SKRIPSI
Sebagai Salah Satu Syarat untuk Memperoleh Gelar Sarjana Sains Program Studi Kimia
Fakultas Sains dan Teknologi
Universitas Islam Negeri Syarif Hidayatullah Jakarta
Oleh: NANI SURYANI
109096000040
PROGRAM STUDI KIMIA FAKULTAS SAINS DAN TEKNOLOGI
UNIVERSITAS ISLAM NEGERI SYARIF HIDAYATULLAH JAKARTA
Bismillahirrahmaanirrahiim…
“Sesungguhnya sesudah kesulitan itu ada kemudahan” (Al-
Insyirah: 6)
Sebuah kado kecil di bulan Oktober…
Kado kecil yang sejak dahulu ingin kupersembahkan untuk kedua
orang tuaku…
Bapak, mama…
Alhamdulillah…
Dengan semangat kegigihan, aku selalu berusaha untuk terus
mewujudkan ini semua..
Semoga melalui goresan ini menjadi langkah awalku untuk menjadi
pribadi yang lebih bermanfaat untuk bangsa dan agama…
ABSTRAK
NANI SURYANI. Pembuatan Pupuk Kalium Sulfat dari Limbah Biodiesel Minyak Goreng Bekas. Isalmi Aziz, MT. dan Hendrawati, M.Si.
Masalah limbah akhir-akhir ini menjadi perhatian di lingkungan kita termasuk limbah domestik atau rumah tangga. Salah satu bahan pokok yang menghasilkan limbah adalah minyak goreng. Untuk mengurangi limbah tersebut, dapat dilakukan dengan memanfaatkannya menjadi sumber energi alternatif dan lebih ramah lingkungan yaitu dalam bentuk biodiesel. Dalam pembuatan biodiesel tersebut dihasilkan limbah crude glycerol yang mengandung katalis KOH, sehingga crude glycerol ini dapat dimanfaatkan dalam proses pembuatan pupuk kalium sulfat dengan cara KOH yang terdapat pada crude glycerol ditambahkan dengan asam sulfat pekat sehingga menghasilkan kalium sulfat. Penelitian ini bertujuan untuk menentukan kondisi optimum (waktu reaksi, suhu, dan konsentrasi asam sulfat) pembuatan pupuk kalium sulfat dan menentukan kualitas pupuk kalium sulfat yang dihasilkan dari limbah biodiesel minyak goreng bekas. Kondisi optimum (dilihat dari jumlah pupuk terbanyak yang dihasilkan) pembuatan pupuk kalium didapatkan pada waktu reaksi 30 menit, suhu 600C dan konsentrasi asam sulfat yang digunakan 2,5% (v/v). Kualitas pupuk kalium sulfat yang dihasilkan pada kondisi optimum adalah kadar kalium 55%, kadar sulfur 18%, kadar klorin 0,006% dan kadar air 1% dengan konversi reaksi sebesar 31%. Analisa sifat fisika kimia ini menunjukkan bahwa pupuk kalium sulfat yang dihasilkan memenuhi persyaratan SNI pupuk kalium sulfat tahun 2005.
ABSTRACT
NANI SURYANI. Potassium Sulfate Fertilizer Production of Biodiesel from Waste of Used Cooking Oil. Isalmi Aziz, MT. dan Hendrawati, M.Si.
The problem of waste recently became attention in our environment including domestic or household waste. One of the essential commodities that produce waste is cooking oil. To reduce the waste, it can be conducted by use them into the alternative energy sources and more environmentally friendly is in biodiesel form. In the manufacture of biodiesel, was produced a crude glycerol of waste that can still be used in the process of the manufacture of potassium sulphate fertilizer by way, that KOH on crude glycerol is added with concentrated sulfuric acid to produce potassium sulfate fertilizer. This research is aimed to determine the condition (time reaction, temperature, and the concentration of sulphuric acid) the manufacture of potassium sulphate fertilizer and determining the quality of potassium sulphate fertilizer produced from the wastes of biodiesel used cooking oil. Optimum conditions of manufacture potassium sulphate fertilizers (seen from the amount of manure produced the highest) obtained in the 30 minutes reaction, temperature 600C and concentration of sulphuric acid used 2.5 % (v/v). The quality of potassium sulphate fertilizer that produced on optimum the conditionis about 55% potassium, 18 % sulphur level, 0,006 % chlorine level and the water level is about 1 % with 50 % conversion value . This analysis of chemical and physical traits showed that potassium sulphate fertilizer produced is meet the standards of SNI requirements of potassium sulphate fertilizer, 2005.
Keywords: Used Cooking Oil, Crude Glycerol, KOH, Potassium Sulfate Fertilizer.
ix
KATA PENGANTAR
Bismillahirrahmaanirrahiim,
Assalaamu’alaikum Wr. Wb.
Puji dan syukur selalu kita panjatkan kehadirat Allah SWT yang telah melimpahkan rahmat dan karunia-Nya yang tiada henti kepada penulis sehingga penulis dapat menyelesaikan skripsi yang berjudul “PEMBUATAN PUPUK KALIUM SULFAT DARI LIMBAH BIODIESEL MINYAK GORENG BEKAS”. Shalawat dan salam semoga senantiasa tercurahkan kepada suri teladan kita Nabi Muhammad SAW, beserta keluarga, sahabatnya dan para pengikutnya yang senantiasa istiqomah dalam menjalankan sunnahnya hingga akhir zaman, dan semoga kita semua termasuk pengikutnya yang istiqomah dalam mengemban risalahnya. Aamiin
Ada pun tujuan dari penulisan skripsi ini adalah untuk mengembangkan penelitian di bidang kimia dan untuk memenuhi syarat akhir kelulusan di jenjang pendidikan strata 1 (S1). Dalam penulisan dan penyusunan skripsi ini penulis menyadari begitu banyaknya dukungan dan bimbingan yang telah diberikan dari berbagai pihak. Oleh karena itu, penulis mengucapkan terima kasih dan rasa hormat yang mendalam kepada:
1. Isalmi Aziz, MT. selaku dosen pembimbing I yang telah membimbing penulis dengan penuh keikhlasan dan kesabaran.
2. Hendrawati, M.Si selaku dosen pembimbing II yang telah membimbing dan memberikan ilmu pengetahuan kepada penulis.
x
3. Drs. Dede Sukandar, M.Si selaku Ketua Program Studi Kimia Fakultas Sains dan Teknologi.
4. Dr. Agus Salim, M.Si selaku Dekan Fakultas Sains dan Teknologi, Universitas Islam Negeri Syarif Hidayatullah Jakarta.
5. Kedua orang tuaku Darta dan Maryati yang telah memberikan pengorbanan dalam materi, do’a dan kasih sayang yang tulus tiada batas kepada penulis.
6. Seluruh Dosen Program Studi Kimia UIN Syarif Hidayatullah Jakarta yang telah memberikan ilmu pengetahuan serta bimbingan kepada penulis selama mengikuti perkuliahan, semoga ilmu yang telah Bapak dan Ibu sampaikan memberikan manfaat dan mendapatkan keberkahan dari Allah SWT.
7. Ibu Anggia Soediro, selaku pimpinan Women’s International Club (WIC) Scholarship yang telah memberikan bantuan dukungan material kepada penulis.
8. Kepada adik dan kakakku tersayang Ka Dewi, Deti dan Mahran, yang selalu memberikan semangat dan keceriaan kepada penulis.
9. Kepada teman-temanku seperjuangan angkatan 2009, Fitri, Nia, Adawiyah, Tiara, Putri, Rafi, Dhoni, Luthfi, Hafiz, dll yang masih tetap semangat dalam menyelesaikan studi S1-nya.
10. Kepada kakak-kakak dan adik-adik kelas yang telah memberikan masukan dan motivasi kepada penulis.
xi
11. Semua pihak yang telah membantu penulis secara langsung maupun tidak langsung yang tidak dapat disebutkan satu per satu.
Penulis menyadari bahwa dalam penyusunan skripsi ini masih banyak kekurangan, baik dalam penulisan maupun penyusunannya. Maka penulis memohon kritik dan saran yang membangun dari para pembaca untuk penyusunan skripsi yang lebih baik di masa yang akan datang.
Semoga skripsi ini bermanfaat bagi penulis dan para pembaca, terutama untuk menambah pengetahuan mengenai kimia khususnya di bidang pemanfaatan energi. Aamiin
Wassalaamu’alaikumWr. Wb.
Jakarta, Oktober 2013
xii DAFTAR ISI
Hal
KATA PENGANTAR ... ix
DAFTAR ISI ... xii
DAFTAR GAMBAR ... xv
DAFTAR TABEL ... xvii
DAFTAR LAMPIRAN ... xviii
BAB I PENDAHULUAN ... 1 1.1. Latar Belakang ... 1 1.2. Rumusan Masalah ... 4 1.3. Hipotesis ... 5 1.4. Tujuan Penelitian ... 5 1.5. Manfaat Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 6
2.1. Pupuk ... 6
2.1.1. Pupuk Kalium ... 9
2.1.2. Pupuk Kalium Sulfat ... 12
2.2. Biodiesel ... 14
2.3. Minyak Goreng ... 18
2.4. Spektrofotometri UV ... 21
2.5. Spektrofotometri Serapan Atom ... 25
xiii
2.5.2. Komponen Utama Instrumentasi Spektrofotometer Serapan
Atom ... 28
BAB III METODE PENELITIAN ... 31
3.1. Waktu dan Tempat Penelitian ... 31
3.2. Alat dan Bahan ... 31
3.2.1. Alat ... 31
3.2.2. Bahan ... 31
3.3. Prosedur Kerja ... 32
3.3.1. Pembuatan Biodiesel ... 32
3.3.2. Pembuatan Pupuk Kalium ... 32
3.3.3. Analisa Kadar Kalium dengan AAS (Atomic Absorption Spectrophometry) ... 33
3.3.4. Analisa Kadar Sulfur dengan Spektrofometri ... 34
3.3.5. Analisa Kadar Klorin ... 35
3.3.6. Analisa Kadar Air ... 36
BAB IV HASIL DAN PEMBAHASAN ... 37
4.1. Pembuatan Pupuk Kalium Sulfat dari Crude Glycerol ... 37
4.2. Optimasi Kondisi Reaksi Pembuatan Pupuk Kalium Sulfat ... 40
4.2.1. Pengaruh Waktu Reaksi Terhadap Massa Pupuk K2SO4 ... 41
4.2.2. Pengaruh Suhu Reaksi Terhadap Massa Pupuk K2SO4 ... 43
4.2.3. Pengaruh Konsentrasi H2SO4 Terhadap Massa Pupuk K2SO4 ... 45
4.3. Hasil Analisa Sifat Fisik dan Kimia Pupuk Kalium Sulfat ... 48
4.3.1. Analisa Kadar Kalium Pada Pupuk Kalium Sulfat ... 49
xiv
4.3.3. Analisa Kadar Klorin ... 51
4.3.4. Analisa Kadar Air ... 52
4.4. Konversi Reaksi Pembuatan Pupuk Kalium Sulfat ... 53
BAB V KESIMPULAN DAN SARAN ... 55
5.1. Kesimpulan ... 55
5.2. Saran ... 55
DAFTAR PUSTAKA ... 56
xv
DAFTAR GAMBAR
Gambar 1. Reaksi Transesterifikasi pada Pembuatan Biodiesel ... 16
Gambar 2. Struktur Gliserol ... 18
Gambar 3. Struktur Trigliserida ... 19
Gambar 4. Minyak Goreng Bekas ... 20
Gambar 5. Diagram Spektrofotometer ... 21
Gambar 6. Spektrofotometer Berkas Tunggal ... 22
Gambar 7. Spektrofotometer Berkas Ganda ... 22
Gambar 8. Skema Alat Monokromator ... 23
Gambar 9. Sel yang Digunakan dalam Spektrofotometer ... 24
Gambar 10. Skema Instrumentasi Spektrofotometer Serapan Atom Berkas Ganda ... 28
Gambar 11. Pemisahan Crude Glycerol dengan Biodiesel ... 38
Gambar 12. Crude Glycerol Setelah Ditambahkan H2SO4 Pekat ... 38
Gambar 13. Pemisahan Endapan K2SO4 dengan Residu ... 39
Gambar 14. Pemisahan Larutan K2SO4 dengan Residu dan Asam Lemak Bebas ... 39
Gambar 15. Pupuk Kalium Sulfat ... 40
Gambar 16. Hasil Pupuk K2SO4 Variasi Waktu (a) 15 Menit, (b) 30 Menit ... 42
Gambar 17. Hasil Endapan Variasi Waktu 60 Menit ... 42
Gambar 18. Hasil Endapan Variasi Waktu 120 Menit ... 43
Gambar 19. Hasil Pupuk K2SO4 Variasi Suhu (a) 300C , (b) 400C, (c) 600C, (d) 800C ... 45
xvi
Gambar 20. Hasil Pemisahan Filtrat K2SO4 Variasi Konsentrasi 1% ... 46 Gambar 21. Hasil Pupuk K2SO4 Variasi Konsentrasi (a) 2%, (b) 2.5%,
(c) 5% ... 47 Gambar 22. Titrasi Cl- dengan AgNO3 ... 51
xvii
DAFTAR TABEL
Tabel 1. Perkembangan Harga Pupuk Kalium di Dunia ... 11
Tabel 2. Syarat Mutu Pupuk Kalium Sulfat ... 12
Tabel 3. Sifat Fisik Gliserol ... 17
Tabel 4. Panjang Gelombang Serapan Maksimum Berbagai Atom Logam ... 27
Tabel 5. Variabel Penelitian ... 33
Tabel 6. Pengaruh Waktu Reaksi Terhadap Massa Pupuk K2SO4 yang Dihasilkan ... 41
Tabel 7. Pengaruh Suhu Terhadap Massa Pupuk K2SO4 yang Dihasilkan ... 44
Tabel 8. Pengaruh Konsentrasi H2SO4 Terhadap Massa Pupuk K2SO4 yang Dihasilkan ... 46
xviii
DAFTAR LAMPIRAN
Lampiran 1. Skema Kerja Penelitian ... 61
Lampiran 2. Perhitungan Kadar Kalium dalam Kalium Sulfat ... 62
Lampiran 3. Perhitungan Mol KOH yang Bereaksi ... 63
Lampiran 4. Perhitungan Mol KOH Mula-mula ... 64
Lampiran 5. Perhitungan Konversi Reaksi ... 65
Lampiran 6. Perhitungan Kadar Sulfur ... 66
Lampiran 7. Perhitungan Mol Sulfat dalam Kalium Sulfat ... 67
Lampiran 8. Perhitungan Standarisasi AgNO3 dengan NaCl 0,01N ... 68
Lampiran 9. Perhitungan Kadar Klorin (Cl-) ... 69
Lampiran 10. Perhitungan Kadar Air ... 70
Lampiran 11. Perhitungan Massa K2SO4 Teoritis ... 71
Lampiran 12. Perhitungan Kadar Kalium dalam K2SO4 Secara Teoritis ... 72
Lampiran 13. Perhitungan Kadar Sulfur dalam K2SO4 Secara Teoritis ... 73
Lampiran 14. Kurva Kalibrasi Standar Kalium ... 74
1 BAB I
PENDAHULUAN
1.1. Latar Belakang
Saat ini masalah-masalah yang terjadi di lingkungan kita menjadi salah satu hal yang hangat untuk dibicarakan. Mulai dari masalah ketersediaan sumber pangan, papan dan sandang hingga masalah limbah yang dihasilkan manusia setiap harinya. Oleh karena itu, sebagai makhluk ciptaan-Nya kita memiliki kewajiban untuk dapat mengatasi setiap masalah-masalah yang terjadi di lingkungan kita dengan menggunakan akal kita. Sebagaimana tertulis dalam firman-Nya Surah Yunus ayat 101, yang berarti:
Katakanlah: "Perhatikanlah apa yang ada di langit dan di bumi.
Tidaklah bermanfaat tanda kekuasaan Allah dan Rasul-rasul yang memberi
peringatan bagi orang-orang yang tidak beriman".(Depag, 1987)
Dari kutipan ayat Allah SWT tersebut dijelaskan bahwa Allah SWT memerintahkan kita untuk memperhatikan segala hal yang ada di sekitar lingkungan kita, dengan memanfaatkan akal kita untuk dapat berfikir memahami dan menganalisa berbagai masalah yang terdapat di sekitar kita untuk dicari solusinya. Berdasarkan firman-Nya yang lain Allah SWT juga memerintahkan kita untuk berfikir dan mengambil manfaat dari setiap hal yang terjadi disekitar kita. Hal ini dapat dilihat pada Surah Ali- Imran ayat 191 yang berbunyi:
2 (yaitu) orang-orang yang mengingat Allah sambil berdiri atau duduk
atau dalam keadan berbaring dan mereka memikirkan tentang penciptaan
langit dan bumi (seraya berkata): "Ya Tuhan Kami, Tiadalah Engkau
menciptakan ini dengan sia-sia, Mahasuci Engkau, Maka peliharalah Kami
dari siksa neraka. (Depag, 1987)
Dalam ayat ini Allah SWT juga menjelaskan bahwa sesungguhnya Dia menciptakan semua ini tidaklah sia-sia. Segala sesuatu semuanya memiliki manfaat jika kita mau berfikir, merenungi dan menganalisanya, dengan tujuan mengembangkan ilmu pengetahuan dan teknologi yang ada di zaman sekarang ini.
Masalah limbah akhir-akhir ini menjadi perhatian di lingkungan kita. Beberapa bahan pokok yang sering kita gunakan dalam kehidupan sehari-hari, dapat pula meninggalkan limbah sehingga mencemari lingkungan apabila tidak dikelola dengan baik. Salah satu bahan pokok yang banyak menghasilkan limbah adalah minyak goreng.
Seperti yang telah kita ketahui, berbagai macam industri yang bergerak dibidang pengolahan pangan mulai dari industri rumah tangga hingga industri yang lebih besar lagi (restoran), menggunakan minyak goreng sebagai bahan untuk mengolah produknya. Semakin sering minyak goreng tersebut digunakan untuk proses penggorengan, akan menimbulkan dampak yang tidak baik untuk kesehatan tubuh kita ketika mengkonsumsi makanan tersebut (Rukmini, A., 2007). Oleh karena itu, untuk mengelola hasil dari limbah-limbah minyak goreng tersebut dapat dilakukan dengan memanfaatkannya
3 menjadi sumber energi baru dan lebih ramah lingkungan yaitu dalam bentuk biodiesel (Imaduddin, et al. 2008).
Pembuatan biodiesel dari minyak goreng bekas (minyak nabati) dilakukan melalui reaksi transesterifikasi dengan alkohol dan katalis seperti KOH. Produk utama yang dihasilkan adalah biodiesel dan produk sampingnya adalah gliserol. Gliserol yang dihasilkan masih merupakan crude glycerol. Pada crude glycerol terkandung katalis KOH. Menurut Yuniwati dan Karim (2009) katalis KOH dapat mempercepat reaksi ke kanan antara trigliserida dan alkohol. Sebagaimana fungsi katalis, yang ikut bereaksi pada saat berlangsungnya reaksi, tetapi dapat diperoleh kembali pada akhir reaksi. Agar katalis KOH ini tidak menjadi limbah yang sia-sia, maka dapat diolah menjadi pupuk kalium sulfat.
Di Indonesia pembuatan pupuk kalium sulfat masih sangat jarang dilakukan. Pupuk kalium sulfat sangat jarang digunakan karena harganya yang cukup mahal jika dibandingkan dengan pupuk kalium yang lainnya seperti kalium klorida (Gunadi, 2009). Oleh karena itu, melalui penelitian ini akan dibuat pupuk kalium sulfat dari limbah biodiesel yang dapat menekan biaya produksi agar relatif lebih murah dan lebih efisien. Selain itu, pupuk kalium sulfat juga mengandung sulfur (belerang) yang juga dibutuhkan oleh tanaman sebagai makro nutrien yang dapat meningkatkan hasil pertanian.
Menurut Setyaningsih, et al.(2007) pembuatan pupuk kalium sulfat dari limbah gliserol hasil samping biodiesel dapat dibuat dari minyak jarak dengan cara menambahkan asam sulfat pekat tetes demi tetes. Konversi reaksi
4 pembuatan pupuk kalium sulfat sebesar 2,8% dengan recovery sebesar 18%. Hasil pengujian pupuk kalium sulfat menunjukkan kadar air sebesar 7,76%, kadar sulfat 61% dan kadar potassium 0,078%.
Sutiyono(2007) juga melakukan penelitian pembuatan kalium sulfat dari kotoran burung puyuh yang mengandung K2O dengan cara menambahkan asam sulfat yang berasal dari air kawah Gunung Ijen. Proses ini menghasilkan kadar K2SO4 sebesar 44.503,5403 (mg/L) dan konversi reaksi sebesar 86,62%, dengan suhu optimum 900C dan lama waktu pengadukan 25 menit.
Merujuk pada referensi penelitian-penelitian sebelumnya, metode yang akan dilakukan pada penelitian ini yaitu dengan menambahkan asam sulfat pekat tetes demi tetes ke dalam crude glycerol yang dihasilkan dari limbah biodiesel minyak goreng bekas. Pupuk kalium sulfat yang dihasilkan diuji kualitasnya sesuai SNI tahun 2005 tentang pupuk kalium sulfat. Analisa kualitas pupuk meliputi, penentuan kadar unsur kalium dengan metode AAS (Atomic Absorption Spectrophotometry), kadar air melalui metode gravimetri,
kadar klorin melalui metode argentometri dan kadar sulfur dengan instrumentasi spektrofotometri.
1.2. Rumusan Masalah
Rumusan masalah dari penelitian ini adalah:
1. Bagaimana pengaruh waktu reaksi, suhu dan konsentrasi asam sulfat terhadap jumlah pupuk kalium sulfat yang dihasilkan?
5 1.3. Hipotesis
Hipotesis dari penelitian ini adalah:
1. Adanya pengaruh waktu reaksi, suhu, dan konsentrasi asam sulfat yang digunakan terhadap jumlah pupuk kalium sulfat yang dihasilkan 2. Pupuk kalium sulfat yang dihasilkan memenuhi standar SNI.
1.4. Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1. Menentukan kondisi optimum (waktu reaksi, suhu dan konsentrasi asam sulfat) pembuatan pupuk kalium sulfat
2. Menentukan kualitas pupuk kalium sulfat yang dihasilkan dari limbah biodiesel minyak goreng bekas.
1.5. Manfaat Penelitian
Penelitian ini diharapkan dapat memberikan kontribusi dan manfaat bagi masyarakat Indonesia, diantaranya:
1. Pemanfaatan limbah industri biodiesel menjadi produk yang bernilai ekonomis dan ramah lingkungan
6 BAB II
TINJAUAN PUSTAKA
2.1. Pupuk
Menurut PP No. 8 tahun 2001, pupuk adalah bahan kimia atau organisme yang berperan dalam penyediaan unsur hara bagi keperluan tanaman secara langsung atau tidak langsung.
Berdasarkan proses terjadinya pupuk dibedakan menjadi 2 (dua) jenis, yaitu: 1. Pupuk alami (organik) yaitu pupuk yang berasal dari pembusukan
makhluk hidup
2. Pupuk buatan (sintetik) yaitu pupuk yang tidak berasal dari pembusukan makhluk hidup.
Berdasarkan unsur hara yang dikandungnya pupuk sintetik dibedakan menjadi 4, yaitu:
1. Pupuk tunggal yaitu pupuk yang hanya mengandung satu unsur hara utama
2. Pupuk campuran adalah campuran dari beberapa pupuk tunggal yang dicampurkan secara manual
3. Pupuk majemuk adalah pupuk yang mengandung lebih dari satu unsur hara di dalamnya
7 4. Pupuk majemuk khusus adalah pupuk majemuk yang dibuat secara
khusus, seperti dalam bentuk tablet atau pellet.
Pupuk mengandung berbagai macam hara tanaman, Hara tanaman merupakan zat-zat yang diperlukan oleh tanaman untuk pertumbuhan, pembentukan jaringan dan kegiatan hidup lainnya (Idrus, F., 1987). Selain mengandung hara tanaman, pupuk juga mengandung bahan lain, yaitu:
1. Zat pembawa atau carrier. Double superfosfat (DS): zat pembawanya adalah CaSO4 dan hara tanamannya fosfor (P).
2. Senyawa-senyawa lain berupa kotoran (impurities) atau campuran bahan lain dalam jumlah relatif sedikit. Misalnya ZA (zwavelzuure amoniak) sering mengandung kotoran sekitar 3% berupa klor, asam
sulfat (H2SO4) dan sebagainya.
3. Bahan mantel (coated) ialah bahan yang melapisi pupuk supaya pupuk mempunyai nilai lebih baik misalnya kelarutannya berkurang, nilai higroskopisnya menjadi lebih rendah, dan agar lebih menarik. Bahan yang digunakan untuk selaput pelindungnya dapat berupa aspal, lilin, malam, wax dan sebagainya. Pupuk yang bermantel harganya lebih mahal dibandingkan tanpa mantel.
4. Filler (pengisi). Pupuk majemuk atau pupuk campur yang kadarnya tinggi sering diberi filler agar ratio fertilizernya dapat sesuai dengan yang diinginkan, juga dengan maksud agar mudah disebar lebih merata (Setyaningsih, et al. 2007).
8 Dalam praktik, perlu diketahui istilah-istilah khusus yang sering digunakan dalam pupuk antara lain ialah:
a. Mutu pupuk atau grade fertilizer artinya angka yang menunjukkan kadar hara tanaman utama (N, P, dan K) yang dikandung oleh pupuk yang dinyatakan dalam persen N total, P2O5 dan K2O. Misalnya pupuk Rustika Yellow 15-10-12 berarti kadar N 15%, P2O5 10% dan K2O 12%.
b. Perbandingan pupuk atau ratio fertilizer ialah perbandingan unsur N, P dan K yang dinyatakan dalam N total, P2O5 dan K2O merupakan penyederhanaan dari grade fertilizer. Misalnya grade fertilizer 16-12-20 berarti ratio fertilizernya 4:3:5.
c. Mixed fertilizer atau pupuk campur ialah pupuk yang berasal dari berbagai pupuk yang kemudian dicampur oleh pemakainya. Misalnya pupuk Urea, TSP, dan KCl dicampur menjadi satu dengan perbandingan tertentu sesuai dengan mutu yang diinginkan. Hal ini berbeda dengan pupuk majemuk, yaitu pupuk yang mempunyai dua atau lebih hara tanaman dibuat langsung dari pabriknya.
Zat-zat penyusun tumbuhan terdiri dari unsur-unsur esensial dan unsur-unsur non esensial.
1. Unsur-unsur esensial adalah unsur-unsur yang mutlak diperlukan oleh segala macam tumbuhan. Unsur-unsur ini disebut juga unsur hara makro dan mikro. Unsur-unsur makro adalah unsur yang diperlukan dalam jumlah banyak, yaitu C, H, O, N, P, K, Mg, dan S. Sedangkan
9 unsur-unsur mikro yaitu zat hara tambahan, misalnya Fe, Mn, Cu, Mo, Cl, Zn, dan B.
2. Unsur-unsur non esensial adalah unsur tambahan yang hanya diperlukan oleh jenis tumbuhan tertentu, baik dalam jumlah besar maupun kecil. Misalnya Na, Co, Al, dan Si.
Berdasarkan macam hara tanaman yang terkandung pupuk dibedakan menjadi: a. Pupuk makro ialah pupuk yang hanya mengandung hara makro saja,
misalnya: NPK, nitrophoska, gandasil.
b. Pupuk mikro ialah pupuk yang hanya mengandung hara mikro saja, misalnya: mikrovet, mikroplek, metalik.
c. Campuran makro dan mikro misalnya pupuk gandasil, bayfolan, rustika. Sering juga ke dalam pupuk campur makro dan mikro ditambahkan juga zat pengatur tumbuh (hormon tumbuh).
2.1.1. Pupuk Kalium
Kalium (K) memainkan beberapa peranan di dalam tanaman dan pada nutrien lain. Kalium tidak menjadi bagian langsung pada struktur tanaman tetapi bertindak sebagai pengatur keseimbangan air, peredaran nutrisi dan gula dalam jaringan tanaman, sintesis protein dan pati serta mengatur fiksasi nitrogen. Gejala yang timbul apabila tanaman kekurangan unsur K meliputi pertumbuhan lambat, perkembangan sistem perakaran kurang baik dan batang menjadi lemah, hasil panen (yield) rendah, biji atau buah menjadi layu, mudah
10 terserang penyakit dan tidak tahan pada musim dingin, penggunaan air kurang efisien dan pengikatan N berkurang (Setyaningsih, et al. 2007).
Kalium diperlukan tanaman untuk berbagai fungsi fisiologis, termasuk di dalamnya adalah metabolisme karbohidrat, aktivitas enzim, regulasi osmotik, efisiensi penggunaan air, serapan unsur nitrogen, sintesis protein, dan translokasi asimilat ( Gunadi, 2009). Unsur K memegang peranan penting di dalam metabolisme tanaman antara lain terlibat langsung dalam beberapa proses fisiologis (Farhad,et al. 2010). Keterlibatan tersebut dikelompokkan dalam dua aspek, yaitu: (1) aspek biofisik dimana kalium berperan dalam pengendalian tekanan osmotik, turgor sel, stabilitas pH, dan pengaturan air melalui kontrol stomata, dan (2) aspek biokimia, kalium berperan dalam aktivitas enzim pada sintesis karbohidrat dan protein, serta meningkatkan translokasi fotosintat dari daun (Taiz dan Zeiger, 2002).
Selain itu unsur K berperan memperkuat dinding sel dan terlibat di dalam proses lignifikasi jaringan sclerenchym (Syakir dan Gusmaini, 2012). Kalium dapat meningkatkan ketahanan tanaman terhadap penyakit tertentu (Fageria, et al.2009). Dengan demikian, adanya pemberian K dapat membentuk senyawa lignin yang lebih tebal, sehingga dinding sel menjadi lebih kuat dan dapat melindungi tanaman dari gangguan dari luar (Syakir dan Gusmaini, 2012). Tanaman memerlukan kalium dalam jumlah yang tinggi yaitu berkisar antara 50-300 kg/ ha/ musim tanam (Laegreid,et al. 1999).
Kebutuhan K oleh tanaman setara dengan kebutuhan N, bahkan pada beberapa tanaman serapan K lebih tinggi dibandingkan N seperti pada lahan
11 sawah dan kering (Fageria, et al. 2001). Hal ini menunjukkan bahwa kebutuhan K oleh tanaman cukup tinggi dan apabila kebutuhan tersebut tidak terpenuhi maka proses metabolisme tanaman terganggu sehingga produktivitas tanaman dan mutu hasil menjadi rendah (Syakir dan Gusmaini, 2012).
Pupuk kalium yang banyak digunakan di Indonesia saat ini adalah KCl (Kalium Klorida) dengan kadar 60% K2O. Selain itu terdapat pula pupuk kalium lainnya, seperti kalium sulfat (K2SO4), kalium magnesium sulfat (K2SO4.MgSO4), dan kalium nitrat (Gunadi, 2009).
Pupuk KCl harganya lebih murah dibandingkan dengan K2SO4. Namun demikian, dari hasil penelitian menunjukkan telah terbukti K2SO4 mampu memperbaiki karakteristik kualitas beberapa produk sayuran (Gunadi, 2007). Hal ini disebabkan karena di dalam pupuk kalium sulfat selain mengandung unsur K juga mengandung unsur S yang berperan penting selama proses sintesis metabolisme tanaman termasuk pembentukan metabolik sekunder (Kumar, et al.2010). Berikut ini adalah tabel perkembangan harga pupuk kalium dari tahun 2000-2002.
Tabel 1. Perkembangan Harga Pupuk Kalium di Dunia
Pupuk Harga (US$/ton)
2000 2001 2002 Urea - 463 - Ammonium sulfat 58 63 56 Ammonium nitrat 40 - - Kalsium nitrat 100 116 106 Potasium sulfat 167 167 177 Sumber: Tyson, 2003
12 2.1.2. Pupuk Kalium Sulfat.
Kalium sulfat merupakan senyawa yang berbentuk kristal yang mempunyai kapasitas panas sebesar 33,l J/K (Perry R.H.,1998). Pupuk kalium sulfat (K2SO4) banyak digunakan baik untuk perkebunan maupun petani kecil. McKenzie (2000) menambahkan bahwa kalium sulfat merupakan pupuk kalium yang penting bagi area yang membutuhkan nutrien Kalium sekaligus Sulfur.
Kalium sulfat (K2SO4) merupakan pupuk yang rendah akan kadar klorida (Cl). Kalium sulfat juga merupakan pupuk yang paling populer di dunia yang menyediakan nutrien dalam konsentrasi tinggi bagi tanaman. Pupuk kalium sulfat memiliki syarat mutu komponen yang terkandung di dalamnya. Berikut merupakan tabel yang menunjukkan syarat mutu pupuk kalium sulfat.
Tabel 2. Syarat Mutu Pupuk Kalium Sulfat
No Uraian Satuan Persyaratan
1. Kalium sebagai kalium oksida K2O % Min. 50
2. Kadar belerang (S) % Min. 17
3. Asam bebas sebagai H2SO4 % Maks. 2,5
4. Klorida (Cl) % Maks. 2,5
5. Kadar air (H2O) % Maks. 1
Sumber : SNI, 2005
Unsur S merupakan makro nutrien keempat bagi tanaman selain N, P dan K. Amonium sulfat, single superphosphate (SSP) dan kalium sulfat (K2SO4) merupakan jenis pupuk yang banyak tersedia di dunia sebagai sumber S. Setiap tahunnya sekitar 75% dari 10 juta ton produksi sulfur digunakan
13 sebagai pupuk. Kebanyakan pupuk sulfat berasal dari anion SO42- (Messick dan Brey, 2002).
Pupuk kalium sulfat dapat dibuat dari garam komplek K2SO4.2MgSO4. Garam komplek ini dilarutkan dalam air kemudian diberi KCl, dengan persamaan reaksi:
K2SO4.2MgSO4(aq) + 4 KCl(aq) 3 K2SO4(s) + 2 MgCl2(aq)
K2SO4 akan mengendap dan untuk memisahkannya maka MgCl2 didekantasi. Pupuk ini sejak lama banyak digunakan di Indonesia untuk tanaman serat misalnya rami, rosella, dan kapas, dengan adanya pemupukan K mengakibatkan kualitas serat tanaman tersebut menjadi lebih tinggi.
Menurut Messick dan Brey (2002), kalium sulfat (K2SO4) dapat diproduksi melalui metode Mannheim, yaitu dengan cara mendekomposisi kalium klorida (KCl) menggunakan asam sulfat (H2SO4). Hidrogen klorida yang terbentuk dievaporasi dan dapat digunakan untuk memproduksi HCl. Mereka juga menyatakan bahwa pupuk kalium sulfat dapat digunakan sebagai sumber K bagi tanaman yang rentan terhadap tingginya kandungan klorida. Kalium sulfat juga lebih disukai karena selain membutuhkan nutrien K, tanaman juga membutuhkan nutrien S sebagai makro nutrien.
Pembuatan pupuk kalium sulfat dilakukan melalui reaksi asam basa, reaksi ini bersifat irreversibel. Pada reaksi irreversibel, laju reaksi dipengaruhi oleh temperatur dan konsentrasi reaktan (Husin, et al. 2007).
Faktor-faktor yang mempengaruhi proses pembuatan kalium sulfat adalah sebagai berikut :
14 1. Waktu Reaksi
Pencampuran biasanya terdiri atas satu fase atau lebih. Fungsi lamanya pengadukan pada saat reaksi adalah untuk mempercepat distribusi, semakin lama waktu pengadukan maka reaksi antara kalium dengan asam sulfat akan semakin sempurna.
2. Suhu Reaksi
Energi yang diperlukan dalam reaksi biasanya dalam bentuk panas (suhu). Umumnya suhu proses yang digunakan adalah di bawah titik didih pelarutnya. Hal ini dimaksudkan agar pelarut tidak ikut menguap. Semakin tinggi suhu yang digunakan maka reaksi pembentukan kalium sulfat akan berjalan lebih cepat.
3. Kecepatan Pengadukan
Adanya pengadukan maka pergerakan panasakan bertambah besar dan perpindahan material dari permukaan partikel ke dalam larutan bertambah cepat. Di samping itu dengan adanya pengadukan akan mencegah terjadinya pengendapan. Semakin cepat pengadukan maka akan semakin banyak partikel yang bertumbukan sehingga reaksi berjalan dengan sempurna dan kalium sulfat yang dihasilkan semakin besar (Damayanti, 1999).
2.2. Biodiesel
Biodiesel merupakan salah satu jenis biofuel (bahan bakar cair dari pengolahan tumbuhan) di samping bio-etanol. Biodiesel adalah senyawa alkil
15 ester yang diproduksi melalui proses alkoholisis (transesterifikasi) antara trigliserida dengan metanol atau etanol menggunakan bantuan katalis basa/asam menjadi alkil ester dan gliserol. Biodiesel juga dapat dibuat dari reaksi esterifikasi asam-asam lemak (bebas) dengan metanol atau etanol serta katalis asam menjadi senyawa alkil ester dan air.
Biodiesel mentah (kasar) yang dihasilkan pada proses transesterifikasi minyak (atau esterifikasi asam-asam lemak) biasanya masih mengandung sisa-sisa katalis, metanol, dan gliserol atau air. Untuk memurnikannya, biodiesel mentah (kasar) tersebut bisa dicuci dengan air, sehingga pengotor-pengotor tersebut larut ke dalam air dan terbawa oleh fase air pencuci yang selanjutnya dipisahkan. Air yang dipakai mencuci disarankan mengandung sedikit asam atau basa untuk menetralkan sisa-sisa katalis ( Yuniwati dan Karim, 2009).
Bahan baku pembuatan biodiesel dapat digunakan antara lain minyak jarak, minyak sawit, minyak kelapa dan lain sebagainya. Minyak goreng bekas dapat juga digunakan sebagai bahan baku pembuatan biodiesel. Minyak ini merupakan limbah sisa penggorengan industri makanan dan rumah tangga. Pemanfaatan minyak goreng bekas ini diharapkan dapat meminimalisir pembuangan limbah ke lingkungan.
Biodiesel mempunyai rantai karbon antara 12 sampai 20 serta mengandung oksigen. Adanya oksigen pada biodiesel membedakannya dengan petroleum diesel (solar) yang komponen utamanya hanya terdiri dari hidrokarbon. Jadi komposisi biodiesel dan petroleum diesel sangat berbeda.
16 Biodiesel terdiri dari metil ester asam lemak nabati, sedangkan petroleum diesel dari senyawa hidrokarbon.
Transesterifikasi adalah suatu reaksi yang menghasilkan ester dimana salah satu pereaksinya juga merupakan senyawa ester. Jadi disini terjadi pemecahan senyawa trigliserida dan migrasi gugus alkil antara senyawa ester (Aziz, 2007). Umumnya, katalis yang digunakan adalah NaOH atau KOH. Transesterifikasi merupakan suatu reaksi kesetimbangan. Untuk mendorong reaksi agar bergerak ke kanan sehingga dihasilkan metil ester (biodiesel) digunakan alkohol dalam jumlah berlebih atau salah satu produk yang dihasilkan harus dipisahkan (Setyaningsih, et al. 2007). Pada Gambar 1 disajikan reaksi transesterifikasi untuk menghasilkan metil ester (biodiesel).
17 Pada proses transesterifikasi selain menghasilkan biodiesel, hasil sampingnya adalah gliserol. Gliserol yang dihasilkan masih merupakan gliserol kasar. Gliserol kasar ini dapat dimurnikan menggunakan H2SO4 pekat. Dari hasil pemurnian ini diperoleh limbah yang kaya akan kalium sehingga dapat dimanfaatkan sebagai bahan pembuat pupuk.
Gliserol (1,2,3-propanatriol) atau disebut juga gliserin merupakan senyawa alkohol trihidrat dengan rumus bangun C3H8O3. Gliserol berwujud cairan jernih, higroskopis, kental, dan terasa manis. Gliserol terdapat pada susunan minyak dan lemak nabati maupun hewani namun jarang ditemukan dalam bentuk tersendiri. Gliserol menyusun minyak dan lemak setelah berkombinasi dengan asam lemak seperti asam stearat, asam oleat, asam palmitat, dan asam laurat. Berikut ini sifat fisik dari gliserol terdapat pada Tabel 3.
Tabel 3. Sifat Fisik Gliserol
Sifat Nilai
Bobot molekul 92,09382 g/mol
Viskositas pada suhu 200C 1499 cP Panas spesifik pada suhu 260C 0,5795 kal/g
Densitas 1,261 g/cm3
Titik leleh 180C
Titik didih 2900C
Sumber: Kern, 1966
Gliserol dari trigliserida dapat diperoleh dari dua sumber. Pertama, gliserol dihasilkan dari pembuatan sabun. Minyak atau lemak direaksikan dengan soda kaustik sehingga menghasilkan garam sabun dan gliserol. Kedua, minyak atau lemak dihidrolisis tanpa penambahan alkali (Kern, 1966).
18 Gliserol juga dihasilkan dari proses pembuatan biodiesel. Pada reaksi transesterifikasi minyak nabati, trigliserida bereaksi dengan alkohol dengan adanya asam atau basa kuat. Produk yang dihasilkan adalah metil ester sebagai biodiesel dan gliserol sebagai produk samping (Schuchardt, et al.1998). Dari 100% biodiesel hasil transesterifikasi, rendemen gliserol yang dihasilkan sebanyak 10% (Bondioli, 2003).
Gliserol memiliki banyak kegunaan, di antaranya sebagai emulsifier, pelembut, plasticizer, stabilizer es krim ,pelembab kulit, pasta gigi, dan obat batuk. Dan juga digunakan sebagai media pencegah reaksi pembekuan sel darah merah, sperma, kornea, dan jaringan lainnya, sebagai tinta printing dan bahan aditif pada industri pelapis dan cat, sebagai bahan antibeku, sumber nutrisi dalam proses fermentasi, dan bahan baku untuk nitogliserin. Rumus struktur gliserol dapat dilihat pada Gambar 2.
Gambar 2.Struktur Gliserol
2.3. Minyak Goreng
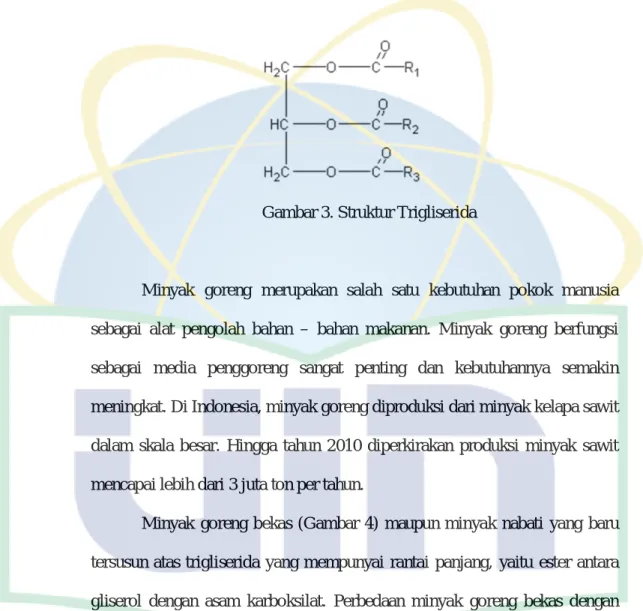
Minyak merupakan trigliserida (Gambar 3) yang tersusun atas tiga unit asam lemak, berwujud cair pada suhu kamar (25°C) dan lebih banyak mengandung asam lemak tidak jenuh sehingga mudah mengalami oksidasi. Minyak yang berbentuk padat biasa disebut dengan lemak. Minyak dapat bersumber dari tanaman, misalnya minyak zaitun, minyak jagung, minyak
19 kelapa, dan minyak bunga matahari. Minyak dapat juga bersumber dari hewan, misalnya minyak ikan sardin, minyak ikan paus dan lain-lain (Ketaren, 1986).
Gambar 3. Struktur Trigliserida
Minyak goreng merupakan salah satu kebutuhan pokok manusia sebagai alat pengolah bahan – bahan makanan. Minyak goreng berfungsi sebagai media penggoreng sangat penting dan kebutuhannya semakin meningkat. Di Indonesia, minyak goreng diproduksi dari minyak kelapa sawit dalam skala besar. Hingga tahun 2010 diperkirakan produksi minyak sawit mencapai lebih dari 3 juta ton per tahun.
Minyak goreng bekas (Gambar 4) maupun minyak nabati yang baru tersusun atas trigliserida yang mempunyai rantai panjang, yaitu ester antara gliserol dengan asam karboksilat. Perbedaan minyak goreng bekas dengan minyak nabati yang baru terletak pada komposisi asam lemak jenuh dan tak jenuh. Hal ini disebabkan pada proses penggorengan terjadi perubahan rantai tak jenuh menjadi rantai jenuh pada senyawa penyusunnya. Komposisi lemak
20 tak jenuh dalam minyak jelantah adalah 30% sedangkan asam lemak jenuh 70% (Kusuma, 2003).
Gambar 4. Minyak Goreng Bekas
Selama penggorengan, minyak goreng akan mengalami pemanasan pada suhu tinggi 170C-180C dalam waktu yang cukup lama. Hal ini menyebabkan terjadinya suatu proses oksidasi, hidrolisis dan polimerisasi yang menghasilkan senyawa-senyawa hasil degradasi minyak seperti keton, aldehid dan polimer yang merugikan kesehatan manusia. Penggunaan minyak nabati berulang kali sangat membahayakan kesehatan. Hal ini dikarenakan selain semakin banyaknya kotoran yang terkandung dalam minyak goreng akibat penggorengan bahan makanan sebelumnya dan semakin banyaknya senyawa – senyawa asam karboksilat bebas di dalam minyak serta warna minyak goreng yang semakin tidak jernih, sedangkan pembuangan minyak goreng bekas secara langsung ke lingkungan akan menimbulkan pencemaran, ( Ketaren, 1986 ).
21 2.4. Spektrofotometri UV
Spektrofotometri adalah suatu cara analisa yang mencakup pengukuran absorbsi oleh senyawa kimia dengan panjang gelombang tertentu menggunakan radiasi monokromatik. Radiasi monokromatik adalah radiasi dari satu panjang gelombang. Di dalam praktek radiasi monokromatik dihasilkan dengan gelombang prisma difraksi kiri yang memiliki panjang gelombang lebih dari satu. Biasanya ruang spektra di isolasi di dalam spektrofotometri.
Spektrofotometer adalah alat untuk mengukur transmitans dan absorbans suatu contoh sebagai fungsi panjang gelombang. Penggunaan absorbansi atau transmitansi dalam spektrofotometer UV-VIS dapat digunakan untuk analisis kualitatif dan kuantitatif spesies kimia ( Khopkar, 2002). Pengukuran terhadap suatu deretan contoh pada suatu panjang gelombang tunggal mungkin juga dapat dilakukan. Alat-alat demikian dapat dikelompokkan baik sebagai manual, perekam maupun sinar tunggal atau sinar rangkap. Berikut ini diagram sederhana dari spektrofotometer :
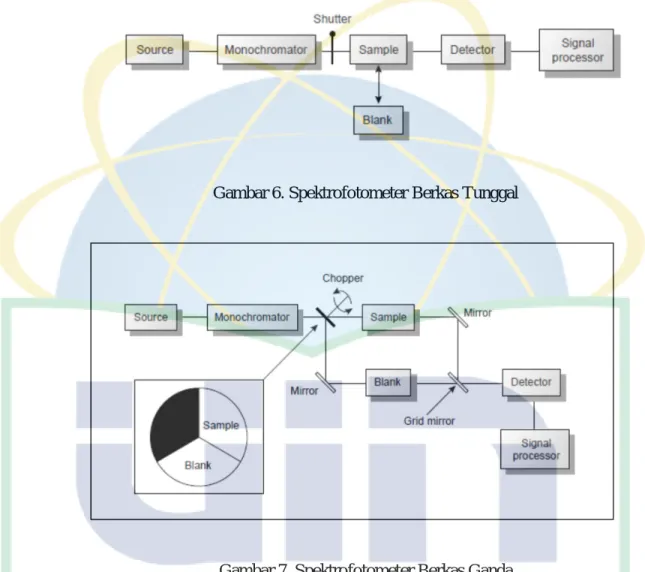
22 Terdapat dua jenis alat spektrofotometer, yaitu berkas tunggal (Gambar 6) dan berkas rangkap (Gambar 7).
Gambar 6. Spektrofotometer Berkas Tunggal
Gambar 7. Spektrofotometer Berkas Ganda Komponen – komponen utama spektrofotometer UV terdiri dari:
1. Sumber Sinar
Sumber sinar yang biasa digunakan pada spektroskopi absorbsi adalah lampu wolfarm, deuterium lampu hidrogen. Lampu wolfarm
23 digunakan untuk daerah visibel (tampak) sedangkan untuk lampu hidrogen atau deuterium digunakan untuk sumber daerah UV.
2. Monokromator
Monokromator merupakan serangkaian alat optik yang menguraikan radiasi polikromatik dan berfungsi untuk memunculkan garis resonansi dari semua garis yang tidak diserap yang dipancarkan oleh sumber radiasi. Alatnya dapat berupa prisma atau grating. Proses kerja dari monokromator dapat dilihat pada Gambar 8.
24 3. Sel Penyerap
Penempatan cuplikan yang akan dipelajari pada daerah UV – VIS, pada pengukuran daerah tampak, kuvet kaca corex dapat digunakan tetapi untuk pengukuran pada daerah UV kita harus menggunakan sel kuarsa karena pada daerah ini gelas tidak tembus cahaya. Umumnya tebal kuvet adalah 10 nm, tetapi yang lebih kecil ataupun yang lebih besar digunakan. Contoh dari sel dapat dilihat pada Gambar 9.
Gambar 9. Sel yang Digunakan dalam Spektrofotometer 4. Detektor
Peranan detektor penerima adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang. Detektor yang digunakan dalam UV – VIS disebut “ detektor fotolistrik”
Persyaratan-persyaratan penting untuk detektor meliputi :
1. Sensivitas tinggi hingga dapat mendeteksi tenaga cahaya yang mempunyai tingkatan rendah sekalipun
25 2. Waktu respon yang pendek.
3. Stabilitas yang panjang
4. Sinar elektronik yang mudah diperjelas dan sistem pembacaan.
2.5. Spektrofotometri Serapan Atom
Alat spektrophotometer yang secara khusus mengukur konsentrasi bahan kimia berupa atom bukan senyawa disebut spektrofotometer nyala (flame spectrophotometer) yang memakai obyek nyala api pembakar.
Berdasarkan metodenya (emisi atau absorpsi), dikenal dua jenis spektrofotometer nyala yaitu Spektrofotometer Emisi Nyala disingkat SEN (Flame Emission Spectrophotometer, FES) dan Spektrofotometer Serapan Atom disingkat SSA (Atomic Absorbtion Spectroscopy, AAS).
2.5.1. Prinsip Kerja Spektrofotometri Serapan Atom
Sampel berupa molekul akan didisosiasikan (terurai) menjadi atom-atom di dalam nyala api pada alat spektrofotometer serapan atom-atom, atom-atom menyerap energi sehingga elektron-elektronnya mengalami eksitasi. Energi eksitasi ini berasal dari pancaran sinar sebuah sumber cahaya lampu, dimana energi yang terserap sama dengan selisih antara dua energi.
Peralihan antara dua energi yang melibatkan posisi dasar biasanya mempunyai intensitas pancaran dan serapan yang lebih kuat daripada kemungkinan peralihan yang lain. Peralihan dari posisi dasar ke posisi eksitasi yang pertama disebut garis resonansi. Garis resonansi ini sangat
26 penting artinya pada atom absorpsi, sebab pada atom absorpsi ini tiap elemen dalam sampel akan menyerap sinar dengan jumlah jarak gelombang yang terbatas dalam kawasan spektrum yang sempit. Dari spektrum serapan ini akan dapat diperoleh data-data mengenai zat sampel. Nyala api gas pembakar molekul / atom yang ada dalam sebuah proses spektrofotometer serapan atom seolah-olah berfungsi sebagai kuvet pada spektrofotometer Ultra Violet – Visibel (UV-Vis).
Dalam prakteknya, kita diharuskan membuat kurva standar antara ekstingsi (serapan) dengan konsentrasi larutan sampel. Dari grafik standar ini kemudian dilarutkan sampel yang telah diukur serapannya, kemudian dapat ditentukan konsentrasinya secara interpolasi atau ekstrapolasi.
Prinsip pengukuran spektrofotometer serapan atom analog dengan prinsip pengukuran pada serapan molekuler spektrofotometer. Garis yang terpenting dalam spektrofotometer serapan atom adalah garis resonansi. Ukuran lebar alami garis resonansi ini terletak dalam kisaran 0,005 nm. Pada garis ini tidak akan muncul pelebaran garis akibat peralihan vibrasi dan rotasi, sebagaimana halnya pada molekuler spektrofotometer. Sebuah monokromator hanya dapat mengisolasikan seberkas sinar sumber cahaya dari suatu kawasan gelombang yang lebarnya sama dengan himpunan spektrum monokromator itu sendiri.
Unsur atau atom yang diselidiki dengan spektrofotometer serapan atom ialah terutama unsur-unsur yang garis resonansinya berada di bawah 500 nm. Untuk unsur-unsur natrium, kalium dan kalsium dapat diukur
27 dangan alat spektrofotometer serapan atom tanpa saling mengganggu terhadap garis-garis spektrumnya. Sedangkan unsur-unsur dalam Tabel 4 berikut harus diselidiki secara sendiri bila menggunakan alat spektrofotometer serapan atom.
Kegunaan spektrofotometer serapan atom lebih berfokus pada analisis kuantitatif atom-atom logam, hingga saat ini sudah ada sekitar 70 jenis atom yang dapat dianalisis, diantaranya tercantum dalam Tabel 4.
Tabel 4. Panjang Gelombang Serapan Maksimum Berbagai Atom Logam
Atom Garis Resonansi (nm)
Ag 328,1 Ar 193,7 Au 142,8 B 149,7 Be 234,9 Ca 422,7 Co 240,7 Cr 357,9 Cu 324,7 Fe 248,3 Hg 253,7 Mg 285,2 Na 589,0 Ni 232,0 Pb 283,3 Pt 265,9 Sb 217,5 Se 296,0 Ti 364,6 Tl 276,8 U 351,4 Zn 215,8 Sumber: Ewing G. W., 1975
28 Pada sistem instrumentasi spektrofotometer serapan atom dikenal dua jenis sistem optik yaitu berkas tunggal dan berkas ganda, namun yang banyak digunakan dalam spektrofotometer serapan atom modern adalah jenis berkas ganda, seperti Gambar 10.
Gambar 10. Skema Instrumentasi Spektrofotometer Serapan Atom Berkas Ganda
2.5.2. Komponen Utama Instrumentasi Spektrofotometer Serapan Atom Beberapa komponen utama pada instrumentasi spektrofotometer serapan atom adalah sebagai berikut :
1. Sumber Cahaya
Sumber cahaya berupa lampu yang dapat memancarkan energi yang cukup. Ada jenis lampu yang dapat memancarkan spektrum kontinyu sebaliknya ada lampu yang dapat memancarkan spektrum garis. Untuk spektrofotometer tipe spektrofotometer serapan atom dipergunakan jenis lampu katoda dengan spektrum garis.
Lampu katoda terdiri atas sebuah katoda berongga berbentuk tabung dan berhadapan dengan anoda dari kawat wolfram, keduanya terbungkus
29 dengan bahan gelas. Lampu ini diisi dangan gas mulia seperti argon, neon, helium atau kripton sampai tekanan maksimal 1 cmHg. Kelemahan lampu katoda berongga ini adalah bahwa pada alat spektrofotometer serapan atom harus dipergunakan lampu dengan katoda yang dibuat dari elemen atau unsur yang sejenis dengan unsur yang dianalisis.
2. Monokromator
Monokromator merupakan suatu alat yang diletakkan diantara nyala dan detektor pada suatu rangkaian instrumentasi spektrofotometer serapan atom. Ada dua jenis monokromator yang dipakai yaitu monokromator celah dan kisi difraksi.
3. Gas dan Alat Pembakar
Gas dan alat pembakar pada spektrofotometer serapan atom dikenal dua jenis gas pembakar yang bersifat oksidasi dan bahan bakar. Gas pengoksidasi misalnya udara (O2) atau campuran O2 dan N2O, sedangkan sebagai bahan bakar adalah gas alam, propana, butana, asetilen dan H2. Gas pembakar dapat pula berupa campuran udara dengan propana, udara dengan asetilen (terbanyak dipakai) dan N2O dengan asetilen.
4. Kuvet
Kuvet merupakan suatu tempat untuk nyala api dan atom-atom yang ada didalamnya, seolah-olah berfungsi sebagai kuvet.
5. Detektor
Detektor berfungsi sebagai alat penguat dari spektrum cahaya yang telah melewati sampel. Syarat yang harus dipenuhi oleh sebuah detektor
30 adalah memiliki respon yang linear terhadap energi sinar dalam kawasan spektrum yang bersangkutan. Pada spektrofotometer serapan atom detektor yang lazim dipakai adalah Detektor Tabung Pengadaan Photon Multiplier Tube Detector (PMTD).
31 BAB III
METODE PENELITIAN
3.1. Waktu dan Tempat Penelitian
Penelitian ini dilakukan di Pusat Laboratorium Terpadu Universitas Islam Negeri Syarif Hidayatullah Jakarta. Penelitian dilaksanakan selama 5 bulan mulai dari bulan Februari sampai Juni 2013.
3.2. Alat dan Bahan 3.2.1. Alat
Alat-alat yang digunakan dalam penelitian ini antara lain hotplate, termometer, gelas piala, magnetic stirrer, pompa vakum, neraca analitik, corong pisah, beaker glass, labu ukur, buret, penyaring TSS, kertas saring, oven, desikator, Spektrofotometer Serapan Atom (SSA) dengan lampu katoda kalium Perkin Elmer dan Spektrofotometer UV-Vis Perkin Elmer.
3.2.2. Bahan
Bahan-bahan yang digunakan dalam penelitian ini antara lain minyak goreng bekas yang berasal dari salah satu Rumah makan di Jakarta, padatan KOH, metanol, etanol 96%, akuades, larutan baku kalium, larutan baku sulfat, larutan AgNO3 0,01N, indikator kromat, dan H2SO4 pekat.
32 3.3. Prosedur Kerja
3.3.1. Pembuatan Biodiesel (Aziz, 2007)
Dilarutkan padatan KOH 1% dari berat minyak (gram) dalam metanol (1L), kemudian dipanaskan minyak goreng bekas (4L) sampai suhu 600C, setelah itu ditambahkan larutan metanol-KOH. Diatur laju pengadukannya sebesar 400 rpm. Biarkan reaksi selama 60 menit dan dijaga suhunya agar tetap konstan. Hasil reaksi dimasukkan ke dalam corong pisah, kemudian dibiarkan selama 12 jam sampai terjadi pemisahan yang sempurna. Lapisan atas menunjukkan biodiesel dan lapisan bawah menunjukkan crude glycerol. Lapisan bawah inilah yang nantinya akan digunakan untuk pembuatan pupuk kalium sulfat.
3.3.2. Pembuatan Pupuk Kalium (Setyaningsih, et al. 2007)
Limbah biodiesel (crude glycerol) sebanyak 100 mL dipanaskan pada suhu 40oC setelah itu ditambahkan H2SO4 pekat 2,5%, (v/v) sedikit demi sedikit. Reaksi dijalankan selama 15, 30, 60 dan 120 menit. Larutan yang terbentuk kemudian didiamkan selama 30 menit. Setelah 30 menit, endapan yang terbentuk dipisahkan dari filtratnya dengan pompa vakum. Endapan yang terbentuk ditambahkan akuades (5:1) untuk memisahkan larutan garam dari residu yang tidak ikut bereaksi. Larutan garam kemudian diuapkan di atas hot plate sampai terbentuk kristal. Kristal yang terbentuk kemudian disaring dengan penyaring vakum sambil dicuci dengan etanol 96% sehingga
33 terbentuk pupuk K2SO4. Selanjutnya ditimbang massa pupuk yang dihasilkan.
Setelah didapatkan waktu optimum selanjutnya dilakukan variasi suhu (30, 40, 60, 80oC) dan variasi konsentrasi asam sulfat (1%, 2%, 2,5%, 5% v/v).
Tabel 5. Variabel Penelitian
Variasi Parameter Konstan Tujuan
Waktu (15, 30, 60 dan 120 menit) H2SO42,5% Suhu 40°C Waktu optimum Suhu (30, 40, 60, 80°C) H2SO42,5% Waktu optimum Suhu optimum H2SO4 (1%, 2%, 2,5%, 5% v/v) Waktu optimum Suhu optimum Kondisi reaksi optimum
Setelah didapatkan kondisi optimum selanjutnya dilakukan uji kualitas pupuk meliputi : uji kadar Kalium (K), kadar Sulfur (S), kadar klorin, dan kadar air. Kemudian dihitung pula konversi reaksi pembuatan kalium sulfat yang dihasilkan dengan menggunakan rumus
=
100% ………...… (1)
3.3.3. Analisa Kadar Kalium dengan AAS (Atomic Absorption
Spectrophotometry) (Thorpe, V.A. 1973)
1. Pembuatan Deret Standar
Dipipet masing-masing 1 mL; 3 mL; 5 mL; dan 10 mL larutan standar kalium 100 mg/L, dimasukkan ke dalam labu ukur 100 mL. Kemudian
34 ditambahkan akuades sampai tanda tera sehingga diperoleh konsentrasi kalium: 1 mg/L; 3 mg/L; 5 mg/L; dan 10 mg/L.
2. Preparasi larutan sampel
Ditimbang dengan teliti 2,5 gram sampel pupuk, kemudian ditambahkan 150 mL akuades dan dipanaskan diatas hot plate selama 30 menit hingga larut. Lalu didinginkan dan dimasukkan ke dalam labu ukur volume 250 mL. Kemudian ditambahkan akuades hingga tanda tera, lalu disaring dengan kertas saring hingga jernih. Selanjutnya diukur larutan sampel dengan AAS pada panjang gelombang 766,5 nm.
= × × ………(2)
Dimana:
C adalah konsentrasi contoh uji hasil pengukuran FP adalah faktor pengenceran
V adalah volume larutan
M adalah massa sampel pupuk yang digunakan
3.3.4. Analisa Kadar Sulfur dengan Spektrofotometri (SNI 06-6989.20-2004)
1. Pereaksi Kondisi
Ditimbang 7,5 gram NaCl ke dalam 27,5 mL akuades, ditambahkan 3 mL HCl pekat, 10 mL etanol dan 5 mL gliserol. Lalu ditepatkan dengan akuades hingga 100 mL (larutan ini stabil kira-kira 2 minggu pada suhu kamar).
35 3. Larutan Baku Sulfat 100 mg/L
Dilarutkan 0,1479 gram Na2SO4 anhidrat dengan akuades dalam labu ukur 1L.
4. Pembuatan Deret Standar
Dipipet masing-masing 5 mL; 10 mL; 15 mL; 20 mL; 25 mL; 30 mL; 35 mL dan 40 mL larutan baku sulfat 100 mg/L, dimasukkan ke dalam labu ukur 100 mL. Kemudian ditambahkan akuades sampai tanda tera sehingga diperoleh konsentrasi sulfat: 5 mg/L; 10 mg/L; 15 mg/L; 20 mg/L; 25 mg/L; 30 mg/L; 35 mg/L dan 40 mg/L.
5. Cara Kerja
Dipipet 100 mL sampel dimasukkan ke dalam Erlenmeyer 250 mL, kemudian ditambahkan 5 mL larutan kondisi dan diaduk dengan magnetic stirrer. Ketika diaduk ditambahkan ±0,2 gram BaCl2.2H2O diaduk selama 2
menit. Setelah itu dilakukan pengukuran dengan spektrofotometer UV-Vis pada panjang gelombang 340 nm.
= ………..……… (3)
Dimana:
C adalah konsentrasi contoh uji hasil pengukuran F adalah faktor pengenceran
=
………..…….. (4)
3.3.5. Analisa Kadar Klorin (Effendi dan Kasno, 2011)
Ditimbang 2,5 gram sampel ke dalam labu ukur 250 mL, ditambah 150 mL akuades, dikocok dengan mesin pengocok selama 30 menit dengan
36 kecepatan 400 rpm. Kemudian ditambah akuades sampai tera 250 mL, dikocok dengan tangan (cara bolak balik). Larutan disaring dengan kertas saring sampai jernih. Dipipet 10 mL sampel jernih ke dalam erlenmeyer, ditambah beberapa tetes indikator kromat 5%. Dititar dengan larutan AgNO3 0,01N, sampai terbentuk endapan merah bata, dicatat volume titran (V), (dilakukan duplo) kemudian dihitung kadar klorin dengan rumus:
( ) = × × . × 100% ………..….(5)
Keterangan:
V= volume AgNO3 yang digunakan (mL) N= normalitas AgNO3 (N)
m= massa sampel yang digunakan (mg)
3.3.6. Analisa Kadar Air (Laksono, et al. 2012)
Cawan porselen dikeringkan dalam oven selama 15 menit, lalu dimasukkan ke dalam desikator. Sebanyak 5 gram sampel pupuk (W1) dimasukan ke dalam cawan tersebut dan ditimbang (W2), dipanaskan selama 4-6 jam pada suhu 130oC. Cawan didinginkan dalam desikator dan ditimbang (W3). Kadar air dicari dengan rumus:
(%) = × 100 ...(6) Keterangan:
W1 = berat sampel (gram)
W2 = berat cawan + sampel pupuk sebelum dipanaskan (gram) W3 = berat cawan + sampel pupuk setelah dipanaskan (gram)
37 BAB IV
HASIL DAN PEMBAHASAN
4.1. Pembuatan Pupuk Kalium Sulfat dari Crude Glycerol
Pembuatan pupuk kalium sulfat dilakukan dengan mereaksikan crude glycerol dari limbah biodiesel minyak goreng bekas yang mengandung katalis
KOH dengan asam sulfat pekat. Sebagai katalis, KOH merupakan katalis homogen yang bersifat basa, yang dalam reaksinya tidak membutuhkan suhu dan tekanan yang tinggi (Kirk & Othmer, 1980; Yucel, et al., 2000). Selain itu, KOH juga memiliki beberapa kelebihan yaitu, nilai konversi yang tinggi, tidak bersifat korosif seperti katalis asam, dan lebih aman dalam penggunaannya (Schuchardt, et al., 1998).
Keberadaan katalis KOH dalam proses pembuatan biodiesel akan dihasilkan kembali pada produknya. Dimana dalam hal ini KOH akan cenderung berada lebih banyak pada crude glycerol dibandingkan pada biodiesel. Hal ini disebabkan karena sifat katalis KOH yang mudah larut dalam air, seperti halnya dengan crude glycerol. Katalis KOH yang terdapat dalam crude glycerol ini dapat dimanfaatkan untuk pembuatan pupuk.
Crude glycerol yang digunakan dalam pembuatan pupuk kalium sulfat
dalam penelitian ini berwarna coklat kehitaman. Hal ini disebabkan masih banyak pengotor-pengotor yang terkandung di dalamnya yaitu meliputi metanol dan minyak goreng bekas yang tidak bereaksi (Aziz, 2009) . Berikut ini pada Gambar 11 dapat dilihat pemisahan dari crude glycerol dengan biodiesel.
38 Gambar 11. Pemisahan Crude Glycerol dengan Biodiesel
Pembuatan pupuk kalium sulfat ini menggunakan H2SO4 pekat yang ditambahkan tetes demi tetes volumenya ke dalam crude glycerol. Penambahan volume H2SO4 dilakukan sedikit demi sedikit agar larutan dapat tercampur secara homogen dan terjadi reaksi yang sempurna antara crude glycerol dengan asam sulfat pekat, pada saat penambahan H2SO4 pekat ke dalam crude glycerol terjadi perubahan larutan menjadi kuning kecokelatan dan larutan yang lebih kental disertai endapan (Gambar 12).
Gambar 12. Crude Glycerol Setelah Ditambahkan H2SO4 Pekat
Endapan yang dihasilkan yaitu merupakan endapan K2SO4, dengan persamaan reaksi sebagai berikut
2KOH(aq) + H2SO4 (l) K2SO4 (s) + 2H2O(aq)
Setelah didapatkan endapan, selanjutnya endapan disaring dengan penyaring vakum. Pada saat penyaringan, endapan disaring perlahan-lahan hingga
Biodiesel
39 terjadi pemisahan antara residu dengan endapan K2SO4 yang terbentuk. Gambar 13 menunjukkan proses penyaringan antara endapan K2SO4 dengan residu.
Gambar 13. Pemisahan Endapan K2SO4 dengan Residu
Endapan K2SO4 yang terbentuk dari hasil penyaringan masih berwarna cokelat kekuningan, hal ini disebabkan karena masih terkandungnya residu dan asam lemak bebas yang tidak ikut bereaksi. Residu yang dihasilkan yaitu berupa senyawa alkena dan air, dimana pada kondisi ini terjadi reaksi dehidrasi alkohol (Fessenden dan Fessenden, 1986) dengan persamaan reaksi.
C3H8O3 C3H4 + 2H2O
Selanjutnya endapan K2SO4 dilarutkan dengan air agar endapan yang terbentuk terpisahkan dari residu dan asam lemak bebas (Gambar 14).
Gambar 14. Pemisahan Larutan K2SO4 dengan Residu dan Asam Lemak Bebas Residu
Endapan K2SO4
Residu dan asam lemak bebas Larutan K2SO4 H2SO4
40 Larutan K2SO4 ditampung, selanjutnya dilakukan proses kristalisasi yaitu dengan menguapkannya di atas hot plate hingga volume larutan berkurang. Setelah itu sisa larutan didinginkan pada suhu ruang, kemudian dilanjutkan dengan pendinginan dengan es. Setelah dingin, larutan K2SO4 akan mengkristal dan membentuk kristal pupuk K2SO4.
Pupuk K2SO4 kemudian disaring dengan penyaring vakum. Pada saat disaring, pupuk tersebut ditambahkan dengan etanol. Hal ini bertujuan untuk memurnikan pupuk K2SO4 dari pengotor-pengotor lain dan mempercepat pengeringan pupuk K2SO4. Selanjutnya dilakukan penimbangan massa pupuk K2SO4 yang dihasilkan. Berdasarkan penelitian diperoleh massa pupuk sebanyak 5,21 gram dari penggunaan 100 mL crude glycerol dan 2,5% asam sulfat pekat. Bentuk pupuk K2SO4 dapat dilihat pada Gambar 15.
Gambar 15. Pupuk Kalium Sulfat
4.2. Optimasi Kondisi Reaksi Pembuatan Pupuk Kalium Sulfat
Kondisi optimum dari pembuatan pupuk kalium sulfat ditentukan terlebih dahulu untuk mendapatkan hasil pupuk yang maksimal. Kondisi optimum ini ditentukan berdasarkan massa pupuk tertinggi yang dihasilkan ditiap parameter.
41 Parameter yang digunakan meliputi waktu reaksi, suhu reaksi, dan konsentrasi H2SO4.
4.2.1. Pengaruh Waktu Reaksi Terhadap MassaPupuk K2SO4
Penentuan kondisi optimum dari pembuatan pupuk kalium sulfat pada penelitian ini dimulai dari penentuan waktu reaksi. Pada penentuan waktu reaksi digunakan waktu yang bervariasi yaitu 15, 30, 60, dan 120 menit. Pada kondisi ini, suhu dan konsentrasi dari H2SO4 yang digunakan dibiarkan tetap, yaitu pada suhu 400C dan konsentrasi H2SO4 2,5% (v/v). Hal ini mengacu pada penelitian Setyaningsih, et al. (2007) yang menunjukkan pada kondisi tersebut didapatkan pupuk kalium yang optimum.
Berdasarkan penelitian, diperoleh massa K2SO4 dari masing-masing variasi waktu yang dapat dilihat pada Tabel 6.
Tabel 6. Pengaruh Waktu Reaksi Terhadap Massa Pupuk K2SO4 yang Dihasilkan Waktu (menit) Massa Pupuk K2SO4 (gram)
15 4.23
30 5.18
60 Tidak terbentuk kristal
120 Tidak terbentuk Kristal
Tabel 6 memperlihatkan pengaruh waktu reaksi terhadap massa pupuk yang dihasilkan. Pada waktu reaksi 15 menit pupuk K2SO4 yang dihasilkan sebanyak 4,23 gram, kemudian waktu reaksi 30 menit pupuk K2SO4 yang dihasilkan meningkat menjadi 5,18 gram (Gambar 16). Selanjutnya pada waktu 60 menit dan 120 menit tidak dihasilkan pupuk. Hal ini disebabkan pada saat waktu
42 reaksi berlangsung selama 60 menit, endapan K2SO4 yang terbentuk mengalami lisis atau terlarut kembali. Endapan K2SO4 kembali larut akibat lamanya proses reaksi. Gambar 17 menunjukkan hasil endapan yang terbentuk.
(a) (b)
Gambar 16. Hasil Pupuk K2SO4 Variasi Waktu (a) 15 Menit, (b) 30 Menit
Gambar 17. Hasil Endapan Variasi Waktu 60 Menit
Seperti halnya pada sampel variasi waktu reaksi 60 menit, pada variasi waktu reaksi 120 menit juga menunjukkan hasil yang sama. Endapan K2SO4 yang dihasilkan larut kembali, hal ini disebabkan karena gliserol yang terlalu lama bereaksi dengan H2SO4 pekat. Sehingga viskositas dari endapan yang dihasilkan semakin meningkat. Hal ini dapat diamati dari tampilan endapan yang terlihat pekat pada Gambar 18.
43 Gambar 18. Hasil Endapan Variasi Waktu 120 Menit
Berdasarkan data tersebut diperoleh waktu optimum reaksi pada penelitian ini adalah pada waktu reaksi 30 menit. Menurut Damayanti (1999) pembuatan kalium sulfat dari limbah pabrik tanah serap (bleaching earth) dan ekstrak abu batang pisang, mencapai kondisi optimum reaksi pada suhu 700C selama 60 menit. Sedangkan pada penelitian Sutiyono (2007) mengenai pembuatan kalium sulfat dari kotoran burung puyuh dan air kawah Gunung Ijen, dicapai kondisi optimum reaksi dalam waktu 25 menit pada suhu 900C. Menurut Setyaningsih, et al. (2007) dalam penelitiannya mengenai pembuatan pupuk kalium dari proses
pemurnian gliserol hasil samping industri biodiesel waktu optimum reaksi terjadi selama 30 menit. Perbedaan ini dilihat dari bahan baku yang digunakan pada pembuatan pupuk kalium sulfat tersebut.
4.2.2. Pengaruh Suhu Reaksi Terhadap Massa PupukK2SO4
Setelah didapatkan waktu optimum reaksi, selanjutnya ditentukan suhu optimum reaksi. Penentuan suhu optimum reaksi dilakukan dengan variasi suhu 30, 40, 60, dan 800C. Konsentrasi H2SO4 yang digunakan dibiarkan tetap yaitu 2,5% (v/v) dengan waktu reaksi yang digunakan yaitu 30 menit sebagai waktu optimum yang telah didapatkan.
44 Tabel 7. Pengaruh Suhu Terhadap Massa Pupuk K2SO4 yang Dihasilkan
Suhu (0C) Massa PupukK2SO4(gram)
30 5.16
40 5.18
60 5.21
80 4.68
Berdasarkan penelitian pada Tabel 7 dapat dilihat massa pupuk K2SO4 yang dihasilkan dari masing-masing variasi suhu reaksi. Penggunaan suhu reaksi 300C menghasilkan massa K2SO4 sebanyak 5,16 gram. Pada suhu 400C massa K2SO4 yang dihasilkan 5,18 gram dan pada suhu 600C dihasilkan massa K2SO4 5,21 gram.
Data tersebut memperlihatkan bahwa semakin tinggi suhu reaksi yang digunakan maka semakin banyak massa pupuk K2SO4 yang dihasilkan. Meskipun kenaikan massa pupuk yang dihasilkan tidak signifikan, yaitu hanya sekitar 0,48% dari pupuk yang dihasilkan. Semakin tinggi suhu, menyebabkan energi kinetik yang dimiliki molekul-molekul pereaksi semakin besar sehingga tumbukan antara molekul pereaksi juga meningkat. Hal ini menyebabkan kecepatan reaksi semakin besar (Aziz, 2007).
Namun pada suhu 800C, massa K2SO4 yang dihasilkan mengalami penurunan. Hal ini terjadi karena suhu yang terlalu tinggi menyebabkan semakin banyaknya tumbukan antar partikel reaktan. Akibatnya K2SO4 yang terbentuk kelarutannya menjadi bertambah, menjadi mudah untuk terlarut kembali. Sehingga dari data tersebut dapat disimpulkan bahwa suhu terbaik yang
45 menghasilkan massa pupuk terbanyak didapatkan pada suhu 600C. Berikut ini Gambar 19 menunjukkan hasil pupuk dari masing-masing variasi.
(a) (b) (c) (d)
Gambar 19. Hasil Pupuk K2SO4 Variasi Suhu (a) 300C,(b) 400C,(c) 600C,(d) 800C
Menurut Edahwati (2010) kondisi terbaik pembuatan pupuk kalium sulfat dari ekstrak abu batang pisang dan limbah pabrik tanah serap (bleaching earth) juga terjadi pada suhu 600C dengan kecepatan alir 10 ml/detik dengan konversi yang dihasilkan sebesar 88,061%. Sedangkan menurut Sutiyono (2007) kondisi terbaik pada penelitiannya mengenai pembuatan kalium sulfat dari kotoran burung puyuh dan air kawah gunung ijen dicapai pada suhu 900C, lama pengadukan 25 menit dan kadar kalium sulfat yang terbentuk 44.503,5403 (mg/L) dengan konversi reaksi sebesar 86,62%.
4.2.3. Pengaruh Konsentrasi H2SO4 Terhadap MassaPupuk K2SO4
Setelah didapatkan waktu dan suhu optimum reaksi, selanjutnya ditentukan konsentrasi H2SO4 optimum dari reaksi tersebut. Untuk pengujiannya digunakan konsentrasi yang bervariasi yaitu 1; 2; 2,5; dan 5% (v/v), dengan
46 penggunaan waktu dan suhu optimum yang telah didapat yaitu waktu 30 menit dan suhu 600C.
Tabel 8. Pengaruh Konsentrasi H2SO4 Terhadap Massa Pupuk K2SO4 yang Dihasilkan
Konsentrasi H2SO4(%) Massa PupukK2SO4(gram)
1 Tidak terbentuk kristal
2 3.45
2.5 5.21
5 3.27
Tabel 8 menjelaskan pengaruh konsentrasi H2SO4 terhadap massa pupuk K2SO4 yang dihasilkan. Pada konsentrasi H2SO4 1% (v/v) tidak dihasilkan pupuk K2SO4, hal ini disebabkan karena konsentrasi H2SO4 yang digunakan terlalu kecil. Sehingga ion SO4-2 tidak dapat mengikat ion K+ seluruhnya. Akibatnya tidak dapat dilakukan proses kristalisasi. Gambar 20 menunjukkan hasil pemisahan filtrat K2SO4 dengan residu yang tidak ikut bereaksi.
Gambar 20. Hasil Pemisahan Filtrat K2SO4 Variasi Konsentrasi 1% (v/v)
Pada konsentrasi H2SO4 2% (v/v) didapatkan massa K2SO4 sebanyak 3,45 gram, dan pada konsentrasi H2SO4 2,5% (v/v) dihasilkan massa K2SO4 sebanyak 5,21 gram. Hal ini menunjukan terjadinya peningkatan jumlah massa K2SO4