SKRI PSI
SRI HENDAH MRIH LESTARI
ISOLASI DAN IDENTIFIKASI SENYAWA GOLONGAN
FLAVONOID DARI DAUN BAUHINIA PURPUREA LINN
F A K U LTA S FAR M ASI UN I V ER SI TAS AI R LAN GGA
S U R A B A Y A
ISOLASI DAN IDENTIFIKASI SENYAWA GOLONGAN FLAVONOID DARI DAUN BAUHI.NIA PURPUREA LINN
SKRIPSI
DIBUAT UNTUK MEMENUHI SYARAT MENCAPAI GELAR SARJANA FARMASI PADA FAKULTAS FARMASI
UNIVERSITAS AIRLANGGA
1989
oleh
SRI HENDAH MRIH LESTARI 058410681
Disetujui oleh Pembimbing
KATA PENGANTAR
Segala puji syukur saya panjatkan kehadirat Allah Su-bhanahu w a t a ’ala atae segala rahmat dan hidayah-Nya yang telah dilimpahkan kepada saya, sehingga berhasil menyusun skripsi ini sebagai syarat untuk memperoleh gelar sarjana Farmasi pada Fakultas Farmasi Universitas Airlangga.
Pada skripsi ini, saya mengambil judul: Isolasi dan identifikasi senyawa golongan flavonoid dari daun Bauhinia purpurea Linn.
Pada kesempatan ini perkenankanlah saya mengucapkan terima kasih dan penghargaan yang sedalam-dalamnya kepada Bapak DR. Noor Xfansyah dan Dra. Mangestuti A, MB selaku pembimbing saya, yang telah banyak meluangkan v/aktu untuk memberikan bimbingan, nasehat serta dorongan semangat da lam menyelesaikan skripsi saya ini.
Para penguji yang telah berkenan memeriksav dan. menerima skripsi saya ini.
Serta semua pihak yang'telah membantu dalam penyelesaian skripsi saya.
Khusus terima kasih yang sebesar-besarnya saya sampaikan kepada Ayah dan Ibu serta saudara-saudaraku tercinta atas
segala bantuan dan dorongan semangat sehingga tugas akhir ini dapat saya selesaikan.
Ucapan terima kasih yang dalam juga saya sampaikan kepada
Saya sadari bahwa skripsi ini jauh dari sempurna, te-tap! harapan saya, semoga penelitian ini dapat berraanfaat untuk penelitian selanjutnya dan berguna pula bagi kita semua.
Halaman
1. Tinjauan tentang tanaman Bauhinia pur purea Linn. ... ...
3
1
.1
. Klasifikasi ... 31
.2
. Uraian tentang tanaman ... 32. Tinjauan umum tentang flavonoid .... k 2.1. Pembagian senyawa golongan fla -- v o n o i d ... •... 5
2.2. Sifat fisika kimia ...
6
2.3. Kegunaan flavonoid ... 7
2i.J*. Isolasi f l a v o n o i d ... 7
2.4*1* Isolasi flavonoid dengan pela-rut alkohol ... 7
2.4.2. Isolasi flavonoid dengan pela-rut a i r ...
8
2.4*3* Isolasi flavonoid dengan raeto-de CHARAUX-PARIS...
8
2.5* Identifikasi flavonoid 9 2.5*1* Reaksi warna ... ... 9
2.5*1*1* Reaksi W i l s t a t e r ... . 9
2.5*1*2. Reaksi Bate Smith-Metcalfe.. 10
iii .
Halaman 2.5 :2. Krornatografi lapisan tipis ... 10 2.5.3* Identifikasi dengan
spektrofo-to meter ultra lembayung berd& sarkan metode pergeseran pan
-Jang gelombang... H
2.5*3*1* Identifikasi senyawa golongan
flavon dan flavonol .»*•••.. 12 2.5*3*2* Identifikasi senyawa golongan
isoflavon ... ^ 2.5-3*3* Identifikasi senyawa golongan
flavanon dan dihidro flavonol.. •. 15 2.5*3*4* Identifikasi senyawa golongan
Kalkon dan A u r o n ... 13
2.2* Isolasi-senyawa golongan flavo«
n o i d ... .
30
2.2.1.,Pembuatan ekstrak ... 30 2.2.2. Identifikasi senyawa hasil
V
2.3. Pemisahan dan pemurnian ... 33 2.3.1. Kromatografi cepat cara vakuns.
2.3.2. Identifikasi senyawa golongan flavonoid hasil kromatografi
cepat cara v a k u m ... 33 2.3-3» Kromatografi kertas preparatif.
36
2.3.4. Identifikasi senyawa golongan flavonoid hasil kromatografi
kertas preparatif ... 37 2.4* Hidrolisa a s a m ... 38 2.4.1. Identifikasi senyawa golongan
flavonoid hasil hidrolisa.... 38 2.4.2. Identifikasi senyawa gula da
ri hasil hidrolisa... 39 2.5* Identifikasi dengan spektrofoto
meter lembayung u l t r a ... 40 BAB IV. HASIL PENELITIAN...
1. Bahan penelitian ... 43 2. Isolasi senyawa golongan flavonoid.. 4-2
2.1. Pembuatan ekstrak... ^3 2.2. Pemisahan dan p e m u r n i a n ... 45 2.3. Identifikasi senyawa hasil
iso-Iasi... ... *. ^ 2.3*1* Reaksi warna ...
2.3.2. Kromatografi lapisan tipis ..
^9
2.3*3. Spektrofotometer ultra
lemba-ji
yung... ^9 -
2
.4
. Hidrolisa dengan a s a m ...59
2.5* Identifikasi senyawa hasil hidrc
lisa... 59
2
.5* 1
*iri»£ii warna.»#*•*•••*•••*•*••« 592*5*2 Ki-omatografi lapican tipis....
59
2.5*3 Spektrofotometer ultra lemba
yung...
^0
2.5*-4 Identifikasi senyav/a gula...
7
®
BAB V . PEMBAHASAN... 7/*
BAB. VI. KSSIMPULAN- DAN SARAN... 82
BAB VII .DAFTAR PUSTAKA...
8
if RINGKASAN... 83BAFTAR TABEL I. Ringkasan identifikasi senyawa golong
an flavon dan flavonol dengan spektro** fotometer ultra lembayung dengan meto-de pergeseran panjang gelombang maksi
mum... ... ...
23
II.’ Ringkasan identifikasi senyawa golong an isoflavon dengan spektrofotometer ultra lembayung dengan metode pergesex
an panjang gelombang maksimum...
24
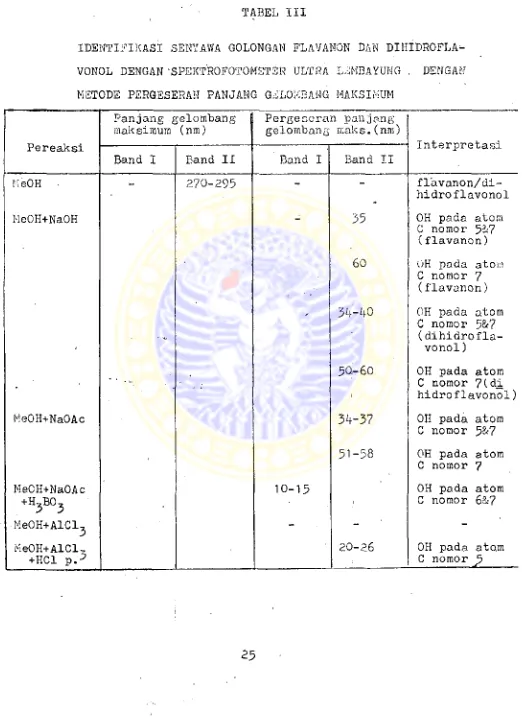
III. Ringkasan identifikasi senyawa golong-^. an flavanon dan dihidroflavonol dengan spektrofotometer ultra lembayung dengan metode pergeseran panjang gelombang :
maksimum... ... 25 IV. Ringkasan identivikaci senyawa golong
an kalkon dan auron dengan spektrofoto meter ultra lembayung dengan metode
pergeseran panjang gelombang maximum..* 26 V. Hasil kromatografi lapisan tipis
dari-fase petroleum eter,dari-fase eter,dari-fase etil asetat,face n—butanol... .
VI. Hasil kromatografi lapisan tipis dari fase etil asetat setelah dilakukan pe misahan dengan kromatografi cepat earn
Tabel VII. Hasil krornatografi lapisan tipis dari
fase n-butanol setelah dilakukan pemi sahan dengan krornatografi cepat cara
-vacum ... ... k ?
VIII. Hasil krornatografi lapisan tipis se
-k9
IX. Data hasil spektrofotometer ultra
lem-50
X. Data hasil spektrofotometer ultra
lern-55
XI. Data hasil spektrofotometer ultra lem~
56
XII. Hasil krornatografi lapisan tipis senya,
60
XIII. Data hasil spektrofotometer ultra
lem-61
XIV. Data hasil spektrofotometer ultra lem
bayung dari senyawa A
1
...6
*t XV. Data hasil spektrofotometer siltralem-67 XVI. Hasil identivikasi senyav/a gula hasil
Gambar 1. Tanaman Bauhinia purpurea Linn.... . 2 T
Spektra ultra lembayung dari senyawa
E ... 51 Spektra ultra lembayung dari senyawa
E ... 52 Spektra ultra lembayung dari senyawa
A ... 5t. Spektra ultra lembayung dari senyawa
A ...
55
Spektra ultra lembayung dari senyawa
B ... . 57 Spektra ultra lembayung dari senyaea
B ... 58 Spektra ultra lembayung dari senyawa
Ej ... *...
62
Spektra ultra lembayung dari senyawa
E, ...
63
Spektra ultra lembayung dari senyawa
Aj ... 65 Spektra ultra lembayung dari senyawa
A
1
... S6
Spektra ultra lembayung dari senyawa
B, ... 68 Spektra ultra lembayung dari senyawa
DAFTAR GAMBAR
Gambar lif. Kromatogram .senyawa liasil isolasi (E)
dan senyawa hasil hidrolisa(E1)... 71 Gambar 15« Kromatogram senyawa hasil isolasi (A)
dan senyawa hasil hidrolisaCA^)... 72 Gambar 16. Kromatogram senyawa hasil isolasi (B)
dan senyav/a hasil hidrolisa(B^)...
73
BAB I PBNDAHULUAN
Indonesia sangat kaya akan sumber alara yang dapat di. gunakan sebagai obat terraasuk bahan~bahan obat tradisio -nal yang telah 4igun&kan oleh sebagian besar rakyat Indo nesia secara turun temurun berdasarkan pengalaman, Oleh
i
karena itu dengan langkah yang tepat perlu dilakukan upaya perabinaan dan pengembangannupaya agar bahanbahan terse -but semaksimal mungkin dapat dimanfaatkan untuk penyeleng garaan upaya-upaya kesehatan masyarakat.
Disamping itu upaya-upaya penelitiannya harus terus digalakkan agar setapak demi setapak poteasi obat alam i-ni dapat diungkapkan semuanya. Dengan mei-ningkatnya hasil-hasil penelitian tersebut, akan meningkat pula pengungka£ an khasiat obat alam. Dengan demikian makin mantap pula peranan obat alam tersebut dalam upaya-upaya kesehatan ma syarakat.
Pemanfaatan obat tradisional yang sebagian besar ber asal dari .tanaman obat perlu ditingkatkan dan dikernbang -kan karena bahannya raudah didapat, tanamannya dapat dita-nain sendiri ol«h masyarakat di pekarangan-pekarangan, mu-rah dan dapat diramu sendiri di rumah.
Bauhinia purpurea Linn adalah salah satu turabuhan o-bat yang digunakan untuk oo-bat tradisional di Indonesia, dalam masyarakat dikenal dengan naraa daun kupu-kupu.(2,5)
t
Dari hasil skrining yang telah dilakukan terhadap Bauhini a purpurea'Linn dengan menggunakan kromatografi kertas di temukan adanya noda flavonoid.
Melihat kegunaan tanaman tersebut dan melihat adanya kan-' dungan flavonoid serta banyaknya tanamnn obat tersebut di daerah Madiun maka dilakukan isolasi dan identifikasi se nyawa golongan flavonoid dari tanaman Bauhinia purpurea Linn.
Flavonoid mempunyai banyak kegunaan antara lain se -bagai anti peradangan, diuretik, anti spasmodik.17,10)
Dengan demikian maka penelitian ini bertujuan untuk mencoba mengisolasi dengan metode Charaux-Paris dan meng-identifikasi dengan reaksi warna, kromatografi lapisan ti
✓
pis dan s£>ektrofotometer ultra lembayung senyawa golongan flavonoid dari daun Bauhinia purpurea Linn.
BAB II
TINJAUAN PUSTAKA
1. Tinjauan tentang tanaman Bauhinia rurpurea Linn. 1.1 Klasi fikasi.(5.4*9)
Divisi j Spermatophyta. Anak divisi '• Angiospermae. Kelas : Dicotyledoneae. Anak kelas Dialypetalae. Bangsa •* Leguminosae. Suku : Caesalpiniaceae. Karga •• Bauhinia.
Jenis ; Bauhinia purpurea Linn 1.2 Uraian tentang tanaman.
Tanaman ini turabuh liar di hutan dan di la dang-ladang sampai setinggi kira-kira 800 m dari permukaan laut. Ada juga yang ditanam orang di ha-laman-halaman sebagai tanaman hiasan.(
5
)Kama daerahnya: Daun lilin, areuy kupukupu, ati
-lil, ping-keping.(2,5) Morfologi tanaman.(
1
,9
)Habitus : perdu tegak atau pohon dengan tinggi
2 - 6
meter.Ranting : pucuk ranting dengan bulu-bulu berwar na gelap.
Bunga : bunganya berkelopsk daun 5 lembar, da -un b-unga obovatus sampai lanset, -ungu dengan dasar pucat, tabung kelopak 7-10 mm. Panjang mayang 2-12 cm dengan 5-25 kuntura, tangkai 7-15 mm, Benang sari 3* Buah : buahnya buah polong panjangnya sampai
25
era berisi 6-16 biji. Untuk keperluan pengobatan dipakai:Bijinya untuk raengobati diare, ulcus de -dan untuk yang terserang ulcus hasil ramu an tadi ditempelkan diterapat luka.
- Getah daunnya untuk batuk, batuk r e j a n i ^ Menurut penelitian yang dilakukan: Alex Pinsky dan Veronica II. Schwimmer (1973); H.P.Bhartiya, P Du-bey, S.B.Katiyar dan P.C.Gupta (1978 dan 1980) , tanaman ini mengandung enzim tripsin dan kherao tripsin, butein V O b e t a arabinoObetadextro -galactoside,
3
,4
-dihydroxychalcone4
-0
-beta-leavus-srabinopyranosyl-O-beta-dextro-galactopyra noside dalam bijinya,
2. Tinjauan umum tentang flavonoid,(10,11,12,13)
Flavonoid adalah suatu pigmen yang terdapat dalam
tumbuhan dengan 15 atom karbon dalam inti dasarnya ,
5
cincin aromatik yang dihubungkan oleh satuan tiga kar-bon yang dapat atau tak dapat raembentuk cincin ketiga. Istilah flavonoid sendiri sebenarnya borasal dari kelorapok senyawa yang paling umum dari golongan terse--but yaitu flavon atau
2
-phenylbenzopyron atau ^-phenyl benzopyron dengan rumus bangun6
ebagai berikut:Flavonoid banyak terdapat dalam tumbuhan sebagai bentuk glikosida baik dalam bentuk O-glikosida atau C-glikosida umuranya didalara bunga, buah, daun, dalam bentuk bebas banyak diketemukan pada jaringan kayu. 2.1 Pembagian senyawa golongan flavonoid.(10,12.15)
Flavonoid dapat digolongkan menjadi beberapa golongan:
a. Flavon
b. Flavonol
d... Isoflavon
e. Dihidroflavonol
f. Kalkon
g. Auron
f. Antoeianin
i. Leukoantosianin
2.2 Sifat fisika kimia. Kelarutan. (15)
Pada umumnya semua flavonoid baik dalam ben-tuk glikosida maupun flavonoid benben-tuk bebas dapat larut d.alam pelarut metanol dan etanol.
7
•Untuk memisahkan senyawa golongan flavonoid ada -lah berdasarkan si fat kelarutannya dalam berbagai raacam pelarut dengan polaritas yang meningkat ya itu:
- untuk flavonoid bentuk bebas atau bentuk
aglikon umuranya larut dalam pelarut eter. - untuk flavonoid bentuk O-glikosida banyak
larut dalara pelarut etil asetat.
- untuk flavonoid bentuk C-glikosida larut dalam pelarut n-butanol, amil alkohol. 2.3 Kegunaan flavonoid.
Kegunaan flavonoid didalam klinik antara la in ditemukan sebagai turunan dari flavonoid yaitu vitamin P. Vitamin P mempunyai fungsi terhadap permeabilita6 dan kerapuhan pembuluh darah kapi -ler. Antosianin, kalkon dan auron bersifat bakte-riostatik sedangkan polihidroksiflavon dalam ben tuk eternya bersifat sebagai insektisida. Akhir -akhir ini dilaporkan bahwa flavonoid mempunyai ak tivitas sebagai anti virus, anti peradangan dan anti spasmodik.(7,10,11,1
4
)2*4 Isolasi flavonoid.
dengan tujuan memisahkan klorofil, lemak dan li -lin dari senyawa golongan flavonoid, Setelah di pisahkan, filtrat yang diperoleh dapat langsung dipakai untuk isolasi.
2.4.2 Isolasi flavonoid dengan pelarut air.(14tl6) Isolasi dengan menggunakan pelarut air me rupakan prosedur umum untuk mengisolasi glikosi . da flavonoid dari daun, bunga dan buah, Selain
itu ekstraksi dengan air panas dari ekstrak ken tal alkohol dapat menghilangkan klorofil, leraak dan lilin. Kemudian ekstrak air yang encer di-ekstraksi dengan pelarut etil asetat atau n-bu-tanol. Fase etil asetat atau n-butanol dipekat-kan, raaka kadang-kadang akan timbul kristal gli kosida flavonoid secara langsung.
2.4.3 Isolasi flavonoid dengan metode CH ARAUX-PARISp ^
Serbuk tanaman diekstraksi dengan metanol, kemudian ekstrak metanol diuapkan sehingga di -dapatkan ekstrak kental. Ekstrak kental yang di peroleh ditambahkan air panas dalam jumlah yang sama sehingga akan didapatkan ekstrak air yang encer. Kemudian ekstrak air ditambah eter dan dilakukan ekstraksi kocok. Selanjutnya fase et er dipisahkan dari fase airnya.
-9
kan ekstraksi kocok, kemudian kedua fase dipi -sahkan.
Fase etil asetat diuapkan sampai kering dan ke-mungkinan didapatkan flavonoid dalam bentuk
0
-glikosida. Sedangkan fase air ditambah pelarut • n-butanol dan dilakukan ekstraksi kocok, kemudian kedua fase dipisahkan.
Fase n-butanol diuapkan maka akan didapat kan ekstrak n-butanol yang kering dan kemungkin an di dalam ekstrak tersebut terdapat flavonoid dalam bentuk C-glikosida dan leukoantosianin. Dari ketiga fase yang didapatkan tersebut dapat langsung dilakukan pemisahan dari komponen-kom-ponen yang ada dalam tiap' fasenya dengan memper gunakan kromatografi kolom. Metode ini sangat ' baik dipakai untuk mengicolasi flavonoid dalam tanaman, karena dapat dilakukan pemisahan flavo noid berdasarkan sifat kepolarannya.(
15
)2*5 Identifikasi flavonoid. 2.5*1 Reaksi warna.(10,1
1
) 2.5 . K 1 Reaksi Y.'ilstater.- warna merah tua, kemungkinan adalah golong an flavon*
- warna merah krimson, kemungkinan adalah go longan flavonol,
warna jingga merah, kemungkinan adalah go -longan flavanon.
2.5*1.2 Reaksi Bate Smith-Metcalfe.
Reaksi warna ini digunakan untuk menun -jukkan adanya senyawa leukoantosianin. Reaksi positif jika terjadi warna merah yang inten -sif atau warna ungu.
2.5*2 Krornatografi lapisan tipis.(6,16,18)
Krornatografi adalah suatu metode analisa untuk pemisahan komponon 'zat dari campurannya dengan cara melewatkan campuran tersebut melalu i sistem dua fase yaitu fase diam dan fase ge -rak.
Mekanisme terjadinya pemisahan pada kroma-;tografi dapat berdasarkan atas prinsip adsorpsi,
partisi, pertukaran ion dan filtrasi.
Pada umumnya pemisahan komponen dari cara -puran zat dilakukan berdasarkan proses adsorpsi atau proses partisi.
Proses adsorpsi.
Proses ini terjadi bila suatu campuran zat dite teskan pada lempeng fase diam, maka mula-mula
ber-11
beda-beda, maka apabila kemudian dilewatkan la rutan fase gerak arah keatas maka untuk molekul zat yang paling lemah diadsorpsi oleh fase diam akan terlarut lebih dahulu, sehingga akan mem -■ bentuk noda yang paling atas. Noda ini kemudian - diikuti noda-noda dari molekul zat lainnya yang teradsorpsi lebih kuat oleh fase diam dan akan membentuk noda yang lebih rendah.
Proses partisi.
Proses ini terjadi bila suatu campuran zat yang akan dipisahkan didistribusikan antara
2
fase yang saling tidak campur. Hal ini berdasarkan -perbedaan kelarutan relatif dari masing-masing komponen di dalam fase di&m dan fase gerak.Kromatografi lapisan tipis adalah salah sa tu tekhnik kromatografi, dimana dapat digunakan untuk identifikasi
6
erta test kemurnian suatu komponen dari campuran zat. Untuk menunjukkan a danya komponen dari campuran zat, dapat diguna kan sinar ultra lembayung atau penampak noda yang sesuai, sehingga didapat kromatogram. Dari kromatogram yang diperoleh dapat diketahui war na dari masing-masing komponen dari campuranzat dan harga Rf nya.
Rf adalah perbandingan jarak yang ditempuh oleh zat dengan jarak yang ditempuh oleh fase gerak. ^ 2«5»3 Identifikasi dengan spektrofotometer ultra lem
bayung berdasarkan metade pergeseran panjang
2.5*3*1 Identifikasi senyav/a golongan flavon dan fla vonol.
2.5*3*1*1 Dalam pelarut metanol p.a.
Secara umum spektra yang dihasilkan dari flavon dan flavonol memberikan
2
pun-cak absorbs! pada Band I dengan panjang ge lorabang maksimum 300-380 nm dan Band II de ngan panjang gelombang maksimum240-280
nm. Band I berfungsi untuk membedakan flavon dari flavonol, dimana untuk flavon terle -tak pada panjang gelombang maksimum antara304-350
nm dan untuk flavonol antara352
-385
nm.2.5*3*1*2 Zat dalam metanol p.ar ditambah NaOH padat. 2.5*3*1.2.1 Adany gugus OH pada atom C nomor 4' di
-tunjukkan oleh pergeseran bathokromik da ri Band I sebesar 4065 nm, bila diban -dingkan dengan hasil spektra ultra lemba yung dalam metanol p.a.
2.5*3*1*2.2 Adanya gugus OH pada atom C nomor 3 dan
4
* ditunjukkan oleh pergeseran b a thokro-. mik dari Band I sebesar 50-60 nm, bila dibandingkan dengan hasil spektra ultra lembayung dalam metanol p.a.2.5*3*1*3 Zat dalam metanol p.a ditambahkan NaOAc kristal.
13
dengan hasil spektra ultra lembayung dalam metanol p.a.
2.5*3.1*4 Zat dalam metanol p.a ditambahkan NaOAc kristal dan H-^BO^ kristal,
Adanya gugus orto-dihidroksi pada atom C nomor
3 1
dan V ditunjukkan oleh pergeseran bathokromik dari Band I sebesar 12-30 nm bi la dibandingkan dengan hasil spektra ultra lembayung dalam metanol p.a.2.5*3*1*5 Zat dalam metanol p.a ditambahkan AlCl^
kristal.
Spektra hasil penambahan AlCl^ kristal di catat panjang gelombang maksimumnya untuk digunakan pada langkah berikutnya.
2.5*3*1
*6
Zat dalain metanol p.a ditambahkan AlCl^ kristal dan HC1 pekat.2.5*3*1*6*1 Adanya gugus orto-dihidroksi pada atom C nomor
3
' dan V dapat ditunjukkan oleh pergeseran hipsokromik pada Band I sebe-sar
30-40
nm, bila dibandingkan dengan h&sil spektra ultra lembayung dalam metanol p.a ditambah AlCl^*
2.5.3*1.6*2 Adanya gugus OH pada atom C nomor 5 dapat ditunjukkan dengan pergeseran bathokromik pada Band I sebesar 35“ 55 nm, bila diban-..dingkan dengan hasil spektra ultra
leinbs-yung dalam metanol p.a.
dapat ditunjukkan dengan pergeseran batho kromik pada Band I sebesar 50-60 nm, bila
dibandingkan dengan hasil spektra ultra lembayung dalam metanol p.a.
Hasil identifikasi senyawa golongan flavon dan flavonol dengan spektrofotometer ultra lembayung dapat dilihat pada tabel I.
2.5*3*2 Identifikasi senyawa golongan isoflavon. 2.5*3.2.1 Zat dalam metanol p.a.
Spektranya mempunyai bentuk yang spesifik t dimana.Band II mempunyai intensitas lebih tinggi dibandingkan dengan Band I, bentuk Band I agak mendatar..
Band II mempunyai paivjang gelombang maksi -mum antara
245-270
nm.2.5*3.2.2 Zat dalam metanol p.a ditanbahkan NaOH pa-dat.
Adanya gugus OH pada atom C nomor 3* dan 4 f dapat ditunjukkan dengan terjadinya penurun an intensitas yang besar pada spektra dari Band II dibandingkan dengan hasil spektra ultra lembayung dalam metanol p.a.
2.5*3*2.3 Zat dalam metanol p.a ditambahkan NaOAc kristal.
2.5.3
.2
2.5.3.2
2.5.3.3
2
.5^3.34 Zat dalam metanol p.a ditambahkan NaOAc kristal dan H,BO, kristal.
3 3
Adanya gugus OH pada atom C nomor
6
dan 7 ditunjukkan oleh pergeseran bathokromik pa da Band I sebesar 10-15 nm, bila dibanding-kan dengan hasil spektra ultra lembayung da lam metanol p.a.5 Zat dalam metanol p.a ditambahkan AlCl^ kristal.
Dengan pereaksi ini tidak spesifik untuk i-soflavon.
6
Zat dalam metanol p,a ditambahkan AlCl^kristal dan HC1 pekat.
Adanya gugus OH pada atom C nomor 5 ditun -jukkan oleh pergeseran bathokromik pada Band II sebesar 10-14 nm, bila dibandingkan dengan hasil spektra ultra lembayung dalam metanol p.a.
Hasil identifikasinya dapat dilihat pada ta -bel II.
Ideptifikasi senyawa golongan flavanon dan di hidroflavonol.
.1 Zat dalam metanol p.a.
Flavanon dan dihidroflavonol mempunyai ben tuk spektra ultra lembayung yang spesifik , seperti dari isoflavon dalam pelarut meta nol p.a, dimana pada Band II mempunyai in
Band I. Perbedaan terletak pada besar pan jang gelombang maksimum yaitu pada flava -non dan dihidroflavonol ditunjukkan oleh panjang gelombang maksimum Band II sebesar
270-295 nm.
2.5*3-3*2 Zat dalam metanol p.a ditambahkan MaOH pa— dat.
Adanya gugus OH pada cincin A akan terjadi pergeseran panjang gelombang maksimum pada Band II, bila dibandingkan dengan hasil spektra ultra lembayung dalam metanol p.a. 2.5.3*3-2.1 Untuk senyawa golongan flavanon.
- Adanya gugus OH pada atom C nomor 5 dan
7
ditunjukkan olefi pergeseran bathokromik pada Band II sebesar 35 nm, bila di
4l.
bandingkan dengan hasil spektra ultra lembayung dalam metanol p-a.
- Adanya gugus OH pada atom C nomor 7 di tunjukkan oleh pergeseran bathokromik pada Band II aebesar 60 nm, bila diban dingkan dengan hasil spektra ultra lem bayung dalam metanol p.a.
2.5*3*3-2.2 Untuk senyawa golongan dihidroflavonol. - Adanya gugus OH pada atom C nomor 5 dan
X?
- Adanya gugus OH pada atom C nomor 7 di tunjukkan oleh pergeseran bathokromik pada Band II sebesar 5°"60 nm, bila di-bandingkan dengan hasil spektra ultra ■ lembayung dalam metanol p.a.
2.5*3*3*3 Zat dalam metanol p.a ditambahkan NaOAc kristal
2.5*3*3*3»1 Adanya gugus OH pada atom C nomor 5 dan 7 ditunjukkan oleh pergeseran bathokromik pada Band II sebesar 34-37 nm, bila diban dingkan dengan hasil spektra ultra lemba yung dalam metanol p.a.
2.5*3*3*3-2 Adanya gugus OH pada atom C nomor 7 ditun jukkan oleh pergeseran bathokromik pada Band II sebesar 51-58 nm, bila dibanding kan dengan spektra ultra lembayung dalam metanol p.a.
2.5*3*3*4 Zat dalam metanol p.a ditambahkan NaOAc kristal dan H^BO^ kristal.
Adanya gugus OH pada cincin A yaitu pada a-tom C nomor
6
dan 7 ditunjukkan oleh perge seran bathokromik pada Band I sebesar 10-15 nm, bila dibandingkan dengan hasil spektra ultra lembayung dalam metanol p.a.2.5.3.3.5 Zat dalam metanol p.a ditambahkan A1C13 kristal.
2.5*3*3*6 Zat dalam metanol p.a ditambahkan AlCl^ kristal dan HC1 pekat,
Adanya gugus OH pada atom C nomor 5 ditun -jukkan oleh pergeseran bathokromik pada Band I sebesar 20-26 nm, bila dibandingkan dengan hasil spektra ultra lembayung dalam
metanol p.a,
Hasil identifikasi senyawa golongan flavonon dan dihidroflavonol dengan spektrofotometer ultra lembayung dapat dilihat pada tabel III* 2.5*3*4 Identifikasi senyawa golongan, Kalkon dan Au «
ron.
2.5*3*4*1 Zat dalam metanol p.a.
Keduanya mempunyai bentuk spektra yang spe sifik, dimana Band I intensitasnya lebih tinggi bila dibandingkan dengan Band II, y^ itu Band I terletak pada panjang gelombang maksimum antara 340-390 nm dan Band II anta
ra
220-270
nm.Sedangkan untuk Auron Band I terletak pada panjang gelombang maksimum antara
370-430
nm.
2.5*3*4*2 Zat dalam metanol p.a ditambahkan dengan kristal NaOH.
2.5*3*4*2.1 Untuk golongan Kalkon.
Adanya gugus OH pada atom C nomor 4 ditunjukkan oleh pergeseran bathokromik pada Band 1 sebesar 60-100 nm, dengan
19
dingkan dengan hasil spektra ultra lemba yung dari metanol p.a.
Adanya gugus OH pada aton C nomor 2 atau nomor
4
* ditunjukkan dengan pergeser. an bathokromik pada Band I sebesar 60-100 nra, tanpa peningkatan intensitas puncak , bila dibandingkan dengan hasil spektra ul tra lembayung dalam metanol p.a.2.5*3-4*2.2 Untuk golongan Auron.
Adanya gugus OH pada atom C nomor 4' ditunjukkan dengan pergeseran bathokromik pada Band I sebesar 80-95 nm, bila diban dingkan dengan hasil spektra ultra lemba yung dalam metanol p.a.
Adanya gugus OH pada atom C nomor i
6
dan
4
' ditunjukkan dengan pergeseran ba -thokromik pada Band I yang lebih kecil, bila dibandingkan dengan hasil spektra ul tra lembayung dalam metanol p.a.2-5*3*4*3 Zat dalam metanol p.a ditambahkan NaOAc kristal.
2.5*3*4*3*1 Untuk golongan Kalkon,
Adanya gugus OH pada atom C nomor 4 atau gugus OH pada atom C nomor 4 dan 4
1
ditunjukkan dengan pergeseran bathokromik Band I, bila dibandingkan dengan hasil spektra ultra lembayung dalarn metanol p.a. 2-5-3*4*3*2 Untuk golongan Auron.
atau gugus OH pada atom C nomor 4 dan
6
' # ditunjukkan oleh pergeseran bathokromikBand I, bila dibandingkan dengan hasil spektra ultra lembayung dalam metanol p.a.. 2 . 5 * Zat dalam metanol p.a ditambahkan NaOAc
kristal dan H^BO^ kristal.
Adanya gugus orto-dihidroksi pada cin cin B ditunjukkan oleh pergeseran bathokro mik Band I sebesar 28-36 nm, bila dibanding kan dengan hasil spektra ultra lembayung da lam metanol p.a.
Adanya gugus orto-dihidroksi pada cin cin A ditunjukkan oleh pergeseran bathokro mik yang lebih kecil bila dibandingkan de -ngan hasil spektra ultra lembayung dalam rne tanol p.a.
2.5*3*4.5 Zat dalam metanol p.a ditambahkan AlCl^ kristal.
Adanya gugus orto-dihidroksi pada cin cin B untuk Kalkon dan Auron ditunjukkan o-leh pergeseran bathokromik pada Band I sebe
ear
40-70
nm, bila dibandingkan dengan hasil spektra ultra lembayung dalam metanol p.a.
21
2.5-3-4-6 Zat dalam metanol p.a ditambahkan AlCl^ kristal dan HC1 pekat.
2.5-3-4.6.1 Untuk golongan Kalkon.
Adanya gugus OH pada atom C nomor 2 1 ditunjukkan oleh pergeseran bathokromik Band I sebesar
48* 64
nra, bila dibanding. -kan dengan hasil spektra ultra lembayungdalam metanol p,a.
Adanya gugus tri-hidroksi pada-atom C nomor 2', 3* dan 4' ditunjukkan dengan pergaeeranvbathokromik pada Band I seki -tar
40
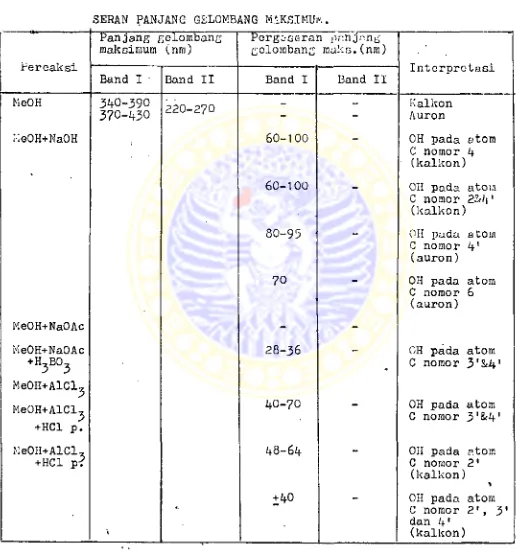
nm, bila dibandingkan dengan hasil spektra ultra lembayung dalam metanol p.a. Hasil identifikasi senyawa golongan Kalkon dan Auron dengan spektrofotometer ultra lem -bayung dapat dilihat pada tabel IV.2.6 Hidrolisa flavonoid.(13.17*20)
Hidrolisa flavonoid dapat digunakan asam
atau enzim, dimana kedua cara hidrolisa ini digu nakan untuk mengetahui flavonoid bentuk aglikon
dan senyawa gula yang terdapat dalam glikosida flavonoid.
senya-wa gula.
Sedangkan hidrolisa dengan enzim umumnya diguna -kan enzim j$, glukoeidase, y
3
-glukoronidase danTABEL I
IDENTIFIKASI SENYAWA GOLONGAW FLAVON DAN FLAVONOL
DENGAN SPLCKTROFOTOMETER ULTRA LEKBAYUNG
DENGAN.
MET
ODE PERGESERAN PANJANG GELOMBAUG MAKSIMUM.
TABEL II
IDENTIFIKASI S2NYAWA GOLONGAN ISOFLAVON DENGAN
SPEKTROFUTOMETER ULTRA LEMBAYUNG DENGAN METCDJ1
*
PERGESERAN PANJAHG GELCMRANG MAKSIMUM.
TABEL III
IDENTIFIKASI SEKYAWA GOLONGAN FLAVANON DAN DIHIDROFLA-
VONOL DENGAN '
S
PE
KTRO
FOT
0
MET
3
R ULTRA L3MBAYUNG .
DENG
A
ft
METODE PERGESERAN PANJANG G*SLQtfBAHG MAKSIMUM
TABEL IV
IDENTIFIKASI SENYAWA GOLONGAN KALKON PAN AURON DENGAN
SPSKTROFOTOMETUS ULTRA LSKBAYUNG DENGAN M
jITODE P^RGS-.
SERAN PANJANG G&LOMBANG MAKSIMUi*..
Pereaksi
Panjang gelombang
makcimum (nm)
Pcrgiseran
p a n j a n g ^ • c l o m b a n ^ mak/3.(nm)Band I ' Band II
Band I
Band II
inLcrproxasiMeOH
340-390
370-430
220-270
--Kalkon
Auron
MeOH+NaOH
-
60-100
OH pada
BAB III
METODE PENELITIAN
1• Bahan penelitian. bahan kimia dan alat-alat. 1•1 Bahan penelitian.
Sebagai bahan penelitian digunakan daun Bauhini £ purpurea Linn yang telah dideterminasi dengan
ban-tuan kunci determinasi. (
9
)Bahan dikumpulkan mulai bulan Desember 1988 da-ri Madiun Jawa Timur.
Gambar 1. Tanaman Bauhinia purpurea Linn.
1.2 Bahan kimla.
Kecuali dinyatakan lain, seraua bahan kimia yang di gunakan berderajat pro analisa (p.a)
Untuk ekstraksi : metanol teknis petroleum eter eter
etil asetat teknis n-butanol teknis
Untuk kromatografl lapisan tipis : lapisan tipis selulosa: Art. 5552
DC Alufolien cellulose n-butanol : asam asetat : air =
4
:1
: 5
aeam asetat : air =
15
s85
pereaksi sitrat borat dalam metanol amonium hidroksida
Untuk kromatografi kertas
Kertas Whatman : Whatman chromatography paper 1 m£ dium flow rate
Untuk kromatografi kolom cepat cara vakum : mikrokristal selulose: Art* 2250
cellulose mikrokristal
campuran air-metanol dengan berbagai macam perban-
29
natrium sulfat eksikatus barium karbonat
pereaksi Molisch pereaksi Barfoed pereaksi Luff ' pereaksi Fehling
1*3 Alat-alat : labu alas bulat pendingin balik penyaring
rotary evaporator Buchi tipe KRV 65/45 corong pisah
sintered glass pipa kapiler
spektrofotoraeter ultra lembayung: Hitachi 557
Double wavelength, Doublebeam Spectrophotg, meter
bejana kroraatografi 2. Cara ker.la
2*1 Penyiapan bahan penelitian
Daun Bauhinia purpurea Linn dikumpulkan dalam keadaan segar, kemudian dibersihkan dari kotoran yang melekat, kemudian dikeringkan dengan bantuan sinar matahari* Setelah kering bahan ditUmbuk dan diayak dengan pengayak B^q.
2*2 Isolasi senyawa golongan flavonoid
2.2.1 Pembuatan ekstrak dengan metode CHARAUX~PARIS
31
lapisan tipis senyawa golongan flavonoid. Ekstrak yang didapat diuapkan dengan tekanan rendah, sam-pai didapatkan ekstrak yang kental.
Ekstrak kental tersebut ditambah dengan air panas lebih kurang
200
ml, kemudian diaduk sampai homo gen dan didinginkan. Fase air dilakukan ekstraksi kocok dengan berbagai macam pelarut antara lain:1. Ekstrak air yang didapat diekstraksi dengan p£ troleum eter sampai fase petroleum eter tidak berwarna, kemudian fase petroleum eter dipisah kan dan diuapkan sampai kering.
2. Fase air hasil pemisahan (1) diekstraksi kemb^ bali dengan eter sampai fase eter tidak berwa£ na.
Fase eter dipisahkan dan diuapkan sampai kering. 3. Fase air hasil pemisahan (2)diekstraksi
kemba-11
dengan etil asetat sampai fase etil asetat tidak berwarna, kemudian fase etil asetat dipi sahkan dan diuapkan sampai kering.if. Fase air hasil pemisahan (3) diekstraksi kemb& li dengan nbutanol sampai fase nbutanol ti
-dak berwarna, kemudian fase n-butanol dipisahf-' kan dan diuapkan sampai kering.
Skema isolasi Fase petroleum"eter Fase air
33
2
.2.2
Identifikasi senyawa golongan flavonoid dari masing-masing fase hasil isolasi*2.2.2.1 Reaksi warna
- Reaksi Wiletater.(10)
Masing-masing fase hasil isolasi yang telah didapat dilarutkan dalam metanol p.a , kemudian ditambah 0,5 rol HC1 pekat dan sedi-kit demi sedisedi-kit serbuk Mg sampai jenuh. Pe-rubahan warna yang terjadi diamati setelah
10
menit, kemudian diencerkan dengan air su~ ling sama banyak dan ditambah1
ml n-butanol. Kemudian perubahan warna ysng terjadi pada kedua lapisan tersebut diamati.- Reaksi Bate Smith-Metealfe.
Masing-masing fase hasil isolasi yang telah didapat dilarutkan dalam metanol p.a, kemudian ditambah 0,5 ml HC1 pekat. Perubah an warna yang terjadi diamati. Setelah itu dipanAskan
15
menit diatas penangas air, pe rubahan warna yang tejadi diamati.2.2.2.2 Kromatografi lapisan tipis
Bahan : Masing-masing fase hasil isolasi. Lempeng : selulose ^
25
^Eluen : n-butanol-asamasetat-air = 1+ : 1 : 5 asam asetat-air =
15
•85
Penampak noda : citrat borat dalam metanol 2.3 Pemisahan dan pemurnian
2.3 Kromatografi cepat cara vakum
yang banyak digunakan untuk memisahkan komponen zat dari campurannya* Pemisahan dieini dilaku -kan dengan kromatografi cepat cara vakum.
Seba-gai fase diam digunakan mikrokristalin selulose,. sedang fase geraknya digunakan campuran air-me-tanol dengan berbagai macam perbandingan, yaitu air-metanol 100 • 0
Volume masing-masing adalah 20 ml. Cara ker.la:
Fase diam dalam keadaan kering dimasukkan ke -dalam sintered glass, ditekan sarabil dihisap dengan pompa vakum dan permukaannya diratakan. - Zat yang akan dikromatografi cepat cara vakum
dilarutkan dalam sedikit pelarut (metanol) ke* mudian dicampur dengan fase diam sampai rata > dikeringkan, dimasukkan ke dalam sintered
glass di atas fase diam yang telah dimarapatkan, kemudian bagian ataBnya ditutup dengan kertas
35
- Fase gerak pertama yaitu air-metanol (100 : 0) sebanyak
20
ml dituangkan ke dalam sintered glass. Untuk merapercepat aliran fase geraknya, fase gerak ditarik dengan pompa hisap sampai cairan tidak raenetes lagi. Cairan tersebut di~ tarapung, diberi kode pada wadahnya.Perlakuan tersebut diulang kembali dengan fase gerak yang sama.
- Sesudah itu fase gerak yang kedua yaitu air-me tanol
(90
:10
) dimasukkan ke dalam : sintered glass, kemudian fase geraknya ditarik . dengan pompa hisap lagi sampai cairan tidak rcenetes lagi. Cairan yang diperoleh ditampung, diberi kode pada wadahnya* Begi'tu seterusnya . aampaifase gerak yang terakhir yaitu air-metanol
(0
:
1 0 0) .
- Setelah semua selesai, masing-masing fraksi di lakukan uji kromatografi lapisan tipis.
2
.3* 2
Identifikasi senvawa golongan flavonoid hasil kromatoprrafi cepat cara vakum.2*3*2.1 Reaksi warna Reaksi wilstater
2*3»2.2 Krornatografi lapisan tipis
Bahan : senyawa hasil krornatografi cepat cara vakum*
Fase diam : letnpeng selulose
^254
Eluen : n-butanol-asamasetat-air asam asetat-air =
15
:85
Penampak noda : pereaksi sitrat borat dalam metanol
2.3*3 Krornatografi kertas preparatlf
Fraksi yang didapat dari krornatografi ce pat ca-ra vakum ternyata masih berupa noda yang tak terpisahkan, sehingga dipakai cara kromato-grafi kertas preparatif. untuk memisahkan noda tersebut.
Bahan yang dipakai : fraksi-fraksi hasil kroma-tografi cepat cara vakum. Fase diam : kertas whatman no 1
Eluen : n-butanol-asam asetat-air = 4 : 1 : 5
asam asetat-air =
15
i 85 Cara kerja- Dasar bejana krornatografi diisi dengan fase gerak,.didiamkan semalam supaya jenuh.
Larutan zat dalam metanol, kemudian ditotol -kan sebagai garis tipis memanjang raulai dari • tepi kertas sampai tepi yang lain dan
dibiar-kan kering.
- Fase gerak dimasukkan ke dalam bak pelarut , kemudian fase diam digantungkan dalam bejana
37
kertas di dalam bak polarut.
Eluasi dihentikan bila fase gerak telah menc& pai batas bawah tertentu.
- Kromatogram yang telah dieluasi dikeringkan untuk menghilangkan sisa-sisa larutan fase ge rak.
Setelah kromatogram kering kemudian ditentu -kan letak noda-nodanya dengan memakai uap amo nia. Noda-noda yang tampak diberi tanda de-i ngan pensil, kemudian digunting.
- Guntingan kromatogram diekstraksi dengan meta nol untuk melarutkan zat yang raenempel pada kromatogram tersebut, kemudian disaring dan dilakukan identifikasi senyawa flavonoid de ngan reaksi warna, kromatografi lapisan tipis
dan spektrofotometer lerabayung ultra.
2.3.^ Identifikasi senyawa golongan flavonoid hasil kromatografi kertas prepa ratif•
2.3.4.1 Reaksi warna
- Reaksi Wiletater
Senyawa hasil kromatografi kertas pre-paratif yang telah dilarutkan dalam metanol p.a ditambah 0,5 ml HC1 pekat dan sedikit serbuk Mg. Perubahan warna diamati setelah
2.3*^*2 Krornatografi lapisan tipis
Bahan : senyawa hasil krornatografi kertas pre paratif.
Fase diam : lempeng selulose
Eluen : n-butanol-asam asetat-air = 4 : 1 : 5 asam asetat-air = 15 • 85
Penampak noda : sitrat borat dalam metanol
2.4 Hldrolisa asam Cara kerja
Ditimbang + 50 rag zat hasil krornatografi ke£ tas preparatif, dimasukkan dalam Erlenmeyer, kemu dian ditambah campuran metanol-air (1 : 1) sampai larut dan 10 ml H^SO^ 2N kemudian dipanaskan JO
menit di atas penangas air. Setelah itu didingin-kan dan kemudian diekstraksi dengan eter* Dalam
corong pisah fase eter dipisahkan dan pada fase eter tersebut ditambah natrium sulfat eksikatus , kemudian disaring dan filtratnya diuapkan sampai kering. Dalam fase eter ini terkandung flavonoid
dalam bentuk bebae sedang senyawa gulanya terda -pat dalam fase air. Fase eter yang kering dilaku kan identifikasi senyawa golongan flavonoid. Fase air dinetralkan dengan barium karbonat. Endapan barium sulfat yang terjadi disaring dan filtrat -nya diuapkan sampai 1/3 bagian. Pada fase air ini dilakukan identifikasi senyawa gula*
39
2.1+.1.1 Reaksi warna
- Reaksi Wilstater
. Senyawa hasil hidrolisa dilarutkan da lam metanol p.a kemudian ditambah 0,5 ml HC1 pekat dan sedikit serbuk Mg. Perubahan warna diamati setelah 10 menit, kemudian di tambah dengan air suling sama banyak dan 1 ml n-butanol, perubahan warna yang terjadi pada kedua lapisan diamati.
2.if. 1.2 Kromatografi lapisan tipis
Bahan : senyawa hasil hidrolisa. Fase diam : lempeng selulose
Eluen : n-butanol-asam asetat-air = 4 : 1 : 5 asam asetat-ail* = 15 * 85
Penampak noda : sitrat borat dalam metanol. 2.if.2 Identifikasi senyawa gula dari hasil hidrolisa
- Reaksi Molish .
Ke dalara larutan zat dalam air ditambah alfa-naftol 3# dalam etanol dan asam sulfat pekat perlahan-lahan melalui dinding tabung reaksi. Warna cincin yang terjadi diamati.
- Reaksi Luff
Ke dalam larutan zat dalam air ditambah pere aksi Luff, kemudian dipanaskan diatas pena -ngas air, endapan yang terjadi diamati.
- Reaksi Fehling
terjadi diamati. - Reaksi Barfoed
Ke dalam larutan ditambahkan pereaksi Barfoed, kemudian dipanaskan dlatas penangas air. Endapan yang terjadi diamati.
2.5 Identifikasi dengan spektrofotometer lembayung ultra Bahan: senyawa hasil krornatografi kertas preparatif
dan senyawa hasil hidrolisa. Pelarut dan pereaksi:
Langkahlangkah yang dilakukan untuk mendapat -kan enam spektra pada metode ini adalah
- Spektra MeOH p. a
Senyawa dilarutkan dalam metanol p.a, kemudian am£ ti dengan spektrofotometer lembayung ultra pada panjang gelombang maksimum
24
O-4
OO nm, panjang ge-lombang maksimum yang dihasilkan dicatat- Spektra NaOMe
Senyawa yang dilarutkan dalam metanol p.a, kemudi an ditambah natrium hidroksida, panjang gelombang maksimum yang dihasilkan dicatat. Pergeseran pan
- Spektra NaOAc
Senyawa yang dilarutkan dalam metanol p.a ditam-bah natrium asetat kristal, panjang gelombang maksimum yang dihasilkan dicatat. Pergeseran pan
jang gelombang maksimumnya diamati dengan cara membandingkan panjang gelombang maksimum hasil
spektra.tersebut dengan panjang gelombang maksi mum hasil spektra dalam metanol.
■ - Spektra NaOAc + H^BO^
Senyawa yang dilarutkan dalam metanol p.a ditam bah natrium asetat kristal, kemudian ditambah a-sam borat kristal, panjang gelombang maksimum yang dihasilkan dicatat. Pergeseran panjang ge lombang maksimumnya diamati dengan cara memban -dingkan panjang gelombang maksiraum hasil spektra tersebut dengan panjang gelombang maksimum hasil spektra dalam metanol.
- Spektra AlCl^ + HC1
Senyawa yang dilarutkan dalam metanol p.a ditam-bah aluminium klorida kristal, kemudian ditamditam-bah aeam klorida pekat, panjang gelombang maksimum yang dihasilkan dicatat. Pergeseran panjang ge lombang maksimumnya diamati dengan cara memban -dingkan panjang gelombang maksimum hasil spektra tersebut dengan panjang gelombang maksimum hasil spektra dalam metanol maupun dengan panjang ge -lombang maksimum hasil spektra dalam metanol di tambah aluminium klorida kristal.
Dari keenam spektra tersebut dapat ditentukan go
BAB IV
HASIL PENELITIAN 1• Bahan penelitian
Sebagai bahan penelitian adalah daun dari tanaman Bauhl-nia -purpurea Linn, seeuai dengan yang tercantum pada kun ci determinasi.
2* Isolasi senyawa golongan flavonoid*
2.1 Pembuatan ekstrak
Dari ekstraksi yang telah dilakukan dengan pelarut me -tanol, didapat ekstrak kental berwarna hijau kehitaman. Setelah dilakukan ekstraksi kocok dengan metode Charaux -Paris diperoleh hasil sebagai berikut:
Pada fase petroleum eter didapat ekstrak kental ber -warna hijau kehitaman* (12,5 g)
- Pada fase eter didapat ekstrak kental berwarna hijau kehitamam. ( 1 g )
- Pada fase etil asetat didapat ekstrak kental berwarna merah coklat* (1,7 g)
- Pada fase n-butanol didapat ekstrak kental berwarna merah coklat. (12,4 g)
Masing-masing fase diatas dilakukan uji krornatografi 1& pisan tipis untuk memdeteksi kandungan flavonoidnya. Fase diam : lapisan tipis selulose
TABEL V
HASIL KROMATOGRAFI LAPISAN TIPIS DARI FASE PETROLEUM ETER,FASE ETER,FASE E-TIL ASETAT,FASE N-BUTANOL
Fase Penampak noda Warna noda R f
Petroleum eter Eter
Etil asetat N-butanol
sitrat borat sitrat borat sitrat borat sitrat borat
kuning kuning
0,61
2.2 Pemisahan dan nemurnian
Dari hasil kromatografi lapisan tipis di atas terlihat bahwa pada fase petroleum eter dan fase eter tidak di dapatkan noda flavonoid. Noda flavonoid didapatkan pa-da fase etil asetat pa-dan fase n-butanol* Untuk proses selanjutnya dalam penelitian ini diamni.l fase etil ase tat dan fase n-butanol*
Terhadap kedua fase tersebut dilakukan pemisahan rtti-ngan kromatografi kolom cepat cara vakunw
Dengan cara tersebut pada masing-masing fase diperoleh 22 fraksi, kemudian dilakukan uji kromatografi lapisan tipis selulose, fase gerak n-butanol~asam asetat-air =
k •
1
'•5
i penampak noda pereaksi sitrat borat dalam✓
metanol*
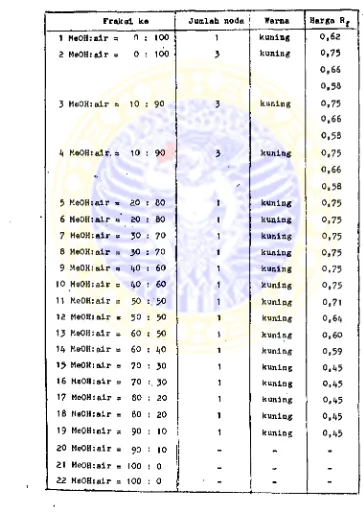
HASIL KROMATOGRAFI LAPISAN TIPIS DARI FASE ETIL ASETAT SETELAH DILAKUKAN PEMISAHAN DE NGAN KROMATOGRAFI CEPAT CARA VAKUM
TABEL VI
Fraksi ke Jumlah noda Warna Harga Rf
h
7
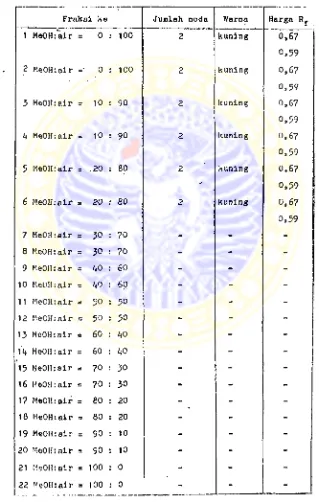
HASIL KROMATOGRAFI LAPISAN TIPIS DARI FASE N - BUTANOL SETELAH DILAKUKAN PEMISAHAN DE NGAN KROMATOGRAFI CEPAT CARA VAKUM
Pada fase etil asetat, fraksi yang mempunyai 3 no da dikumpulkan jadi satu dan fraksi yang mempunyai satu noda dengan harga R^ yang sama juga dikumpul kan jadi' satu.
Untuk identifikasi senyawa golongan flavonoid se lanjutnya digunakan fraksi 6,7 dan 8 karena pada fraksi yang mempunyai 3 noda, nodanya sulit dipi -sahkan dan fraksi lain yang mempunyai 1 noda konsentrasinya terlalu kecil. Untuk memisahkan koto ran yang terdapat dalam fraksi 68 digunakan kro -matografi kertas preparatif. Hasil pemisahan de ngan krornatografi kertas preparatif tersebut untuk selanjutnya disebut senyawa E.
Pada fase n-butanol, untuk identifikasi senyawa go longan flavonoid selanjutnya digunakan fraksi 2 dan .3 yang mempunyai konsentrasi yang lebih besar dibandingkan dengan fraksi lain. Karena fraksi 2 dan 3 mempunyai lebih dari satu noda, maka untuk memisahkannya digunakan krornatografi kertas prepa ratif. Dari hasil pemisahan dengan krornatografi kertas preparatif didapatkan 2 fraksi, yaitu frak
si bawah yang untuk selanjutnya disebut senyawa A dan fraksi atas yang untuk selanjutnya disebut se nyawa B.
2.3 Identifikasi senyawa hasil isolasi 2.3.1 Reaksi warna
2.3.2 Krornatografi lapisan tipis
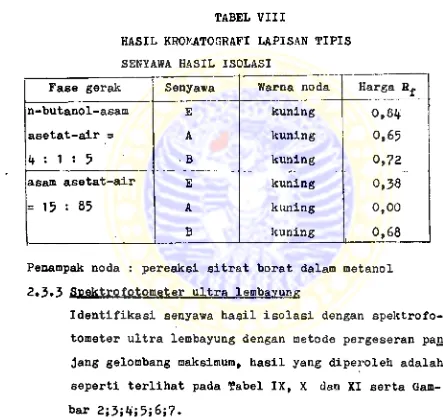
Dengan menggunakan lapisan tipis selulosa, beberapa fase gerak dan penampak noda pereaksi sitrat borat dalam metanol, hasil yang diperoleh adalah seperti terlihat pada Tabel VIII.
49
TABEL VIII
HASIL KROMATOGRAFI LAPISAN TIPIS SENYAWA HASIL ISOLASI
Fase gerak Senyawa Warna noda Harga
n-butanol-asam E kuning
0,84
asetat-air = A kuning 0,65
4 : 1 : 5 ■ B kuning 0,72
asam asetat-air E kuning 0,38
= 15 : 85 A kuning
0,00
B kuning
0,68
Penampak noda : pereaksi sitrat borat dalam metanol 2*3»3 Spektrofotometer ultra lembavung
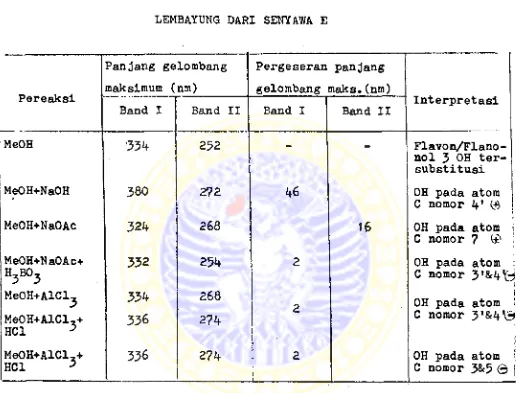
Identifikasi senyawa hasil isolasi dengan spektrofo tometer ultra lembayung dengan metode pergeseran pan Jang gelombang maksimum, hasil yang diperoleh adalah seperti terlihat pada Tabel IX, X dan XI serta
TABEL IX
DATA HASIL SPEKTR0F0T0METER ULTRA
LEMBAYUNG DARI SENYAWA E
Panjang gelombang Pergeseran panjang
Pereaksi maksimum (nm) gelombang maks.(nm) Interpretasi Band I Band II Band I Band II
MeOH 3 3 k 252 - - FIavo
n/Flano-nol 3 OH ter-substitusi
MeOH+NaOH 380 272 k6 OH pada atom
C nomor k f (& |
i
MeOH+NaOAc 32k 268 16 OH pada atom i
Gambar 2. Spektra ultra lembayung dari senyawa E (a). Spektra dalam MeOH
Gambar 3* Spektra ultra lembayung dari senyawa E Spektra dalam
NaOAc+H^BO-* j j
Spektra dalam AlCl^ Spektra dalam A1C1^+HC1 (d).
53
TABEL X
DATA HASIL SPEKTROFOTOMETER ULTRA LEMBAYUNG DARI SENYAWA A
Panjang gelombang Pergeseran panjang
Pereaksi
maksimum (nm) gelombang maks.(nm)
Interpretasi i
Band I Band II Band I Band II
MeOH 353 255 - - Flavonol
MeOH+NaOH 398 272 45 OH pada atom
C nomor 4' ©
MeOH+NaOAc 372 267 12 OH pada atom
Gambar i|. Spektra ultra lembayung dari senyawa A (a)* Spektra dalam MeOH
Gambar 5. Spektra ultra lembayung dari senyawa (d). Spektra dalam NaOAc+H^BO^
TABEL XI
DATA HASIL SPEKTROFOTOMETER ULTRA LEMBAYUNG DARI SENYAWA B
Panjang gelombang maksimum (nm)
Pergeseran panjang gelombang maks.(nm) Pereaksi
Band I Band.II Band I Band II Interpretasi
MeOH y*? 255 — , •
Flavon/Flavon-MeOH+NaOAc
366
27if 19 OH apda atom C57
Gambar 6. Spektra ultra lerobayung dari senyawa B (a). Spektra dalara MeOH
Gambar 7. Spektra ultra lerabayung dari seayav/a B (d). Spektra dalam NaOAc+H-jBO^
j 3 (e). Spektra dalam AlCl^
59
Dari Tabel IX dan Gambar 2;3 dapat diketahui bahwa se nyawa E merupakan golongan flavon yang mempunyai gu -gus OH pada atom C nomor 7,3* dan if1.
Dari Tabel X dan Gambar **;5 dapat diketahui bahwa se nyawa A merupakan golongan flavonol yang mempunyai gu gus OH pada atom C nomor 5>7»3' dan V *
Sedang dari Tabel XI dan Gambar
6
;7 dapat diketahui bahwa senyawa B merupakan golongan flavon yang mempu nyai gugus OH pada atom C nomor 5,7 dan V2*k Hidrolisa dengan asam
Pada senyawa E, X maupun B dilakukan hidrolisa dengan
asam sulfat 2N. Dipanaskan selama 15 menit, setelah itu dilakukan ekstraksi kocok dengan eter untuk mena-rik aglikonnya. Setelah fase eter diuapkan pada se nyawa E didapatkan serbuk amorf berwarna kuning ( se nyawa E j K Pada senyawa A didapatkan serbuk amorf ber warna kuning (senyawa A^)« Pada senyawa B didapatkan serbuk amorf berwarna kuningC senyawa B^}.
Fase air yang mengandung asam sulfat dinetralkan de -ngan barium karbonat, kemudian endapan barium sulfat yang terjadi disaring. Fase air yang mengandung gula digunakan untuk identifikasi senyawa gula*
2*5 Identifikasi senyawa hasil hidrolisa 2*5*1 Reaksi warna Wilstater
Dengan pereaksi Wilstater memberikan v/arna merah yang dapat ditarik dengan n-butanol.
2.5.2 Kromatografi lapisan tipis
fase gerak dan penampak noda pereaksi sitrat borat dalam metanol, hasil yang didapat adalah seperti terlihat pada Tabel XII*
TABEL XII
HASIL KROMATOGRAFI LAPISAN TIPIS SENYAWA HASIL HIDROLISA
Fase gerak Senyawa Warna noda Harga R
n-butanol-asam
E1
kuning 0,85asetat-air = A. kuning o , a e
4 : 1 : 5 B. kuning 0,85
asam asetat-air E kuning
0
,01
*= 15 : 85' A i kuning
0,00
B1 kuning
0,02
Penampak noda : pereaksi sitrat borat dalam metanol* 2.5*3 Spektrofatometer ultra lemba.yung
Identifikasi senyawa hasil hidrolisa dengan spektro-fotometer ultra lembayung dengan inetode pergeseran panjang gelombang maksimum, diperoleh hasil seperti terlihat pada Tabel XIII,XIV,XV dan Gambar
8
;9;10;114
12;13-61
TABEL XIII
DATA HASIL SPEKTROFOTOMETER ULTRA LEMBAYUNG DARI SENYAWA
Panjang gelombang Pergeseran panjang maksimum (nm) gelombang maks.(nm)
Pereaksi Interpretasi
Band I Band II Band I Band II
MeOH 364 254 - - Flavonol
MeOH+NaOH
410
276^6
OH pada atomC nomor 4 ’ €■
MeOH+NaOAc 376 272 18 OH pada atom
C nomor 7 0
270
60 OH pada atomGambar 8* Spektra ultra lerabayung dari senyawa (a). Spektra dalam MeOH
63
(d). Spektra dalam NaOAc+H^BO^ (©)• Spektra dalam AlCl^
TABEL XXV
DATA HASIL SPEKTROFOTOMETER ULTRA LEMBAYUNG DARI SENYAWA A ^
P.ereaksi
MeOH 364 269 - - FlavonoX
MeOH+NaOH
400
272 36 OH pada atomC nomor 4'
MeOH+NaOAc 380 273 4 OH pada atom
65
Gambar 10. Spektra ultra lembayung dari senyawa (a ).« Spektra dalam MeOH
(b). Spektra dalam NaOMe . (c). Spektra dalam NaOAc
! i:
II
t
i
I Li_U
iii
i.i
I
pI.:.
Qambar 11. Spektra ultra lembayung dari senyawa (d). Spektra dalara NaOAc+H,BO,
67
TABEL XV
DATA HASIL SPEKTROFOTOMETER ULTRA LEMBAYUNG DARI SENYAWA B
1
MeOH 362 254 - - Flavonol
MeOH+NaOH
412
273 50 OH pada atomC nomor 3&4'(+)
MeOH+NaOAc 374 272 18 OH pada atom
Gambar 12. Spektra ultra lembayung dari senyawa B
1
69
Gambar 13* Spektra ultra lembayung dari senyawa B (d). Spektra dalam NaOAc+H^BO^
2.5*4 Identifikasi senyawa gula
Haeil identifikasi senyawa gula hasil hidrolisa se perti terlihat pada Tabel XVI
TABEL XVI
HASIL IDENTIFIKASI SENYAWA GULA HASIL HIDROLISA
Pereaksi Senyawa Hasil
Molisch E (?) cincin warna ungu A (±) cincin warna ungu B (+) cincin warna ungu
Luff E © endapan merah bata
. A G> endapan merah bata
‘ B <
3
' endapan merah bata Fehling E © endapan merah bata A @ endapan merah bata B ® endapan merah bata Barfoed E @ endapan merah bataA
0
71
O
0Gambar 14* Kromatogram senyawa hasil isolasi (2) dan senyawa hasil hidrolisa (£^)
Lapisan tipis : selulosa
Faeo gerak : n-butanol~asam
acetat-air = 4 : 1 : 5