BAB II
TINJAUAN PUSTAKA
2.1 Uraian Pati Jagung
Pati merupakan homopolimer glukosa dengan ikatan α-glikosidik, yang
banyak terdapat pada tumbuhan terutama pada biji-bijian, umbi-umbian. Berbagai
macam pati tidak sama sifatnya, tergantung dari panjang rantai atom karbonnya,
serta lurus atau bercabang (Jane, 1995). Pati dalam jaringan mempunyai bentuk
butir yang berbeda-beda. Umumnya butir pati terdiri dari lapisan-lapisan yang
mengelilingi suatu titik yang disebut hillus. Hillus dapat terletak ditengah atau
dapat pula dipinggir. Biji jagung mengandung pati 54,1% - 71,7%, karbohidrat
pada jagung sebagian besar merupakan komponen pati, sedangkan komponen
lainnya adalah pentose, dekstrin, sukrosa, dan gula pereduksi (Fahn, 1992)
Granul pati utuh tidak larut dalam air dingin. Granul pati dapat menyerap
air dan mengembang, tetapi dapat kembali seperti semula. Apabila granul pati
ditambahkan air panas atau dingin yang kemudian dipanaskan, maka pati dapat
mengalami gelatinasi (Winarno, 1995).
Granula pati terdiri dari dua fraksi yang dapat dipisahkan dengan air panas.
Fraksi terlarut disebut amilosa dan fraksi yang tidak terlarut disebut amilopektin
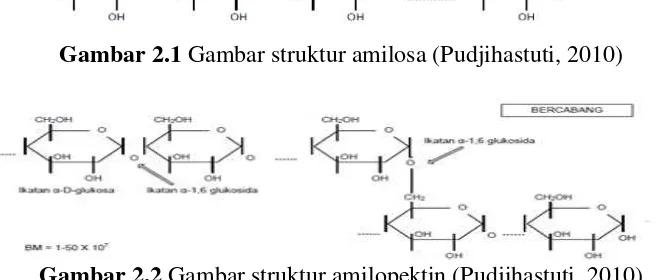
(Winarno, 2002). Amilosa merupakan bagian polimer dengan ikatan α-(1,4) dari
unit glukosa, yang membentuk rantai lurus, yang umumnya dikatakan sebagai
linier dari pati. Struktur ini mendasari terjadinya interaksi iodamilosa membentuk
warna biru (Pudjihastuti, 2010).
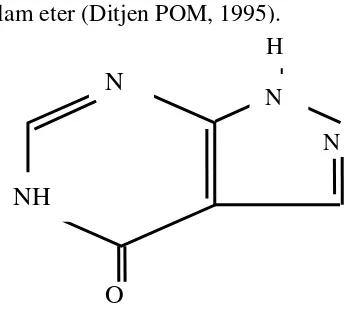
D-glukosa dalam jumlah yang besar. Perbedaannya ada pada tingkat percabangan yang tinggi dengan ikatan α-(1,6)-D-glukosa dan bobot molekul yang besar Bila
amilosa direaksikan dengan larutan iod akan membentuk warna biru tua,
sedangkan amilopektin akan membentuk warna merah (Taggart, 2004).
Gambar 2.1 Gambar struktur amilosa (Pudjihastuti, 2010)
Gambar 2.2 Gambar struktur amilopektin (Pudjihastuti, 2010)
2.2 Klasifikasi Tanaman Jagung Divisio : Spermatophyta
Sub-divisio : Angiospermae
Klass : Monocotyledoneae
Ordo : Poales
Famili : Poaceae
Genus : Zea
Spesies : Zea mays L (Hartono, 2007)
Gelatinasi merupakan proses pembengkakan granula pati ketika
dipanaskan dalam media air. Granula pati tidak larut dalam air dingin, tetapi
granula pati dapat mengembang dalam air panas. Naiknya suhu pemanasan akan
meningkatkan pembengkakan granula pati. Pembengkakan granula pati
menyebabkan terjadinya penekanan antara granula pati dengan lainnya
(Pomeranz, 1991). Pembengkakan yang diikuti dengan gelatinasi pati terjadi
ketika energi kinetik molekul-molekul air menjadi lebih kuat dari pada daya tarik
menarik antara molekul pati di dalam granula yang menyebabkan air dapat masuk
ke dalam butir-butir pati (Winarno, 1995). Gelatinasi adalah perubahan yang
terjadi pada granula pada waktu mengalami pembengkakan yang luar biasa dan
tidak dapat kembali ke bentuk semula (Winarno, 2002).
Gelatinasi juga disebut sebagai peristiwa koagulasi koloid dengan ikatan
rantai polimer atau penyerapan zat terlarut yang membentuk jaringan tiga dimensi
yang tidak terputus sehingga dapat mengakibatkan terperangkapnya air dan
terhentinya aliran zat cair yang ada di sekelilingnya kemudian mengalami proses
pengorientasian partikel (Meyer, 1973). Suhu gelatinasi adalah suhu pada saat
granula pati pecah. Suhu gelatinasi berbeda-beda bagi tiap jenis pati dan
merupakan suatu kisaran. Menurut Singh, dkk., (2005) suhu gelatinasi pati jagung
69°C - 72°C.
Rahman (2007) menyatakan bahwa gelatinasi merupakan fenomena
kompleks yang bergantung pada:
a. ukuran granula
pada umumnya granula yang besar membentuk gel lebih lambat sehingga
b. persentase amilosa
pati yang memiliki amilosa dengan kadar tinggi suhu gelatinasinya juga akan
tinggi.
c. bobot molekul
makin besar bobot molekul dari granul pati pembentukan gel akan semakin
lambat.
d. derajat kristalisasi dari molekul pati di dalam granula.
Makin besar derajat kristalisasi dari granula pati, pembentukkan gel semakin
lambat.
Menurut Pomeranz (1991), tidak semua granula pati tergelatinasi pada titik
yang sama, tetapi terjadi pada suatu kisaran suhu tertentu. Proses gelatinasi
melibatkan peristiwa-peristiwa sebagai berikut:
a. hidrasi dan swelling (pengembangan) granula
b. hilangnya sifat birefringent
c. peningkatan kejernihan
d. peningkatan konsistensi dan pencapaian viskositas puncak
e. pemutusan molekul-molekul linier
f. penyebarannya dari granula yang telah pecah.
Suhu gelatinasi tergantung pada konsentrasi dan pH larutan pati. Makin
kental larutan, suhu gelatinasi makin sulit tercapai. Bila pH terlalu tinggi,
pembentukan gel semakin cepat tercapai tetapi cepat turun lagi. Pembentukan gel
optimum pada pH 4 - 7. Selain itu, penambahan gula juga berpengaruh terhadap
kekentalan gel yang terbentuk. Gula akan menurunkan kekentalan, hal ini
pati menjadi lebih lambat, akibatnya suhu gelatinasi akan lebih tinggi. Adanya
gula akan menyebabkan gel lebih tahan terhadap kerusakan mekanik (Winarno,
2002).
2.4Allopurinol 2.4.1 Tinjauan umum Rumus molekul : C5H4N4O
Nama kimia : 1H-Pirazolol[3,4-d]pirimidin-4-ol[315-30-0]
Berat molekul : 136,11
Pemerian : Serbuk halus putih hingga hampir putih, berbau lemah.
Kelarutan : Sangat sukar larut dalam air dan etanol; larut dalam kalium dan
natrium hidroksida; praktis tidak larut dalam kloroform dan
dalam eter (Ditjen POM, 1995).
Gambar 2.3. Rumus Bangun Alopurinol (Ditjen POM, 1995). 2.4.2 Farmakologi
Allopurinol bekerja dengan cara mengurangi sintesa asam urat atas dasar
persaingan substrat dengan zat-zat purin berlandaskan enzim xanthin oksidase.
Enzim yang mengubah hipoxantin menjadi xantin dan selanjutnya menjadi asam
urat. Melalui mekanisme umpan balik allopurinol menghambat sintesa purin yang
merupakan prekursor xanthin (Katzung, 2004).
N H N N
NH
Allopurinol di dalam tubuh mengalami metabolisme menjadi oksipurinol
(alloxantin) yang juga bekerja sebagai penghambat enzim xantin oksidase.
Mekanisme kerja senyawa ini berdasarkan katabolisme purin dan mengurangi
produksi asam urat, tanpa mengganggu biosintesa purin. Allopurinol dapat
meningkatkan frekuensi serangan artritis gout akut sehingga sebaiknya obat anti
inflamasi atau kolkisin diberikan bersama pada awal terapi (Katzung, 2004).
Allopurinol kira-kira 80% diserap setelah pemakaian oral.
Persenyawaan hasilnya oksipurinol mempertahankan kemampuannya untuk
menghambat xanthine oxidase dan mempunyai durasi kerja yang cukup
panjang sehingga allopurinol cukup diberikan satu kali sehari (Katzung, 2004).
2.5 Pengertian Tablet
Tablet adalah sediaan padat yang mengandung bahan obat dengan atau
tanpa bahan pengisi. Sebagian besar tablet dibuat dengan cara pengempaan dan
merupakan bentuk sediaan yang paling banyak digunakan. Tablet kempa dibuat
dengan memberikan tekanan tinggi pada serbuk atau granul menggunakan cetakan
baja. Tablet dibuat dengan berbagai ukuran, bentuk dan penandaan permukaan
tergantung pada desain cetakan (Ditjen POM, 1995).
Untuk mendapatkan tablet yang baik, maka bahan pengisi yang akan
dikempa menjadi tablet harus memenuhi sifat- sifat berikut :
a. mudah mengalir, artinya jumlah bahan yang akan mengalir dalam corong alir
ke dalam ruang cetakan selalu sama setiap saat, dengan demikian bobot tablet
b. kompatibel, artinya bahan mudah kompak jika dikempa, sehingga dihasilkan tablet yang keras.
c. mudah lepas dari cetakan, hal ini dimaksudkan agar tablet yang dihasilkan
mudah lepas dan tidak ada bagian yang melekat pada cetakan, sehingga
permukaan tablet halus dan licin (Sheth, dkk., 1980).
Tablet dibuat dengan 3 cara umum yaitu : Granulasi basah, granulasi
kering dan cetak langsung. Tujuan granulasi basah dan kering adalah untuk
meningkatkan aliran campuran dan atau kemampuan kempa. Granulasi kering
dibuat dengan cara menekan massa serbuk pada tekanan tinggi sehingga menjadi
tablet yang besar kemudian digiling dan diayak hingga diperoleh granul dengan
ukuran partikel yang diinginkan. Cetak langsung merupakan pengempaan
langsung dengan kecepatan tinggi tanpa tahap granulasi terlebih dahulu (Ditjen
POM, 1995).
2.6 Metode Granulasi Basah
Metode ini merupakan metode pembuatan yang paling banyak digunakan
dalam memproduksi tablet kompresi. Langkah-langkah yang diperlukan dalam
pembuatan tablet dengan metode ini dapat dibagi sebagai berikut: menimbang dan
mencampur bahan-bahan, pembuatan granulasi basah, pengayakan granul basah,
pengeringan, pengayakan granul kering, pencampuran bahan pelicin dan bahan
penghancur, pembuatan tablet dengan kompresi (Ansel, 1989).
Metode granulasi basah dilakukan dengan terlebih dahulu mencampur zat
berkhasiat, zat pengisi dan zat penghancur dicampur baik-baik, lalu dibasahi
menjadi granul, dan dikeringkan dalam almari pengering pada suhu 40oC - 50oC.
Setelah kering diayak lagi untuk memperoleh granul dengan ukuran yang
diperlukan dan ditambahkan bahan pelicin dan dicetak menjadi tablet dengan
mesin tablet (Ansel, 1989).
2.7 Teori Pencampuran
Proses pencampuran merupakan proses yang sangat penting sebelum
dilakukan pencetakan tablet. Pencampuran bertujuan untuk memperolah
campuran homogen antar partikel-partikel penyusunnya, pencampuran yang
kurang baik atau tidak homogen akan menyebabkan kadar zat aktif dalam tablet
kurang seragam (Parrott, 1971).
Campuran yang homogen pada pencampuran serbuk dipengaruhi oleh
bentuk partikel. Bentuk partikel berpengaruh terhadap gerakan partikel pada
waktu pencampuran. Partikel-partikel yang ideal berbentuk bola karena lebih
mudah bergerak, sedangkan partikel yang berbentuk jarum dan partikel yang tidak
teratur lebih sukar bergerak dan membentuk agregat (Parrott, 1971).
Untuk partikel-partikel yang besar akan cenderung memisah dari
partike-partikel yang kecil, yakni partike-partikel besar cenderung ke bawah dan partike-partikel yang
kecil cenderung ke atas dalam bentuk fines. Kerapatan massa, dalam proses
pencampuran di dalam alat pencampuran dapat terjadi segregasi karena gesekan
dari partikel yang mempunyai perbedaan kerapatan massa, untuk komponen yang
kerapatan massanya besar akan turun ke bawah, sedangkan komponen yang
kerapatan massanya kecil akan tetap di atas sehingga dibutuhkan waktu
Kelengketan dan kelicinan, untuk bahan yang bersifat lengket, maka pada proses
pencampuran partikelnya akan bergerombol satu sama lain dan melekat pada
dinding mixer sehingga proses pencampuran akan lebih sukar, lain halnya bila
didapatkan bahan yang licin, bahan tersebut akan membantu dalam proses
pencampuran. Kelembaban, pengaruh kelembaban tinggi yang dominan adalah
gaya kapiler, gaya ini mengakibatkan bahan cenderung menggumpal dan melekat
pada dinding mixer, sedangkan pada kelembaban yang rendah gaya yang dominan
adalah gaya elektrostatik, gaya ini menyebabkan partikel-partikel menjadi
bermuatan, cenderung membentuk agregat dan mengalami segregasi. Lama
campuran, keefektifan waktu yang digunakan untuk proses pencampuran akan
mempengaruhi hasil pencampuran karena campuran yang sudah homogen bila
proses pencampurannya dilanjutkan maka pada waktu tertentu tidak homogen lagi
(Parrott, 1971).
2.8 Uji Preformulasi
Untuk menghasilkan tablet yang baik maka perlu diketahui sifat fisis dari
campuran bahan yang akan dicetak, pemeriksaan kualitas campuran bahan
meliputi :
2.8.1 Waktu alir
Waktu alir adalah waktu yang dibutuhkan bila sejumlah granul dituangkan
dalam suatu alat kemudian dialirkan. Mudah tidaknya aliran granul dapat
dipengaruhi oleh bentuk granul, sifat permukaan granul dan kelembabannya. Bila
granul memiliki ukuran yang tidak seragam menyebabkan daya kohesinya
waktu alir yaitu sifat-sifat granul yaitu ukuran partikel, distribusi ukuran partikel
dan kelembaban (Lachman, dkk., 1994).
2.8.2 Sudut diam
Sudut diam yaitu sudut tetap yang terjadi antara timbunan partikel bentuk
kerucut dengan bidang horisontal. Besar kecilnya sudut diam dipengaruhi oleh
bentuk, ukuran dan kelembapan granul. Granul atau serbuk kualitas farmasi
mempunyai sudut diam 20° - 40°, sudut yang lebih kecil menunjukkan sifat alir
yang baik (Lachman, dkk., 1994).
2.8.3 Indeks tap
Uji indeks tap dilakukan untuk mengamati penurunan jumlah
serbuk/granul akibat adanya gaya hentakan, juga untuk mengetahui secara tidak
langsung perilaku sifat alir sewaktu kompresi/pencetakan tablet, sifat alir
dikatakan baik apabila indeks tap kurang dari 20% (Voight, 1994).
2.9 Pemeriksaan Kualitas Tablet
Pemeriksaan kualitas tablet dilakukan untuk mengetahui mutu fisik dari
tablet yang dihasilkan, pemeriksaan kualitas tablet meliputi :
2.9.1 Kekerasan tablet
Kekerasan adalah parameter yang menggambarkan ketahanan tablet dalam
melawan tekanan mekanik seperti goncangan, kikisan dan terjadi keretakan tablet
selama pembungkusan, pengangkutan dan pemakaian. Kekerasan ini dipakai
sebagai ukuran dari tekanan pengempakan. Kekerasan tablet biasanya 4 - 8 kg,
rapuh, tapi bila kekerasan tablet lebih besar dari 8 kg akan didapatkan tablet yang
cenderung keras (Parrott, 1971).
Faktor-faktor yang mempengaruhi kekerasan tablet adalah tekanan pada
saat pentabletan, sifat bahan yang dikempa serta jumlah serta jenis bahan obat
yang ditambahkan saat pentabletan akan meningkatkan kekerasan tablet (Ansel,
1989).
2.9.2 Kerapuhan tablet
Kerapuhan adalah parameter lain dari ketahanan tablet dalam melawan
pengikisan dan goncangan, besaran yang dipakai adalah % bobot yang hilang
selama pengujian dengan alat friabilator. Faktor-faktor yang mempengaruhi
kerapuhan antara lain banyaknya kandungan serbuk (fitnes), kerapuhan di atas 1%
menunjukkan tablet yang rapuh dan dianggap kurang baik (Lachman, dkk., 1994).
2.9.3 Waktu hancur tablet
Waktu hancur tablet adalah waktu yang dibutuhkan untuk hancurnya tablet
dalam medium yang sesuai sehingga tidak ada bagian tablet yang tertinggal di atas
kasa alat pengujian. Faktor-faktor yang mempengaruhi waktu hancur adalah sifat
fisika kimia granul dan kekerasan tablet, kecuali dinyatakan lain, waktu hancur
tablet tidak bersalut tidak boleh lebih dari 15 menit (Lachman, dkk., 1994).
Waktu hancur yang semakin cepat maka akan semakin cepat pula
pelarutan dari bahan berkhasiat sehingga akan lebih cepat berkhasiat dalam tubuh
2.9.4 Keseragaman sediaan
Keseragaman sediaan dapat ditetapkan dengan dua cara, yaitu :
1. Keragaman bobot, dilakukan terhadap tablet yang 50% bahan aktifnya lebih
2. Keseragaman kandungan, dilakukan terhadap tablet yang 50% bahan aktifnya
urang dari 50 mg. (Ditjen POM, 1995)
2.9.5 Uji penetapan kadar zat berkhasiat
Uji penetapan kadar zat berkhasiat dilakukan untuk mengetahui apakah
tablet tersebut memenuhi syarat sesuai dengan etiket. Bila kadar obat tersebut
tidak memenuhi syarat maka obat tersebut tidak memiliki efek terapi yang baik
dan tidak layak di konsumsi. Uji penetapan kadar dilakukan dengan menggunakan
cara-cara yang sesuai pada masing-masing monografi antara lain di Farmakope
Indonesia (Dirjen POM RI, 1995).
2.9.6 Disolusi
Disolusi adalah proses melarutnya suatu obat (Ansel, 1989). Saat sekarang
ini disolusi dipandang sebagai salah satu uji pengawasan mutu yang paling
penting dilakukan pada sediaan farmasi. Pada uji disolusi dapat diketahui bahan
obat dalam larutan dengan kecepatan yang seharusnya. Cepatnya obat atau tablet
melarut menentukan kadar bahan berkhasiat terlepas didalam tubuh. Karena itu
laju larut berhubungan langsung dengan kemanjuran dari tablet dan perbedaan
bioavaibilitas dari berbagai formula (Lachman, dkk., 1994).
Pada tiap pengujian, volume dari media disolusi (seperti yang
dicantumkan dalam masing-masing monografi) di tempatkan dalam bejana dan
biarkan mencapai temperature 37 ± 0,5°C. Kemudian 1 tablet yang diuji
dicelupkan kedalam bejana atau ditempatkan dalam keranjang dan pengaduk
diputar dengan kecepatan seperti yang ditetapkan dalam monografi. Pada waktu-
yang terlarut. Tablet harus memenuhi persyaratan seperti yang terdapat dalam
monografi untuk kecepatan disolusi (Ansel, 1989).
2.10Spektrofotmetri
Spektrofotometri UV-Vis adalah pengukuran panjang gelombang dan
intensitas sinar ultraviolet dan cahaya tampak yang diabsorbsi oleh sampel. Sinar
ultraviolet dan cahaya tampak memiliki energi yang cukup untuk mempromosikan
elektron pada kulit terluar ke tingkat energi yang lebih tinggi (Dachriyanus,
2004).
2.10.1 Instrumen
Menurut Khopkar (1990), suatu spektrofotometer tersusun dari:
a. Sumber
Sumber yang biasa digunakan adalah lampu wolfram. Tetapi untuk daerah
UV digunakan lampu hydrogen atau lampu deuterium. Kebaikan lampu wolfram
adalah energi radiasi yang dibebaskan tidak bervariasi pada berbagai panjang
gelombang. Untuk memperoleh tegangan yang stabil dapat digunakan
transformator. Jika potensial tidak stabil, kita akan mendapatkan energi yang
bervariasi. Untuk mengompensasikan hal ini maka dilakukan pengukuran
transmitan larutan sempel selalu di sertai larutan pembanding.
b. Monokromator
Digunakan untuk memperoleh sumber sinar yang monokromatis. Alatnya
berupa prisma ataupun grating. untuk mengarahkan sinar monokromatis yang
diinginkan dari hasil penguraian dapat digunakan celah.
Pada pengukuran di daerah tampak kuvet kaca dapat digunakan, tetapi
untuk pengukuran pada daerah UV kita harus menggunakan sel kuarsa karena
gelas tidak tembus cahaya pada daerah ini. Umumnya tebal kuvetnya adalah 10
mm, tetapi yang lebih kecil ataupun yang lebih besar dapat digunakan. Sel yang
biasa digunakan berbentuk persegi, tetapi bentuk silinder dapat juga digunakan.
Kita harus menggunakan kuvet untuk pelarut organik. Sel yang baik adalah kuarsa
atau gelas hasil leburan serta seragam keseluruhannya.
d. Detektor
Peranan detektor penerima adalah memberikan respon terhadap cahaya
pada berbagai panjang gelombang. Pada spektrofotometer, tabung pengganda
elektron yang di gunakan prinsip kerjanya telah diuraikan.
2.10.2 Penggunaan
Menurut Rohman dan Ganjar (2007), metode spektrofotometri UV-Vis
digunakan untuk menetapkan kadar senyawa obat dalam jumlah yang cukup
banyak. Cara untuk menetapkan kadar sampel adalah dengan menggunakan
perbandingan absorbansi sampel dengan absorbansi baku, atau dengan
menggunakan persamaan regresi linier yang menyatakan hubungan antara
konsentrasi baku dengan absorbansinya. Persamaan kurva baku selanjutnya
digunakan untuk menghitung kadar dalam sampel.
Analisis kuantitatif dengan metode spektofotometri UV-Vis dapat digolongkan
atas tiga macam pelaksanaan pekerjaan, yaitu:
a. analisis zat tunggal atau analisis satu komponen
b. analisis kuantitatif campuran dua macam zat atau analisis dua komponen
Jika penetapan kadar atau pengujian menggunakan baku pembanding,
lakukan pengukuran spektrofotometri dengan larutan yang dibuat dari baku
pembanding menurut petunjuk resmi dan larutan yang dibuat dari zat uji. Lakukan
pengukuran kedua secepat mungkin setelah pengukuran pertama menggunakan
kuvet dari kondisi pengujian yang sama. Kuvet atau sel yang dimaksudkan untuk
diisi larutan uji dan cairan pelarut, bila diisi dengan pelarut yang sama, harus