ix
ABSTRAK
PENGARUH LAJU ALIR DAN TEKANAN TERHADAP WAKTU
RETENSI PADA HPLC
HPLC (High Pressure Liquid Chromatography) merupakan suatu teknik kromatografi yang digunakan untuk memisahkan komponen tertentu dalam suatu campuran. Proses Pemisahan pada HPLC merupakan hasil dari interaksi molekul – molekul sampel dengan fase diam. Molekul – molekul yang terpisah dapat diidentifikasi berdasarkan waktu retensinya.
x
ABSTRACT
THE INFLUENCE OF FLOW RATE ANDPRESSURE FOR RETENTION
TIME IN HPLC
HPLC (High Pressure Liquid Chromatography) is a chromatographic technique that can separate a mixture of compounds. Chromatographic separation in HPLC is the result of specific interactions between sample molecules with the stationary phase. Molecules that have been separated can be identified by their retention time.
RETENSI PADA HPLC
Skripsi
Diajukan Untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Sains
Jurusan Fisika
Oleh:
Maria Fransiska Putriyani NIM : 073214002
PROGRAM STUDI FISIKA JURUSAN FISIKA
FAKULTAS SAINS DAN TEKNOLOGI UNIVERSITAS SANATA DHARMA
ii
TIMEIN HPLC
A THESIS
Presented as Partial Fulfillment of the Requirement to Obtain the Sarjana Science
in Physics Department
by:
Maria Fransiska Putriyani NIM : 073214002
PHYSICS STUDY PROGRAM PHYSICS DEPARTMENT
FACULTY OF SCIENCE DAN TECHNOLOGY SANATA DHARMA UNIVERSITY
v
P esi m i st i s t a k l ebi h d a r i si k a p t a k a bu r m en d a h u l u i
n a si b.P a d a h a l k i t a t a k k a n p er n a h m en d a h u l u i n a si b.
(A n d r ea H i r a t a – Sa n g P em i m p i )
Ev er y t h i n g i s si m p l er t h a n ca n be i m a gi n ed ,
y et m or e i n t r i ca t e t h a n ca n be com p r eh en d ed .
vi
Sa y a p er sem ba h k a n k a r y a i n i k ep a d a :
P a p a & M a m a k u t er ci n t a d a n
ix
ABSTRAK
PENGARUH LAJU ALIR DAN TEKANAN TERHADAP WAKTU
RETENSI PADA HPLC
HPLC (High Pressure Liquid Chromatography) merupakan suatu teknik kromatografi yang digunakan untuk memisahkan komponen tertentu dalam suatu campuran. Proses Pemisahan pada HPLC merupakan hasil dari interaksi molekul – molekul sampel dengan fase diam. Molekul – molekul yang terpisah dapat diidentifikasi berdasarkan waktu retensinya.
x
ABSTRACT
THE INFLUENCE OF FLOW RATE ANDPRESSURE FOR RETENTION
TIME IN HPLC
HPLC (High Pressure Liquid Chromatography) is a chromatographic technique that can separate a mixture of compounds. Chromatographic separation in HPLC is the result of specific interactions between sample molecules with the stationary phase. Molecules that have been separated can be identified by their retention time.
xiii
DAFTAR ISI
Halaman
HALAMAN JUDUL ……… i
HALAMAN PERSETUJUAN PEMBIMBING ………iii
HALAMAN PENGESAHAN ………...iv
HALAMAN MOTTO ……… v
HALAMAN PERSEMBAHAN ………... vi
HALAMAN PERNYATAAN KEASLIAN KARYA ………. vii
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ……… viii
ABSTRAK ……… ix
ABSTRACT ……….. x
KATA PENGANTAR ……….. xi
DAFTAR ISI ………...xiii
DAFTAR TABEL ………....xvi
xiv
BAB I PENDAHULUAN ………...1
A. Latar Belakang ………....1
B. Rumusan Masalah ……….. 4
C. Batasan Masalah ……….4
D. Tujuan Penelitian ………4
E. Manfaat Penelitian ………. 4
F. Sistematika Penulisan ……….5
BAB II DASAR TEORI ……….6
A. Pengukuran ……….6
B. High Pressure Liquid Chromatography (HPLC) ………8
BAB III EKSPERIMEN ………...15
A. Tempat Penelitian ……….15
B. Alat dan Bahan ………. 15
1. Alat – alat ………15
2. Bahan ………..17
C. Metode Eksperimen ………..18
1. Penyiapan fase gerak ………...18
2. Penyiapan sampel ………18
xv
4. Pengukuran waktu retensimolekulParasetamol dan Kafein dalam kondisi laju alir yang bervariasi pada tekanan tertentu dan tekanan
yang bervariasi pada laju alir tertentu………..20
BAB IV HASIL DAN PEMBAHASAN ………..21
A. Hasil ………. 21
1. Penyiapan fase gerak ……….. 23
2. Penyiapan sampel ………23
3. Penentuan waktu retensi dari masing – masing molekul……….24
4. Pengukuran waktu retensimolekulParasetamol dan Kafein dalam kondisi laju alir yang bervariasi pada tekanan tertentu dan tekanan yang bervariasi pada laju alir tertentu………...27
B. Pembahasan ……….. 34
BAB V KESIMPULAN DAN SARAN……… 46
A. Kesimpulan ………...46
B. Saran ………. 46
DAFTAR PUSTAKA ………...47
xvi
DAFTAR TABEL
Halaman Tabel 4.1 :Nilai waktu retensi Parasetamol dan Kafein untuk laju alir yang
bervariasi pada tekanan sebesar 100 bar………..30 Tabel 4.2 : Nilai waktu retensi Parasetamol dan Kafein untuk tekanan yang
bervariasi pada laju alir sebesar 1,45 ml/min………...31 Tabel 4.3 : Tabel hubungan nilai waktu retensi (menit) Parasetamol terhadap laju
alir fase gerak (ml/min) dan tekanan (bar)………...41 Tabel 4.4 : Tabel hubungan nilai waktu retensi (menit) Kafein terhadap laju alir
xvii
DAFTAR GAMBAR
Halaman
Gambar 2.1. Skema HPLC………...……….9
Gambar 2.2. Proses pemisahan pada kolom………...10 Gambar 2.3. Grafik pemisahan ………..11 Gambar 3.1. Skema rangkaian alat yang digunakan dalam eksperimen……….17 Gambar 4.1. Grafik waktu retensi Parasetamol………..26 Gambar 4.2. Grafik waktu retensi Kafein………...26 Gambar 4.3. Grafik pemisahan Parasetamol dan Kafein pada laju alir
1 ml/min dan tekanan 100 bar………28 Gambar 4.4. Grafik pemisahan Parasetamol dan Kafein pada laju alir
1,9 ml/min dan tekanan100 bar………..29 Gambar 4.5. Grafik hubungan antara tRdan 1 / v pada tekanan 100 bar………32
Gambar 4.6. Grafik hubungan antara tRdan P pada laju alir 1,45 ml/min…….33
Gambar 4.7. Grafik hubungan waktu retensi (menit) terhadap laju alir fase gerak (ml/min) dan tekanan (bar) untuk pengukuran Parasetamol pada panjang gelombang 263 nm dengan menggunakan kolom C-18 yang berukuran panjang 100mm diameter 4,6mm………43 Gambar 4.8. Grafik hubungan waktu retensi (menit) terhadap laju alir fase gerak
1
BAB I
PENDAHULUAN
A. Latar Belakang
Dewasa ini teknologi semakin berkembang pesat. Seiring dengan perkembangannya, teknik – teknik yang digunakan dalam suatu penelitian juga mengalami perubahan pesat. Dalam suatu penelitian, seseorang harus memiliki pemahaman yang mendalam tentang prinsip – prinsip dan variabel - variabel fisika pada instrumen yang digunakan. Karena prinsip – prinsip dan variabel – variabel tersebut akan mempengaruhi hasil eksperimen. Sehingga untuk dapat melaksanakan suatu eksperimen dengan berhasil diperlukan pengetahuan tentang berbagai prinsip pengukuran dan instrumentasi [Holman dan Jasjfi, 1984].
Dalam suatu pengukuran ada dua buah hal yang penting yaitu input dan output. Input dibedakan menjadi tiga bagian yang meliputi input yang diinginkan, input pengubah dan input pengganggu, sedangkan output dibedakan menjadi output pengganggu dan output yang diinginkan [Doebelin, 2004]. Nilai input akan berpengaruh terhadap hasil keluaran outputnya.
Dalam suatu pengukuran dibutuhkan suatu instrumen atau alat ukur. Masing - masing instrumen memiliki karakteristik tersendiri. Oleh karena itu dalam suatu pengukuran, instrumen akan diperlakukan sedemikan rupa sehingga dapat menghasilkan pengukuran yang akurat.
Instrumen yang digunakan dalam suatu pengukuran harus memenuhi persyaratan tertentu. Persyaratan tersebut adalah: sensitif, selektif, tidak mengganggu sampel yang diukur dan memiliki waktu tanggap cepat. Sensitif menunjukkan bahwa instrumen tersebut mampu mengukur input yang ada. Selektif menunjukkan bahwa instrumen tersebut mampu membedakan antara input yang satu dengan yang lain. Sedangkan tidak mengganggu sampel yang diukur berarti bahwa pengukuran yang dilakukan tidak merubah sampel dan waktu tanggap yang cepat berarti bahwa pengukuran langsung terjadi saat instrumen bersentuhan dengan sampel.
unsur logam sedangkan HPLC digunakan untuk mengidentifikasi zat – zat secara luas serta zat – zat yang tidak mudah menguap. Jangkauan pengidentifikasian HPLC lebih luas dibandingkan dengan GC, karena GC hanya untuk zat – zat yang mudah menguap. Sehingga dalam penelitian ini dipilih HPLC sebagai alat ukur yang digunakan.
HPLC merupakan kepanjangan dari High Pressure Liquid Chromatography.HPLC merupakan salah satu metode kromatografi cair yang fase geraknya dialirkan dengan cepat menggunakan bantuan tekanan dan hasilnya dideteksi oleh detektor [Willard, et. al., 1988]. Kromatografi merupakan teknik pemisahan, jadi HPLC berfungsi untuk memisahkan komponen – komponen tertentu yang terdapat dalam suatu campuran. Hasil dari pemisahan yang terjadi ditunjukkan berupa grafik puncak – puncak. Puncak – puncak tersebut menunjukkan molekul – molekul yang telah berhasil terpisah.
Suatu proses pemisahan dikatakan baik jika waktu analisis yang dibutuhkan singkat serta daya pisahnya tinggi [Gritter, et. al., 1991]. Agar mendapatkan kondisi yang sensitif dan selektif dalam pemisahan maka faktor -faktor yang mempengaruhi pemisahan diteliti satu per satu. Contoh beberapa faktor yang mempengaruhi pemisahan yaitu laju alir fase gerak, tekanan, jenis fase gerak, parameter kolom, dll.
B. Rumusan Masalah
Berdasarkan latar belakang yang telah dipaparkan di atas, pokok permasalahan yang diangkat dalam skripsi ini dapat dirumuskan sebagai berikut :
1. Bagaimana cara kerja HPLC dalam memisahkan molekul – molekul tertentu.
2. Bagaimana hubungan antara laju alir fase gerak dan tekanan terhadap waktu retensi pada pemisahan molekul – molekul tertentu dalam suatu campuran.
C. Batasan Masalah
1. Pemisahan molekul Parasetamol dan Kafeindengan fase gerak Methanol menggunakan HPLC yang terdapat di Laboratorium Analisa Kimia Fisika Pusat, Universitas Sanata Dharma.
D. Tujuan Penelitian
1. Dapat memahami cara kerja HPLC dalam memisahkan molekul – molekul. 2. Mendapatkan hubungan antara laju alir, tekanan dan waktu retensi dalam
proses pemisahan menggunakan HPLC untuk mendapatkan hasil pemisahan yang baik.
E. Manfaat Penelitian
2. Memberikan informasi tentang hubungan laju alir,tekanan dan waktu retensi dalam proses pemisahan menggunakan HPLC.
F. Sistematika Penulisan
Penelitian ini akan dituliskan dengan sistematika sebagai berikut :
BAB I Pendahuluan
Bab ini berisi uraian tentang latar belakang masalah, rumusan masalah, batasan masalah, tujuan penelitian, manfaat penelitian, dan sistematika penulisan.
BAB II Dasar Teori
Bab ini berisi uraian tentang teori kromatografi, serta teori yang terkait dengan prinsip kerja HPLC secara keseluruhan yang berguna dalam penelitian yang dilakukan.
BAB III Eksperimen
Bab ini berisi uraian tentang tempat pelaksanaan penelitian, alat dan bahan yang digunakan dalam penelitian, dan prosedur penelitian.
BAB IV Hasil dan Pembahasan
Bab ini berisi uraian tentang hasil dan pembahasan dari penelitian yang telah dilakukan.
Bab V Penutup
6
BAB II
DASAR TEORI
A. Pengukuran
Pengukuran merupakan suatu kegiatan yang sering dilakukan sehari – hari.Pengukuran dilakukan untuk memberikan informasi dari suatu hal yang diukur dengan menggunakan sejumlah angka [Rangan, et. al., 1985].Angka tersebut menunjukkan nilai dari sesuatu yang diukur. Proses suatu pengukuran dapat dibedakan menjadi tiga bagian, yaitu memonitoring, mengkontrol, dan menganalisis [Doebelin, 2004]. Memonitoring meliputi mencatat atau merekam data, mengkontrol meliputi mengatur beberapa variabel yang berhubungan dengan pengukuran yang dilakukan, menganalisis meliputi menganalisa data yang telah didapatkan.
Dalam suatu pengukuran terdapat dua hal yang penting, yaitu input dan output. Input dibedakan menjadi tiga bagian, yaitu input yang diinginkan, input pengubah, dan input pengganggu [Doebelin, 2004]. Input yang diinginkan merupakan masukan yang ingin diukur. Input pengubah merupakan masukan yang bisa menyebabkan perubahan dalam hubungan antara input dan output. Sedangkan input pengganggu merupakan masukan yang dapat mengganggu pengukuran.
karena itu dalam pengukuran setiap instrumen memiliki perlakuan yang berbeda – beda. Salah satu hal yang dapat menyebabkan pengukuran menjadi tidak akurat adalah kurangnya sensitivitas suatu instrumen. Sehingga untuk menghindari terjadinya pengukuran yang tidak akurat, ada beberapa persyaratan tentang instrumen yang akan digunakan. Instrumen yang akan digunakan sebaiknya memiliki persyaratan: sensitif, selektif, tidak mengganggu sampel yang diukur, dan waktu tanggap cepat.
Suatu pengukuran dikatakan ideal bila tidak mengubah kondisi sampel yang diukur. Pengubahan kondisi sampel akan menyebabkan perubahan nilai besaran yang diukur dari nilai sebenarnya. Munculnya gangguan pada instrumen dan masukan yang mengganggu saat pengukuran, dapat membuat hasil pengukuran tidak akurat dan mengakibatkan timbulnya kesalahan. Untuk menghindari hal tersebut, gangguan harus dieliminasi [Doebelin,2004].
Kesalahan yang terjadi dalam pengukuran bisa dibedakan menjadi dua, yaitu kesalahan sistematik dan kesalahan acak [Morris, 1996]. Kesalahan sistematik merupakan kesalahan yang terjadi secara tetap pada bagian yang sama, misalnya selalu menghasilkan nilai kesalahan yang sama. Kesalahan ini terjadi biasanya disebabkan oleh perubahan karakteristik instrumen. Sedangkan kesalahan acak merupakan kesalahan yang terjadi secara acak tidak menentu. Kesalahan ini biasanya terjadi karena adanya gangguan yang berasal dari luar.
merupakan suatu cara untuk mendapatkan hubungan antara input dan output dengan cara memvariasikan input yang akan diukur sedangkan input yang lain dibuat tetap. Instrumen juga berperan penting dalam usaha mendapatkan pengukuran yang akurat. Syarat suatu instrumen yang baik yaitu: sensitif, selektif, tidak mengganggu sampel yang diukur dan memiliki waktu tanggap cepat. Selektif berarti instrumen tersebut mampu mengidentifikasikan antara komponen yang satu dengan yang lain. Salah satu alat yang memiliki kriteria tersebut adalah HPLC.
B. High Pressure Liquid Chromatography (HPLC)
HPLC merupakan salah satu metode kromatografi cair yang fase geraknya dialirkan dengan cepat menggunakan bantuan tekanan dan hasilnya dideteksi oleh detektor [Willard, et. al., 1988]. Secara umum HPLC digunakan untuk mencari besar konsentrasisuatu zat di dalam sampel. Disebut sebagai High Pressure Liquid Chromatography karena pada HPLC digunakan tekanan tinggi untuk memaksimalkan pemisahan antar molekul.
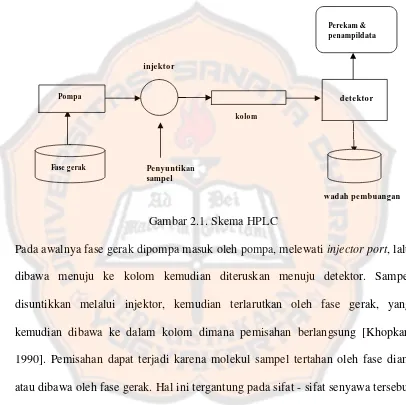
HPLC bekerja sebagai sebuah sistem yang terdiri dari beberapa komponen.Komponen – komponen dari HPLC ditunjukkan pada gambar (2.1), yang terdiri dari wadah fase gerak, pompa, tempat memasukkan sampel (injector
port), kolom, detektor, perekam dan penampil data.
Gambar 2.1. Skema HPLC
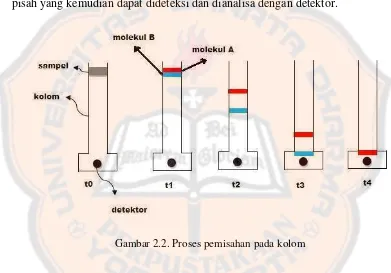
Contoh proses terjadinya pemisahan ditunjukkan pada gambar (2.2), misalnya ada molekul A dan B yang terdapat dalam suatu sampel, sampel tersebut dimasukkan ke dalam sistem. Kedua senyawa tersebut akan terdistribusi di antara fase gerak dan diamnya menurut sifat masing – masing. Komponen yang tertahan kuat akan berjalan lambat, sebaliknya yang tertahan lemah akan berjalan cepat. Karena perbedaan mobilitas inilah komponen – komponen sampel akan terpisah – pisah yang kemudian dapat dideteksi dan dianalisa dengan detektor.
Gambar 2.2. Proses pemisahan pada kolom
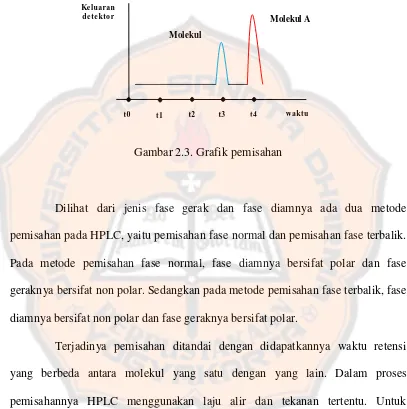
dengan dua puncak yang ditunjukkan oleh gambar (2.3). Masing – masing puncak mewakili molekul tertentu.
Gambar 2.3. Grafik pemisahan
Dilihat dari jenis fase gerak dan fase diamnya ada dua metode pemisahan pada HPLC, yaitu pemisahan fase normal dan pemisahan fase terbalik. Pada metode pemisahan fase normal, fase diamnya bersifat polar dan fase geraknya bersifat non polar. Sedangkan pada metode pemisahan fase terbalik, fase diamnya bersifat non polar dan fase geraknya bersifat polar.
Terjadinya pemisahan ditandai dengan didapatkannya waktu retensi yang berbeda antara molekul yang satu dengan yang lain. Dalam proses pemisahannya HPLC menggunakan laju alir dan tekanan tertentu. Untuk penelitian analitis pada HPLC, laju alirfase gerak yang digunakan berkisar antara 0.5 – 5 ml/min [Johnson dan Stevenson, 1991].Semakin rendah laju alirnya maka kemampuan untuk memisahkan komponen – komponen akan semakin tinggi serta menghemat penggunaan fase gerak dan waktu yang dibutuhkan untuk analisis
akan semakin lama. Besar waktu retensi suatu molekul dipengaruhi oleh laju alir fase gerak, tekanan, parameter kolom serta sifat – sifat molekul itu sendiri.
Kolom pada HPLC tersusun atas bagian - bagian penyusun kolom. Ketika ada suatu molekul tertentu yang melewati kolom maka terjadi interaksi antara molekul yang lewat dengan bagian – bagian penyusun kolom. Interaksi yang terjadi dipengaruhi oleh jenis kolom dan molekul yang lewat. Jika jenis kolomnya tetap maka besar waktu retensi bergantung pada molekul yang lewat.
Besar waktu retensi satu jenis molekul yang melewati kolom pada suatu tekanan tertentu ditunjukkan oleh persamaan (2.1) di bawah ini [Willard, et. al., 1988].
Dengan v = kecepatan linear fase gerak (ml/min) dc = diameter kolom bagian dalam (µm) ε = faktor porositas kolom
L = panjang kolom (mm)
tR =waktu yang diperlukan oleh molekul untuk melewati kolom
(min)
Waktu retensi (tR) berbanding lurus terhadap volum kolom (Vcol) serta
faktor porositas kolom (ε) dan berbanding terbalik terhadap kecepatan fase gerak (v). Kecepatan fase gerak (v) pada persamaan (2.1) dapat disebut juga sebagai jumlah volume fase gerak per satuan waktu.Besar volum kolom bergantung pada ukuran kolom.Besar faktor porositas kolom bergantung pada jenis kolom [Willard, et. al., 1988]. Laju alir berpengaruh terhadap waktu retensi, untuk laju alir yang tinggi akan didapatkan waktu retensi yang singkat sedangkan untuk laju alir yang rendah akan didapatkan waktu retensi yang lama.
Dalam proses kerja sistem HPLC digunakan tekanan. Tekanan pada sistem HPLC dihasilkan oleh pompa.Penurunan tekanan yang terjadi pada kolom pada suatu laju alir tertentu ditunjukkan oleh persamaan (2.2) [Kuwana, 1980].
Dengan ΔP = penurunan tekanan pada kolom (bar) Ø = faktor resistan kolom
η = viskositas fase gerak (mbar s)
L = panjang kolom (mm)
v = laju alir fase gerak (mm/min)
dp = diameter bagian - bagianpenyusun kolom (µm)
Penurunan tekanan (ΔP) berbanding lurus terhadap faktor resistan kolom
15
BAB III
EKSPERIMEN
A. Tempat Penelitian
Penelitian ini dilaksanakan di Laboratorium Analisa Kimia Fisika Pusat, Kampus III Universitas Sanata Dharma, Paingan Maguwoharjo Depok Sleman Yogyakarta.
B. Alat dan Bahan
1. Alat – alat:
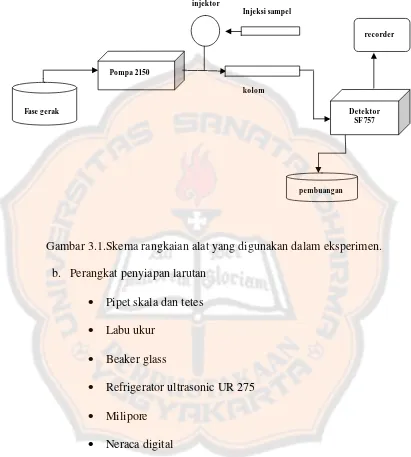
a. Satu unit HPLC, yang terdiri dari: Pompa HPLC
Pompa yang digunakan adalah pompa LKB – BROMA tipe 2150. Pompa ini memiliki 2 buah kepala pompa. Fase gerak selalu bergerak melalui kedua kepala pompa dalam satu arah. Pompa ini bertugas memberikan tekanan sehingga mendorong fase gerak masuk ke dalam kolom. Tekanan tertinggi yang bisa diberikan oleh pompa ini adalah 400 bar.
Injektor
akanbergerak masuk ke dalam kolom ketika tuas berada pada posisi INJECT. Injektor ini mampu menampung sampel sebanyak 20μl.
Kolom
Kolom yang digunakan adalah kolom CPTM sphere C-18 (Oktadesil Silica) dengan panjang 100 mm dan diameter sebesar 4,6 mm.
Detektor
Detektor yang digunakan adalah detektor Spectroflow 757. Detektor ini berfungsi untuk mendeteksi molekul – molekul yang telah terpisah. Prinsip kerja detektor ini berdasarkan prinsip serapan cahaya. Detektor ini mengubah besaran cahaya menjadi besaran listrik,memiliki sumber lampu deuterium (190 nm – 380 nm) dan tungsten (380 nm – 800 nm).
Perekam dan penampil data
Untuk merekam dan menampilkan data digunakan recorder BD Kipp zonen.
Gambar 3.1.Skema rangkaian alat yang digunakan dalam eksperimen. b. Perangkat penyiapan larutan
Pipet skala dan tetes
Labu ukur Beaker glass
Refrigerator ultrasonic UR 275
Milipore Neraca digital
2. Bahan – bahan :
a. Methanol
Methanol berfungsi sebagai fase gerak dan pelarut.
b. Sampel
Sampel yang digunakan adalah campuran larutanParasetamol dan Kafein.
C. Metode Eksperimen
1. Penyiapan fase gerak
Fase gerak yang digunakan adalah methanol. Sebelum fase gerak dimasukkan ke dalam wadah yang akan digunakan, maka terlebih dahulu wadah tersebut dibilas dengan methanol. Untuk menghindari adanya partikel – partikel asing maka methanol disaring dengan menggunakan milipore yang berukuran 0,45 µm. Setelah itu, untuk menghilangkan gelembung – gelembung udara maka dilakukan degassing pada methanol menggunakan refrigerator ultrasonic UR 275.
2. Penyiapan sampel
Dengan C1 = kadar larutan induk (ppm)
V1 = volume larutan induk yang diambil (ml)
C2 = kadar yang diinginkan (ppm)
V2 = volume larutan yang diinginkan (ml)
Untuk menghindari adanya partikel – partikel asing maka larutan Parasetamol dan Kafein tersebut disaring dengan menggunakan milipore yang berukuran 0,45 µm.
3. Penentuan waktu retensi dari masing – masing molekul
Suatu campuran dikatakan terpisah jika molekul - molekul penyusun campuran tersebut memiliki waktu retensi yang berbeda. Waktu retensi dari Parasetamol dan Kafein harus diketahui terlebih dahulu. Sebab, waktu retensi akan menunjukkan identitas suatu molekul pada saat pemisahan.
4. Pengukuran waktu retensi Parasetamol dan Kafein dalam kondisi laju
alir yang bervariasi pada tekanan tertentu dan tekanan yang bervariasi
pada laju alir tertentu.
Sampel yang digunakan adalah campuran larutan Parasetamol dan Kafein. Hasil data yang akan didapatkan adalah nilai waktu retensi Parasetamol dan Kafein dalam kondisi laju alir bervariasi pada tekanan tertentu dan tekanan bervariasi pada laju alir tertentu.
Pengukuran waktu retensi Parasetamol dan Kafein dalam kondisi laju alir bervariasi pada tekanan tertentu, dilakukan dengan laju alir fase gerak 0,55 ml/min; 0,7 ml/min; 0,85 ml/min; 1 ml/min; 1,15 ml/min; 1,3 ml/min; 1,45 ml/min; 1,6 ml/min; 1,75 ml/min; dan 1,9 ml/min pada tekanan 100 bar. Selanjutnya dilakukan hal yang sama untuk tekanan 125 bar, 150 bar, 175 bar, 200 bar, 225 bar, dan 250 bar.
Pengukuran waktu retensi Parasetamol dan Kafein dalam kondisi tekanan bervariasi pada laju alir tertentu, dilakukan dengan tekanan 100 bar, 125 bar, 150 bar, 175 bar, 200 bar, 225 bar, dan 250 bar pada laju alir 0,55 ml/min. Selanjutnya dilakukan hal yang sama untuk laju alir 0,7 ml/min; 0,85 ml/min; 1 ml/min; 1,15 ml/min; 1,3 ml/min; 1,45 ml/min; 1,6 ml/min; 1,75 ml/min; dan 1,9 ml/min.
21
BAB IV
HASIL DAN PEMBAHASAN
A. Hasil
HPLC (High Pressure Liquid Chromatography) merupakan alat yang bekerja berdasarkan prinsip kromatografi yang berguna untuk memisahkan komponen –komponen zat yang terdapat di dalam suatu campuran. Salah satu tujuan dari penelitian ini adalah untuk memahami cara kerja HPLC dalam memisahkan molekul – molekul.Terjadinya suatu pemisahan ditandai dengan didapatkannya nilai waktu retensi yang berbeda. Proses pemisahan molekul – molekul menggunakan HPLC dipengaruhi oleh banyak faktor. Sehingga dalam penelitian ini dilakukan percobaan mencari pengaruh laju alir dantekananterhadap waktu retensi.
kemudian bergerak bersama menuju kolom. Pada kolom terjadi pemisahan antar molekul, setelah terpisah molekul – molekul tersebut akan masuk ke dalam detektor satu per satu. Detektor akan mendeteksi molekul – molekul tersebut satu per satu. Setelah terdeteksi molekul tersebut dengan sendirinya akan keluar menuju pembuangan. Prinsip kerja dari detektor yang digunakan adalah serapan cahaya oleh molekul penyerap yaitu sampel. Sehingga proses pendeteksian dilakukan pada satu nilai panjang gelombang analisis. Panjang gelombang analisis merupakan panjang gelombang dimana kedua zat mengalami serapan yang baik. Data yang dikeluarkan oleh detektor berupa nilai tegangan. Besarnya nilai tegangan, menunjukkan besarnya nilai absorbansi.Mekanisme proses pemisahan ini ditunjukkan pada gambar (2.2).
Dalam penelitian ini dilakukan pengukuran waktu retensi dari Parasetamol dan Kafein dalamkondisi laju alir yang bervariasi pada tekanan tertentu dan tekanan yang bervariasi pada laju alirtertentu. Ada beberapa set pada alat yang dibuat bervariasi, namun ada juga yang dibuat tetap. Set pada alat yang dibuat tetap adalah:
a. Pompa LKB-Broma 2150
Lower limit pressure : 000 bar
b. Detektor Spectroflow 757
Panjang gelombang analisis : 263 nm
Filter rise time : 1 s
Langkah kerja yang telah dilakukan pada penelitian:
1. Penyiapan fase gerak
Fase gerak yang digunakan adalah methanol pro analis, yaitu methanol yang sudah dibersihkan dari pengotor – pengotor. Walaupun demikian, untuk memastikan methanol yang digunakan benar – benar bersih maka sebelum dialirkan masuk ke dalam pompa, terlebih dahulu methanol tetap harus disaring dengan menggunakan milipore yang berukuran 0.45 µm.Milipore merupakan penyaring yang terbuat dari sejenis kertas khusus yang memiliki pori –pori berukuran tertentu. Hal ini dilakukan untuk menghindari terjadinya penyumbatan pada saluran – saluran pompa dan kolom, karena jika terjadi penyumbatan akan mengganggu proses pemisahan yang terjadi.
Setelah dilakukan penyaringan, makaselanjutnya dilakukan degassing
selama 15 menit menggunakan refrigerator ultrasonic UR275.
Degassingmerupakan proses penghilangan gelembung – gelembung udara. Adanya gelembung udara akan menyebabkan timbulnya ruang – ruang kosong pada larutan. Sehingga gelembung udara harus dihilangkan karena dapat mengganggu proses pemisahan dan pendeteksian.
2. Penyiapan sampel
menjadi larutan standar Parasetamol dan Kafein sesuai dengan konsentrasi yang diinginkan, pengenceran dihitung dengan menggunakan persamaan (3.1).
Sampel yang digunakan dalam penelitian ini merupakan campuran antara larutan Parasetamol danKafein. Sampel yang akan disuntikkan ke dalam HPLC harus dipastikan bebas dari kotoran. Oleh karena itu sebelum diinjeksikan, dilakukan penyaringan terlebih dahulu dengan menggunakan milipore yang berukuran 0,45 µm. Hal ini bertujuan untuk menghindari penyumbatan pada saluran – saluran dalam pompa dan kolom.
3. Penentuan waktu retensi dari masing – masing molekul
Waktu retensi adalah selang waktu yang diperlukan molekul mulai pada saat injeksi sampai terdeteksi oleh detektor. Sehingga dapat dikatakan bahwawaktu retensi merupakan waktu lamanya sampel berada di dalam kolom.
Waktu retensi merupakan hal yang penting dalam kromatografi, karena waktu retensi menunjukkan identitas suatu molekul. Jika dua buah molekul memiliki waktu retensi yang berbeda berarti molekul – molekul tersebut telah mengalami pemisahan.Molekul yang akan dipisahkan dengan menggunakan HPLCadalah molekul Parasetamoldan Kafein. Sehingga sebelum melakukan proses pemisahan, waktu retensi dari Parasetamol dan Kafein perlu diketahui terlebih dahulu.
Parasetamol diinjeksikan ke dalam sistem HPLC, bersamaan dengan itu recorder dijalankan.Parasetamol kemudian bergerak memasuki kolom.Pada saat berada di kolom, Parasetamolakan berinteraksi dengan bagian – bagian penyusun kolom. Parasetamol terus bergerak hingga akhirnya keluar dari kolom.Setelah itu, Parasetamol terdeteksi oleh detektor.Saat Parasetamol belum terdeteksi oleh detektor, recorder hanya memunculkan garis lurus.Ketika Parasetamol terdeteksi oleh detektor, grafik pada recorder membentuk sebuah puncak.Puncak tersebut menunjukkan molekul Parasetamol yang telah terdeteksi.Proses ini juga berlaku untuk Kafein. Besar waktu retensi dihitung dengan menggunakan stopwatch. Stopwatch dijalankan saat larutan diinjeksikan ke dalam injektor dan dihentikan saat larutan terdeteksi oleh detektor yang ditandai dengan timbulnya puncak pada grafik
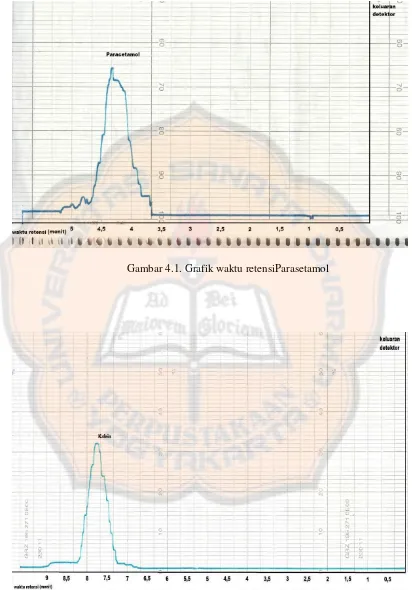
Gambar 4.1. Grafik waktu retensiParasetamol
Dari gambar (4.1) dan (4.2)terlihat bahwaParasetamol memiliki waktu retensi yang lebih singkat dibandingkan dengan Kafein. Waktu retensi Parasetamol adalah 4,38 menit sedangkan Kafein adalah 7,71 menit. Berdasarkan hal tersebut dapat diketahui bahwa dalam pemisahan antara molekul Parasetamoldan Kafein, Parasetamolakan terdeteksi terlebih dahulu.
4. Pengukuran waktu retensi molekul Parasetamol dan Kafein dalam
kondisi laju alir yang bervariasi pada tekanan tertentu dan tekanan yang
bervariasi pada laju alir tertentu.
Pengukuran waktu retensi Parasetamol dan Kafein dalam kondisi laju alir bervariasi pada tekanan tertentu, dilakukan dengan laju alir fase gerak 0,55 ml/min; 0,7 ml/min; 0,85 ml/min; 1 ml/min; 1,15 ml/min; 1,3 ml/min; 1,45 ml/min; 1,6 ml/min; 1,75 ml/min; dan 1,9 ml/min pada tekanan 100 bar. Selanjutnya dilakukan hal yang sama untuk tekanan 125 bar, 150 bar, 175 bar, 200 bar, 225 bar, dan 250 bar.
Pengukuran waktu retensi Parasetamol dan Kafein dalam kondisi tekanan bervariasi pada laju alir tertentu, dilakukan dengan tekanan 100 bar, 125 bar, 150 bar, 175 bar, 200 bar, 225 bar, dan 250 bar pada laju alir 0,55 ml/min. Selanjutnya dilakukan hal yang sama untuk laju alir 0,7 ml/min; 0,85 ml/min; 1 ml/min; 1,15 ml/min; 1,3 ml/min; 1,45 ml/min; 1,6 ml/min; 1,75 ml/min; dan 1,9 ml/min.
HPLC.Sampel bergerak memasuki kolom.Pada saat berada di dalam kolom, sampel berinteraksi dengan bagian – bagian penyusun kolom.Sampel terus berjalan hingga akhirnya terdeteksi oleh detektor.Grafik yang dihasilkan pada recorder menunjukkan dua buah puncak.Masing – masing puncak menunjukkan nilai waktu retensi yang berbeda.Waktu retensi yang berbeda menunjukkan bahwa sampel mengalami pemisahan menjadiParasetamol dan Kafein.Hasil yang didapatkan dalam eksperimen ini adalah nilai waktu retensi dari Parasetamol dan Kafein.Parasetamol dan Kafein dapat diidentifikasi dengan melihat nilai waktu retensi yang didapatkan.
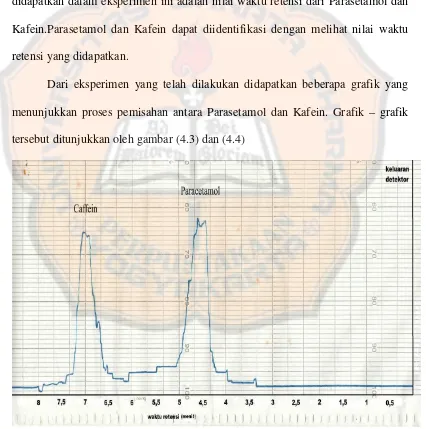
Dari eksperimen yang telah dilakukan didapatkan beberapa grafik yang menunjukkan proses pemisahan antara Parasetamol dan Kafein. Grafik – grafik tersebut ditunjukkan oleh gambar (4.3) dan (4.4)
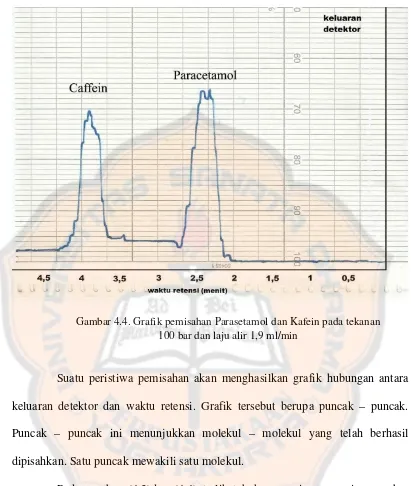
Gambar 4.4. Grafik pemisahan Parasetamol dan Kafein pada tekanan 100 bar dan laju alir 1,9 ml/min
Suatu peristiwa pemisahan akan menghasilkan grafik hubungan antara keluaran detektor dan waktu retensi. Grafik tersebut berupa puncak – puncak. Puncak – puncak ini menunjukkan molekul – molekul yang telah berhasil dipisahkan. Satu puncak mewakili satu molekul.
gambar (4.3)dan (4.4) berbeda satu sama lain karena memakai laju alir yang berbeda.
Hasil nilai waktu retensi dari Parasetamol dan Kafein dalam kondisi laju alir bervariasi pada tekanan sebesar 100 bar ditunjukkan pada tabel (4.1). Untuk data nilai waktu retensi Parasetamol dan Kafein dalam kondisi laju alir bervariasi pada tekanan sebesar 125 bar, 150 bar, 175 bar, 200 bar, 225 bar dan 250 bar dapat dilihat pada lampiran A.
Tabel 4.1 : Tabel nilai waktu retensi Parasetamol dan Kafein untuk laju alir yang
bervariasipada tekanan sebesar 100 bar.
Laju alir (ml/min) tRParasetamol (menit) tRKafein (menit)
0,55 5,36 7,46
Hasil nilai waktu retensi dariParasetamol dan Kafein dalam kondisi tekanan bervariasi pada laju alir sebesar 1,45ml/min ditunjukkan pada tabel (4.2). Untuk data nilai waktu retensi Parasetamol dan Kafein dalam kondisi tekanan bervariasi pada laju alir sebesar 0,55 ml/min; 0,7 ml/min; 0,85 ml/min;1 ml/min; 1,15 ml/min;1,3 ml/min; 1,6 ml/min; 1,75 ml/min dan 1,9 ml/min terdapat pada lampiran B.
Tabel 4.2 : Tabel nilai waktu retensi Parasetamol dan Kafein untuk tekanan yang
bervariasi pada laju alir sebesar 1,45 ml/min.
Tekanan (P) bar tRParasetamol (menit) tRKafein (menit)
100 3,01 4,45
Berdasarkan tabel (4.2) di atas terlihat bahwa tekanan mempengaruhi waktu retensi. Semakin tinggitekanannya maka waktu retensinya semakin singkat.Perbedaan waktu retensi antara tekanan yang satu dengan tekanan yang lain pada laju alir yang sama untuk tiap molekul sangat kecil.
Gambar 4.5. Grafik hubungan antara tRdan 1 / v pada tekanan sebesar 100 bar
Berdasarkan tabel data (4.2) maka didapatkan gambar grafik (4.6). Gambar (4.6) merupakan grafik hubungan waktu retensi dan tekanan untuk laju alir sebesar 1,45 ml/min.
Gambar 4.6. Grafik hubungan antara tRdan P pada laju alir sebesar 1,45
ml/min.
B. Pembahasan
Pengukuran merupakan kegiatan yang sering dilakukan sehari – hari. Suatu pengukuran yang ideal akan menghasilkan hasil pengukuran yang akurat. Dalam suatu pengukuran terdapat dua hal yang penting yaitu input dan output.Input merupakan masukan yang akan diukur sedangkan output merupakan hasil akhir keluaran yang diinginkan dalam suatu pengukuran. Nilai dari output yang dikeluarkan bergantung pada input dan instrumen yang digunakan.
Suatu instrumen atau alat ukur berfungsi untuk mengukur suatu besaran tertentu. Suatu pengukuran yang ideal membutuhkan instrumen yang memenuhi beberapa persyaratan yaitu: sensitif, selektif, tidak mengganggu sampel yang diukur dan memiliki waktu tanggap cepat. Pengukuran yang menggunakan instrumen dengan kriteria seperti di atas diharapkan dapat menghasilkan output yang akurat.
HPLC atauHigh Pressure Liquid Chromatographyadalah salah satu alat yang bekerja berdasarkan prinsip kromatografi.Kromatografi merupakan suatu teknik pemisahan.Sehingga HPLC berfungsi untuk memisahkan molekul yang satu dengan yang lain. HPLC berbeda dibandingkan dengan kromatograf lainnya.Pada HPLC untuk memaksimalkan pemisahan digunakan laju alir tertentudan tekanan tinggi. Proses pemisahan pada HPLC terjadi di dalam kolom. Oleh karena itu, kolom merupakan bagian yang paling penting dalam sistem HPLC.Metode pemisahan yang digunakan bergantung pada jenis fase gerak dan kolom.
Metode kromatografi yang digunakan dalam penelitian ini adalah metode kromatografi fase terbalik. Pada metode pemisahan ini, fase gerak yang digunakan yaitu methanol bersifat polar sedangkan fase diam yaitu kolom C-18 (oktadesil silica) bersifat non polar. Parasetamol dan Kafein yang digunakan pada penelitian ini sebagai sampel merupakan zat yang bersifat polar.Metode kromatografi fase terbalik sangat baik digunakan untuk memisahkan sampel yang bersifat polar [Khopkar, 1990].
Kolom tersusun oleh bagian – bagian penyusun kolom.Sehingga interaksi yang terjadi bergantung pada bagian – bagian penyusun kolom dan molekul yang melewati kolom. Bagian – bagian penyusun kolom dan jenis kolom mempengaruhi besar faktor porositas dan faktor resistan kolom. Bila jenis kolom yang digunakan adalah tetap maka besar waktu retensi bergantung pada molekul yang melewati kolom.Sehingga bila ada sampel melewati kolom terdiri dari dua buah molekul maka didapatkan dua buah nilai waktu retensi yang berbeda untuk tiap molekul.Besar waktu retensi yang berbeda menunjukkan bahwa kedua molekul tersebut terpisah.
Proses pemisahan yang terjadi dalam penelitian ini adalah antara Parasetamol dan Kafein. Molekul Parasetamol dan Kafein berinteraksi terhadap bagian - bagianpenyusun kolom.Akibat interaksi tersebut Kafein tertahan lebih lama pada kolom dibandingkan dengan Parasetamol.SehinggaParasetamol dan Kafein terpisah.Contoh proses pemisahan yang terjadi di dalam kolom ditunjukkan pada gambar (2.2).
menampilkan terdeteksinya Parasetamol saat 4,38 menit yang ditunjukkan oleh sebuah puncak. Sedangkan gambar (4.2) menampilkan terdeteksinya Kafein saat 7,71 menit yang juga ditunjukkan dengan sebuah puncak. Dari kedua gambar grafik tersebut diketahui bahwa Parasetamol memiliki waktu retensi yang lebih singkat dibandingkan dengan Kafein.
Penelitian selanjutnya dilakukan penentuan waktu retensiParasetamol dan Kafein yang terdapat dalam suatu campuran.Hasil dari proses ini ditunjukkan oleh gambar (4.3) dan (4.4). Keduabuah gambar tersebut masing – masing menghasilkan dua buah puncak, yang menunjukkan Parasetamol dan Kafein.Gambar (4.3) merupakan grafik penentuan waktu retensi Parasetamol dan Kafein untuk laju alir 1ml/min, pada keadaan ini didapatkan waktu retensi Parasetamol adalah 4,6 menit dan Kafein adalah7 menit. Gambar (4.4) merupakan grafik penentuan waktu retensi Parasetamol dan Kafein untuk laju alir 1,9 ml/min, pada keadaan ini didapatkan waktu retensi Parasetamol adalah 2,36 menit dan Kafein adalah3,86 menit.
Berdasarkan gambar (4.3) dan (4.4) terlihat bahwa Parasetamol dengan Kafein terpisah.Parasetamol memiliki waktu retensi yang berbeda dari Kafein.Parasetamolmemiliki waktu retensi yang lebih singkat dibandingkan dengan Kafein.Semakin tinggi laju alirnya waktu retensinya akan semakin singkat sehingga dapat disimpulkan bahwa besar laju alir mempengaruhi nilai waktu retensi.
alir 0,55 ml/min; 0,7 ml/min; 0,85 ml/min; 1 ml/min; 1,15 ml/min; 1,3 ml/min; 1,45 ml/min; 1,6 ml/min; 1,75 ml/min; dan 1,9 ml/min untuk tekanan 100 bar. Selanjutnya dilakukan hal yang sama untuk tekanan 125 bar, 150 bar, 175 bar, 200 bar, 225 bar dan 250 bar, data yang dihasilkan dapat dilihat pada lampiran A. Sedangkan pengukuran waktu retensi dalam kondisi tekanan yang bervariasi pada laju alir tertentu, dilakukan pada tekanan 100 bar,125 bar, 150 bar, 175 bar, 200 bar, 225 bar dan 250 bar untuk laju alir 0,55 ml/min. Selanjutnya dilakukan hal yang sama untuk laju alir 0,7 ml/min; 0,85 ml/min; 1 ml/min; 1,15 ml/min; 1,3 ml/min; 1,45 ml/min; 1,6 ml/min; 1,75 ml/min; dan 1,9 ml/min, data yang dihasilkan dapat dilihat pada lampiran B.
Contoh data waktu retensi Parasetamol dan Kafein untuk kondisi laju alir yang bervariasi pada tekanan tertentu adalah tabel (4.1). Pada tabel (4.1) terlihat bahwa semakin tinggi laju alirnya maka waktu retensi dari kedua molekul semakin singkat. Hal ini sesuai dengan persamaan (2.1) yaitu waktu retensi berbanding terbalik terhadap laju alir. Sedangkan contoh data waktu retensi Parasetamol dan Kafein untuk kondisi tekanan yang bervariasi pada laju alir tertentu adalah tabel (4.2). Pada tabel (4.2) terlihat bahwa tekanan juga mempengaruhi waktu retensi, semakin tinggi tekanannya maka waktu retensinya semakin singkat.
dantekanannya maka waktu retensinya semakin singkat. Berdasarkan tabel – tabel data yang didapatkan terlihat bahwa waktu retensi lebih dipengaruhi oleh laju alir dibandingkan dengan tekanan. Perbedaan waktu retensi antara laju alir yang satu dengan laju alir yang lainpada kondisi tekanan tertentu untuk tiap molekul cukup besar, sedangkan perbedaan waktu retensi antara tekanan yang satu dengan tekanan yang lainpada kondisi laju alir tertentu untuk tiap molekul sangat kecil.
Berdasarkan tabel – tabel data yang ada dapat diperoleh grafik hubungan antara waktu retensi dengan laju alir dan tekanan.Contoh grafik ditunjukkan pada gambar (4.5) dan (4.6).Pada gambar (4.5) dan (4.6) terdapat grafik biru yang menunjukkan Parasetamol dan grafik merah yang menunjukkan Kafein.
Gambar (4.5) menunjukkan hubungan antara antara tR dan 1 / v pada
tekanan sebesar 100 bar. Waktu retensi Parasetamol berada pada rentang antara 1,5 menit hingga 5,5 menit untuk rentang seper laju alir 0,5 bar-1 (ml/min)-1 hingga 2 (ml/min)-1. Waktu retensi Kafein berada pada rentang antara 3 menit hingga 7,5 menit pada rentang seper laju alir 0,5 (ml/min)-1 hingga 2 (ml/min)-1. Waktu retensi Parasetamol dan Kafein berbeda.Semakin tinggi laju alir maka waktu retensi semakin singkat.
Gambar (4.6) menunjukkan hubungan antara tR dan P pada laju alir 1,45
grafik berwarna merah. Waktu retensi Kafein berada pada rentang antara 4 menit hingga 5 menit pada rentang tekanan dari 100 bar hingga 250 bar.
41
Tabel 4.3: Tabel hubungan nilai waktu retensi (menit) Paracetamol terhadap laju alir fase gerak (ml/min) dan tekanan (bar)
Laju alir (ml/min)
Tabel 4.4: Tabel hubungan nilai waktu retensi (menit) Kafein terhadap laju alir fase gerak (ml/min) dan tekanan (bar)
Tabel (4.3) dan (4.4) menunjukkan hubungan antara waktu retensiterhadap laju alir dan tekanan untuk masing – masing molekul Parasetamol dan Kafein.Tabel (4.3) dan (4.4) mempermudah dalam melihat data nilaiwaktu retensi untuk masing – masing molekul Parasetamol dan Kafein.Tabel tersebut menunjukkan secara langsung nilai waktu retensi untuk laju alirdantekanan tertentu.
0 .6
Gambar 4.7.Grafik hubungan waktu retensi (menit) terhadap laju alir fase gerak (ml/min) dan tekanan (bar) untuk pengukuran Parasetamol pada
panjang gelombang 263 nm dengan menggunakan kolom C-18 yang berukuran panjang 100mm diameter 4,6mm
0 .6
Gambar 4.8.Grafik hubungan waktu retensi (menit) terhadap laju alir fase gerak (ml/min) dan tekanan (bar) untuk pengukuran Kafein pada panjang gelombang 263 nm dengan menggunakan kolom C-18 yang berukuran
Grafik pada gambar (4.7) dan (4.8) menampilkan semua data nilai waktu retensi pada laju alir dan tekanan tertentu.Hubungan antara waktu retensi terhadap laju alir dan tekanan membentuk suatu bidang miring yang bergelombang tidak beraturan. Pada bidang miring tersebut terdapat warna yang berbeda – beda. Warna – warna yang berbeda menunjukkan rentang nilai waktu retensi yang terjadi pada kondisi laju alir dan tekanan tertentu.
Grafik pada gambar (4.7) menampilkan hubungan nilai waktu retensi (menit) Parasetamol terhadap laju alir fase gerak (ml/min) dan tekanan (bar). Waktu retensi Parasetamol dimulai dari rentang 2 menit hingga 5 menit pada rentang laju alir fase gerak dari 0,6 ml/min hingga 1,8 ml/min dan tekanan dari 100 bar hingga 250 bar.
Grafik pada gambar (4.8) menampilkan hubungan nilai waktu retensi (menit) Kafein terhadap laju alir fase gerak (ml/min) dan tekanan (bar). Waktu retensi Kafein dimulai dari rentang 4 menit hingga 7 menit pada rentang laju alir fase gerak dari 0,6 ml/min hingga 1,8 ml/min dan tekanan dari 100 bar hingga 250 bar.
ini dapat dilihat pada gambar (4.7) dan (4.8).Sehingga dapat disimpulkan bahwa Laju alir fase gerak lebih berpengaruh pada waktu retensi Parasetamol dan Kafein dibandingkan dengan tekanan. Perubahan laju alir yang semakin besar mengakibatkan waktu retensi Parasetamol dan Kafein menjadi semakin singkat.
46
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
Telah dilakukan penelitian untuk mencari pengaruh laju alir dantekanan terhadap waktu retensi Parasetamol dan Kafein dengan menggunakan HPLC. Berdasarkan penelitian yang telah dilakukan, dapat disimpulkan bahwa :
1. HPLC atau High Pressure Liquid Chromatography merupakan alat yang memiliki selektivitas tinggi dalam pemisahan dua buah molekul.
2. Laju alir fase gerak lebih berpengaruh terhadap waktu retensi dibandingkan dengan tekanan.
3. Pada kondisi laju alir, tekanan dan kolom yang sama dapat dihasilkan waktu retensi yang berbeda untuk tiap molekul.
B. Saran
47
DAFTAR PUSTAKA
Doebelin, E.O., 2004. Measurement System Application and Design, 5th Ed. New York: McGraw-Hil.
Gritter, R. J., Bobbit, J. M., Schwarting, A. M. 1991. Introduction to Chromatography. Penerjemah : Kosasih Padmawinata. Bandung : ITB. Holman, J. P., Jasjfi, E. 1984. Metode Pengukuran Teknik, 4th Ed. Jakarta :
Erlangga.
Johnson, E. L., Stevenson, R. 1991.Basic Liquid Chromatography. Penerjemah : Kosasih Padmawinata. Bandung : ITB.
Khopkar, M. S. 1990. Konsep Dasar Kimia Analitik. Jakarta : Universitas Indonesia Press.
Kuwana, T. 1980. Physical Methods in Modern Chemical Analysis,2nd Ed. New York : Academic Press.
Morris, A. S., 1996.The Essenceof Measurement. Britain: TJ Press.
Rangan, C. S., Sarma, G. R., Mani, V. S. V., 1985.Instrumentation Devices and Systems. New Delhi: Tata McGraw - Hill.
LAMPIRAN A
A. Pengukuran waktu retensi Parasetamol dan Kafein untuk kondisi laju alir bervariasi pada tekanan tertentu.
a. Tabel A.1 :Nilai waktu retensi Parasetamol dan Kafein untuk laju alir yang bervariasi
pada tekanan sebesar 125 bar.
Laju alir (ml/min) tRParasetamol (menit) tRKafein (menit)
0,55 5,25 7,31
b. Tabel A.2 :Nilai waktu retensi Parasetamol dan Kafein untuk laju alir yang
bervariasi pada tekanan sebesar 150 bar.
Laju alir (ml/min) tRParasetamol (menit) tRKafein (menit)
c. Tabel A.3 : Nilai waktu retensi Parasetamol dan Kafein untuk laju alir yang
bervariasi pada tekanan sebesar 175 bar
Laju alir (ml/min) tRParasetamol (menit) tRKafein (menit)
0,55 5,21 7,25
d. Tabel A.4 : Nilai waktu retensi Parasetamol dan Kafein untuk laju alir yang
bervariasi pada tekanan sebesar 200 bar
Laju alir (ml/min) tRParasetamol (menit) tRKafein (menit)
e. Tabel A.5 :Nilai waktu retensi Parasetamol dan Kafein untuk laju alir yang bervariasi
pada tekanan sebesar 225 bar.
Laju alir (ml/min) tRParasetamol (menit) tRKafein (menit)
0,55 5,27 7,28
f. Tabel A.6 :Nilai waktu retensi Parasetamol dan Kafein untuk laju alir yang
bervariasi pada tekanan sebesar 250 bar.
Laju alir (ml/min) tRParasetamol (menit) tRKafein (menit)
LAMPIRAN B
B. Pengukuran waktu retensi Parasetamol
dan Kafein dalam kondisi tekanan yang bervariasi pada laju alir tertentu.
a. Tabel B.1 : Nilai waktu retensi Parasetamol dan Kafein untuk tekanan yang bervariasi pada laju alir sebesar 0.55 ml/min
Tekanan (P) bar tRParasetamol (menit) tRKafein (menit)
100 5,36 7,46
b. Tabel B.2 : Nilai waktu retensi Parasetamol dan Kafein untuk tekanan yang bervariasi pada laju alir sebesar 0.7 ml/min
Tekanan (P) bar tRParasetamol (menit) tRKafein (menit)
100 5,00 7,17
c. Tabel B.3 : Nilai waktu retensi Parasetamol dan Kafein untuk tekanan yang bervariasi pada laju alir sebesar 0.85 ml/min
Tekanan (P) bar tRParasetamol (menit) tRKafein (menit)
d. Tabel B.4 : Nilai waktu retensi Parasetamol dan Kafein untuk tekanan yang bervariasi pada laju alir sebesar 1ml/min
Tekanan (P) bar tRParasetamol (menit) tRKafein (menit)
100 4,01 6,22
e. Tabel B.5 : Nilai waktu retensi Parasetamol dan Kafein untuk tekanan yang bervariasi pada laju alir sebesar 1.15 ml/min
Tekanan (P) bar tRParasetamol (menit) tRKafein (menit)
100 3,31 5,54
f. Tabel B.6 : Nilai waktu retensi Parasetamol dan Kafein untuk tekanan yang bervariasi pada laju alir sebesar 1.3 ml/min
Tekanan (P) bar tRParasetamol (menit) tRKafein (menit)
g.Tabel B.7 : Nilai waktu retensi Parasetamol dan Kafein untuk tekanan yang bervariasi pada laju alir sebesar 1.6 ml/min
Tekanan (P) bar tRParasetamol (menit) tRKafein (menit)
100 2,33 4,21
h.Tabel B.8 : Nilai waktu retensi Parasetamol dan Kafein untuk tekanan yang bervariasi pada laju alir sebesar 1.75 ml/min
Tekanan (P) bar tRParasetamol (menit) tRKafein (menit)
100 2,17 4,03
i. Tabel B.9 : Nilai waktu retensi Parasetamol
dan Kafein untuk tekanan yang bervariasi pada laju alir 1,9 ml/min
Tekanan (P) bar tRParasetamol (menit) tRKafein (menit)