ANALISIS KESADAHAN TOTAL PADA AIR BERSIH
TUGAS AKHIR
OLEH:
DWI PERTIWI NIM 102410047
PROGRAM STUDI DIPLOMA III ANALIS FARMASI DAN MAKANAN
FAKULTAS FARMASI
UNIVERSITAS SUMATERA UTARA MEDAN
2013
KATA PENGANTAR Bismillahirrahmanirrahim,
Setinggi puja sedalam syukur kehadirat Allah SWT yang senantiasa memberikan ridho dan karunia-Nya, sehingga penulis dapat menyusun dan menyelesaikan Tugas Akhir berjudul “Analisis Kesadahan Total Pada Air Bersih”. Tugas Akhir ini disusun sebagai salah satu syarat untuk dapat menyelesaikan Pendidikan Program Studi Diploma III Analis Farmasi dan Makanan di Fakultas Farmasi Universitas Sumatera Utara, Medan.
Penulis menyadari sepenuhnya bahwa tanpa bantuan dari berbagai pihak, penulis tidak akan dapat menyelesaikan Tugas Akhir ini sebagaimana mestinya.
Penulis mengucapkan terima kasih yang sebesar-besarnya kepada berbagai pihak antara lain:
1. Bapak Prof. Dr. Sumadio Hadisahputra, Apt., sebagai Dekan Fakultas Farmasi Universitas Sumatera Utara Medan.
2. Bapak Prof. Dr. Jansen Silalahi, M.App.Sc., Apt., sebagai Ketua Program Studi Diploma III Analis Farmasi dan Makanan.
3. Bapak Drs. Agusmal Dalimunthe, M.S., Apt., sebagai Dosen Pembimbing Tugas Akhir yang telah banyak memberikan bimbingan dan pengarahan dengan penuh perhatian hingga Tugas Akhir ini selesai.
4. Bapak Drs. Maralaut Batubara, M.Phill., Apt., sebagai Dosen Penasehat Akademis yang telah memberikan pengarahan dalam hal akademik.
5. Seluruh Dosen dan Pegawai Fakultas Farmasi Program Diploma III Analis Farmasi dan Makanan yang berupaya mendukung kemajuan mahasiswa.
6. Seluruh Pegawai Balai Teknik Kesehatan Lingkungan dan Pengendalian Penyakit (BTKLPP) Kelas I Medan yang telah meluangkan waktu, tenaga dan pikiran kepada penulis dalam melaksanakan Praktik Kerja Lapangan.
7. Teman-teman Analis Farmasi Dan Makanan stambuk 2010 khususnya Sari, Anisa, Fatimah, dan Rama. Kakak, abang dan adik stambuk 2008-2012 tanpa terkecuali, terima kasih untuk kebersamaan, motivasi serta masukan dalam penyusunan Tugas Akhir ini.
8. Teristimewa kepada Ayahanda Suprayitno dan Ibunda Hj. Nurmala Matondang S.Pd., yang telah membesarkan dan mendidik penulis dengan penuh kasih sayang dan cinta, selalu memberikan motivasi, kekuatan dan restu serta materi yang tak ternilai harganya dengan apapun, dan yang tersayang kakanda Maulidya Sari, SP. dan adinda Tri Nur Putri.
Penulis menyadari bahwa Tugas Akhir ini masih terdapat kekurangan dan kelemahan serta masih jauh dari kesempurnaan, untuk itu penulis mengharapkan saran dan kritik demi kesempurnaan Tugas Akhir ini dan demi peningkatan mutu penulisan Tugas Akhir di masa yang akan datang.
Akhir kata, penulis sangat berharap semoga Tugas Akhir ini dapat memberikan manfaat kepada semua pihak yang membutuhkan, Amin.
Medan, April 2013 Penulis,
Dwi Pertiwi NIM 102410047
Analysis of Total Hardness at Clean Water
Abstract
Clean water is the water used for day to day needs of eligible health and quality can be drunk when cooked. Clean water is obtained from wells dug, artesian well, rainwater, tap water, ground water, and water from springs.
Total hardness is the amount of calcium ions and magnesium, which can be determined by titration using EDTA (Ethylene Diamin Tetra Acetic acid) as well as indicators titran EBT (Eriochrom Black T) sensitive cation valence two.
The purpose of writing this final task to find out whether the water meets analyzed according to the quality standard set PERMENKES 416/MENKES/PER/IX/1990.
Samples taken from three locations is ground water, tap water and dig wells.
Determination of total hardness titration method kompleksometri done according to the appropriate installation procedures used in chemical laboratories BTKLPP Class I Medan.
Total hardness analysis results showed that the examined water containing total hardness in a row, namely: 529,92 mg CaCO3/L; 91,52 mg CaCO3/L, and 218,24 mg CaCO3/L. The maximum limit on the total hardness of the quality of raw water according 416/MENKES/PER/IX/1990 PERMENKES is 500 mg CaCO3/L.
Keywords: clean water, total hardness, and titration kompleksometri.
Analisis Kesadahan Total Pada Air Bersih Abstrak
Air bersih adalah air yang digunakan untuk keperluan sehari-hari yang kualitasnya memenuhi syarat kesehatan dan dapat diminum apabila telah dimasak.
Air bersih ini diperoleh dari sumur gali, sumur bor, air hujan, air ledeng, air tanah, dan air dari sumber mata air.
Kesadahan total adalah jumlah ion–ion kalsium dan magnesium yang dapat ditentukan melalui titrasi menggunakan EDTA (Etilen Diamin Tetra Asam asetat) sebagai titran serta indikator EBT (Eriochrom Black T) yang peka terhadap kation valensi dua. Tujuan penulisan tugas akhir ini untuk mengetahui apakah air bersih yang dianalisis memenuhi sesuai dengan baku mutu yang telah ditetapkan PERMENKES 416/MENKES/PER/IX/1990.
Sampel diambil dari tiga lokasi yakni air tanah, air ledeng dan sumur gali.
Penentuan kadar kesadahan total dilakukan menurut metode titrasi kompleksometri sesuai dengan prosedur yang digunakan di instalasi laboratorium kimia BTKLPP Kelas I Medan.
Hasil analisis kesadahan total menunjukkan bahwa air bersih yang diperiksa mengandung kesadahan total berturut-turut yaitu: 529,92 mg CaCO3/L;
91,52 mg CaCO3/L; dan 218,24 mg CaCO3/L. Batas maksimum baku mutu kesadahan total pada air bersih menurut PERMENKES 416/MENKES/PER/IX/1990 yaitu 500 mg CaCO3/L.
Kata kunci: air bersih, kesadahan total, dan titrasi kompleksometri.
DAFTAR ISI
Halaman
JUDUL ... i
LEMBAR PENGESAHAN ... ii
KATA PENGANTAR ... iii
ABSTRACT ... iv
ABSTRAK ... x
DAFTAR ISI ... vii
DAFTAR TABEL ... ix
DAFTAR LAMPIRAN ... x
DAFTAR GAMBAR ... xi
BAB I PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Tujuan dan Manfaat ... 2
1.2.1 Tujuan ... 2
1.2.2 Manfaat ... 3
BAB II TINJAUAN PUSTAKA ... 4
2.1 Air Bersih ... 4
2.1.1 Sumber Air bersih ... 4
2.1.2 Persyaratan dalam Penyediaan Air Bersih ... 6
2.2 Kesadahan Total ... 8
2.2.1 Kalsium ... 10
2.2.2 Magnesium ... 10
2.2.3 Dampak Buruk dari Kesadahan Total ... 11
2.2.4 Pelunakan Kesadahan Total ... 12
2.3 Titrasi Kompleksometri ... 13
2.3.1 Larutan Baku EDTA ... 13
2.3.2 Indikator EBT ... 15
2.3.3 Larutan Penyangga ... 16
BAB III METODE PENGUJIAN ... 17
3.1 Tempat ... 17
3.2 Sampel, Alat, dan Bahan ... 17
3.2.1 Sampel ... 17
3.2.2 Alat ... 18
3.2.3 Bahan ... 18
3.3 Prosedur ... 18
3.3.1 Prosedur Pembuatan Pereaksi dan Indikator ... 18
3.3.2 Prosedur Pembuatan Larutan Standar CaCO3 ... 19
3.3.3 Prosedur Standarisasi Larutan Na2EDTA ... 19
3.3.4 Prosedur Kesadahan Total ... 20
3.3.5 Perhitungan ... 21
BAB IV HASIL DAN PEMBAHASAN ... 22
4.1 Hasil ... 22
4.2 Pembahasan ... 22
BAB V KESIMPULAN DAN SARAN ... 23
5.1 Kesimpulan ... 23 5.2 Saran ... 23 DAFTAR PUSTAKA ... 24
DAFTAR TABEL
Halaman Tabel 1. Data Analisa ... 25 Tabel 2. Baku Mutu Air Bersih Parameter Kimia ... 29
DAFTAR LAMPIRAN
Halaman Lampiran 1. Perhitungan Kesadahan Total ... 25 Lampiran 2. Gambar Perubahan Warna pada Kompleksometri ... 28 Lampiran 3. Baku Mutu Air Bersih Parameter Kimia ... 29
DAFTAR GAMBAR
Halaman Gambar 1. Rumus Bangun EDTA ... 14 Gambar 2. Rumus Bangun EBT ... 15 Gambar 3. Perubahan Warna pada Titrasi Kompleksometri ... 28
BAB I
PENDAHULUAN
1.1 Latar Belakang
Air merupakan senyawa kimia yang sangat penting bagi kehidupan umat manusia dan mahkluk hidup lainnya dan fungsinya bagi kehidupan tersebut tidak akan dapat digantikan oleh senyawa lainnya. Hampir semua kegiatan yang dilakukan manusia membutuhkan air, mulai dari membersihkan diri (mandi), membersihkan ruangan tempat tinggal, menyiapkan makanan dan minuman sampai aktifitas–aktifitas lainnya (Achmad, 2004).
Saat ini, masalah utama yang dihadapi oleh sumber daya air meliputi kuantitas air yang sudah tidak mampu memenuhi kebutuhan yang terus menerus meningkat dan kualitas air untuk keperluan rumah tangga yang semakin menurun.
Kegiatan industri, rumah tangga, dan kegiatan lain berdampak negatif terhadap sumber daya air, antara lain menyebabkan penurunan kualitas air. Kondisi ini dapat menimbulkan gangguan, kerusakan, dan bahaya bagi semua makhluk hidup yang bergantung pada sumber daya air. Oleh karena itu, diperlukan pengelolaan dan perlindungan sumber daya air secara seksama (Effendi, 2003).
Pencemaran air adalah penyimpangan sifat–sifat air dari keadaan normal, bukan dari kemurniannya. Air yang tersebar di alam semesta ini tidak pernah terdapat dalam bentuk murni, namun bukan berarti bahwa semua air sudah tercemar. Karena kebutuhan makhluk hidup akan air sangat bervariasi, maka batas pencemaran untuk berbagai jenis air juga berbeda. Air sadah merupakan bagian
dari pencemaran air, yang disebut dengan air sadah adalah air permukaan dan air sumur yang mengandung bahan-bahan metal, seperti Na, Mg, Ca, dan Fe (Kristanto, 2002).
Dalam air bersih ditemukan kandungan kesadahan total dalam kadar yang berlebih. Berdasarkan hal di atas maka penulis berminat menentukan ”Analisis Kesadahan Total Pada Air Bersih” karena analisis tersebut sangat penting untuk menilai kualitas air bersih.
Masyarakat wilayah Sumatera Utara menggunakan air bersih untuk keperluan mandi, membersihkan dan diolah sebagai air minum. Air bersih mempunyai persyaratan salah satunya adalah kandungan tingkat kesadahan total tidak melewati ambang batas sesuai PERMENKES 416/MENKES/PER/IX/1990.
Dari hal-hal yang disebutkan di atas penulis ingin memeriksa kadar kesadahan total pada air bersih berupa air tanah, air sumur gali dan air ledeng yang digunakan oleh masyarakat Sumatera Utara dan sekitarnya.
1.2 Tujuan Dan Manfaat 1.2.1 Tujuan
Adapun tujuan dari analisis kesadahan total pada air bersih adalah:
1. Analisis kesadahan total bertujuan untuk mengetahui kadar kesadahan yang disebabkan oleh ion kalsium dan magnesium yang terdapat di dalam suatu larutan.
2. Analisis kesadahan total bertujuan untuk mengetahui apakah air bersih yang diperiksa memenuhi persyaratan yang sesuai dengan PERMENKES 416/MENKES/PER/IX/1990.
1.2.2 Manfaat
Analisis kesadahan total pada air bersih bermanfaat untuk menambah wawasan dari penulis agar dapat mengetahui cara menganalisis kesadahan total yang berasal dari kalsium dan magnesium pada air bersih juga pengaruh kesadahan total dalam air bersih.
BAB II
TINJAUAN PUSTAKA
2.1 Air Bersih
Berdasarkan PERMENKES 416/MENKES/PER/IX/1990 air bersih adalah air yang digunakan untuk keperluan sehari-hari yang kualitasnya memenuhi syarat kesehatan dan dapat diminum apabila telah dimasak. Air bersih ini diperoleh dari air tanah yang terdiri dari sumur gali dan sumur bor, air hujan, air ledeng, serta air dari sumber mata air.
Pemanfaatan air bersih dapat digunakan untuk keperluan-keperluan seperti: akan diolah menjadi air siap minum, untuk keperluan keluarga (cuci, mandi), sarana pariwisata (air terjun), pada industri (sarana pendingin), sebagai alat pelarut (dalam bidang farmasi/kedokteran), sebagai sarana irigasi, sebagai sarana peternakan, dan sebagai sarana olahraga (kolam renang)
(Gabriel, 2001).
2.1.1 Sumber Air Bersih
Air yang berada di permukaan bumi ini dapat berasal dari berbagai sumber. Berdasarkan letak dan asal sumbernya, dibagi menjadi air tanah yang terdiri dari sumur gali dan sumur bor, air hujan (air angkasa), air ledeng, serta mata air.
1. Air Tanah
Air tanah berasal dari air hujan yang jatuh ke permukaan bumi yang kemudian mengalami perkolasi atau penyerapan ke dalam tanah dan mengalami proses filtrasi secara alamiah. Air tanah mengandung zat–zat mineral dalam konsentrasi tinggi, semacam magnesium dan kalsium yang menyebabkan kesadahan air (Chandra, 2012).
Air tanah terbagi atas:
a. Sumur Gali
Sumur gali adalah air sumur yang didapat dengan cara menggali ke dalam tanah untuk mendapatkan mata air. Sumur ini disebut juga sumur dangkal, dengan kedalaman ± 15 m yang memiliki sumber air berasal dari resapan air hujan (Chandra, 2012).
b. Sumur Bor
Sumur bor adalah Sumur yang dibuat dengan cara membor ke dalam lapisan kerapatan tanah dengan kedalaman 100-300 m. Sumur ini disebut juga dengan sumur dalam yang memiliki sumber air berasal dari proses purifikasi alami air hujan sehingga airnya memenuhi syarat sanitasi (Chandra, 2012).
2. Air Hujan
Air hujan merupakan sumber utama air di bumi. Walau pada saat presipitasi merupakan air yang paling bersih, air tersebut cenderung mengalami pencemaran ketika berada di atmosfer. Pencemaran yang berlangsung di atmosfer itu dapat disebabkan oleh partikel debu, mikroorganisme, karbon dioksida, nitrogen, dan ammonia (Chandra, 2012).
3. Air Ledeng
Air ledeng adalah air yang diproduksi melalui proses penjernihan dan penyehatan sebelum dialirkan kepada konsumen melalui suatu instalasi berupa saluran sumber air (pipa) yang dikelola oleh pemerintah maupun swasta (Chandra, 2012).
4. Mata Air
Mata air adalah air tanah yang keluar dengan sendirinya ke permukaan tanah. Berasarkan keluarnya (munculnya ke permukaan tanah) terbagi atas:
a. Rembesan, di mana air ke luar dari lereng–lereng.
b. Umbul, di mana air ke luar ke permukaan pada suatu dataran (Sutrisno, 2002).
2.1.2 Persyaratan Air Bersih
Agar air bersih tidak menyebabkan gangguan kesehatan, maka air tersebut harus memenuhi persyaratan–persyaratan kesehatan. Menurut Mulia (2005) persyaratan air bersih dapat ditinjau dari parameter fisika, parameter kimia, dan parameter mikro biologik.
1. Parameter Fisika
a. Air yang baik idealnya tidak berbau, karena air yang berbau busuk dapat disebabkan oleh proses penguraian bahan organik yang terdapat di dalam air.
b. Air yang baik idealnya harus jernih, karena air yang keruh mengandung partikel padat tersuspensi yang dapat berupa zat–zat yang berbahaya bagi kesehatan.
c. Air yang baik idealnya tidak memiliki rasa atau rasa tawar, karena air yang tidak tawar mengindikasikan adanya zat–zat tertentu di dalam air.
d. Air yang baik tidak boleh memiliki perbedaan suhu yang mencolok dengan udara sekitar (udara ambien), umumnya 25oC ± 3oC. Karena suhu yang berada di atas atau di bawah dari udara ambien berarti sedang terjadi proses biokimia yang mengeluarkan atau menyerap energi dalam air.
e. Air yang baik memiliki padatan terlarut total (Total Dissolved Solid) adalah bahan–bahan terlarut (diameter ≤ 10-6) dan koloid (diameter 10-6 – 10-3 mm).
2. Parameter Kimia
Air bersih tidak boleh mengandung bahan-bahan kimia dalam jumlah yang melampaui batas. Beberapa persyaratan kimia antara lain adalah: pH, zat organik, kesadahan, besi (Fe), mangan (Mn), tembaga (Cu), seng (Zn), klorida (Cl-), nitrit (NO2-
), fluorida (F), logam berat, zat reaktif serta zat–
zat beracun dan berbahaya.
3. Parameter Mikro biologik
Parameter ini menggunakan bakteri Coliform sebagai organisme petunjuk (indicator organism). Total coliform menunjukkan bakteri Coliform dari tinja, tanah atau sumber alamiah lainnya. Berdasarkan PERMENKES 416/MENKES/PER/IX/1990 kadar maksimum untuk total coliform adalah 50 (jumlah/100 ml) pada non perpipaan dan 10 (jumlah/100ml) pada
perpipaan. Fecal coliform (koliform tinja) menunjukkan bakteri Coliform yang berasal dari tinja manusia atau hewan berdarah panas lainnya.
2.2 Kesadahan Total
Kesadahan (hardness) adalah merupakan sifat air yang disebabkan oleh adanya ion–ion (kation) logam bervalensi dua. Ion–ion semacam itu mampu bereaksi dengan sabun membentuk kerak air. Kation–kation penyebab utama kesadahan yaitu: Ca2+, Mg2+, Sr2+, Fe2+, dan Mn2+. Sedangkan anion–anion yang biasa terdapat dalam air adalah HCO3-, SO42-, Cl-, NO3-, SiO2- (Sutrisno, 2002).
Kesadahan total adalah jumlah ion–ion Ca2+ dan Mg2+ yang dapat ditentukan melalui titrasi kompleksometri menggunakan EDTA (Etilen Diamin Tetra Asam asetat) sebagai titran dan menggunakan indikator yang peka terhadap semua kation tersebut. Kesadahan total dapat juga ditentukan dengan menggunakan jumlah ion Ca2+ dan ion Mg2+ yang dianalisis secara terpisah misalnya dengan metode Spektrofotometri Serapan Atom (Alaerts dan Santika, 1987).
Keberadaan kation lain, misalnya Sr2+, Fe2+ Mn2+serta kation valensi tiga seperti Al3+ dan Fe3+ juga memberikan kontribusi bagi nilai kesadahan total, namun mengingat sifat kelarutannya yang relatif rendah pada pH netral maka peran kation tersebut sering diabaikan. Kesadahan dinyatakan dengan satuan mg CaCO3/liter (Effendi, 2003).
Berdasarkan kandungan mineral Kristanto (2002) membagi kesadahan air dalam dua golongan, yaitu:
1. Kesadahan air sementara atau temporer disebabkan karena garam–garam karbonat (CO32-) dan bikarbonat (HCO3-) dari kalsium (Ca2+) dan magnesium (Mg2+). Garam karbonat merupakan garam yang tidak larut, sedangkan garam bikarbonat merupakan garam larut. Garam karbonat dengan air dan karbondioksida di udara akan membentuk garam bikarbonat yang larut. Oleh karena itu, semakin tinggi konsentrasi karbondioksida di udara, maka semakin mudah melarutkan kalsium dari mineral–mineral karbonatnya sebagai berikut:
Reaksi:
CaCO3 + H2O + CO2 → Ca(HCO3) 2
Tidak larut larut
Kesadahan air ini bersifat sementara, karena dapat dihilangkan dengan cara pemanasan, di mana terbentuk garam kalsium karbonat yang tidak larut dan mengendap, sehingga dapat dihilangkan dengan mudah.
Ca(HCO3) 2 CaCO3
dipanaskan
2. Kesadahan air menetap atau permanen disebabkan oleh adanya garam–
garam klorida (Cl-) dan sulfat (SO42-) dari kalsium (Ca2+) dan magnesium (Mg2+). Kesadahan karena garam–garam tersebut bersifat tetap dan sukar dihilangkan.
Kesadahan berasal dari kontak air dengan tanah dan bebatuan. Air hujan sebenarnya tidak memiliki kemampuan untuk melarutkan ion–ion penyusun kesadahan yang banyak terikat di dalam tanah dan bebatuan kapur (limestone), meskipun memiliki kadar karbondioksida yang relatif tinggi. Larutnya ion–ion
yang dapat meningkatkan nilai kesadahan tersebut lebih banyak disebabkan oleh aktivitas bakteri di dalam tanah, yang banyak mengeluarkan karbondioksida (Effendi, 2003).
2.2.1 Kalsium
Kalsium adalah merupakan sebagian dari komponen yang merupakan penyebab kesadahan. Selain itu, adanya kalsium dalam air adalah sangat diperlukan untuk dapat memenuhi kebutuhan akan unsur tersebut, yang khususnya diperlukan untuk pertumbuhan tulang dan gigi. Untuk menghindari efek yang tidak diinginkan akibat dari terlalu rendah atau terlalu tingginya kadar kalsium dalam air bersih yang akan diolah menjadi air minum, ditetapkan standar persyaratan konsentrasi kalsium sebagaimana yang ditetapkan oleh DepKes RI sebesar 75–200 mg/L. Standar yang ditetapkan oleh WHO inter-regional water study-group adalah sebesar 75–150 mg/L (Sutrisno, 2002).
Berdasarkan kadar kalsium di dalam air (Gabriel, 2001) membagi tingkat kesadahan air dalam empat kelompok, yaitu:
a. Kadar CaCO3 terdapat dalam air 0–75 mg/L disebut air lunak (soft water).
b. Kadar CaCO3 terdapat dalam air 75–150 mg/L disebut air cukup keras (moderately hard water).
c. Kadar CaCO3 terdapat dalam air 150–300 mg/L disebut air keras (hard water).
d. Kadar CaCO3 terdapat dalam air 300 mg/L ke atas disebut air sangat keras (very hard water).
2.2.2 Magnesium
Seperti halnya kalsium, magnesium juga merupakan bagian dari komponen penyebab kesadahan pada air. Dalam jumlah kecil magnesium dibutuhkan oleh tubuh untuk pertumbuhan tulang, akan tetapi dalam jumlah yang lebih besar dari 150 mg/L dapat menyebabkan rasa mual (Sutrisno, 2002).
Densitas (kepadatan) muatan ion magnesium jauh lebih besar dan ikatan yang lebih kuat dengan air untuk melakukan hidrasi dibandingkan ion kalsium.
Pada umumnya konsentrasi magnesium dalam air tawar lebih kecil dibandingkan kalsium. Telah diteliti bahwa di lautan magnesium dalam bentuk larutan lebih lama dari kalsium. Hal ini disebabkan senyawa magnesium mengendap lebih lambat dibandingkan senyawa kalsium (Achmad, 2004).
Kesadahan kalsium dan magnesium sering kali perlu diketahui untuk menentukan jumlah kapur dan soda abu yang dibutuhkan dalam proses pelunakan air (lime-soda ash softening). Jika nilai kesadahan kalsium diketahui maka kesadahan magnesium dapat ditentukan melalui persamaan:
Kesadahan total – kesadahan kalsium = kesadahan magnesium
(Effendi, 2003).
2.2.3 Dampak Buruk dari Kesadahan Total
1. Menurunnya fungsi sabun sebagai zat pembersih sebab sabun yang tersusun oleh garam natrium dari asam lemak dengan garam kalsium dan magnesium bereaksi membentuk garam yang tidak larut dan tidak berbusa
mengakibatkan pewarnaan pada bahan yang dicuci. Residu endapan tertahan pada pori–pori pakaian sehingga pakaian terasa kasar. Demikian juga, kulit tangan menjadi kasar (Effendi, 2003).
2. Menimbulkan kerak pada ketel yang dapat menyumbat katup-katup ketel karena terbentuknya endapan kalsium karbonat pada dinding atau katup ketel. Akibatnya hantaran panas pada ketel air berkurang sehingga memboroskan bahan bakar. Terjadi penyumbatan pada pipa–pipa air ledeng, serta korosif terhadap baja dan mengakibatkan pipa-pipa besi berkarat (Kristanto, 2002).
3. Menimbulkan konsentrasi kalsium dan magnesium di dalam tubuh meningkat apabila air sadah dimanfaatkan menjadi air minum sehingga mengakibatkan rasa mual, penyakit tulang rapuh (osteoporosis), pengapuran ginjal (urolithiasis) dan menjurus ke uremia (Gabriel, 2001).
2.2.4 Pelunakan Kesadahan Total
Menurut (Gabriel, 2001) pelunakan air (water softening) yaitu suatu proses menghilangkan atau mengurangi kadar kalsium maupun magnesium dalam air, dengan cara:
1. Untuk kesadahan temporer atau sementara dengan cara pemanasan.
Pemanasan air memakai wadah ketel di mana dasar ketel diletakkan segelondong benang katun agar karbonat akan mengendap pada katun dan bukan pada dasar ketel.
2. Untuk kesadahan menetap atau permanen dilakukan proses presipitasi atau pengendapan dengan memakai salah satu cara diantaranya:
a. Kapur mati [Ca(OH)2] disebut proses Clark
b. Penambahan soda kapur (Na2CO3) atau dengan kaustik soda (NaOH)
3. Memakai resin dengan sistem pertukaran ion. Air yang melewati resin maka kalsium dan magnesium yang ada di dalam air akan ditukar dengan natrium (Na+). Resin tidak dapat menghilangkan bahan non organik yang sudah larut serta organisme yang ada di dalam air. Air yang sudah dilembutkan oleh resin hanya cocok untuk mandi dan mencuci, tidak baik untuk diminum.
2.3 Titrasi Kompleksometri
Titrasi kompleksometri didasarkan pada reaksi zat–zat pengompleks organik tertentu dengan ion–ion logam, menghasilkan pasangan kimiawi (chelated complex) yang mantap. Zat pengompleks yang paling sering digunakan adalah
asam Etilen Diamin Tetra Asam asetat (EDTA), yang membentuk senyawa kompleks yang mantap dengan beberapa ion logam valensi dua dan tiga yang kestabilannya bervariasi. Titik Akhir Titrasi (TAT) ditetapkan dengan indikator logam (Rivai, 1995).
2.3.1 Larutan Baku EDTA (Etilen Diamin Tetra Asam asetat)
Untuk pembuatan larutan baku EDTA digunakan garam natrium dari EDTA yang susunan molekulnya sering ditulis seperti berikut:
C11H14Na2O8.2H2O (bobot molekul = 372,16). Kepekatan larutan yang di pakai dalam titrasi kompleksometri dinyatakan dalam istilah kemolaran, karena
kompleks logam dengan EDTA selalu terbentuk dalam perbandingan 1:1 (Rivai, 1995).
Garam natrium dari EDTA tidak memenuhi persyaratan sebagai baku utama. Karena itu larutan EDTA tidak dapat dipakai langsung sebagai pentiter, tetapi harus dibakukan terlebih dulu dengan zat baku utama. Zat baku utama yang lazim digunakan untuk pembakuan larutan EDTA adalah logam murni atau garam–garam logam seperti magnesium sulfat (MgSO4) atau seng sulfat (ZnSO4).
Larutan EDTA berubah kepekatannya selama penyimpanan karena besarnya kemampuan EDTA membentuk kompleks sehingga kalsium yang ada dalam bahan pembentuk wadah tempat penyimpanannya dapat ditarik oleh EDTA, terutama bila wadah tempat penyimpanan itu terbuat dari kaca bermutu rendah (Rivai, 1995).
Titrasi dengan EDTA dapat dilakukan dengan cara langsung, yaitu ion logam dititrasi dengan larutan standar EDTA, kondisi lingkungan titrasi dan indikator harus cocok dengan logam analit dan reaksi pembentukan logam kelat atau kompleks harus cepat. Pada umumnya selain untuk titrasi langsung Mg2+, Zn2+, dan Ca2+, tidak ada lagi indikator yang cocok (Satiadarma, 2004).
Gambar 1. Rumus Bangun EDTA (Etilen Diamin Tetra Asam asetat)
(Anissa, 2011).
EDTA berpotensi sebagai ligan polidentat yang dapat berkoordinasi dengan sebuah ion logam melalui gugus dua nitrogen dan empat karboksilnya. Asam poliaminokarboksilat seperti EDTA, dan berbagai senyawa relevan yang membentuk kompleks–kompleks yang stabil, larut dalam air membentuk kompleks 1:1 dengan ion logam oleh sebab itu dapat dipergunakan sebagai titran untuk logam–logam (Day dan Underwood, 2002).
2.3.2 Indikator EBT (Eriochrom Black T)
Eriochrom Black T (Solochrom Black T) adalah sejenis indikator yang berubah dari warna biru menjadi warna merah muda bila berada dalam larutan yang mengandung ion kalsium dan ion magnesium dengan pH 10 ± 0,1 (Alaerts dan Sumestri, 1987).
EBT dapat digunakan sebagai indikator asam basa maupun indikator logam. Kompleks logamnya umumnya merah, jadi untuk mendeteksi ion logam pH larutan harus ≥ 7 agar pada waktu tidak ada ion logam warna larutannya biru dan ketika pada titrasi terdapat kelebihan ion logam sedikit, terjadi perubahan warna ke merah (Satiadarma, 2004).
Gambar 2. Rumus Bangun EBT (Eriochrom Black T)
2.3.3 Larutan Penyangga
Larutan penyangga merupakan larutan berair yang mengandung asam dan garamnya atau basa dan garamnya memperlihatkan kecenderungan menahan perubahan pH larutan bila ditambahkan asam atau basa. Larutan penyangga tidak berubah pH nya bila diencerkan dan pH tersebut tidak banyak berubah bila sejumlah kecil asam kuat atau basa kuat ditambahkan ke dalam larutan penyangga. Kegunaan larutan penyangga adalah untuk mengatur dan mencegah terjadinya perubahan pH yang disebabkan oleh ion hidrogen yang terlepas pada saat titrasi dan mencegah terbentuknya endapan logam hidroksida, serta menyingkirkan logam besi sebagai endapan (Rivai, 1995).
BAB III
METODE PENGUJIAN
3.1 Tempat
Analisis kesadahan total dilakukan di Balai Teknik Kesehatan Lingkungan dan Pengendalian Penyakit (BTKLPP) Kelas I Medan yang bertempat di Jln.
Wahid Hasyim No. 15, Medan.
3.2 Sampel, Alat, dan Bahan 3.2.1 Sampel
1. Air bersih yang berasal dari air tanah Lokasi: Mabar, Medan
Kode: 51/K/AB/01.2013
Organoleptis: warna (bening kehijau-hijauan), rasa (sedikit kelat), bau (tidak berbau)
pH: 6,1
Temperatur: 27,8
2. Air bersih yang berasal dari air ledeng
Lokasi: Padang Sidempuan, Mandailing Natal Kode: 484/K/AB/02.2013
Organoleptis: warna (tidak berwarna), rasa (tidak berasa), bau (tidak berbau).
pH: 7,0
Temperatur: 24,1
3. Air bersih yang berasal dari sumur gali Lokasi: Perbaungan, Serdang Bedagai Kode: 578/K/AB/02.2013
Organoleptis: warna (tidak berwarna), rasa (tidak berasa), bau (tidak berbau).
pH: 8,4
Temperatur: 28,9 3.2.2 Alat
Buret 25 ml (ketelitian 0,05 ml), erlenmeyer 250 ml, gelas ukur 100 ml, bola karet, spatula, pipet tetes, beaker glass 25 ml, dan pipet volume 10 ml.
3.2.3 Bahan
Sampel air bersih, air suling, Na2EDTA (dinatrium Etilen Diamin Tetra Asam asetat), indikator EBT (Eriochrome Black T), larutan penyangga pH 10 ± 0,1.
3.3 Prosedur
3.3.1 Prosedur Pembuatan Pereaksi dan Indikator 1. EBT (Eriochrom Black T)
Ditimbang 200 mg EBT dan 100 gram kristal NaCl, dihomogenkan. Gerus campuran hingga mempunyai ukuran 40 s/d 50 mesh. Dan simpan dalam botol bertutup rapat.
2. Larutan penyangga pH 10 ± 0,1
Dilarutkan 1,179 gram Na2EDTA dihidrat dan 780 mg magnesium sulfat penta hidrat (MgSO4.7H2O) dalam 50 ml air suling. Tambahkan larutan tersebut ke dalam 16,9 gram NH4Cl dan 143 ml NH4OH P sambil dilakukan pengadukan. Encerkan dengan air suling hingga volumenya menjadi 250 ml.
3. Larutan baku Na2EDTA.2H2O = C11H14N2Na2O8.2H2O = tritiplek 0,01 M Dilarutkan 3,723 gram Na2EDTA dihidrat dengan air suling di dalam labu ukur 1000 ml, tepatkan sampai tanda tera.
3.3.2 Prosedur Pembuatan Larutan Standar CaCO3 0,01 M
1. Timbang 1 gram CaCO3 anhidrat, masukkan ke dalam labu erlenmeyer 500 ml.
2. Larutkan dengan sedikit asam klorida (HCl) 1:1, tambahkan dengan 200 ml air suling.
3. Didihkan beberapa menit untuk menghilangkan CO2, lalu dinginkan.
4. Setelah dingin, tambahkan beberapa tetes indikator metal merah.
5. Tambahkan NH4OH 1:1 atau HCl 1:1 sampai terbentuk warna orange (pH 5)
6. Pindahkan secara kuantitatif ke dalam labu ukur 100 ml, kemudian tepatkan sampai tanda tera.
3.3.3 Prosedur Standarisasi Larutan Na2EDTA 0,01 M
1. Pipet 10 ml larutan standar CaCO3 0,01 M, masukkan ke dalam Erlenmeyer 250 ml.
2. Tambahkan 40 ml air suling dan 1 ml larutan penyangga pH 10 ± 0,1.
3. Tambahkan seujung spatula 30 mg sampai dengan 50 mg indikator EBT.
4. Titrasi dengan larutan Na2EDTA sampai terjadi perubahan warna dari merah keunguan menjadi biru (seperti yang terlihat pada Lampiran 2).
5. Catat volume larutan Na2EDTA yang digunakan.
6. Hitung molaritas larutan baku Na2EDTA dengan menggunakan rumus sebagai berikut:
M
EDTA=
MCaCO 3 x VCaCO 3 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉Keterangan:
MCaCO3 = molaritas CaCO3 yang digunakan yaitu 0,01M VCaCO3 = volume CaCO3 0,01 M yang dipipet
VEDTA = volume titrasi yang digunakan mencapai TAT (dibuat triplo) 3.3.4 Prosedur Analisis Kesadahan Total
1. Ambil 25 ml sampel, masukkan ke dalam erlenmeyer 250 ml.
2. Encerkan dengan air suling sampai volume 50 ml.
3. Tambahkan 1 ml larutan penyangga pH 10 ± 0,1.
4. Tambahkan seujung spatula 30 mg sampai dengan 50 mg indikator EBT.
5. Titrasi dengan larutan baku Na2EDTA secara perlahan sampai terjadi perubahan warna merah keunguan menjadi biru (seperti yang terlihat pada Lampiran 2).
6. Catat volume larutan Na2EDTA yang digunakan.
7. Apabila larutan Na2EDTA yang dibutuhkan untuk titrasi lebih dari 15 ml, encerkan sampel dengan air suling dan ulangi langkah 1 sampai dengan 6.
3.3.5 Perhitungan
Kesadahan total (mg CaCO3/L) = 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑥𝑥 𝑀𝑀𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑥𝑥 𝐵𝐵𝑀𝑀 𝑥𝑥 1000 𝑥𝑥 𝐹𝐹𝐹𝐹 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑆𝑆𝑆𝑆𝑉𝑉𝐹𝐹𝑉𝑉𝑉𝑉
Keterangan:
VEDTA = volume titrasi Na2EDTA sampai TAT
MEDTA = molaritas Na2EDTA yang digunakan untuk titrasi BM = berat molekul CaCO3 (100 g/mol)
Fp = faktor pengenceran
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil
Data analisis kesadahan total dapat dilihat pada Tabel 1 di bawah ini.
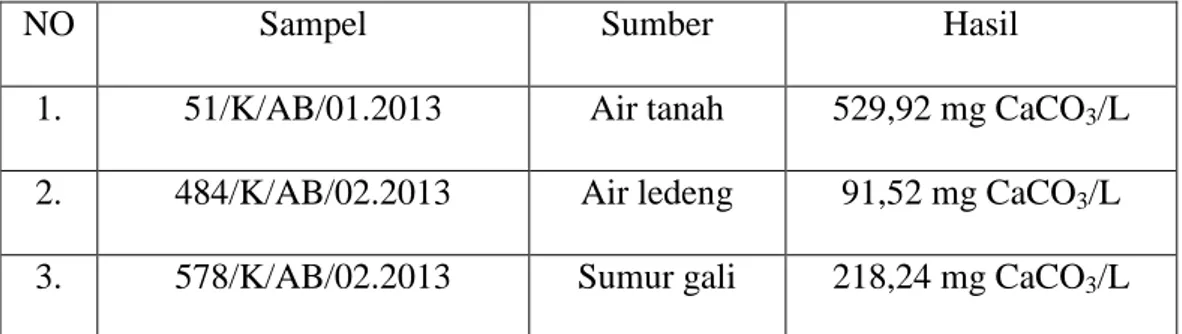
Tabel 1. Data Analisis
NO Sampel Sumber Hasil
1. 51/K/AB/01.2013 Air tanah 529,92 mg CaCO3/L 2. 484/K/AB/02.2013 Air ledeng 91,52 mg CaCO3/L 3. 578/K/AB/02.2013 Sumur gali 218,24 mg CaCO3/L Perhitungan dari hasil tabel di atas dapat dilihat pada Lampiran 1.
4.2 Pembahasan
Pada analisis kesadahan total digunakan metode titrasi kompleksometri. Dari hasil analisis pada sampel air bersih dengan kode 51/K/AB/01.2013, 484/K/AB/02.2013, dan 578/K/AB/02.2013 diperoleh hasilnya berturut-turut yaitu: 529,92 mg CaCO3/L; 91,52 mg CaCO3/L; dan 218,24 mg CaCO3/L. Di mana baku mutu kesadahan total pada air bersih menurut PERMENKES 416/MENKES/PER/IX/1990 adalah 500 mg CaCO3/L. Dari data di atas dinyatakan bahwa kadar kesadahan total pada salah satu sampel air bersih tidak memenuhi syarat karena melebihi baku mutu yang telah ditetapkan, yaitu sampel dengan kode 51/K/AB/01.2013.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari hasil analisis yang dilakukan, maka dapat disimpulkan kesadahan total pada air bersih yang berasal dari air sumur gali dan air ledeng memenuhi syarat sedangkan air bersih yang berasal dari air tanah tidak memenuhi syarat karena telah melebihi baku mutu sesuai dengan ketentuan PERMENKES 416/MENKES/PER/IX/1990 adalah 500 mg CaCO3/L.
5.2 Saran
Sebelum melakukan pengujian, harus memahami metode, prinsip kerja serta prosedur analisis seperti saat pemipetan sampel, titrasi sampel dari buret.
Agar diperoleh hasil yang maksimal saat melakukan analisis kesadahan total yang berasal dari kalsium dan magnesium pada air bersih.
DAFTAR PUSTAKA
Achmad, R. (2004). Kimia Lingkungan. Yogyakarta: Penerbit ANDI Yogyakarta.
Halaman 15, 47-49.
Alaerts dan Sumestri. (1987). Metoda Penelitian Air. Surabaya: Penerbit Usaha Nasional. Halaman 79.
Anissa, Syabatini. Titrasi Kompleksometri. (2011).
http://annisanfushie.wordpress.com/open-the-page-in-blog/page/6/2011.
Tanggal 19 April 2013.
Chandra, B. (2012). Pengantar Kesehatan Lingkungan. Jakarta: Penerbit Buku Kedokteran. Halaman 42.
Day dan Underwood. (2002). Analisis Kimia Kualitatif. Jakarta: Penerbit Erlangga. Halaman 197.
Effendi, H. (2003). Telaah Kualitas Air. Yogyakarta: Penerbit Kanisius. Halaman 11, 106-109.
Gabriel, J.F. (2001). Fisika Lingkungan. Jakarta: Penerbit Hipokrates. Halaman 48-49, 92, 96-97.
Kristanto, P. (2002). Ekologi Industri. Yogyakarta: Penerbit ANDI Yogyakarta.
Halaman 72-73, 76.
Peraturan Menteri Kesehatan Republik Indonesia. (1990). PERMENKES RI NO 416/MENKES/PER/IX/1990 Syarat-syarat dan Pengawasan Kualitas Air Bersih.
Mulia, R. (2005). Kesehatan Lingkungan. Yogyakarta: Penerbit Graha Ilmu.
Halaman 59-62.
Rivai, H. (1995). Asas Pemeriksaan Kimia. Jakarta: Penerbit Universitas Indonesia. Hal 109-111, 229, 246-248.
Satiadarma, K. (2004). Asas Pengembangan Prosedur Analisis. Surabaya:
Penerbit Universitas Airlangga. Halaman 78, 79.
Slamet, S.J. (2002). Kesehatan Lingkungan. Yogyakarta: Penerbit Universitas Gadjah Mada. Halaman 83-84.
Sutrisno, T. (2002). Teknologi Penyediaan Air Bersih. Jakarta: Penerbit Rineka Cipta. Halaman 18-19, 36-37.
LAMPIRAN
Lampiran 1
Data analisis kesadahan total dapat dilihat pada Tabel 1 di bawah ini.
Tabel 1. Data Analisis
NO Sampel Sumber Hasil
1. 51/K/AB/01.2013 Air tanah 529,92 mg CaCO3/L 2. 484/K/AB/02.2013 Air ledeng 91,52 mg CaCO3/L 3. 578/K/AB/02.2013 Sumur gali 218,24 mg CaCO3/L
Perhitungan:
MEDTA = MCaCO 3 x VCaCO 3 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉
Keterangan:
MCaCO3 = molaritas CaCO3 yang digunakan yaitu 0,01M VCaCO3 = volume CaCO3 0,01 M yang dipipet
VEDTA = volume titrasi yang digunakan mencapai TAT (dibuat triplo) a. MEDTA = MCaCO 3 x VCaCO 3
𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉
= 0,01 𝑥𝑥 10
10,86
= 0,1
10,86
= 0,0092 M
b. MEDTA = MCaCO 3 x VCaCO 3 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉
= 0,01 𝑥𝑥 10
11,36
= 0,1
11,36
= 0,0088 M
Kesadahan total (mg CaCO3/L) = 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑥𝑥 𝑀𝑀𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑥𝑥 𝐵𝐵𝑀𝑀 𝑥𝑥 1000 𝑥𝑥 𝐹𝐹𝐹𝐹 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑆𝑆𝑆𝑆𝑉𝑉𝐹𝐹𝑉𝑉𝑉𝑉
Keterangan:
VEDTA = volume titrasi Na2EDTA sampai TAT
MEDTA = molaritas Na2EDTA yang digunakan untuk titrasi BM = berat molekul CaCO3 (100 g/mol)
Fp = faktor pengenceran Sampel: 51/K/AB/01.2013
Kesadahan total (mg CaCO3/L) = 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑥𝑥 𝑀𝑀𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑥𝑥 𝐵𝐵𝑀𝑀 𝑥𝑥 1000 𝑥𝑥 𝐹𝐹𝐹𝐹 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑆𝑆𝑆𝑆𝑉𝑉𝐹𝐹𝑉𝑉𝑉𝑉
= 14,40 x 0,0092 x 100 x 1000 x 2 50
= 26496
50
= 529,92 mg CaCO3/L Sampel: 484/K/AB/02.2013
Kesadahan total (mg CaCO3/L) = 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑥𝑥 𝑀𝑀𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑥𝑥 𝐵𝐵𝑀𝑀 𝑥𝑥 1000 𝑥𝑥 𝐹𝐹𝐹𝐹 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑆𝑆𝑆𝑆𝑉𝑉𝐹𝐹𝑉𝑉𝑉𝑉
= 2,60 x 0,0088 x 100 x 1000 x 2 50
= 4576
50
= 91,52 mg CaCO3/L
Sampel: 578/K/AB/02.2013
Kesadahan total (mg CaCO3/L) = 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑥𝑥 𝑀𝑀𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑥𝑥 𝐵𝐵𝑀𝑀 𝑥𝑥 1000 𝑥𝑥 𝐹𝐹𝐹𝐹 𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉𝑉 𝑆𝑆𝑆𝑆𝑉𝑉𝐹𝐹𝑉𝑉𝑉𝑉
= 6,20 x 0,0088 x 100 x 1000 x 2 50
= 10912
50
= 218,24 mg CaCO3/L
Lampiran 2
Gambar 3. Perubahan warna dari ungu (merah anggur) menjadi biru
Lampiran 3
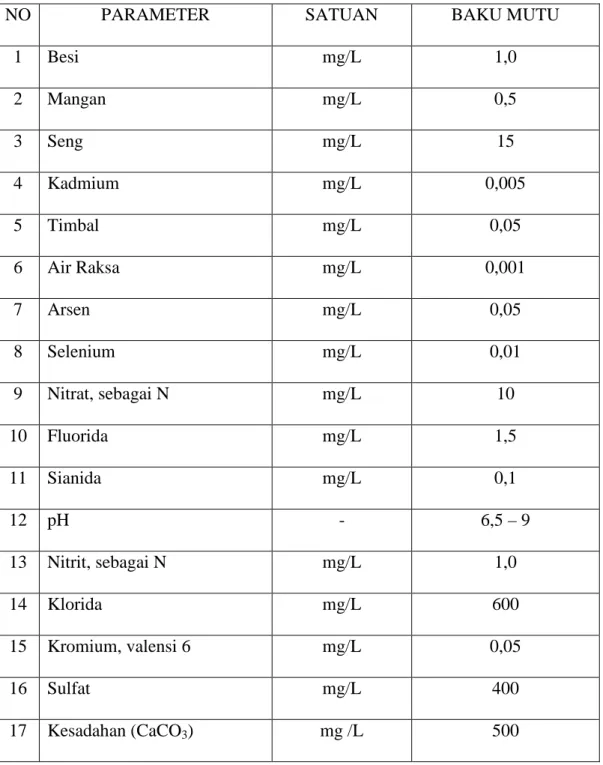
PERMENKES RI No: 416/MENKES/PER/IX/1990 standar kualitas baku mutu air bersih Tanggal 3 September 1990, dapat dilihat pada Tabel 2 di bawah ini.
Tabel 2. Baku Mutu Air Bersih Parameter Kimia
NO PARAMETER SATUAN BAKU MUTU
1 Besi mg/L 1,0
2 Mangan mg/L 0,5
3 Seng mg/L 15
4 Kadmium mg/L 0,005
5 Timbal mg/L 0,05
6 Air Raksa mg/L 0,001
7 Arsen mg/L 0,05
8 Selenium mg/L 0,01
9 Nitrat, sebagai N mg/L 10
10 Fluorida mg/L 1,5
11 Sianida mg/L 0,1
12 pH - 6,5 – 9
13 Nitrit, sebagai N mg/L 1,0
14 Klorida mg/L 600
15 Kromium, valensi 6 mg/L 0,05
16 Sulfat mg/L 400
17 Kesadahan (CaCO3) mg /L 500