PENERAPAN KONSEP TERMODINAMIKA PADA
MESIN PENDINGIN (KULKAS)
Diajukan untuk memenuhi tugas Fisika Dasar I, yang dibimbing
oleh : Rianita Puspa Sari, ST.
Disusun oleh
Yudi Susanto
1510631140144
JURUSAN TEKNIK INDUSTRI
FAKULTAS TEKNIK
ABSTRAK
Termodinamika adalah cabang fisika
yang mempelajari hubungan antara kalor dan
usaha mekanik. Secara luas termodinamika
mengkaji tentang suhu dan kalor serta teori
kinetik gas.
Konsep dasar termodinamika
dilaksanakan pada mesin-mesin yang dapat
membantu dan mempermudah pekerjaan
manusia.
Mesin yang bekerja sesuai dengan
perumusan Clausius (Hukum kedua
Termodinamika) adalah mesin pendingin
(refrigator). Dalam prakteknya, mesin
pendingin memakai energi listrik untuk
memindahkan kalor dari benda yang
didinginkan ke udara luar yang suhunya lebih
tinggi.
Di dalam makalah ini kita akan
membahas tentang kulkas yang merupakan
salah satu contoh mesin pendingin
(refrigator).
ABSTRACT
Thermodynamics is a branch of physics
that studies the relationship between heat and
mechanical effort. Extensively investigated
the thermodynamic temperature and the heat
and the kinetic theory of gases.
The basic concept of thermodynamics
carried out on machines that can assist and
facilitate the work of man.
Machines that work according to the
formulation Clausius (second law of
thermodynamics) is the engine coolant
(refrigator). In practice, the engine coolant
wearing electrical energy to move heat from
the cooled object to the outside air
temperature is higher.
In this paper we will discuss about the
refrigerator which is one example of engine
KATA PENGANTAR
Puji syukur kehadirat Tuhan Yang Maha Esa, karena berkat rahmat dan hidayah-Nya penulis
dapat menyelesaikan makalah yang berjudul Penerapan Termodinamika pada Mesin Pendingin
(Kulkas). Makalah ini di susun dalam rangka memenuhi tugas Fisika Dasar I.
Melalui kesempatan yang sangat berharga ini penulis menyampaikan ucapan terima kasih
kepada semua pihak yang telah membantu menyelesaikan tugas Fisika Dasar I ini, dan terutama
kepada yang terhormat :
1. Rianita Puspa Sari, ST. Selaku dosen dan pembimbing mata kuliah Fisika Dasar I.
2. Rekan-rekan jurusan Teknik Industri angkatan 2015.
3. Semua pihak yang telah memberikan bantuan baik berupa moral ataupun materil dalam
proses penyelesaian makalah ini.
Semoga Tuhan yang Maha Esa memberikan balasan yang setimpal atas segala bantuan yang
telah diberikan. Serta penulis berharap agar makalah ini dapat bermanfaat, khususnya bagi penulis
sendiri, umumnya bagi semua pihak.
Karawang, Januari 2016
DAFTAR ISI
2.5 Usaha dan Proses dalam Termodinamika ... 3
2.7 Hukum kedua Termodinamika ... 4
2.8 Koefisien Performansi ... 4
2.9 Entropi ... 4
2.10 Mesin Pendingin (Refrigator) ... 4
2.11 Kulkas ... 4
2.12 Penguraian Konsep Termodinamika ... 5
2.12.1 Klasifikasi Sistem Termodinamika ... 5
2.12.2 Proses-Proses dalam Termodinamika ... 6
2.12.3 Hukum Kedua Termodinamika ... 9
BAB III PEMBAHASAN ... 11
3.1 Penerapan Hukum kedua Termodinamika pada Kulkas... 11
3.2.1 Komponen-Komponen pada Kulkas ... 11
3.1.1 Prinsip Kerja pada Kulkas ... 14
BAB IV PENUTUP ... 16
4.1 Kesimpulan ... 16
4.2 Saran ... 16
DAFTAR GAMBAR
Gambar 2.12.1 Ilustrasi klasifikasi sistem termodinamika... 5
Gambar 2.12.2.1 Diagram Proses Isotermal ... 6
Gambar 2.12.2.2 Diagram Proses Isokhorik... 7
Gambar 2.12.2.3 Diagram Proses Isobarik ... 7
Gambar 2.12.2.4 Diagram Proses Adiabatik ... 8
Gambar 2.12.3 Ilustrasi Hukum kedua Termodinamika ... 9
Gambar 3.1 Kulkas ... 11
BAB I
PENDAHULUAN
1.1 Latar Belakang
Termodinamika (bahasa Yunani: thermos = 'panas' and dynamic = 'perubahan') adalah fisika energi , panas, kerja, entropidan kespontanan proses. Termodinamika berhubungan
dekat dengan mekanika statistik di mana hubungan termodinamika berasal.
Hukum termodinamika kebenarannya sangat umum, dan hukum-hukum ini tidak bergantung
kepada rincian dari interaksi atau sistem yang diteliti. Ini berarti mereka dapat diterapkan ke sistem
di mana seseorang tidak tahu apa pun kecuali perimbangan transfer energi dan wujud di antara
mereka dan lingkungan.
Hukum kedua termodinamika terkait dengan entropi. Tidak ada bunyi untuk hukum kedua
termodinamika yang ada hanyalah pernyataan kenyataan eksperimental yang dikeluarkan oleh
kelvin-plank dan clausius. Pernyataan clausius: tidak mungkin suatu sistem apapun bekerja
sedemikian rupa sehingga hasil satu-satunya adalah perpindahan energi sebagai panas dari sistem
dengan temperatur tertentu ke sistem dengan temperatur yang lebih tinggi. Pernyataan
kelvin-planck: tidak mungkin suatu sistem beroperasi dalam siklus termodinamika dan memberikan
sejumlah netto kerja kesekeliling sambil menerima energi panas dari satu reservoir termal.(sumber
Fundamentals of engineering thermodynamics (Moran J., Shapiro N.M. - 6th ed. - 2007 - Wiley)
Bab5). "total entropi dari suatu sistem termodinamika terisolasi cenderung untuk meningkat
seiring dengan meningkatnya waktu, mendekati nilai maksimumnya hal ini disebut dengan prinsip
kenaikan entropi" merupakan korolari dari kedua pernyataan diatas (analisis Hukum kedua
termodinamika untuk proses dengan menggunakan sifat entropi).
Di masa sekarang ini hukum kedua termodinamika banyak diterapkan di bidang teknologi,
khususnya pada mesin pendingin (refrigator), contohnya kulkas.
1.2 Rumusan Masalah
Dari latar belakang di atas maka masalah dapat di rumuskan sebagai berikut:
1. Apa yang dimaksud dengan Termodinamika ?
2. Bagaimana konsep Hukum kedua Termodinamika ?
1.3 Tujuan
1. Menjelaskan apa itu Termodinamika.
2. Menjelaskan Hukum kedua Termodinamika.
3. Menjelaskan dan menguraikan bagaimana Hukum kedua Termodinamika diterapkan
pada kulkas.
1.4 Manfaat
1. Sebagai sumber bacaan (referensi) bagi para akademisi yang sedang menjalani
pendidikan.
BAB II
LANDASAN TEORI
2.1 Termodinamika
Termodinamika adalah kajian tentang kalor (panas) yang berpindah. Dalam termodinamika
banyak membahas tentang sistem dan lingkungan. Kumpulan benda-benda yang sedang ditinjau
disebut sistem, sedangkan semua yang berada di sekeliling (diluar) sistem disebut lingkungan.
2.2 Kalor
Kalor adalah salah satu bentuk energi sama halnya dengan energi kimia, potensial maupun
kinetik. Kalor didefinisikan sebagai energi panas yang dimiliki oleh suatu zat.
2.3 Suhu
Kata suhu sering diartikan sebagai suatu besaran yang menyatakan derajatpanas atau
dinginnya suatu benda.
2.4 Energi
Dalam fisika, energi adalah properti fisika dari suatu objek, dapat
berpindah melalui interaksi fundamental, yang dapatdiubah bentuknya namun tak dapat diciptakan
maupun dimusnahkan. Joule adalah satuan SI untuk energi, diambil dari jumlah yang diberikan
pada suatu objek (melalui kerja mekanik) dengan memindahkannya sejauh 1 meter dengan gaya 1
newton.
2.5 Usaha dan Proses dalam Termodinamika
Dalam melakukan pengamatan mengenai aliran energi antara panas dan usaha dikenal dua
istilah yaitu sistem dan lingkungan. Kumpulan benda-benda yang sedang ditinjau disebut sistem,
sedangkan semua yang berada di sekeliling (di luar) sistem disebut lingkungan.Usaha yang
dilakukan oleh sistem (gas) terhadap lingkunganya bergantung pada proses proses–proses dalam
termodinamika, di antaranya proses isobarik, isokhorik, isotermik dan adiabatik.
2.6 Hukum Termodinamika
Hukum-hukum termodinamika pada prinsipnya menjelaskan peristiwa
telah menjadi salah satu hukum terpenting dalam fisika dan berbagai cabang ilmu lainnya yang
berhubungan dengan termodinamika. Hukum-hukum ini sering dikaitkan dengan konsep-konsep
yang jauh melampau hal-hal yang dinyatakan dalam kata-kata rumusannya.
2.7 Hukum kedua Termodinamika
Hukum II Termodinamika memberikan batasan-batasan terhadap perubahan energi yang
mungkin terjadi dengan beberapa perumusan.
1. Tidak mungkin membuat mesin yang bekerja dalam satu siklus, menerima kalor dari
sebuah reservoir dan mengubah seluruhnya menjadi energi atau usaha luas (Kelvin
Planck).
2. Tidak mungkin membuat mesin yang bekerja dalam suatu siklus mengambil kalor dari
sebuah reservoir rendah dan memberikan pada reservoir bersuhu tinggi tanpa memerlukan
usaha dari luar (Clausius).
3. Pada proses reversibel, total entropi semesta tidak berubah dan akan bertambah ketika
terjadi proses irreversibel (Clausius).
2.8 Koefisien Performansi
Koefisien performansi merupakan hasil bagi kalor Q2 yang dipindahkan dari reservoir dingin
dengan usaha W yang dibutuhkan untuk memindahkan kalor ini.
2.9 Entropi
Entropi adalah salah satu besaran termodinamika yang mengukur energi dalam sistem per
satuan temperatur yang tak dapat digunakan untuk melakukan usaha.
2.10 Mesin Pendingin (Refrigator)
Mesin pendingin merupakan peralatan yang prinsip kerjanya berkebalikan dengan mesin
kalor. Pada mesin pendingin terjadi aliran kalor dari reservoir bersuhu rendah ke reservoir bersuhu
tinggi dengan melakukan usaha pada sistem.
2.11 Kulkas
Kulkas atau lemari es atau lemari pendingin adalah sebuah alat rumah tangga listrik yang
2.12 Penguraian Konsep Termodinamika
Termodinamika adalah ilmu tentang energi, yang secara spesifik membahas tentang
hubungan antara energi panas dengan kerja. Seperti telah diketahui bahwa energi didalam alam
dapat terwujud dalam berbagai bentuk, selain energi panas dan kerja, yaitu energi kimia, energi
listrik, energi nuklir, energi gelombang elektromagnit, energi akibat gaya magnit, dan lain-lain .
Energi dapat berubah dari satu bentuk ke bentuk lain, baik secara alami maupun hasil
rekayasa tehnologi. Selain itu energi di alam semesta bersifat kekal, tidak dapat dibangkitkan atau
dihilangkan, yang terjadi adalah perubahan energi dari satu bentuk menjadi bentuk lain tanpa ada
pengurangan atau penambahan. Prinsip ini disebut sebagai prinsip konservasi atau kekekalan
energi. Prinsip thermodinamika tersebut sebenarnya telah terjadi secara alami dalam kehidupan
sehari-hari. Bumi setiap hari menerima energi gelombang elektromagnetik dari matahari, dan
dibumi energi tersebut berubah menjadi energi panas, energi angin, gelombang laut, proses
pertumbuhan berbagai tumbuh-tumbuhan dan banyak proses alam lainnya. Proses didalam diri
manusia juga merupakan proses konversi energi yang kompleks, dari input energi kimia dalam
maka nan menjadi energi gerak berupa segala kegiatan fisik manusia, dan energi yang sangat
bernilai yaitu energi pikiran kita. Dengan berkembangnya ilmu pengetahuan dan teknologi, maka
prinsip alamiah dalam berbagai proses thermodinamika direkayasa menjadi berbagai bentuk
mekanisme untuk membantu manusia dalam menjalankan kegiatannya.
2.12.1 Klasifikasi Sistem Termodinamika
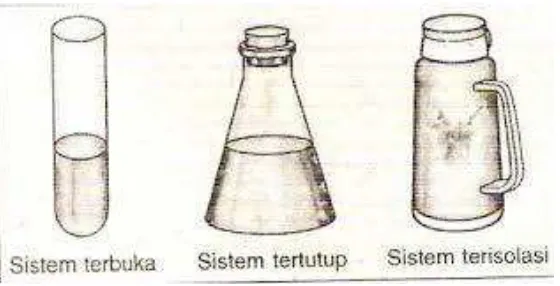
Gambar 2.12.1 Ilustrasi klasifikasi sistem termodinamika
Suatu sistem thermodinamika adalah sustu masa atau daerah yang dipilih, untuk
dijadikan obyek analisis. Daerah sekitar sistem tersebut disebut sebagai lingkungan. Batas
1. Sistem tertutup
Merupakan sistem massa tetap dan identitas batas sistem ditentukan oleh ruang zat
yang menempatinya.
2. Sistem terbuka
Pada sistem ini, zat melewati batas sistem. Panas dan kerja bisa juga melewati batas
sistem.
3. Sistem terisolasi
Adalah sebuah sistem yang sama sekali tidak dipengaruhi oleh lingkungannya.
Sistem ini massanya tetap dan tidak ada panas atau kerja yang melewati batas sistem.
2.12.2 Proses-Proses dalam Termodinamika
Terdapat empat proses dalam gas pada bahasan termodinamika. Usaha yang terdapat
pada gas yang mengalami proses-proses termodinamika tersebut akan diuraikan sebagai
berikut :
1. Proses isotermal
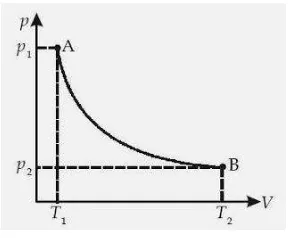
Gambar 2.12.2.1 Diagram Proses Isotermal
Proses isotermal adalah suatu proses perubahan keadaan gas pada suhu tetap.
Menurut Hukum Boyle, proses isotermal dapat dinyatakan dengan persamaan :
pV = konstan atau p1V1 = p2V2
Dalam proses ini, tekanan dan volume sistem berubah sehingga persamaan W = p ΔV tidak dapat langsung digunakan. Untuk menghitung usaha sistem dalam proses isotermal ini digunakan cara integral. Misalkan, pada sistem terjadi
Jika konstanta n R, dan besaran suhu (T) yang nilainya tetap dikeluarkan dari
integral, akan diperoleh :
W = nR T (lnV2 – lnV1) W = n RT ln (V2/V1) atau W = n RT ln (p2/p1)
2. Proses isokhorik
Gambar 2.12.2.2 Diagram Proses Isokhorik
Proses isokhorik adalah suatu proses perubahan keadaan gas pada volume tetap.
Menurut Hukum Gay-Lussac proses isokhorik pada gas dapat dinyatakan dengan
persamaan :
p/T = konstan atau p1/T1 = p2/T2
Oleh karena perubahan volume dalam proses isokhorik ΔV = 0 maka usahanya
W = 0.
3. Proses isobarik
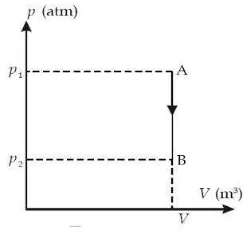
Gambar 2.12.2.3 Diagram Proses Isobarik
Proses isobarik adalah suatu proses perubahan keadaan gas pada tekanan tetap.
Menurut Hukum Charles, persamaan keadaan gas pada proses isobarik dinyatakan
V/T = konstan atau V1/T1 = V2/T2
Oleh karena volume sistem berubah, sedangkan tekanannya tetap, usaha yang
dilakukan oleh sistem dinyatakan dengan persamaan :
W = pΔV = p (V2– V1)
4. Proses Adiabatik
Proses adiabatik adalah suatu proses perubahan keadaan gas di mana tidak ada
kalor (Q) yang masuk atau keluar dari sistem (gas). Proses ini dapat dilakukan
dengan cara mengisolasi sistem menggunakan bahan yang tidak mudah
menghantarkan kalor atau disebut juga bahan adiabatik.
Adapun, bahan-bahan yang bersifat mudah menghantarkan kalor disebut bahan
diatermik Proses adiabatik ini mengikuti persamaan Poisson sebagai berikut :
p Vγ = konstan atau p1 V1γ = p2 V2γ (1–6)
Oleh karena persamaan gas ideal dinyatakan sebagai pV = nRT maka Persamaan (9–4) dapat ditulis :
T1V1(γ –1) = T2 V2(γ –1) (1–7)
Dengan γ = CP/CV = konstanta Laplace, dan CP/CV > 1. CP adalah kapasitas kalor gas pada tekanan tetap dan CV adalah kalor gas pada volume tetap.
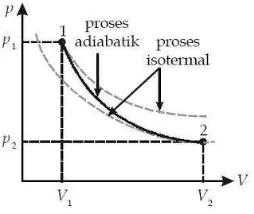
Gambar 2.12.2.4 Diagram Proses Adiabatik
Perhatikan diagram p – V pada Gambar di atas. Dari kurva hubungan p – V
tersebut, kita dapat mengetahui bahwa:
2. Suhu, tekanan, maupun volume pada proses adiabatik tidak tetap. Oleh karena
sistem tidak melepaskan atau menerima kalor, pada kalor sistem proses adiabatik
Q sama dengan nol.
Dengan demikian, usaha yang dilakukan oleh sistem hanya mengubah energi
dalam sistem tersebut. Besarnya usaha pada proses adiabatik tersebut dinyatakan
dengan persamaan berikut :
W= 3/2 nRT−T = 3/2 (p1 V1 − p2 V2) (1–8)
2.12.3 Hukum Kedua Termodinamika
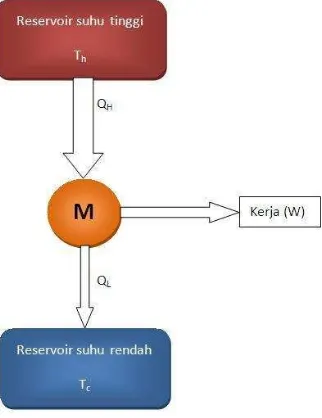
Gambar 2.12.3 Ilustrasi Hukum kedua Termodinamika
Ada dua perumusan untuk Hukum kedua Termodinamika, yaitu :
1. Rumusan Kelvin–Planck
Menyatakan bahwa tidak mungkin membuat mesin yang bekerja dalam
suatu siklus secara terus menerus, menerima kalor dari suatu reservoir dan
mengubah kalor tersebut seluruhnya menjadi usaha luar.
2. Rumusan Clausius
Menyatakan bahwa tidak mungkin membuat mesin yang bekerja menurut
satu siklus, mengambil kalor dari reservoir bersuhu rendah dan
memberikannya pada tandon bersuhu tinggi tanpa dilakukan kerja dari luar.
Hukum kedua termodinamika dirumuskan untuk menyatakan pembatasan-pembatasan
arah perubahan proses di alam. Dalam bentuknya yang paling umum, hukum kedua
termodinamika dirumuskan dengan mempergunakan suatu fungsi keadaan yang
disebut entropi.
Jika ∆ S as ialah perubahan entropi yangterjadi di alam semesta, maka bagi setiap
proses spontan berlaku, ∆S as > 0. Dengan memandang alam semesta itu sebagai sistem
dan lingkungan, maka dapat pula dikatakan bahwa untuk semua proses spontan berlaku, ∆S Sistem + ∆S lingkungan > 0 dengan∆S sistem ialah perubahan entropi sistem dan∆S lingkungan ialah perubahan entropi lingkungan.
Ukuran penampilan dari sebuah mesin pendingin disebut koefisien performansi (diberi
lambang Cp). Koefisien performansi merupakan hasil bagi kalor Q2 yang dipindahkan dari
reservoir dingin dengan usaha W yang dibutuhkan untuk memindahkan kalor ini. Sehingga
dapat dirumuskan sebagai berikut :
�� = ��
Dengan W = Q1 – Q2 sehingga :
�� = � − ��
Dengan gas ideal sebagai fluida kerja, persamaan tersebut menjadi :
BAB III
PEMBAHASAN
3.1 Penerapan Hukum kedua Termodinamika pada Kulkas
Gambar 3.1 Kulkas
Kulkas menjadi salah satu kebutuhan yang krusial bagi rumah tangga masyarakat Indonesia
di masa sekarang. Kulkas umumnya digunakan untuk menyimpan bahan makanan mentah,
sayur-sayuran, buah-buahan, minuman kaleng, dan es krim agar tidak membusuk, tahan lama, dan tetap
terjaga awet di dalam suhu yang telah dikondisikan.
3.2.1 Komponen-Komponen pada Kulkas
1. Kompresor
Kompresor merupakan bagian terpenting di dalam kulkas . Apabila di
analogikan dengan tubuh manusia, kompresor sama dengan jantung yang berfungsi
memompa darah ke seluruh tubuh begitu juga dengan kompresor. Kompresor
berfungsi memompa bahan pendingin keseluruh bagian kulkas .
· 2. Kondensor
Kondensor adalah alat penukar kalor untuk mengubah wujud gas bahan
pendingin pada suhu dan tekanan tinggi menjadi wujud cair. Jenis kondensor yang
banyak digunakan pada teknologi kulkas saat ini adalah kondensor dengan
sedang. kondensor seperti ini memiliki bentuk yang sederhana dan tidak
memerlukan perawatan khusus .saat lemari es bekerja kondensor akan terasa hangat
bila dipegang.
· 3. Filter
Filter (saringan) berguna menyaring kotoran yang mungkin terbawa aliran bahan
pendingin yang keluar setelah melakukan serkulasi agar tidak masuk kedalam
konpresor dan pipa kapiler. Selain itu , bahan pendingan yang akan disalurkan pada
proses berikutnya lebih bersih sehingga dapat menyerap kalor lebih maksimal.
· 3. Evaporator
Evaporator berfungsi menyerap panas dari benda yang di masukkan kedalam
kulkas, kemudian evaporator menguapkan bahan pendingin untuk melawan panas
dan mendinginkannya. Sesuai fungsinya evaporator adalah alat penguap bahan
pendingin agar efektif dalam menyerap panas dan menguapkan bahan pendingin,
evaporator di buat dari bahan logam anti karat, yaitu tembaga dan almunium.
· 4. Thermostat
Thermostat memiliki banyak sebutan antara lain temperatur kontrol dan cool
control. Apapun sebutannya, thermostat berfungsi mengatur kerja kompresor
secara otomatis bedasarkan batasan suhu pada setiap bagian kulkas. Bisa dikatakan,
thermostat adalah saklar otomatis berdasarkan pengaturan suhu. Jika suhau
evaperator sesuai dengan pengatur suhu thermostat, secara otomatis thermostat
akan memutuskan listrik ke kompresor.
· 4. Heater
Hampir keseluruan kulkas nofrost dan sebagian kecil kulkas defrost dilengkapi
dengan pemanas ( heater ). Pemanas berfungsi mencairkan bunga es yang terdapat
di evaporator . selain itu pemanas dapat mencegah terjadinya penimbunan bunga
es pada bagian rak es dan rak penyimpan buah di bawah rak es.
· 5. Fan motor
Fan motor atau kipas angin berguna untuk menghembuskan angin . pada kulkas
1. Fan motor evaporator
Berfungsi menghembuskan udara dingin dari evaporator keseluruh bagian
rak (rak es , sayur ,dan buah).
2. Fan motor kondensor
Kipas angin ini diletakkan pada bagian bawah kulkas yang memiliki
kondensor yang berukuran kecil yang berfungsi mengisap atau mendorong
udara melalui kondensor dan kompresor . selain itu berfungsi mendinginkan
kompresor.
· 6. Overload motor protector
Adalah komponen pengaman yang letaknya menyatu dengan terminal
kompresor. Cara kerjanya serupa dengan sekering yang dapat menyambung dan
memutus arus listrik. Alat ini dapat melindungi komponen kelistrikan dari
kerusakan arus akibat arus yang dihasilkan kompresor melebihi arus acuan normal.
· 7. Bahan pendingin (Refrigerant)
Refrigerant adalah zat yang mudah diubah wujudnya dari gas menjadi cair,
ataupun sebaliknya. Jenis bahan pendingin sangat beragam. Setiap jenis bahan
3.1.1 Prinsip Kerja pada Kulkas
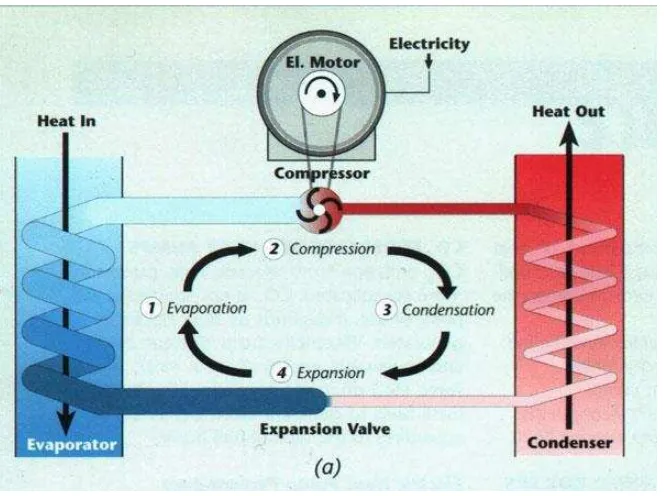
Gambar 3.1.1 Prinsip Kerja pada Kulkas
Kulkas adalah suatu unit mesin pendingin di pergunakan dalam rumah tangga, untuk
menyimpan bahan makanan atau minuman. Untuk menguapkan bahan pendingin di
perlukan panas.
Lemari es memanfaatkan sifat ini. Bahan pendingin yang digunakan sudah menguap
pada suhu -200C. panas yang diperlukan untuk penguapan ini diambil dari ruang
pendingin, karena itu suhu dalam ruangan ini akan turun. Penguapan berlangsung dalam
evaporator yang ditempatkan dalam ruang pendingin. Karena sirkulasi udara, ruang
pendingin ini akan menjadi dingin seluruhnya.
Lemari Es merupakan kebalikan mesin kalor. Lemari Es beroperasi untuk
mentransfer kalor keluar dari lingkungan yang sejuk kelingkungn yang hangat. Dengan
melakukan kerja W, kalor diambil dari daerah temperatur rendah TL (katakanlah, di dalam
lemari Es), dan kalor yang jumlahnya lebih besar dikeluarkan pada temperature tinggi
Th (ruangan).
Sistem lemari Es yang khas, motor kompresor memaksa gas pada temperatur tinggi
melalui penukar kalor (kondensor) di dinding luar lemari Es dimana Qh dikeluarkan dan
gas mendingin untuk menjadi cair. Cairan lewat dari daerah yang bertekanan tinggi ,
menguap pada tekanan yang lebih rendah ini dan kemudian menyerap kalor (QL) dari
bagian dalam lemari es. Fluida kembali ke kompresor dimana siklus dimulai kembali.
Lemari Es yang sempurna (yang tidak membutuhkan kerja untuk mengambil kalor
dari daerah temperatur rendah ke temperatur tinggi) tidak mungkina ada. Ini merupakan
pernyataan Clausius mengenai hukum Termodinamika kedua. Kalor tidak mengalir secara
spontan dari benda dingin ke benda panas. Dengan demikian tidak akan ada lemari Es yang sempurna.
Jadi kesimpulannya, kulkas menggunakan penerapan Hukum kedua Termodinamika,
dan bisa dikatakan kulkas menggunakan salah satu konsep Termodinamika.
1. Cara Kerja Instalasi Mesin Kulkas
Setelah ke dalam kompresor diisi gas freon , maka gas itu dapat dikeluarkan kembali
dari silinder oleh kompresor untuk diteruskan ke kondensor, setelah itu menuju saringan,
setelah itu menuju ke pipa kapiler dan akan mengalami penahanan. Adanya penahanan ini
akan menimbulkan suatu tekanan di dalam pipa kondensor. Sebagai akibatnya gas tersebut
menjadi cairan di dalam pipa kondensor. Dari pipa kapiler cairan tersebut terus ke
evaporator dan terus menguap untuk menyerap panas. Setelah menjadi gas terus dihisap
lagi ke kompresor. Demilian siklus kembali terulang.
2. Jenis Aliran Udara Pendingin
Jenis aliran udara pada lemari es ada 2 macam :
Secara alamiah tanpa fan motor, di dalam lemari es udara dingin pada bagian atas dekat evaporator mempunyai berat jenis lebih besar. Dari beratnya sendiri udara
dingin akan mengalir ke bagian bawah lemari es. Udara panas pada bagian bawah
lemari es karena berat jenisnya lebih kecil dan di desak oleh udara dingin dari atas,
akan mengalir naik ke atas menuju evaporator. Udara panas oleh evaporator
didinginkan menjadi dingin dan berat lalu mengalir ke bawah lagi. Demikianlah
terjadi terus menerus secara alamiah.
Aliran udara di dalam lemari es dengan di tiup oleh fan motor, lemari es yang memakai fan motor, dapat terjadi sirkulasi udara dingin yang kuat dan merata ke
semua bagian dari lemari es. Udara panas di dalam lemari es dihisap oleh fan
motor lalu dialirkan melalui evaporator. Udara menjadi dingin dan oleh fan motor
di dorong melalui saluran atau cerobong udara, di bagi merata ke semua bagian
BAB IV
PENUTUP
4.1 Kesimpulan
Berdasarkan pembahasan dan hasil penelitian di atas, dapat disimpulkan sebagai berikut :
1. Termodinamika adalah ilmu tentang energi, yang secara spesifik membahas tentang
hubungan antara energi panas dengan kerja.
2. Hukum-hukum termodinamika pada prinsipnya menjelaskan peristiwa
perpindahan panas dan kerja pada proses termodinamika.
3. Hukum kedua termodinamika terkait dengan entropi. Tidak ada bunyi untuk hukum
kedua termodinamika yang ada hanyalah pernyataan kenyataan eksperimental yang
dikeluarkan oleh kelvin-plank dan clausius.
4. Klasifikasi pada sistem dibagi 3, yaitu : sistem terbuka, sistem tertutum, dan sistem
terisolasi
5. Kulkas adalah salah satu contoh penerapan termodinamika di bidang teknologi
yang dapat kita temukan sehari-hari.
6. Prinsip kerja kulkas menerapkan hukum kedua termodinamika.
4.2 Saran
Berdasarkan pembahasan dan hasil penelitian di atas, penyusun menyarankan :
1. Karena pembahasan pada Termodinamika termasuk banyak, maka bagi para
akademisi yang sedang menjalani pendidikan dan ingin lebih tau banyak hal tentang
Termodinamika, haruslah bekerja keras dalam memahami konsep Termodinamika,
khususnya dalam penerapan di berbagai bidang.
2. Bagi pembimbing / pengajar ilmu fisika, makalah ini dapat diajarkan kepada pelajar
DAFTAR PUSTAKA
Wikipedia.org Prinsipkerja.com
Kamus Istilah-Istilah Fisika
Sears, Zemansky, 1985 “Fisika untuk Universitas”, terj Binacipta
Micheal E. Browne, “Theory and Problem of Physics for Engineering and Scince” Schaum’s
Outline Series
Foster, Bob. 2003 “Fisika Terpadu 2” Jakarta : Erlangga
Tim Fisika SMK Teknik. 2005 “ Fisika Tingkat 2” Jakarta : PT Galaxy Puspa Mega