56
Analisa Pemanfaatan Gas Produk dari Reaksi Steam Reforming Methanol pada Permukaan
Katalis Cu/ZnO/Al
2O
3Ahmad Rifqy Marully, Mikrajuddin Abdullah
yang Disintesis Menggunakan Metoda Simple Heating
(a)
Kelompok Keahlian Fisika Material Elektronik,
, dan Khairurrijal
Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Teknologi Bandung Jalan Ganesa 10, Bandung 40132, Indonesia;
(a)
E-mail: [email protected]
Diterima Editor : 23 Mei 2009
Diputuskan Publikasi : 30 Mei 2009
Abstrak
Telah disintesis tiga sampel katalis Cu/ZnO/Al2O3
Kata kunci : Steam Reforming Methanol, katalis Cu/ZnO/Al
dengan metoda simple heating. Semua katalis yang dihasilkan memiliki luas permukaan realtif lebih kecil dibandingkan dengan katalis serupa yang disintesis dengan metoda copresipitasi. Dengan kecilnya luas permukaan ini, aktifitas katalis pada reaksi Steam Reforming Methanol mejadi rendah. Rendahnya aktifitas katalis ini, justru menjadi keuntungan apabila gas produk dari reaksi tersebut dapat dijadikan bahan bakar untuk mesin motor bakar konvensional
2O3, Simple Heating, Copresipitasi
1. Pengantar
Nanokatalis Cu /ZnO/Al2O3 adalah s alah s atu katalis y ang da pat digunakan pada r eaksi Steam Reforming Methanol (SRM), sesuai dengan reaksi
3 ( ) 2 ( ) 2 2
o 1
CH OH H O CO 3H
Hr 50 kJ mol
g g
−
+ → +
∆ = (1) Gas hi drogen yang di hasilkan di peruntukkan sebagai
bahan ba kar untuk ke ndaraan be rbasis f uel cell. Reaksi tersebut b erlangsung di pe rmukaan ka talis pa da temperatur 3000
Hasil y ang di peroleh dengan m etoda i ni menunjukkan bahwa l uas pe rmukaan ka talis Cu/ZnO/Al
C [11]. Katalis ini dapat disintesis dengan metoda Impregnasi dan Co-presipitasi [7,4,10]. Namun,
Sintesis ka talis menggunakan ke dua m etoda tersebut membutuhkan satu sampai dua hari. Oleh karenanya, saat ini k ami m engembangkan metoda s intesis katalis y ang memerlukan w aktu lebih s ingkat da ri ke dua metoda sebelumnya, h anya dalam o rade j am. M etoda i ni k ami namakan simple heating. Diharapkan s ingkatnya wa ktu
sintesis da pat menurunkan bi aya pr oduksi pe mbuatan katalis.
2O3 yang dihasilkan memiliki luas permukaan yang relatif lebih kecil dibanding dengan kedua metoda sebelumnya, sesuai dengan hasil yang kami peroleh pada penelitian i ni. Ha l i nilah y ang m enjadi pe nyebab rendahnya konversi m ethanol ke hidrogen pa da temperatur dibawah 3000C. Karenanya, selain mensintesis katalis, ka mi j uga m elakukan s tudi u ntuk m elihat kemungkinan penggunaan katalis i ni pa da ke ndaraan motor bakar konvensional—bukan berbasis fuel cell.
2. Eksperimen
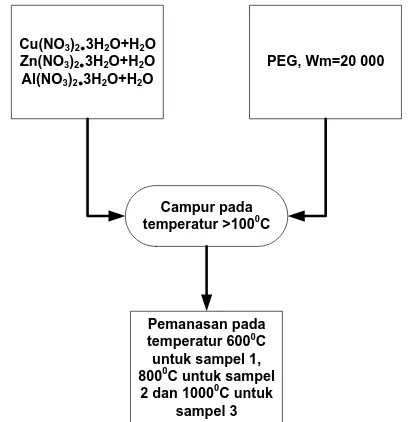
Tiga sampel dibuat de ngan k omposisi perbandingan mol C u : Zn : A l = 2 : 1 : 0,1. S etiap prekursor di campur dengan PEG dan aquades, kemudian dipanaskan hi ngga t emperatur 6000C u ntuk s ampel pertama, 8 000C unt uk s ampel ke dua dan 10000C unt uk sampel k e t iga. Secara u mum p rosedur s intesis diperlihatkan oleh Gambar 1.
Cu(NO3)2●3H2O+H2O Zn(NO3)2●3H2O+H2O Al(NO3)2●3H2O+H2O
PEG, Wm=20 000
Campur pada temperatur >1000C
Pemanasan pada temperatur 6000C untuk sampel 1, 8000C untuk sampel
2 dan 10000C untuk sampel 3
Hasil karakterisasi BET, diketahui luas permukaan spesifik u ntuk sampel pertama adalah 4,5294 m2/g, sampel kedua 1,2268 m2/g dan sampel ketiga 0,4008 m2/g. Sedangkan ukuran p ori u ntuk s ampel pe rtama a dalah 11,101 Å, s ampel ke dua 11,032 Å dan s ampel ketiga 10,917 Å.
Dari hasil BET ini, terlihat bahwa luas permukaan spesifik u ntuk s emua s ampel masih ja uh dibawah ha sil yang di peroleh Firmansyah[4] 43,2 m 2/g ( semua parameter p embuatan k atalisnya sama, h anya b erbeda metoda, Firmansyah menggunakan metoda copresipitasi).
Namun de mikian, w aktu y ang diperlukan pa da m etoda simple heating hanyalah 1,5 jam, jauh lebih singkat dari yang dibutuhkan oleh metoda copresipitasi (kurang lebih
2 hari).
Luas permukaan yang relatif kecil ini, menjadikan aktifitas k atalis j adi t idak s empurna, karennya hidrogen yang dihasilkan pa da reaksi S RM y ang menggunkan katalis ini tidaklah sebanyak yang dihasilkan oleh katalis yang sama dengan metoda copresipitasi pada temperatur reasi yang sama. S ehingga, g as produk dari r eaksi S RM masih mengandung methanol dan air yang tidak bereaksi. Masalah i ni j ustru a kan m enjadi keunggulan jika gas produk dari r eaksi S RM da pat diaplikasikan pada mesin motor bakar konvensional.
3. Gas Produk SRM pada Motor Bakar
Pengaplikasian gas hidrogen (100% hidrogen) pada mesin m otor bakar konvensional t ersandung m asalah
backfiring dan preignition. Back firing adalah ke luarnya
api d ari intake manifold. Hal i ni di karenakan hidrogen
yang m asuk ke da lam r uang ba kar t elah t erlebih da hulu terbakar oleh busi sebelum katup intake manifold tertutup.
Sedangkan pre ignition adalah terbakarnya hidrogen
karena hot spot (dari karbon) da lam ruang ba kar.
Sehingga hi drogen t erbakar sebelum busi menyala.
Ditambah lagi karena temperatur pembakaran yang tinggi pada r uang b akar, pembakaran (oksidasi) hidrogen da n udara (O2 + N2) akan memperbanyak k adar N Ox pada gas b uang. Di s isi l ain, k arena densitas energi g as hidrogen y ang ke cil, m aka pembakaran a kan c enderung stabil pada k ondisi lean operation dan vol ume tangki
penyimpanan bahan bakar akan membesar. Semua inilah masalah-masalah y ang di hadapai ketika gas hi drogen di aplikasikan pada motor bakar konvensional.
Namun k arena ya ng d iinginkan a dalah pengaplikasian g as pr oduk da ri r eaksi S RM ya ng tid ak sempurna ( masih m engandung a ir dan m ethanol y ang tidak bereaksi
p Q• =m c• ∆T
), maka permasalahan yang muncul, seperi
pre-ignition dan back firing, ada kemungkinan berkurang.
Selain i tu, k alor yang terbuang pa da motor ba kar konvensional da pat digunakan untuk r eaksi S RM, sehingga efisiensinya meningkat.
Banyaknya kalor tersedia pada saluran gas buang, yang dapat digunakan untuk reaksi SRM, dapat dihitung menggunakan persamaan
(2) Dengan Q• adalah laju perpindahan kalor dari gas buang,
dan
∆
T
adalah pe rbedaan t emperatur a ntara t emperatur di s istem da n di l ingkungan. Sedangkan m• adalah l ajumasa f luida (dalam h al i ni; laju ga s buang) da lam pipa pembuangan. m• didefinisikan oleh persamaan
m
m• =ρU Aτ (3)
Dengan ρ adalah m asa j enis g as b uang, dan Umserta Aτadalah kecepatan rata-rata fluida dan luas frontal dari
aliran fluida. Untuk mencari Um digunakan hubungan
Re m m
ρ adalah masa jenis fluida / gas buang (kg/m³)
µadalah viskositas dinamik dari fluida (Pa·s or N·s/m²) νadalah viskositas kinetik dari fluida (m²/s)
Red adalah bilangan Reynolds yang menyatakan apakah a liran s uatu fluida i tu l aminar a tau t urbulen. Apabila Re d > 230 0, maka a liran s uatu f luida dikategorikan beraliran turbulen.
besarnya ka lor y ang b isa di manfaatkan untuk memanaskan katalis.
Dengan kalor sebesar ini, sesuai dengan persamaan (1), maka hidrogen yang bisa dihasilkan adalah 0,03 mol / s a tau 0 ,6 l iter/s p ada k eadaan STP. N ilai i ni setara dengan ni lai heating value bahan bakar yang di perlukan
untuk menjalankan motor bebek 10 Hp.
Salah satu alasan menggunakan h idrogen sebagai bahan ba kar adalah ka rena ni lai energi pembakarannya (Heating Value) ny a y ang t inggi, dibandingkan d engan
bahan bakar yang lain. Seperti diperlihatkan oleh Tabel 1 Tabel 1. Komparasi HHV dan LHV berbagai bahan bakar
Fuel Higher Heating energi y ang paling t inggi. Steam Reforming Methanol
yang m enghasilkan ga s hidrogen, dengan de mikian, memiliki ke unggulan dari p ada m enggunakan m ethanol langsung u ntuk dibakar. Dengan m engubahnya m enjadi hidrogen, m aka t erjadi pe ningkatan e nergi ba han bakar, sehingga terjadi juga peningkatan efisiensi termal, dalam hal i ni t erjadi heat recovery untuk m enaikkan he ating
value ba han bakar [ 13]. Diperkenalkanlah d erajat kenaikan heating value
Sehingga, keseluruhan efisiensi termal untuk motor bakar torak adalah
keseluruahan i r
η =ηη (6)
Selain karena tingginya heating value dari hidrogen, masalah y ang di hadapi a dalah de nsitas hidrogen y ang sangat ke cil d ibandingkan dengan ba han ba kar lainnya. Karena s ifat i ni, hidrogen s ulit be roperasi pa da rich operation dalam motor ba kar. Y ang t entunya a kan
menurunkan power output dari mesin. Selain itu, densitas
hidrogen y ang ke cil a kan menyulitkan menyimpanannya dalam kendaraan, dibandingkan dengan bahan bakar cair lainnya. Kecilnya de nsitas hidrogen i ni, a kan s ecara langsung a kan m enurunkan pula energi densitas nya
Sebagai pe rbandingan, di butuhkan s etidaknya 8 000 l iter hidrogen pa da t ekanan 3600 p si u ntuk menghasilkan pembakaran y ang s etara dengan 500 l iter s olar. P ada Tabel 2 diperlihatkan komparasi berbagai energi desnisity bahan bakar
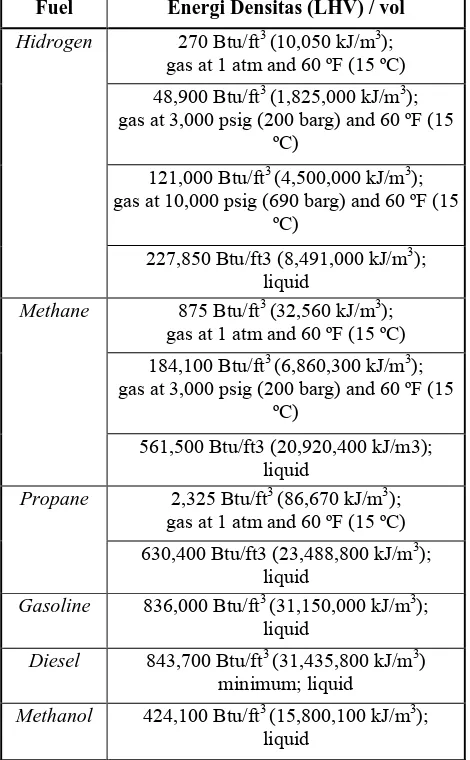
Tabel 2. Perbandingan energi densitas dari berbagai bahan bakar
Fuel Energi Densitas (LHV) / vol
Hidrogen 270 Btu/ft3 (10,050 kJ/m3);
227,850 Btu/ft3 (8,491,000 kJ/m3); liquid 630,400 Btu/ft3 (23,488,800 kJ/m3);
liquid
Oleh ka rena i tulah di butuhkan reaktor h idrogen yang portabel agar nantinya tidak dibutuhkan lagi tangki hidrogen bertekan u ntuk m enyimpan hidrogen. C ukup dengan m enyimpan c ampuran m etanol a ir dalm t angki bahan ba kar. Inilah ke lebihan da ri penggunaan reaktor SRM dalam kendaraan.
Dengan a danya C O dan ua p m etanol (yang tid ak bereaksi) da pat ju ga m empengaruhi e fisiensi m esin. Ha l ini d isebabkan, walaupun tid ak banyak hid rogen ya ng masuk ke r uang bakar ( karena de nsitas energi n ya yang kecil), adanya C O dan uap m etanol a kan mengkompensasi kekurangan i ni. Mengingat metanol memiliki densitas e nergi yang lebih tinggi daripada hidrogen.
Selain d ari s isi energi dan densitasnya, s ifat-sifat pembakaran hidrogen juga harus dianalisis. Sifat hidrogen yang m emiliki flammability limit yang l uas m enjadikan
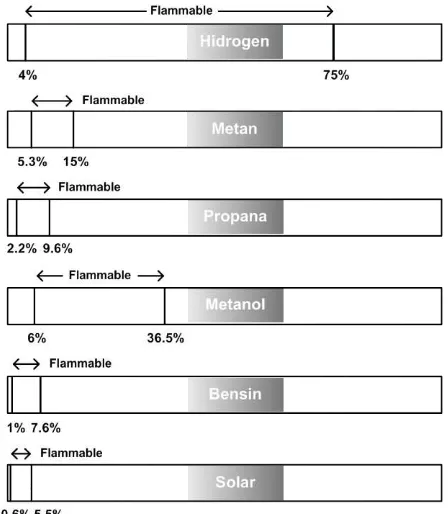
luas. sehingga dengan sedikit saja hidrogen, motor bakar sudah mulai dapat di nyalakan. P ada G ambar 2 di perlihatkan perbandingan flammability limit dari berbagai
bahan bakar.
Gambar 2. P erbandingan flammability limit berbagai
bahan bakar
Luasnya flammability limit ini, menjadikan
dimungkinkan pe ningkatan pe rbandingan k ompresi. Dengan m eninggkatnya pe rbandingan k ompresi, maka sesuai dengan nilai efisiensi teoretik mesin Otto 4 langkah
(8) dengan
r adalah perbandingan kompresi yang didefinisikan oleh
VL = volume langkah torak, cm3 VS = volume sisa , cm3
efisiensi teoretik akan meningkat pula. Selain itu, octan number dari hidrogen juga s angat t inggi di bandingkan
dengan bahan ba kar l ainnya, s eperti ditunjukkan ol eh Tabel 3. Tingginya nilai oktan da ri hidrogen, akan memperkecil kemungkinan terjadinya detonasi.
Selain s emua k elebihan t ersebut,kelemahan pembakaran hidrogen disebabkan oleh flame speed yang
tinggi, quencing distance yang ke cil s erta r endahnya
ignition energy. sifat-sifat inilah yang meningkatkan
terjadinya preignition dan back firing. I nilah masalah
terbesar y ang di hadapi oleh m otor bakar a pabila diaplikasikan hidrogen.
Tabel 3. Perbandingan Oc tane number da ri be rbagai bahan bakar
fuel Octane Number Hidrogen 130+
(lean burn)
Methane 125
Propane 105
Octane 100
Gasoline 87
Diesel 30
Namun, karena ki ta t idak m empergunakan hi drogen murni s ebagai ba han bakar, m elainkan gas ha sil r eaksi SRM, maka k ekurangan t erebut d apat diminimalisir. Adanya uap a ir ( yang t idak bereaksi) a kan m enurunkan temperatur ruang ba kar, s ehingga da pat m engurangai kemungkinan t erjadinya preignition. Hal i ni t erjadi
lantaran hot s pot y ang a da dalam r uang bakar m enurun temperaturnya. Dan karena uap air ini akan menurunkan temperatur pembakaran maksimal, maka kadar NOx akan menurun pula.
4. Kesimpulan
Dengan kecilnya l uas pe rmukaan katalis y ang disintesis de ngan metoda simple heating, m enjadikan reaksi S RM t idak s empurna p ada t emperatur 3000
[1] M. Adullah, I.W. Lenggoro, B. Xia, and K. Okuyama. J. Ceram. Soc. Jpn. 113, 97 (2005)
C. Namun, j ustru karena ke tidaksempurnaan r eaksi ini, ga s produk da ri r eaksi S RM dimungkinkan u ntuk diaplikasikan pada kendaraan motor bakar konvensional. Masalah-masalah y ang t imbul ke tika hi drogen dijadikan bahan ba kar ke ndaraan motor ba kar, akan tereduksi dengan adanya gas CO dan campuran methanol air yang tidak bereaksi.
Referensi
[2] M. Ad ullah, I. W L enggoro, B . Xia, K .Taya, a nd K.Okuyama, J. Non-Crystalline S olids. 351, 697 (2005)
[3] M. Abdullah and K. Okuyama.Proc. ITB En g. Sci. 36 B ,(2004)
[4] D. Firmansyah, Tesis Magister, I nstitut T eknologi Bandung(2006)
[5] J.H. Hirschenhofer, D .B. Stauffer, a nd R .R. Engleman, Fuel Cell Handbook, Fourth Edition. U.S
Department of Energi(1998)
[6] E.S. Janitra dan S .B.G. Sianturi, T ugas K uliah T K-40Z1. (2006)
[8] P. Reuse, A. Renken, K. Haas-Santo, O. Görke, and K. Schubert, Chem. Eng. J. 101, 133 (2004)
[9] J. T. Richardson, Principles of Catalyst Development,
New York: Plennum Press (1989).
[10]M.V. Twigg, Catalyst Handbook, London: Manson
Publishing (1997)
[11]V. Agarwal et al. Appl. Catal. 279, 155 (2005). [12]Collage of D esert, Modu le 3 : Hydrogen Use in
Internal Combustion Engine, Desember (2001).
[13]T. Shudo, Int. J. Veh. Design 41, 206 (2006). [14]A. D. Putra, Tugas Akhir Jurusan Teknik Mesin ITB
(2007)
[15]Collage o f D esert, M odule 1: Hydrogen Properties,