BAB II
TINJAUAN PUSTAKA
2.1 PLASTIK
Produksi utama pembuatan plastik selama ini berbasis bahan baku turunan minyak bumi [9]. Plastik adalah bahan sintestis atau alami yang terdiri dari rantai panjang dengan komponen utama C atau karbon [8]. Ikatan ini sangat kuat sehingga material plastik cocok untuk digunakan dalam berbagai aplikasi [2].
Plastik merupakan bahan yang murah, tahan lama, serbaguna, dan sangat disukai sebagai material bahan baku pembuatan produk. Plastik mempunyai bobot ringan, kuat, tahan bahan kimia, dan mudah dalam pemasaran. Komoditas plastik terbesar didunia adalah polipropilen, diikuti oleh PVC dan HDPE [10]. Plastik dapat dibagi dalam dua klasifikasi, yaitu material termoplastik dan material termoset. Proses pembentukan plastik diakhiri oleh reaksi curing, yaitu reaksi ikatan sambung silang (cross – linking) yang irreversible dari polimer. Perbedaan termoplastik dimana termoplastik dapat diproses dengan panas, ketika material diberi panas, material termoplastik akan mencair dimana material tersebut dapat dibentuk menjadi produk yang diinginkan. Setelah didinginkan material akan mengeras dan mempertahankan bentuknya. Material termoplastik dapat diproses ulang dengan pemanasan dan pembentukan atau pencetakan. Berbeda dengan material termoset yang tidak dapat diproses dengan pemanasan berulang kali atau dengan kata lain mempunyai bentuk yang permanen setelah pemrosesan [11]. Contoh plastik termoplastik adalah polietilen, polipropilen, nilon, polikarbonat, dll, yang contoh aplikasinya seperti ember polietilen, cangkir polistiren, tali nilon, dll. Contoh plastik termoset adalah fenol formaldehid, urea formaldehid, melamin Formaldehid, termosetting poliester, dll, yang contoh aplikasinya seperti : switch listrik, meja sermica, melamin Cutlery [12].
2.1.1 Pembuatan Plastik
Polimerisasi katalitik atau inisiasi peroksida dari monomer seperti etilena,
propilena, atau butadiena ditambah dengan stirena (kopolimer).
Polikondensasi dari monomer yang tidak sama seperti asam organik bifungsional dan alkohol atau amina.
Poliadisi dari molekul monomer yang reaktif
Sebelum suatu monomer dikonversi menjadi suatu plastik, biasanya ditambah dengan bahan – bahan aditif untuk meningkatkan kemudahan pemrosesan dan sifat mekanis sesuai dengan fungsi dan pemakaian plastik tersebut (pemakaian luar ruangan, terpapar sinar matahari, dll). Beberapa bahan aditif yang ditambahkan biasanya adalah [8] :
Antioksidan (1%)
Stabilizer panas dan cahaya (5%)
Plastisizer (40%)
Penguat resistan terhadap impak (10%)
Pigmen atau pewarna (5%)
Ketahanan api (15%)
Pelumas atau Agent foaming (2%)
Bahan pengisi (40%)
Plastik dapat digolongkan dalam beberapa basis kriteria [8] :
Komposisi kimia, berhubungan dengan monomer dan metode
polimerisasi, plastik dapat digolongkan menjadi poliolefin, vinyl polymers, styrenics, polyamides, polyesters, epoxy resins, polycarbonates, polyurethanes, dll.
Struktur kimia, misalnya rantai linear (High Density Polyethylene), rantai
bercabang (Low Density Polyethylene), ikatan sambung silang (Termosers, karet).
Kekakuan, elastis, fleksibel, atau rigid / keras / kaku.
Tipe pengaplikasian, pemakaian umum atau pemakaian khusus.
Metode pemrosesan, injection molding, extrusion, film blowing, blow
molding, thermforming, casting, calendaring, dan sebagainya
titik lebur (Tm), temperatur transisi (Tg) dan temperatur dekomposisi. Temperatur transisi adalah temperatur ketika plastik mengalami perengganan struktur sehingga terjadi perubahan dari kondisi kaku menjadi lebih fleksibel. Di atas titik lebur, plastik mengalami pembesaran volume sehingga molekul bergerak lebih bebas yang ditandai dengan peningkatan kelenturannya. Temperatur lebur adalah temperatur di mana plastik mulai melunak dan berubah menjadi cair. Temperatur dekomposisi merupakan batasan dari proses pencairan. Jika suhu dinaikkan di atas temperatur lebur, plastik akan mudah mengalir dan struktur akan mengalami dekomposisi. Dekomposisi terjadi karena energi termal melampaui energi yang mengikat rantai molekul. Secara umum polimer akan mengalami dekomposisi pada suhu di atas 1,5 kali dari temperatur transisinya. Data sifat termal yang penting pada proses daur ulang plastik bisa dilihat pada Tabel 2.1.
Tabel 2.1 Data Temperatur Transisi dan Temperatur Lebur Plastik [13]
Jenis Bahan Tm (°C) Tg (°C ) Temperatur Kerja
Tabel 2.2 Konsumsi Plastik Per kapita Beberapa Negara di Dunia [12] Negara Konsumsi Per kapita dalam kg
India (1998) 1,6
Beberapa jenis plastik dapat didaur ulang. Hal ini dapat dilihat dari simbol yang terdapat pada produk plastik. Tabel 2.3 menunjukkan berbagai jenis limbah plastik dengan tanda standar daur ulangnya agar dapat diidentifikasi dengan mudah pada pengaplikasiannya.
Tabel 2.3 Jenis-jenis Limbah Plastik dan Tanda Daur Ulang [15] Lambang Daur Ulang Singkatan Deskripsi
Ya PET Polietilen tereftalat Aplikasi : Botol Minuman
Ya HDPE
High-Density Polyethylene
Aplikasi : Susu, deterjen & minyak botol, mainan, wadah penggunaan luar, komponen dan kantong plastik
Ya V/PVC
Vinyl / Polyvinyl khlorida
Aplikasi : Pembungkus makanan,
Tabel 2.3 Jenis-jenis Limbah Plastik dan Tanda Daur Ulang [15] (Lanjutan) Lambang Daur Ulang Singkatan Deskripsi
Ya, tapi tidak umum PS
Polistirena
Aplikasi : pengepakan daging, pelindung packing.
Beberapa
Polimer lainnya.
Biasanya yang berlapis atau campuran
Pada daur ulang plastik dengan metode pirolisis, poliolefin (PE, PP, PS) memberikan hasil distilat terbaik karena memiliki rantai lurus dari struktur hidrokarbon. Polietilen dan polipropilen merupakan bahan yang paling bagus untuk dijadikan bahan bakar sedangkan polietilen tereftalat yang paling tidak cocok seperti yang dapat dilihat pada Tabel 2.4.
Tabel 2.4 Pemilihan Plastik [16]
Jenis Polimer Kecocokan Sistem Bahan Bakar
Polietilen (PE) Sangat Baik
Polipropilen (PP) Sangat Baik
Polistiren (PS) Sangat Baik (Menghasilkan Minyak yang baik)
Resin ABS (ABS) Baik
Polyvinylclorida (PVC) Tidak cocok, harus dihindari Poliuretan (PUR) Tidak cocok, harus dihindari Polietilen Tereftalat (PET) Tidak cocok, harus dihindari
2.1.3 Plastik Jenis Propilena (PP)
Tabel 2.5 Sifat Umum Polipropilena [11] Ekspansi linear termal (mm/mm K) 3,8 x 10-5
Kekerasan (Shore) D76
Resistivitas volume (Ω.cm) 1,0 x 1017
Linear mold shrinkage (in./in.) 0,01 – 0,02
Penggunaan polipropilen kebanyakan pada kemasan minuman, komponen otomotif, perlengkapan rumah tangga, dan mainan. Polipropilen dapat diekstrusi menjadi bentuk serat atau kawat untuk penggunaan pengikat pada karpet [11]. Limbah plastik yang terbuat dari polipropilen (PP) mengandung 85% karbon dan sisanya adalah hidrogen, hal ini membuat material ini sangat cocok untuk didaur ulang menjadi produk hidrokarbon yang berguna seperti bahan bakar. Polipropilen (PP) membutuhkan energi aktivasi yang lebih rendah untuk memecah ikatan C – H daripada polietilen (PE) karna rantai karbon polimer PP terdiri dari atom karbon tersier yang kurang tahan terhadap degradasi [18]
2.2 SILIKA
Silika adalah hasil polimerisasi asam silikat, yang mana dapat berstruktur kristalin maupun amorf. Silika tersusun dari rantai satuan SiO4 tetrahedral dengan
formula umum SiO2. Senyawa silika yang terdapat dialam dapat ditemukan di
beberapa bahan alam seperti pasir, kuarsa, gelas, dan sebagainya. Silika yang terdapat dialam mempunyai struktur kristalin, sedangkan silika sintetis berstruktur amorf. secara sintetis senyawa silika dapat dibuat dari larutan silikat atau dari pereaksi silan [19]. Silika yang terakumulasi didalam makhluk hidup, baik hewan atau tumbuhan memiliki bentuk amorf, berbeda dengan silika yang tidak berasal dari makhluk hidup seperti batuan dan debu yang memiliki struktur silika kristalin [20].
komponen katalis. Silika juga dapat digunakan sebagai kristal piezoelectric, elemen optical, dan bahan pecah belah. Silika adalah material dasar bahan – bahan gelas, keramik, dan industri bahan – bahan tahan api [21].
2.2.1 Silika Kristalin
Silika kristalin memiliki banyak bentuk, bergantung dari orientasi dan posisi dari tetrahedron yang dibentuk meskipun memiliki struktur kimia yang sama. Tiga bentuk umum silika kristalin adalah kuarsa, tridimit, dan kristobalit. Pada tekanan atmosferik siika kuarsa terbentuk pada temperatur 870 °C, tridimit terbentuk pada temperatur 870 – 1470 °C, sementara kristobalit terbentuk pada 1470 °C. Struktur dari silika bergantung pada temperatur dan tekanan terbentuknya atau pada kasus tertentu kecepatan pendinginan sehingga padatan silika membentuk struktur yang berbeda.
Gambar 2.1 Struktur Kristalin dari Sebuah Kristal Silika Tunggal [20]
Struktur sederhana dari silika kristalin dapat dilihat pada Gambar 2.1. Si adalah kristal berbentuk diamond yang terdiri dari empat atom yang diposisikan pada sudut bangun tetrahedron, yang berikatan secara kovalen dengan Si yang berada di pusat [20].
2.2.2 Silika Amorf
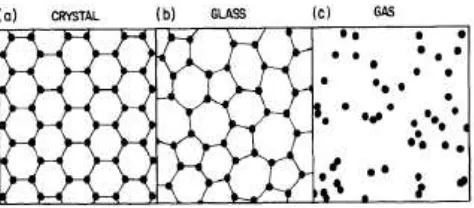
Gambar 2.2 Sketsa Skema Susunan Atom dalam (a) Padatan Kristalin, (b) Padatan Amorf, dan (c) Gas [20]
Baik silika kristalin maupun non kristalin banyak ditemukan dialam seperti di tanah, batu – batuan, dan pasir. Kedua bentuk silika ini banyak dimanfaatkan dalam indutri kaca, bangunan, dan elektronik. Silika amorf biasanya terdapat dalam makhluk hidup seperti diatom, radiolarian, silicoflagellata, dan beberapa sponges. Silika non kristalin atau amorf memiliki susunan atom dan molekul berbentuk pola acak dan tidak beraturan. Akibat pola acak dan tidak beraturan tersebut, silika amorf memiliki struktur spherikal yang rumit. Struktur rumit tersebut menyebabkan luas permukaan yang tinggi, biasanya diatas 3m2/g [21].
Silika amorf dalam berbagai kondisi dianggap lebih reaktif dibandingkan silika kristalin. Tingkat kereaktifan dari silika amorf disebabkan karena adanya gugus hidroksil (silanol) yang didapat setelah pemanasan mencapai temperatur 400°C. Gugus silanol (-SiOH) ini dapat ditemukan diatas permukaan dari sampel silika yang menyebabkan terbentuknya daerah yang reaktif.
Silika amorf dapat dibuat menjadi berbagai macam produk komersil. Berbagai cara memproduksinya dan cara partikelnya membentuk agregat, silika amorf dapat dibuat menjadi silika sol, silika gel, silika endapan, dan silika pirogenik. Silika amorf telah diklasifikasi sebagai material tidak beracun [20].
2.2.3 Sifat – Sifat Reaksi Silika
oleh hidrogen, karbon, dan beberapa elemen metal. Gas silikon monoksida juga terbentuk pada tekanan > 40 Mpa (400 atm) [21]. Tabel 2.6 menunjukkan produk yang terbentuk apabila silika bereaksi dengan komponen halogen.
Tabel 2.6 Reaksi Komponen Halogen dan Silika [21]
Komponen Halogen Produk
HF SiF4
FNO SiF4, N2O3
SeOF2 SiF4, SeO2
BrF3 SiF4, O2, Br2
BF3 SiF4 (BOF)3 ,SiF4, Siklo (SiOF2),
B2OF4
CF3CF3 SiF4, CO, CO2
2.2.4 Silika Gel
Silika gel adalah senyawa silika sintetis yang berstruktur amorf. Silika gel merupakan bahan kimia berbentuk padatan yang banyak dimanfaatkan sebagai adsorben. Hal ini disebabkan oleh mudahnya produksi dan juga mempunyai beberapa kelebihan yang lain yaitu, sangat bersifat inert, hidrofilik, mempunyai kestabilan termal dan mekanik yang tinggi, serta relatif tidak mengembang dalam pelarut organik jika dibandingkan dengan padatan resin polimer organik. Silika gel merupakan silika amorf yang terdiri atas globula – globula SiO4 tetrahedral yang
tersusun secara tidak teratur dan beragregasi membentuk kerangka tiga dimensi yang lebih besar. Rumus kimia silika gel secara umum adalah SiO2.xH2O. Struktur
satuan mineral silika pada dasarnya mengandung kation Si4+ yng terkoordinasi secara tetrahedral dengan anion O-2. Namun demikian, struktur dan susunan
tetrahedral SiO4 pada silika gel tidak beraturan seperti yang terlihat pada gambar
2.3 [19].
Sifat silika gel ditentukan oleh orientasi dari ujung tempat gugus hidroksil berkombinasi. Oleh karena ketidak-teraturan susunan permukaan SiO4 tetrahedral,
maka jumlah distribusinya per unit area bukan menjadi ukuran kemampuan adsorpsi silika gel, meskipun gugus silanol dan siloksan terdapat pada permukaan silika gel. Kemampuan adsorpsi ternyata tidak sebanding dengan jumlah gugus silanol dan gugus siloksan yang ada pada permukaan silika gel, tetapi tergantung pada distribusi gugus OH per unit area adsorben.
Pada permukaan silika gel terdapat dua jenis gugus, yaitu gugus silanol dan gugus siloksan. Gugus siloksan ada dua macam, yaitu Si-O-Si rantai lurus dan gugus siloksan yang membentuk struktur lingkar dengan empat anggota. Jenis yang pertama tidak reaktif dengan pereaksi pada umumnya, tetapi sangat reaktif terhadap senyawa logam alkali. Jenis gugus siloksan yang membentuk lingkar dengan empat anggota mempunyai reaktivitas yang tinggi, dapat mengadakan kemisorpsi dengan air, amoniak dan metanol. Reaksi dengan air akan menghasilkan dua gugus Si-OH, reaksi dengan amoniak akan menghasilkan gugus Si-NH2 dan silanol , sedangkan
reaksi dengan metanol akan menghasilkan gugus silanol dan Si–O-CH3. Ada
beberapa jenis gugus silanol, yaitu gugus silanol tunggal terisolasi, gugus silanol yang berdekatan satu sama lain dan dua gugus silanol yang terikat pada satu atom Si [19].
2.3 PROSES PIROLISIS
[4]. Pirolisis merupakan suatu alternatif untuk memperoleh energi dari limbah plastik. Hal ini menggunakan prinsip dimana kebanyakan substansi organik secara termal tidak stabil sehingga rantainya dapat pecah pada keadaan bebas oksigen [7]. Oleh karena itu, konversi limbah plastik menjadi bahan bakar memiliki beberapa keuntungan, yaitu [2] :
1. Membentuk siklus pemakaian energi tidak terbarukan.
2. Dapat menjadi sumber petrokimia alternatif untuk menurunkan pembelian atau pemakaian energi tidak terbarukan.
3. Solusi alternatif yang efektif untuk mengurangi limbah plastik yang berakibat tercegahnya pencemaran lingkungan yang biasanya ditimbulkan oleh cara pengolahan insinerasi dan landfill.
2.3.1 Thermal Cracking / Thermal Degradation
Degradasi secara termal adalah suatu proses sederhana dimana pada temperatur tinggi polimer mencair dan pecah menjadi molekul yang lebih kecil. Akan tetapi produk yang dihasilkan berkualitas rendah [8]. Thermal cracking pada hal ini adalah dalam artian tidak menggunakan katalis. Thermal cracking dari polietilena dan polipropilena biasanya dilakukan pada temperatur tinggi (>700 °C), untuk memproduksi campuran olefin (C1– C4) dan kompenen aromatis (terutama
benzen, toluen, dan xylen) atau pada temperatur rendah (400 – 500 °C) dimana tiga fraksi dihasilkan yaitu gas bernilai kalor tinggi, minyak hidrokarbon terkondensasi, dan lilin (waxes). Cracking pada suhu rendah menghasilkan produk yang agak keras
(waxy) didalam reaktor yang mana terdiri dari parafin dengan char karbon. Fraksi cair mempunyai komponen utama olefin linear dan parafin C11– C14 atom karbon. Thermal Cracking dari poliolefin berlangsung melalui mekanisme pemotongan acak pada empat langkah: inisiasi, propagasi, inter- atau intra- molekular transfer hidrogen diikuti dengan pemotongan – β dan terminasi. Secara umum, thermal cracking menggunakan energi dalam jumlah besar [22].
2.3.2 Catalytic Cracking
Waktu Reaksi (menit) Penggunaan katalis pada metode cracking akan menghasilkan reaksi pada suhu yang lebih rendah, sehingga akan menurunkan jumlah penggunaan energi [22]. Penambahan katalis juga bertujuan untuk meningkatkan yield produk cair dan memperbaiki kualitas minyak [17]. Aguado et al [23] melaporkan bahwa catalytic degradation mampu memecah rantai dalam waktu yang lebih singkat dan distribusi produk yang lebih baik dibadingkan dengan pemecahan secara termal. Pemecahan dengan katalis menghasilkan laju degradasi yang tinggi sehingga produk cair akan lebih banyak terbentuk. Dengan demikian apabila waktu reaksi singkat, dimana pemecahan termal akan membentuk banyak produk berviskositas tinggi seperti wax
daripada pemecahan dengan katalis karena laju degradasinya yang rendah [24]. Tabel 2.7 dan Gambar 2.4 menunjukkan perbandingan yield antara pemecahan tanpa katalis dan dengan menggunakan katalis.
Tabel 2.7 Perbandingan Yield Gas, Cairan, dan Residu dari Pemecahan Secara Termal dan Katalitik dari Limbah HDPE pada 430 °C [24]
Gas (%) Cairan (%) Residu (%)
Thermal Degradation 20,0 75,7 4,5
Catalytic Degradation 19,4 79,7 0,9
Ada dua jenis katalis, yaitu katalis homogen dan katalis heterogen. Katalis homogen digunakan untuk degradasi poliolefin kebanyakan asam lewis seperti AlCl3, metal tetrakloroaluminat, dan katalis baru berbasis cairan organik ionik [8].
Beberapa variasi katalis hidrogen telah diuji pada catalytic cracking dari poliolefin dan polistirena, yang dapat digolongkan sebagai berikut :
Padatan asam konvensional : zeolit, silika alumina, katalis FCC
Farah et al [10] meneliti penggunaan beberapa jenis katalis (NaOH, HUSY, dan Hbeta Zeolite) untuk mendegradasi limbah botol HDPE. Penggunaan padatan asam dapat memperpendek panjang rantai karbon dari parafin menjadi C10 – C28, dan mengubah komposisi produk.
Diperoleh dari hasil penelitian bahwa katalis Zeolit Hbeta menghasilkan cairan yang paling banyak dengan rantai karbon yang paling pendek C11–
C29. Dalam penelitian ini juga dapat disimpulkan penggunaan reaktor
berunggun dapat meningkatkan efektivitas produksi bahan bakar tanpa pengunaan katalis yang mahal. Gonzales et al [7] meneliti tentang pengaruh penggunaan beberapa jenis katalis pada degradasi katalitik polietilen. Perbedaan jenis katalis mempengaruhi suhu yang diperlukan untuk didapatkan konversi maksimum. Penggunaan katalis silika gel mencapai konversi maksimum pada suhu 450 °C, 5A molecular sieve pada suhu 700 °C, dan karbon aktif pada suhu 450 °C. Komposisi fraksi yang dihasilkan juga berbeda pada setiap jenis katalis. Fraksi gas yang didapatkan pada pemecahan dengan silika gel mempunyai komposisi metana tertinggi yaitu 34 %. Jerry et al [25] meneliti konversi limbah polietilen dan polistiren menjadi bahan bakar dengan memvariasikan beberapa katalis seperti zeolit dan Fluid Cracking Catalyst (FCC). Didapatkan suhu optimum pada pengunaan katalis jenis FCC pada 410 – 430 °C dengan konversi fraksi gas dan bahan bakar sebesar 90 %.
Katalis mesostruktur : MCM-41, FSM-16, Al-SBA-15
C12 dan C3 – C22. MCM-41 mempunyai luas permukaan yang besar
walaupun punya keasaman yang lebih rendah daripada zeolit.
2.3.3 Mekanisme Catalytic Cracking
Mekanisme perengkahan senyawa rantai panjang seperti alkana pada permukaan katalis asam berlangsung melalui mekanisme pembentukan ion karbonium [27,28], sedangkan reaksi perengkahan tanpa menggunakan katalis akan melalui mekanisme pembentukan radikal bebas [28]. Katalis silika akan mendonorkan H+ pada rantai hidrokarbon sehingga karbon memiliki muatan positif (karbokation). Kemudian atom karbon yang bermuatan positif akan memutuskan ikatan dengan atom lainnya [27,28]. Seperti dapat dilihat pada Gambar 2.5 [28].
Gambar 2.5 Tahap Pembentukan Ion Karbonium / Karbokation [28]
Kemudian katalis yang telah berikatan dengan hidrokarbon akan berikatan dengan hidrokarbon lainnya dari reaktan seperti pada Gambar 2.6 [28].
Gambar 2.6 Tahap Interaksi Ion Karbonium dengan Reaktan [28]
Gambar 2.7 Tahap Penataan Ion Karbonium Melalui Pemutusan Beta [28]
Kemudian katalis akan terbentuk kembali dengan memutuskan ikatan pada ion karbonium seperti pada Gambar 2.8 [28].
Gambar 2.8 Tahap Pembentukan Katalis Kembali [28]
2.3.4 Hydro Cracking
Hydro cracking adalah proses cracking dengan mereaksikan plastik dengan hidrogen di dalam wadah tertutup yang dilengkapi dengan pengaduk pada temperatur antara 423 – 673 K dan tekanan hidrogen 3 – 10 MPa. Dalam proses
hydrocracking ini dibantu dengan katalis. Untuk membantu pencapuran dan reaksi biasanya digunakan bahan pelarut 1-methil naphtalene, tetralin dan decalin. Beberapa katalis yang sudah diteliti antara lain alumina, amorphous silica alumina, zeolite dan sulphate zirconia [29]. Hydro Cracking sampah polimer biasanya melibatkan reaksi dengan hidrogen katalis yang berlebih dalam autoclave batch
yang diaduk pada suhu sedang dan tekanan (biasanya 423-673 K dan 3-10 MPa hidrogen). Pekerjaan tersebut bertujuan untuk memperoleh kualitas bensin tinggi mulai dari berbagai feed. Feed seperti polietilena, polietilen tereftalat polistiren, polyvinil Klorida dan polimer campuran, polimer limbah dari sampah kota dan sumber-sumber lain telah dievaluasi dan termasuk logam transisi (misalnya, Pt, Ni, Mo, Fe) didukung oleh padatan asam (seperti alumina, amorf silika-alumina, zeolit dan zirkonia sulfat). Katalis ini menggabungkan kedua kegiatan hidrogenasi dan
Suhu (°C)
2.4 FAKTOR YANG MEMPENGARUHI PROSES PIROLISIS
Aktivitas dan selektivitas katalis bergantung pada beberapa variabel yaitu, temperatur, jumlah katalis, jenis katalis, waktu proses, jenis plastik, dan komposisi plastik.
2.4.1 Temperatur
Temperatur adalah variabel yang paling penting yang mempengaruhi proses
cracking plastik. Temperatur reaksi biasanya berkisar pada 300 – 450 °C. Secara umum, kenaikan temperatur membuat peningkatan aktivitas katalis. Namun demikian, harus diperhitungkan bahwa pada suhu tinggi terjadinya reaksi dapat mengubah selektivitas produk [8]. Gambar 2.9 menunjukkan grafik pengaruh suhu dengan yield gas dan distilat yang dihasilkan [25].
Gambar 2.9 Pengaruh Temperatur dalam Pemecahan Termal Polietilen [25]
Walendziewski dan Steiniger [25] melaporkan hasil pemecahan termal dan pemecahan dengan katalis pada rentang temperatur 370 – 450 °C. Hasil penelitian menunjukkan bahwa peningkatan temperatur reaksi akan meningkatkan produk gas dan cair, dan juga akan mengurangi hasil residu.
reaksi pada suhu 450 °C menghasilkan produk utama minyak cair dan pada temperatur yang lebih tinggi (475 – 550 °C) menghasilkan produk utama minyak cair kental dan wax.
Sharatt et al [30] mengamati bahwa, pada cracking HDPE dengan katalis zeolit HZSM-5 pada reaktor fluidized bed pada suhu 290 – 430 °C. Kenaikan temperatur menyebabkan peningkatan hasil hidrokarbon ringan. Namun kenaikan suhu reaksi juga mengakibatkan penurunan hasil fraksi gas.
2.4.2 Jumlah katalis
Jumlah katalis dan rasio katalis terhadap bahan baku mempengaruhi hasil proses pemecahan seperti konversi proses. Sharatt et al [30] mengamati pemecahan HDPE dengan zeolite HZSM-5 dan memvariasikan rasio massa katalis dengan polimer mulai dari 1 : 10 hingga 1 : 1 pada 360 °C. Konversi yang didapat selalu diatas 90 %. Perbedaan yang terlihat adalah pada distribusi produk. Peningkatan rasio katalis dengan polimer akan menghasilkan jumlah C3– C4 yang lebih banyak.
Gonzales et al [7] rasio katalis/PE pada semua percobaan yaitu 01:10 berat (1,0 g katalis untuk 10,0 g PE limbah). percobaan sebelumnya dan data yang diperoleh oleh penulis lain menunjukkan rasio ini menjadi optimal dalam penggunaan katalis untuk konversi tertinggi. rasio 0,1 : 10 dan 0,3 : 10 juga diuji, yang pertama tidak memadai (konversi lebih rendah dari 5%) dan yang kedua yang dilakukan untuk nilai yang sama dari konversi PE.
2.4.3 Waktu
Jenis Plastik
Y
ie
ld
(
%
)
Cairan Padatan Gas 2.4.4 Jenis dan Komposisi Plastik
Komposisi limbah plastik mempunyai pengaruh yang besar pada kemampuan katalis. Bagaimanapun, katalis akan menghasilkan konversi yang tinggi pada reaksi pemecahan yang menggunakan polimer murni atau satu jenis polimer saja. Akan tetapi dapat kehilangan aktivitasnya apa bila bahan baku adalah limbah plastik yang bercampur (tidak satu jenis) [8]. Jenis plastik bahan baku juga mempengaruhi distribusi produk seperti yang ditunjukkan pada Gambar 2.10.
Gambar 2.10 Yield Cairan, Padatan, dan Gas dari Pemecahan dengan Katalis FCC [8]
Pada jenis termoplastik pada umumnya, hasil produk cairan adalah 80 % atau lebih, dimana PS > PP > PE. Plastik dengan struktur polisiklik mempunyai hasil cairan dan padatan yang lebih banyak dibandingkan plastik yang mempunyai struktur poliolefin.
2.5 PARAMETER KUALITAS BAHAN BAKAR
Tabel 2.8 Kualitas Bahan Bakar Diesel Komersil yang Diizinkan Pemerintah Indonesia [4]
Parameter Unit Diesel 48 (Solar) Diesel 51 (Pertamina Dex)
Densitas dari bahan bakar sering ditampilkan dalam istilah API gravity, skala yang ditetapkan oleh American Petroleum Institute (API) dan National Bureau of Standards. API gravity berkebalikan dengan spesifik gravity (rasio antara densitas bahan bakar pada 60 °F dengan densitas air pada 60 °F), berdasarkan persamaan seperti berikut :
°API = (141,5/spgr 60°F/60°F) – 131,5 (2.1) API gravity dapat diukur dengan menggunakan standard ASTM D287 atau D1298. Secara umum, API gravity dari bahan bakar cair dapat berhubungan secara kualitatif dengan kualitas lainnya seperti [31] :
Semakin tinggi API gravity maka semakin rendah viskositas dan residu
karbon.
Semakin tinggi API gravity maka rasio C/H semakin rendah.
Semakin tinggi API gravity maka semakin rendah nilai kalor volumetrik
(Btu/gal) dan semakin tinggi nilai kalor gravimetrik (Btu/lb).
Semakin tinggi API gravity maka kecepatan pembakaran semakin tinggi dan
nyala api semakin singkat.
2.5.2 Viskositas
adalah viskositas kinematis, yang mana dapat ditentukan dengan metode ASTM D 445 [31].
Pada minyak dengan fraksi yang berat akan memiliki viskositas yang tinggi, sehingga pada penggunaan saat musim dingin pemompaan akan sulit dilakukan. Viskositas yang tinggi pada bahan bakar cair dapat menyebabkan beberapa masalah sebagai berikut [31] :
Sulitnya pemompaan dari tangki penyimpanan menuju burner, terdapat
loss pada pump suction.
Aliran minyak yang tidak cukup akan menyebabkan masalah pada sistem
starter dan pembakaran yang tidak menentu.
Atomisasi yang tidak bagus akan menyebabkan pembakaran yang tidak
efisien
Viskositas yang rendah juga dapat menyebabkan beberapa masalah sebagai berikut [31]:
Terlalu banyak minyak yang terpompakan pada burner dapat
menyebabkan pembakaran yang tidak sempurna, menghasilkan asap, karbonisasi (pembentukan kerak karbon) pada mesin, dan pembentukan jelaga di ruang bakar.
Pembentukan panas yang sedikit karena pada minyak dengan viskositas
minyak yang rendah memiliki heating value yang rendah.
2.5.3 Nilai Kalor / Heating Value
![Tabel 2.1 Data Temperatur Transisi dan Temperatur Lebur Plastik [13]](https://thumb-ap.123doks.com/thumbv2/123dok/1774000.1128131/3.595.116.509.374.543/tabel-data-temperatur-transisi-dan-temperatur-lebur-plastik.webp)
![Tabel 2.2 Konsumsi Plastik Per kapita Beberapa Negara di Dunia [12]](https://thumb-ap.123doks.com/thumbv2/123dok/1774000.1128131/4.595.124.539.412.753/tabel-konsumsi-plastik-per-kapita-beberapa-negara-dunia.webp)
![Tabel 2.3 Jenis-jenis Limbah Plastik dan Tanda Daur Ulang [15] (Lanjutan)](https://thumb-ap.123doks.com/thumbv2/123dok/1774000.1128131/5.595.121.539.102.244/tabel-jenis-jenis-limbah-plastik-tanda-ulang-lanjutan.webp)
![Tabel 2.5 Sifat Umum Polipropilena [11]](https://thumb-ap.123doks.com/thumbv2/123dok/1774000.1128131/6.595.116.514.96.247/tabel-sifat-umum-polipropilena.webp)
![Gambar 2.1 Struktur Kristalin dari Sebuah Kristal Silika Tunggal [20]](https://thumb-ap.123doks.com/thumbv2/123dok/1774000.1128131/7.595.262.361.359.459/gambar-struktur-kristalin-dari-sebuah-kristal-silika-tunggal.webp)
![Gambar 2.3 Struktur Senyawa Silika Gel [19]](https://thumb-ap.123doks.com/thumbv2/123dok/1774000.1128131/9.595.139.483.183.302/gambar-struktur-senyawa-silika-gel.webp)
![Tabel 2.7 Perbandingan Yield Gas, Cairan, dan Residu dari Pemecahan Secara Termal dan Katalitik dari Limbah HDPE pada 430 °C [24]](https://thumb-ap.123doks.com/thumbv2/123dok/1774000.1128131/12.595.148.538.356.688/perbandingan-cairan-residu-pemecahan-secara-termal-katalitik-limbah.webp)
![Gambar 2.5 Tahap Pembentukan Ion Karbonium / Karbokation [28]](https://thumb-ap.123doks.com/thumbv2/123dok/1774000.1128131/14.595.164.478.514.607/gambar-tahap-pembentukan-ion-karbonium-karbokation.webp)
![Gambar 2.7 Tahap Penataan Ion Karbonium Melalui Pemutusan Beta [28]](https://thumb-ap.123doks.com/thumbv2/123dok/1774000.1128131/15.595.154.496.258.330/gambar-tahap-penataan-ion-karbonium-melalui-pemutusan-beta.webp)