BAB 2
TINJAUAN PUSTAKA
2.1.
Alumina dan Aluminium
Aluiminium adalah unsur melimpah ketiga terbanyak dalam kerak
bumi (sesudah oksigen dan silikon), mencapai 8,2 % dari massa total.
Keberadaannya umumnya bersamaan dengan silikon dalam aluminosilikat dari
feldspar dan mika dan di dalam lempung, yaitu aluminium oksida terhidrasi
yang mengandung 50 % sampai 60 % Al
2O
3: 1 % sampai 20 % Fe
2O
3: 1 %
sampai 10 % silika: sedikit sekali titanium, zirkonium, vanadium, dan oksida
logam transisi yang lain: dan sisanya (20 % sampai 30 %) adalah air. Bauksit
sebagai bahan baku peleburan aluminium dimurnikan melalui proses Bayer,
yang mengambil manfaat dimana fakta menunjukkan bahwa oksida alumina
amfoter larut dalam basa kuat tetapi besi (III) oksida tidak. Bauksit mentah
dilarutkan dalam natrium hidroksida
Al
2O
3(s) + 2 OH
-(aq) + 3 H
2O(l)
2 Al(OH)
4-(aq)
dan dipisahkan dari besi oksida dalam bentuk terhidrasi serta zat asing terlarut
lainnya dengan penyaringan. Aluminium oksida dalam bentuk terhidrasi murni
mengendap bila larutan didinginkan sampai lewat-jenuh dan dipancing
menjadi kristal dari produk:
2 Al(OH)
4-(aq)
Al
2O
3.3H
2O(s) + 2 OH
-(aq)
Air hidrasi dibuang melalui kalsinasi pada suhu tinggi sekitar 1200
0C. (David
W.Oxtoby, 2003)
2.2.
Sejarah Aluminium
Logam aluminium pertama kali dibuat dalam bentuk murni oleh H.C.
Oersted, pada tahun 1825, yang memanaskan amonium klorida dengan
amalgum kalium-raksa. Pada tahun 1854, Henri Saint-Cleire Deville membuat
aluminium dari natrium-aluminium klorida dengan jalan memanaskannya
dengan logam natrium. Proses ini beroperasi selama 35 tahun dan logamnya
dijual dengan harga $ 220 per kilogram. Pada tahun 1886, harganya sudah
turun menjadi $ 17 per kilogram. Pada tahun 1886, Charles Hall mulai
memproduksi aluminium dengan proses skala besar seperti sekarang, yaitu
melalui elektrolisis alumina di dalam kriolit lebur. Pada tahun itu pula, Paul
Heroult mendapat paten (Perancis) untuk proses serupa dengan proses Hall.
Hingga pada tahun 1893, produksi aluminium menurut cara Hall ini sudah
sedemikian meningkat, sehingga harganya sudah jatuh menjadi $ 4,40
perkilogram. Industri ini berkembang dengan mantap, berdasarkan suatu
pasaran yang sehat dan berkembang atas dasar penelitian mengenai sifat-sifat
aluminium dan cara-cara pemakaian yang ekonomis bagi bahan itu. Dengan
berkembangnya produksi itu, biaya pun berkurang dan ini diteruskan untuk
dinikmati oleh para konsumen. Harganya bahkan mencapai 33 sen per
kilogram pada tahun 1945. Harga ini meningkat kembali naik kembali hingga
menjadi $ 1,58 per kilogram pada tahun 1980, yang mencerminkan adanya
inflasi dan kenaikan biaya listrik. (George T. Austin, 1996)
2.3.
Bahan Baku
2.3.1.
Bahan Baku Utama Proses Elektrolisis2.3.1.2.
AluminaAdapun pembagian dari alumina berdasarkan ukuran partikelnya adalah :
1.
Alumina sandy ( γ – Al
2O
3)
Alumina sandy banyak ditemukan di Amerika, yang berbentuk serbuk
yang diproduksi pada pembakaran yang lebih rendah dari alumina floury.
Alumina sandy yang terbentuk digunakan pada tungku peleburan karena sifat
dari alumina tersebut yang bergerak bebas dan tidak dipengaruhi oleh gaya
dari luar.
2.
Alumina floury (α – Al
2O
3)
Alumina floury banyak ditemukan di Eropa, dimana alumina jenis ini diperoleh melalui proses Bayer, selanjutnya diproses lagi untuk memperoleh aluminium cair. Proses yang digunakan adalah Hall – Heroult, prinsip yang dipakai melalui reduksi alumina. Reduksi dilakukan secara elektrolisa terhadap alumina yang dilarutkan dalam larutan elektrolit cair dan dialirkan arus listrik. Dengan mengalirkan arus listrik tersebut pada kedua elektroda (anoda dan katoda) maka akan terjadi proses elektrolisa, sehingga terbentuk endapan aluminium cair pada katoda.
PT. INALUM tidak menghasilkan alumina sendiri tetapi diperoleh dari negara lain terutama dari negara Australia. Spesifikasi alumina yang diperlukan untuk peleburan aluminium adalah :
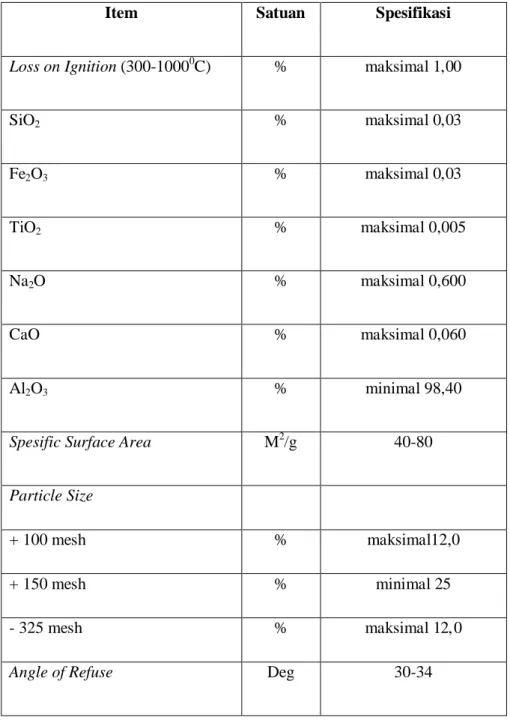
Tabel 2.1. Spesifikasi Alumina
Item Satuan Spesifikasi
Loss on Ignition (300-10000C) % maksimal 1,00
SiO2 % maksimal 0,03 Fe2O3 % maksimal 0,03 TiO2 % maksimal 0,005 Na2O % maksimal 0,600 CaO % maksimal 0,060 Al2O3 % minimal 98,40
Spesific Surface Area M2/g 40-80
Particle Size
+ 100 mesh % maksimal12,0
+ 150 mesh % minimal 25
- 325 mesh % maksimal 12,0
Angle of Refuse Deg 30-34
Anoda karbon berfungsi sebagai reduktor dalam proses elektrolisis alumina. Anoda karbon diproduksi pada pabrik karbon (Carbon Plant). Komposisi karbon terdiri dari 60% kokas minyak, 15% hardpitch, dan 20% butt (puntung anoda). Sifat-sifat anoda yang dipakai adalah :
1) Tahan terhadap perubahan panas (heat shock) sehingga sulit retak pada saat beroperasi pada temperatur tinggi.
2) Angka muai panas yang rendah agar anoda sulit terlepas dari tangkai anoda pada temperatur tinggi.
3) Konduktivitas panas tinggi agar segera mencapai temperatur tinggi pada proses pemanasan (baking).
4) Konduktivitas listrik tinggi (0,0036 – 0,0091 ohm.cm) agar aliran listrik efektif.
2.3.1.3.
KatodaKatoda adalah elektroda bermuatan listrik negatif. Ditinjau dari bahan bakunya dan prose pembuatannya, katoda dibagi atas 4 jenis, yaitu :
1). Blok katoda Amorphous, bahan bakunya antrasit, dipanggang pada suhu ± 1.200oC
2). Blok katoda semi graphitic, bahan bakunya grafit, dipanggang pada suhu ± 1.200oC
3). Blok katoda semi graphitic, bahan bakunya yang mengalami proses pemanasan sampai suhu ± 2.300oC
4). Blok katoda graphitic, bahan bakunya kokas mengalami proses grafitasi suhu ± 3.000o (Jody, B. J., dkk, 1992)
2.3.2.1.
KriolitKriolit dapat mengandung CaF2 dan AlF3 yang dapat membentuk kriolit Na3AlF6. Sifat-sifat kriolit adalah :
1) Konduktivitas listrik baik.
2) Memiliki berat jenis yang rendah. 3) Temperatur kristalisasi primer rendah. 4) Stabil dalam keadaan cair.
5) Dapat melarutkan alumina dalam jumlah besar.
Untuk memperbaiki sifat- sifat kriolit tersebut, bath biasanya ditambah dengan beberapa bahan tambahan seperti fluorida, alkil metal, AlF3 dan CaF2.
2.3.2.2.
Soda Abu (Na2CO3)Soda abu berfungsi memperkuat struktur katoda dan dinding samping agar sulit tererosi. Lapisan dinding samping dengan Na2CO3 dilakukan pada tahap transisi untuk membantu proses pembentukan kerak samping. Selain mencegah erosi oleh
bath, soda abu berfungsi sebagai isolasi termal. Spesifikasi soda abu yang digunakan
oleh PT INALUM adalah:
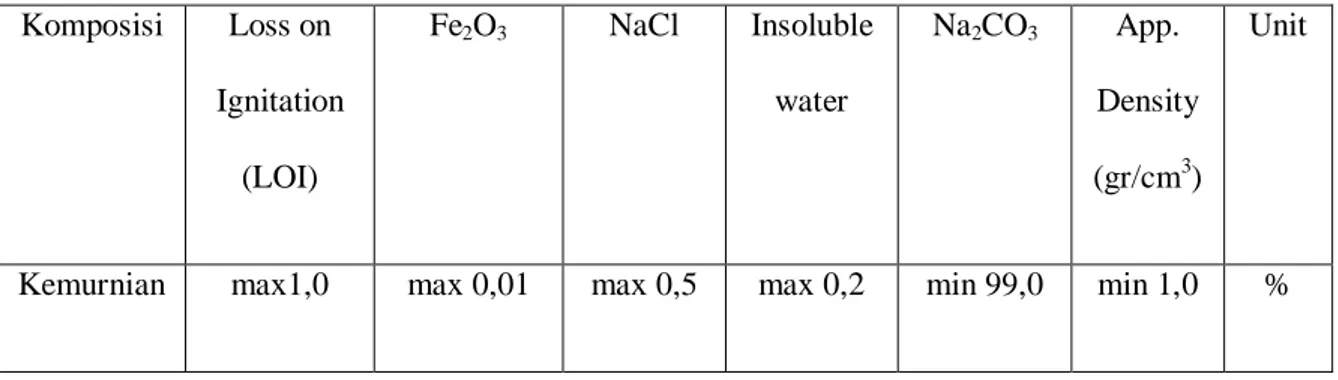
Tabel 2.2. Spesifikasi Soda Abu (Na2CO3)
Komposisi Loss on Ignitation (LOI) Fe2O3 NaCl Insoluble water Na2CO3 App. Density (gr/cm3) Unit
2.3.2.3.
Aluminium Fluorida (AlF3)Aluminium fluorida berfungsi menjaga keasaman bath dan merupakan bahan yang dituangkan secara manual jika kelebihan AlF3 kurang didalam bath. Spesifikasi AlF3 yang digunakan oleh PT INALUM adalah:
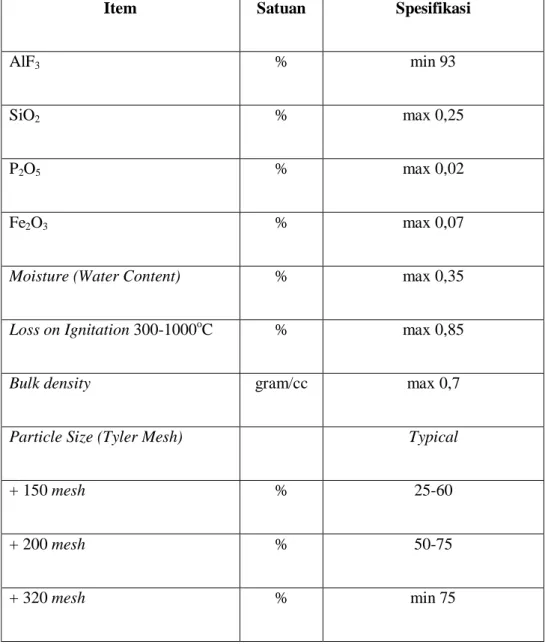
Tabel 2.3. Spesifikasi AlF3
Item Satuan Spesifikasi
AlF3 % min 93
SiO2 % max 0,25
P2O5 % max 0,02
Fe2O3 % max 0,07
Moisture (Water Content) % max 0,35
Loss on Ignitation 300-1000oC % max 0,85
Bulk density gram/cc max 0,7
Particle Size (Tyler Mesh) Typical
+ 150 mesh % 25-60
+ 200 mesh % 50-75
2.4.
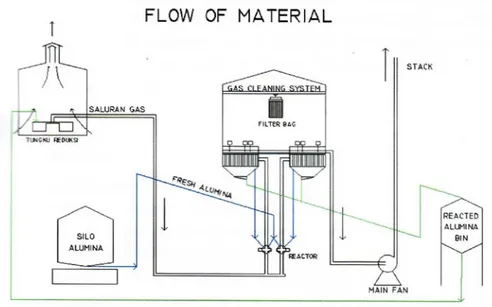
Aliran Proses Peleburan Aluminium
2.4.1. Diagram Alir Bahan BakuBahan-bahan untuk keperluan produksi Aluminium pertama sekali didatangkan melalui pelabuhan. Bahan-bahan tersebut adalah alumina, kokas, hard pitch. Alumina akan dimasukkan ke silo alumina (alumina silo), kokas kedalam silo kokas (coke silo),
pitch kedalam pitch storage house. Pemasukan bahan-bahan tersebut menggunakan belt conveyer.
Alumina yang berada didalam silo alumina kemudian kemudian dibawa ke dry
scrubber system untuk direaksikan dengan gas hidrogen flourida (HF) yang berasal dari
pot tungku reduksi. Hasil dari reaksi ini adalah reacted alumina yang akan dimasukkan kedalam hopper pot dengan menggunakan Anode Changing Crane (ACC). Dari hopper
pot, reacted alumina akan dimasukkan kedalam tungku reduksi.
Kokas yang ada dalam silo kokas akan bercampur dengan butt (puntung anoda) dan mengalami pemanasan. Kemudian dicampur dengan hard pitch yang berfungsi sebagai perekat (binder). Campuran ketiga bahan ini akan dicetak menggunakan Shaking
Machine di Anode Green Plant dan selanjutnya mengalami pemanggangan pada baking furnace. Hasilnya adalah blok anoda (anode block) di Anode Baking Plant.
Blok-blok anoda kemudian akan dipasangi tangkai (anode assembly) di Anode
Baking Plant. Anoda tersebut kemudian akan dikirimkan ke Reduction Plant untuk
keperluan proses elektrolisis alumina menjadi aluminium. Setelah + 28 hari anoda diganti dan sisa-sisa anoda (butt) dibersihkan. Butt ini kemudian akan dihancurkan dan dimasukkan ke silo butt. Butt kemudian dipakai kembali (recycle) sebagai bahan pembuatan anoda bersama kokas dan pitch.
Pada tungku reduksi akan terjadi proses elektrolisis alumina. Proses ini akan menghasilkan gas HF yang akan dialirkan ke dry scrubber system untuk bereaksi dengan alumina dan dibersihkan lalu dibuang melalui cerobong gas cleaning system. Aluminium cair (molten) yang dihasilkan dibawa ke Casting Shop menggunakan Metal Transport
Car (MTC). Di casting shop aluminium cair dimasukkan kedalam holding furnace, lalu
dituang ke casting machine untuk dicetak menjadi ingot aluminium dengan berat masing-masing ingot seberat 50 lbs (22,7 kg).
Gambar 2.1. Aliran Material
2.4.2. Fasilitas Utama di Gas Cleaning a. Fresh Alumina Handling System
Sistem ini menangani penyimpanan fresh alumina di dalam silo alumina dan pengirimannya ke dry scrubbing system. Banyaknya alumina yang dikirimkan diukur dengan flowmeter.
Sistem ini berfungsi menyaring debu dan mengadsorbsi gas fluoride yang berasal dari pot reduksi. Fresh alumina dari silo, dialirkan melalui air slide kedalam reactor dan direaksikan dengan gas buang dari pot reduksi. Gas dihisap dari pot reduksi dengan menggunakan main exhaust fan. Debu dan alumina yang bereaksi ini kemudian disaring di dalam bag filter. Udara yang sudah bersih dibuang ke atmosfer melalui exhaust stack.
Untuk menjaga tekanan di dalam bag filter stabil, alumina dan debu yang menempel di kain bag filter perlu dihembus secara periodic dengan udara bertekanan rendah yang diatur melalui damper. Udara ini berasal dari reverse flow fan. Alumina yang jatuh kemudian ditampung didalam hopper bag filter, dialirkan dan disirkulasikan kembali kedalam reactor untuk bereaksi kembali dengan gas buang. Dengan cara demikian, kontak antara gas buang dengan alumina di dalam reactor lebih efektif.
Setelah reaksi adsorpsi selesai melalui sistem overflow, alumina dari hopper bag
filter dikeluarkan dan dialirkan memakai air slide menuju bin reacted alumina.
c.
Reacted Alumina Handling SystemSistem ini menangani penyimpanan sementara reacted alumina di bin reacted
alumina. Reacted alumina kemudian dialirkan menuju Bath Material Mixing Centre
(BMMC) untuk dicampur dengan material bath. Campuran alumina dan material
bath kemudian disimpan sementara di day-bin melalui belt conveyer. Campuran ini
selanjutnya digunakan di pot reduksi sebagai bahan baku. (PT INALUM, 2009)
Aluminium terutama masih sekedar menjadi bahan penelitian di
laboratorium sampai tahun 1886, ketika Charles Hall di Amerika Serikat
(lulusan Oberlin College yang berusia 21 tahun) dan Paul Heroult
(berkebangsaan Perancis, berusia sama) secara sendiri-sendiri menemukan
proses yang efisien untuk memproduksikannya. Pada tahun 1990-an produksi
aluminium di seluruh dunia yang menggunakan proses Hall-Heroult mencapai
1,5 × 10
7ton metrik.
Proses Hall-Heroult melibatkan pengendapan aluminium secara
katodik, dari lelehan kriolit (Na
3AlF
6) yang mengandung Al
2O
3terlarut, dalam
sel elektrolisis. Setiap sel terdiri dari kotak baja persegi panjang yang
panjangnya sekitar 6 m, lebar 2 m, dan tinggi 1 m, yang berfungsi sebagai
katode, dan grafit pejal sebagai anode yang mencuat melewati atap sel hingga
ke bak lelehan kriolit. Arus yangh sangat besar (50.000 sampai 100.000 A)
dilewatkan dalam sel, dan sebanyak 100 sel seperti ini disusun secara seri.
Lelehan kriolit, yang berdisosiasi sempurna menjadi ion-ion Na
+dan
AlF
63-, merupakan pelarut yang baik untuk aluminium oksida, menghasilkan
distribusi kesetimbangan dari ion-ion seperti Al
3+, AlF
2+, . . . , AlF
63-, dan O
2-dalam elektrolit. Kriolit meleleh pada suhu 1000°C, tetapi titik lelehnya turun
dengan adanya aluminium oksida terlarut, sehingga suhu sel operasi hanya
950°C. Dibandingkan dengan titik leleh Al
2O
3murni (2050°C), suhu tersebut
merupakan suhu yang rendah, dan inilah sebabnya proses Hall-Heroult bias
berhasil. Lelehan aluminium memiliki kerapatan yang sedikit lebih besar
daripada lelehennya pada suhu 950°C sehingga materi ini mengumpul di dasar
sel, untuk selanjutnya disadap secara berkala. Oksigen merupakan produk
anode yang utama, tetapi zat ini bereaksi dengan electrode grafit menghasilkan
karbon dioksida. (David W. Oxtoby, 2003)
Secara umum reaksi yang terjadi dalam pot tungku reduksi adalah
sebagai berikut :
1. Reaksi Penangkapan Gas Hidrogen Flourida (HF)
Gas HF dapat terbentuk selama proses elektrolisis. Reaksi pembentukan gas HF adalah sebagai berikut :
Na3AlF6 + 3/2 H2→ Al(l) + 3 NaF(l) + 3 HF(g)
Potensial listrik 1,53 volt pada suhu operasi. Gas HF juga dapat terbentuk melalui reaksi:
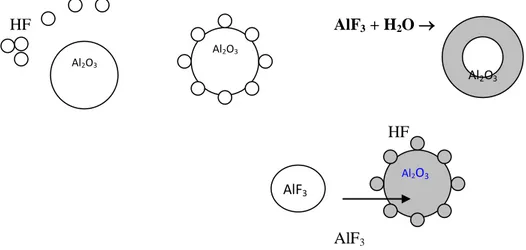
2 AlF3 + H2O → Al2O3(l) + 6 HF
Gas HF selanjutnya akan bereaksi dengan alumina (Al2O3).
HF AlF3 + H2O →
HF
AlF3
Gambar 2.2. Reaksi Penangkapan Gas HF
Reaksi (1) : adsorpsi HF pada permukaan alumina
Reaksi (2) : reaksi kimia antara HF dan Al2O3 menghasilkan aluminium fluorida (AlF3) dan H2O
Al2O3 Al2O3
Al2O3
AlF3
Reaksi difusi : reaksi difusi ion AlF3 ke dalam alumina dan menghasilkan AlF3
2. Reaksi Pada Anoda
Dalam Proses elektrolisis reaksi yang dapat terjadi pada anoda adalah :
C (s) + O2 (g)→ CO2 (g)
C (s) + CO2(g)→ 2 CO (g)
Jika potensial sel elektrolisis lebih besar dari 1,02 volt maka reaksi yang dapat terjadi adalah :
2 Al2O3(sat) + 3 C (s) → 4 Al (l) + 3 CO2(g)
3. Reaksi Pada Katoda
Reaksi yang dapat terjadi di sekitar katoda adalah dekomposisi ion AlF4- dari kriolit menjadi ion Al3+ dan ion F- :
AlF4-→ Al3+ + 4F-
Reaksi Al3+ :
Al3+ + 3e → Al (l)
Dan reaksi antara natrium dari kriolit dengan Al :
Al (l) + 3 Na+→ 3 Na + Al3+
4. Reaksi Utama Elektrolisis Alumina
Reaksi keseluruhan pada industri elektrolisis alumina dengan menggunakan anoda karbon adalah sebagai berikut :
Reaksi ini berlangsung pada temperatur sekitar 945o – 965o, beda potensial 1,18 volt. Mekanisme reaksi yang paling sering terjadi adalah reduksi Al2O3 secara langsung dengan reaksi : Al2O3 → AlO + AlO+ AlO2 → Al 3+ + 2 O2- Reaksi katodik : 2 Al3+ + 6e-→ 6 Al Reaksi anodik : 3 O2-→ 3/2 O2 + 6e
Reaksi diatas adalah reaksi utama, reaksi ini tidak mengabaikan fakta bahwa Na mengendap pada katoda.
Gambar 2.3. Reduksi Alumina
5. Gaya Magnetik
Adanya arus searah dan medan magnetik yang timbul oleh susunan pot akan menimbulkan gaya magnetik. Gaya magnetik tersebut akan menimbulkan pergerakan dan konversi aluminium cair didalam pot.
Intensitas gaya magnetik ditentukan oleh distribusi metal pada katoda dan komponen arus horizontal pada katoda. Untuk menghilangkan komponen arus horizontal adalah dengan membuat kerak samping.
(a) (b)
Gambar 2.5. Pengaruh Kerak Samping Pada Aliran Arus (a) tanpa kerak samping; (b) dengan kerak samping