Jurnal Hutan Tropis Borneo No. 23, September 2008 87 INDUKSI KALUS PADA BUDI DAYA JARINGAN
DAUN ULIN (Eusideroxylon zwageri T. et B.) SECARA in VITRO Oleh/By
ENY DWI PUJAWATI
Program Studi Budidaya Hutan Fakultas Kehutanan Unlam
ABSTRACT
The aim of this research is to know potential growth of ulin leaf explants with combination of sucrose and 2,4-D plant growth regulator by in vitro culture.The research was located in Tissue Culture Laboratory of Forestry Faculty of Lambung Mangkurat University, Banjarbaru.
Materials of the research are ulin leaves, MS medium, aquades, 2,4-D plant growth regulator, sucrose, agrimycin, masalgin, alcohol, spiritus and tween 20. Equipments that used in the research are balance, laboratory glasses, LAF, autoclave, spiritus burner, dissecting kit and sprayer. Data analysis used statistic of analysis of varian and descriptive analysis.
The result of the research showed that . combination of sucrose 30gr/liter and 2,4-D 2,0mg/liter is best treatment for callus induction from ulin leaf explants. Callus was formed with potential of embryogenic.
Keywords : Eusideroxylon zwageri T. et B., callus induction, Murashige and Skoog (MS) medium, 2,4-D, potential of embryogenic
PENDAHULUAN
Tanaman ulin dengan nama ilmiah Eusideroxylon zwageri T et. B. adalah tanaman asli Indonesia dengan penyebaran terbatas hanya di Kalimantan, Bangka, Belitung dan Sumatera bagian selatan (Beekman, 1949; Whitmore dan Tantra, 1986). Tanaman ulin ini mempunyai banyak nama daerah antara lain : kayu besi, onglen, bulian, talin dan tabelian (Nezriyetti, 1992).
Tanaman ulin menghasilkan kayu dengan sifat istimewa baik kekuatan maupun keawetannya, sehingga banyak digunakan untuk kayu bangunan dan kayu konstruksi (Nezriyetti, 1992). Kebutuhan masyarakat akan kayu ulin yang semakin meningkat mengakibatkan penebangan jenis ini terus berlangsung, sementara usaha budi daya belum memadai menyebabkan populasi di alam semakin menurun.
Hasil penelitian Puslitbang Biologi LIPI tahun 1993 menyatakan
bahwa jenis ulin termasuk langka dengan status rawan (Wiriadinata dkk, 1993) dan berdasarkan Surat Keputusan Menteri Pertanian Nomor 54/Kpts/um/2/19872 jenis ulin dilindungi. Kelangkaan jenis ulin juga disebabkan karena kemerosotan lingkungan hutan, berkurangnya luas kawasan hutan dan karena sifat tanaman ulin itu sendiri yang sulit berkembang biak dan lambat pertumbuhannya.
Untuk memenuhi kebutuhan kayu ulin yang semakin meningkat, maka perlu diusahakan budi daya tanaman ulin dalam skala besar dengan membangun hutan-hutan tanaman di tempat yang cocok. Guna menunjang usaha budi daya tersebut tentunya diperlukan bibit dalam jumlah besar dengan kualitas baik dan umur yang seragam.
Salah satu alternatif pengadaan bibit tanaman ulin adalah
Jurnal Hutan Tropis Borneo No. 23, September 2008 88 mendapatkan bibit tanaman ulin
dalam jumlah banyak dengan umur dan sifat yang seragam serta waktu yang singkat. Bibit tanaman ulin yang diharapkan dapat berasal dari jalur embriogenesis somatik maupun organogenesis.
Induksi kalus merupakan penelitian awal untuk mengetahui kemampuan suatu jenis tumbuhan apakah dapat dikembangkan secara budi daya in vitro atau tidak. Untuk penelitian awal dengan induksi kalus, pada umumnya dilakukan untuk mencari komposisi medium yang tepat dan jenis serta konsentrasi zat pengatur tumbuh yang cocok. Zat pengatur tumbuh 2,4 D merupakan jenis auksin yang paling banyak
digunakan untuk induksi kalus secara
in vitro.
Penelitian yang akan dilakukan adalah menanam eksplan irisan daun ulin ke dalam medium MS padat dengan penambahan sukrosa 20, 30 dan 40 gr/l dan zat pengatur tumbuh 2,4 D 0,0; 1,5; 2,0 dan 2,5 mg/l.
Penelitian ini bertujuan untuk mengetahui respon pertumbuhan eksplan irisan daun ulin yang ditumbuhkan pada medium MS dengan perlakuan penambahan sukrosa dan zat pengantur tumbuh 2,4 D. Manfaat dari penelitian ini adalah sebagai langkah awal pembudidayaan tanaman ulin secara
in vitro.
METODE PENELITIAN
Penelitian dilakukan di Laboratorium Kultur Jaringan Program Studi Budidaya Hutan Fakultas Kehutanan Unlam selama 6 bulan.
Bahan yang digunakan adalah
(1) Eksplan yang diambil dari daun
kedua dan ketiga tanaman ulin yang berasal dari stek pucuk dan biji, berukuran 1 cm x 1 cm tanpa tulang daun utama; (2) medium yang digunakan adalah medium dasar MS
(Murashige and Skoog) dengan
penambahan berbagai konsentrasi sukrosa dan 2,4 D sesuai perlakuan, 100 mg/l kasein hidrolisat dan 7 gr/l agar; dan (3) Bahan kimia yang digunakan adalah penyusun medium dasar MS, aquadest, alkohol 70%, NaOH 0,1 M, HCl 0,1 M, arang aktif, PVP terlarut, 2,4 D, deterjen, bayclin,
fungisida Masalgin, bakterisida
Agrimycin, spiritus dan Tween 20. Alat-alat yang dipergunakan
dalah autoclave, laminar air flow
cabinet, botol kultur, erlenmeyer, gelas ukur, cawan petri, pengaduk, pinset, skalpel, aluminium foil, thermostat, mikroskop, kamera, sprayer, lampu spiritus, kompor,
magnetic stirrer, hot plate dan timbangan.
Semua peralatan yang akan digunakan seperti botol media, erlenmeyer, cawan petri, pinset, skalpel, kertas saring dan aquadest disterilkan dengan pemanasan dalam
autoclave selama 20 menit pada suhu
121o C, sedangkan LAF cabinet
disterilkan dengan alkohol 70% dilanjutkan dengan penyinaran ultra violet selama 20 menit. Makronutrien, mikronutrien, besi dan vitamin dari larutan stok diambil sesuai volume yang akan dibuat, kemudian ditambahkan sukrosa, bubuk agar serta aquadest sampai volume yang dikehendaki. Selanjutnya larutan tadi dipanaskan di atas kompor sambil terus diaduk sampai mendidih. Setelah mendidih kemudian diukur pH-nya sekitar 5,8 bila terlalu asam ditambahkan NaOH 0,1 M, bila terlalu basa ditambahkan HCl 0,1 M beberapa tetes. Selanjutnya ditambahkan zat pengatur tumbuh sesuai perlakuan lalu dimasukkan ke dalam botol kultur dan ditutup rapat dengan aluminium foil. Botol-botol media tadi selanjutnya disterilkan
Jurnal Hutan Tropis Borneo No. 23, September 2008 89
dalam autoclave selama 20 menit
pada suhu 121o C dan tekanan 1,5
atm. Daun ulin yang baru dipetik dicuci dengan air mengalir kemudian direndam dalam larutan deterjen selama 10 menit lalu dibilas dengan air mengalir, selanjutnya direndam
dalam larutan campuran masalgin 2
gr/l, agrimycin 2 gr/l dan tween 20 2 mg/l selama 20 menit lalu dibilas dengan air mengalir. Sterilisasi
selanjutnya dilakukan di dalam LAF
dengan perendaman bayclin 10% selama 5 menit lalu dibilas aquadest sekali dan perendaman bayclin 5% selama 5 menit lalu dibilas dengan aquadest steril 3 kali. Sebelum
penanaman dimulai LAF dibersihkan
dan disterilkan dengan penyinaran ultra violet selama 20 menit. Semua peralatan dan botol media yang akan dimasukkan ke dalam LAF disemprot terlebih dahulu dengan alkohol 70% atau spritus. Eksplan yang sudah disterilkan lalu dipotong dengan ukuran 1 x 1 cm di dalam larutan 25 mg/l asam askorbat. Dengan
menggunakan pinset dan dilakukan dekat lampu spritus, eksplan daun ulin ditanam dalam botol dengan permukaan adaksial bersentuhan dengan medium. Setelah selesai penanaman botol-botol kultur disimpan dalam ruang inkubasi pada temperatur 25-28o C.
Parameter yang diamati adalah (a) hari mulai tumbuh kalus dan (b) sifat morfologis kalus (potensi kalus).
Penelitian menggunakan rancangan faktorial. Faktor I adalah konsentrasi sukrosa (20, 30 dan 40 g/l), faktor II dalah konsentrasi 2,4 D (0,0; 1,5; 2,0 dan 2,5 mg/l) dan masing-masing perlakuan dengan 5 ulangan. Data kuantitatif dianalisis secara statistik dengan menggunakan analisis varian untuk mengetahui adanya perbedaan pengaruh antar perlakuan, bila ada perbedaan antar perlakuan maka dilanjutkan dengan uji BNT pada taraf uji 5%. Data kualitatif berupa ciri morfologis dianalisis secara deskriptif.
HASIL DAN PEMBAHASAN
Induksi atau pemacuan pembentukan kalus merupakan penelitian tahap awal untuk mengetahui potensi suatu jenis tumbuhan untuk dikembangkan melalui budi daya in vitro. Memang tidak semua jenis dapat dikembangkan melalui teknik budi daya ini meskipun secara teoritis semua sel mempunyai potensial regenerasi yang sama untuk dapat membentuk individu baru yang sempurna, yang disebut dengan konsep totipotensi sel.
Ada banyak faktor yang mempengaruhi pertumbuhan dan perkembangan sel tumbuhan untuk dapat menunjukkan totipotensinya, antara lain adalah jenis tumbuhan, status nutrisi, status fisiologis dan status kesehatan tumbuhan yang dijadikan sumber eskplan, jenis dan
komposisi medium yang digunakan, jenis dan konsentrasi zat pengatur tumbuh yang digunakan, keadaan lingkungan tumbuhnya serta pemeliharaan kultur. Komposisi medium dan jenis serta konsentrasi zat pengatur tumbuh sangat berperan dalam kecepatan pembentukan kalus dan arah pertumbuhan serta perkembangan kalus yang dihasilkan.
Kecepatan pembentukan kalus ditunjukkan dengan hari mulai terbentuk kalus setelah penanaman eksplan pada medium. Arah pertumbuhan dan perkembangan dari kalus dapat mengarah pada pembentukan organ seperti tunas atau akar yang disebut sebagai organogenesis atau menjadi embrio (calon individu baru) yang disebut embriogenesis. Respon pertumbuhan dan perkembangan suatu jenis dalam
Jurnal Hutan Tropis Borneo No. 23, September 2008 90
budi daya in vitro tidak selalu
didahului dengan pembentukan kalus, tetapi dapat langsung terbentuk organ ataupun embrio.
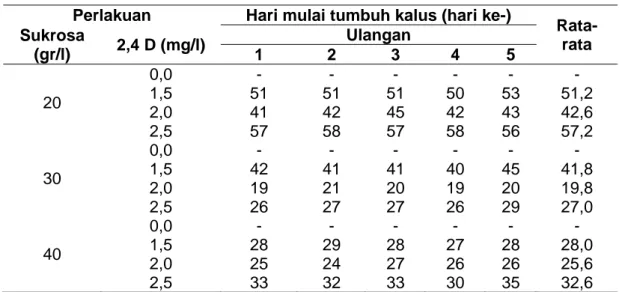
Hari Mulai Tumbuh Kalus. Hasil pengamatan hari mulai tumbuh kalus pada eksplan disajikan pada Tabel 1. Pengamatan hari mulai tumbuhnya kalus pada medium dengan penambahan sukrosa 20 gr/l menunjukkan hasil yang paling lambat responnya dibandingkan dengan sukrosa 30 gr/l dan 40 gr/l. Tumbuhnya kalus yang lambat pada perlakuan ini mungkin disebabkan karena sukrosa 20 gr/l yang digunakan sebagai sumber energi kurang mencukupi untuk proses metabolisme sel-sel dan bahan untuk pembentukan sel-sel kalus.
Pada penelitian ini semua eksplan yang ditanam pada medium tanpa penambahan zat pengatur tumbuh (2,4 D 0,0 mg/l) tidak menunjukkan respon pembentukan kalus sampai akhir penelitian. Hal ini menunjukkan bahwa penambahan zat pengatur tumbuh eksogen ke dalam medium sangat penting dalam kultur
in vitro, karena pasokan hormon endogen terputus dan simpanan dalam jaringan juga terbatas (George dan Sherington, 1987). Zat pengatur tumbuh golongan auksin termasuk 2,4 D ini sangat diperlukan untuk proses pembentangan dan pembelahan serl serta diferensiasi.
Penambahan zat pengatur tumbuh 2,4 D sebanyak 2,5 mg/l juga menghambat pertumbuhan kalus pada eksplan. Hal ini kemungkinan karena konsentrasi tersebut sudah melebihi konsentrasi optimal untuk pembentangan, dediferensiasi, pembelahan dan proliferasi sel-sel, sehingga justru akan menghambat pembentukan kalus. Seperti diketahui bahwa zat pengatur tumbuh auksin seperti 2,4 D ini apabila konsentrasinya terlalu tinggi justru
akan menghambat pertumbuhan tanaman (Salisbury dan Ross, 1995).
Menurut Wilkins dan Dodds (1983), kecepatan proliferasi sel-sel kalus sangat bervariasi tergantung kepada jenis dan varitas tumbuhan sumber eksplan, selain penambahan zat pengatur tumbuh dan bentuk fisik medium. Tanaman ulin termasuk jenis yang lambat tumbuh sehingga kemungkinan pembentukan kalus juga lambat. Secara teoritis, tanaman yang lambat tumbuh secara alami akan lambat pula bila dikulturkan secara in vitro (Pierik, 1987).
Hasil pengujian dengan analisis varian dan uji BNT menunjukkan adanya perbedaan yang nyata antar perlakuan kombinasi konsentrasi sukrosa dan 2,4 D terhadap hari mulai terbentuknya kalus pada eksplan irisan daun ulin. Medium dengan kombinasi sukrosa 30 gr/l dan 2,4 D 2,0 mg/l merupakan perlakuan yang paling responsif dibandingkan dengan perlakuan lain, karena rata-rata hari mulai terbentuk kalus paling kecil yaitu pada hari ke 19,8 atau minggu ke 2-3. Hasil uji BNT terhadap hari mulai tumbuh kalus disajikan pada Tabel 2.
Hasil penelitian juga menunjukkan bahwa penambahan sukrosa dan zat pengatur tumbuh 2,4 D sangat diperlukan untuk pertumbuhan eksplan membentuk kalus, tanpa zat pengatur tumbuh eksplan tak mampu membentuk kalus dan konsentrasi sukrosa yang kurang juga menghambat pembentukan kalus.
Ciri Morfologis Kalus yang Terbentuk. Kalus yang terbentuk setelah 8 (delapan) minggu penanaman mempunyai tekstur yang
remah (friable), bahkan langsung
hancur begitu diangkat menggunakan pinset. Pada awalnya kalus mempunyai warna kuning transparan kemudian berubah menjadi kehijauan dan akhirnya berubah warna menjadi cokelat (mengalami pencoklatan atau
Jurnal Hutan Tropis Borneo No. 23, September 2008 91
browning). Warna kecoklatan ini menunjukkan adanya penuaan jaringan kalus yang akhirnya dapat mengalami kematian. Untuk mengatasi ini perlu dilakukan pemindahan kultur ke medium baru yang segar agar jaringan kalus dapat bertahan hidup.
Kalus yang diinduksi dengan zat pengatur tumbuh 2,4 D pada umumnya mempunyai tekstur yang remah sedangkan yang diinduksi dengan NAA mempunyai tekstur yang kompak (George dan Sherington, 1984). Menurut Pedroso dan Pais
(1995), tekstur kalus yang remah pada umumnya menunjukkan potensi embriogenik artinya apabila kalus tersebut terus dipelihara akan diperoleh embrio somatik, sedangkan tekstur kalus yang kompak menunjukkan adanya potensi organogenik. Tekstur kalus yang remah dan cenderung hancur apabila diangkat tersebut kemungkinan merupakan calon embrio somatik pada stadium globuler, karena menurut Naik (1965 dalam Robert, 1983) sel-sel kalus akan berdiferensiasi setelah 28 hari kultur. Tabel 1. Data pengamatan hari mulai terbentuk kalus pada eksplan.
Perlakuan Hari mulai tumbuh kalus (hari ke-)
Rata-rata Sukrosa (gr/l) 2,4 D (mg/l) Ulangan 1 2 3 4 5 20 0,0 1,5 2,0 2,5 - 51 41 57 - 51 42 58 - 51 45 57 - 50 42 58 - 53 43 56 - 51,2 42,6 57,2 30 0,0 1,5 2,0 2,5 - 42 19 26 - 41 21 27 - 41 20 27 - 40 19 26 - 45 20 29 - 41,8 19,8 27,0 40 0,0 1,5 2,0 2,5 - 28 25 33 - 29 24 32 - 28 27 33 - 27 26 30 - 28 26 35 - 28,0 25,6 32,6 Tabel 2. Hasil uji BNT terhadap hari mulai tumbuh kalus.
Perlakuan Hari mulai tumbuh kalus (hari ke-) Sukrosa (gr/l) 2,4 D (mg/l) Rata-rata SD 20 0,0 1,5 2,0 2,5 Tidak tumbuh 51,2 42,6 57,2 Tidak tumbuh 1,09545 f 1,51658 e 0,83666 g 30 0,0 1,5 2,0 2,5 Tidak tumbuh 41,8 19,8 27,0 Tidak tumbuh 1,92354 e 0,83666 a 1,22474 bc 40 0,0 1,5 2,0 2,5 Tidak tumbuh 28,0 25,6 32,6 Tidak tumbuh 0,70711 c 1,14018 b 1,81659 d Ket: Angka-angka yang diikuti huruf yang sama tidak berbeda nyata
Jurnal Hutan Tropis Borneo No. 23, September 2008 92 KESIMPULAN DAN SARAN
Kesimpulan. Induksi kalus pada budi daya jaringan daun ulin ditentukan oleh konsentrasi sukrosa dan zat pengatur tumbuh 2,4 D pada medium. Kombinasi sukrosa 30 gr/l dan 2,4 D 2,0 mg/l merupakan perlakuan paling respontif terhadap pembentukan kalus eksplan irisan daun ulin. Kalus yang terbentuk mempunyai tekstur yang remah dan menunjukkan potensi embriogenik.
Saran. Perlu penelitian lanjutan untuk mendapatkan plantlet dengan melakukan subkultur ke dalam medium baru sehingga proembrio dapat berkembang menjadi embrio lengkap dan plantlet.
DAFTAR PUSTAKA
Beekman, H.A.J.M. 1949. Kayu Besi
(Eusideroxylon zwageri T. et B. Lauraceae) terjemahan A. Azis
Lahiya. Seri Himpunan
Peninggalan Penulisan Yang Berserakan. Bandung. 63 halaman.
George, E.F. and P.D. Sherington.
1984. Plant Propagation by
Tissue Culture. Exegetics ltd. England.
Nezriyetti. 1992. Pemanfaatan
Beberapa Jenis Kayu dalam Pembuatan Alat Transportasi Air di Jambi dalam Prosiding Seminar dan Lokakarya
Nasional Etnobotani.
Kerjasama LIPI, Depdikbud, Deptan dan Perpusnas. Bogor. Hal 358-361.
Pedroso, M.C. and M.S. Pais. 1995.
Factor Controlling Somatic Embryogenesis: Cell Wall Change As An In Vitro Marker Of Embryogenic Competence. Plant cell, tiss. And org. cult. 43: 147-154.
Pierik, R.L.M. 1987. In Vitro Culture of Higher Plant. Martinus Nijhoff publisher. Dordrecht-Boston-Lancaster. Pp. 5-6, 107-111, 200-203, 215.
Robert, L.W. 1983. The Influence of Physical Factor On Xylem Differentiation In Vitro dalam J.H. Dodds (ed). Tissue.
Sallisbury, F.B. and C.W., Ross. 1995. Fisiologi Tumbuhan Jilid II ed. IV Terjemahan. ITB bandung hal. 145-147.
Whitmore, T.C. and I.G.M., Tantra. 1986. Tree Flora of Indonesia-Check List Sumatera. LPH. Bogor p. 123.
Wilkins, C.P. and J.H., Dodds. 1983.
Tissue Culture Propagation of Temperate Fruit Trees dalam J.H. Dodds. Tissue culture of
tree. Avi pub. Co. Inc.
Connecticut. Pp. 65, 69.
Wiriadinata, dkk. 1993. Jenis-Jenis Tumbuhan Langka Indonesia dalam Prosiding Seminar Hasil Penelitian dan Pengembangan
Sumberdaya Hayati.
Puslitbang Biologi LIPI hal. 58-67.