II TINJAUAN PUSTAKA
2.1 Tanaman Nyamplung (Calophyllum inophyllum L.) 2.1.1 Sifat-Sifat Tanaman Nyamplung
Nyamplung mempunyai nama daerah bintangor, bintol, mentangur, penanga di Sumatera, bunut, nyamplung, bintangur, sulatri, punaga di Jawa, bataoh, bentangur, butoo, jampelung, jinjit, mahadingan, maharunuk di Kalimantan, betau, bintula, dinggale, pude, wetai di Sulawesi, balitoko, bintao, bitaur, petaule di Maluku, dan bentango, gentangir, mantau, samplong di NTT (Martawijaya et al. 1981). Negara Malaysia mengenal nyamplung sebagai bintangor, bakokol, entangor, mentangor dan penanga laut (Martawijaya et al. 1981). Calophyllum inophyllum L. atau Calophyllum bintangor Roxb.) di Inggris diketahui sebagai Alexandrian Laurel, Tamanu, Pannay Tree, Sweet Scented Calophyllum (Dweek dan Meadows 2002). Daerah penyebaran di Indonesia meliputi Sumatera Barat, Riau, Jambi, Sumatera Selatan, Lampung, Jawa, Kalimantan Barat, Kalimantan Tengah, Sulawesi, Maluku, Nusa Tenggara Timur (Martawijaya et al. 1981). Taksonomi nyamplung (Calophyllum inophyllum L.) adalah sebagai berikut:
• dunia : Plantae (tumbuhan)
• super divisi : Spermatophyta (menghasilkan biji) • divisi: Magnoliophyta (berbunga)
• kelas:Magnoliopsida (berkeping dua) • subkelas: Dilleniidae
• ordo: Theales • famili: Clusiaceae • genus: Calophyllum
• spesies: Calophyllum inophyllum L.
Kayu nyamplung dapat digunakan untuk berbagai keperluan yaitu: tiang layar, dayung, balok, tiang rumah, papan lantai perumahan, peti, tiang listrik, roda, sumbu gerobak, kano, tong dan kepala pemukul golf (Martawijaya et al. 1981). Tanaman nyamplung tumbuh di hutan tropis dengan curah hujan A dan B, pada
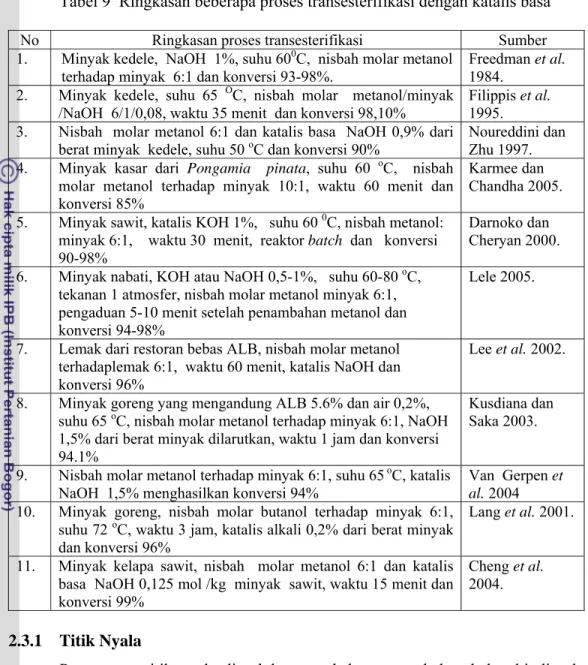
tanah berawa dekat pantai sampai pada tanah kering berbukit-bukit sampai ketinggian 800 m dari permukaan laut (Martawijaya et al. 1981). Kondisi lingkungan pertumbuhan tanaman nyamplung dapat dilihat pada Tabel 1 sedangkan tanaman dan buah nyamplung dapat dilihat pada Gambar 1.
Tabel 1 Kondisi lingkungan untuk pertumbuhan nyamplung No Parameter Kondisi lingkungan yang sesuai
1 Iklim Suhu sedang (moderat) sampai basah dan tidak cocok pada kondisi sangat dingin • Ketinggian 0-800 m dari permukaan laut
• Curah hujan 1000-5000 mm (40-200 inci) • Lama musim kering dengan
curah hujan < 40 m
5 bulan • Suhu rata-rata tahunan 33 0C (91 0F) • Suhu maksimum rata-rata
pada bulan paling panas
37 0C (99 0F)
• Suhu minimum rata-rata pada bulan paling dingin
120C (540F)
2 Tanah Tumbuh baik pada tanah berpasir dengan hujan yang cukup di pantai tetapi toleran pada tanah lempung (clay) dan tanah berbatu (rocky soils), tanah yang dangkal (shallow) dan tanah asin (saline soils) • Tekstur tanah Toleran pada tanah sands, sandy loams,
loams dan sandy clay loams • Drainase tanah Toleran pada drainase jelek
• Keasaman pH 7,4 - 4,0
3 Toleransi kondisi ekstrim Merupakan pohon keras yang tumbuh pada daerah pantai, toleran terhadap angin, air laut, dan kekeringan
• Kekeringan Toleran pada kemarau selama 5 bulan • Sinar Matahari Lebih cocok pada sinar matahari penuh
dan dapat tumbuh baik pada tempat teduh • Pembekuan Tidak toleran pada kondisi beku
• Waterlogging Toleran pada kondisi dikelilingi air (waterlogging) pada area pantai. Sumber: Friday dan Okano 2005.
Buah nyamplung berbentuk bulat seperti peluru dengan ujung berbentuk lancip berwarna hijau terusi selama masih bergantung pada pohon tetapi menjadi kekuning-kuningan atau berwarna seperti kayu yang sudah luruh setelah
masak, daging buahnya tipis yang lambat laun menjadi keriput, rapuh dan mengelupas, di dalamnya terdapat sebuah inti yang berwarna kuning terutama jika dijemur (Heyne 1987). Biji digunakan untuk mengobati kudis, bila dimakan akan mengakibatkan mabuk bahkan kematian akan tetapi minyaknya dapat digunakan untuk menyembuhkan borok dan penumbuh rambut dan untuk penerangan (Heyne 1987). Inti nyamplung mengandung abu 1,7%, protein kasar 6,2%, minyak 55,5 %, pati 0,34%, air 10,8%, hemiselulosa 19,4 %, dan selulosa 6,1% (Wilde et al. 2004).
Sumber: http://www.aromatrading.co.uk/calophyl [26 Juni 2005]. Gambar 1 Tanaman dan buah nyamplung.
2.1.2 Minyak Biji Nyamplung
Inti (kernel) nyamplung mempunyai kandungan minyak yang sangat tinggi yaitu sebesar 75% (Dweek dan Meadows 2002), 71,4% pada inti yang kering dengan kadar air 3,3% (Heyne 1987), 40-73 % (Soerawidjaja 2005), 55,5% pada
inti yang segar dan 70,5% pada inti yang benar-benar kering (Greshoff dalam Heyne 1987). Pada inti yang kering proses pengepresan dapat menghasilkan minyak 60% (Dweek dan Meadows 2002). Produksi biji nyamplung mencapai 100 kg per pohon (Dweek dan Meadows 2002; Friday dan Okano 2005). Minyak dapat diperoleh dengan pengepresan dingin (dari 100 kg buah akan dihasilkan 18 kg minyak) kemudian dijernihkan sehingga dihasilkan minyak yang berwarna kuning kehijauan serupa dengan minyak olive dengan aroma dan rasa yang hambar (Dweek dan Meadows 2002). Buah yang matang tapi belum bertunas dipecah tanpa merusak inti kemudian secara cepat dipindahkan dan disusun dalam lapisan yang tipis dan dibeberkan pada matahari (jika tidak segera dibeberkan maka akan ditumbuhi jamur) selanjutnya dilakukan proses pengeringan inti sampai kehilangan bobot 2,5 gram dari setiap 7 gram inti segar sehingga bobot kering menjadi kira-kira 4,5 gram dan setelah kering inti menjadi kecoklatan dan kandungan minyaknya akan naik (Dweek dan Meadows 2002). Selama pengeringan akan terjadi kehilangan kemampuan bertunas, dan pengeringan secara sempurna dengan kondisi cuaca cukup kering inti dapat disimpan pada waktu lama (Dweek dan Meadows 2002).
Menurut Heyne (1987) minyak nyamplung digunakan sebagai obat oles terhadap encok dan telah dipasarkan ke Eropa dengan nama ndilo-olie. Minyak nyamplung di beberapa daerah digunakan untuk penerangan (Dweek dan Meadows 2002 ; Lele 2005). Bau minyak nyamplung yang tidak sedap dapat dihilangkan dan kegunaanya dapat ditingkatkan setelah dinetralkan pada suhu 60oC dengan alkali (Heyne 1987). Tidak seperti kebanyakan minyak sayur, minyak nyamplung (tamanu oil) tidak terkandung dalam buah yang segar akan tetapi terbentuk selama proses pengeringan biji (Dweek dan Meadows 2002). Minyak
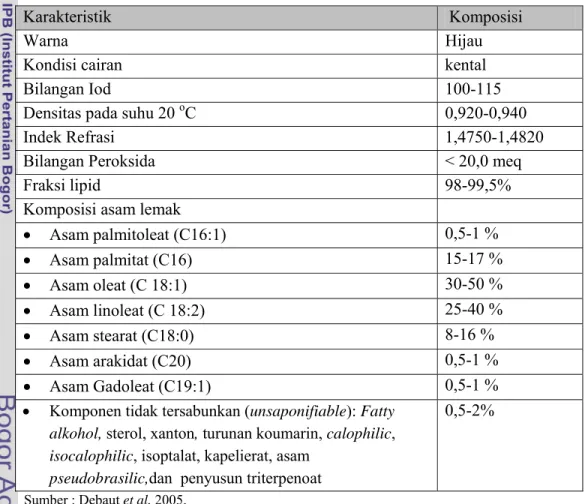
nyamplung (Tamanu oil) adalah minyak yang berharga dan merupakan minyak kental berwarna coklat kehijauan beraroma seperti karamel didapat dari buah yang telah matang dari pohon Callophyllum inophyllum L. mempunyai fungsi penyembuhan yang signifikan khususnya untuk jaringan terbakar (Kilham 2003). Minyak nyamplung mempunyai karakteristik spesifik yaitu berwarna hijau tua kental, dan mempunyai aroma yang menyengat. Karakteristik minyak nyamplung dapat dilihat pada Tabel 2.
Tabel 2 Karakteristik fisiko-kimia minyak Calophyllum inophyllum L.
Karakteristik Komposisi
Warna Hijau
Kondisi cairan kental
Bilangan Iod 100-115
Densitas pada suhu 20 oC 0,920-0,940
Indek Refrasi 1,4750-1,4820
Bilangan Peroksida < 20,0 meq
Fraksi lipid 98-99,5%
Komposisi asam lemak
• Asam palmitoleat (C16:1) 0,5-1 % • Asam palmitat (C16) 15-17 % • Asam oleat (C 18:1) 30-50 % • Asam linoleat (C 18:2) 25-40 % • Asam stearat (C18:0) 8-16 % • Asam arakidat (C20) 0,5-1 % • Asam Gadoleat (C19:1) 0,5-1 %
• Komponen tidak tersabunkan (unsaponifiable): Fatty alkohol, sterol, xanton, turunan koumarin, calophilic, isocalophilic, isoptalat, kapelierat, asam
pseudobrasilic,dan penyusun triterpenoat
0,5-2%
Sumber : Debaut et al. 2005.
Menurut Lele (2005) biodiesel dapat dibuat dari minyak non edible yang diperoleh dari Jatropha curcas, Pangamia pinnata, Calophyllum inophyllum L. (Nagchampa), Havea brasiliensis (biji karet) dan sebagainya. Hal itu sesuai dengan Soerawidjaja (2001) yang menyatakan bahwa terdapat 30 jenis tanaman
yang memilki potensi minyak yang dapat digunakan sebagai biodiesel diantaranya adalah kelapa (Cocos nusifera), kecipir (Psophocarpus tetrag), kelor (Moringa olifera), nimba (Azadirachta indica), saga hutan (Adenathera pavonina), nyamplung (Calophyllum inophyllum L.), dan lain-lain. Kadar minyak inti nyamplung relatif tinggi (40-73%) dibanding dengan jarak pagar (40-60%), saga utan (14-28%), kapok (24-40%), kesumba (30-60%), kelor (30-49%), kemiri (57-69%) dan daging buah kelapa sawit (45-70%).
2.2 Biodiesel 2.2.1 Biodiesel dan Manfaat Penggunaannya
Biodiesel secara kimia didefinisikan sebagai metil ester atau monoalkil ester yang diturunkan dari minyak/lemak alami, seperti minyak nabati, lemak hewan atau minyak goreng bekas yang dapat digunakan langsung atau dicampur dengan minyak diesel (Peeples 1988 ; Darnoko et al. 2001). Biodiesel adalah bahan bakar diesel alternatif yang terdiri dari alkil monoester asam lemak dari minyak sayur atau lemak hewan (Canakci & Van Gerpen 2003). Metil ester atau etil ester merupakan senyawa yang relatif stabil, berupa cairan pada suhu ruang (titik leleh antara 4-18 oC), non korosif, titik didihnya rendah. Metil ester lebih disukai
daripada etil ester untuk alasan ekonomis dan stabil secara pirolitik dalam proses distilasi fraksional (Herawan dan Sadi 1997).
Penggunaan CPO sebagai bahan baku untuk produksi biodiesel mempunyai keuntungan karena biodiesel yang dihasilkan mempunyai bilangan setana yang tinggi yaitu 62 lebih tinggi dari persyaratan minimal yaitu 45 (Darnoko et al. 2001). Negara-negara Eropa seperti Austria, Perancis dan Itali memproduksi metil ester dari biji bunga lobak dikenal dengan istilah RME (rapeseed oil methyl ester),
metil ester dari minyak kedele dikenal dengan SME (soybean oil methyl ester) dan methyl ester dari minyak sawit dikenal dengan POME (palm oil methyl ester) (Nakazono 2001).
Keuntungan penggunaan biodiesel diantaranya adalah: sifat bahan bakunya dapat diperbarui (renewable), penggunaan energi lebih efisien, dapat menggantikan bahan bakar diesel dan turunannya dari petroleum, dapat digunakan kebanyakan peralatan diesel dengan tidak ada modifikasi atau hanya modifikasi kecil, dapat mengurangi emisi/ pancaran gas yang menyebabkan pemanasan global, dapat mengurangi emisi udara beracun, bersifat biodegradable, cocok untuk lingkungan sensitif dan mudah digunakan (Tyson 2004). Emisi gas buang dari uji ketahanan mesin motor diesel selama 250 jam dari penggunaan B30 dibandingkan dengan solar menunjukkan bahwa kadar CO < 7,3%, CO2 < 3,7%, NOx < 3,2%, HC lebih
rendah 11,4%, SO2 < 20,9% dan opasitas gas buang < 27,8% (Legowo et al. 2006).
Emisi gas buang dari uji jalan dari penggunaan B30 dibandingkan dengan solar menunjukkan bahwa kadar CO < 2,06%, CO2 < 3,22%, NOx < 7,82%, HC <
4,73%, SO2 < 6,33% dan opasitas gas buang lebih rendah 23,18% (Legowo et al.
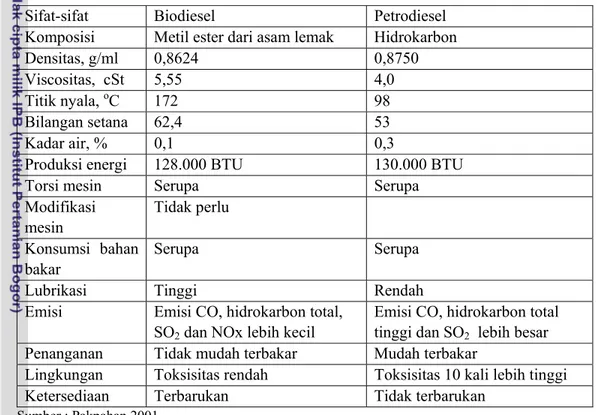
2006). Penggunaaan biodiesel akan menurunkan biaya pemeliharaan (penggantian filter oli, penggantian filter bahan bakar, penggantian filter udara) dan peningkatan kualitas udara emisi cerobong (ammonia, free chlorine, NO2 dan Hidrolic acid) (Pakpahan 2001). Perbandingan sifat biodiesel dan petrodiesel disajikan pada Tabel 3.
Menurut Fajar et al. (2003) penggunaan biodiesel dengan campuran 20% PME, 30 % PME dan 40 % PME pada mesin satu silinder (engine single cylinder Hydra) di Pusat Termodinamika Motor dan Propulsi BPPT menunjukkan bahwa
biodiesel 30 % (30% PME) mempunyai emisi asap CO dan HC paling rendah, keperluan bahan bakar emisi NO sama dibandingkan dengan bahan bakar diesel, dengan demikian biodiesel 30 % merupakan pencampuran biodiesel yang paling optimum.
Tabel 3 Perbandingan sifat biodiesel dan petrodiesel Sifat-sifat Biodiesel Petrodiesel Komposisi Metil ester dari asam lemak Hidrokarbon
Densitas, g/ml 0,8624 0,8750
Viscositas, cSt 5,55 4,0
Titik nyala, oC 172 98
Bilangan setana 62,4 53
Kadar air, % 0,1 0,3
Produksi energi 128.000 BTU 130.000 BTU
Torsi mesin Serupa Serupa
Modifikasi mesin Tidak perlu Konsumsi bahan bakar Serupa Serupa
Lubrikasi Tinggi Rendah
Emisi Emisi CO, hidrokarbon total, SO2 dan NOx lebih kecil
Emisi CO, hidrokarbon total tinggi dan SO2 lebih besar Penanganan Tidak mudah terbakar Mudah terbakar
Lingkungan Toksisitas rendah Toksisitas 10 kali lebih tinggi
Ketersediaan Terbarukan Tidak terbarukan
Sumber : Pakpahan 2001.
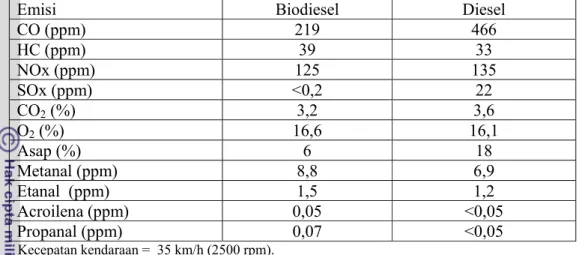
Dengan menggunakan biodiesel akan meningkatkan kualitas emisi udara dilihat dari parameter hidrokarbon, gas CO, CO2, NOx, SOx (Legowo et al. 2001
dan Nakazono 2001)seperti tercantum pada Tabel 4.
2.2.2 Produksi Biodiesel Melalui Proses Esterifikasi dan Transesterifikasi Proses produksi biodiesel dikembangkan oleh beberapa negara maju di dunia, contoh industri biodiesel di beberapa negara disajikan pada Tabel 5.
Tabel 4 Perbedaan karakteristik emisi bahan bakar diesel dan biodiesel e-OIL
Emisi Biodiesel Diesel
CO (ppm) 219 466 HC (ppm) 39 33 NOx (ppm) 125 135 SOx (ppm) <0,2 22 CO2 (%) 3,2 3,6 O2 (%) 16,6 16,1 Asap (%) 6 18 Metanal (ppm) 8,8 6,9 Etanal (ppm) 1,5 1,2 Acroilena (ppm) 0,05 <0,05 Propanal (ppm) 0,07 <0,05 Kecepatan kendaraan = 35 km/h (2500 rpm). Sumber : Nakazono 2001.
Tabel 5 Pabrik biodiesel di beberapa negara
No Perusahaan Kota Negara Kapasitas
terpasang (ton/tahun)
1 Biodiesel Industries Las Vegas USA 40.000
2 Biodiesel Industries California USA 3.500
3 Biodiesel Industries Colorado USA 10.000
4 Biodiesel Industries New South Wales Australia 20.000
5 Biodiesel Industries Texas USA 10.000
6 Impersial Western Product Coachelia USA 40.000
7 Ag Enviromental Products Sergeant Bluff USA 100.000
8 West Central Soy Ralston USA 40.000
10 Lurgi Life Science Marf Germany 100.000
11 Fortum Porvoo Finland 170.000
12 Argent Energy Motherwell UK 35.000
13 Biofuel corp Tesside UK 250.000
Menurut Lele (2005) proses produksi biodiesel dapat dilakukan dengan proses transesterifikasi secara batch pada suhu kamar, tekanan 1 atm dan katalis KOH seperti yang dilakukan di Comprimo/Vogel and Noot, Idaho University Conemann/Cold and Hann ataupun pada transesterifikasi secara kontinyu pada suhu 60-70 OC dengan katalis NaOH seperti dilakukan oleh Lurgi dan IFP/Sofiprotest. Di Indonesia biodiesel diproduksi di beberapa perusahaan/instansi diantaranya adalah PT Tracon Industri (500 liter/hari), PT Pindad (500 liter/hari), PT Energi Alternatif (1500 liter hari), ITB (500 liter/hari), BPPT (3.000 kg / hari),
PT Ganesha Energy (6.000 ton/tahun), PT Eterindo Wahanatama (100.000 ton/tahun) dan PT Sumiasih (36.000 ton/tahun).
Kebanyakan biodiesel di Indonesia diproduksi dari minyak sawit dan minyak jarak pagar pada hal menurut Soerawidjaja (2001) dan Lele (2005), biodiesel dapat dibuat dari berbagai jenis minyak dan lemak lain salah satunya adalah minyak nyamplung (Calophyllum inophyllum L.). Dalam lemak/minyak, yang memegang peranan penting dalam menentukan kualitas biodiesel adalah komposisi asam lemaknya. Komposisi asam lemak minyak sawit kasar (CPO), minyak nyamplung dan minyak jarak pagar dapat dilihat pada Tabel 6. Terdapat empat jenis asam lemak penyusun utama CPO dan minyak jarak pagar yaitu asam palmitat, asam stearat, asam oleat, dan asam linoleat yang mempunyai kemiripan dengan minyak nyamplung. Sifat-sifat fisiko kimia minyak nabati sebagai bahan baku biodiesel sangat dipengaruhi oleh jenis asam lemak penyusun minyak tersebut. Sifat-sifat beberapa jenis minyak sebagai bahan baku biodiesel dapat dilihat pada Tabel 7.
Tabel 6 Komposisi asam lemak beberapa jenis sumber minyak nabati Komponen Minyak Nyamplung a (%) Minyak Jarak pagarb (%) CPOc (%) Minyak Kanolad (%) Minyak Jagungd (%) Minyak Kedeled (%) Minyak Kelapad (%) Asam n-Kaprilat (C8) 0,1 7,7 Asam Kaprat (C10) 0,1 6,0 Asam Laurat (C12) - 0,9 46,7 Asam Miristat C14) - 1,3 0,3 0,1 18,3 Asam Palmitat (C16) 17,1 11,9 43,9 3,0 9,9 10,3 9,2 Asam stearat (C18) 9,05 5,2 4,9 1,8 2,0 3,9 2,9 Asam Oleat (C 18:1) 50,8 29,9 39,9 58,0 28,7 22,1 6,9 Asam Linoleat (C 18:2) 20 46,1 9,5 21,0 56,9 54,1 1,7 Asam Linolenat (C 18:3) 4,7 0,3 11,1 1,1 8,3 - Asam Arachidat (C20) - - 0,7 0,5 0,3 - Asam Erukat (C20:1) 3,3 - - 1,7 0,4 0,4 - a: Soerawidjaja et al. 2005, b: Haas & Mittelbach 2000, c: Allen et al. 2000, d: Hui 1996.
Teknologi proses produksi biodiesel satu tahap tidak cocok digunakan untuk memproduksi bahan yang mempunyai bilangan asam tinggi. Menurut Lele (2005) transesterifikasi hanya bekerja secara baik terhadap minyak yang mempunyai kualitas baik, apabila minyak mengandung asam lemak bebas
melebihi 1 % maka akan membentuk formasi emulsi sabun yang menyulitkan pemisahan biodiesel yang dihasilkan. Minyak yang mengandung asam lemak bebas lebih dari 2 % proses tidak dapat dilaksanakan (Lele 2005). Menurut Canakci dan Van Gerpen (2001) terbentuknya sabun pada proses produksi biodiesel dari minyak yang mempunyai kadar air dan kadar ALB tinggi akan menyulitkan proses pencucian dan memungkinkan hilangnya produk yang berguna, alternatifnya dilakukan dengan dua tahap reaksi dengan menggunakan katalis asam dan katalis basa.
Tabel 7 Sifat-sifat fisiko-kimia beberapa jenis minyak nabati yang digunakan sebagai bahan dasar biodiesel
Karakteristik Minyak sawit (CPO) Minyak inti sawit (PKO) Minyak Kelapa Minyak biji kapok Minyak jarak Minyak mete Bahan bakar diesel Densitas pada suhu 15 OC (kg/l) 0,92-0,95 0,90 0,92-0,94 0,92-0,93 0,962 0,92-0,98 0,80-0,86 Viskositas pada suhu 20 OC (cSt) 88,6 66,3 51,9 293 150-160 2-8 Nilai panas (MJ/kg) 39,5 39,7 37,5 3,7 45,2 Titik nyala (OC) 314 <260 270-300 >55 Bilangan Setana 42 >45 Titik didih (OC) 25-30 22-60 17 Air (%) 0,1 0,3-0,4 <0,25 <0,25 <0,20 Sulfur (%) <0,30 Sumber : Legowo et al. 2001.
Rendemen transesterifikasi dapat ditingkatkan dari 25% menjadi 96% dengan menurunkan kadar asam lemak bebas dan air masing-masing berturut-turut 10 % menjadi 0,23 % dan 0,2 % menjadi 0,02 % (Lee et al. 2002). Menurut Tyson (2004) minyak yang mengandung asam lemak bebas 10 % akan kehilangan rendemen biodiesel sebesar 30 % apabila diproses menjadi biodiesel dengan cara transesterifikasi.
Proses pembuatan biodiesel menurut Nakazono (2001) dilakukan dengan perlakukan pendahuluan untuk mengurangi kadar air dan kotoran kurang dari
0,05% dengan metode fisik misalnya filtrasi, pemisahan dengan spesific grafity dan evaporasi, selanjutnya dilakukan reaksi singkat (waktu < 5 menit, menggunakan penambahan NaOH atau KOH yang dilarutkan dalam metanol (MeOH), pemisahan gliserol dilakukan berdasarkan perbedaan secara spesifik grafity atau menggunakan sentrifugasi sehingga dihasilkan produk akhir biodiesel.
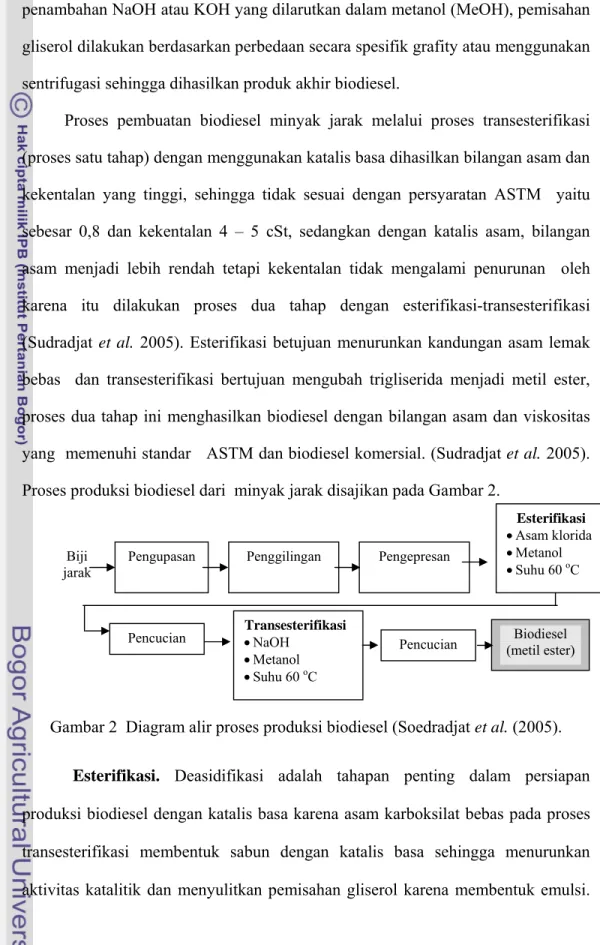
Proses pembuatan biodiesel minyak jarak melalui proses transesterifikasi (proses satu tahap) dengan menggunakan katalis basa dihasilkan bilangan asam dan kekentalan yang tinggi, sehingga tidak sesuai dengan persyaratan ASTM yaitu sebesar 0,8 dan kekentalan 4 – 5 cSt, sedangkan dengan katalis asam, bilangan asam menjadi lebih rendah tetapi kekentalan tidak mengalami penurunan oleh karena itu dilakukan proses dua tahap dengan esterifikasi-transesterifikasi (Sudradjat et al. 2005). Esterifikasi betujuan menurunkan kandungan asam lemak bebas dan transesterifikasi bertujuan mengubah trigliserida menjadi metil ester, proses dua tahap ini menghasilkan biodiesel dengan bilangan asam dan viskositas yang memenuhi standar ASTM dan biodiesel komersial. (Sudradjat et al. 2005). Proses produksi biodiesel dari minyak jarak disajikan pada Gambar 2.
Gambar 2 Diagram alir proses produksi biodiesel (Soedradjat et al. (2005). Esterifikasi. Deasidifikasi adalah tahapan penting dalam persiapan produksi biodiesel dengan katalis basa karena asam karboksilat bebas pada proses transesterifikasi membentuk sabun dengan katalis basa sehingga menurunkan aktivitas katalitik dan menyulitkan pemisahan gliserol karena membentuk emulsi.
Biji
jarak Pengupasan Penggilingan Pengepresan
Esterifikasi
•Asam klorida •Metanol •Suhu 60 oC
Pencucian Transesterifikasi •NaOH •Metanol •Suhu 60 oC
Biodiesel (metil ester) Pencucian
Minyak mengandung lebih dari 5 % asam lemak bebas akan terbentuk gel setelah penambahan KOH atau KOH (Canakci dan Van Gerpen 1999). Minyak yang mengandung 0,5 - 4 % akan menyebabkan kehilangan hasil transesterifikasi dan apabila minyak mengandung ALB sekitar 4% maka minyak tersebut sulit diproses menjadi biodiesel (Haas et al. 2005). Deasidifikasi dapat dilakukan dengan proses netralisasi atau dengan esterifikasi. Reaksi esterifikasi merupakan reaksi antara metanol atau etanol dengan asam lemak bebas sehingga terbentuk metil ester atau etil ester dengan katalis asam dan pemberian panas. Reaksi kimia esterifikasi adalah sebagai berikut:
Reaksi esterifikasi dipengaruhi oleh beberapa faktor diantaranya adalah jumlah pereaksi, (metanol dan asam lemak bebas), waktu reaksi, suhu, konsentrasi katalis, dan kandungan air pada minyak (Guner et al. 1995; Kirbaslar et al. (2000); Canakci dan Van Gerpen 2001; Oluwaniyi et al. 2003). Deasidifikasi adalah proses penting karena asam lemak bebas akan membentuk sabun dan dengan gliserol akan membentuk emulsi yang sukar dipisahkan pada proses transesterifikasi (Canakci dan Van Gerpen 1999). Menurut Sudradjat et al. (2005) perlakuan terbaik proses esterifikasi minyak jarak yang mengandung kadar air 1,54 %, bilangan asam 39,02 mg KOH/g minyak, bilangan penyabunan 186,08 mg KOH/g minyak dan bilangan ester teoritis sebesar 147,06 mg KOH/g minyak diperoleh pada penggunaan katalis HCl 1% (v/v), waktu reaksi 120 menit dan jumlah metanol sebanyak 10 % (v/v). Asam laurat, asam stearat, atau asam oleat secara lengkap dilakukan esterifikasi
R
1COOH
+
CH
3OH
R
1COOCH
3Katalis asam dan suhu
+
H
2O
Asam lemakdengan gliserol pada suhu 230-400 oC selama 3 jam jika menggunakan suhu 170-180 oC menjadi lebih lama (Hui 1996). Menurut Haas et al. (2002) air yang dihasilkan selama proses esterifikasi menghambat reaksi esterifikasi lebih lanjut. Menurut Oluwaniyi et al. (2003) esterifikasi dengan katalis HCl dan H2SO4
mempunyai kecenderungan yang sama, akan tetapi penggunaan katalis H2SO4
dengan nisbah molar asam lemak bebas terhadap alkohol 1:1 kurang baik dibandingkan dengan HCl. Katalis asam selain mengesterifikasi asam lemak bebas juga mengkonversi trigliserida menjadi metil ester tetapi kecepatan lebih rendah dibandingkan dengan transesterifikasi menggunakan katalis basa (Freedman et al. 1984). Menurut Van Gerpen et al. (2004) esterifikasi dengan katalis asam terhadap minyak kadar ALB tinggi dan telah dikeringkan terlebih dahulu memerlukan alkohol tinggi 20:1, suhu 60 oC, waktu 1-2 jam. Menurut Canakci dan Van Gerpen (2001) esterifikasi minyak kedele yang mengandung ALB asam palmitat 20% dengan menggunakan nisbah molar metanol 9:1 dan katalis asam sulfat 5 % dan 15% menunjukkan bahwa semakin lama waktu esterifikasi sampai dengan 0,5 jam penurunan kadar ALB semakin besar, akan tetapi antara 0,5 jam dengan 1 jam tidak ada perbedaan. Ringkasan beberapa proses esterifikasi dengan katalis asam dapat dilihat pada Tabel 8.
Transesterifikasi. Reaksi transesterifikasi disebut juga reaksi alkoholisis atau metanolisis karena menggunakan alkohol rantai pendek seperti metanol atau etanol dengan katalis asam atau basa (Hui 1996). Katalis basa lebih banyak digunakan karena reaksinya sangat cepat, sempurna dan dapat dilakukan pada suhu yang rendah. Transesterifikasi dengan katalis basa berlangsung antara metanol dan trigliserida melalui pembentukan berturut-turut digliserida dan monogliserida menghasilkan metil ester pada setiap tahapnya. Gambar reaksi transesterifikasi ditunjukkan pada Gambar 3.
Tabel 8 Ringkasan beberapa proses esterifikasi dengan katalis asam
No Ringkasan proses esterifikasi Sumber
1. Nisbah molar metanol terhadap ALB 10:1, waktu 30 menit, katalis asam sulfat 15% dari berat ALB menurunkan bilangan asam 41,33 mgKOH /gram menjadi 1,37 mgKOH /gram.
Canakci dan Van Gerpen 2001 2. Nisbah molar metanol terhadap ALB 20:1 , waktu 1 jam,
katalis asam sulfat 5% dari ALB, suhu 55-60 oC menurunkan
bilangan asam yellow grease dari 18,03 mgKOH /gram menjadi 4,26 mgKOH /gram, dilanjutkan esterifikasi ke dua dengan nisbah molar metanol terhadap ALB 40:1, waktu, katalis, suhu yang sama dapat menurunkan bilangan asam dari 4,26 mgKOH /gram menjadi 0,85 mgKOH /gram
Canakci dan Van Gerpen 2003
3. Nisbah molar metanol terhadap ALB 20:1 , waktu 1 jam, katalis asam sulfat 10% dari ALB suhu 55-60 oC dapat menurunkan bilangan asam yellow grease dari 79,2 mgKOH /gram menjadi 6,96 mgKOH /gram dilanjutkan dengan esterifikasi kedua dengan nisbah molar metanol terhadap ALB 40:1, waktu, katalis, suhu yang sama dapat
menurunkan bilangan asam dari 6,96 mgKOH /gram menjadi 1,54 mgKOH /gram
Canakci dan Van Gerpen 2003
4. Nisbah molar metanol terhadap ALB 10:1, katalis HCl 0,1 mol, waktu 105 menit menghasilkan konversi 84%
Oluwaniyi et al. 2003 5. Nisbah molar terhadap ALB 20:1, suhu 60 oC, waktu 1-2
jam . Van Gerpen et al. 2004 HC O H2C O C R'' O O C R' 3 CH3OH O H2C C R''' O CH3O CH3O CH3O C R'' O C R' O C R''' O HC H2C H2C OH OH OH Katalis Kalor + +
Gambar 3 Reaksi transesterifikasi (Ma et al. 1999 ;Van Gerpen et al. 2004).
Reaksi transesterifiksi dipengaruhi oleh faktor internal misalnya kandungan air, kandungan asam lemak bebas, dan kandungan zat terlarut maupun tak terlarut dan faktor internal seperti suhu, waktu, kecepatan pengadukan, jenis dan konsentrasi katalis dan jumlah nisbah molar metanol terhadap minyak (Ma dan
Hanna 1999; Darnoko dan Cheryan 2000; Cheng et al. 2004). Reaksi metanolisis mempunyai syarat yaitu minyak harus bersih, tanpa air dan netral, minyak yang mempunyai kandungan asam lemak bebas yang tinggi akan menghasilkan sabun yang akan mengurangi kebasaan katalis dan membentuk lapisan gel yang dapat mempersulit pemisahan dan pengendapan gliserol (Canaki dan Van Gerpen 2001). Kandungan asam lemak bebas dan air yang masing-masing lebih dari 0,5% dan 0,3% dapat menurunkan rendemen transesterifikasi minyak (Freedman et al. 1986).
Produksi minyak menjadi metilester dilakukan melalui reaksi transesterifikasi menggunakan metanol dengan katalis basa atau asam pada suhu 50-70 0C (Darnoko et al. 2001). Proses transesterifikasi dapat dilakukan secara curah (batch) atau sinambung (kontinyu) pada suhu 50-70 0C (Darnoko et al. 2001). Metilasi minyak sawit mencapai kesetimbangan setelah 60 menit pada suhu reaksi 50 0C (Darnoko dan Cheryan 2000).
Menurut Freedman et al. (1984), katalis NaOH yang dapat dipakai adalah 1,0% dari bobot minyak atau kurang dan nisbah molar terhadap minyak adalah 6:1, tidak ada peningkatan rendemen yang signifikan jika kedua variabel tersebut ditingkatkan dan reaksi ini menghasilkan 95% metil ester dalam waktu 1 jam pada suhu 650C. Ringkasan proses transesterifikasi dengan katalis basa dari beberapa sumber disajikan pada Tabel 9.
2.3 Kualitas biodiesel
Kualitas biodiesel sebagai produk bahan bakar mesin diesel ditentukan oleh beberapa parameter penting antara lain bilangan setana, viskositas, titik nyala, titik kabut, kandungan sulfur, kandungan fosfor, air dan endapan, residu karbon, kadar gliserol bebas, bilangan asam, kadar gliserol total dan lain-lain. Standar biodiesel menurut SNI 04-7182:2006 ditampilkan pada Tabel 10, sedangkan menurut ASTM D6751 ditampilkan pada Tabel 11.
Tabel 9 Ringkasan beberapa proses transesterifikasi dengan katalis basa
No Ringkasan proses transesterifikasi Sumber
1. Minyak kedele, NaOH 1%, suhu 600C, nisbah molar metanol
terhadap minyak 6:1 dan konversi 93-98%.
Freedman et al.
1984. 2. Minyak kedele, suhu 65 OC, nisbah molar metanol/minyak
/NaOH 6/1/0,08, waktu 35 menit dan konversi 98,10%
Filippis et al.
1995. 3. Nisbah molar metanol 6:1 dan katalis basa NaOH 0,9% dari
berat minyak kedele, suhu 50 oC dan konversi 90%
Noureddini dan Zhu 1997. 4. Minyak kasar dari Pongamia pinata, suhu 60 oC, nisbah
molar metanol terhadap minyak 10:1, waktu 60 menit dan konversi 85%
Karmee dan Chandha 2005. 5. Minyak sawit, katalis KOH 1%, suhu 60 0C, nisbah metanol:
minyak 6:1, waktu 30 menit, reaktor batch dan konversi
90-98%
Darnoko dan Cheryan 2000. 6. Minyak nabati, KOH atau NaOH 0,5-1%, suhu 60-80 oC,
tekanan 1 atmosfer, nisbah molar metanol minyak 6:1, pengaduan 5-10 menit setelah penambahan metanol dan konversi 94-98%
Lele 2005.
7. Lemak dari restoran bebas ALB, nisbah molar metanol terhadaplemak 6:1, waktu 60 menit, katalis NaOH dan konversi 96%
Lee et al. 2002.
8. Minyak goreng yang mengandung ALB 5.6% dan air 0,2%, suhu 65 oC, nisbah molar metanol terhadap minyak 6:1, NaOH
1,5% dari berat minyak dilarutkan, waktu 1 jam dan konversi 94.1%
Kusdiana dan Saka 2003. 9. Nisbah molar metanol terhadap minyak 6:1, suhu 65oC, katalis
NaOH 1,5% menghasilkan konversi 94%
Van Gerpen et al. 2004
10. Minyak goreng, nisbah molar butanol terhadap minyak 6:1, suhu 72 oC, waktu 3 jam, katalis alkali 0,2% dari berat minyak
dan konversi 96%
Lang et al. 2001.
11. Minyak kelapa sawit, nisbah molar metanol 6:1 dan katalis basa NaOH 0,125 mol /kg minyak sawit, waktu 15 menit dan konversi 99%
Cheng et al.
2004.
2.3.1 Titik Nyala
Persyaratan titik nyala diperlukan untuk keamanan bahan bakar biodiesel selama penyimpanan, transportasi dan penggunaan. Titik nyala adalah suhu paling rendah terbentuknya asap pada saat tes pengapian (flame test) (Kinast dan Tyson 2003). Menurut standar ASTM D975 persyaratan titik nyala B 100 adalah 150 0C lebih tinggi dari titik nyala bahan bakar diesel yaitu 70 0C. Titik nyala berkaitan dengan residu metanol yang tertinggal dalam biodiesel. Residu metanol dalam jumlah kecil mengurangi flash point ( metanol mempunyai titik nyala 11,11 oC) sehingga berpengaruh terhadap pompa bahan bakar, seals dan elastomers dan dapat menghasilkan sifat-sifat yang jelek dalam pembakaran (Tyson 2004).
Tabel 10 Standar Biodiesel menurut SNI 04-7182:2006
No. Parameter Satuan Metode Syarat
1. Massa jenis pada 40 oC kg/m3 ASTM D 1298 850-890 2. Viskositas kinematik pada
40 oC
mm2/s (cSt)
ASTM D445 2,3-6,0 3. Bilangan setana - ASTM D 613 min. 51 4. Titik nyala (mangkok
tertutup)
oC ASTM D 93 min. 100
5. Titik kabut oC ASTM D 2500 maks. 18
6. Korosi kepingan tembaga (3 jam pada 50 oC)
ASTM D 130 maks. no. 3 7. Residu karbon (mikro)
- dalam contoh asli - dalam 10 % ampas distilasi % -massa ASTM D 4530 Maks 0.05 maks. 0,30 8. Air dan sedimen % -vol ASTM D 2709 atau
ASTM 1796
maks. 0,05 * 9. Suhu distilasi 90% oC ASTM D 1160 maks. 360 10. Abu tersulfatkan % -massa ASTM D 874 maks. 0,02 11. Belerang ppm atau (mg/kg) ASTM D 5453 atau ASTM D-1296 maks. 100 12. Fosfor ppm atau (mg/kg) AOCS Ca 12-55 maks. 10 13. Bilangan asam mg-KOH/g AOCS Cd 3d-63 atau ASTM D 664 Maks 0,8 14. Gliserol bebas %- massa AOCS Ca 14-56 atau ASTM D 6584 maks.0,02 15. Gliserol total %- massa AOCS Ca 14-56 ASTM D 6584 maks.0,24 16. Kandungan ester alkil %-
massa
Dihitung ** min. 96,5 17. Bilangan Iodium % massa
(g-I2 / 100 g)
AOCS Cd 1-25 maks. 115
18. Uji Helphen - AOCS Cb 1-25 Negatif
* : dapat diuji terpisah dengan ketentuan kandungan sedimen maksimum 0,01%-vol 100(As-Aa-4,57Gt )
** : Kadar ester (%-massa) = --- As
As adalah bilangan penyabunan yang ditentukan dengan metode AOCS Cd 3-25 (mg KOH/g biodiesel)
A a adalah bilangan asam yang ditentukan dengan metode AOCS Cd 3-63 atau ASTM D-664 (mg KOH/g biodiesel)
Gt adalah kadar gliserol total dalam biodiesel yang ditentukan dengan metode AOCS Ca 14-56 (% massa)
2.3.2 Air dan Sedimen
Air dan sedimen harus sekecil mungkin (standar ASTM D6751 max 0,05% vol). Air dalam biodiesel akan menyebabkan kekeruhan yang mengindikasikan adanya kontaminan seperti surfaktan (Kinast dan Tyson 2003). Pengukuran air dan sedimen dilakukan dengan sentrifugasi. Menurut Tyson (2004) teknikpengeringan yang kurang baik selama proses atau adanya kontak bahan bakar dengan air selama transportasi dan penyimpanan dapat menyebabkan Biodiesel 100% (B 100) tidak memenuhi persyaratan dilihat dari kandungan air dan sedimen. Air akan mengkibatkan korosi dan mengkondisikan lingkungan yang cocok untuk mikroorganisme.
Tabel 11 Standar biodiesel menurut ASTM D6751-3
No. Kreteria mutu bahan bakar biodiesel Cara Uji Standar
1 Titik nyala (oC) D93 min 130
2 Air dan sedimen (% vol) D2709 maks 0,050 3 Viskositas kinematik 40oC (mm2/s) D445 1,9-6,0
4 Abu sulfat (% massa) D874 maks 0,02
5 Sulfur (% massa) D5453 maks 0,05
6 Korosi kepingan tembaga D130 maks No. 3
7 Bilangan setana D 613 min 47
8 Titik kabut (oC) D2500 Laporan konsumen 9 Residu karbon * (% massa) D 4530 maks 0,05
10 Bilangan asam (mg KOH/gram) D664 maks 0,80 11 Gliserol bebas (% massa) D6584 maks 0,020 12 Gliserol total (% massa) D6584 maks 0,240 13 Kandungan fosfor (% massa) D4951 maks 0,001 14 Suhu distilasi memperoleh kembali 90
% (T 90) ** (oC) D1160 maks 360
* Residu karbon saat kendaraan berjalan pada 100% sampel ** Ekivalen dengan suhu atmosfer
2.3.3 Viskositas.
Viskositas dan tegangan permukaan merupakan faktor yang penting dalam mekanisme terpecahnya serta atomisasi bahan bakar sesaat setelah keluar dari mulut pipa semprot (nozzle) menuju ruang bakar (Soerawidjaja et al. 2005). Minimum viskositas diperlukan untuk beberapa mesin, karena berkaitan dengan kehilangan power pada pompa injeksi dan kebocoran injektor. Persyaratan
viskositas biodiesel dibuat sama dengan persyaratan viskositas petroleum diesel. Viskositas yang tidak terlalu kecil akan menguntungkan karena dapat meningkatkan kemampuan daya lumas bahan bakar terhadap mesin kendaraan diesel walaupun bilangan yang tinggi (di atas 5,5 cSt) tidak diharapkan karena akan menghambat jalannya mesin karena terlalu kental. Bahan bakar yang mempunyai viskositas yang lebih besar menyebabkan pembakaran bahan bakar rendah oleh karena itu perlu pengenceran (Tyson 2004). Berdasarkan standar ASTM 975 viskositas pada suhu 40 0C maksimum 4,1 mm/s dan minimum 1,3 mm/s. Viskositas berkaitan dengan komposisi asam lemak dan tingkat kemurnian biodiesel (Mittelbach dan Remschmidt 2004). Pada umumnya, kontaminan bahan bakar dari proses pengolahan seperti residu gliserida akan berpengaruh terhadap visositas (Allen dan Watts 2000).
2.3.4 Abu Sulfat
Abu tersulfatkan menunjukkan adanya residu alkali dalam biodiesel seperti NaOH. Dengan demikian abu tersulfatkan yang tinggi menunjukkan pencucian biodiesel kurang sempurna.Abu sulfat mempunyai kontribusi dalam injector atau terjadinya penyumbatan (fouling) pada sistem bahan bakar (Tyson 2004).
2.3.5 Sulfur.
Sulfur dibatasi untuk mengurangi emisi polutan asam sulfat dan SO2 serta
untuk melindungi pengeluaran sistem katalis ketika bahan bakar disebarkan dalam sistem engine (Tyson 2004). Korosi yang disebabkan oksida belerang dapat menyebabkan keausan mesin karena setelah mesin berhenti terjadi kondensasi oksida dan dengan adanya air akan terbentuk asam sulfat yang dapat merusak dinding logam silinder dan sistem gas buang kendaraan bermotor (Surono dan Batti. 1980). Biodiesel pada umumnya mengandung kurang dari 15 ppm sulfur
(Tyson 2004) sehingga memenuhi standar ASTM D 6751 yaitu maksimum 0,05% atau 500 ppm.
2.3.6 Pengujian Korosi Kepingan Tembaga
Uji ini dilakukan untuk mengukur tingkat korosi tembaga oleh biodiesel yang berkaitan dengan kadar asam lemak bebas biodiesel tersebut (Kinast dan Tyson 2003). Korosi kepingan tembaga mengindikasikan kesulitan potensial Cu dan Br oleh pengaruh komponen biodiesel, dengan demikian diharapkan biodiesel tidak menyebabkan rusaknya Cu dan Br pada saat kontak dalam waktu yang lama (Tyson 2004). Penggunaan bahan bakar biodiesel B 100 sesuai standar D6751 selalu lolos dalam uji ini (Tyson 2004).
2.3.7 Bilangan Setana
Bilangan setana diperlukan untuk keperluan engine yang baik. Bahan bakar diesel konvensional harus mempunyai bilangan setana paling kecil 40 di Amerika Serikat. Bilangan setana yang lebih tinggi akan menolong memastikan start yang baik dan meminimumkan pembentukan asap putih (Tyson 2004). Batas bilangan setana untuk B 100 adalah 47 yang disebut dengan bahan bakar diesel premium. Biodiesel yang mengandung asam lemak jenuh (asam laurat, miristat, palmitat, stearat, arakhidat dan lain-lain) yang tinggi mempunyai bilangan setana yang tinggi sedangkan yang mengandung asam lemak dengan ikatan rangkap 1 (palmitoleat, oleat dan erukat) yang tinggi mempunyai bilangan setana sedang serta yang mengandung asam lemak dengan ikatan rangkap 2 atau lebih (linoleat, linolenat dan arakhidonat) yang tinggi mempunyai bilangan setana yang rendah (Tyson 2004). Komposisi asam lemak dalam biodiesel mempengaruhi sifat-sifat bilangan setana, titik awan, stabilitas dan emisi NOx seperti yang ditunjukkan pada Tabel 12.
Tabel 12 Sifat bahan bakar dilihat dari komposisi asam lemak Jenuh Satu ikatan
rangkap
Dua atau lebih ikatan rangkap Asam lemak 12:0,14:0, 16:0, 18:0, 20:0 dan 22:0 16:1, 18:1, 20:1, 22:1 18:2, 18:3
Bilangan setana Tinggi Sedang Rendah
Titik kabut Tinggi Sedang Rendah
Stabilitas Tinggi Sedang Rendah
Emisi NOx Reduksi Kenaikan tipis Kenaikan besar Sumber : Tyson 2004.
Menurut Soerawidjaja et. al. (2005) bilangan setana dari biodiesel dapat diprediksi dengan menentukan sifat fisik biodiesel seperti titik didih, viskositas, titik leleh, panas penguapan, dan densitas. Beberapa persamaan untuk menentukan bilangan setana disajikan pada Tabel 13 dan sifat-sifat fisik beberapa metil ester yang digunakan sebagai dasar penentuan bilangan setana dapat dilihat pada Tabel 14.
Tabel 13 Sifat-sifat fisik biodiesel yang dapat digunakan untuk memprediksi bilangan setana
Sifat fisik Persamaan R2 Standar
kesalahan Titik didih (oC) Y= (41,3) +0,2785X + 0,001209X 2 + 3E-06X3 0,9999 0,1
Viskositas (cSt) Y = (-23,48) + 61,6828X + (-12,7738X2) +
0,8769 X3 0,9985 1,4
Panas penguapan (Cal/gr)
Y = (-1054,9) + 32,324X + (-0,23097X2) 0,9930 1,4
Nilai kalor netto (kCal/mol) Y=(-62,96)+0,097X-1,69E-0,5X2 0,9921 2,6 Banyak atom C asam Y = (-57,26) +14,892X-0,4149X2 0,9919 2,6 Titik leleh (oC) Y = 58,22 + 0,556X 0,9822 3,4 Indeks bias Y (-2107,38) + 1522,21X 0,9805 3,5 Densitas (g/cm3) Y= 7216,14 + (-8848,96X) 0,9799 3,6
Sumber : Soerawidjaja et al. 2005.
2.3.8 Titik Kabut
Titik kabut penting untuk memastikan kinerja pada suhu yang dingin. Titik kabut B 100 lebih tinggi daripada titik kabut diesel konvensional (Tyson 2004). Titik kabut berhubungan dengan komposisi asam lemak yang ada dalam biodiesel.
Tabel 14 Sifat fisik beberapa metil ester Metil ester Bilangan
setana Titik didih (OC) Viskositas pada 40 oC (cSt) Bobot molekul Titik leleh (OC) Metil laurat 60,8 224 1,69 214,35 5 Metil miristat 73,5 262 2,28 242,41 18,4 Metil palmitat 74,3 323 3,23 270,46 28 Metil stearat 75,6 330 4,32 298,51 39 Metil oleat 55 356 5,79 296,49 -20 Metil linoleat 33 218,5 4,47 294,48 -35 Metil linolenat 13 215 3,68 292,46 -57
Sumber : Soerawidjaja et al. 2005.
Biodiesel yang mengandung asam lemak jenuh (asam laurat, miristat, palmitat, stearat, arakhidat) yang tinggi mempunyai titik kabut yang tinggi, yang mengandung asam lemak dengan ikatan rangkap satu (palmitoleat, oleat dan erukat) yang tinggi mempunyai titik kabut sedang, serta yang mengandung asam lemak dengan ikatan rangkap dua atau lebih (linoleat, linolenat dan arakhidonat) yang tinggi mempunyai titik kabut yang rendah (Tyson 2004).
2.3.9 Residu Karbon
Karbon residu mempunyai tendensi untuk terbentuknya deposit karbon dalam engine, untuk bahan bakar diesel konvensional residu karbon diukur pada residu destilasi 10 % (Tyson 2004). Pengotoran ruang bakar dan mesin diesel disebabkan oleh deposit karbon yang dapat terjadi dengan cepat jika kadar fraksi-fraksi yang memiliki titik didih tinggi dalam bahan bakar cukup besar atau jika bahan bakar mengandung komponen yang tidak dapat terbakar sempurna pada kondisi mesin berjalan normal (Surono dan Batti 1980). Sisa katalis mempunyai pengaruh terhadap nilai residu karbon yang lebih besar dibandingkan dengan asam lemak bebas dan gliserida (Schindlbauer 1998).
2.3.10 Bilangan Asam
Bilangan asam disebut juga bilangan netralisasi karena ukuran yang dipakai adalah jumlah basa (KOH) yang diperlukan untuk menetralisasi kandungan asam. Bilangan asam biodiesel menunjukkan asam lemak bebas yang berasal dari degradasi ester. Bilangan asam yang tinggi mengindikasikan adanya degradasi dari ester selama penyimpanan biodiesel yang kurang baik. Bilangan asam yang tinggi lebih dari 0,8 diasosiasikan terjadi deposit sistem bahan bakar dan mengurangi umur dari pompa dan filter (Tyson 2004).
2.3.11 Bilangan Gliserin Total dan Bebas
Bilangan gliserin total diukur dari jumlah seluruh gliserin yang ada dalam bahan bakar baik dalam bentuk terikat maupun bebas. Keberadaan gliserol dan sisa gliserida yang belum terkonversi disinyalir membahayakan mesin terutama karena adanya gugus OH yang secara kimiawi agresif terhadap logam bukan besi dan campuran krom selain itu juga menyebabkan deposit pada ruang pembakaran (Soerawidjaja et al. 2005). Konversi yang tidak sempurna dari minyak atau lemak menjadi biodiesel dan pencucian terhadap crude biodiesel yang tidak sempurna dapat membuat gliserin total yang tinggi. Gliserin total yang tinggi dapat menyebabkan penyumbatan (fouling) tanki penyimpanan sistem bahan bakar dan engine. Kadar gliserol bahan bakar yang melebihi batas minimum menyebabkan terjadinya plug pada filter dan masalah lainya (Tyson 2004). Menurut ASTM, jumlah senyawa gliserol total harus kurang dari 0,24% b/b.
2.3.12 Kandungan Fosfor
Kandungan fosfor dibatasi maksimum 10 ppm dalam biodiesel sebab fosfor dapat merusak catalytic converters dan fosfor diatas 10 ppm dapat dihasilkan dari beberapa minyak sayur (Tyson 2004). Kandungan fosfor biasanya muncul dalam bentuk zat yang bersifat seperti perekat yang dapat merusak katalis yang terdapat
pada mesin diesel sehingga dapat meningkatkan jumlah emisi partikulat ke udara (Soerowidjaja et al. 2003). Kandungan fosfor selain dipengaruhi oleh fosfor dari bahan baku juga dipengaruhi oleh proses pencucian setelah degumming dan proses esterifikasi apabila kedua proses tersebut menggunakan katalis asam fosfat.
2.4 Pengujian Karakteristik Biodiesel
Biodiesel minyak sawit B30 memenuhi peryaratan spesifikasi solar meliputi: spesific grafity, viskositas kinematik, index setana, kandungan sulfur, korosi keping tembaga, kandungan air, kandungan abu, titik nyala dan suhu distilasi 300 oC (Legowo et al. 2006). Parameter lain tidak memenuhi persyaratan yaitu conradson carbon residue dan bilangan asam total. Menurut Sudradjat et al. (2005) parameter kualitas yang penting dari biodiesel jarak pagar memenuhi ASTM PS-121 meliputi indek setana, viskositas kinematik, densitas, bilangan asam, abu tersulfatkan, air dan sedimen, residu karbon, kandungan sulfur dan titik nyala. Legowo et al. (2001) menyatakan bahwa beberapa parameter kualitas biodiesel sawit yang penting seperti titik nyala, air & sedimen, viskositas kinematik 40 oC, abu tersulfatkan, kandungan sulfur, korosi keping tembaga dan bilangan setana, memenuhi standar biodiesel ASTM D6751-3 (lihat Tabel 15).
2.5 Pengujian Kinerja Biodiesel
Biodiesel digunakan sebagai bahan bakar motor diesel secara langsung tanpa pencampuran ataupun dengan pencampuran solar pada berbagai perbandingan. Menurut Legowo et al. (2006) motor diesel diklasifikasikan menjadi tiga jenis yaitu motor diesel putaran tinggi (≥ 1000 rpm) dengan bahan bakar minyak solar, putaran sedang (400 sampai < 1000 rpm) dengan bahan bakar minyak diesel dan putaran rendah (<400 rpm) dengan bahan bakar minyak bakar.
Tabel 15 Karakteristik metil ester minyak sawit dan campurannya
No. Karakteristik Produk Spesifikasi Diesel Indonesia
Metil Ester
Diesel : Metil Ester 70:30
Diesel Min Max Methode ASTM 1 Spec. Gravity 60/60 oF (g/ml) 0,88 0,85 0,83 0,82 0,87 D1298 2 Bilangan setana 53,5 60,2 63 48 - D976 3 Viskositas kinematik 40 oC ( CSt) 4,97 4,07 3,78 1,6 5,8 D445 4 Pour Point (oC) 12 6 3 - 18 D97
5 Residu konsentrasi karbon (%-wt)
0,03 0,02 0 - 0,1 D189
6 Kandungan sulfur (%-wt) 0,03 0,1 0,14 - 0,5 D1551
7 Copper Strip Corr. 100 oC 2 hrs IA IA IA - No.1 D130 8 Warna ASTM 5 4 3,5 - 3 D 1500 9 Bilangan netralisasi • SAN (mg KOH/g) • TAN (mgKOH/g) • TBN( mg KOH/g) nil 10,6 nil nil 2,98 nil nil 0,15 0,27 nil 2,42 - nil - - D664
10 Titik nyala COC ( oC) 186 - D92
11 • Distilation ( oC) 305 192 187 D 86 • IBP ( oC) 319 225 201 • Rec. 5% Vol ( oC) 320 243 227 • Rec. 10% Vol ( oC) 321 272 250 • Rec. 60% Vol ( oC) 340 328,5 324 • Rec. 70% Vol ( oC) 346 338,5 342 • Rec. 80% Vol ( oC) - 356 368
12 Kandungan abu (%-wt) 0,01 0 nil - 0,01 D482
13 Kandungan air (%-vol) Trace Trace Trace - - D95
14 Nilai kalori (Btu/lb) 16,83 20,764 22,45 - - D240
15 Ekstrak sedimen (%-wt) 0,01 nil nil nil nil D473
16 BS&W (%-vol) Trace Trace nil - - D1796
Sumber : Legowo et al. 2001.
Spesifikasi mutu minyak bakar lebih rendah daripada minyak diesel dan minyak diesel lebih rendah daripada solar (Legowo et al. 2006). Motor diesel putaran tinggi digunakan untuk otomotif, traktor dan mesin gergaji, motor diesel putaran sedang digunakan pada pembangkit listrik tenaga diesel (PLTD) dan kapal laut sedangkan motor diesel putaran rendah digunakan untuk PLTD dan kapal laut berukuran besar (Legowo et al. 2006).
Uji coba penggunaan campuran biodiesel Methyl Ester Rapeseed Oil (RME) 27,9% dengan 2-D diesel (2D) 82,1% pada kendaraan truk terbuka (pickup truck)
dengan mesin diesel 5,9 L pada jarak 161000 km (100000) mil menunjukkan bahwa pemakian RME menghasilkan penurunan tenaga 5% dan penurunan densitas asap 32% sedangkan untuk pemakaian 20RME menghasilkan penurunan tenaga 1,5% dan penurunan densitas asap 6,6% dari 2-D serta tidak terjadi kerusakan mesin (Peterson et al. 1999).
Uji kinerja mesin stasioner type 4-stroke diesel engine, No. Cylender 4, displacement 2,238 cm3, ratio kompresi 21:1, bore stroke 88 x 92 mm menunjukkan bahwa torsi mesin menurun ketika kandungan ester dinaikkan, dan torsi mesin maksimum untuk minyak diesel diperoleh pada kecepatan 2500 rpm yaitu 117nM lebih tinggi pada penggunaan campuran minyak diesel dan metil ester 70/30 yaitu 114nM (Legowo el al. 2001). Uji ketahanan mesin selama 250 jam terhadap biodiesel sawit B30 dibandingkan dengan bahan bakar solar (B00) adalah torsi motor lebih rendah 2,77%, daya lebih rendah 2,77%, konsumsi bahan bakar lebih tinggi 5,94% deposit nosel injektor lebih tinggi 3,2%, deposit piston lebih tinggi 4,20%, deposit klep lebih tinggi 0,85%, deposit kepala silinder lebih tinggi 30,84% dan deposit pada saringan bahan bakar lebih tinggi 57,3% (Legowo et al. 2006). Menurut Reksowardojo (2006) pada umumnya hasil pengujian bed test dan road test menunjukkan bahwa bahan bakar biodiesel yang diproduksi memenuhi standar FBI-S01-03 (SNI 04-7182-2006) tidak signifikan merubah kinerja mesin, gas emisi, dari mesin baik kondisi mesin diesel stasioner maupun mesin diesel kendaraan bermotor.
2.6 Perancangan Proses Produksi Biodiesel
2.6.1 Perancangan Proses
Perancangan merupakan proses kreatif dan berdisiplin untuk memecahkan masalah mencakup pendefinisian dan penyelesaian masalah dengan menggunakan
prinsip metode ilmiah dan seni, informasi teknis, dan imajinasi menentukan struktur, mesin, proses atau sistem baru yang memenuhi fungsi yang diinginkan dengan nilai ekonomis dan efisiensi tinggi (Johnston et al. 2000). Proses perancangan pada intinya merupakan kegiatan berurutan secara sistematis dan terpadu dalam bentuk sintesis yaitu bagaimana suatu masalah yang sulit dan kompleks diurai menjadi beberapa masalah yang lebih mudah kemudian dilanjutkan dengan menggabungkan masing-masing pemecahan masalah menjadi pemecahan masalah aslinya (Johnston et al. 2000). Skema proses perancangan menurut Roy dan Cross dalam Johnston et al. (2000) dapat dilihat pada Gambar 4.
Gambar 4 Model proses perancangan (Roy dan Cross 1983 diacu dalam Johnston et al. 2000). invensi Sumber ide: • Kreativitas individu/tim • Penelitian pasar • Masukan konsumen • Produk pesaing • Komponen/material baru • Penelitian dasar • Masalah yang harus
diselesaikan • Tantangan • Kemampuan teknologi, pengetahuan, material termasuk keterampilan Engineering science
Sketsa model / pola Pengembangan percobaan
Spesifikasi dan disain prototipe
Pengembangan manufacturing Rancangan produk dan
peralatan Produksi Pemasaran Inovasi Science Pengembangan bertahap Inovasi tambahan dan pengembangan rancangan Maturity Penurunan / penggantian Engineering design
Dua teknik dasar dalam sintesis proses adalah teknik heuristik dan algoritma. Teknik algoritma adalah analisis sederhana untuk menganalisis masalah komplek dengan cara pengamatan susunan terstruktur (structural array) (sedangkan teknik heuristik adalah teknik pemilihan proses berdasarkan logika dan informasi dasar (Ruud dan Watson 1973). Sintesis proses secara heuristik merupakan pengambilan keputusan berdasarkan teori dan penyelesaian yang dapat dipercaya: rule of thumb, spekulasi, dan subyektif ( Seider et al. 1999). Teknik heuristik dalam sintesis proses adalah proses penjabaran sejumlah langkah praktis untuk mencapai tujuan kegiatan.
Beberapa teknik heuristik dalam sintesis proses dikembangkan oleh Rudd dan Watson (1973), Douglas (1988) dan Seider et al. (1999). Sintesis proses menurut Ruud dan Watson (1973) meliputi: (1) pemilihan jalur reaksi proses, (2) alokasi bahan atau pereaksi, (3) pertimbangan teknik pemisahan atau proses hilir (4) pemilihan operasi pemisahan dan (5) pemaduan atau integrasi rancangan satu sampai empat. Sedangkan menurut Douglas (1988) sintesis proses meliputi: (1) teknis reaksi/proses (2) analisis input-output (3) pengalokasian output dan (4) operasi pemisahan dan jaringan penukar panas. Sintesis proses menurut Seider et al. (1999) meliputi: penghilangan / memperkecil perbedaan (2) distribusi bahan (3) teknik pemisahan (4) eliminasi dan (5) integrasi.
Perancangan proses yang bersifat interaktif juga dikembangkan oleh Sinnot (1999) seperti disajikan pada Gambar 5. Tahapan penting dalam perancangan tersebut adalah pengumpulan data, sifat fisika, dan metoda dan pemilihan dan evolusi proses (optimasi) seperti data kinetika reaksi. Perancangan proses melalui analisis sistem proses disampaikan oleh Hartmann dan Kaplick (1990) seperti disajikan pada Gambar 6.
Gambar 5 Model proses perancangan interaktif (Sinnot 1999).
Gambar 6 Perancangan proses melalui tahapan analisis sistem proses (Hartmann dan Kaplick 1990).
Tahapan perancangan proses kimia untuk menghasilkan rancangan rinci (detailed design) dikembangkan oleh Seider et al. (1999) pada dasarnya terdiri atas peluang dan permasalahan, kreasi proses dan pengembangan proses seperti disajikan pada Gambar 7.
Tujuan (spesifikasi rancangan) Pengumpulan data, sifat fisika, (metoda perancangan sifat fisik)
Generalisasi dari perekaan rancangan yang mungkin
Seleksi dan evaluasi (optimisasi) Rancangan akhir Tujuan (Spesifikasi rancangan) Sintesis (perancangan sistem) Analisis / Modeling dan Simulasi Optimasi dan Evaluasi
(Multiobjective) Apakah properties sistem tercapai Tujuan, spesifikasi kebutuhan Sistem yang ada
Rancangan proses akhir ya
Pengembangan proses berdasarkan kasus
`
Gambar 7 Tahap perancangan proses kimia (Seider et al. 1999). Sintesis proses awal: reaksi, separasi, perubahan operasi,
integrasi tugas, seleksi peralatan
ya
tolak Kreasi proses
(Process creation)
Menciptakan flowsheet proses
Integrasi proses
Pengetesan Pilot-Plant Modifikasi flowsheet
tdk
Proses rinci
Sintesis – Metode Algoritma
Sintesis separasi Analisis hukum / aturan
Integrasi panas dan daya
tdk Konstruksi Startup Operasi Penilaian start up Peralatan tambahan Simulasi dinamik
• Analisis keamanan dan uji ketahanan
• Pengetesan pilot plant
Penilaian pengendalian : Sintesis struktrur pengendalian, Analisis pengendalian,Simulasi dinamik
Peluang(Opportunity)
Survei literatur
Percobaan
Kreasi database awal (Preliminary Databse Creation)
Create a detailed database
Rancangan rinci (Detailed Design): kondisi optimum proses, ukuran alat & estimasi biaya modal
tolak
ya
ya
Menganalisis permasalahan
Simulasi model
Rancangan akhir: gambar peralatan, diagram perpipan, diagram instrumentasi, lay out
peralatan, skala model konstruksi,
Apakah ada keuntungan kasar?
tdk
Apakah proses menjanjikan ?
Apakah proses feaseble?
Perancangan proses dilakukan karena adanya peluang Opportunity) untuk menghasilkan produk yang menguntungkan dan memuaskan serta adanya permasalahan langsung dari masyarakat (Seider et al. 1999). Permasalahan dirumuskan secara spesifik berdasarkan informasi dari survei literatur. Informasi yang dimaksud berkaitan dengan bahan baku, skala proses, permintaan pasar, harga jual produk dan lain-lain. Invensi dalam perancangan proses dimulai dengan membuat pernyataan masalah sederhana (statemen problem primitif), kemudian dilanjutkan pembentukan tim perancang, pengumpulan informasi, kreasi proses untuk menyelesaikan masalah spesifik.
Kreasi proses dilakukan setelah permasalahan dirumuskan dan survei literatur dilaksanakan. Kreasi proses dilakukan melalui pengumpulan data sifat-sifat termofisika bahan kimia dan percobaan laboratorium. Kegiatan terpenting dari kreasi proses adalah sintesis yang terdiri atas eliminasi perbedaan tipe molekul, pencampuran, pemisahan, eliminasi perbedaan suhu, tekanan dan fase dan integrasi proses (Seider et al. (1999). Kreasi proses diakhiri dengan analisis keuntungan kasar. Proses dihentikan ketika harga produk melebihi harga bahan baku.
Pengembangan proses hanya dilakukan terhadap proses yang memberikan keuntungan. Tim perancang membuat diagram alir (flowsheet) proses yang detail disertai dengan neraca masa, neraca energi dan daftar peralatan. Beberapa kasus dapat diselesaikan dengan kumputer program HYSYS. Tiga alternatif kegiatan ditambahkan meliputi kreasi data rinci (Create a detailed database), pengetesan Pilot-Plant dan simulasi model. Kreasi data rinci dilakukan untuk medetailkan rancangan, seperti reaksi kinetik, fisibilitas pemisahan, ukuran peralatan dan lain-lain. Pengetesan pilot plant dilakukan untuk mengkonfirmasi variasi peralatan yang akan dioperasikan dan untuk menghaluskan data. Simulasi model proses dilakukan untuk generalisasi data berkaitan dengan komposisi dan sifat fisik bahan kimia, tahapan proses, kondisi operasi dan lain-lain. Simulasi dapat menggunakan data hasil regresi dari percobaan di laboratorium. Akhir kegiatan pengembangan adalah
analisis fisibilitas, jika diketemukan tidak fisibel maka kembali pada tahapan kreasi proses atau integrasi proses.
Inti dari perancangan proses adalah menemukan pilihan-pilihan proses yang layak untuk dikembangkan sehingga pemilihan proses merupakan titik awal yang cukup menentukan (Suryani dan Mangunwidjaja 2002). Perancangan proses berhubungan erat dengan kegiatan sintesis yang merupakan kegiatan yang berurutan dan terpadu. Dalam sintesis dilakukan pemilihan proses dengan mengikuti kaidah umum (heuristik) seperti mempertimbangkan biaya rendah, aman, memenuhi persyaratan lingkungan dan mudah mengoperasikannya. Proses perancangan dan penilaian teknologi produksi biodiesel dilakukan oleh Zhang et al. (2003) dengan menggunakan empat alternatif yaitu (1) bahan baku minyak sayur asli dengan katalis basa; (2) bahan baku minyak goreng bekas dengan katalis basa ; (3) bahan baku minyak goreng bekas dengan katalis asam; dan (4) bahan baku ekstraksi heksan dengan katalis asam dengan.
2.6.2 Kinetika Reaksi pada Proses Pembuatan Biodiesel
Kinetika reaksi kimia adalah ilmu yang mempelajari laju reaksi kimia secara kuantitatif serta faktor-faktor yang mempengaruhi kecepatan reaksi kimia tersebut. Kinetika reaksi dalam reaksi kimia adalah laju perubahan konsentrasi pereaksi atau hasil reaksi pada suatu periode waktu tertentu (Petrucci 1992). Kinetika reaksi berguna untuk menetapkan kondisi operasi, metode pengendalian, kebutuhan peralatan dan teknologi dari suatu proses kimia, sehingga dapat dimanfaatkan untuk merancang reaktor yang sesuai (Petrucci 1992). Menurut Wallas (1981) kinetika reaksi mempunyai beberapa fungsi utama yaitu: (1) menentukan mekanisme reaksi kimia; (2) mengumpulkan data percobaan secara matematis atau membuat persamaan matematik untuk mewakili data percobaan; (3) merancang reaktor yang sesuai dan (4) menetapkan kondisi operasi, cara pengontrolan dan alat-alat bantunya. Laju reaksi kimia dinyatakan dengan satuan mol /liter-detik adalah jumlah mol reaktan per satuan volume yang bereaksi dalam
waktu tertentu. Syarat terjadinya reaksi kimia adalah energi kinetik molekul harus melebihi energi aktivasi. Energi kinetik ditingkatkan dengan meningkatkan suhu reaksi dan pengadukan, sedangkan katalis berperan untuk mendapatkan jalan reaksi alternatif yang mengarahkan pada reaksi dengan energi aktivasi lebih rendah (Petrucci 1992).
2.6.2.1 Kinetika Reaksi Esterifikasi. Reaksi esterifikasi antara metanol dengan asam lemak bebas secara umum dapat digambarkan sebagai berikut:
k1
R1COOH + R2OH R1COO–R2 + H2O
k2
d[ALB] / dt = - k 1[ALB][A] + k 2 [H2O] [E]
d[E]/dt = - k 1[ALB][A] + k 2[H2O] [E]
d[ALB] / dt = d[E]/dt
Menurut Hangx et al. (2001) kinetika reaksi esterifikasi antara etanol dengan asam asetat dengan katalis asam membentuk etil asetat menunjukkan bahwa tetapan laju reaksi pembentukan etil asetat (k1) jauh lebih besar daripada
tetapan laju reaksi penguraian (k2), nilai k1 65 oC adalah 0,147 mol/kg-s sedangkan
k2 65 oC adalah 0,0268 mol/kg-s. Kondisi tersebut juga ditemukan oleh Nijhuis et
al. (2001) yang menyatakan bahwa tetapan laju reaksi pembentukan ester dari asam heksanoat dengan etanol (k1) jauh lebih besar daripada tetapan laju reaksi
penguraian ( k2), nilai k1 = 0,46 l/g katalis- menit sedangkan k2 adalah 0,l/g
katalis-menit.
Pola grafik konsentrasi asam dengan waktu selama proses esterifikasi berdasarkan penelitian Kirbaslar et al. (2000); Guner et al. (1996); Oluwaniyi et al. (2003) adalah turun sebanding dengan peningkatan konsentrasi alkil ester sampai dengan waktu tertentu kemudian konstan. Berdasarkan pola hubungan konsentrasi asam asetat dan waktu, dengan menggunakan metode integrasi dengan asumsi reaksi berjalan secara irreversibel menunjukkan bahwa laju reaksi orde dua
merupakan plot yang paling baik dari seluruh percobaan (Guner et al. 1996) seperti ditunjukkan pada Gambar 8. Kondisi tersebut sesuai dengan hasil penelitian Grezik et al. (2003) yang menyatakan bahwa reaksi esterifikasi antara alkohol berupa n-heksanol dengan asam malat anhidrid dengan katalis tetrabutil titanat mempunyai orde reaksi dua.
0,000 0,005 0,010 0,015 0,020 0,025 0,030 0,035 0,040 0 25 50 75 100 125 150 175 Waktu (Menit) 1/C
Gambar 8 Plot hubungan seperkonsentrasi asam (1/C) dengan waktu reaksi selama proses esterifikasi (Guner et al. 1996).
Penetapan kinetika reaksi esterifikasi asam malat anhidrat dengan n-heksanol menggunakan katalis asam sulfat anhidrat 0,05%-0,2% dan tetrabutil titanat anhidrat pada suhu 383-433 K dengan perbandingan alkohol dan asam malat anhidrat 3:1, 5:1, dan 10:1 melalui reaksi dua tahap yaitu pembentukan monoester dan diester dilakukan oleh Gresik et al. (2003) sebagai berikut:
• Katalis asam sulfat
r = k CCat Cm k = 4,63 10 5 exp(-14400±200/RT) [m3/(mol/min)]
• Katalis tributil titanat
r = k CACm k = 1,86 10 3exp(-17200±400/RT) [m3/(mol/min)]
• Tidak menggunakan katalis
r = k Cm 2 k = 1,20 10 4exp(-18000±400/RT) [m3/(mol/min)]
Kinetika reaksi esteririfikasi asam lemak bebas dari minyak biji Thevetia Peruviana dengan metanol pada orde satu menunjukkan bahwa nilai tetapan laju reaksi dipengaruhi oleh nisbah molar asam lemak bebas dengan metanol, tetapan
laju reaksi nisbah molar metanol 1:1 adalah 0,0017/menit dan nisbah molar metanol 1:3 adalah 0,0076 /menit (Oluwaniyi dan Ibiyemi 2003). Menurut Guner et al. (1996) tetapan laju esterifikasi antara asam oleat dengan gliserol dengan katalis asam sulfat tidak ada perbedaan yang nyata terhadap pengaruh konsentrasi katalis, namun ada perbedaan yang nyata terhadap pengaruh suhu, nilai k pada suhu 180 oC adalah 1,6334 x10-4 % /menit, pada suhu 200 oC adalah 2,7556 x 10-4 %
/menit, suhu 220 oC adalah 6,9700 x 10-4% /menit dan pada suhu 240 oC adalah 2,1292 X 10-3% /menit.
2.6.2.2 Kinetika Reaksi Transesterifikasi. Menurut Freedman et al. (1986); Noureddini dan Zhu (1997) ; Darnoko dan Cheryan (2000), reaksi transesterifikasi pada pembuatan biodiesel adalah sebagai berikut:
Reaksi keseluruhan:
TG + 3 ROH 3RCO2 –R + GL (1)
Reaksi secara bertahap adalah :
TG-DG (k1) TG + 3 ROH DG + 3RCO2 –R (2) DG-TG (k2) DG-MG (k3) DG + 3 ROH MG + 3RCO2 –R (3) MG-DG (k4) MG-Gl (k5) MG + 3 ROH GL + 3RCO2 –R (4) Gl-MG(k6) d[TG] / dt = - k1[TG][A] +k 2[DG] [E]
d[DG] / dt = k1[TG] [A] - k 2[DG] [E] - k 3[DG][A] + k 4[MG] [E]
d[MG] / dt = k3[DG] [A] - k 4[MG] [E] - k 5[MG][A] + k 6[GL] [E]
d[GL] / dt = k5[MG][A] - k 6[GL] [E]
d[E] / dt = k1[TG][A]-k2[DG] [E] + k3[DG][A]-k 4[MG] [E]+k5[MG][A]-k 6[GL] [E] d[A] / dt = - d[E] / dt
[TG] : konsentrasi molar triglirida [MG] : konsentrasi monogliserida [DG] : konsentrasi digliserida [A] : konsentrasi metanol [GL] : konsentrasi gliserol [E] : konsentrasi ester Menurut Darnoko dan Cheryan (2000) reaksi hidrolisis pada orde dua adalah :
Integrasi dari persamaan 5 menghasilkan:
kTG t = 1/[TG] – 1/ [TG0] (6)
diaplikasikan pada persamaan 3 dan 4 menjadi
kDG t = 1/[DG] – 1/ [DG0] (7)
kMG t = 1/[MG] – 1/ [MG0] (8)
Notasi k merupakan tetapan laju reaksi keseluruhan (overall pseudo rate constant), t adalah waktu reaksi, TG0 konsentrasi trigliserida awal paling tinggi,
DG0 konsentrasi digliserida awal paling tinggi dan MG0 konsentrasi monogliserida
awal paling tinggi.
Pola grafik hubungan antara konsentrasi trigliserida, digliserida, monogliserida dan metil ester dengan waktu selama proses transesterifikasi berdasarkan penelitian Freedman et al. (1986); Noureddini dan Zhu (1997); Darnoko dan Cheryan (2000); dan Cheng (2003) adalah serupa yaitu selama proses transesterifikasi konsentrasi trigliserida turun sampai mencapai level konstan, konsentrasi monogliserida dan digliserida naik kemudian turun sampai mencapai level konstan sedangkan konsentrasi metil ester naik sampai mencapai level konstan.
Berdasarkan pola hubungan konsentrasi trigliserida, digliserida, monogliserida dan metil ester dengan waktu, Freedman (1986); Darnoko dan Cheryan (2000) menghitung tetapan laju reaksi transesterifikasi secara bertahap berdasarkan perubahan konsentrasi reaktan yaitu perubahan trigliserida menjadi digliserida, perubahan digliserida menjadi monogliserida dan perubahan monogliserida menjadi gliserol, sedangkan Nourdinni dan Zhu (1997) selain menghitung laju reaksi transesterifikasi secara bertahap juga menghitung tetapan laju reaksi transesterifikasi pembentukan metil ester secara keseluruhan. Karena penurunan tigliserida sebanding dengan peningkatan metil ester selama proses
transesterifikasi maka Cheng (2003) melakukan pengukuran kinetika reaksi transesterifikasi berdasarkan fungsi konversi trigliserida, sedangkan Sofiah (1999) melakukan pengukuran tetapan laju reaksi transesterifikasi berdasarkan gliserol yang dibentuk karena didasarkan bahwa mol konversi trigliserida sebanding dengan mol gliserol yang dibentuk.
Menurut Freedman (1986) nilai tetapan laju reaksi transesterifikasi minyak kedele dipengaruhi oleh katalis. Nilai k orde dua untuk reaksi TG menjadi DG pada 1 % katalis sodium butoxide (NaoBu) adalah 3,822 x 10-3 mmol/ menit dan pada
0,5% katalis NaoBu adalah 26,626 x 10-3 mmol/ menit, untuk reaksi DG menjadi
MG pada 1 % katalis NaoBu adalah 1,215 x 10-3 mmol/ menit dan pada 0,5%
katalis NaoBu adalah 3,584 x 10-3 mmol/ menit, energi aktivasi reaksi perubahan
TG menjadi GL adalah 22,022 Cal/mol. Menurut Noureddini dan Zhu (1997) reaksi transesterifikasi dipengaruhi oleh kecepatan pengadukan dan suhu dan mekanisme reaksi transesterifikasi mengikuti orde reaksi dua. Dijelaskan pula bahwa nilai tetapan laju reaksi orde dua untuk reaksi perubahan TG menjadi DG adalah 0,049 % b/b /menit sedangkan arah sebaliknya 0,102 % b/b /menit, untuk reaksi perubahan DG menjadi MG adalah 0,218 % b/b /menit reaksi sebaliknya % b/b /menit, untuk reaksi perubahan MG menjadi Gliserol 0,239 % b/b /menit, reaksi sebaliknya 0,007 % b/b /menit dan untuk reaksi keseluruhan dari TG menjadi ME adalah 7,84 x 10-5 % b/b /menit dan reaksi sebaliknya 1,58 x 10 -5 % b/b /menit.
Menurut Canacki dan Van Gerven (2003) dan konversi trigliserida (TG) digliserida (DG) dan monogliserida (MG) sampai dengan reaksi 30 menit memiliki orde dua (pseudo second-order model) namun setelah 30 menit memiliki orde satu. Grafik hubungan antara waktu reaksi (t) dengan 1 / [TG] dalam bentuk garis lurus (persamaan 6) sampai dengan waktu reaksi 30 menit digunakan untuk menentukan
kTG (% b/b-menit)-1 yang merupakan slope dari garis lurus tersebut. Cara tersebut
sama untuk menentukan kMG dan kDG. Darnoko dan Cheryan (2000) menentukan
nilai k pada berbagai suhu reaksi transesterifikasi yang dilakukan dengan menggunakan katalis KOH 1 %, nisbah molar metanol : minyak 6:1 pengamatan dilakukan setiap 5 menit sekali selama 30 menit seperti ditunjukkan pada Tabel 16.
Tabel 16 Konstata laju reaksi (k) hidrolisa trigliserida, digliserida monogliserida dan pada berbagai perbedaan suhu
Gliserida Suhu (OC) Tetapan laju reaksi (% b/b-menit)-1 R 2 TG DG 50 0,018 0,9865 55 0,024 0,9966 60 0,036 0,9822 65 0,048 0,9903 DG MG 50 0,036 0,9940 55 0,051 0,9974 60 0,070 0,9860 65 0,094 0,9678 DG MG 50 0,112 0,9733 55 0,156 0,9619 60 0,141 0,9862 65 0,191 0,9843
Sumber: Darnoko dan Cheryan 2000.
Penentuan tetapan laju reaksi transesterifikasi oleh Cheng et al. (2004) berdasarkan reaksi transesterifikasi secara keseluruhan sebagai berikut:
TG + 3ML 3 ME + Gl r = - d [TG]/ dt = k [TG ] [ML]
r = laju reaksi (rate of reaction), k = tetapan laju reaksi, [TG] = konsentrasi minyak dan [ML] = konsentrasi metanol
kt = 1/[ML] – 3 [TG] ln [ML]/[TG]- ln {[ML]0/[TG]0
t = 1 /k f(XTG) XTG ={ [TG0] – [TG] } / [TG]
Tetapan laju reaksi (k) untuk setiap reaksi ditentukan dari slope antara f(XTG)
minyak sawit (palm oil) dengan menggunakan katalis sodium hidroksida dan sodium methoksida menghasilkan tetapan kinetik yang tinggi dalam pembentukan metil ester dengan konversi 99% yaitu 0,163 liter / mol menit yang diperoleh dari nisbah molar metanol minyak 10:1, konsentrasi katalis 0,125 mol/kg minyak pada suhu 60 oC dan nilai k untuk kondisi yang lain dapat dilihat pada Tabel 17.
Tabel 17 Nilai tetapan laju transesterifikasi pada beberapa kondisi proses Nisbah molar minyak dan metanol Kecepatan pengadukan (rpm) Suhu
(0C) Konsentrasi katalis (mol/kg oil) Tetapan laju reaksi k (liter / mol menit) 1:10 350 60 0,1250 0,163 1:10 350 60 0,1875 0,313 1:10 350 60 0,2500 0,526 1:6 350 60 0,1250 0,097 1:8 350 60 0,1250 0,147 1:10 350 70 0,1250 0,309
Sumber: Cheng et al. 2004.
Energi aktivasi pada reaksi transesterifikasi ditentukan menggunakan persamaan arrhenius log10 k = (-Ea/2,303R)T +C, Ea energi aktivasi, R tetapan gas constan dan C adalah tetapan maka untuk trigliserida menjadi digliserida adalah 14,7 k Cal /mol, digliserida menjadi monogliserida 14,2 k Cal /mol dan untuk monogliserida menjadi gliserol 6,4 k Cal /mol (Darnoko dan Cheryan 2000). 2.6.3 Optimasi Proses dengan Response Surface Methodology (RSM)
Metodologi permukaan respon (Response Surface Methodology) terdiri atas sekelompok teknik yang digunakan untuk studi empirik yang berkaitan dengan satu atau lebih respon pengukuran seperti hasil, indek warna, viskositas, disamping itu sejumlah input variabel seperti waktu, suhu, tekanan, konsentrasi dan lain-lain (Box et al. 1978). Metodologi permukaan respon merupakan kumpulan teknik-teknik statistik dan matematika yang berguna untuk menganalisis permasalahan tentang beberapa variabel bebas yang mempengaruhi variabel tak bebas (respon)