LAMPIRAN B
PERHITUNGAN NERACA ENERGI
Dari hasil perhitungan neraca massa selanjutnya dilakukan perhitungan neraca energi. Perhitungan neraca energi didasarkan pada :
Basis : 1 jam operasi
Satuan Panas : Kilo Joule (kJ)
Temperatur Referensi : 25˚C (298,15K)
Neraca energi
{(Energi masuk) - (Energi Keluar) + Generasi Energi) - (Konsumsi Energi)} =
{Akumulasi Energi}
(Himmelblau,ed.6,1996)
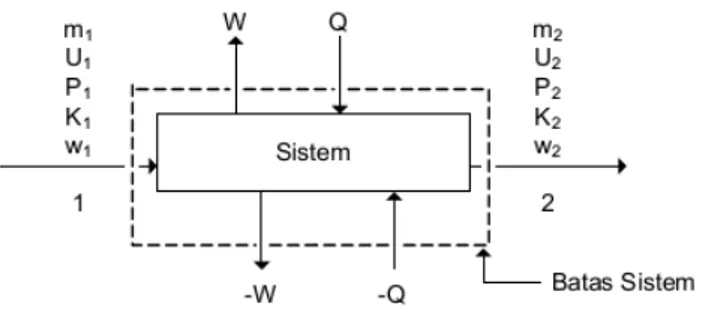
Energi secara umum yang terlibat berupa energi panas (Q) dan kerja (W). Perhatikan gambar dibawah ini :
Pada Gambar B.1 terlihat proses perpindahan energi secara pada suatu sistem. Pada keadaan 1, suatu materi atau bahan memiliki empat buah energi yaitu energi kinetik (K1), energi potensial (P1), energi dalam (U1), dan energi berupa kerja p1v1(w1) serta memiliki laju alir massa m1. Materi atau bahan tersebut kemudian melewati sebuah sistem tertentu, dimana materi atau bahan tersebut membutuhkan energi dari luar berupa panas (-Q) dan kerja (-W) atau sebaliknya, dapat menghasilkan energi berupa panas (Q) dan kerja (W). Setelah melewati sistem, bahan atau materi tersebut berada pada keadaan 2, dimana materi tersebut memiliki energi berupa energi kinetik (K2), energi potensial (P2), energi dalam (U2), dan energi berupa kerja p2v2 (w2) serta memiliki laju alir massa m2.
Sehingga persamaan neraca energi secara umum menjadi :
(U1 +K1 +P1)m1 - (U2 +K2 +P2)m2 + Q +W + w1 = w2 = ΔE
(U1 +K1 +P1)m1 - (U2 +K2 +P2)m2 + Q +W + (p1v1)m1 - (p2v2)m2 = ΔE
Jika tidak ada perubahan laju alir massa sebesar m1 = m2 = m dan tidak akumulasi energi pada sistem, maka persamaan tersebut dapat disederhanakan menjadi :
{( U2 - U1) + ( K2 - K1) + ( P2 - P1) + (p2v2)- (p1v1)}m = Q + W
Sistem berada pada tekanan tetap sehingga terdapat hubungan ΔH = ΔU + Δpv. (Smith,J.M., Ed.6th, 2001, Pers.2.11., hal. 38)
{ΔH + ΔEk + ΔP}m = Q + W
(Himmelblau,ed.6,1996)
Jika pada sistem perubahan energi kinetik dan energi potensial sangat kecil dibandingkan energi yang timbul akibat adanya reaksi maka nilai ∆Ek dan ∆P dapat diabaikan (bernilai nol) dan jika tidak ada kerja yang diberikan atau dihasilkan ke dan dari sistem maka persamaan neraca energi tersebut menjadi,
Q = ΔH
Q = ΔH = Hproduk - Hreaktan
Jika tidak ada panas yang timbul akibat perubahan fasa materi pada suatu sistem maka,
Q = ΔH = ( n Cp dT)Ʃ keluar - ( n Cp dT)Ʃ masuk
Jika sistem yang ditinjau berada dalam keadaan adiabatis maka,
0 = ΔH = ( n Cp dT)Ʃ keluar - ( n Cp dT)Ʃ masuk
( n Cp dT)Ʃ keluar - ( n Cp dT)Ʃ masuk
Keterangan :
ΔH = Perubahan Panas (kJ)
Cp = Kapasitas Panas (Kj/kmol.K)
Dt = Perbedaan Temperatur (K)
(Himmelblau,ed.6,1996)
Entalpi bahan pada temperatur dan tekanan tertentu adalah :
∆H = ∆HT – ∆Hf
(Himmelblau,ed.6,1996)
Keterangan :
∆H = Perubahan entalpi
∆HT = Entalpi bahan pada suhu T
∆Hf = Entalpi bahan pada suhu referensi (25˚C)
Enthalpi bahan untuk campuran dapat di rumuskan sebagai berikut :
∆H = Σ n Cp dT
(Himmelblau,ed.6,1996)
Keterangan :
∆H = Perubahan entalpi
n = mol
dT = Perbedaan termperatur (K)
Perhitungan Kapasitas Panas (Cp)
∫
Tref T CpdT=∫
Tref T(
A + BT + CT2 + DT3 + ET4)
dT∫
Tref T CpdT=∫
Tref T A(
T - Tref)
+ B 2(
T 2 - T2ref)
+ C 3(
T 3 - T3ref)
+ D 4(
T 4 - T4ref)
+ E 5(
T 5 - T5ref)
Keterangan :Cp : Kapasitas panas (J/mol K) A,B,C,D,E : Konstanta
Tref : Temperatur referensi = 298,15 K T : Temperatur operasi (K)
Kapasitas Panas Cairan
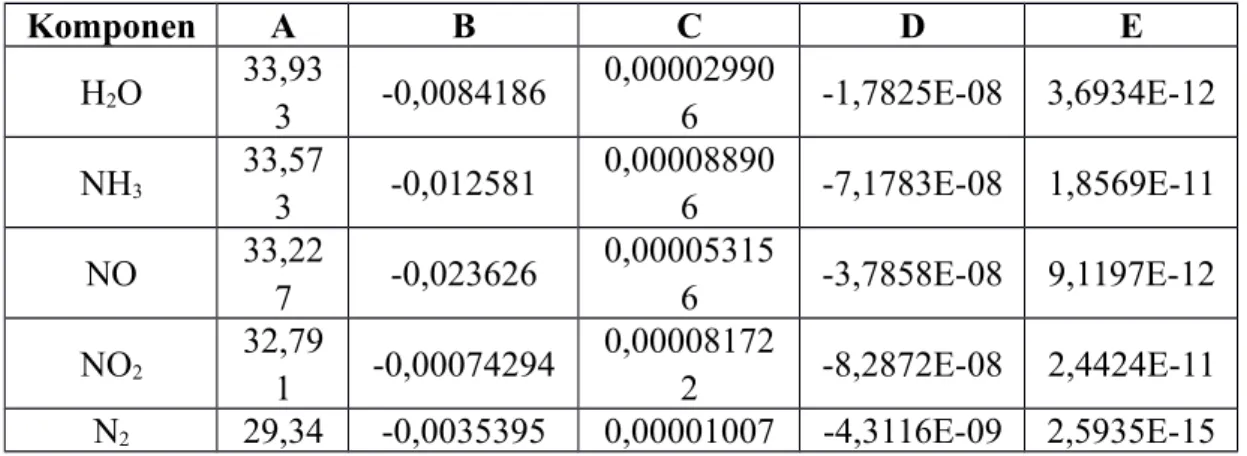
Tabel B.1 Data Konstanta Kapasitas Panas Gas dalam (J/mol.K)
Komponen A B C D E H2O 33,93 3 -0,0084186 0,00002990 6 -1,7825E-08 3,6934E-12 NH3 33,57 3 -0,012581 0,00008890 6 -7,1783E-08 1,8569E-11 NO 33,22 7 -0,023626 0,00005315 6 -3,7858E-08 9,1197E-12 NO2 32,79 1 -0,00074294 0,00008172 2 -8,2872E-08 2,4424E-11 N2 29,34 -0,0035395 0,00001007 -4,3116E-09 2,5935E-15
2 6 O2 29,52
6 -0,008999
0,00003808
3 -3,2629E-08 8,8607E-12 (Reff : Carl L. Yaws, “Thermodynamic and Physical Data”)
Kapasitas Panas Gas
Tabel B.2 Data Konstanta Kapasitas Panas Cairan dalam (J/mol.K) Kompone n A B C D E H2O 92,053 -0,039953 -0,00021163 5,3469E-07 0 NH3 -182,157 3,3618 -0,014398 0,00002037 1 0 HNO3 214,478 0,76762 0,001497 -3,0208E-07 0 (Reff : Carl L. Yaws, “Thermodynamic and Physical Data”)
Berat molekul untuk masing-masing komponen
Komponen Rumus kimia Berat molekul Kg/kmol
Asam nitrat HNO3 63,0180
Amonia NH3 17,0310 Nitric Oxide NO 30,0000 Nitrogen dioxide NO2 46,0000 Oxygen O2 32,0000 Water H2O 18,0000 Nitrogen N2 28,0000
(Reff : Carl L. Yaws, “Thermodynamic and Physical Data”)
Tekanan Uap Murni masing-masing Komponen
Untuk menentukan tekanan uap murni suatu komponen pada suhu tertentu dinyatakan dengan persamaan :
log P0 = A +
T B
+ C log T + D T + E T2
Dimana :P0 = tekanan uap murni suatu komponen pada suhu tertentu (mmHg) T = suhu (K) A,B,C,D,E = konstanta Kompone n A B C D E H2O 29,8605
-3,1522E+03 -7,3037E+00 -2,4247E-09 1,8090E-06 NH3 31,1575
-2,0277E+03 -1,1601E+01 7,4625E-03 -9,5811E-12 N2 23,8572
-4,7668E+02 -8,6689E+00 2,0128E-02 -2,4139E-11 O2 20,6695
-5,2697E+02 -6,7062E+00 1.,2926E-02 -9,8832E-13 (Reff : Carl L. Yaws, “Thermodynamic and Physical Data”)
Panas Penguapan
Untuk P 1 atm, maka persamaan Watson digunakan untuk menghitung panas penguapan, sebagai fungsi dari suhu.Untuk mencari panas penguapan pada suhu tertentu digunakan persamaan :
Hv = A (1 - Tc
T
Dimana :Tc = suhu kritis masing-masing komponen (oK) Hv = panas penguapan pada titik didihnya (kJ/mol)
Komponen A Tc N
H2O 52,053 647,13 0,321
NH3 31,523 405,65 0,364
N2 9,430 126,10 0,533
O2 8,040 158,58 0,201
(Reff : Carl L. Yaws, “Thermodynamic and Physical Data”)
Viskositas Gas
Untuk mengetahui viskositas gas suatu komponen pada suhu tertentu dinyatakan dengan persamaan :
µ gas = A + BT + CT2 ( cp ; T = oK )
Komponen A B C Tmin Tmax
H2O -36,826 4,2900E-01 -16,200E-05 280 1073 NH3 -7,874 3,6700E-01 -4,4700E-06 195 1000 N2 42,606 4,7500E-01 -9,8800E-05 150 1500 O2 44,224 5,6200E-01 -1,1300E-04 150 1500
(Reff : Carl L. Yaws, “Thermodynamic and Physical Data”)
Viskositas Cairan
Untuk mengetahui viskositas cairan suatu komponen pada suhu tertentu dinyatakan dengan persamaan :
Log µ cair = A + B/T + CT + DT2 ( cp ; T = oK ) Komponen A B.102 C.10-2 D.10-6 T min Tmax Water -7,1711 7,4736 2,1697 -27,176 143 470 Ammonia -7,4005 11,815 1,4888 -13,713 285 562 Nitric oxide -5,8058 10,140 1,0909 -9,7803 230 658 NO2 -4,5611 3,0811 1,8030 -38,145 105 202 Nitrogen -4,2694 2,8954 1,7111 -36,092 98 305 Oxygen -5,2585 8,3065 1,0784 -10,618 210 617 Nitric acid -7,3801 3,1925 4,793 -141,2 91 191 (Reff : Smith, J.M, Van Ness, H.C, Abbott, M.M, “Introduction to Chemical
Engineering Thermodynamics”, 5th ed.)
Konduktivitas Panas Gas
Untuk mengetahui konduktivitas panas gas suatu komponen pada suhu tertentu dinyatakan dengan persamaan :
k gas = A + BT + CT2 ( W/ m K ; T = oK )
Komponen A B.10-5 C.10-8 T max T min
Water -0,00137 1,8081 12,136 225 480 Ammonia -0,00565 3,4493 6,9298 325 700 Nitric oxide -0,01063 5,9356 2,5488 457 1000 NO2 -0,01936 12,547 3,8298 225 825 Nitrogen -0,00123 3,6219 12,459 150 750 Oxygen -0,00797 4,0572 6,7289 400 825 Nitric acid -0,00935 14,028 3,3180 97 1400 (Reff : Carl L. Yaws, “Thermodynamic and Physical Data”)
Konduktivitas Panas Cairan
Untuk mengetahui konduktivitas panas cairan suatu komponen pada suhu tertentu dinyatakan dengan persamaan :
Log k cair = A + B(1-T/c)2/7 ( W/ m K ; T = oK )
Komponen A B C T max T min
Water -1,2287 0,5322 469,65 143 446
Ammonia -1,6846 1,0520 562,16 279 534
Nitric oxide -1,7474 0,9969 657,96 230 625
Nitrogen -1,3314 0,8527 282,36 104 268
Oxygen -1,7498 1,0437 617,17 178 586
Nitric acid -1,0976 0,5387 190,58 91 181 (Reff : Carl L. Yaws, “Thermodynamic and Physical Data”)
k cair = A + BT + CT2
Komponen A B.10-3 C.10-6 T max T min
Water -0,2758 4,6120 -5,5391 273 633
Nitric acid
(Reff : Carl L. Yaws, “Thermodynamic and Physical Data”)
Berikut ini adalah perhitungan neraca panas pada masing-masing alat :
1. Neraca Panas di Sekitar Heater NH3
Fungsi :Memanaskan cairan umpan vaporizer sebanyak 882 kg/jam dari -33,5C menjadi 17,4 C.
Dimana : ∆Hin = Laju alir panas NH3 masuk Heater (kJ/jam) ∆Hout = Laju alir panas NH3 keluar Heater (kJ/jam) ∆Hsteam in = Laju alir panas steam masuk (kJ/jam) ∆Hsteam out = Laju alir panas steam keluar (kJ/jam)
a. Panas masuk heater (Aliran 1)
T bahan : 273.15 + (-33,5)˚C = 239,5 K T referensi : 273.15 + 25˚C = 298.15 K Kompone n n(Kmol) ʃCpdT(kJ/kmol) Qin NH3(l) 51,834 -4528,23 -234719,66
H2O(l) 0,049 -4473,59 -219,22
Total 51,883 -234938,88
b. Panas Keluar heater (Aliran 2)
T bahan : 273,15 + 17,4˚C = 290,4 K T referensi : 273,15 + 25˚C = 298.15 K
Kompone n
n(Kmol) ʃCpdT(kJ/kmol) Qout
NH3(l) 51,834 -674,52 -34963,55
H2O(l) 0,049 -642,68 -31,49
Total 51,883 -34995,05
c. menghitung laju alir massa dan laju alir panas steam ∆Hsteam = ∆H2 - ∆H1
= (-34995,05) - (-234938,88) = 199943,83
Oleh karena itu membutuhkan fluida panas yang berfungsi sebagai pemanas yaitu saturated steam pada steam tabel dengan kondisi :
- Temperatur (T) = 100˚C - Tekanan (P) = 101,35 kPa - H1 = 419,04 kJ/kg
- Hv = 2676,1 kJ/kg
- λs = Hv – Hl = 2676,1 - 419,04 = 2257,06 kJ/kg - maka massa steam :
Ws=∆H λs
=199943,83 kJ/jam
2257,06 kJ/kg =88,59 - Panas steam masuk (∆Hsteam in)
∆Hsteam in = Ws × Hv = (88,59 kg/jam) × (2676,1 kJ/kg) = 237064,9 kJ/jam
- Panas steam keluar (∆Hsteam out)
∆Hsteam out = Ws × Hl = (88,59 kg/jam) × (419,04 kJ/kg) = 37121,06 kJ/jam
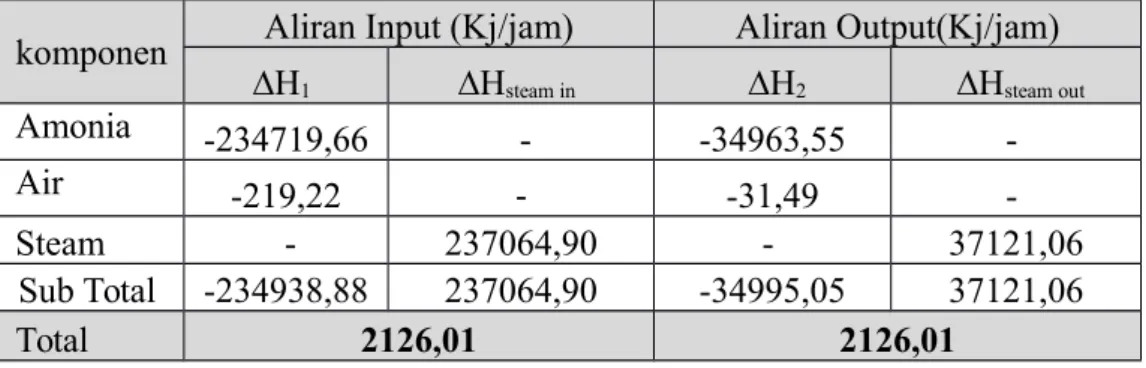
Setelah dilakukan perhitungan neraca panas pada masing-masing komponen maka dapat disusun tabel neraca panas komponen sebagai berikut :
komponen Aliran Input (Kj/jam) Aliran Output(Kj/jam) ∆H1 ∆Hsteam in ∆H2 ∆Hsteam out
Amonia -234719,66 - -34963,55 -
Air -219,22 - -31,49 -
Steam - 237064,90 - 37121,06
Sub Total -234938,88 237064,90 -34995,05 37121,06
Total 2126,01 2126,01
2. Neraca Panas di Sekitar Vaporizer (V-01)
Kode : V-01
Fungsi : Menguapkan Amonia dari preheater sebanyak 5979,3614 kg/jam sebagai umpan segar ke Reaktor (R-01).
Tujuan : a. Menghitung beban panas di vaporizer b. Menghitung kebutuhan steam
Gambar B.1 Aliran panas di sekitar Vaporizer
Dimana : ∆H1 = Laju alir panas NH3 masuk vaporizer (kJ/jam) ∆H2 = Laju alir panas NH3 keluar vaporizer (kJ/jam) ∆Hsteam in = Laju alir panas steam masuk (kJ/jam) ∆Hsteam out = Laju alir panas steam keluar (kJ/jam)
a. Menghitung beban panas di vaporizer
Menghitung dew point dan bubble point
Penentuan tekanan uap dengan menggunakan persamaan Antoine :
T C B A P Ln komposis i A B C NH3 16.9481 2132.500 -32.9800 H2O 18.3036 3816.44 0 -46.1300 ( Coulson, 1980 ; Apendiks D )
Dicari nilai Temperature Dew Point (TDP) dan Temperature Bubble Point (TBP) dengan cara trial, menggunakan nilai tekanan uap yang didapat dari persamaan Antoine, sehingga diperoleh xi =1 (untuk TDP) dan yi =1 (untuk TBP). P operasi = 6 atm. Komposis i Kmol Yi K Xi K Yi Amonia 51.8347 0.999 1.3795 0.7242 1.0009 0.999999 Air 0.0490 0.001 0.0038 0.2506 0.0020 0.000002 1 xi = 1 yi = 1 Didapat : Tdew = 20˚C = 293K Tbubble = 10,2124 = 283,2K
Menghitung beban panas Vaporizer
Vaporizer menguapkan input dari Pre-Heater pada 283,2K Tinput = 283,2K
Pada vaporizer, panas yang dibutuhkan adalah panas sensibel , sehingga : H out = Hv m dT Cp m 283,2 298,15
Dimana : Hv = panas penguapan pada suhu tertentu (kJ/kmol) Neraca Panas Total
H 1 + Hs = Hc + Q 1 H 1 + ms Hs = mc Hc + Q 1 Karena ms = mc dan m1 = m2, maka
λ total Q ms vap) H ( m ) ms(λ .dT Cp m .dT Cp m ) H -(H m Hc) -(Hs ms 1 443,45 298 L 2 303 298 L 1 1 2 1
a. Panas masuk Vaporizer keluaran dari Heater NH3 T bahan : 273.15 + 17.4˚C = 290.4 K T referensi : 273.15 + 25˚C = 298.15 K Kompone n n(Kmol) ʃCpdT(kJ/kmol) Qin NH3(l) 51,834 -603,67 -31291,44 H2O(l) 0,049 -574,54 -0,028 Total 51,88 -31291,47
b. Panas masuk Vaporizer dari aliran recycle T bahan : 273.15 + 17.4˚C = 290.4 K T referensi : 273.15 + 25˚C = 298.15 K Kompone n n(Kmol) ʃCpdT(kJ/kmol) Qin NH3(l) 10,36 -603,67 -6,25 H2O(l) 0,0098 -574,54 -0,0056 Total 10,37 -6,26
c. Panas Keluar vaporizer
T bahan : 273,15 + 17,4˚C = 290,4 K T referensi : 273,15 + 25˚C = 298.15 K
Kompone n
n(Kmol) ʃCpdT(kJ/kmol) Qout
NH3(g) 51,834 -272,67 -14133,98
H2O(g) 0,049 -255,50 -12,52
NH3(rec) 10,36 -603,67 -6258,26
H2O(rec) 0,0098 -57,54 -5,63
Total 62,26 -20410,40
d. menghitung laju alir massa dan laju alir panas steam ∆Hsteam = ∆H2 - ∆H1
= (-20410,40) - (-31297,73) = 10887,33
Oleh karena itu membutuhkan fluida panas yang berfungsi sebagai pemanas yaitu saturated steam pada steam tabel dengan kondisi :
- Temperatur (T) = 100˚C - Tekanan (P) = 101,35 kPa - H1 = 419,04 kJ/kg
- Hv = 2676,1 kJ/kg
- λs = Hv – Hl = 2676,1 - 419,04 = 2257,06 kJ/kg - maka massa steam :
Ws=∆H λs =
10887,33 kJ/jam 2257,06 kJ/kg =4,82 - Panas steam masuk (∆Hsteam in)
∆Hsteam in = Ws × Hv = (4,82 kg/jam) × (2676,1 kJ/kg) = 12908,6 kJ/jam
- Panas steam keluar (∆Hsteam out)
∆Hsteam out = Ws × Hl = (4,82 kg/jam) × (419,04 kJ/kg) = 2021,31 kJ/jam
Setelah dilakukan perhitungan neraca panas pada masing-masing komponen maka dapat disusun tabel neraca panas komponen sebagai berikut :
komponen Aliran Input (Kj/jam) Aliran Output(Kj/jam) ∆H1 ∆Hsteam in ∆H2 ∆Hsteam out
NH3(l) -31297,70 - -6258,26 - H2O(l) -0,034 - -5,63 - NH3(g) - - -14133,98 -H2O(g) - - -12,52 -Steam - 12908,6 2021,31 Sub Total -31297,74 12908,6 -20410,0 2021,31 Total -18389,09 -18389,09
3. Neraca Panas di Heater NH3
Fungsi :Memanaskan cairan umpan vaporizer sebanyak 882 kg/jam dari 17,4 ˚C menjadi 210 ˚C.
Dimana : ∆Hin = Laju alir panas NH3 masuk Heater (kJ/jam) ∆Hout = Laju alir panas NH3 keluar Heater (kJ/jam) ∆Hsteam in = Laju alir panas steam masuk (kJ/jam) ∆Hsteam out = Laju alir panas steam keluar (kJ/jam)
a. Panas masuk heater
T bahan : 273.15 + 17,4˚C = 290,4 K T referensi : 273.15 + 25˚C = 298.15 K
Kompone n
NH3(l) 51,834 -272,67 -14133,99
H2O(l) 0,049 -285,73 -14,00
Total 51,883 -14147,99
b. Panas Keluar heater
T bahan : 273,15 + 210˚C = 483 K T referensi : 273,15 + 25˚C = 298.15 K
Kompone n
n(Kmol) ʃCpdT(kJ/kmol) Qout
NH3(l) 51,834 7110,87 368589,98
H2O(l) 0,049 6339,17 310,64
Total 51,883 368900,62
c. menghitung laju alir massa dan laju alir panas steam ∆Hsteam = ∆H2 - ∆H1
= (368900,62) - (-14147,99) = 383048,61
Oleh karena itu membutuhkan fluida panas yang berfungsi sebagai pemanas yaitu saturated steam pada steam tabel dengan kondisi :
- Temperatur (T) = 100˚C - Tekanan (P) = 101,35 kPa - H1 = 419,04 kJ/kg
- Hv = 2676,1 kJ/kg
- λs = Hv – Hl = 2676,1 - 419,04 = 2257,06 kJ/kg - maka massa steam :
Ws=∆Hλ s
=383048,61 kJ/jam
2257,06 kJ/kg =169,71 - Panas steam masuk (∆Hsteam in)
∆Hsteam in = Ws × Hv = (169,71 kg/jam) × (2676,1 kJ/kg) = 454164,44 kJ/jam
- Panas steam keluar (∆Hsteam out)
∆Hsteam out = Ws × Hl = (169,71 kg/jam) × (419,04 kJ/kg) = 71115,8 kJ/jam
Setelah dilakukan perhitungan neraca panas pada masing-masing komponen maka dapat disusun tabel neraca panas komponen sebagai berikut :
Komponen Aliran Input (Kj/jam) Aliran Output(Kj/jam) ∆H1 ∆Hsteam in ∆H2 ∆Hsteam out
Amonia -14133,99 - 368589,98 -
Air -14,00 - 310,64 -
Steam - 454164,44 - 71115,8
Sub Total -14147,99 454164,44 368900,62 71115,8
Total 440016,45 440016,45
4. Neraca Panas di Sekitar Cooler (Primary Air)
Fungsi : Untuk mendinginkan bahan baku udara dari temperatur 275˚C menjadi 210˚C.
a. Panas masuk Cooler
T bahan : 273.15 + 275˚C = 548 K T referensi : 273.15 + 25˚C = 298.15 K Kompone n n(Kmol) ʃCpdT(kJ/kmol) Qin O2(g) 97,97 7605,56 745098,44 N2(g) 368,54 7338,77 2704665,49 H2O(g) 14,49 8637,72 129126,37 Total 481,46 3578890,30
b. Panas Keluar Cooler
T bahan : 273,15 + 210˚C = 483 K T referensi : 273,15 + 25˚C = 298.15 K
Kompone n
n(Kmol) ʃCpdT(kJ/kmol) Qout
O2(g) 97,97 5576,60 546325,93
N2(g) 368,54 5413,21 1995010,65
H2O(g) 14,49 6339,17 94765,04
Total 481,46 2636101,63
c. Menghitung kebutuhan cooling water (Mcw)
H in = H liquid keluar + H cooling water
H cooling water = H in - H liquid keluar
H cooling water (Hcw) = 3578890,30 - 2636101,63 = 942788,67 Kj/jam
Untuk menyerap panas tersebut maka di butuhkan cooling water dengan kondisi :
T in = 160 (380 K)
T out = 220 (493 K)
Maka, Cp N2 = 77616833,2 Kj/mol
Cp O2 =
5. Neraca Panas di Sekitar Cooler (Secondary Air)
Fungsi : Untuk mendinginkan bahan baku udara dari temperatur 210˚C menjadi 50˚C.
a. Panas masuk Cooler
T bahan : 273.15 + 210˚C = 483 K T referensi : 273.15 + 25˚C = 298.15 K
n
O2(g) 17,29 5576,60 96410,45
N2(g) 65,03 5413,21 352060,70
H2O(g) 2,63 6339,17 16723,24
Total 84,96 465194,40
b. Panas Keluar Cooler
T bahan : 273,15 + 50˚C = 323 K T referensi : 273,15 + 25˚C = 298.15 K
Kompone n
n(Kmol) ʃCpdT(kJ/kmol) Qout
O2(g) 17,28 738,51 12767,66
N2(g) 65,03 727,20 47295,23
H2O(g) 2,63 842,59 2222,83
Total 84,96 62285,74
6. Neraca Panas di Sekitar Reaktor
Fungsi : Untuk mereaksikan Amonia (NH3)dan Oksigen (O2) menghasilkan Nitrogen oksida (NO) dan air (H2O).
a. Panas masuk Reaktor dari keluaran Separator (Aliran 5) T bahan : 273.15 + 210 ˚C = 483 K T referensi : 273.15 + 25˚C = 298.15 K Kompone n n(Kmol) ʃCpdT(kJ/kmol) Qin NH3(g) 51,834 7110,87 368589,98 H2O(g) 0,049 6339,17 310,64 Total 51,883 368900,62
b. Panas masuk Reaktor dari keluaran Kompressor (Aliran 8) T bahan : 273,15 + 210˚C = 483 K T referensi : 273,15 + 25˚C = 298.15 K Kompone n n(Kmol) ʃCpdT(kJ/kmol) Qin O2(g) 97,96 5576,60 546325,92 N2(g) 368,54 5413,21 1995010,65 H2O(g) 14,94 6339,17 94765,04 Total 481,44 2636101,63
T bahan : 273,15 + 850˚C = 1123 K T referensi : 273,15 + 25˚C = 298.15 K Kompone
n
n(Kmol) ʃCpdT(kJ/kmol) Qout
O2(g) 34,47 27036,21 931939,93
N2(g) 369,84 25186,92 9315145,66
NO(g) 49,24 26463,98 1303164,55
H2O(g) 92,75 31179,66 2891918,93
Total 546,3 14442169,1
d. Menghitung panas reaksi :
Reaksi yang terjadi di Reaktor :
NH3(g) + 5 4 O2(g) NO(g) + 3 2 H2O(g) NH3(g) + 3 4 O2(g) 1 2 N2(g) + 3 2 H2O(g)
Panas pembentukan standar {H˚Rx298,15 K}
Data H˚Rx masing-masing komponen pada keadaan standar (298,15 K): Hf˚ NH3 = -45.900 J/gmol Hf˚ N2 = 0 J/gmol Hf˚ O2 = 0 J/gmol Hf˚ H2O = -241.800 J/gmol Hf˚ NO = 90300 J/gmol ( Yaws, 1985 )
H298 reaksi 1 = {(Hf˚298 NO + Hf˚298 3 2 H2O) – (Hf˚298 NH3 + Hf˚298 5 4 O2)} = {(90.300 + 32 x (-241.800)) – ((-45.900) + 0)} = -226.500 H298 reaksi 2 = {(Hf˚298 1 2 N2 + Hf˚298 3 2 H2O) – (Hf˚298 NH3 + Hf˚298 3 4 O2)} = {( 12 x 0 + 32 x (-241.800)) – ((-45.900) + 34 x 0)} = -316.800
H298 reaksi total = {H298 reaksi 1 - H298 reaksi 2}
= {(-226.500) – (-316.800)}
= 90.300
e. Menghitung entalpi pada kondisi operasi (HR)
Perubahan entalpi reaktan dari suhu 511,52 K menjadi 1176,36 K dapat ditentukan dengan persamaan sebagai berikut :
HR = H˚R +
(
∫
T 1 T 2 Cpi dT)
HR (1176,36 K) = H˚R (511,52 K) +(
∫
511,52 1176,36 Cpi dT)
∫
511,52 1176,36 CpdT=∫
T1 T 2(
A + BT + CT2 + DT3 + ET4)
dT Sehingga,∫
Tref T CpdT=∫
Tref T A(
T - Tref)
+ B 2(
T 2 - T2ref)
+ C 3(
T 3 - T3ref)
+ D 4(
T 4 - T4ref)
+ E 5(
T 5 - T5ref)
= -3479004,8 kJ/kmolMenghitung panas reaksi
Jumlah NH3 mula-mula (FA0) = 51,83 kmol/jam
Konversi = 95% = 0,95 (Reaksi 1)
Maka, panas reaksi 1 (Q1) = HR (1176,36) . FA0 . X
= -226.500 x 0,95 x 51,83
= -11.153.527,71 kJ/jam
Konversi = 5% = 0,05 (Reaksi 2)
= -316.800 x 0,05 x 51,83
= -821.061,36 kJ/jam
Sehingga Q total = Q1 + Q2
= {-11.153.527,71 + (-821.061,36)}
= -11.974.589,08 kJ/jam
Menghitung panas dan massa air pendingin
Neraca Energi :
Qin – Qout + Qgen - Qkon = Qacc
Q cw = Qin – Qout + Qgen
= {3.005.002,25 – (14.442.169,1) + (-11.974.589,08)}
= 537.422,2 kJ/jam
Menghitung kebutuhan air pendingin
Cooling water (cw) yang digunakan pada pabrik Asam Nitrat masuk ke cooler pada temperatur 30c dan keluar pada temperatur 50c. Dari data kapasitas panas (Cp) air diperoleh sebagai berikut :
Cp air pada 30c = 4,181 kJ/kg.K
H = Cp x T
Sehingga :
H = H (50C) - H (30C)
= {(4,183 x (323,15 – 298,15) – (4,181 x (303,15 – 298,15)}
= 83,67 kJ/kg
Maka kebutuhan air pendingin :
F cw = Q cw/H = 537.422,2 : 83,67 = 6.423,117 kg/jam Q cw masuk = F cw x H (30c) = 6.423,117 x 4,181 = 26.855,05 kJ/jam Q cw keluar = F cw x H (50c) = 6.423,117 x 4,183 = 26.867,9 kJ/jam
7. Neraca Panas di WHB
Fungsi : digunakan untuk proses quenching (pendinginan) gas yang keluar
dari reaktor.
a. Panas masuk WHB (Aliran 11)
T bahan : 273,15 + 850˚C = 1123 K T referensi : 273,15 + 25˚C = 298.15 K Kompone
n
n(Kmol) ʃCpdT(kJ/kmol) Qin
O2(g) 34,47 27036,21 931939,93
N2(g) 369,84 25186,92 9315145,66
NO(g) 49,24 26463,98 1303164,55
H2O(g) 92,75 31179,66 2891918,93
Total 546,3 14442169,1
b. Panas keluar WHB (Aliran 12) T bahan : 273,15 + 500˚C = 773 K T referensi : 273,15 + 25˚C = 298.15 K Kompone
n
n(Kmol) ʃCpdT(kJ/kmol) Qout
O2(g) 29,54 14925,28 440979,06 N2(g) 369,84 14137,42 5228591,99 H2O(g) 92,75 16963,63 1573379,41 NO2(g) 9,84 21350,95 210276,77 NO(g) 39,39 14682,96 578425,90 Total 541,36 8031653,14
8. Neraca Panas di Heater (HE-01)
Fungsi : Untuk mendinginkan gas yang keluar dari Waste Heat Boiler (WHB).
a. Panas masuk Heater (Aliran 12) T bahan : 273,15 + 500˚C = 773 K T referensi : 273,15 + 25˚C = 298.15 K
Kompone n
n(Kmol) ʃCpdT(kJ/kmol) Qin
O2(g) 29,54 14925,28 440979,06 N2(g) 369,84 14137,42 5228591,99 H2O(g) 92,75 16963,63 1573379,41 NO2(g) 9,84 21350,95 210276,77 NO(g) 39,39 14682,96 578425,90 Total 541,36 8031653,14
b. Panas keluar Heater (Aliran 13) T bahan : 273,15 + 170˚C = 443 K T referensi : 273,15 + 25˚C = 298.15 K Kompone
n
n(Kmol) ʃCpdT(kJ/kmol) Qout
O2(g) 23,63 4347,06 102749,92 N2(g) 369,84 4235,30 1566386,50 H2O(g) 92,75 4945,25 458672,88 NO2(g) 21,66 5799,47 125656,64 NO(g) 27,57 4357,15 120153,18 Total 535,47 2373619,14
9. Neraca Panas di Heater (HE-02)
a. Panas masuk Heater (Aliran 13)
T bahan : 273,15 + 170˚C = 443 K T referensi : 273,15 + 25˚C = 298.15 K
Kompone n
n(Kmol) ʃCpdT(kJ/kmol) Qin
O2(g) 23,63 4347,06 102749,92 N2(g) 369,84 4235,30 1566386,50 H2O(g) 92,75 4945,25 458672,88 NO2(g) 21,66 5799,47 125656,64 NO(g) 27,57 4357,15 120153,18 Total 535,47 2373619,14
Fungsi : Mendinginkan dan mengembunkan air yang terkandung pada
campuran gas keluar Heat Exchanger. a. Panas masuk Cooler Condenser T bahan : 273.15 + 170˚C = 443 K T referensi : 273.15 + 25˚C = 298.15 K
Kompone n
n(Kmol) ʃCpdT(kJ/kmol) Qin
O2(g) 23,63 4347,06 102749,92 N2(g) 369,84 4235,30 1566386,50 H2O(g) 92,75 4945,25 458672,88 NO2(g) 21,66 5799,47 125656,64 NO(g) 27,57 4357,15 120153,18 Total 535,47 2373619,14
b. Panas Keluar Cooler
T bahan : 273,15 + 50˚C = 323 K T referensi : 273,15 + 25˚C = 298.15 K
Kompone n
n(Kmol) ʃCpdT(kJ/kmol) Qout
O2(g) 11,22 738,51 8291,55 N2(g) 369,84 727,20 268948,71 H2O(g) 9,27 842,59 7815,08 NO2(g) 4,64 954,67 4437,76 NO(g) 16,70 749,21 12514,29 HNO3(l) 27,89 14704,26 410119,67 H2O(l) 69,52 1881,63 130829,13 Total 509,11 842956,20
11. Neraca Panas di Absorber
Fungsi : Mengoksidasi NO menjadi NO2 dan menyerap NO2 dengan bantuan
H2O menjadi larutan HNO3. A. Panas masuk Absorber
1. Panas masuk Absorber keluaran dari Separator (Aliran 15) T bahan : 273.15 + 50˚C = 323 K
T referensi : 273.15 + 25˚C = 298.15 K Kompone
n
O2(g) 11,22 738,51 8291,55 N2(g) 369,84 727,20 268948,71 H2O(g) 9,27 842,59 7815,08 NO(g) 4,65 954,66 4437,76 NO2(g) 16,70 749,21 12514,29 Total 411,69 302007,40
2. Panas masuk Absorber keluaran dari Separator (Aliran 16) T bahan : 273.15 + 50˚C = 323 K
T referensi : 273.15 + 25˚C = 298.15 K Kompone
n
n(Kmol) ʃCpdT(kJ/kmol) Qin HNO3(l) 27,89 14704,26 410119,67 H2O(l) 69,52 1881,63 130829,13
Total 97,42 540948,80
3. Panas masuk Absorber keluaran dari Kompressore (Aliran 19) T bahan : 273.15 + 50˚C = 323 K
T referensi : 273.15 + 25˚C = 298.15 K Kompone
n
n(Kmol) ʃCpdT(kJ/kmol) Qout
O2(g) 17,28 738,51 12767,66
N2(g) 65,03 727,20 47295,23
H2O(g) 2,63 842,59 2222,83
Total 84,96 62285,74
4. Panas masuk Absorber dari Make up water T bahan : 273.15 + 30˚C = 303 K
T referensi : 273.15 + 25˚C = 298.15 K Kompone
n
n(Kmol) ʃCpdT(kJ/kmol) Qout
H2O(l) 6,94 1130,19 7844,80
Total 6,94 7844,80
B. Panas keluar Absorber
1. Panas Keluar Absorber bagian atas (Aliran 20) T bahan : 273,15 + 40˚C = 313 K
Kompone n
n(Kmol) ʃCpdT(kJ/kmol) Qout
O2(g) 20,58 738,51 15199,85 N2(g) 434,87 727,20 316243,95 H2O(g) 11,91 842,59 10037,91 NO2(g) 1,02 954,66 979,31 NO(g) 7,33 749,21 5493,30 Total 475,73 347954,34
2. Panas Keluar Absorber bagian bawah (Aliran 21) T bahan : 273,15 + 40˚C = 313 K
T referensi : 273,15 + 25˚C = 298.15 K
Kompone n
n(Kmol) ʃCpdT(kJ/kmol) Qout HNO3(l) 40,88 14704,26 601184,46 H2O(l) 69,97 1881,63 131664,92