III. BAHAN DAN METODE
3.1.Waktu dan Tempat
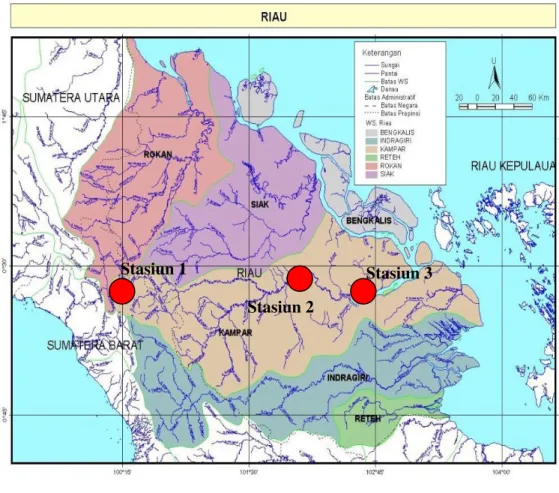
Penelitian ini dilaksanakan di Sungai Kampar Provinsi Riau (Gambar 6), laboratorium parasit dan penyakit dan laboratorium lingkungan Fakultas Perikanan dan Ilmu Kelautan Institut Pertanian Bogor. Adapun waktu penelitian dilaksanakan pada bulan Juli - September 2006.
Keterangan :
1. Stasiun 1 : Hulu sungai 2. Stasiun 2 : Sekitar pabrik 3. Stasiun 3 : Muara sungai
Gambar 6. Lokasi penelitian di Provinsi Riau
3.2. Bahan dan Alat
Untuk pengukuran kualitas air, bahan dan alat yang digunakan dapat dilihat pada Tabel 5, sedangkan untuk kegiatan lainnya yang dilakukan dalam penelitian ini dapat dilihat pada Tabel 6.
Stasiun 1 Stasiun 3
Tabel.5. Metode pengukuran parameter kualitas air No. Parameter Kualitas air Alat Keterangan
1 2 Fisika Suhu air (ºC) TSS Termometer Gravimetrik Insitu Laboratorium 3 4 5 Kimia Salinitas (ppt) pH Logam (Pb,Cd) Refraktometer pH meter Spektofotometrik Insitu Insitu Laboratorium
Tabel 6. Bahan dan alat yang dipergunakan
No Alat Bahan
1 Penangkapan Ikan Jaring insang Dasar
2 Sedimen Petersen Grabe Pengawet
3 Histologi Botol film, gelas objek glass, microtome, incubator, water bath, mikroskop dan kamera, scaple.
insang dan ginjal ikan BNF (buffered neutral
formalin), ethanol 70 %,
80%, 90 % dan absolut, xylol, parafin
4 Logam Spektrofotometer (AAS) air, sedimen dan organ ikan (insang dan ginjal)
3.3. Metode
3.3.1. Stasiun Pengambilan Sampel
Pengambilan sampel dilakukan di tiga stasiun yang dipilih atas dasar jenis aktivitas-aktivitas di sekitarnya yang dapat menimbulkan pencemaran. Pada setiap stasiun dilakukan 3 kali pengulangan. Penentuan stasiun tersebut adalah sebagai berikut:
Stasiun I: Bagian hulu dari muara sungai Stasiun II: Sekitar aktivitas pabrik
Stasiun III: Muara sungai
Pada masing-masing stasiun pengamatan diambil sampel ikan baung (Hemibagrus nemurus). Jumlah ikan yang diambil pada masing-masing stasiun sebanyak 3 ekor untuk dilihat perubahan karakteristik dari organ tubuh ikan yang terkena dampak dari limbah tersebut dan untuk pengamatan histologi.
3.3.2.Metode Parameter Kualitas Air
Metode pengambilan dan penanganan contoh air serta metode kualitas air mengacu pada APHA (1989).
3.3.3.Pembuatan Preparat Histologi
Pengamatan biota ikan yang terkena dampak limbah, dilakukan pengamatan dengan menggunakan metode mikroteknik, yaitu dengan cara membuat preparat histologis. Preparat histologis yang dibuat adalah insang dan ginjal ikan. Adapun prosedur dalam pembuatan preparat histologis adalah:
1. Ikan dibedah dan diambil bagian insang dan ginjalnya. 2. Diawetkan dengan formalin 4 % selama 24 jam. 3. Difiksasi dengan alkohol 70 % selama 24 jam.
4. Alkohol 80%, 90%, 95 %, absolut i dan ii masing-masing 1 jam. 5. Alkohol : xylol (1:1) selama 1 jam.
6. Xylol I dan II masing-masing 1 jam
7. Infiltrasi parafin dalam oven 600 C, xylol:parafin (1:1), Parafin I dan II masing-masing 1 jam
8. Sampel ditanam dalam cetakan dan dibiarkan mengeras. 9. Blok ditempel pada holder atau blok kayu.
10. Sampel dipotong dengan microtome dengan ketebalan 6-10 mikron. 11. Potongan ditempel pada objek glass yang sebelumnya telah diolesi dengan
glycerin albumin.
12. Sample dikeringkan pada incubator 400 C selama 24 jam lalu diwarnai dengan HE. Proses pewarnaan dengan menggunakan hemotoxylin dan eosin dengan langkah sebagai berikut :
Deparaffinasi dengan xylol I dan II masing-masing 2 menit.
Dimasukkan ke dalam alkohol absolut, 96 % dan 90 % masing-masing selama 2 menit.
Kemudian dimasukkan ke dalam alkohol 80 % dan 70% masing-masing selama 20 detik.
Dicuci dengan air mengalir lebih kurang 2 menit Dimasukkan ke dalam haemotoxylin selama 4 menit
Dicuci dengan air mengalir sampai jernih. Dimasukkan ke dalam eosin selama 1,5 menit. Dicuci dengan air mengalir sampai jernih
Direndam dengan alkohol 70 %, 89%, 90%, absolute, xylol i dan ii masing-masing 2 menit.
13. Ditutup dengan cover glass yang sudah di tetesi dengan entelan neu. 14. Dikeringkan dalam oven pada suhu 400 C selama 24 jam, kemudian di
amati di bawah mikroskop.
3.3.4. Pengukuran Kandungan Logam Berat
Analisa logam berat dilakukan dengan menggunakan spektrofotometrik serapan atom (AAS) yaitu dengan menggunakan prinsip berdasarkan Hukum Lambert-Beert yaitu banyaknya sinar yang diserap berbanding lurus dengan kadar zat. Persamaan garis antara konsentrasi logam berat dengan absorbansi adalah persamaan linier dengan koefisien arah positif: Y = a + bX. Dengan memasukkan nilai absorbansi larutan contoh ke persamaan garis larutan standar maka kadar logam berat contoh dapat diketahui (Hutagalung et al., 1997).
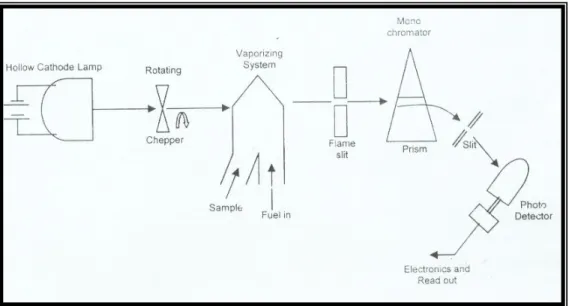
Larutan contoh yang mengandung ion logam dilewatkan melalui nyala udara-asetilen bersuhu 20000 C sehingga terjadi penguapan dan sebagian tereduksi menjadi atom. Lampu katoda yang sangat kuat mengeluarkan energi pada panjang gelombang tertentu dan akan diserap oleh atom-atom logam berat yang sedang di analisis. Jumlah energi cahaya yang diserap atom logam berat pada panjang gelombang tertentu ini sebanding dengan jumlah zat yang diuapkan pada saat dilewatkan melalui nyala api udara-asetilen. Setiap unsur logam berat membutuhkan lampu katoda yang berbeda. Keseluruhan prosedur ini sangat sensitif dan selektif karena setiap unsur membutuhkan panjang gelombang yang sangat pasti (Tinsley, 1979). Untuk lebih jelasnya prinsip kerja spektrofemetrik dapat dilihat pada Gambar 7.
Gambar 7. Prinsip kerja spektrofotometrik
3.3.4.1. Pengukuran Kandungan Logam berat Untuk Ikan
Organ yang dibutuhkan untuk dapat digunakan dalam analisis AAS sebesar 5 gram. Kemudian ditimbang, dilakukan pengabuan kering sesudah penghilangan bahan-bahan organik dengan pengabuan kering, residu dilarutkan dalam asam encer. Larutan disebarkan dalam nyala api yang ada dalam alat AAS sehingga absorpsi/emisi logam dapat dianalisa dan diukur pada panjang gelombang tertentu.
Adapun prosedur metode Spektrofotometrik (AAS) adalah : (A).Larutan abu berasal dari pengabuan basah
1. Memindahkan larutan abu ke dalam labu takar. Pilih labu takar yang sesuai sehingga diperoleh konsentrasi logam yang sesuai dengan kisaran kerjanya.
2. Ditepatkan sampai tanda tera dengan air lalu campur sampai merata. (B). Abu berasal dari pengabuan kering
1. Ditambahkan 5-6 ml HCN 6 N ke dalam cawan/pinggan berisi abu, kemudian dengan ginjal-ginjal panaskan di atas hot plate (pemanas) dengan pemanasan rendah sampai kering.
2. Ditambahkan 15 ml HCN 3N, dan cawan dipanaskan di atas pemanas sampai mulai mendidih.
3. Didinginkan dan saring dengan menggunakan kertas saring, masukkan filtrat ke dalam labu takar yang sesuai. Usahakan padatan tertinggi sebanyak mungkin dalam cawan.
4. Ditambahkan 10 ml HCN 3N ke dalam cawan, kemudian panaskan sampai larutan mendidih.
5. Didinginkan, saring dan masukkan filtrat ke dalam labu takar.
6. Cawan dicuci dengan air sedikitnya 3 kali, saring air cucian lalu masukkan ke dalam labu takar.
7. Cuci kertas saring dan masukkan air cucian ke dalam labu takar. (C). Kaliberasi alat dan penetapan sampel
1. Diset alat AAS sesuai dengan instruksi dalam manual alat tersebut. 2. Diukur larutan standar logam dan blanko.
3. Diukur larutan sampel, selama penetapan sampel, diperiksa secara periodik apakah nilai standar konstan.
4. Dibuat kurva standar untuk masing-masing logam (nilai absorpsi/emisi vs konsentrasi logam m/ml.
Untuk mendapatkan konsentrasi logam berat yang sebenarnya digunakan rumus:
Kering Berat Penetapan Vol. x AAS K Sebenarnya K
3.3.4.2. Pengukuran Kandungan Logam berat dalam Air
1. Contoh air laut 500 ml disaring dengan kertas saring 0,45 m.
2. pH diatur kisarannya 3,5-4 dengan menambahkan dengan HNO3pekat. 3. Ditambahkan 1 ml larutan HNO3pekat.
4. Ditambahkan 5 ml campuran penahan buffer asetat.
5. Ditambahkan 5 ml amonium pirolidin ditiokarbonat (apdc), dikocok sekitar 5 menit.
6. Ditambahkan 10 ml pelarut organik metil iso butil keton (mibk), dikocok sekitar 3 menit dan biarkan ke dua fasa terpisah.
7. Ditampung fasa airnya. Fasa air ini digunakan untuk pembuatan larutan blanko laboratorium dan standar.
sekitar 5 detik dan biarkan kedua fasa terpisah. Buang fasa airnya.
9. Ditambahkan 1 ml HNO3 pekat, dan dikocok sebentar dan dibiarkan sekitar 15 menit.
10. Ditambahkan 9 ml air suling ganda bebas ion dan dikocok sekitar 2 menit serta ke dua fasa dibiarkan terpisah.
11. Ditampung fasa airnya dan siap diukur dengan AAS menggunakan nyala udara-asetilen.
3.3.4.3. Pengukuran Kandungan Logam berat dalam sedimen
1. Dimasukkan masing-masing contoh sedimen ke dalam beaker teflon secara merata agar mengalami proses pengeringan sempurna.
2. Kemudian dikeringkan contoh sedimen dalam oven pada suhu 1050 C selama 24 jam.
3. Contoh sedimen yang telah kering kemudian ditumbuk sampai halus. 4. Setiap contoh sedimen ditimbang sebanyak kurang lebih 4 gram dengan
alat timbang digital.
5. Contoh sedimen yang telah ditimbang dimasukkan kedalam beaker teflon yang tertutup.
6. Selanjutnya ditambahkan 5 ml larutan aqua regia dan dipanaskan pada suhu 1300C.
7. Setelah semua sedimen larut, pemanasan diteruskan hingga larutan hampir kering dan selanjutnya didinginkan pada suhu ruang dan dipindahkan ke sentrifus polietilen.
8. Kedalamnya ditambahkan aquades hingga volumenya mencapai 30 ml dan dibiarkan mengendap, kemudian tampung fasa airnya. Selanjutnya siap diukur dengan AAS, menggunakan nyala udara-asetilen.
Baku mutu sedimen
Baku mutu logam berat di dalam lumpur atau sedimen di Indonesia belum ditetapkan, sehingga sebagai acuan digunakan baku mutu yang dikeluarkan oleh IADC/CEDA (1997) mengenai kandungan logam yang dapat ditoleransi
keberadaannya dalam sedimen berdasarkan standar kualitas Belanda, seperti dapat dilihat pada Tabel 7.
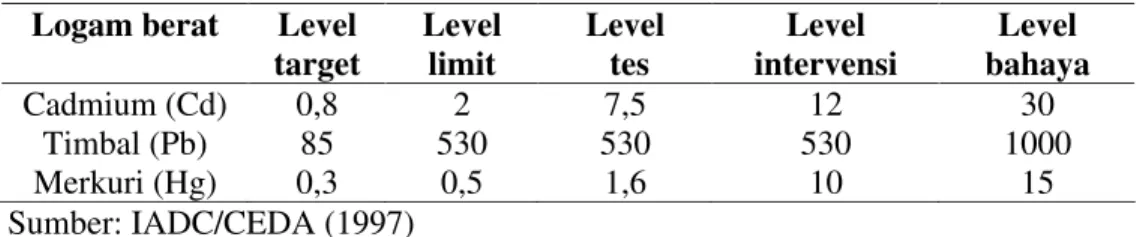
Tabel 7. Kandungan logam berat dalam sedimen (dalam ppm) Logam berat Level
target Level limit Level tes Level intervensi Level bahaya Cadmium (Cd) 0,8 2 7,5 12 30 Timbal (Pb) 85 530 530 530 1000 Merkuri (Hg) 0,3 0,5 1,6 10 15 Sumber: IADC/CEDA (1997) Keterangan :
a. Level target. Jika konsentrasi kontaminan yang ada pada sedimen memiliki nilai yang lebih kecil dari nilai level target, maka substansi yang ada pada sedimen tidak terlalu berbahaya bagi lingkungan.
b. Level limit. Jika konsentrasi kontaminan yang ada di sedimen memiliki nilai maksimum yang dapat ditolerir bagi kesehatan manusia maupun ekosistem. c. Level tes. Jika konsentrasi kontaminan yang ada di sedimen berada pada
kisaran nilai antara level limit dan level tes, maka dikategorikan sebagai tercemar ringan.
d. Level intervensi. Jika konsentrasi kontaminan yang ada di sedimen berada pada kisaran nilai antara level tes dan level intervensi, maka dikategorikan sebagai tercemar sedang.
e. Level bahaya. Jika konsentrasi kontaminan berada pada nilai yang lebih besar dari baku mutu level bahaya maka harus dengan segera dilakukan pembersihan sedimen.
3.3.4.4. Pengukuran Koefisien Distribusi (Kd) dan Biokonsentrasi Faktor (BCF)
Untuk melihat perbandingan koefisien distribusi (Kd) logam berat dalam air sedimen dan ikan digunakan rumus:
air berat] [Logam sedimen t] bera [Logam Kd
Untuk melihat tingkat biokonsentrasi faktor (BCF) digunakan rumus : air berat] [Logam ikan t] bera [Logam BCF1 sedimen berat] [Logam ikan t] bera [Logam BCF2
3.4. Analisa Data dan Penyajian Data 3.4.1. Analisa Deskriptif
Keseluruhan data parameter kualitas air dan logam berat yang ada di sedimen, badan air maupun yang terkandung pada ikan disajikan secara deskriptif.
3.4.2. Analisa Histopatologi
Disamping menganalisa besarnya kandungan logam berat yang ada dalam tubuh ikan, dilakukan pula analisa hasil foto histologis beberapa jaringan tubuh ikan yaitu insang dan ginjal ikan. Melalui cara ini dapat diketahui jenis-jenis kerusakan yang diakibatkan dari adanya penetrasi logam berat ke dalam tubuh ikan. Disamping itu juga untuk mengetahui tingkat kerusakan sel-sel pada organ.
Adapun rancangan yang digunakan adalah Rancangan Faktorial (Gasperz, 1991) dengan model matematis sebagai berikut :
Y
ijk= µ +
i+
j+ (
)
ij+
ijki = 1, 2,3 j = 1,2,3 Keterangan:
Y
ijk = Nilai kandungan logam berat di perairan Sungai Kampar yangmemperoleh kombinasi ij (taraf ke-i dari perlakuan air, sedimen, organ ikan dan taraf ke-j dari stasiun pengamatan)
µ
= Pengaruh umumi = Besar kandungan logam berat pada perlakuan ke-i j = Besar kandungan logam berat pada stasiun ke-j