5 BAB 2
TINJAUAN PUSTAKA
2.1 Resting Metabolic Rate (RMR) 2.1.1 Definisi
Pada keadaan beristirahat penuh, seseorang tetap membutuhkan sejumlah energi untuk mengerjakan seluruh reaksi kimia tubuh. Tingkat energi minimum yang diperlukan untuk bertahan hidup dinamakan Resting Metabolic Rate (RMR) dan mencakup sekitar 50 sampai 70 persen pengeluaran energi harian pada individu yang tidak aktif (sedentary) (Guyton & Hall, 2014). Selain itu, Resting Metabolic Rate (RMR) didefinisikan juga sebagai energi minimal yang dibutuhkan untuk
menunjang fungsi vital organ seperti jantung, paru-paru, hati, ginjal, saluran pencernaan, sistem saraf, organ seksual, otot dan kulit (Kumagai & Yahagi, 2013). Pada dasarnya resting metabolic rate dan basal metabolic rate adalah sama, perbedaan keduanya adalah BMR diukur pada pagi hari, setelah berpuasa selama semalam, tidak berolahraga 24 jam sebelumnya, bebas dari kondisi stres emosional, mengenal dengan baik alat yang akan digunakan untuk pengukuran dan subjek dalam kondisi istirahat total, sedangkan RMR diukur dalam kondisi terjaga, postabsorptif, termonetral dan tidak berolahraga 12 jam sebelumnya (McMurray et al., 2014). Resting metabolic rate atau basal metabolic rate mempunyai porsi
terbesar dalam total daily energi expenditure (TDEE) yang merupakan jumlah energi yang diperlukan tubuh untuk beraktivitas dalam sehari (Hills et al., 2014). 2.1.2 Peran RMR dalam mengatur keseimbangan energi
yang masuk sama dengan jumlah kalori yang dikeluarkan oleh otot-otot yang melakukan kerja eksternal ditambah dengan pengeluaran energi internal basal yang akhirnya muncul sebagai panas tubuh, pemasukan dan pengeluaran kalori berada dalam keseimbangan dan berat tubuh tidak berubah (Sherwood, 2014). Energi menjadi tidak seimbang ketika jumlah kalori yang dikonsumsi lebih besar daripada jumlah kalori yang dipakai untuk menjalankan proses dalam tubuh seperti bernafas, proses pencernaan, termogenesis. Penyebab terjadinya ketidakseimbangan energi ini dipengaruhi oleh banyak faktor. Faktor-faktor ini dapat dibagi menjadi 2 kelompok yaitu, penyebab proksimal serta penyebab distal (Gambar 2.1). Penyebab proksimal di antaranya adalah rasa lapar, rasa kenyang, pengeluaran energi, dan
Gambar 2.1
Penyebab distal dan proksimal ketidakseimbangan energi (Sansbury & Hill, 2014)
penyerapan nutrisi. Sedangkan yang termasuk penyebab distal di antaranya, pekerjaan, lingkungan sosial, keluarga, keadaan ekonomi, kebiasaan olahraga dan lingkungan tempat tinggal (Sansbury & Hill, 2014). Keseimbangan energi dalam tubuh sangat tergantung pada dua hal, yaitu energy intake dan energy expenditure.
Pola energy intake dipengaruhi oleh sinyal fisiologis yang kompleks yang berasal dari traktus gastrointestinal. Pada traktus gastrointestinal terdapat hormon dan enzim yang bekerja untuk memberikan sinyal episodik berupa inhibisi dan stimulus ke pusat kontrol sensasi rasa lapar di otak. Selain sinyal yang berasal dari traktus gastrointestinal, pusat kontrol terhadap sensasi rasa lapar juga dipengaruhi oleh sinyal tonik stimulus dan inhibisi yang berasal dari fat mass (jaringan lemak) dan fat-free mass (jaringan non lemak seperti otot, tulang, dan organ parenkim) yang
menyusun komposisi tubuh (Gambar 2.2). Fat-free mass dalam tubuh merupakan Gambar 2.2
Skema Mekanisme Kontrol Keseimbangan Energi (Blundell et al., 2020)
determinan utama yang menentukan RMR seseorang karena menunjukkan sumber fisiologis suatu rasa lapar yang mengatur intake makanan pada keadaan basal. Fat mass, yang merupakan inhibitor tonik utama, juga berkontribusi 5-7% pada RMR.
Komposisi tubuh, terutama fat-free mass, mempunyai nilai yang cenderung stabil, sehingga RMR juga mempunyai nilai yang cenderung stabil untuk memberikan sinyal jangka panjang (tonik) yang cenderung sama pula terhadap daily energy intake (Blundell et al., 2020).
Faktor-faktor yang mempengaruhi perbedaan RMR pada tiap individu, yaitu : 1. Usia
Peningkatan RMR yang terjadi setiap tahun pada usia anak-anak dan dewasa muda lebih tinggi bila dibandingkan dengan usia dewasa. Akan tetapi, semakin dewasa dan bertambah umur, RMR akan mengalami penurunan. Hal ini disebabkan karena komposisi tubuh manusia mengalami penurunan seiring bertambahnya umur, terutama massa otot. Selain itu, pertambahan usia juga akan menyebabkan organ-organ vital, seperti otak, ginjal, hati, dan limpa, yang memiliki tingkat metabolisme yang tinggi akan mengalami penurunan massa. Massa otot dan organ-organ vital termasuk komponen penyusun komposisi tubuh. Setiap tahun terjadi penurunan massa sebesar 0,002 kg pada otak, 0,001 kg pada ginjal, 0,003 kg pada hepar, dan 0,001 pada limpa (He et al., 2009; Lazzer et al., 2010). Akan tetapi, penuaan dikaitkan dengan peningkatan jaringan adiposa putih di perut dan pengendapan lemak pada otot rangka yang secara signifikan mempengaruhi sensitivitas insulin. Perubahan gaya hidup pada lansia saat memasuki masa
pensiun, dapat menyebabkan keadaan ketidakseimbangan energi kronis yang mengarah pada akumulasi jaringan lemak berlebih (Jura & Kozak, 2016). Penelitian yang dilakukan oleh Lam dan Ravussin (2016) menyebutkan bahwa RMR orang yang mengalami obesitas bernilai normal atau tinggi. 2. Jenis kelamin
RMR seseorang dipengaruhi oleh jenis kelamin karena perbedaan komposisi tubuh. Perempuan memiliki lebih banyak lemak tubuh (kurang aktif dalam proses metabolisme) daripada massa otot yang lebih banyak dimiliki oleh laki-laki (DeLany, 2017). RMR cenderung bergantung pada jaringan yang aktif dalam proses metabolisme, utamanya massa otot. (McMurray et al., 2014). Sehingga, laki-laki cenderung memiliki nilai RMR yang lebih tinggi daripada perempuan karena laki-laki memiliki massa otot yang lebih banyak. 3. Ukuran tubuh
Individu dengan ukuran tubuh yang besar akan membutuhkan jumlah energi yang lebih tinggi daripada individu dengan ukuran tubuh lebih kecil, karena jaringan tubuh yang dimiliki juga lebih banyak sehingga membutuhkan aktivitas metabolisme yang lebih besar. Berbagai faktor yang berpengaruh terhadap perbedaan tingkat metabolisme antarindividu adalah genetik, etnis serta lingkungan (Hills et al., 2014).
4. Komposisi tubuh
Fat-free mass yang merupakan komponen dari komposisi tubuh memiliki
peran besar dalam menentukan RMR. Fat-free mass memiliki aktivitas metabolisme yang tinggi. Meskipun kurang aktif dalam metabolisme, fat
mass merupakan faktor penting untuk memprediksi RMR, hal ini dikarenakan
fat mass berkontribusi sebanyak 5-7% pada RMR. Komposisi tubuh yang
berperan pada RMR dapat diprediksi dengan menggunakan rumus Kulkarni (Kulkarni et al., 2013) untuk menentukan fat-free mass dan Deurenberg equation untuk menentukan body fat percentage yang menunjukkan fat mass.
a. Rumus Kulkarni
Fat free mass (Kg) = -15.605 – (0.032 × usia dalam tahun) + (0.192 ×
tinggi dalam cm) + (0.502 × berat badan dalam Kg) b. Deurenberg equation
Body fat percentage (%) = (1.2 × BMI dalam Kg/m2) + (0.23 × usia dalam tahun) – (10.8 × jenis kelamin*) – 5.4
*Laki-laki = 1, perempuan = 0
Selain dengan menggunakan rumus, fat mass dan fat-free mass dapat diestimasi dengan menggunakan alat body impedance analysis (BIA). Kelebihan dari penggunaan BIA adalah metode pengukuran komposisi tubuh yang bersifat non-invasif, sederhana, murah, dan dapat digunakan pada kelompok besar dengan perbedaan karakteristik individu seperti umur, jenis kelamin dan etnis serta riwayat penyakit (Langer et al., 2016)
5. Etnis
Perbedaan RMR yang signifikan dipengaruhi oleh perbedaan etnis. Pada individu dengan etnis Eropa-Australia memiliki RMR yang lebih tinggi dibandingkan dengan etnis Afrika-Eropa (Nsatimba et al., 2015). Hal ini dikarenakan etnis Afrika-Eropa memiliki massa organ dengan
high-metabolic-rate (HMR), seperti liver, ginjal, lien, jantung dan otak, yang lebih
rendah dibanding etnis Eropa-Australia (Gallagher et al., 2006). 6. Genetik
Genetik merupakan salah satu faktor yang menentukan komposisi tubuh dari tiap individu. Hubungan antara RMR dan genetik didasarkan pada peran gen-gen yang berkaitan dengan indeks masa tubuh (IMT) dan obesitas, yaitu gen-gen PLA2G6, NEGR1, dan NRXN3. Gen PLA2G6 diekspresikan di kelenjar tiroid, sedangkan NEGR1 dan NRXN3 diekspresikan di otak (Leon-Mimila et al., 2013).
7. Kebugaran dan latihan fisik
Pada umumnya atlet mempunyai nilai RMR lebih tinggi dibandingkan dengan non-atlet. Pengaruh kebugaran dan latihan fisik secara langsung terhadap RMR masih belum bisa dijabarkan. Meskipun demikian, latihan aerobik dan kekuatan secara signifikan menghasilkan tingkat metabolisme lebih tinggi pada laki-laki maupun perempuan (DeLany, 2017).
8. Pengaruh lingkungan
Salah satu faktor lingkungan yang dianggap berpengaruh terhadap RMR adalah iklim. Inividu yang tinggal di lingkungan beriklim hangat memiliki RMR yang lebih rendah daripada individu yang tinggal di lingkungan beriklim lebih dingin (Froehle, 2008). Individu yang tinggal di daerah dataran tinggi (2500-3500 mdpl) memiliki RMR yang lebih tinggi, hal ini disebabkan karena pada saat berada di dataran tinggi menstimulasi sistem simpatoadrenal
sehingga terjadi peningkatan sekresi norepinefrin (Hill, Stacey, & Woods, 2011).
9. Status hormonal
Hormon tiroid mempunyai peranan penting dalam mengatur tinggi rendahnya RMR. Mekanisme pasti bagaimana hormon tiroid mempengaruhi RMR masih belum dipahami sepenuhnya (Yehuda-Shnaidman, Kalderon, & Bar-Tana, 2014), namun, diketahui bahwa hormon tiroid dapat meregulasi metabolisme oksidatif dan meningkatkan respirasi dari mitokondria (Oktay, Uslu, & Emekli, 2016).
2.1.3 Pengukuran RMR
Nilai RMR bisa didapatkan dari cara berikut: 1. Persamaan Harris-Benedict
a. Laki-laki: RMR (kcal/24h) = 66.473 + 5.003 × Tinggi + 13.75 × berat badan - 6.75 × usia
b. Wanita: RMR = 665.09 + 9.56 × tinggi + 1.84 × berat badan – 4.67 × usia
2. Kalorimeter
Metabolisme energi pada manusia melibatkan produksi energi dari pembakaran bahan bakar dalam bentuk karbohidrat, protein, dan lemak. Selama proses pembakaran ini, tubuh mengkonsumsi O2 dan memproduksi
CO2 sebagai zat buangan. Pengukuran energy expenditure (EE) melibatkan
pengukuran panas yang diproduksi atau panas yang hilang secara langsung, inilah yang dinamakan sebagai kalorimeter direk. Sedangkan pengukuran
panas yang diproduksi atau hilang dari tubuh dengan mengukur konsumsi O2 dan/atau produksi CO2 disebut sebagai kalorimeter indirek. Pada
awalnya kalorimeter yang dipakai untuk mengukur EE adalah kalorimeter direk, namun sebagian besar pengukuran EE yang dilakukan saat ini menggunakan kalorimeter indirek (Hills et al., 2014).
Metode dalam pengukuran RMR menggunakan kalorimeter indirek terbagi menjadi 2 yaitu, metode sirkuit terbuka dan tertutup. Pada pengukuran dengan metode sirkuit tertutup, CO2 yang terproduksi akan
diabsorpsi oleh soda lime. O2 ditambahkan untuk menjaga volume gas tetap
konstan (Gambar 2.3). RMR dihitung berdasarkan jumlah CO2 yang
diabsorpsi dan O2 yang dihirup (Henry, 2005). Pada metode sirkuit terbuka,
subjek bernafas dari atmosfer dan ekspirasi ke sistem. Selama proses
ekspirasi, gas berjalan melalui sistem (ventilasi meter) yang mengukur udara dan O2 serta CO2 ekspirasi. Perbedaan antara volume ekspirasi dan
inspirasi adalah VO2. Jumlah dari volume gas dan udara ekspirasi digunakan
Gambar 2.3
Kalorimeter Indirek Sirkuit Tertutup (McArdle, Katch, & Katch, 2010)
untuk menghitung uptake O2 (Welis & Sazeli, 2013). Volume O2 yang
diperoleh kemudian diubah dari ATPS (Ambient Temperature, Pressure and Saturated) menjadi STPD (Standard Temperature, Pressure and Dry) berdasarkan rumus : V STPD = V ATPS × 273 273+T × PB- PH20 760 Keterangan : T = Suhu Ruangan
P
B=
Tekanan barometerPH20 = Tekanan uap air (berdasarkan temperatur pada
kalorimeter)
Setelah didapatkan volume O2 yang standar, kemudian diukur selama 5
menit dikalikan dengan 4.825 Kcal dan diubah ke dalam satuan jam
Gambar 2.4
dengan mengalikan dengan 12 sehingga diperoleh hasil dengan satuan Kcal/jam. Hasil dari perhitungan tersebut kemudian dibagi dengan luas permukaan tubuh sesuai dengan normogram (Gambar 2.4) sehingga diperoleh hasil akhir RMR yang dinyatakan dalam Kcal/Jam/m2.
Pengukuran RMR menggunakan kalorimeter indirek idealnya dilakukan selama 10 menit. Pada interval 5 menit pertama, jumlah O2 yang
terukur pada recording drum diabaikan. Jumlah O2 yang dikonsumsi pada
interval 5 menit kedua yang digunakan untuk menghitung RMR. Hal ini disebabkan karena pada interval 5 menit kedua telah tercapai kondisi stabil pada konsumsi O2 (Borges et al., 2016)
2.2. Respirasi Mitokondria 2.2.1 Definisi
Respirasi mitokondria merupakan serangkaian reaksi metabolik dan proses yang membutuhkan oksigen bertempat di mitokondria untuk mengubah energi yang tersimpan dalam makronutrien menjadi adenosine triphosphate (ATP), donor energi universal yang diperlukan sel tubuh (Hoeks et al., 2012). Respirasi mitokondria terdiri dari beberapa tahap yaitu glikolisis, siklus asam sitrat, dan fosforilasi oksidatif. Proses utama sintesis ATP pada respirasi mitokondria terjadi pada tahap fosforilasi oksidatif yang terdiri dari rantai transpor elektron dan sintesis ATP (Sherwood, 2014).
2.2.2 Fosforilasi oksidatif dalam respirasi mitokondria
Bagian krista dari membran dalam mitokondria mengandung banyak komponen rantai respiratori yang disebut sebagai komplek fosforilasi oksidatif (I-IV).
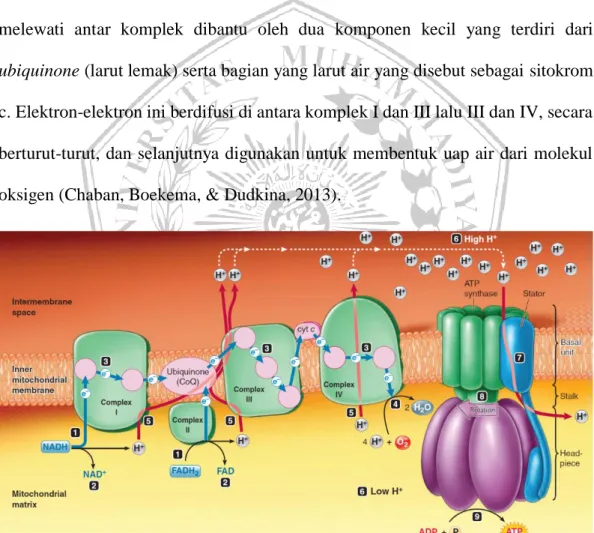
Keempat komplek ini beserta komplek V, yang berperan untuk sintesis ATP, membentuk mesin yang menghasilkan suplai energi untuk sel. Komplek I-IV berperan sebagai multisubunit enzim yang menghasilkan gradien elektrokimia. Proton menyeberangi membran dalam mitokondria, kemudian digunakan oleh komplek V untuk memproduksi ATP melalui fosforilasi oksidatif. NADH yang diproduksi selama glikolisis, siklus asam sitrat, dan oksidasi asam lemak menyusun bahan bakar utama untuk menggerakkan rantai respirasi. Elektron dihantarkan melewati antar komplek dibantu oleh dua komponen kecil yang terdiri dari ubiquinone (larut lemak) serta bagian yang larut air yang disebut sebagai sitokrom
c. Elektron-elektron ini berdifusi di antara komplek I dan III lalu III dan IV, secara berturut-turut, dan selanjutnya digunakan untuk membentuk uap air dari molekul oksigen (Chaban, Boekema, & Dudkina, 2013).
Gambar 2. 5 Fosforilasi Oksidatif (Sherwood, 2014)
Tahapan dalam fosforilasi oksidatif adalah sebagai berikut (Sherwood, 2014) (Gambar 2.5)
1. Elektron berenergi tinggi yang diekstraksi dari hidrogen dalam NADH dan FADH2 dipindahkan dari satu molekul pengangkut elektron ke yang lain.
2. NADH dan FADH2 diubah menjadi NAD+ dan FAD, yang memungkinkan
keduanya untuk mengambil lebih banyak atom hidrogen yang dibebaskan selama glikolisis dan siklus asam sitrat.
3. Elektron berenergi tinggi jatuh dari tingkat energi tinggi ke rendah sewaktu dipindahkan dari satu molekul pengangkut ke yang lain dalam sistem transpor elektron.
4. Elektron diberikan ke O2, akseptor elektron terakhir pada sistem transpor
elektron. Oksigen ini, kini bermuatan negatif karena mendapat tambahan elektron, bergabung dengan ion H+, yang bermuatan positif karena mendonorkan elektron pada awal sistem transpor elektron, untuk membentuk H2O.
5. Ketika bergerak melalui sistem transpor elektron, elektron melepaskan energi bebas. Sebagian energi yang dibebaskan hilang sebagai panas, tetapi sebagian lagi dimanfaatkan untuk transpor H+ melintasi membran dalam mitokondria dari matriks menuju ruang antarmembran pada kompleks I, III, dan IV. 6. Akibatnya, ion H+ lebih terkonsentrasi di ruang antarmembran daripada di
matriks. Gradien H+ ini menghasilkan energi yang menggerakkan sintesis ATP oleh ATP sintase.
7. Karena gradien ini, ion H+ memiliki kecenderungan tinggi untuk mengalir ke
dalam matriks melintasi membran dalam lewat saluran-saluran di antara unit dasar dan stator pada kompleks ATP sintase.
8. Aliran ion H+ ini mengaktifkan ATP sintase dan menggerakkan sintesis ATP oleh headpiece, proses yang dinamakan kemi osmosis. Aliran ion H+ melalui saluran ini membuat headpiece dan tangkai berputar ke atas.
9. Akibat perubahan bentuk dan posisi sewaktu berputar, headpiece mengambil ADP dan Pi, menggabungkan keduanya dan membebaskan produk ATP.
Fosforilasi oksidatif dalam respirasi mitokondria tidak sepenuhnya efisien karena tidak semua molekul O2 yang dikonsumsi dalam rantai transpor elektron
digunakan untuk proses sintesis ATP. Kebocoran proton, yang termasuk salah satu proses uncoupling, merupakan penyebab signifikan yang membuat respirasi mitokondria tidak efisien.
2.2.3 Konsep coupling dan uncoupling serta korelasi dengan RMR
Coupling adalah kondisi dimana konsumsi O2 oleh respirasi mitokondria
digunakan untuk mengkatalis ADP sehingga terbentuk menjadi ATP. Namun efisiensi sintesis ATP tersebut tidak 100% karena adanya kebocoran proton dari
Rantai transpor elektron
Sintesis ATP
Kebocoran proton Gambar 2.6
Kebocoran proton pada fosforilasi oksidatif (Hoeks et al., 2012)
ruang antarmembran ke matriks mitokondria sehingga gradien proton akan menghilang dan terjadi uncoupling (Gambar 2.6). Uncoupling adalah suatu keadaan dimana ada O2 yang dikonsumsi pada rantai respirasi tanpa disertai dengan sintesis
ATP karena konsumsi O2 tersebut hanya digunakan untuk mengkompensasi
hilangnya gradien proton yang disebabkan oleh kebocoran proton (Thrush et al., 2013; Hoeks et al., 2012).
Terdapat 3 mekanisme uncoupling yaitu basal and inducible proton leak, electron leak, dan electron slip. Basal proton leak terjadi ketika proton secara
langsung lepas dari ruang antarmembran dengan cara berdifusi melalui membran dalam mitokondria. Proton leak juga bisa terjadi dengan cara diinduksi atau diregulasi oleh beberapa protein seperti UCPs (Uncoupling Proteins) atau ANTs (Adenine Nucleotide Translocases). Dalam kondisi normal, elektron ditransfer ke oksigen untuk membentuk molekul air. Electron leak adalah proses dimana elektron lepas dari rantai transport elektron sehingga dapat menyebabkan terbentuknya anion superoksida (O2-) atau radikal hidroperoksil (•OH). Electron slip terjadi saat
adanya proses transfer elektron melalui kompleks respirasi tanpa disertai proton pumping (Demine et al., 2019)
Dari beberapa mekanisme di atas, kebocoran proton adalah sumber signifikan dari proses uncoupling yang menyebabkan fosforilasi oksidatif tidak bisa berjalan efisien dan diperkirakan menyumbang 20-25% dari jumlah RMR. Kebocoran proton dapat dikurangi dengan menurunkan ekspresi protein adenine nucleotide translocase (ANT) (Larsen et al., 2011).
2.3. Semangka Kuning (Citrullus lanatus) 2.3.1 Taksonomi (ITIS report, 2011)
Kingdom : Plantae Subkingdom : Viridiplantae Infrakingdom : Streptophyta Superdivisi : Embryophyta Divisi : Tracheophyta Subdivisi : Spermatophytina Kelas : Magnoliopsida Superordo : Rosanae Ordo : Cucurbitales Family : Cucurbitaceae
Genus : Citrullus Schrad
Species : Citrullus lanatus 2.3.2 Morfologi
Semangka termasuk tanaman semusim sehingga di Amerika, Eropa, Jepang digolongkan ke dalam kelompok tomat, cabe, terong sebagai golongan sayuran buah. Di Indonesia, semangka termasuk golongan buah-buahan seperti melon dan stroberi. Semangka tumbuh merambat hingga mencapai panjang 3,5-5,6 meter dengan batang berbentuk bulat, lunak, berambut, dan sedikit berkayu. Cabang-cabang lateral mirip dengan Cabang-cabang utama. Permukaan tanaman (batang dan daunnya) tertutup bulu-bulu halus dan tajam. Daun semangka berseling, bertangkai, helaian daunnya lebar dan berbulu, menjari, dengan ujungnya runcing. Panjang
daun sekitar 3-25 cm dengan lebar 1,5-5 cm. Bagian tepi daun bergelombang dan permukaan bawahnya berambut rapat pada tulangnya (Sobir & Siregar, 2010). Bunga tanaman semangka muncul pada ketiak tangkai daun, berwarna kuning cerah. Semangka memiliki tiga jenis bunga, yaitu bunga jantan (staminate), bunga betina (pistillate), dan bunga sempurna (hermaphrodite). Pada umumnya bunga betina memiliki bunga jantan dan bunga betina dengan proporsi 7:1. Penyerbukan bunga terjadi secara silang (cross compatible) melalui perantara lebah madu dan lalat hijau. Mahkota bunganya berwarna kuning. Tangkai bunga jantan berdiameter kecil dan panjang, sedangkan pada tangkai bunga betina tampak bakal buah yang menggelembung. (Wulandari, 2012)
Bentuk buah semangka bermacam-macam, ada yang berbentuk bulat, oval, dan lonjong. Berdasarkan ukuran buah semangka dibedakan berdasarkan beratnya, yaitu:
a. Buah besar, beratnya lebih dari 4 kg b. Buah sedang, beratnya 2-4 kg
c. Buah kecil, beratnya kurang dari 2 kg 2.3.3 Syarat tumbuh (Kalie, 2008)
1) Semangka berasal dari Afrika, suatu daerah tropika dengan cahaya matahari penuh, sedangkan suhu udara tinggi dan kering. Iklim yang kering dan panas, sinar matahari dan air yang cukup merupakan kebutuhan tanaman yang utama
2) Perkecambahan biji akan berlangsung dengan baik pada suhu 25-30oC. Suhu 18-20oC merupakan suhu minimum untuk perkecambahan biji.
Suhu udara yang tinggi di atas 20oC (suhu siang antara 25-30oC dan suhu
malam antara 12-18oC) merupakan suhu yang paling cocok bagi pertumbuhan karena tanaman akan tumbuh dengan cepat dan kuat 3) Suhu yang lebih tinggi lagi masih diperlukan bila calon buah sudah
terbentuk. Proses pemasakan buah yang baik membutuhkan panas yang berkisar suhu 30oC
4) Curah hujan yang baik bagi tanaman semangka adalah 40-50 mm/bulan 5) Akar tanaman semangka menghendaki media tumbuh yang berpori
dengan lahan yang gembur dan subur, mengandung banyak bahan organik, serta mempunyai drainase yang baik. Tanah berpasir atau tanah lempung berpasir yang banyak mengandung nitrogen cocok untuk tanaman ini
6) Pertumbuhan semangka akan baik pada pH 6-6,7, akan tetapi tanaman ini juga dapat tumbuh pada pH 5-7 karena memiliki toleransi yang cukup besar
2.3.4 Kandungan semangka kuning
Semangka merupakan buah segar yang dapat langsung dikonsumsi tanpa pengolahan. Namun, beberapa masyarakat biasa mengolah semangka menjadi berbagai produk lain, seperti selai, salad, puding, dan jus buah. Daging buah semangka mengandung berbagai macam unsur gizi, baik makro (zat gizi yang dibutuhkan dalam jumlah besar oleh tubuh) maupun unsur mikro (zat gizi yang dibutuhkan dalam jumlah kecil oleh tubuh. Daging buah semangka relatif rendah kalori dan banyak mengandung air (92%). Kandungan zat gizi lain dalam semangka
adalah protein (0,5%), karbohidrat (6,9%), lemak (0,2%), dan berbagai vitamin. Berikut kandungan zat gizi semangka secara lengkap (Tabel 2.1) dan (Tabel 2.2).
Tabel 2.1 Nutrisi pada 100 g Semangka kuning
Komponen Jumlah Energi 28 kal Air 92,1% Protein 0,5 g Lemak 0,2 g Karbohidrat 6,9 g Vitamin A 590 SI Vitamin C 6 mg Nikotinamid - Niasin 0,2 mg Riboflavin 0,05 mg Thiamin 0,05 mg Abu 0,3 mg Kalsium (Ca) 7 mg Besi (Fe) 0,2 mg Fosfor (P) 12 mg
Tabel 2.2 Kandungan sitrulin dari beberapa varietas semangka Varietas Warna Daging
Buah
Kandungan Sitrulin (mg/g)
Dengan biji
Cream of Saskatchewan Putih 1,0
Jamboree Merah 3,1
Sangria Merah 1,6
Summer Flavor 800 Merah 1,2
Summer Gold Kuning 3,6
Tender Sweet Orange Oranye 0,5
Tanpa biji
Hazera 6009 Merah 2,4
Hazera 6007 Merah 2,5
Hazera SW1 Merah 3,5
Orange Sunshine Oranye 3,0
Scarlet Trio Merah 1,4
Solid Gold Kuning 3,5
(Rimando & Perkinz-Veazie, 2005) (Kalie, 2008)
Di dalam semangka juga terdapat kandungan asam amino L-sitrulin. L-sitrulin adalah asam amino yang merupakan prekursor efektif dalam sintesis arginin, yang mana arginin akan diubah menjadi nitric oxide (NO) oleh enzim Endotelial Nitric Oxide Synthase (eNOS). Kandungan L-sitrulin tertinggi terdapat pada semangka
kuning berbiji dengan varietas Summer Gold (Tabel 2.2). 2.3.5 Pengaruh L-sitrulin terhadap NO
Setelah mengkonsumsi semangka kuning, L-sitrulin yang masuk ke dalam tubuh manusia akan mengalami metabolisme efektif di intestin dan liver, yang memungkinkan untuk mencapai ginjal. Di dalam ginjal, L-sitrulin diabsorbsi di sel tubulus proksimal ginjal kemudian dikonversi menjadi argininosuksinat dengan bantuan enzim argininosuccinate synthase (ASS). Selanjutnya, argininosuksinat akan dikonversi menjadi L-arginin dengan bantuan enzim argininosuccinate lyase (ASL). Oleh enzim Nitric Oxide Synthase (NOS), L-arginin akan terkonversi menjadi nitrit oksida (NO) dan juga L-sitrulin. NO hasil konversi dari L-arginin akan masuk ke dalam mitokondria yang ada di dalam sel (Figueroa et al., 2017). Konsentrasi L-arginin dalam sirkulasi mencapai puncak setelah sekitar 1-2 jam (Moinard et al., 2007). Rata-rata waktu paruh (T1/2) L-sitrulin dalam tubuh adalah
1 jam, dengan volume distribusi 0,9 L/kg dan clearance L-sitrulin pada ginjal diestimasi sekitar 0,6 L/kg/jam (Barr et al., 2007). Rentang dosis klinis konsumsi L-sitrulin yang bisa ditoleransi pada orang sehat adalah 2-15 g secara per oral dalam sehari (Johnson et al., 2017).
2.4. Pengaruh NO terhadap RMR
Setelah masuk ke mitokondria yang ada di dalam sel, NO akan berkompetisi dengan oksigen (O2) untuk berikatan dengan sitokrom c oksidase (COX). Karena
O2 memiliki afinitas yang lebih rendah daripada NO, maka jumlah molekul O2 yang
berikatan dengan COX akan menurun. Ikatan NO dengan COX akan menurunkan ekspresi protein ANT sehingga kebocoran proton dapat dikurangi (Poderoso et al., 2019; Larsen et al., 2011). Pengurangan kebocoran proton akan meningkatkan efisiensi fosforilasi oksidatif. Efisiensi ini menunjukkan bahwa sebagian besar potensial membran didistribusikan ke mekanisme sintesis ATP. Mekanisme efisiensi fosforilasi oksidatif yang dicapai mengindikasikan adanya penurunan RMR (Larsen et al., 2011). Dengan adanya penurunan RMR menyebabkan penurunan sinyal tonik yang merangsang nafsu makan dan menyebabkan intake makanan menurun sehingga jumlah konsumsi kalori dapat dikendalikan dengan lebih baik (Blundell et al., 2015).