1
UJI AKTIVITAS ANTIOKSIDAN DAN SITOTOKSISITAS FRAKSI DAUN KENTUTAN (Paederia foetida L.)
Djoko Parwanto1*, Muhamad Agus Wibowo1
1Program Studi Kimia Fakultas MIPA, Universitas Tanjungpura,
Jl. Prof. Dr. H. Hadari Nawawi 78124
*Email: Djo_ko15@yahoo.com ABSTRAK
Kentutan (Paederia foetida L.) termasuk tumbuhan famili Rubiaceae.Tumbuhan ini telah diketahui memiliki sifat antioksidan dan sitotoksisitas pada ekstrak kasar metanol. Penelitian ini bertujuan untuk mengetahui perbandingan kandungan metabolit sekunder, kandungan total fenol, aktivitas penangkapan radikal 2,2-difenil-1-pikrilhidrazin (DPPH) dan aktivitas sitotoksik terhadap larva Artemia salina oleh fraksi-fraksi nya. Fraksi yang digunakan pada penelitian ini adalah fraksi n-heksana, fraksi kloroform, dan fraksi metanol. Berat sampel ekstrak daun P.foetida adalah 46,326 gram dengan rendeman dari masing-masing fraksi adalah 0,3084%, 0,5369%, dan 2,1243%. Hasil skrining fitokimia dan kromatografi lapis tipis (KLT) menunjukkan bahwa semua fraksi mengandung senyawa alkaloid, flavonoid, polifenol, dan terpenoid. Fraksi metanol pada penelitian ini telah diketahui memiliki kandungan total fenol dan IC50
paling baik yaitu sebesar 37,960 µgTAE/mg dan 39,836. Sedangkan pada fraksi n-heksana memiliki nilai LC50 paling baik yaitu sebasar 291,031. Berdasarkan hasil penelitian menunjukkan bahwa pada
fraksi-fraksi daun P.foetida berpotensi sebagai antioksidan dan sitotoksisitas.
Kata kunci:Kentutan (Paederia foetida L), Total fenol, Antioksidan, Sitotoksisitas. PENDAHULUAN
Kentutan (Paederia foetida L.) termasuk tanaman famili Rubiaceae yang tersebar luas di Indonesia.Masyarakat sering memanfaatkannya sebagai antirematik, penghilang rasa sakit, peluruh kentut, antibiotik, antibatuk, penghilang racun, obat cacing, dan pereda kejang (Hariana, 2007).Uji skrining fitokimia terhadap ekstrak metanol daun P.foetida telah diketahui mengandung senyawa bioaktif seperti fenol, flavonoid, alkaloid dan terpenoid (Thirupathi et al., 2013).Menurut penelitian Osman et al (2009) kandungan total fenol dan aktivitas antioksidan pada ekstrak metanol daun P.foetida menggunakan metode β-karoten dan 2,2-azinobis (3-ethylbenzothiazoline-6-sulfonic acid) (ABTS) menunjukkan aktivitas antioksidan yang tinggi yaitu 80%. Penelitian lain tentang ekstrak metanol daun P.foetida juga diketahui bersifat sitotoksik yang sangat signifikan terhadap Artemia salina dengan nilai LC50 1,5625 μg/mL (Morshed et al., 2012).
Antioksidan dapat bersumber dari tanaman karena umumnya mengandung senyawa bioaktif dalam bentuk metabolit sekunder seperti alkaloid, flavanoid, steroid, terpenoid dan lain-lain. Salah satu sumber antioksidan alami yang berpotensi sebagai antikanker dari famili Rubiaceae yang telah diketahui aktivitas nya sepertibuah mengkudu (Morinda citrifolia L.), ranggitan (Rubia cordifolia L.) dan rumput mutiara (Hedyotis corymbosa L.)(Sukamdi et al., 2008; Govind, 2011).
Kajian tentang kandungan total fenol, aktivitas antioksidan dan aktivitas sitotoksik dari
ekstrak metanol kasar daun P.foetida telah dilakukan, namun perbandingan fraksi (metanol, kloroform dan n-hekasana) belum pernah dilakukan. Berdasarkan penelusuran literatur yang telah dilakukan, maka penelitian ini bertujuan membandingkan kandungan total fenol dan aktivitas antioksidan ekstrak daun P.foetida diukur menggunakan metode 2,2-difenil-1-pikrilhidrazil (DPPH) serta aktivitas sitotoksik untuk mengetahui tingkat toksisitas dari masing-masing fraksi tersebut menggunakan metode Brine Shrimp Lethality Test (BSLT).
METODOLOGI PENELITIAN
Alat
Alat-alat yang digunakan adalah seperangkat
alat gelas kimia yang umum di laboratorium kimia, rotary evaporator, spektrofometer UV/Vis, labu ukur, kaca arloji, spatula, neraca analitik, tabung reaksi dan vial.
Bahan
Bahan kimia yang digunakan antara lain
akuades(H2O), asam klorida (HCl), asam sulfat (H2SO4), 2,2-difenil-1-pikril-hidrazil (DPPH), dimetil sulfoksida (DMSO), plat KLT, vanilin, dinatrium, kloroform (CHCl3), metanol (CH3OH), n-heksana (C6H14), natrium karbonat (Na2CO3), natrium klorida(NaCl), reagen Wegner, reagen Dragendroff’s, reagen Folin-Ciocalteu, dan serbuk Mg.
JKK, Tahun 2015, Volume 4(1), halaman 1-6 ISSN 2303-1077
2 Bahan Uji
Sampel yang digunakan pada penelitian ini adalah P.foetida yang berasal dari kawasan desa Sukadana Kabupaten Kayong Utara yang diambil pada titik S 01o 15’ 08,9” dan E 19o 57’ 10,0”. Keakuratan spesies dari tumbuhan berdasarkan hasil determinasi di Fakultas MIPA, Universitas Brawijaya.
Gambar 1. Daun P.foetidaL Cara Kerja
Ekstraksi dan Partisi
Serbuk kering daun P.foetida 2 kg dilakukan maserasi dengan pelarut metanol pada suhu ruang. Proses maserasi dilakukan selama 3 x 24 jam. Ekstrak kemudian disaring untuk mendapatkan filtrat dan residu. Maserat yang dihasilkan disaring, dikumpulkan dan diuapkan dengan alatrotary evaporator, sehingga diperoleh ekstrak kental metanol.
Ekstrak metanol kemudian dilakukan partisi menggunakan pelarut dengan tingkat kepolaran yang berbeda.Pertama menggunakan pelarut n-heksana, fraksi metanol kemudian dilakukan partisi kembali dengan pelarut kloroform dan diperoleh fraksi kloroform. Semua fraksi selanjutnya dilakukan uji aktivitas antioksidan dengan DPPH dan kandungan total fenol untuk mengetahui kekuatan antioksidannya serta melakukan uji toksisitas dengan menggunakan udang Artemia Salina Leach untuk mengetahui potensi antikanker (sitotoksik).
Uji Metabolit Sekunder
Identifikasi alkaloid
Masing-masing sampel di ambil beberapa tetes dan ditambahkan dengan pereaksi Dragendorf dan pereaksi Wagner.Jika terbentuk endapan berwarna merah jingga dan coklat maka sampel menunjukkan hasil positif adanya alkaloid (Harborne, 1987).
Identifikasi flavonoid
Masing-masing sampel di ambil beberapa tetes dan ditambahkan dengan beberapa tetes asam klorida (HCl) dan 0,2 gram logam Mg. Selanjutnya di amati terbentuknya warna merah
yang menunjukkan hasil positif adanya flavonoid. (Harborne, 1987).
Identifikasi tanin/polifenol
Masing-masing sampel di ambil beberapa tetes dan ditambahkan dengan 2-3 tetes larutan feriklorida (FeCl3) 5%.Terbentuknya warna hitam kebiruan atau hijau menunjukkan adanya tanin (Harborne, 1987).
Penentuan terpenoid-steroid
Uji Lieberman–Burchard,masing-masing sampel diambil beberapa tetes dan ditambahkan dengan pereaksi Lieberman-Buechard.Senyawa terpenoid ditunjukkan dengan terjadinya warna merah jingga atau ungu, sedangkan adanya steroid ditunjukkan dengan adanya warna biru.(Pembuatan reagen Lieberman-Buechard: terdiri dari asam sulfat pekat dan asam asetat anhidrat dan disimpan dalam botol coklat). (Harborne, 1987).
Kromatografi Lapis Tipis (KLT) (Irianti dkk., 2011)
Sampel dari masing-masing fraksi dilakukan analisis KLT menggunakan plat silika dengan pelarut yang memiliki tingkat kepolaran berbeda yaitu metanol, kloroform, etil asetat, dan n-heksan. Selanjutnya ditotolkan ekstrak kasar kasar dan masing-masing fraksi didalam chamber yang berisi pelarut dengan perbandingan dari setiap sampel sebagai berikut : ekstrak fraksi N-heksana etil asetat : n-heksana (1:9), ekstrak fraksi kloroform etil asetat : n-heksana (9:1) dan ekstrak fraksi metanol terlarut metanol : n-heksana (9:1) kemudian kromatogram dikeringkan dan disemprot dengan larutan dragendroff, H2SO4 2N, dan FeCl3 1% dan vanilin 1%.Setelah 30 menit kromatogram diamati untuk melihat senyawa yang aktif. Pengujian ekstrak dan fraksi dari sampel daun P.foetida dilakukan dengan penyemprotan menggunakan dragendroff (coklat, jingga), H2SO4 (kuning, jingga), FeCl3 (biru, hitam, hijau), vanilin 1% (ungu, biru, merah
Penentuan kandungan total fenol
Uji kandungan total fenol ditentukan menggunakan metode Folin-Ciocalteu mengacu pada metode Makkar, et al, (1993). Sebanyak 0,2 mL larutan ekstrak dicampur dengan 0,5 mL reagen Folin-Ciocalteu 1N. Campuran dihomogenkan selama 5 menit kemudian ditambahkan 1,0 mL Na2CO3 20%. Campuran dibiarkan dan digoyang pada kondisi gelap selama 1 jam.Absorbansi diukur pada λmaks 735 nm dengan menggunakan spektrofotometer UV-Vis.
3 Uji Aktivitas Antioksidan dengan Metode DPPH (Khanahmadi.,et al 2010)
Sebanyak 10 mg sampel dilarutkan dalam 10 mL metanol untuk memperoleh 1000 µg/mL ekstrak. Dari 1000 µg/mL larutan ekstrak dibuat variasi konsentrasi 20, 50, 100, 250 dan 500 µg/mL yang dilarutkan dengan metanol dan dicampurkan dengan 2 mL larutan DPPH 0,002% dalam metanol, digoyang kemudian campuran didiamkan selama 30 menit. Diukur absorbansinya pada λmaks 525 nm dengan menggunakan spektrofotometer UV-Vis. Rumus hasil % peredaman yaitu:
Hasil persen (%) peredaman yang diperoleh, dapat dihitung dengan persamaan regresi kemudian ditentukan nilai IC50, dimana konsentrasi efektif yang dibutuhkan untuk menurunkan 50% intensitas serapan.
Uji Toksisitas dengan Metode Brine Shrimp
Lethality Test (BSLT) (McLaughlin, 1998) Uji sitotoksisitas dilakukan dengan membuat larutan induk yaitu menimbang sebanyak 50 mg sampel kemudian dilarutkan dalam 25 mL air laut buatan (
38 g garam laut
dilarutkan dalam 1L akuades)
, ditambah 3 tetes DMSO (dimetil sulfoksida). Konsentrasi larutan induk yaitu 2000 ppm, kemudian diencerkan menjadi tiga macam konsentrasi yaitu 0, 10, 100 dan 1000 ppm. Konsentrasi 0 ppm sebagai kontrol.Sebanyak 10 ekor udang dimasukkan ke dalam masing-masing botol vial yang telah diisi larutan sampel dengan konsentrasi masing-masing 10, 100, 1000 ppm dengan tiga kali ulangan. Botol vial masing-masing berisi 5 mL (air laut, sampel dan 10 ekor udang dan satu sebagai kontrol. Setelah 24 jam, diamati jumlah udang yang mati untuk tiap-tiap konsentrasi. HASIL DAN PEMBAHASAN
Ekstraksi dan partisi
Hasil maserasi sampel degan pelarut metanol diperoleh sekitar 46,326g dengan rendeman sekitar 2,3163%. Ekstrak berbentuk cairan kental dan berwarna kehijauan. Hasil partisi ekstrak P.foetida diperoleh tiga fraksi
yaitu fraksi terlarut n-heksana, fraksi kloroform dan fraksi metanol (Tabel 1)
Tabel 1. Rendemen fraksi n-heksana, kloroform dan metanol daun P.foetida
Sampel Rendeman (%)
Fraksi n-heksana 0,3084
Fraksi kloroform 0,5369
Fraksi metanol 2,1243
Skrining Fitokimia dan Kromatografi Lapis Tipis (KLT) Daun P.foetida
Pengujian skrining fitokimia dilakukanmenggunakan reagen-reagen kimia untuk menguji kandungan alkaloid, flavonoid, polifenol dan terpenoid/steroid. Selain itu, dilakukan juga uji kromatografi lapis tipis (KLT) pada sampel penelitian ini untuk lebih menegaskan hasil yang didapat dari skrining fitokimia
Hasil uji metabolit sekunder pada fraksi n-heksana, fraksi kloroform dan fraksi metanol menunjukkan bahwa mengandung alkaloid, flavonoid, polifenol, terpenoid.Senyawa dominan pada fraksi n-heksana yaitu senyawa terpenoid.Hasil ini ditandai terbentuknya noda ungu yang sangat kuat pada plat KLT di Rf3 (Gambar (A.vi)).Senyawa dominan pada fraksi kloroform yaitu senyawa alkaloid.Hasil ini ditandai terbentuknya noda hijau dengan latar jingga yang sangat kuat pada plat KLT di Rf2 (Gambar (B.iii)).Senyawa dominan pada fraksi metanol yaitu senyawa flavonoid.Hasil ini ditandai terbentuknya noda biru flouresensi kuning yang sangat kuat pada plat KLT di Rf2 (Gambar (C.v)).
Tabel 2. Hasil Uji Fitokimia
Fitokimia n-Heksana Ekstrak Kloroform Metanol
Alkaloid -Wagner -Dragendoff + + + + + + Flavonoid -Mg-HCl - + + Tanin/ Polifenol - + + Steroid/ Terpenoid + + +
JKK, Tahun 2015, Volume 4(1), halaman 1-6 ISSN 2303-1077
4
Gambar 2. (A) Profil KLT fraksi n-heksana, fasa diam silika gel 60 F254 dan fasa gerak etil asetat : n-heksana (1:9).
(B) Profil KLT fraksi kloroform, fasa diam silika gel 60 F254 dan fasa gerak etil asetat : n-heksana (9:1).
(C) Profil KLT fraksi metanol, fasa diam silika gel 60 F254 dan fasa gerak metanol : n-heksana (9:1).
Bercak noda yang terbentuk diamati (i) langsung, (ii) Cahaya UV254nm, (iii), Dragendroff, (iv) FeCl3 5%,
(v) H2SO4, (vi) Vanilin 1%
Tabel 3. Hasil KLT Fraksi n-Heksana
Tabel 4. Hasil KLT Fraksi Kloroform
Tabel 5. Hasil KLT Fraksi Metanol
Rf langsung Secara Cahaya UV
254 Dragendroff FeCl3 H2SO4 Vanilin 1% Ket
0,40 Noda terlihat jelas Noda terlihat jelas Hitam dengan latar jingga - Biru kemerahan Hijau kehitaman Terdapat senyawa alkaloid, flavonoid, polifenol dan terpenoid 0,57 Noda terlihat jelas Noda terlihat jelas Hitam dengan latar jingga Hitam kehijauan Ungu Hijau kehitaman 0,71 Noda terlihat jelas Noda terlihat jelas Hitam dengan latar jingga - - ungu 0,80 Noda terlihat jelas Noda terlihat jelas Hitam dengan latar jingga Hitam kehijauan Kuning Hijau Kehitaman 0,89 - Noda terlihat jelas
- Hitam kehijauan Biru Kehitaman -
Rf langsung Secara Cahaya UV
254 Dragendroff FeCl3 H2SO4 Vanilin 1% Ket
0,34 - Noda terlihat jelas Hitam dengan latar jingga Hitam kehijauan Hijau flourensi kuning Hitam kehijauan Terdapat senyawa alkaloid, flavonoid, polifenol dan terpenoid 0,51 Noda terlihat jelas Noda terlihat jelas Hitam dengan latar jingga Hitam kehijauan Hijau flourensi kuning Hitam 0,63 - Noda terlihat jelas - Hitam kehijauan Hijau flourensi kuning Hitam 0,69 Noda terlihat jelas Noda terlihat jelas Hitam dengan latar jingga - - - 0,74 Noda terlihat jelas Noda terlihat jelas Hitam dengan latar jingga - - - 0,97 Noda terlihat jelas Noda terlihat jelas Hitam dengan latar jingga Hitam kehijauan Hijau flourensi kuning Merah kehitaman
Rf langsung Secara Cahaya UV
254 Dragendroff FeCl3 H2SO4 Vanilin 1% Ket
0,06 Noda terlihat jelas Noda terlihat jelas
- Hitam kemerahan Jingga Cokelat Terdapat senyawa alkaloid, flavonoid,p olifenol 0,80 - - - - Biru flourensi kuning Hitam 089 Noda terlihat jelas Noda terlihat jelas Hitam dengan latar jingga Hitam Hijau flourensi kuning Cokelat
5 Penentuan Kandungan Total Fenol
Penentuan kandungan total fenol dilakukan berdasarkan kemampuan senyawa fenolik mereduksi fosfomolibdat fosfotungstat dalam Folin-Cioucalteu membentuk molibdenum yang berwarna biru.
Tabel 6. Kandungan Total Fenol Fraksi Daun P.foetida
Sampel Kandungan Total Fenol (µgTAE/mg)
Fraksi n-heksana 19.125
Fraksi Kloroform 28.630
Fraksi metanol 37.960
Hasil penentuan kandungan total fenol menunjukkan bahwa senyawa golongan fenol banyak terdapat di fraksi metanol. Hasil ini juga telah dibuktikan dengan pengujian menggunakan plat KLT dengan FeCl3 dan H2SO4 juga menunjukkan noda hitam dan biru flouresensi kuning yang kuat dibandingkan dengan fraksi n-hekana dan fraksi kloroform. Hal ini dapat terjadi karena senyawa golongan fenol bersifat polar atau semi polar. Fraksi dari masing-masing sampel kemudian ditentukan aktivitas antioksidannya dengan metode DPPH, Uji Aktivitas Antioksidan dengan Metode DPPH
Pengujian aktivitas antioksidan dengan metode DPPH prinsipnya berdasarkan kemampuan antioksidan menghambat radikal bebas dengan cara mendonorkan atom hidrogen kepada DPPH. Reaksi DPPH dengan antioksidan akan menetralkan radikal bebas dari DPPH dan membentuk DPPH-H (Molyneux, 2004).
Tabel 7. Nilai IC50 Fraksi daun P.foetida
Sampel Aktivitas antioksidan
IC50 (ppm)
Fraksi n-heksana 155,000
Fraksi kloroform 75,472
Fraksi metanol 39,836
Berdasarkan uji aktivitas antioksidan yang dilakukan dengan metode DPPH, nilai aktivitas antioksidan dikatakan sangat kuat apabila nilai IC50<50 μg/mL dan dikatakan sangat lemah apabila nilai IC50>150 μg/mL (Ariyanto, 2006).Hasil uji aktivitas antioksidan dengan metode DPPH menunjukan bahwa nilai IC50 dari fraksi metanol yang mempunyai aktivitas yang sangat kuat karena memilki nilai IC50 sebesar 39,836. Sangat kuatnya aktivitas antioksidan ini didukung dengan tingginya nilai kandungan total fenol yang terdapat pada fraksi metanol. Kandungan total fenolik saling berhubungan dengan aktivitas antioksidan, semakin tinggi kandungan total fenolik dari suatu sampel, maka nilai IC50 semakin rendah (Hardiana R.,2012). Hal ini dapat dilihat dari nilai koefisien r2 =0.974.
Nilai ini menunjukkan 97,4% kandungan total fenol memberikan kontribusi pada aktivitas antioksidan, sedangkan 2,6% dipengaruhi oleh senyawa lain. Hasil pengujian dengan metode pearson juga menunjukan kandungan total fenol memiliki hubungan yang sangat kuat dengan kekuatan antioksidan dengan nilai r=0,986. Nilai r menunjukan korelasi yang sangat kuat apabila termasuk dalam rentang 0,79-0,99.
Gambar 5. Korelasi kandungan total fenol dengan kekuatan antioksidan fraksi daun P.foetida.
Uji Sitotoksisitas dengan Metode BSLT Uji toksisitas dilakukan dengan metode BSLT (Brime Shirmp Lethality Test) yang diujikan dengan larva udang Artemia Salina Leach.A.salina digunakan sebagai hewan uji karena pertumbuhan sel dari larva A.salina hampir sama dengan pertumbuhan sel kanker.Ekstrak sampel bersifat toksik apabila mempunyai nilai LC50<1000 ppm (Meyer et al.1982).
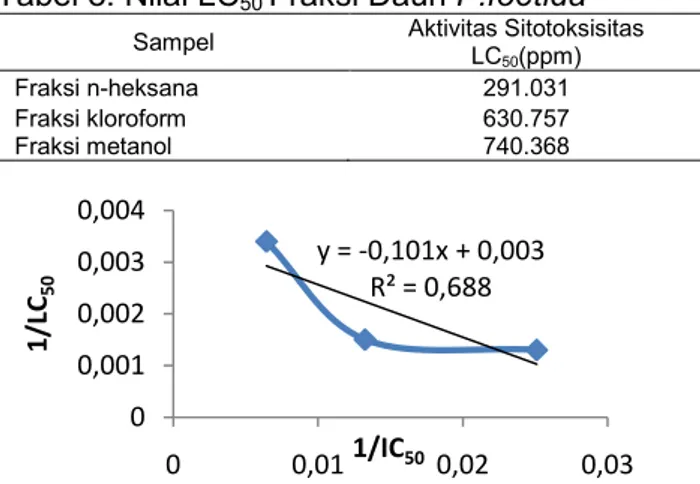
Tabel 8. Nilai LC50 Fraksi Daun P.foetida
Sampel Aktivitas Sitotoksisitas LC
50(ppm)
Fraksi n-heksana 291.031
Fraksi kloroform 630.757
Fraksi metanol 740.368
Gambar 6. Korelasi kekuatan antioksidan dan kekuatan sitotoksisitas fraksi daun P.foetida
Hasil yang ditunjukkan pada tabel 8 menunjukkan bahwa semua fraksi dari daun P.foeidatoksik.Sedangkan nilai LC50 dari fraksi n-heksana yang memiliki potensi toksisitas paling aktf terhadap udang A.salina sebesar 291,031 ppm.Hasil uji KLT yang telah dilakukan pada fraksi n-heksana saat di uji dengan vanilin
y = 0,001x - 0,013 R² = 0,974 0 0,01 0,02 0,03 0 10 20 30 40 1/IC 50
Kandungan Total Fenol µgTAE/mg
y = -0,101x + 0,003 R² = 0,688 0 0,001 0,002 0,003 0,004 0 0,01 0,02 0,03 1/LC 50 1/IC50
6 1% juga menunjukkan noda ungu yang kuat dibandingkan dengan fraksi metanol dan fraksi kloroform.Hal ini menunjukkan kalau senyawa yang banyak terkandung didalam fraksi n-heksana adalah senyawa golongan terpenoid sehingga berkontribusi dalam aktivitas sitotoksiknya.
Berdasarkan Gambar 7 dikorelasikan antara kekuatan antioksidan dengan kekuatan sitotoksisitas. Hasil yang di dapat menunjukkan hasil negatif yaitu r= -0,829. Hal ini menunjukkan bahwa semakin kuat aktivitas sitotoksik nya maka nilai aktivitas antioksidan nya semakin kecil.
SIMPULAN
Berdasarkan penelitian yang telah dilakukan pada fraksi daun P.foetida dapat disimpulkan bahwa skrining fitokimia dan kromatografi lapis tipis (KLT) menunjukkan semua fraksi mengandung senyawa alkaloid, flavonoid, polifenol, dan terpenoid. Fraksi metanol pada penelitian ini telah diketahui memiliki kandungan total fenol dan IC50 paling baik yaitu sebesar 37,960 µgTAE/mg dan 39,836 ppm. Sedangkan pada fraksi n-heksana memiliki nilai LC50 paling baik yaitu sebasar 291,031 ppm. Hasil penelitian ini juga menunjukkan bahwa pada fraksi daun P.foetida bersifat antiokidan dan sitotoksik
DAFTAR PUSTAKA
Ariyanto R., 2006, Uji Aktivitas Antioksidan, Penentuan Kandungan Total Fenolik dan Flavonoid Total Fraksi Kloroform dan Fraksi Air Ekstrak Metanolik Pegagan (Cantella asiatica L. Urban), Skripsi, Fakultas Farmasi Universitas Gajah Mada
Govind P., 2011, Some Important Anticancer Herbs, International Research of Pharmacy ; 02 (7) 45-52.
Harborne J.B., 1987, Metode Fitokimia, Penuntun Cara Modern Menganalisis Tumbuhan, Penterjemah: K. Padmawinata dan I. Soediro, terbitan ke-2, Penerbit ITB, Bandung.
Hardiana R., Rudiansyah., Zaharah T A., 2012, Aktivitas Antioksidan Senyawa Golongan Fenol dari Beberapa Jenis Tumbuhan Famili Malvaceae, JKK,1 (1) : 8-13 Hariana A., 2007, Tumbuhan Obat dan
Khasiatnya, Penebar Swadaya, Jakarta : 76-79.
Irianti T., Puspitasari A., Suryani E., 2011, Aktivitas Penangkapan Radikal 2,2-Difenil-1-Pikrilhidrazil Oleh Ekstrak Etanolik Batang Brotowali (Tinospora
crispaL. Miers) dan Fraksi-Fraksinya, Majalah Obat Tradisional, 16(3), 138 – 144
Khanahmadi M., Rezazaedah S.H. dan Taran M., 2010, In Vitro Antimicrobial and Antioxidant Properties of Smyrnium cordifolium Boiss. (Umbelliferae) Extract, Asian Journal of Plant Sciences, 9(2) : 99-103.
Makkar, H.P.S.,Bluemmel, M., Borowy, N.K., and Becker, K., 1993, Gravimetric Determination Of Tannin An Their Correlations With Chemicalman Protein Precipitation Methods, J, Sci. Food Agric, 61 : 161-165.
Meyer B.N., Ferrigni N.R., Putnam J.E., Jacobsen L.B., Nichols D.E, and McLaughlin J.L., 1982, Brine Shrimp: A Convenient General Bioasay for Active Plant Constituents, Planta Medica, 45 : 31–34.
McLaughlin J.L and Roger L.L., 1998, The Use Of Medical Assays To Evaluate Botanicals, Drug Information Journal, 32 : 513-524
Molyneux P., 2004, The Use Of The Stable Free Radical Dyhenylpicrylhydrazil (DPPH) For Estimating Antioxidant Activity, Journals Science and Technology, 26 : 211-219.
Morshed H., Islam M.S., Parvin S., Ahmed M.U., Islam M.S., Mustofa A.G.M., Sayeed M.S., 2012, Antimicrobial and Cytotoxic Activity of the Methanol Extract of Paederia foetida Linn. (Rubiaceae), Journal of Applied Pharmaceutical Science, 02 (01) : 77-80
Osman H., Rahim A.A., Isa N.M., Bakhir N.M., 2009, Antioxidant Activity and Phenolic Content of Paederia foetida and Syzygium aqueum. Molecules, 14: 970-978.
Sukamdi D.P., Stefani, Palupi K.D., Susidarti R.A., Meiyanto E., 2008, Potensi Antiproliferasi Ekstrak Etanolik Hedyotis Corymbosa (L.) Lamk. Terhadap Sel Hepar Tikus Terinduksi 7,12 Dimetil Benz(A)Antrazena, Prosiding Kongres Ilmiah XVI ISFI.
Thirupathi M., Srinivas D., Rajendar K., Raju D., and Reddy K.J., 2013, Phytochemical Screening of Paederia Foetida a Rare Medicinal Plant, J. Atoms and Molecules, 3(1) : 17–22.