ISOLASI DAN UJI TOKSISITAS SENYAWA METABOLIT SEKUNDER DARI FRAKSI 4 DAN 5 VLC EKSTRAK
n-HEKSANA DAUN RUKAM (Flacourtia rukam)
Ratna Iza Manullang1*, Hilwan Yuda Teruna2 1Mahasiswa Program S1 Kimia
2Dosen Bidang Kimia Organik Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Riau Kampus Binawidya, Pekanbaru, 28293,
Indonesia
ABSTRACT
Flacourtia rukam is one of the species of Flacourtiaceae which is widely spread in Indonesia. This plant commonly used as traditional medicine by various tribes in Indonesia. The study is to isolate secondary metabolite compound from combine fraction with Vacuum Liquid Chromatography (VLC) method and Flash Chromatography method from sub fraction F3. The purity of the compound was analyzed by TLC and melting point. The melting point was obtained at 120-122oC. The isolated compound from extract n-hexane rukam leaf was characterized by FT-IR spectroscopy, which showed the presence of the OH group, CH2 (methylene), CH3 (mehyl), aliphatic C-H and C-O (alcohol). FR-H-02 revealed as a steroid β-Sitosterol after the spectroscopy data were compared with published data. Combine fraction was toxic, based on the toxicity test showed the LC50 values of 776,24 ppm. Toxicity test of β-Sitosterol showed that LC50 value >1,000 ppm which indicated the compound was not toxic against Artemia salina .
Keywords: isolation, rukam, spectroscopy
ABSTRAK
Flacourtia rukam merupakan salah satu famili Flacourtiaceae yang banyak tersebar di Indonesia. Tumbuhan ini banyak dimanfaatkan sebagai obat tradisional oleh berbagai
suku di Indonesia. Penelitian ini bertujuan mengisolasi senyawa metabolit sekunder dari gabungan fraksi menggunakan metode pemisahan Vacuum Liquid Chromatography (VLC) dan metode Flash Chromatography dari subfraksi F3. Analisis kemurnian senyawa ditentukan dengan uji KLT dan uji titik leleh. Titik leleh senyawa yang diperoleh pada rentang 120-122oC. Senyawa dari ekstrak n-heksana daun rukam yang berhasil diisolasi dikarekterisasi dengan FT-IR yang menunjukkan adanya gugus OH, CH2
(metilen), CH3 (metil), C-H alifatik dan C-O (alkohol). Senyawa FR-H-02 diduga merupakan senyawa golongsn steroid yaitu β-sitosterol setelah data spektroskopi dibandingkan dengan data literature ilmiah. Fraksi gabungan 4a, 4b, 5a bersifat toksik dengan nilai LC50 776,24 ppm. Uji toksisitas terhadap senyawa murni β-sitosterol diperoleh LC50
>1.000 ppm yang menandakan senyawa tersebut tidak toksik terhadap larva udang Artemia salina.
Kata kunci: isolasi, rukam, spectroscopi
PENDAHULUAN
Indonesia merupakan negara tropis yang memiliki kekayaan biodiversity terbesar kedua didunia. (Abdullah &
Mustikaningtyas, 2010). Indonesia memiliki sekitar 30.000 spesies tumbuhan dan 1.845 spesies telah diidentifikasi memiliki khasiat sebagai obat. tumbuhan tersebut sudah banyak dimanfaatkan sebagai obat tradisional oleh berbagai suku di Indonesia dan diolah dengan keunikan ramuan atau penyajiannnya.
Salah satu tumbuhan yang dapat dimanfaatkan adalah tumbuhan rukam (Flacourita rukam). Tumbuhan ini merupakan salah satu spesies dari famili Flacourtiaceae yang banyak tersebar di Indonesia. Rukam juga dikenal dengan
nama rukem (Jawa), landak (Madura), rukem, tonggolen, rukam (Sumatera).
Rukam memiliki keunikan yaitu pohonnya beduri dengan tinggi tumbuhan 7 m, diameter batang 17 cm dan dapat tumbuh di hampir semua jenis tanah dengan ketinggian 2 sampai 200 m diatas permukaan air laut (Lim, 2013).
Rukam sudah banyak dikenal dan banyak dimanfaatkan, buah rukam banyak digunakan untuk membuat selai pada pie atau roti, batangnya digunakan sebagai bahan untuk membuat rumah. Daun rukam juga telah lama dimanfaatkan sebagai obat mata, daun muda dari tumbuhan ini digunakan sebagai obat diare. Akar rukam digunakan sebagai ramuan atau jamu untuk wanita setelah melahirkan
(Ragasa et al., 2016)
Ikram et al., (2009) menyatakan buah rukam memiliki kandungan fenolik yang lebih tinggi dibandingkan buah jambu biji (Psidium guajava). Ekstrak pati dari daun rukam memiliki aktivitas antibakteri (Putri et al., 2019).
Penelitian sebelumnya telah melaporkan beberapa bioaktivitas family flacourtiaceae dari berbagai spesies, diantaranya Singh et al. (2017) melaporkan senyawa yang terkandung dalam F. indica menunjukkan aktivitas antimalaria terhadap Plasmodium berghei. F. inermis menunjukkan adanya aktivitas antioksidan DPPH yang tinggi pada ekstrak buah tumbuhan tersebut (Sitti, 2018). Ekstrak daun F. montana dilaporkan oleh Joshy et al., 2016 menunujukkan aktivitas hepaprotektif, antiinflamasi dan antioksidan.
Analisis toksisitas merupakan analisis awal untuk menentukan efektivitas komponen obat. Metode yang sering digunakan pada analisis toksisitas yaitu brine shrimp lethality test (BSLT).
Uji menggambarkan tingkat ketoksikan ekstrak terhadap larva Artemia salina.
Hasil uji ini dapat dimanfaatkan untuk mengidentifikasi bioaktivitas tumbuhan yang lebih luas (Zuraida, 2018).
Dari uraian diatas, maka perlu
dilakukan penelitian lanjutan untuk mengisolasi dan mengidentifikasi senyawa metabolit sekunder yang ada pada daun tumbuhan rukam. Penelitian ini merupakan penelitian lanjutan dari Munharie (2018) yang telah mengisolasi senyawa metabolit sekunder dari ekstrak n-heksana daun rukam (F. rukam) yang diambil dari suku talang mamak di desa Kelayang kecamatan Kelayang, Kabupaten Indragiri Hulu, Provinsi Riau.
Pada penelitian ini senyawa metabolit sekunder yang diperoleh dikarekterisasi menggunakan Spektroskopi FT-IR.
METODOLOGI PENELITIAN a. Alat dan Bahan
Alat yang digunakan dalam penelitian ini adalah neraca analitik, seperangkat alat ultrasonik, seperangkat alat destilasi, satu unit rotary evaporator (Buchi R-114), satu set alat kromatografi cair vakum, satu set kromatografi flash alat penentu titik leleh Fisher John (SMP 11-Stuart), lampu UV (Cole Permer 254 dan 366 nm), spektroskopi FT-IR (Shimadzu, IR Prestige-21) serta peralatan gelas yang umum digunakan sesuai cara kerja.
Bahan-bahan yang digunakan dalam penelitian ini adalah fraksi F4a, F4b, F5a, n-heksana, diklorometana, etil asetat, dimetil sulfoksida, metanol, reagen penampak noda anisaldehid, aluminium
foil,air laut, larva udang, silika gel 60 GF254 (230-400 mesh), dan plat KLTsilikagel GF254.
b. Isolasi Metabolit Sekunder
Gabungan fraksi F4a, f4B, dan F5a hasil fraksinasi yang dilakukan (Munharie, 2018) dipisahkan dengan metode vacum liquid chromatography (VLC) yang diisi dengan silika gel GF254
sebanyak 80 gram sehingga tinggi silika gel dalam kolom mencapai ketinggian 8 cm dengan diameter kolom 5 cm. Silika gel dimasukkan dan dipadatkan dalam keadan vakum, sebanyak 2,30 gram sampel diambil dan di preadsorpsi menggunakan silika gel hingga homogen kemudian dimasukkan ke bagian atas kolom yang sudah berisi silika padat.
Kolom yang sudah berisi silika dan sampel selanjutnya dielusi dengan perbandingan pelarut dan volume yang sesuai dimulai dari n-heksana 100%, n- heksana:etil asetat (8:2; 6:4; 4:6; 2:8), hingga etil asetat 100%, Perbandingan volume eluen yang dipakai adalah 150 mL/eluen. Hasil elusi ditampung dalam erlenmeyer dan kemudian dipekatkan menggunakan rotary evaporator dan ditampung ke dalam vial yang beratnya sudah diketahui sebelumnya dengan tujuan memudahkan dalam mengetahui berat.
Subfraksi yang diperoleh di uji KLT dengan pelarut yang sesuai untuk mengetahui hasil pemisahan dari gabungan fraksi. Berdasarkan profil KLT subfraksi yang memiliki noda yang sama digabungkan dan dilakukakan pemisahan dengan metode flash chromatography.
Silika dicampurkan dengan pelarut n- heksana dan diaduk rata agar terbentuk bubur, yang kemudian dimasukkan kedalam kolom secara perlahan menggunakan corong kemudian dielusi dengan n-heksana sampai kerapatan silika dalam kolom maksimum. Proses elusi dibantu dengan tekanan dari gas nitrogen.
Sampel yang akan dipisahkan dipreadsorpsi dengan mencampurkan silika dengan sampel kering dan digerus sampai homogen, kemudian dimasukkan kedalam kolom. Kolom yang berisi silika dan sampel kemudian dielusi secara bergradien dengan perbandingan eluen tertentu. Hasil pemisahahan ini ditampung di dalam vial yang telah diberi nomor.
Hasil pemisahan flash
chromatography diuji dengan KLT dengan cara menotolkan sampel pada pelat KLT. Pelat yang ditotol dielusi dengan pelarut yang sesuai dan pelat diangkat setelah eluen mencapai garis batas atas lalu dikering anginkan dan dilihat dibawah lampu UV. Jika noda yang diperoleh
memiliki nilai retardation factor (Rf) yang sama maka dilakukakan penggabungan vial. Hasil penggabungan vial yang membentuk padatan/ kristal, dilanjutkan dengan metode rekritalisasi untuk memisahkan senyawa dengan pengotornya, sehingga diperoleh senyawa murni. Senyawa murni dapat dianalisis menggunakan uji KLT dengan menunjukkan satu noda pada profil KLT, dan dilakukkan pengujian titik leleh menggunakan alat penentu tiik leleh Fisher-Johns yang ditentukan melalui selisih suhu ketika kristal mulai meleleh sampai habis meleleh sempurna ≤ 2oC.
c. Karakterisasi Senyawa
Senyawa murni yang diperoleh dikarekterisasi menggunakn analisis spektroskopi FT-IR yang dilakukan di Jurusan Kimia Universitas Riau.
d. Uji Toksisitas
Fraksi gabungan dan senyawa murni yang diperoleh diuji toksisitas menggunakan metode BSLT (brine shrimp lethality test).
HASIL DAN PEMBAHASAN
a. Isolasi Senyawa Metabolit Sekunder
Berat hasil pengabungan fraksi F4a, F4b dan F5a adalah sebanyak 2,3 gram.
Senyawa metabolit sekunder pada fraksi tersebut diisolasi menggunakan metode
Vacuum Liquid Chromatography (VLC).
Pemisahan dilakukan menggunakan kolom berdiameter 5 cm dengan tinggi 20 cm yang diisi dengan silika gel GF254
sebanyak 80 gram sampai ketinggian mencapai 8 cm. Pemisahan dilakukan dengan gradient elusi dengan eluen
dimulai dari n-heksana 100%, n-heksana:etil asetat (8:2; 6:4; 4:6; 2:8),
hingga etil asetat 100% %. Perbandingan volume eluen yang dipakai adalah 150 mL/eluen. Hasil elusi ditampung dalam Erlenmeyer dan diperoleh 5 subfraksi yang kemudian dipekatkan menggunakan rotary evaporator dan ditampung dalam vial yang telah ditimbang. Berat sub fraksi yang diperoleh F2, F3, F4, F5 dan F6 adalah 0,04 gram, 0,4 gram,0,38 gram, 0,24 gram dan 0,06 gram. Subfraksi yang diperoleh di uji KLT, berdasarkan profil KLT dilakukakan pemisahan pada subfraksi F3 dipisahakan menggunakan metode flash chromatography. Kolom yang digunakan berdiameter 2 cm yang diisi dengan silika gel G60 (230-400 mesh) sampai ketinggian 25 cm. Pemisahan dilakukan menggunakan gradient elusi yang dimulai dari n-heksana: etil asetat (9:1; 8,5:1,5; 8:2; 7,5:2,5; 7:3; 6,5:3,5; 6:4;
5,5:4,5; 5:5) dan etil asetat 100%. Hasil pemisahan ditampung menggunakan vial sebanyak 68 vial. Pada vial 11-13 diamati
terbentuknya endapan putih kemudian dilakukan uji KLT, hasil KLT menunjukkan ketiga vial memiliki noda yang mirip sehingga dapat digabungkan.
Rekristalisasi gabungan vial 11,12,13 dilakukakan untuk memisahkan senyawa dari pengotornya. Hasil rekristalisasi diperoleh kristal jarum jarum berwarna putih, kemudian dilakukan uji KLT dengan menggunakan penampak noda anisaldehid dan diperoleh satu noda yang menandakan senyawa sudah murni, dengan berat senyawa yang diperoleh 13 mg dan didapatkan titik leleh senyawa pada 120-122oC. Senyawa murni yang berhasil diisolasi diberi kode nama FR-H- 02.
Senyawa murni FR-H-02 diduga
senyawa golongan steroid yaitu β-sitosterol dilihat dari bentuk fisik kristal
bewarna putih jarum jarum dan uji KLT menggunakan penampak noda anisaldehid yang merupakan reagen khusus untuk senyawa golongan steroid dan terpenoid. Kemudian data spektroskopi FT-IR dibandingkan dengan data dalam literatur ilmiah. Titik leleh senyawa β-sitosterol menurut literatur adalah 137oC sedangkan titik leleh senyawa yang diperoleh adalah 120- 122oC namun hasil uji KLT menunjukkan senyawa FR-H-02 dengan β-sitosterol
memiliki retardation factor (Rf) yang sama yang mana kode A merupakan senyawa FR-H-02 dan B adalah β-sitosterol Gambar 1.
Gambar 1. Kromatogram perbandingan FR-H-02 dan β-sitosterol
b. Karakterisasi Senyawa dengan Spektroskopi FT-IR
Senyawa murni FR-H-02
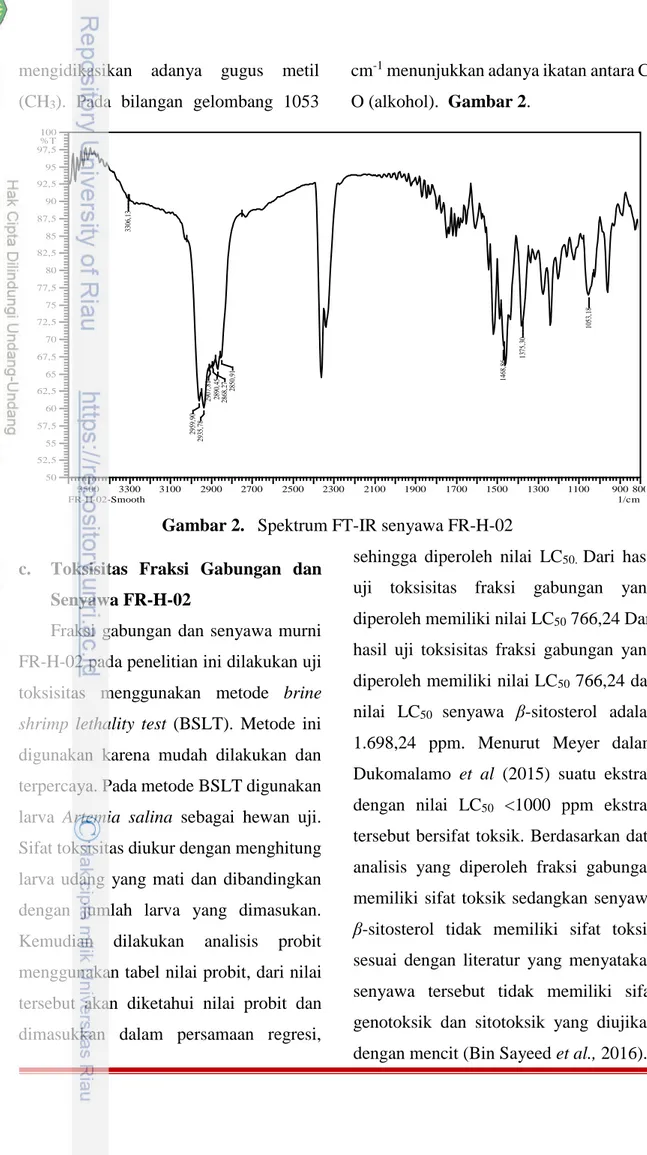
dikarakterisasi menggunakan alat spektroskopi FT-IR. Analisis dilakukan untuk menunjukkan gugus fungsi yang terdapat pada senyawa tersebut. Spektrum IR senyawa FR-H-02 menunjukkan adanya serapan melebar pada bilangan gelombang 3.306 cm-1 yang menunjukkan adanya vibrasi gugus O-H, kemudian pada bilangan gelombang 2850-2959 cm-1 dengan intensitas serapan yang kuat menunjukkan adanya ikatan C-H alifatik alkana, pada bilangan gelombang 1468 cm-1 menunjukkan adanya gugus metilen CH2 dan pada bilangan 1375 cm-1
mengidikasikan adanya gugus metil (CH3). Pada bilangan gelombang 1053
cm-1 menunjukkan adanya ikatan antara C- O (alkohol). Gambar 2.
Gambar 2. Spektrum FT-IR senyawa FR-H-02 c. Toksisitas Fraksi Gabungan dan
Senyawa FR-H-02
Fraksi gabungan dan senyawa murni FR-H-02 pada penelitian ini dilakukan uji toksisitas menggunakan metode brine shrimp lethality test (BSLT). Metode ini digunakan karena mudah dilakukan dan terpercaya. Pada metode BSLT digunakan larva Artemia salina sebagai hewan uji.
Sifat toksisitas diukur dengan menghitung larva udang yang mati dan dibandingkan dengan jumlah larva yang dimasukan.
Kemudian dilakukan analisis probit menggunakan tabel nilai probit, dari nilai tersebut akan diketahui nilai probit dan dimasukkan dalam persamaan regresi,
sehingga diperoleh nilai LC50. Dari hasil uji toksisitas fraksi gabungan yang diperoleh memiliki nilai LC50 766,24 Dari hasil uji toksisitas fraksi gabungan yang diperoleh memiliki nilai LC50 766,24 dan nilai LC50 senyawa β-sitosterol adalah 1.698,24 ppm. Menurut Meyer dalam Dukomalamo et al (2015) suatu ekstrak dengan nilai LC50 <1000 ppm ekstrak tersebut bersifat toksik. Berdasarkan data analisis yang diperoleh fraksi gabungan memiliki sifat toksik sedangkan senyawa β-sitosterol tidak memiliki sifat toksik sesuai dengan literatur yang menyatakan senyawa tersebut tidak memiliki sifat genotoksik dan sitotoksik yang diujikan dengan mencit (Bin Sayeed et al., 2016).
800 900 1100 1300 1500 1700 1900 2100 2300 2500 2700 2900 3100 3300 3500
1/cm 50
52,5 55 57,5 60 62,5 65 67,5 70 72,5 75 77,5 80 82,5 85 87,5 90 92,5 95 97,5 100
%T
3306,13 2959,90 2935,78 2907,81 2890,45 2868,27 2850,91 1468,86 1375,30 1053,18
FR-H-02-Smooth
KESIMPULAN
Isolasi senyawa metabolit sekunder dari ekstrak n-heksana daun rukam diperoleh senyawa dengan kode nama FR-H-02.
Senyawa FR-H-02 dikarekterisasi dengan spektroskopi FT-IR yang menunjukkan adanya gugus OH, CH2 (metilen), CH3
(metil), C-H alifatik dan C-O (alcohol).
Senyawa FR-H-02 yang diperoleh diduga
senyawa golongan steroid yaitu β-sitosterol. Toksisitas fraksi gabungan
diperoleh nilai LC50 776,24 dan nilai LC50
senyawa FR-H-02 adalah 1.698,24 ppm.
DAFTAR PUSTAKA
Abdullah, M., & Mustikaningtyas, D.
2010. Inventarisasi jenis-jenis tumbuhan berkhasiat obat di hutan hujan dataran rendah desa Nyamplung Pulau Karimunjawa.
Biosaintifika: Journal of Biology &
Biology Education, 2(2), 75–81.
Bin Sayeed, M., Karim, S., Sharmin, T., Morshed, M. 2016. Critical Analysis on Characterization, Systemic Effect, and Therapeutic Potential of Beta- Sitosterol: A Plant-Derived Orphan Phytosterol. Medicines, 3(4), 29.
Dukomalamo, I., Sangi, M. S., & Rorong, J. A. 2015. Analisis Senyawa Toksik Tepung Pelepah Batang Aren (Arenga pinnata) dengan Spektroskopi UV-Vis dan Inframerah. Jurnal MIPA, 4(2), 54.
Ikram, E. H. K., Eng, K. H., Jalil, A. M.
M., Ismail, A., Idris, S., Azlan, A., &
Mokhtar, R. A. M. 2009. Antioxidant capacity and total phenolic content of Malaysian underutilized fruits.
Journal of Food Composition and Analysis, 22(5), 388–393.
Joshy, C., Thahimon, P. A., Arun Kumar, R., Carla, B., & Sunil, C. (2016).
Hepatoprotective, anti-inflammatory and antioxidant activities of Flacourtia montana J. Grah leaf extract in male Wistar rats. Bulletin of Faculty of Pharmacy, Cairo University, 54(2), 209–217.
Lim, T. K. 2013. Edible Medicinal and Non-Medicinal Plants: Volume 5, Fruits. Springer (Vol. 5).
Munharie. 2018. Isolasi san uji toksisitas senyawa metabolit sekunder dari ekstrak n-heksana daun rukam (Flacourtia rukam). Skripsi, Universitas Riau.
Putri, D. V., Lestari, F., & Widiya, M.
2019. Uji daya antibakteri sari pati daun rukam (Flacourtia rukam) terhadap zona hamabat Escherichia coli. Jurnal Biosilampari : Jurnal Biologi, 2(1), 23–28.
Ragasa, C. Y., Reyes, J. M. A., Tabin, T.
J., Tan, M. C. S., Chiong, I. D., Brkljača, R., & Urban, S. (2016).
Chemical constituents of Flacourtia rukam Zoli. & Moritzi fruit.
International Journal of Pharmaceutical and Clinical Research, 8(12), 1625–1628.
Singh, S. V., Manhas, A., Singh, S. P., Mishra, S., Tiwari, N., Kumar, P., &
, A. (2017). A phenolic glycoside from Flacourtia indica induces heme mediated oxidative stress in Plasmodium falciparum and
attenuates malaria pathogenesis in mice. Phytomedicine, 30, 1–9.
Sitti, B. 2018. Fitokimia dan antioksidan pada buah Tome-Tome (Flacoutia Inermis). hospital majapahit, 10(1), 43–50.
Zuraida, Z. 2018. Analisis toksisitas beberapa tumbuhan hutan dengan metode brine shrimplLethality Test (Bslt). Jurnal Penelitian Hasil Hutan, 36(3), 239–246.