KAJIAN AKTIVITAS ANTIBAKTERI SENYAWA TRIFENILTIMAH(IV) 4-HIDROKSIBENZOAT DAN TRIFENILTIMAH(IV) 4-
KLOROBENZOAT TERHADAP BAKTERI GRAM POSITIF Bacillus sp.
(Skripsi)
Oleh ADI SETIAWAN
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
BANDAR LAMPUNG 2016
ABSTRAK
KAJIAN AKTIVITAS ANTIBAKTERI SENYAWA TRIFENILTIMAH(IV) 4-HIDROKSIBENZOAT DAN TRIFENILTIMAH(IV) 4-
KLOROBENZOAT TEHADAP BAKTERI GRAM POSITIF Bacillus sp.
Oleh Adi Setiawan
Dalam penelitian ini telah dilakukan sintesis senyawa trifeniltimah(IV) 4- hidroksibenzoat dan trifeniltimah(IV) 4-klorobenzat dari senyawa trifeniltimah(IV) hidroksida dengan ligan asam 4-hidroksibenzoat dan asam 4- klorobenzoat, kemudian didapatkan serbuk putih dengan berat masing-masing 1,3105 gram (89,57%) dan 1,333 gram (87,90%). Hasil karakterisasi dengan spektrofotometer IR tedapat serapan C=O dari kedua senyawa hasil sintesis pada daerah 1617,18 cm-1 dan daerah 1640,11 cm-1 yang menunjukkan telah terbentuknya senyawa hasil sintesis. Hasil karakterisasi dengan spektrofotometer UV-Vis didapatkan transisi elektron π→π* dan n→π* berturut-turut yaitu pada λmaks 232,00 nm dan 305,00 nm, serta 237,00 nm dan 282,00 nm. Karakterisasi dengan mikroelemental analyzer menunjukkan bahwa senyawa hasil telah murni.
Pengujian aktivitas antibakteri pada metode difusi didapatkan senyawa trifeniltimah(IV) 4-klorobenzoat memiliki aktivitas antibakteri terbaik dengan konsentrasi 300 ppm dan pada uji dilusi menunjukkan senyawa trifeniltimah(IV) 4-klorobenzoat memiliki aktivitas antibakteri terbaik dengan kadar 0,75 mg dalam 15 mL media agar.
Kata kunci : antibakteri, Bacillus sp., trifeniltimah(IV) 4-hidroksibenzoat, trifeniltimah(IV) 4-klorobenzoat.
ABSTRACT
STUDY OF ANTIBACTERIAL ACTIVITY COMPOUNDS TRIPHENYLTIN(IV) 4-HYDROXYBENZOATE AND
TRIPHENYLTIN(IV) 4-CHLOROBENZOATE ON BACTERIA GRAM POSITIVE Bacillus sp.
By Adi Setiawan
In this research the syntheses of triphenyltin(IV) 4-hydroxybenzoate and triphenyltin(IV) 4-chlorobenzoate compounds have been conducted by reacting triphenyltin(IV) hydroxide with ligands of 4-hydroxybenzoic acid and 4- chlorobenzoic acid, the products obtaineds were white powder with the weight of 1.3105 gram (89.57%) and 1.333 gram (87.90%), respectively. The characterization with IR spectrometry showed functional group of C=O of the synthesized compounds in the area of 1617.18 cm-1and 1640.11 cm-1showing the formation of compounds synthesized. The characterization with UV-Vis spectrometry showed electron transition of π→π* and n→π* with λmax232.00 nm and 305.00 nm for triphenyltin(IV) 4-hydroxybenzoate, and 237.00 nm and 282.00 nm for triphenyltin(IV) 4-chlorobenzoate. The results of microelemental analyzer showed that the compounds synthesized have high purity with the difference with the theory was less than 2%. The result of antibacterial activity test with diffusion method for triphenyltin(IV) 4-chlorobenzoic have the best antibacterial activity at concentration of 300 ppm, while the dilution test showed that the triphenyltin(IV) 4-chlorobenzoic have the best of antibacterial activity at 0.75 mg in 15 mL media.
Keywords: antibacterial, Bacillus sp., triphenyltin(IV) 4-hydroxybenzoate, and triphenyltin(IV) 4-chlorobenzoate.
KAJIAN AKTIVITAS ANTIBAKTERI SENYAWA TRIFENILTIMAH(IV) 4-HIDROKSIBENZOAT DAN TRIFENILTIMAH(IV) 4-
KLOROBENZOAT TERHADAP BAKTERI GRAM POSITIF Bacillus sp.
Oleh
Adi Setiawan
Skripsi
Sebagai Salah Satu Syarat Untuk Memperoleh Gelar SARJANA SAINS
Pada
Jurusan Kimia
Fakultas Matematika dan Ilmu Pengetahuna Alam
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
BANDAR LAMPUNG 2016
RIWAYAT HIDUP
Penulis dilahirkan di Desa Keputran, Kecamatan Sukoharjo, Kabupaten Pringsewu, pada tanggal 11 Februari 1994. Penulis merupakan anak ke enam dari enam bersaudara dari pasangan Bapak Bakhrun dan Ibu Sumartini. Pada Tahun 2006, penulis menyelesaikan pendidikan sekolah di SD N 2 Keputran. Penulis melanjutkan
pendidikan tingkat menengah di SMP N 1 Sukoharjo hingga tahun 2009. Kemudian, menyelesaikan pendidikan SMA (Sekolah Menengah Atas) di SMA N 1 Sukoharjo pada tahun 2012. Pada tahun yang sama, penulis menjadi mahasiswa di S1 Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung.
Selama menempuh pendidikan di kampus, penulis pernah menjadi asisten mata kuliah Sains Dasar Jurusan Fisika dan Biologi pada tahun 2015, asisten mata kuliah Kimia Dalam Kehidupan, dan Praktikum Kimia Anorganik 1 pada tahun 2016.
Aktivitas organisasi penulis di mulai sejak terdaftar sebagai Kader Muda Himaki (KAMI) pada tahun 2012.
Penulis juga pernah menjadi Sekretaris Umum UKMF Rois FMIPA Unila pada tahun 2014/2015, Ketua DPM FMIPA Unila pada tahun 2015/2016, dan menjadi Wakil Ketua I MPM KBM Unila pada tahun 2016.
Selain itu, prestasi yang pernah diraih oleh penulis diantaranya pernah menerima Pendanaan PKM-P (Program Kreatifitas Mahasiswa Bidang Penelitian) pada tahun 2015 dan Juara I Provinsi OSP (Olimpiade Sains Pertamina) Bidang Kimia pada tahun 2015.
Atas limpahan rahmat dan nikmat dari Allah SWT, kupersembahkan karya sederhana ini teruntuk...
Kedua orang tuaku, Bapak Bakhrun dan Ibu Sumartini, atas semua do’a, cinta, dan kasih sayang.
Segenap keluarga besar yang selalu mendo’akan keberhasilanku.
Prof. Sutopo Hadi, S.Si., M.Sc., Ph.D., dan Bapak Ibu Dosen Jurusan Kimia FMIPA Unila, atas semua ilmu
yang telah diberikan.
Seluruh sahabat yang senantiasa memberikan semangat, dukungan, dan bantuan untukku.
Serta almamater tercinta, Universitas Lampung...
MOTTO
“Hai orang-orang yang beriman, bertakwalah kepada Allah dan hendaklah setiap diri memperhatikan apa yang telah
diperbuatnya untuk hari esok (akhirat); dan bertakwalah kepada Allah, sesungguhnya Allah Maha Mengetahui apa yang
kamu kerjakan”.
(QS. Al Hasyr: 18).
“Sesungguhnya orang-orang yang beriman itu hanyalah orang- orang yang percaya (beriman) kepada Allah dan Rasul-Nya,
kemudian mereka tidak ragu-ragu dan mereka berjuang (berjihad) dengan harta dan jiwa mereka pada jalan Allah.
Mereka itulah orang-orang yang benar”.
(QS. Al Hujurat: 15).
“Hai orang-orang yang beriman, sukakah kamu aku tunjukkan suatu perniagaan yang dapat menyelamatkanmu dari azab yang pedih?”.“(yaitu) kamu beriman kepada Allah dan Rasul-
Nya dan berjihad di jalan Allah dengan harta dan jiwamu.
Itulah yang lebih baik bagimu, jika kamu mengetahui”.”Niscaya Allah akan mengampuni dosa-dosamu dan memasukkanmu ke dalam jannah yang mengalir di bawahnya sungai-sungai; dan
(memasukkan kamu) ke tempat tinggal yang baik di dalam surga 'Adn. Itulah keberuntungan yang besar”.
(QS. Ash Shaff: 10-12).
“Hai orang-orang beriman, janganlah hartamu dan anak- anakmu melalaikan kamu dari mengingat Allah. Barangsiapa yang berbuat demikian maka mereka itulah orang-orang yang
merugi”.” Dan belanjakanlah sebagian dari apa yang telah Kami berikan kepadamu sebelum datang kematian kepada salah seorang di antara kamu; lalu ia berkata: "Ya Rabb-ku, mengapa Engkau tidak menangguhkan (kematian)ku sampai
waktu yang dekat, yang menyebabkan aku dapat bersedekah dan aku termasuk orang-orang yang saleh?”.”Dan Allah sekali-
kali tidak akan menangguhkan (kematian) seseorang apabila telah datang waktu kematiannya. Dan Allah Maha Mengenal
apa yang kamu kerjakan”
(QS. Al Munafiqun : 9-11).
SANWACANA
Assalamu’alaykum wr.wb.
Puji syukur kehadirat Allah SWT karena berkat limpahan rahmat, nikmat, dan
karunianya penulis dapat menyelesaikan skripsi ini sebagai syarat untuk memperoleh gelar Sarjana Sains (S.Si) pada program studi S1 Jurusan Kimia FMIPA Universitas Lampung dengan judul skripsi “Kajian Aktivitas Antibakteri Senyawa
Trifeniltimah(IV) 4-hidroksibenzoat dan Trifeniltimah(IV) 4-klorobenzoat terhadap Bakteri Gram Positif Bacillus sp.”.
Sholawat serta salam semoga selalu tercurah kepada Rasulullah Muhammad SAW, karena berkat perjuangan beliau dalam menegakkan agama Allah, kita semua dapat merasakan indahnya Islam, semoga kita termasuk umat yang akan mendapatkan syafaatnya kelak, aamiin.
Dalam menyusun skripsi ini, penulis menyadari bahwa skripsi ini selesai karena adanya bantuan dari berbagai pihak. Maka dari itu penulis mengucapkan terima kasih kepada :
1. Allah SWT, atas segala rahmat, nikmat, dan karunianya sehingga skripsi ini dapat terselesaikan.
2. Kedua orang tercinta, Bapak Bakhrun dan Ibu Sumartini yang telah mendidik dan membesarkan penulis. Sungguh, hanya Allah-lah yang mampu membalas semua yang telah mereka berikan kepada penulis, dan semoga Allah senantiasa menjaga mereka sampai ke Jannah-Nya.
3. Bapak Prof. Sutopo Hadi, M.Sc.,Ph.D., selaku pembimbing I yang dengan penuh kesabaran, keikhlasan, dan perhatian telah memberikan ilmu, arahan, semangat, dan motivasi sehingga skripsi ini dapat terselesaikan. Semoga Allah membalas semua kebaikan beliau kepada penulis.
4. Ibu Prof. Dr. Tati Suhartati, M.S., selaku pembimbing II penulis, yang telah memberikan ilmu, arahan, dan semangat sehingga skripsi ini dapat terselesaikan.
Semoga Allah membalas semua kebaikan beliau kepada penulis.
5. Bapak Mulyono, Ph.D., selaku pembahas dalam penelitian penulis yang telah memberikan ilmu, arahan, dan semangat sehingga skripsi ini dapat terselesaikan.
Semoga Allah membalas semua kebaikan beliau kepada penulis
6. Bapak Prof. Dr. Yandri A.S, M.S., selaku dosen pembimbing akademik yang telah memberikan arahan, saran, dan nasihat kepada penulis.
7. Bapak Dr. Rudy T.M. Situmeang, M.Sc., selaku Kepala Laboratorium Kimia Anorganik/Fisik atas izinnya untuk menyelesaikan penelitian.
8. Bapak Dr. Eng. Suripto Dwi Yuwono, M.T., selaku ketua jurusan kimia FMIPA Unila.
9. Bapak Ibu dosen jurusan Kimia FMIPA Universitas Lampung atas seluruh ilmu dan bimbingan yang diberikan selama penulis menjalani perkuliahan. Semoga Allah S.W.T. melimpahkan berkah kepada Bapak dan Ibu semua.
10. Kakek dan nenekku tercinta, atas semua yang telah mereka selama ini, semoga Allah senantiasa mencurahkan rahmat dan karunia-Nya kepada mereka
11. Kakak dan mbakku tercinta, Mas Mansur, Yuk Mar, Mas Andri, Mbak Erni, dan Mas Ifan atas semangat dan motivasinya, sehingga penulis dapat menyelesaikan skripsi ini.
12. Bibi, Paman, dan Keponakan-keponakanku yang luar biasa.
13. Saudari Jean Pitaloka, selaku partner penelitian penulis, yang telah banyak membantu penulis dalam suka dan duka sehingga skripsi ini dapat terselesaikan.
Semoga Allah membalas semua kebaikannya.
14. Rekan-rekan kerja satu penelitian, Sukamto, Murni Fitria, Mbak Nopitasari, Mbak Melli Novita W., dan Mbak Hapin Afriyani yang telah banyak membantu penulis dalam menyelesaikan skripsi ini. Semoga Allah membalas kebaikan mereka.
15. Rekan-rekan kerja penelitian di Laboratorium Kimia Anorganik/fisik (Rifki, Nila, Iin, Indri, Ismi, Nova, Febri, Dela, Kartika, dll) dan Laboratorium Biokimia (Moly, Ma’ul, Mbak Putri, dll) yang tidak dapat penulis sebutkan satu persatu.
16. Keluarga besar Kimia angkatan 2012 (Khoirul Anwar, Zubaidi, Rizal Rio S., M.
Rijal Robbani, Rifki Khusnul K., Tri Marital, Sofian Sumilat R., Febi Rinaldo P.
K, Tian Reno, Dery Vardella, Riandra Pratama U., Radius Uly A., Aditian Sulung P., Agus Ardiansyah), dll yang tidak dapat penulis sebutkan satu persatu, semoga ukhuwah ini akan selalu terjaga sampai nanti, aamiin.
17. Kang Ridho Nahrowi, Kak Ari Susanto, Kak Irkham Bariklana, Kak Ali Akbar H., Kak Ade Pamungkas, Kak Sammi Rizki, dan Alaudin Al Ayubi, atas kebersamaannya selama ini.
18. Bapak Subian Saidi, M.Si., selaku murobbi penulis yang telah banyak
memberikan ilmu, arahan, dan motivasi kepada penulis selama ini. Semoga Allah membalas kebaikan beliau, dan semoga kita dipertemukan di surga-Nya kelak, aamiin.
19. Rekan-rekan holaqoh cinta (Zubaidi, M. Iqbal Yuliansyah, Bang Purnomo Aji, Alaudin Al Ayubi, dll), semoga ukhuwah ini selalu terjaga sampai menuju Jannah-Nya.
20. Rekan-rekan Hafizh Qur’an Unila, terutama Ust. Hasan Basri, Lc., M.A., Al Hafidz, beserta Uje, Surya, Mahfudin, Agum Aldino, Hamidin, dll.
21. Rekan-rekan presidium, pimpinan, dan pengurus Rois FMIPA Periode 2014- 2015.
22. Anggota DPM FMIPA Unila tahun 2015/2016 (Didin, Wulan, Concon, Taskia, Rifki, Agung, Audi, Iqbal, dan Aldino).
23. Presidium MPM U KBM Unila 2016 (Opi Sumardi dan Mbak Lina Nur Hayati), serta presidium DPM dan anggota DPM U KBM Unila 2016.
24. Keluarga besar Kimia 2009-2015.
25. Almamater tercinta, Universitas Lampung.
26. Seluruh pihak yang telah membantu penulis, yang tidak dapat penulis sebutkan satu persatu.
Semoga segala bentuk bantuan dan dukungannya mendapatkan pahala dari Allah SWT. Penulis menyadari bahwa dalam penulisan ini masih terdapat kesalahan, oleh karena itu kritik dan saran sangat diharapkan oleh penulis supaya skripsi ini menjadi lebih baik lagi.
Wassalaamu’alaykum wr.wb.
Bandar Lampung, Juni 2016 Penulis
Adi Setiawan
ii
DAFTAR ISI
Halaman
DAFTAR TABEL ... iii
DAFTAR GAMBAR ... iv
I. PENDAHULUAN A. Latar Belakang ... 1
B. Tujuan Penelitian ... . 4
C. Manfaat Penelitian ... 5
II. TINJAUAN PUSTAKA A. Senyawa Organologam ... 6
B. Senyawa Organotimah ... 6
1. Senyawa organotimah halida ... 8
2. Senyawa organotimah hidroksida dan oksida ... 9
3. Senyawa organotimah karboksilat ... 9
C. Aplikasi Senyawa Organotimah ... 10
D. Bakteri ... 12
E. Bakteri Bacillus sp ... 13
F. Antibakteri... 14
G. Uji Aktivitas Antibakteri ... 16
1. Metode Dilusi ... 16
2. Metode Difusi ... 18
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ... 20
B. Alat dan Bahan ... 20
C. Cara Kerja ... 21
1. Sintesis senyawa trifeniltimah(IV) 4-hidroksibenzoat ... 21
2. Sintesis senyawa trifeniltimah(IV) 4-klorobenzoat ... 22
3. Uji aktivitas antibakteri ... 22
a. Penyiapan media uji ... 22
b. Uji bioaktiviatas dengan metode difusi agar ... 23
c. Uji bioaktivitas dengan metode dilusi agar ... 24
ii
IV. HASIL DAN PEMBAHASAN
A. Sintesis ... 25
1. Sintesis senyawa difeniltimah(IV) 4-hidroksibenzoat ... 25
2. Sintesis Senyawa trifeniltimah(IV) 4-klorobenzoat ... 27
B. Karakterisasi Menggunakan Spektrofotometer IR ... 28
1. Asam 4-hidroksibenzoat ... 28
2. Asam 4-klorobenzoat ... 29
3. Senyawa trifeniltima(IV) hidroksida ... 31
4. Senyawa trifeniltima(IV) 4-hidroksibenzoat ... 32
5. Senyawa trifeniltima(IV) 4-klorobenzoat 33 C. Karakterisasi Menggunakan Spektrofotometer UV-VIS... 35
1. Senyawa trifeniltima(IV) hidroksida, trifeniltima(IV) 4-hidroksibenzoat, trifeniltima(IV) 4-klorobenzoat ... 35
D. Analisis Unsur Menggunakan Microelemental Analyzer ... 37
E. Uji Aktivitas Antibakteri ... 38
1. Uji difusi ... 38
2. Uji dilusi ... 43
V. KESIMPULAN DAN SARAN A. Kesimpulan ... 47
B. Saran ... 48
DAFTAR PUSTAKA LAMPIRAN 1. Perhitungan persentase berat senyawa hasil sintesis ... 54
2. Perhitungan data mikroanalisis ... 56
3. Hasil uji difusi. ... 59
DAFTAR TABEL
Tabel Halaman
1. Bilangan gelombang untuk gugus fungsi yang terdapat pada asam 4-
hidroksibenzoat ... 29 2. Bilangan gelombang untuk gugus fungsi yang terdapat pada asam 4-
klorobenzoat... 30 3. Bilangan gelombang untuk gugus fungsi yang terdapat pada senyawa
trifeniltimah(IV) hidroksida... 31 4. Bilangan gelombang untuk gugus fungsi yang terdapat pada senyawa
trifeniltimah(IV) 4-hidroksibenzoat... 32 5. Bilangan gelombang untuk gugus fungsi yang terdapat pada senyawa
trifeniltimah(IV) 4-klorobenzoat ... 35 6. Data spektrum UV-Vis untuk senyawa trifeniltimah(IV)
4-hidroksibenzoat dan trifeniltimah(IV) 4-klorobenzoat... 37 7. Hasil mikroanalisis unsur... 37 8. Ukuran zona hambat dari senyawa trifeniltimah(IV) hidroksida
terhadap bakteri Bacillus sp... 39 9. Ukuran zona hambat dari senyawa trifeniltimah(IV)
4-hidroksibenzoat terhadap bakteri Bacillus sp... 40 10. Ukuran zona hambat dari senyawa trifeniltimah(IV) 4-klorobenzoat
terhadap bakteri Bacillus sp... 41 11. Data hasil uji aktivitas antibakteri beberapa senyawa turunan
organotimah(IV) karboksilat terhadap bakteri Bacillus sp. ... 43 12. .Hasil uji dilusi senyawa trifeniltimah(IV) 4-klorobenzoat... 46
iii
DAFTAR GAMBAR
Gambar Halaman
1. Gambar sel bakteri Bacillus sp ... 14
2. Senyawa trifeniltimah(IV) 4-hidroksibenzoat ... 26
3. Sintesis senyawa trifeniltimah(IV) 4-hidroksibenzoat... 26
4. Senyawa trifeniltimah(IV) 4-klorobenzoat ... 27
5. Sintesis senyawa trifeniltimah(IV) 4-klorobenzoat ... 28
6. Spektrum asam 4-hidroksibenzoat ... 29
7. Spektrum asam 4-klorobenzoat... 30
8. Spektrum trifeniltimah(IV) hidroksida ... 31
9. Spektrum trifeniltimah(IV) 4-hidroksibenzoat ... 32
10. Spektrum trifeniltimah(IV) 4-klorobenzoat ... 34
11. Spektrum UV senyawa trifeniltimah(IV) hidroksida, trifeniltimah(IV) 4-hidroksibenzoat, dan trifeniltimah(IV) 4-klorobenzoat ... 35
12. Uji dilusi senyawa trifeniltimah(IV) 4-klorobenzoat... 45
1
I. PENDAHULUAN
A. Latar Belakang.
Kesehatan memungkinkan setiap manusia hidup produktif secara sosial dan ekonomis dengan kondisi yang sejahtera dari raga, jiwa, dan sosial. Pada kondisi saat ini tingkat kesehatan menghadapi tantangan yang sangat berat (Nurwidodo, 2006). Jenis penyakit yang masih paling banyak diderita oleh penduduk di negara berkembang termasuk Indonesia yakni penyakit infeksi. Penyebab penyakit infeksi salah satunya adalah bakteri. Bakteri dapat dilihat hanya dengan bantuan mikroskop tidak dapat dilihat dengan mata telanjang ini dikarenakan bakteri merupakan mikroorganisme (Radji, 2011).
Bacillus sp. merupakan bakteri gram positif, berbentuk batang, dapat tumbuh pada kondisi aerob dan anaerob. Sporanya tahan terhadap panas (suhu tinggi), mampu mendegradasi xylane dan karbohidrat (Cowan dan Steel, 1973). Bacillus sp.
adalah salah satu genus bakteri yang berbentuk batang dan merupakan anggota dari divisi Firmicutes. Bacillus sp. merupakan bakteri yang bersifat aerob obligat atau fakultatif, dan positif terhadap uji enzim katalase.
2
Bacillus sp. secara alami terdapat dimana-mana dan termasuk spesies yang hidup bebas atau bersifat patogen. Beberapa spesies Bacillus sp menghasilkan enzim ekstra seluler seperti protease, lipase, amilase, dan selulase yang bisa membantu pencernaan dalam tubuh hewan (Wongsa and Werukhamkul, 2007).
Senyawa organologam merupakan senyawa yang setidaknya terdapat satu atom karbon dari gugus organik yang berikatan langsung dengan logam. Sebagai contoh suatu alkoksida seperti Ti(C3H7O)4bukan termasuk senyawa
organologam, karena gugus organiknya terikat pada Ti melalui atom oksigen Sedangkan senyawa (C6H5)Ti(OC3H7)3adalah senyawa organologam karena terdapat satu ikatan langsung antara karbon C dari gugus fenil dengan logam Ti.
Dari bentuk ikatan pada senyawa organologam, senyawa ini dapat dikatakan sebagai jembatan antara kimia organik dan anorganik (Cotton dan Wilkinson, 2007).
Senyawa organotimah adalah senyawa-senyawa yang mengandung sedikitnya satu ikatan kovalen C-Sn. Sebagian besar senyawa organotimah dapat dianggap sebagi turunan dari RnSn(IV)X4n(n = 1-4) dan diklasifikasikan sebagai mono-, di, tri- dan tetra- organotimah (IV), tergantung pada jumlah gugus alkil (R) atau aril (Ar) yang terikat. Anion yang terikat (X) biasanya adalah klorida, fluorida, oksida, hidroksida, suatu karboksilat atau suatu thiolat (Pellerito and Nagy, 2002).
Senyawa organotimah karboksilat pada umumnya dapat disintesis melalui dua cara yaitu dari organotimah oksida atau organotimah hidroksidanya dengan asam
3
karboksilat, dan dari organotimah halidanya dengan garam karboksilat. Metode yang biasa digunakan untuk sintesis organotimah karboksilat adalah dengan menggunakan organotimah halida sebagai material awal. Organotimah halida direaksikan dengan garam karboksilat dalam pelarut yang sesuai, biasanya aseton atau karbon tetraklorida (Wilkinson, 1982).
Ketertarikan terhadap senyawa organotimah(IV) tidak hanya karena sifat kimia dan strukturnya yang sangat menarik (Tiekink, 1991), tetapi juga karena
penggunaannya yang terus meningkat diantaranya sebagai biosida pertanian (Pellerito and Nagy, 2002; Gielen, 2003), antifouling bagi cat kapal di lautan (Blunden and Hill, 1987), pengawet kayu (Blunden and Hill, 1991), antifungi (Bonire et al., 1998; Hadi et al., 2009), sebagai katalis (Blunden et al., 1987), antikanker (de Vos et al., 1998; Gielen, 2003; Hadi and Rilyanti, 2010; Hadi et al., 2012), dan penelitian terbaru menerangkan bahwa turunan senyawa
organotimah(IV) karboksilat memiliki aktivitas sebagai inhibitor korosi (Rastogi et al., 2005; Singh et al., 2010; Rastogi et al., 2011).
Senyawa organotimah(IV) diketahui memiliki aktivitas biologi yang kuat.
Sebagian besar senyawa organotimah(IV) bersifat toksik walaupun pada konsentrasi rendah. Aktivitas biologi ini ditentukan oleh jumlah dan gugus organik yang terikat pada pusat atom Sn. Senyawa organotimah karboksilat diberikan perhatian khusus dikarenakan senyawa ini memiliki kemampuan biologi yang kuat dibandingkan senyawa organotimah lainnya (Mahmood et al., 2003;
Pellerito and Nagy, 2002).
4
Senyawa organotimah memiliki rentang aplikasi yang luas dan merupakan salah satu bahan kimia organologam yang paling banyak digunakan. Senyawa organotimah(IV) menunjukkan aktivitas biologis yang signifikan (Kang et al., 2009; Wu et al., 2009; Alama et al., 2009; Affan et al., 2009). Senyawa- senyawa tersebut telah diketahui sebagai antibakterial (Maiti et al., 1988;
Gleeson et al., 2008), antijamur ( Hadi et al., 2008; Manav et al., 2000; Singh dan Kaushik, 2008), antitumor (Mohan et al., 1988; Ruan et al., 2011; Hadi et al, 2012; Hadi and Rilyanti, 2010), dan antiviral (Singh et al., 2000).
B. Tujuan Penelitian.
Tujuan dari penelitian ini adalah sebagai berikut :
1. Mensintesis senyawa trifeniltimah(IV) 4-hidroksibenzoat dan trifeniltimah(IV) 4-klorobenzoat.
2. Mengkarakterisasi senyawa trifeniltimah(IV) 4-hidroksibenzoat dan
trifeniltimah(IV) 4-klorobenzoat menggunakan spektrofotometer UV-Vis, spektrofotometer IR, dan microelemental analyzer.
3. Menguji aktivitas antibakteri dari senyawa trifeniltimah(IV) 4-
hidroksibenzoat dan trifeniltimah(IV) 4-klorobenzoat terhadap bakteri gram positif Bacillus sp. dan membandingkan aktivitas antibakterinya dengan streptomisin sebagai kontrol positif.
4. Membandingkan aktivitas antibakteri dari kedua senyawa tersebut.
5
C. Manfaat Penelitian.
Hasil penelitian ini diharapkan dapat memberikan informasi bagi
perkembangan ilmu pengetahuan, khususnya dalam bidang organologam, serta untuk mengetahui lebih banyak dari senyawa organologam yang dapat digunakan sebagai zat antibakteri.
6
II. TINJAUAN PUSTAKA
A. Senyawa Organologam.
Senyawa organologam merupakan senyawa yang setidaknya terdapat satu atom karbon dari gugus organik yang berikatan langsung dengan logam. Sebagai contoh suatu alkoksida seperti Ti(C3H7O)4bukan termasuk senyawa
organologam, karena gugus organiknya terikat pada Ti melalui atom oksigen.
Sedangkan senyawa (C6H5)Ti(OC3H7)3adalah senyawa organologam karena terdapat satu ikatan langsung antara karbon C dari gugus fenil dengan logam Ti.
Dari bentuk ikatan pada senyawa organologam, senyawa ini dapat dikatakan sebagai jembatan antara kimia organik dan anorganik (Cotton dan Wilkinson, 2007).
B. Senyawa Organotimah.
Senyawa organotimah adalah senyawa-senyawa yang mengandung sedikitnya satu ikatan kovalen C-Sn. Sebagian besar senyawa organotimah dapat dianggap sebagai turunan dari RnSn(IV)X4-n(n = 1-4) dan diklasifikasikan sebagai mono-, di-, tri- dan tetra- organotimah(IV), tergantung pada jumlah gugus alkil (R) atau
7
aril (Ar) yang terikat. Anion yang terikat (X) biasanya adalah klorida, fluorida, oksida, hidroksida, suatu karboksilat atau suatu thiolat (Pellerito and Nagy, 2002).
Ikatan Sn-X memiliki derajat ion tertentu bergantung pada anion (X) dan alkil (R). Sebagai contoh, titik leleh dari (CH3)3SnX bervariasi untuk: fluorida (300ºC)
> klorida (37ºC) > bromida (27ºC) > iodida (3,4ºC) (Tayer, 1988). Pemanfaatan senyawa organotimah diantaranya sebagai penstabil dalam produksi plastik, pestisida dalam pertanian, katalis, pelapis kaca, stabilizer poliviniklorida, antikanker dan antitumor (Gielen, 2003), antifouling agents pada cat (Blunden and Hill, 1991), antimikroba dan antifungi (Bonire et al., 1998).
Kecenderungan terhidrolisis dari senyawa organotimah lebih lemah dibandingkan senyawa Si atau Ge yang terkait dan ikatan Sn-O dapat bereaksi dengan larutan asam. Senyawa organotimah tahan terhadap hidrolisis atau oksidasi pada kondisi normal walaupun dibakar menjadi SnO2, CO2dan H2O. Kemudahan putusnya ikatan Sn-C oleh halogen atau reagen lainnya bervariasi berdasarkan gugus organiknya dan urutannya meningkat dengan urutan : Bu (paling stabil) < Pr < et
< me < vinil < Ph < Bz < alil < CH2CN < CH2CO2R (paling tidak stabil).
Penggabungan SnR4melalui gugus alkil tidak teramati sama sekali. Senyawa- senyawa dengan rumus R3SnX atau R2Sn2X tergabung secara luas melalui jembatan X sehingga meningkatkan bilangan koordinasi Sn menjadi lima, enam atau bahkan tujuh. Dalam hal ini, F lebih efektif dibandingkan unsur-unsur halogen lainnya. Sebagai contoh Me3SnF memiliki struktur trigonal bipiramida, Me2SnF2memiliki struktur oktahedral sedangkan jembatan Cl yang lebih lemah memiliki struktur terdistorsi.
8
Kereaktifan dari senyawa organotimah(II) tinggi seperti dialkil timah dan diaril timah sederhana mengalami polimerisasi yang cepat. Kondisi ini dapat ditemukan pada senyawa organotimah yang memilki kestabilan divalen kemungkinan besar pada senyawa organik, bentuk adduct dengan basa Lewis atau pasangan
menyendiri Sn terkoordinasi. Pada asam Lewis yang sesuai perbedaan bilangan koordinasi dan geometri juga mungkin terjadi pada senyawa organotimah(II) pada penggunaan orbital 5d, yaitu trigonal planar (hibridisasi sp2), tetrahedral (sp3), trigonal bipiramida (sp3d) dan oktahedral (sp3d2) (Van der Weij, 1981).
1. Senyawa organotimah halida
Senyawa organotimah halida dengan rumus umum RnSnX4-n(n = 1-3; X = Cl, Br, I) pada umumnya merupakan padatan kristalin dan sangat reaktif.
Organotimah halida ini dapat disintesis secara langsung melalui logam timah, Sn(II) atau Sn(IV) dengan alkil halida yang reaktif. Metode ini secara luas digunakan untuk pembuatan dialkiltimah dihalida. Sintesis langsung ini ditinjau ulang oleh Murphy dan Poller melalui persamaan reaksi :
2 EtI + Sn Et2Sn + I2
Metode lain yang sering digunakan untuk pembuatan organotimah halida adalah reaksi disproporsionasi tetraalkiltimah dangan timah(IV) klorida.
Caranya adalah dengan mengubah perbandingan material awal, seperti ditunjukkan pada persamaan reaksi berikut :
3 R4Sn + SnCl4 4 R3SnCl R4Sn + SnCl4 2 R2SnCl4
9
Senyawa organotimah klorida digunakan sebagai kloridanya dengan memakai logam halida lain yang sesuai seperti ditunjukkanpada persamaan reaksi berikut :
R4SnCl4-n+ (4-n) MX R4SnX4-n+ (4-n) MCl (X = F, Br atau I; M = K, Na, NH4)
(Wilkinson, 1982).
2. Senyawa organotimah hidroksida dan oksida.
Produk kompleks yang diperoleh melalui hidrolisis dari trialkiltimah halida dan senyawa yang berikatan R3SnX, merupakan rute utama pada trialkiltimah oksida dan trialkiltimah hidroksida. Prinsip tahapan intermediet ditunjukkan pada reaksi di bawah ini :
(Wilkinson, 1982).
3. Senyawa organotimah karboksilat.
Senyawa organotimah karboksilat pada umumnya dapat disintesis melalui dua cara yaitu dari organotimah oksida atau organotimah hidroksidanya dengan asam karboksilat, dan dari organotimah halidanya dengan garam karboksilat.
Metode yang biasa digunakan untuk sintesis organotimah karboksilat adalah
10
dengan menggunakan organotimah halida sebagai material awal. Organotimah halida direaksikan dengan garam karboksilat dalam pelarut yang sesuai, biasanya aseton atau karbon tetraklorida. Reaksinya adalah sebagai berikut : RnSnCl4-n+ (4-n) MOCOR RnSn(OCOR)4-n+ (4-n) MCl
Reaksi esterifikasi dari asam karboksilat dengan organotimah oksida atau hidroksida dilakukan melalui dehidrasi azeotropik dari reaktan dalam toluena, seperti ditunjukkan pada reaksi berikut :
R2SnO + 2 R’COOH R2Sn(OCOR’)2+ H2O R3SnOH + R’COOH R3SnOCOR’ + H2O (Wilkinson, 1982).
C. Aplikasi Senyawa Organotimah.
Senyawa organotimah memiliki aplikasi yang luas dalam kehidupan sehari-hari.
Aplikasi senyawa organotimah dalam industri antara lain sebagai senyawa
stabilizer polivinilklorida, pestisida nonsistematik, katalis antioksidan, antifouling agents dalam cat, stabilizer pada plastik dan karet sintetik, stabilizer untuk parfum dan berbagai macam peralatan yang berhubungan dengan medis dan gigi
(Pellerito dan Nagy, 2002).
Mono- dan diorganotimah digunakan secara luas sebagai stabilizer
polivinilklorida untuk mengurangi degradasi polimer polivinilklorida. Empat tipe utama penstabil timah berdasarkan gugus alkilnya yaitu : oktil, butil, fenil dan metil. Oktiltimah diketahui memiliki kandungan timah paling sedikit dan tidak
11
efisien. Ligan-ligan utama yang digunakan untuk membedakan berbagai penstabil timah yaitu, asam tioglikolat ester dan asam karboksilat. Senyawa organotimah yang paling umum digunakan sebagai katalis dalam sintesis kimia yaitu katalis mono dan diorganotimah. Senyawa organotimah merupakan katalis yang bersifat homogen yang baik untuk pembuatan polisilikon, poliuretan dan untuk sintesis poliester. Senyawa organotimah ditemukan berikutnya antara lain sebagai biocide (senyawa yang mudah terdegradasi), sebagai pestisida yang pertama kali
diperkenalkan di Jerman yaitu dari senyawa trifeniltimah asetat pada akhir 1950-an. Kegunaan yang utama dari agrokimia senyawa organotimah karena senyawa ini relatif memiliki fitotoksisitas (daya racun pada tanaman) yang rendah dan terdegradasi dengan cepat sehingga residunya tidak berbahaya terhadap lingkungan (Cotton dan Wilkinson, 2007).
Senyawa organotimah(IV) telah diketahui memiliki aktivitas biologi yang kuat.
Sebagian besar senyawa organotimah(IV) bersifat toksik walaupun pada konsentrasi rendah. Aktivitas biologi ini ditentukan oleh jumlah dan gugus organik yang terikat pada pusat atom Sn. Senyawa organotimah karboksilat diberikan perhatian khusus dikarenakan senyawa ini memiliki kemampuan biologi yang kuat dibandingkan senyawa organotimah lainnya (Mahmood et al., 2003;
Pellerito dan Nagy, 2002).
Senyawa organotimah memiliki rentang aplikasi yang luas dan merupakan salah satu bahan kimia organologam yang paling banyak digunakan. Senyawa organotimah(IV) menunjukkan aktifitas biologis yang signifikan (Kang et al.,
12
2009; Wu et al., 2009). Senyawa-senyawa tersebut telah diketahui sebagai antibakterial (Maiti et al., 1988; Gleeson et al., 2008), antijamur ( Hadi et al., 2008; Manav et al., 2000; Singh dan Kaushik, 2008), antitumor (Mohan et al., 1988; Ruan et al., 2011; Hadi et al, 2012; Hadi and Rilyanti, 2010), dan antiviral (Singh et al., 2000).
D. Bakteri.
Mikroorganisme adalah oganisme berukuran sangat kecil atau mikroskopis, hanya dapat dilihat dengan bantuan mikroskop. Dunia organisme terdiri dari lima
kelompok organisme yaitu bakteri, protozoa, virus, alga, dan jamur mikroskopis (Pelezar dan Chan, 1986).
Bakteri merupakan organisme hidup bersel tunggal, tidak memiliki klorofil, dan memiliki DNA dan RNA. Bakteri dapat melakukan metabolisme, tumbuh dan berkembang biak. Sebagian besar bakteri berukuran sangat kecil misalnya kokus bergaris tengah 1 sehingga tidak dapat dilihat oleh mata telanjang. Lapisan terluar bakteri terdiri dari dua komponen yakni dinding sel yang kaku dan membran sitoplasma atau membran plasma. Di dalamnya terdapat sitoplasma seperti ribosom, mesosom, granula, vakuola, dan inti sel. Sel bakteri dapat diliputi oleh lapisan berupa gel yang mudah lepas atau tersusun sebagai suatu simpai. Selain itu beberapa bakteri juga mempunyai struktur tumbuhan lain seperti filamen yang menonjol keluar dari permukaan sel yaitu flagella yang berfungsi sebagai alat penggerak dan fimbria sebagai alat untuk melekatkan diri (Gupte, 1990).
13
Di alam terdapat ribuan jenis bakteri dan setiap jenis mempunyai sifat-sifat sendiri. Sebagian besar dari jenis bakteri tersebut tidak berbahaya bagi manusia, bahkan ada yang sangat bermanfaat bagi kehidupan mausia seperti bakteri pencernaan, Lactobacillus bulgaricus yang digunakan dalam pembuatan youghurt, dan lain-lain. Tetapi juga terdapat bakteri yang dapat menyebabkan penyakit pada manusia (bersifat patogen) seperti Escherihcia coli, Salmonella thypimurium (bakteri gram negatif) serta Staphylococcus aureus dan Bacillus sp (bakteri gram positif) yang menyebabkan keracunan pada makanan (Alaerts dan Santika, 1984).
E. Bakteri Bacillus sp.
Bacillus sp merupakan bakteri gram positif, berbentuk batang, dapat tumbuh pada kondisi aerob dan anaerob. Sporanya tahan terhadap panas (suhu tinggi), mampu mendegradasi xylane dan karbohidrat (Cowan dan Steel, 1973).
Bacillus adalah salah satu genus bakteri yang berbentuk batang dan merupakan anggota dari divisi Firmicutes.
Bacillus merupakan bakteri yang bersifat aerob obligat atau fakultatif, dan positif terhadap uji enzim katalase. Bacillus secara alami terdapat dimana-mana dan termasuk spesies yang hidup bebas atau bersifat patogen. Beberapa spesies Bacillus menghasilkan enzim ekstraseluler seperti protease, lipase, amilase, dan selulase yang bisa membantu pencernaan dalam tubuh hewan (Wongsa and Werukhamkul, 2007).
14
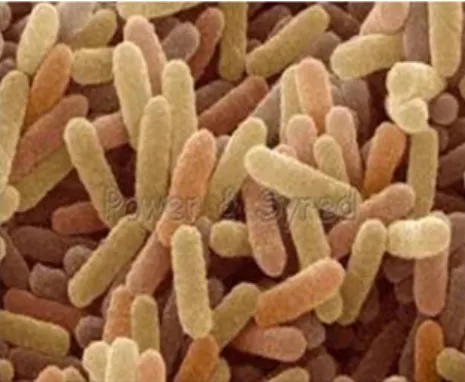
Gambar 1. Gambar sel bakteri Bacillus sp (Wikipedia, 2015).
F. Antibakteri.
Antibakteri merupakan zat yang dapat membasmi bakteri, khususnya bakteri yang merugikan bagi manusia (Vincent, 1987). Antibakteri digolongkan berdasarkan cara kerja, spektrum kerja, dan daya bunuh terhadap bakteri. Menurut Crueger (1984), antibakteri digolongkan berdasarkan pada susunan kimia dan sasaran kerjanya.
Kelompok antibakteri dilihat dari cara kerjanya, yaitu:
1. Menghambat sintesis dinding sel bakteri.
Tekanan osmosis dalam sel mikroba lebih tinggi daripada di luar sel, sehingga kerusakan dinding sel mikroba akan menyebabkan terjadinya lisis, yang merupakan dasar dari efek bakterisidal terhadap mikroba yang peka
(Setyaningsih, 2004). Seperti golongan polypeptide, cephalosporin, penicillin, vankomisin, basitrasin, dan sikloserin (Jawetz et al., 2005).
15
2. Menghambat sintesis protein.
Banyak jenis antibakteri, terutama golongan aminoglycoside, macrolide, chloramphenicol, streptomycin, tetracycline, oxytetracycline, gentamycine, kanamycine (Todar, 2009). Menghambat sintesis asam nukleat seperti
quinolon, pyrimethamin, rifampicin, sulfonamide, trimethoprim (Jawetz, et al., 2005).
Antibakteri yang mempengaruhi sintesis asam nukleat dan protein mempunyai mekanisme kegiatan pada tempat yang berbeda, antara lain:
a) Antibakteri mempengaruhi replikasi DNA, seperti bleomisin, phleomisin, mitomisin, edeine, dan porfiromisin.
b) Antibakteri mempengaruhi transkripsi, seperti aktinomisin, ekonomisin, rifamisin, korisepin,dan streptolidigin.
c) Antibakteri mempengaruhi pembentukan aminoacyl-tRNA, seperti borrelidin.
d) Antibakteri mempengaruhi translasi, antara lain chloramphenicol, streptomisin, neomisin, kanamisin, karbomisin, crytromisin, linkomisin, fluidic acid,dan tetrasiklin (Suwandi, 1992).
e) Menghambat fungsi membran sel seperti, kolistin, imidasol, triasol, polien, polimiycin, dan amfoterisin (Jawetz, et al., 2005). Membran sel sebagai barrier permeabilitas selektif, membawa fungsi transpor aktif kemudian mengontrol komposisi internal sel.
16
Jika fungsi integritas membran sitoplasma dirusak, makromolekul dan ion keluar dari sel, kemudian sel rusak atau sel bakteri mengalami lisis (Jawetz et al., 2005).
G. Uji Aktivitas Antibakteri.
Uji aktivitas antibakteri terdiri dari dua metode utama yaitu :
1. Metode difusi
Pada metode ini, zat antibakteri akan berdifusi ke dalam media agar yang telah ditanami bakteri. Teknik metode ini secara umum adalah dengan menginokulasikan kuman secara merata diseluruh pemukaan media agar, kemudian sampel yang diuji ditempatkan diatas permukaan tersebut.
Setelah inkubasi, selama 18 - 24 jam pada suhu 37oC, akan terbentuk zona hambat di sekeliling reservoir sampel. Pengamatan berdasarkan ada atau tidaknya zona hamabat pertumbuhan bakteri disekeliling cakram. Ada tiga macam teknik difusi, yaitu : cara parit, cara lubang atau sumuran, dan cara cakram.
Pada metode parit, media agar yang ditanami bakteri dibuat parit yang kemudian diisi dengan larutan yang mengandung zat antibakteri dan diinkubasi selama 18 - 24 jam pada suhu 37oC. Kemudian dilihat ada atau tidaknya zona hambatan disekeliling parit (Balsam dan Sagarin, 1972;
Jawetz et al., 1986). Cara lubang atau sumuran, pada media agar yang
17
ditanami bakteri dibuat lubang atau dengan meletakkan silinder besi tahan karat pada medium agar yang kemudian diisi dengan larutan yang
mengandung zat antibakteri dan diinkubasikan selama 18 – 24 jam pada suhu 37oC, kemudian dilihat ada atau tidaknya zona hambatan disekeliling silinder (Balsam dan Sagarin, 1972; Jawetz etal., 1986).
Cara cakram, pada media agar yang telah ditanami bakteri diletakkan diatas kertas cakram yang mengandung zat antibakteri dan diinkubasikan selama 18 – 24 jam pada suhu 37oC, kemudian dilihat ada atau tidaknya zona hambatan di sekeliling cakram. Cara lubang maupun cara cakram terdapat persamaan dimana larutan akan berdifusi secara tiga dimensi.
Sedangkan pada cara parit, sampel hanya berdifusi secara dua dimensi (Jawetz et al., 1986).
Faktor-faktor yang mempengaruhi metode difusi adalah ketebalan agar, komposisi dari media agar, konsentrasi inokulum, suhu, dan waktu inkubasi. Ketebalan lapisan agar yang sedikit saja bervariasi akan
menghasilkan efek dan besar zona hambat yang jauh berbeda. Oleh karena itu, diperlukan ketebalan lapisan agar yang sama. Cawan petri yang
digunakan harus benar-benar rata dan agar harus dituang pada posisi yang tepat. Media agar mempengaruhi besarnya zona hambatan dengan 3 cara, yaitu : mempengaruhi aktivitas suatu antibakteri, mempengaruhi kecepatan difusi suatu sampel antibakteri, dan mempengaruhi kecepatan
pertumbuhan bakteri.
18
Aktivitas dari antibakteri dipengaruhi oleh berbagai faktor seperti adanya kation dalam media, pH dari media, dan adanya bermacam-macam zat antagonis (pengganggu).
Kecepatan difusi dari obat ditentukan oleh konsenstrasi agar, konsentrasi beberapa ion dalam media, dan perpanjangan pengikatan elektrostatik antar sampel dan group yang terionisasi di dalam media agar.
Viskositas dari media juga mempengaruhi kecepatan difusi dan hal ini tergantung juga pada waktu inkubasi. Kapasitas nutrisi dari media agar sangat ditentukan oleh panjangnya fasa lag dan waktu pertumbuhan untuk bakteri yang diteliti.
Konsentrasi inokulum yang besar akan memperkecil zona hambat, sebab masa kritis sel akan tercapai dengan cepat. Suhu harus sesuai dengan suhu optimal untuk pertumbuhan bakteri, yaitu pada 37oC. Bila tidak sesuai maka akan mengakibatkan kecepatan pertumbuhan bakteri tidak sesuai sehingga jumlah bakteri yang diinginkan tidak akan tercapai. Suhu inkubasi yang rendah dapat memperbesar zona hambat karena akan memperlambat pertumbuhan bakteri atau dapat juga memperkecil zona hambat karena difusi sampel antibakteri berjalan lambat. Tetapi efek memperbesar zona hambatan lebih dominan. Lamanya waktu inkubasi harus merupakan waktu minimal yang diperlukan pertumbuhan normal dari bakteri percobaan. Perpanjangan waktu dapat menurunkan aktivitas dan dapat pula menimbulkan muatan resisten.
19
2. Metode Dilusi
Metode ini digunakan untuk menentukan Konsentrasi Hambat Minimum (KHM) sampel antibakteri terhadap bakteri uji. Metode dilusi ini dilakukan dengan mencampurkan zat antibakteri dengan media yang kemudian diinokulasikan dengan bakteri. Pengamatannnya dengan melihat ada atau tidaknya pertumbuhan bakteri (Lorian, 1980). Berdasarkan media yang digunakan dalam percobaan, metode ini dibagi menjadi dua yaitu penipisan lempeng agar dan pengenceran tabung. Pada penipisan lempeng agar, zat antibakteri yang akan diuji dilarutkan lebih dahulu dalam air suling steril atau dalam pelarut steril lain yang sesuai. Kemudian dilakukan dengan pengenceran secara serial dengan kelipatan dua sampai kadar terkecil yang dikehendaki. Pada pengenceran tabung, zat antibakteri dilarutkan dalam pelarut yang sesuai, kemudian diencerkan dengan kaldu berturut-turut pada tabung-tabung yang disusun dalam satu deret terkecil yang dikehendaki, dengan metode Kerby Bauwer yang dimodifikasi.
Tiap tabung yang berisi 1 mL campuran dengan berbagai kadar tersebut diinokulasikan dengan suspensi kuman yang mengandung kira-kira 105 sampai 106sel bakteri/mL. Kemudian diinkubasikan selama 18 sampai 24 jam pada suhu 37oC. Sebagai kontrol gunakan paling sedikit satu tabung cair dengan inokulum bakteri tersebut. Kedua cara diatas biasanya
digunakan dalam penentuan Kadar Hambat minimal (KHM) (Lorian, 1980;
Case dan Johnson, 1984).
20
III. METODE PENELITIAN
A. Waktu dan Tempat Penelitian.
Penelitian ini dilaksanakan pada bulan November 2015 sampai dengan bulan Mei 2016 di Laboratorium Kimia Anorganik-Fisik FMIPA Universitas Lampung.
Analisis senyawa menggunakan spektrofotometer UV-Vis dilakukan di Laboratorium Kimia Anorganik FMIPA Universitas Lampung dan analisis senyawa menggunakan spektrofotometer IR dilakukan di Universitas Islam Indonesia. Untuk analisis unsur, yakni dengan menggunakan microelemental analyzer dilakukan di School of Chemical and Food Technology, Universitas Kebangsaan Malaysia, dan pengujian aktivitas antibakteri dilakukan di Laboratorium Biokimia, Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Lampung.
B. Alat dan Bahan.
Alat-alat yang digunakan dalam penelitian ini yaitu gelas ukur, cawan petri, gelas kimia, kertas saring Whatman No. 42, bulp, pipet gondok, satu set alat refluks,
21
hot plate stirrer, desikator, instrumentasi: spektrofotometer IR, spektrofotometer UV-Vis, dan microelement alanalyzer (untuk analisis unsur).
Sedangkan bahan-bahan yang digunakan dalam penelitian ini adalah asam 4- klorobenzoat, asam 4-hidroksibenzoat, trifeniltimah(IV) hidroksida, NaOH, metanol p.a., akuades, akuabides, media agar NA (Nutrient Agar), DMSO, dan bakteri Bacillus sp.
C. Cara Kerja.
Prosedur umum untuk sintesis senyawa R2Sn(OOCR)2ataupun R3Sn(OOCR) dengan R baik alkil maupun fenil dilakukan berdasarkan prosedur yang telah dilakukan sebelumnya (Hadi et al., 2009; Hadi and Rilyanti, 2010; Hadi et al., 2012) yang merupakan adaptasi dari Szorcsik et al. (2002). Sedangkan
prosedur uji antibakteri dilakukan berdasarkan prosedur yang telah dilakukan oleh Windiyani dan Nopitasari (2015).
1. Sintesis senyawa trifeniltimah(IV) 4-hidroksibenzoat.
Senyawa trifeniltimah(IV) hidroksida [(C6H5)3SnOH)] sebanyak 1,1001 gram direaksikan dengan asam 4-hidroksibenzoat [(C6H5(OH)COOH)]
sebanyak 0,417 gram dengan perbandingan mol 1:1 dalam 30 mL pelarut metanol p.a. dan direfluks selama 4 jam dengan pemanasan pada suhu 60oC. Setelah reaksi sempurna, metanol diuapkan dan dikeringkan di
22
dalam desikator sampai diperoleh kristal kering. Kristal hasil sintesis dikarakterisasi dengan spektrofotometer IR dan UV-Vis yang diukur pada panjang gelombang 190-380 nm (Sudjadi,1985), dan dianalisis
kandungan unsur C dan H dengan microelementer analyzer, serta diuji aktivitas antibakterinya terhadap Bacillus sp.
2. Sintesis senyawa trifeniltimah(IV) 4-klorobenzoat.
Senyawa trifeniltimah(IV) hidroksida [(C6H5)3SnOH)] sebanyak 1,1001 gram direaksikan dengan asam 4-kloroksibenzoat [(C6H5(Cl)COOH)] sebanyak 0,4725 gram dengan perbandingan mol 1:1 dalam 30 mL pelarut metanol p.a.
dan direfluks selama 4 jam dengan pemanasan pada suhu 60oC. Setelah reaksi sempurna, metanol diuapkan dan dikeringkan di dalam desikator sampai diperoleh kristal kering. Kristal hasil sintesis dikarakterisasi dengan
spektrofotometer IR dan UV-Vis yang diukur pada panjang gelombang 190- 380 nm (Sudjadi,1985), dan dianalisis kandungan unsur C dan H dengan microelementer analyzer, serta diuji aktifitas antibakterinya terhadap bakteri Bacillus sp.
3. Uji Aktivitas Antibakteri
a. Penyiapan Media Uji.
Penyiapan media uji dilakukan dengan pembuatan NA (Nutrient Agar).
Sebanyak 2,8 gram NA dilarutkan dalam 100 mL aquades, kemudian
23
dipanaskan dan disterilkan dalam autoclave pada suhu 121°C dan tekanan 1 atm selama 15 menit. Sebanyak 15 mL media NA yang telah steril
kemudian dituangkan ke dalam cawan petri yang telah disterilisasi.
Penuangan tersebut dilakukan dalam Laminar Air Flow. Kemudian media didinginkan sampai memadat, jika tidak terlihat adanya
kontaminan/pengotor, maka media ini dapat digunakan untuk pengujian aktifitas antibakteri.
b. Uji Bioaktivitas Dengan Metode Difusi Agar.
Sebanyak 1 mata ose bakteri Bacillus sp. diencerkan dengan 1 mL air salin kemudian digunakan sebagai suspensi bakteri. Kemudian suspensi bakteri tersebut dituangkan kedalam media uji dan diratakan menggunakan sprider (batang berbentuk huruf L). Sebanyak 3 kertas cakram diletakkan pada permukaan agar.
Pada kertas cakram pertama diberikan senyawa antara dan senyawa hasil sintesis dengan variasi konsentrasi 100, 150, 200; 250; dan 300 ppm.
Senyawa antara yang digunakan yaitu trifeniltimah(IV) hidroksida, sedangkan senyawa hasil sintesis terdiri dari trifeniltimah(IV) 4-
hidroksibenzoat dan trifeniltimah(IV) 4-klorobenzoat. Kertas cakram kedua diberikan kontrol negatif yaitu pelarut senyawa inhibitor. Kertas cakram terakhir diberi larutan kontrol positif (dalam percobaan ini menggunakan kontrol positif streptomisin).
24
Kemudian diinkubasi selama 2-3 hari pada suhu 25-30 °C. Dilakukan pengamatan pertumbuhan bakteri setiap harinya. Senyawa yang memiliki konsentrasi penghambatan paling efektif akan kembali diuji dengan metode dilusi (Ismiyati, 2010).
c. Uji Bioaktivitas Dengan Metode Dilusi Agar
Dari hasil pengujian secara difusi didapatkan senyawa trifeniltimah(IV) 4- hidroksibenzoat atau trifeniltimah(IV) 4-klorobenzoat yang memiliki konsentrasi penghambatan paling efektif, kemudian senyawa tersebut dilarutkan dalam pelarut DMSO. Selanjutnya senyawa uji dicampurkan ke dalam 15 mL media agar dengan variasi volume 0,5; 1,0; 1,5; 2,0; dan 2,5 mL. Bakteri Bacillus sp. diletakkan tepat ditengah media NA yang telah tercampur dengan senyawa kimia uji. Kemudian diinkubasi pada suhu 25-30 ºC selama 24 jam, dan setelahnya diamati untuk melihat zona hambat
terhadap pertumbuhan bakteri (Ismiyati, 2010).
47
V. SIMPULAN DAN SARAN
A. Simpulan.
Berdasarkan hasil pembahasan, maka diperoleh simpulan sebagai berikut:
1. Pada sintesis senyawa trifeniltimah(IV) 4-hidroksibenzoat dan senyawa trifeniltimah(IV) 4-klorobenzoat didapatkan serbuk berwarna putih dengan rendemen masing-masing 89,57 % dan 87,90% .
2. Hasil analisis menggunakan microelemental analyzer menunjukkan selisih komposisi unsur C dan H pada senyawa hasil sintesis terhadap perhitungan teori sekitar 1-5 %, sehingga senyawa hasil sintesis dapat dikategorikan murni.
3. Pada uji difusi senyawa trifeniltimah(IV) hidroksida, trifeniltimah(IV) 4- hidroksibenzoat, dan trifeniltimah(IV) 4-klorobenzoat memiliki aktivitas
antibakteri, dimana senyawa trifeniltimah(IV) 4-klorobenzoat memiliki aktivitas antibakteri terbaik.
4. Pada uji dilusi, senyawa trifeniltimah(IV) 4-klorobenzoat efektif menghambat pertumbuhan bakteri pada kadar 75 mg dalam 15 mL media agar.
48
B. Saran
Adapun saran dalam penelitian ini yaitu:
1. Perlu dilakukan kajian aktivitas antibakteri lebih lanjut dengan menggunakan turunan senyawa organotimah(IV) dengan subtituen ligan lainnya.
2. Perlu dilakukan rekristalisasi terhadap senyawa hasil sintesis, agar kemurnian senyawa hasil yang diperoleh tinggi.
3. Perlu dilakukan uji titik leleh, untuk membuktikan apakah senyawa hasil yang diinginkan diperoleh atau tidak.
49
DAFTAR PUSTAKA
Alaerts, G. dan S. S. Santika. 1984. Metode Penelitian Air. Usaha Nasional.
Surabaya.
Alama, A., B. Tasso, F. Novelli and F. Sparatore. 2009. Organometallic compound in oncology: implications of novel organotins as antitumor agents. Drug Discov. Today, 14: 500-508
Balsam, M. S. and E. Sagarin. 1972. Cosmetics Science and Technology.
2ndEdition.
Blunden, S. J. and R. Hill. 1987. In Surface Coating. Wilson, A.D., J.W
Nicholson,. and H.J. Prosser. (Eds). Elsevier Applied Science Publisher, pp. 17 – 167.
Blunden, S. J. and R. Hill. 1991. Bis(tributyltin) Oxide as a Wood Preservative:
It’s Conversion to Tributyltin Carboxylates in Pinus sylvestris. Applied Organometallic Chemistry, 4: 63-68.
Blunden, S. J., P. A. Cusack, R. Hill. 1987. in The Industrial Uses of Tin Chemicals. The Royal Society of Chemistry. London.
Bonire, J. J., G. A. Ayoko, P. F. Olurinola, J. O. Ehinmidu, N. S. N. Jalil, and A.
A. Omachi. 1998. Synthesis and Antifungal Activity of Some Organotin(IV) Carboxylates. Metal-Based Drugs. 5 (4): 233-236.
Case, C. L. And Johnson, T. R. 1984. Laboratory Experiments in Microbiology.
Benjamin/Cummings Publishing Company, Inc. New York.
Cotton, F. A. dan G. Wilkinson. 2007. Kimia Anorganik Dasar. Alih bahasa S.
Suharto . Penerbit UI Press. Jakarta.
Caprette, D.R. 2007. Using a Caunting Chamber. Lab Guides. Rice University.
50
Cowan, J and W. Steel. 1973. Manual and for the Identification of Medical Bacteria. 3rdEdition. Cambridge University Press. New York. pp. 21-25.
Crueger, W. And Crueger, A. 1984. Biotechnology, A Text Book of Industrial Microbiology. Stnaeur Associates, Inc. Sunderland.
de Vost, D., R. Willem, M. Gielen, K. E. Van Wingerden, and K. Nooter. 1998.
The Development of Novel Organotin Anti-Tumor Drugs: Structure and Activity. Metal-Based Drugs. 5 (4): 179-188.
Djide, P dan Sartini. 2008. Dasar-Dasar Mikrobiologi Farmasi. Lephas.
Makassar.
Gupte, S. 1990. Mikrobilogi Dasar. Terjemahan E. Suryawidjaja : The Short Textbook of Medical Microbiology. Bina Rupa Aksara. Jakarta.
Hadi , S., B. Irawan and Efri. 2008. The Antifungal Activity Test Of Some Organotin(IV) Carboxylates. J. Appl. Sciences. Res. 4 (11): 1521-1525.
Hadi, S., M. Rilyanti, Nurhasanah, 2009. Comparative Study on the Antifungal Activity of Some Di- and Tributylin(IV) Caroxylate Compounds. Modern Applied Science. 3 (2): 12-17.
Hadi, S. and M. Rilyanti. 2010. Synthesis and In Vitro Anticancer Activity of some Organotin(IV) Benzoate Compounds. Oriental Journal of Chemistry. Vol. 26 (3), pp 775-779.
Husna, M. 2007. Mycorrhiza Application to Support Grow of Teak in Muna. Balai Besar Penelitian Bioteknologi dan Pemuliaan Tanaman Hutan. Fakultas Pertanian Unhalu.
Indriani,Y. H. 2007. Membuat Kompos Secara Kilat. Penebar Swadaya. Jakarta.
Ismiyati, D. 2010. Isolasi dan Karakterisasi Senyawa Turunan Fenol Dari Kayu Akar Shorea leprosula Miq Serta Uji Bioaktivitas Terhadap Bakteri Escherichia coli. (Skripsi). Universitas Lampung. Bandar Lampung.
Jawetz, E. and M. Adelberg. 1986. Mikrobiologi untuk Profesi Kesehatan. Edisi ke-XVI. Diterjemahkan oleh dr. G. Bonang. EGC Press. Jakarta. Hal 336-338.
Jawetz, E. and M. Adelberg. 2005. Mikrobiologi Kedokteran Edisi Ke-3. Alih Bahasa : Huriwati Hartanto dkk. Penerbit Buku Kedokteran ECG.Jakarta.
51
Kang, W., X. Wu and J. Huang, 2009. Synthesis, Crystal Structure and Biological Activities of Four Novel Tetranuclear Di-organotin(IV) Carboxylates. J. Organo.Chem. 694: 2402-2408.
Lorian, V. 1980. Antibiotics in Laboratory Medical. Wiliam and Wilkins Co.
Baltimore. London. Hal. 1-22, 170-178, 511-512.
Mahmood, S., S. Ali, M.H. Bhatti, M. Mazhar, and R. Iqbal. 2003. Synthesis, Characterization, and Biological Applications of Organotin(IV) Derivates of 2-(2-Fluoro-4-biphenyl) Propanoid Acid. Turkish Journal of Chemistry.
27: 657-666.
Maiti, A., A. K. Guha and S. Ghosh. 1988. Ligational Behavior of Two Biologically Actives N-S Donors Toward Oxovanadium(IV) Ion and Potentiation of Their Antibacterial Activities by Chelation to. J. Inorg.
Biochem. 33: 57-65.
Mohan, M., A. Agarwal, and N. K. Jha. 1988. Synthesis, Characterization, and Antitumor Properties of Some Metal Complexes of 2,6-diacetylpyridine bis(N4- azacyclic thiosemicarbazones). J. Inorg. Biochem. 34: 41-54.
Nopitasari. 2015. Sintesis, Karakterisasi, dan Uji Aktivitas Antibakteri Senyawa Organotimah(IV) 3-nitrobenzoat pada Bakteri Gram Positif Bacillus sp (Skripsi). Universitas Lampung. Bandar Lampung.
Nurwidodo. 2006. Pencegahan dan Promosi Kesehatan Secara Tradisonal untuk Peningkatan Status Masyarakat di Sumenep. Madura.Jurnal Humanity.
1(2):96-105.
Pelczar M. J. and E. C. S. Chan. 1986. Dasar-dasar Mikrobiologi 2.
Diterjemahkan oleh Hadioetomo R. S, Imas T, Tjitrosomo S. S, Angka SL. Penerbit Universitas Indonesia. Jakarta. Hal.489-522.
.
Pellerito, L. and L. Nagy. 2002. Organotin(IV)n+Complexes Formed with Biologically Active Ligands: Equilibrium and Structural Studies, and Some Biological Aspects. Coord. Chem. Rev. 224: 111 – 150.
Radji, M. 2011. Mikrobiologi. Buku Kedokteran. ECG. Jakarta.
Rastogi, R. B., M. M. Singh, K. Singh and M. Yadav. 2005. Organotin Dithiohydrazodicarbonamides as Corrosion Inhibitors for Mild Steel Dimethyl Sulfoxide Containing HCl. Port. Electrochim. Acta. 22: 315–
332.
52
Singh, N. K., A. Srivastava, A. Sodhi, and P. Ranjan. 2000. In vitro and in vivo Antitumour Studies of a NewTthiosemicarbazide Derivative and its Complexes with 3d-metal Ions. Transit. Metal Chem. 25: 133-140.
Sudjadi. 1985. Penentuan Struktur Senyawa Organik. Ghalia Indonesia. Jakarta.
Hlm 128-188.
Sulistyaningsih. 2010. Uji Kepekaan Beberapa Sediaan Antiseptik terhadap Bakteri S. Aureus dan Pseudomonas sp Resisten Metisilin (MRSA). Tesis.
Universitas Padjajaran. Bandung.
Szorcsik, A., L. Nagy, L. Pellerito, T. Yamaguchi, and K. Yoshida. 2002.
Preparation and Structural Studies of Organotin(IV) Complexes Formed with Organic Carboxylic Acids. Journal Radioanalytical and Nuclear Chemistry. 256(1): 3-10.
Tayer, J. 1988. Organometallic Chemistry and Overview. VCH Publisher Inc/United State. Page 7, 12, 14.
Todar, K. 1990. Biological identity of Procaryotes. Department of Bacteriology University of Wisconsin-Madison. USA.
Tiekink, E. R. T. 1991. Structural Chemistry of Organotin Carboxylates: a Review of the Crystallographic Literature. App. Organometal. Chem. 5: 1-30.
Van Der Weij, F. W. 1981. Kinetics and Mechanism of Urethane Formation Catalysed by Organotin Compound. Journal of Polymer Science:
Polymer Chemistry. 19 (2): 381-388.
Vincent, G. 1987. Farmakologi dan Terapi. Edisi ke-3. Bagian Farmakologi Fakultas Kedokteran UI. Jakarta.
Wilkinson, G. 1982. Compreherensive Organometalic Chemistry. International Tin Research Institude, Publication No.618, Pergamon Press.
Windiyani, Melli N. 2015. Sintesis, Karakterisasi, dan Uji Aktivitas Biologi Beberapa Senyawa Turunan Trifeniltimah(IV) 4-NO2benzoat sebagai Antibakteri terhadap Bakteri Bacillus sp (Skripsi). Universitas Lampung.
Bandar Lampung.
Wongsa, P. And P. Werukhamkul. 2007. Product Development and Technical Service, Bisolution International. Thailand : Bangkadi Industrial Park 133/4.